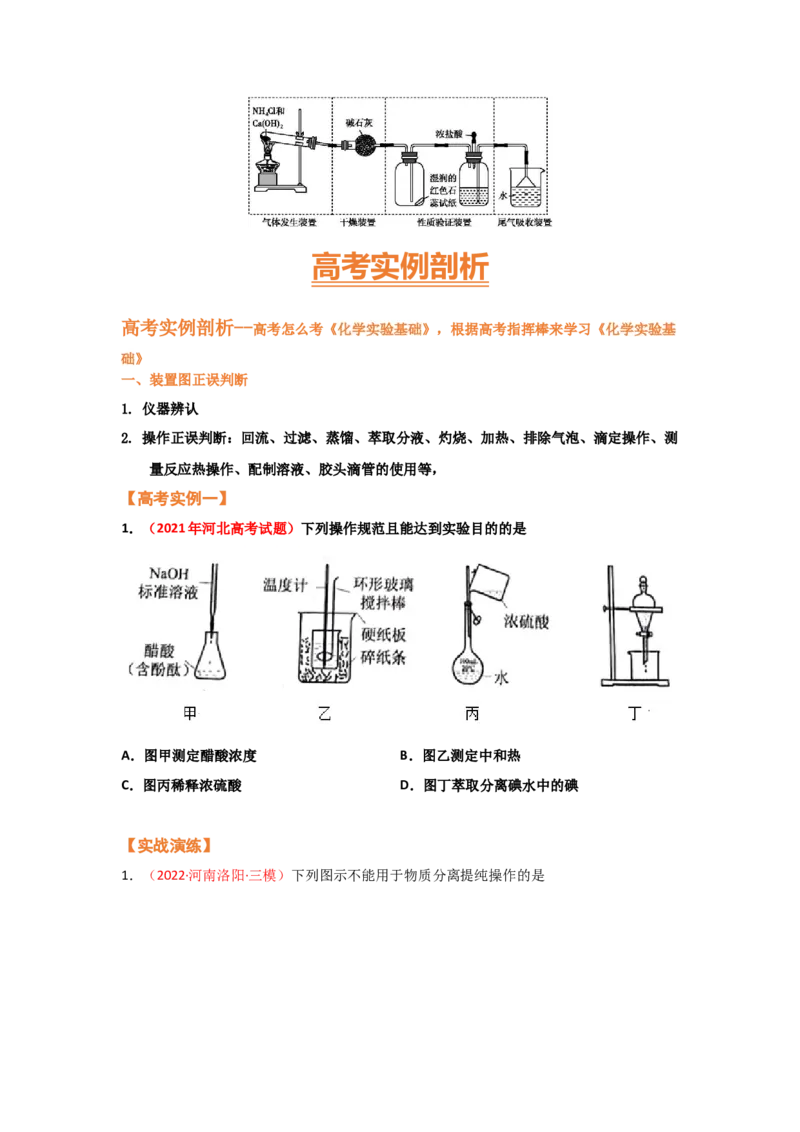
文档内容
专题八 化学实验基础
必备知识 解读
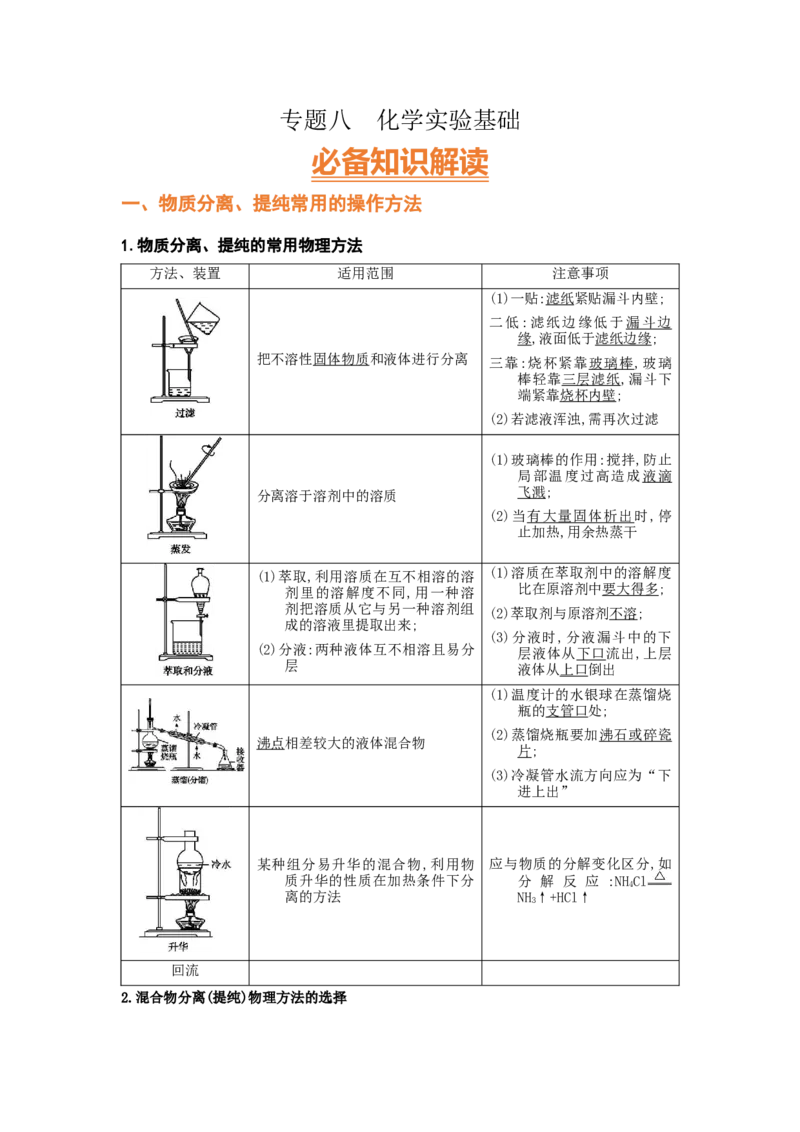
一、物质分离、提纯常用的操作方法
1.物质分离、提纯的常用物理方法
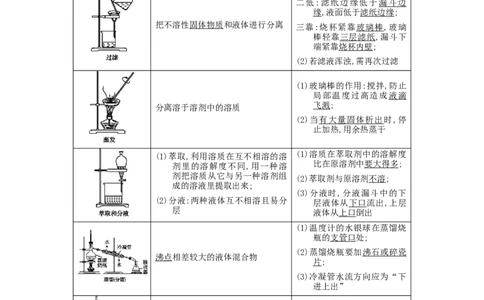
方法、装置 适用范围 注意事项
(1)一贴:滤纸紧贴漏斗内壁;
二低:滤纸边缘低于漏斗边
缘,液面低于滤纸边缘;
把不溶性固体物质和液体进行分离 三靠:烧杯紧靠玻璃棒,玻璃
棒轻靠三层滤纸,漏斗下
端紧靠烧杯内壁;
(2)若滤液浑浊,需再次过滤
(1)玻璃棒的作用:搅拌,防止
局部温度过高造成液滴
分离溶于溶剂中的溶质 飞溅;
(2)当有大量固体析出时,停
止加热,用余热蒸干
(1)萃取,利用溶质在互不相溶的溶 (1)溶质在萃取剂中的溶解度
剂里的溶解度不同,用一种溶 比在原溶剂中要大得多;
剂把溶质从它与另一种溶剂组 (2)萃取剂与原溶剂不溶;
成的溶液里提取出来;
(3)分液时,分液漏斗中的下
(2)分液:两种液体互不相溶且易分 层液体从下口流出,上层
层 液体从上口倒出
(1)温度计的水银球在蒸馏烧
瓶的支管口处;
(2)蒸馏烧瓶要加沸石或碎瓷
沸点相差较大的液体混合物
片;
(3)冷凝管水流方向应为“下
进上出”
某种组分易升华的混合物,利用物 应与物质的分解变化区分,如
质升华的性质在加热条件下分 分 解 反 应 :NHCl
4
离的方法 NH↑+HCl↑
3
回流
2.混合物分离(提纯)物理方法的选择① “固+固”混合物的分离(提纯)
② “固+液”混合物的分离(提纯)
③ “液+液”混合物的分离(提纯)
3.物质分离、提纯常用的化学方法
化学
原理 举例
方法
如除产品中所含杂质离子 Cl-、S 、C 及
沉淀法 将杂质离子转化为沉淀
Mg2+、Ca2+、Fe3+、Fe2+、Cu2+等
如除产品中所含杂质离子C 、HC 、S 、
气化法 将杂质离子转化为气体
HS 、N 等
杂转 将杂质转化为需要提纯的物 杂质中含不同价态的相同元素(用氧化剂或还原
剂)、同一种酸的正盐与酸式盐(对应用酸、
纯法 质 酸酐或碱)
氧化 用氧化剂(还原剂)除去具有 如用酸性KMnO 溶液除去CO 中的SO,用灼热的铜
4 2 2
还原法 还原性(氧化性)的杂质 网除去N 2 中的O 2
热分 加热使不稳定的物质分解除
如除去NaCl中的NHCl等
解法 去 4
酸碱 利用物质与酸或碱溶液混合
如用过量的NaOH 溶液可除去FeO 中的AlO
溶解法 后的差异进行分离 2 3 2 3
加入试剂调节溶液的pH,使 如向含有Cu2+和Fe3+的溶液中加入CuO、Cu(OH)
调pH 2
溶液中某种成分生成沉 或 Cu(OH)CO 等调节 pH,使 Fe3+转化为
法 2 2 3
淀而除去 Fe(OH) 而除去
3
电解法 利用电解原理除去杂质 如精炼Cu
二、常见气体的制备、净化和收集以及装置的创新
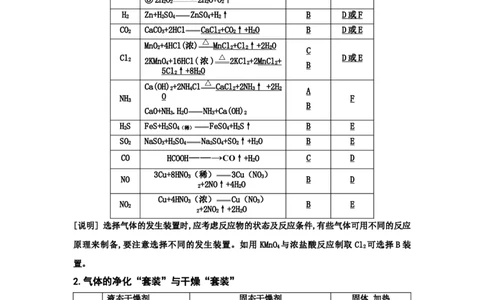
1.气体的发生“套装”和收集“套装”气体 反应原理 发生装置 收集装量
①2KMnO KMnO+MnO+O↑
4 2 4 2 2
O ②2KClO 2KCl+3O↑ A或B D或E
2 3 2
③2HO 2HO+O↑
2 2 2 2
H Zn+HSO ZnSO+H↑ B D 或 F
2 2 4 4 2
CO CaCO+2HCl CaCl+CO ↑ + HO B D 或 E
2 3 2 2 2
MnO+4HCl(浓) MnCl+Cl ↑ +2 HO
2 2 2 2 C
Cl D 或 E
2 2KMnO+16HCl(浓) 2KCl+2MnCl+
4 2 2 B
5 C l ↑ + 8 HO
2 2
Ca(OH)+2NHCl CaCl+2NH ↑ +2 H
2 4 2 3 2 A
NH O F
3
B
CaO+NH.HO NH+Ca(OH)
3 2 3 2
HS FeS+HSO FeSO+HS↑ B E
2 2 4(稀) 4 2
SO NaSO+HSO NaSO+SO↑+HO B E
2 3 2 4 2 4 2 2
CO HCOOH――→CO↑+HO C D
2
3Cu+8HNO(稀) 3Cu(NO)
NO 3 3 B D
+2NO↑+4HO
2 2
Cu+4HNO(浓) Cu(NO)
NO 3 3 B E
2 +2NO↑+2HO
2 2 2
[说明] 选择气体的发生装置时,应考虑反应物的状态及反应条件,有些气体可用不同的反应
原理来制备,要注意选择不同的发生装置。如用 KMnO 与浓盐酸反应制取Cl 可选择B装
4 2
置。
2.气体的净化“套装”与干燥“套装”
液态干燥剂 固态干燥剂 固体,加热
装
置
液态干燥剂 固态干燥剂 固体,加热
浓硫酸(酸性、强氧 无 水 氯 化 钙 ( 碱 石 灰 ( 除杂试剂(Cu、CuO、
化性) 中性) 碱性) Mg)H 、 O 、 Cl 、 H 、O 、CO、
H、O、Cl、SO、 2 2 2 2 2
2 2 2 2 SO 2 、 N 2 、CH 4 、 可除去O 2 、H 2 、CO等
CO、CO、CH、N 等
2 4 2 CO、CO、CH 等 NH 等
2 4 3
Cl、SO、
2 2
NH 、HBr、HI、HS
3 2 NH CO、NO、
等 3 2 2
HCl等
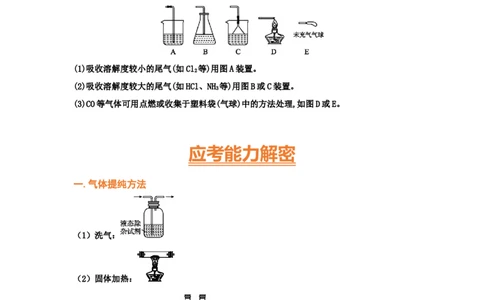
3.尾气的处理“套装”
通常有毒和有污染的尾气必须适当处理。常用仪器有:
(1)吸收溶解度较小的尾气(如Cl 等)用图A装置。
2
(2)吸收溶解度较大的尾气(如HCl、NH 等)用图B或C装置。
3
(3)CO等气体可用点燃或收集于塑料袋(气球)中的方法处理,如图D或E。
应考能力 解 密
一.气体提纯方法
(1)洗气:
(2)固体加热:
(3)固体不加热:
例如:除去下列气体中的杂质
(1) CO(HCl)让混合气通过盛有_______溶液的洗气瓶。
2
(2) Cl(HCl)让混合气通过盛有_______溶液的洗气瓶。
2
(3) SO(HCl)让混合气通过盛有_______溶液的洗气瓶。
2
(4) CO(SO)让混合气通过盛有_______溶液的洗气瓶。
2 2(5) HCl(Cl)让混合气通过盛有_______的洗气瓶。
2
(6) HBr(Br)让混合气通过盛有_______的洗气瓶。
2
二、装置的创新
1.分离、提纯的创新装置
过滤装置的创新——抽滤
由于水流的作用,使图1装置a、b中气体的压强减小,故使过滤速率加快。
回流装置
图2由于冷凝管竖立,使液体混合物能冷凝回流,若以此容器作反应容器,可使反应物能循环
利用,提高了反应物的转化率。
2.利用“启普发生器”原理的制气装置创新
①装置的优点是:能做到随开随用,随关随停。
②使用范围:块状固体与液体反应生成气体,反应不需要加热,且生成的气体难溶于水。这些
装置能制取的气体有H(Zn—稀HSO),CO(CaCO—稀盐酸)、HS(FeS—稀HSO)。
2 2 4 2 3 2 2 4
(2)“固(液)+液 气体”装置的创新图1的改进优点是能控制反应液的温度。
图2的改进优点是使圆底烧瓶和分液漏斗中的气体压强相等,便于液体流下。
3.“块状固体+液体 气体”装置的创新
大试管内的小试管中盛有液体反应物,起液封的作用,防止气体从长颈漏斗中逸出,这样设计
可节约试剂。
(4)试管形状的创新
改进的目的:用于加热易熔化的固体物质的分解,这样可有效地防止固体熔化时造成液体的
流动,如草酸晶体受热分解制取CO 气体。
2
4.排液集气装置的创新
从a管进气b管出水可收集难溶于水的气体,如H 、O 等。若将广口瓶中的液体更换,还可
2 2
以收集以下气体:
(1)饱和食盐水——收集Cl。
2
(2)饱和NaHCO 溶液——收集CO。
3 2
(3)饱和NaHS溶液——收集HS。
2
(4)四氯化碳——收集HCl或NH。
3三.气体制备装置的连接
1..仪器连接顺序:
气体发生装置→洗气装置→干燥装置→化学反应装置→干燥装置→尾气吸收装置或
气体发生装置→洗气装置→性质检验装置(或收集装置)→尾气处理装置
接口的连接:总体做到“自下而上,从左到右”。
净化装置应“长”进“短”出:
量气装置应“短”进“长”出:
干燥管应“粗”进“细”出
2.常见气体制备装置的连接
Cl 的实验室制备系统
2
SO 的实验室制备系统
2
NH 的实验室制备系统
3高考实例剖析
高考实例剖析--
高考怎么考《化学实验基础》,根据高考指挥棒来学习《化学实验基
础》
一、装置图正误判断
1. 仪器辨认
2. 操作正误判断:回流、过滤、蒸馏、萃取分液、灼烧、加热、排除气泡、滴定操作、测
量反应热操作、配制溶液、胶头滴管的使用等,
【高考实例一】
1.(2021年河北高考试题)下列操作规范且能达到实验目的的是
A.图甲测定醋酸浓度 B.图乙测定中和热
C.图丙稀释浓硫酸 D.图丁萃取分离碘水中的碘
【实战演练】
1.(2022·河南洛阳·三模)下列图示不能用于物质分离提纯操作的是A. B.
C. D.
2.(2022·安徽合肥·三模)下列做法或实验(图中部分夹持装置已省略),能达到目的的是
A B C D
橡皮管能减小气体体 分离碘和四氯化 浓硫酸与萤石(主要成分 防止铁管道被腐
积测量的误差 碳的混合液 为CaF )加热制备HF 蚀
2
二、常见气体的制备、净化和收集装置和方法的正误判断
1、气体的制备装置正误判断
2、气体的除杂、净化、收集装置正误判断
3、气体的性质检验
4、尾气处理:防倒吸
【高考实例二】
2.(2021年全国高考乙卷)在实验室采用如图装置制备气体,合理的是化学试剂 制备的气体
A
B (浓)
C
D (浓)
【实战演练】
1.(2022·广东卷)实验室用 和浓盐酸反应生成 后,按照净化、收集、性质检验
及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是
2.(2022·安徽蚌埠·模拟预测)实验室制取下列气体,所选反应试剂、制备装置与收集方
法合理的是选项 气体 反应试剂 制备装置 收集方法
A NH Ca(OH) 、NH Cl a e
3 2 4
B Cl MnO 、浓盐酸 c d
2 2
C NO Cu、浓硝酸 c d
D SO Na SO 、70%硫酸 b f
2 2 3
三、表格式实验题--实验方案设计现象结论正误判断
表格实验题常见问题:
一、性质比较
1.比较酸碱性,结合H+的能力和酸性强弱
2.比较反应速率:过量问题和温度高低
3.比较Ksp
4比较氧化性强弱
5.与酸(或HO)的活泼性,比较金属活泼性
2
6.比较非金属性
7.比较水解常数,水解程度大小
二、产物验证、检验
1. Cl 不具有漂白性
2
2. 离子检验方法
3. 制乙烯的产物验证
4. 制备物质:如乙酸乙酯,溴苯
5. 制备高浓度的次氯酸
三.产物检验和离子检验
1.卤代烃检验卤素离子
2.石蜡裂解
3.漂白性问题
4.淀粉水解
5.蔗糖碳化
四、实验操作
1.分离除杂:蒸馏、萃取2.PH值的测定问题
3.原电池、金属腐蚀
4.气体的制法、收集
5.喷泉实验
6.配制溶液
7.铝热反应
8.清洗仪器
【高考实例三】
3.(2022·全国乙卷)由实验操作和现象,可得出相应正确结论的是
实验操作 现象 结论
向NaBr溶液中滴加过量氯水,再加入淀 先变橙色,后变蓝 氧化性:
A
粉KI溶液 色 Cl Br I
2 2 2
向蔗糖溶液中滴加稀硫酸,水浴加热,加
B 无砖红色沉淀 蔗糖未发生水解
Cu(OH)
入新制的 2悬浊液
Br
石蜡油加强热,将产生的气体通入 2的 气体中含有不饱和
C 溶液红棕色变无色
CCl 烃
4溶液
试管口润湿的蓝色 氯乙烯加聚是可逆
D 加热试管中的聚氯乙烯薄膜碎片
石蕊试纸变红 反应
【实战演练】
1.(2022·安徽芜湖·三模)下列各组实验中,用所给玻璃仪器和试剂不能完成实验目的的
是(非玻璃仪器任选)
实验目的 玻璃仪器 试剂
配制500mL1mol·L-1NaOH 烧杯、玻璃棒、量筒、500mL
A NaOH固体、蒸馏水
溶液 容量瓶、胶头滴管
冰醋酸、无水乙醇、饱
B 制备乙酸乙酯 试管、量筒、导管、酒精灯
和Na CO 溶液
2 3
除去NaBr溶液中的少量 烧杯、玻璃棒、胶头滴管、分
C 溴水、CCl
NaI 液漏斗 4
圆底烧瓶、导气管、烧杯、胶 干燥的二氧化碳气体、
D 模拟喷泉实验
头滴管 浓NaOH溶液
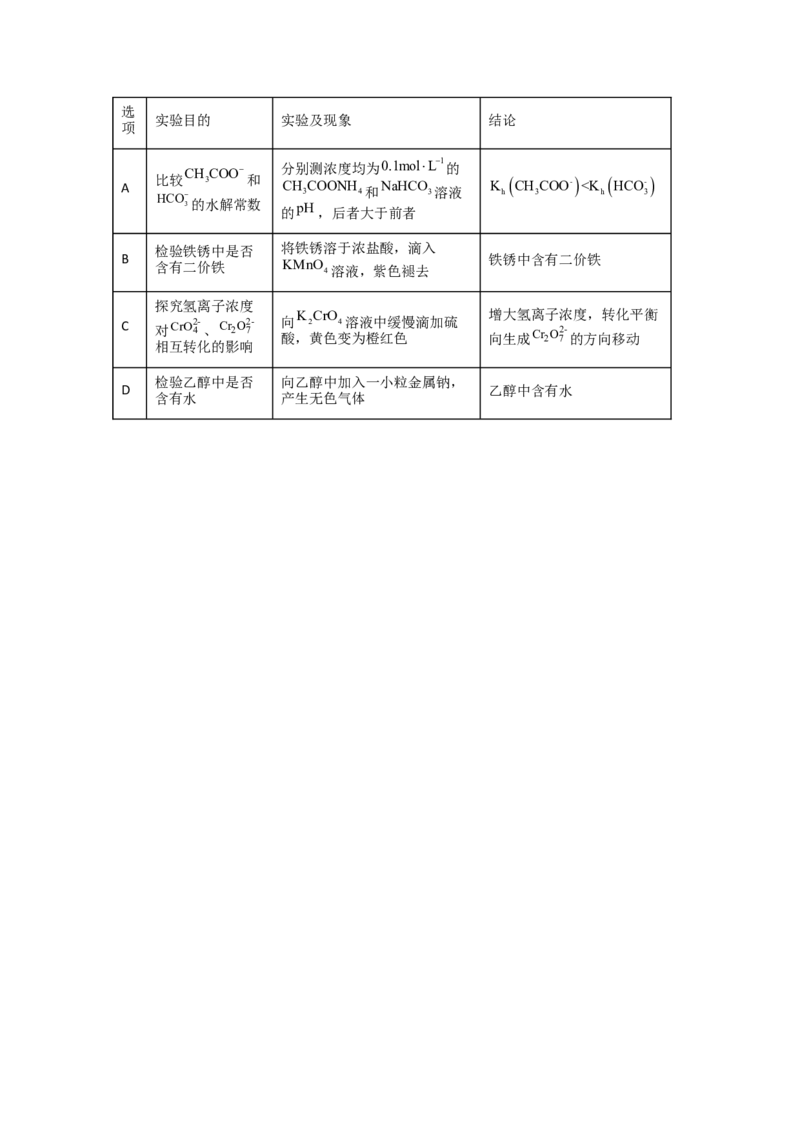
2.(2022·全国甲卷)根据实验目的,下列实验及现象、结论都正确的是选
实验目的 实验及现象 结论
项
CH COO
分别测浓度均为0.1molL1
的
A 比 HC 较 O 3 和 CH 3 COONH 4和 NaHCO 3溶液 K h CH 3 COO-