文档内容
2025新教材化学高考第一轮
专题十三 盐类水解和沉淀溶解平衡
1.苯甲酸(PhCOOH)是一种弱酸,用于制备防腐剂苯甲酸钠,下列说法正确的是( )
A.稀释苯甲酸钠溶液,溶液的pH减小
B.苯甲酸钠的溶液中:c(PhCOOH)+c(OH-)=c(H+)+c(Na+)
C.常温下,1 L pH=4.00的苯甲酸溶液中,水电离出的c(H+)为1.0×10-4mol·L-1
D.用NaOH溶液滴定苯甲酸溶液测浓度时,用甲基橙作指示剂
2.常温下,向饱和氯水中以恒定速率滴加NaOH溶液,测得溶液的pH随时间的变化如下图
所示,溶液中氯元素的存在形式仅考虑Cl 、Cl-、ClO-、HClO,该过程不考虑HClO的分解,
2
下列说法错误的是( )
A.M点:c(H+)>c(Cl-)>c(HClO)
B.N点:c(Na+)=c(Cl-)+c(ClO-)
c(HClO)
C.从M点到P点, 逐渐减小
c(ClO-)
D.从M点到P点,水的电离程度逐渐增大
3.室温下,以氟磷灰石[Ca (PO ) F]为原料,经酸浸、转化可得到 Ca(H PO ) 、H PO 和
5 4 3 2 4 2 3 4
HF。已知:25 ℃,H PO 的pK =2.12、pK =7.21、pK =12.36(pK =-lgK )。下列说法不正
3 4 a a a a a
1 2 3
确的是( )
A.Ca (PO ) F的沉淀溶解平衡可表示为Ca (PO ) F(s) 5Ca2+(aq)+3PO3−(aq)+F-(aq)
5 4 3 5 4 3 4
B.酸浸过程中溶液pH=6时,c(H PO- )c(NO- )>c(OH-)>c(H+)
2 2
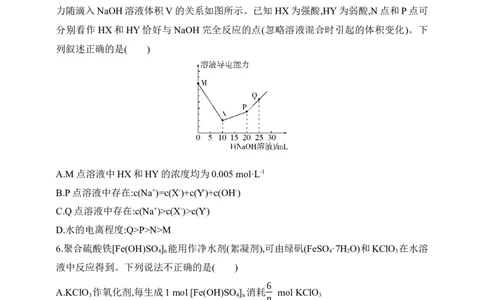
5.常温下,用0.01 mol·L-1的NaOH溶液滴定10 mL HX和HY的混合酸,测得溶液的导电能
力随滴入NaOH溶液体积V的关系如图所示。已知HX为强酸,HY为弱酸,N点和P点可
分别看作HX和HY恰好与NaOH完全反应的点(忽略溶液混合时引起的体积变化)。下
列叙述正确的是( )
A.M点溶液中HX和HY的浓度均为0.005 mol·L-1
B.P点溶液中存在:c(Na+)=c(X-)+c(Y-)+c(OH-)
C.Q点溶液中存在:c(Na+)>c(X-)>c(Y-)
D.水的电离程度:Q>P>N>M
6.聚合硫酸铁[Fe(OH)SO ] 能用作净水剂(絮凝剂),可由绿矾(FeSO ·7H O)和KClO 在水溶
4 n 4 2 3
液中反应得到。下列说法不正确的是( )
6
A.KClO 作氧化剂,每生成1 mol [Fe(OH)SO ] 消耗 mol KClO
3 4 n n 3
B.生成聚合硫酸铁后,水溶液的pH增大
C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强
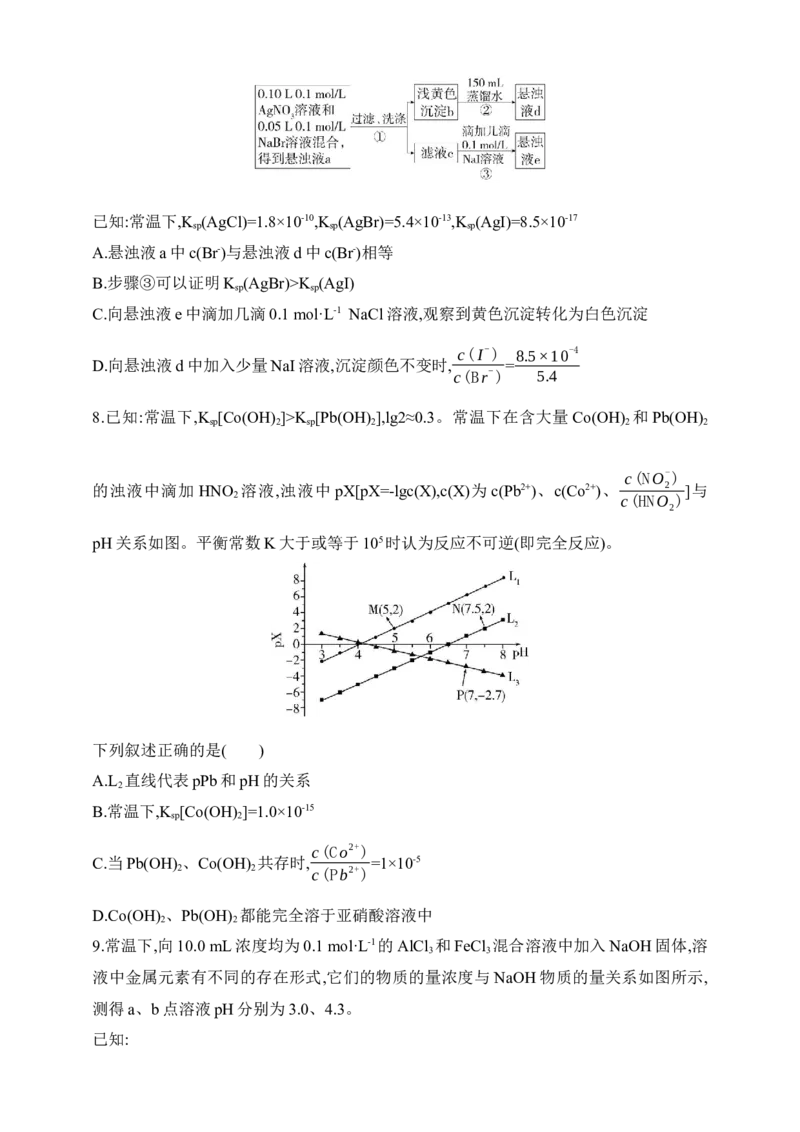
7.某中学化学社进行沉淀溶解平衡相关实验,操作流程如下。下列说法正确的是( )已知:常温下,K (AgCl)=1.8×10-10,K (AgBr)=5.4×10-13,K (AgI)=8.5×10-17
sp sp sp
A.悬浊液a中c(Br-)与悬浊液d中c(Br-)相等
B.步骤③可以证明K (AgBr)>K (AgI)
sp sp
C.向悬浊液e中滴加几滴0.1 mol·L-1 NaCl溶液,观察到黄色沉淀转化为白色沉淀
c(I-) 8.5×10-4
D.向悬浊液d中加入少量NaI溶液,沉淀颜色不变时, =
c(Br-) 5.4
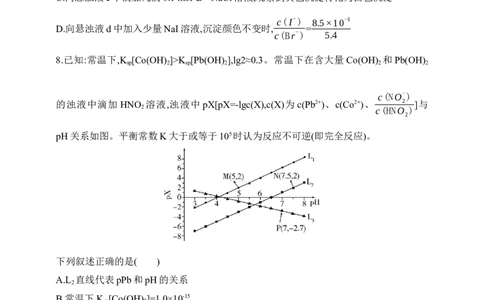
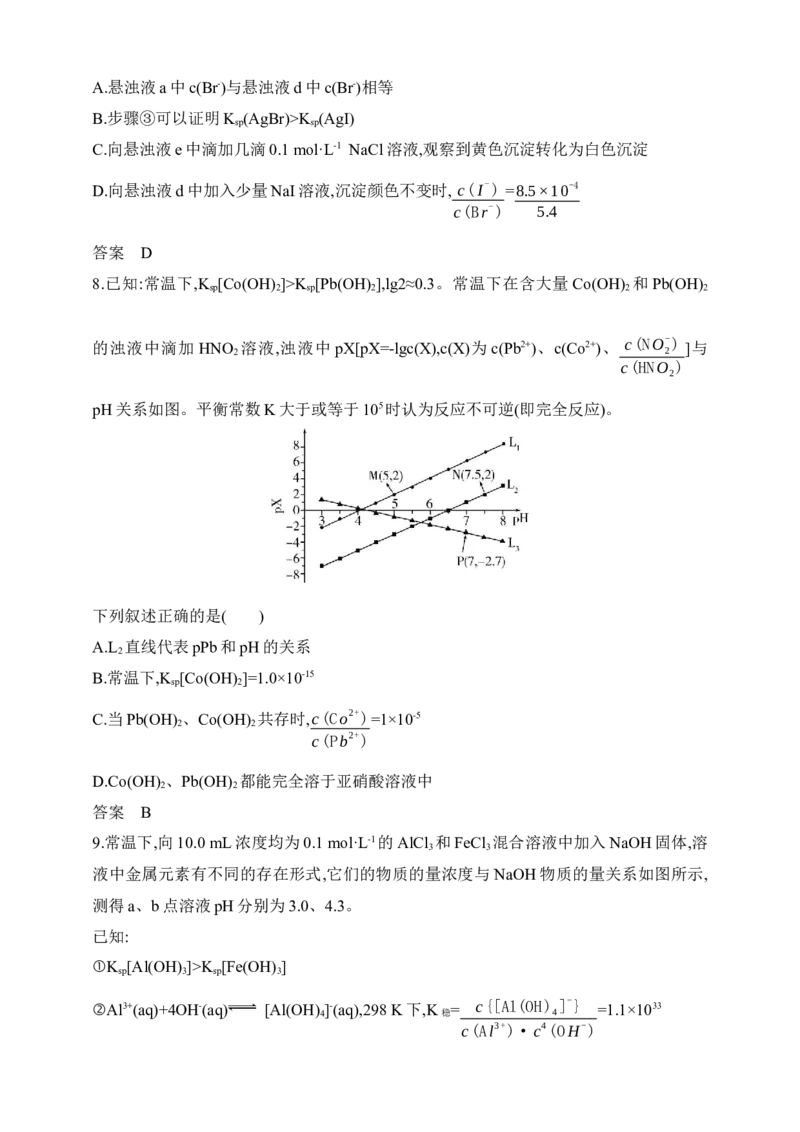
8.已知:常温下,K [Co(OH) ]>K [Pb(OH) ],lg2≈0.3。常温下在含大量Co(OH) 和Pb(OH)
sp 2 sp 2 2 2
c(NO-)
的浊液中滴加 HNO 溶液,浊液中 pX[pX=-lgc(X),c(X)为 c(Pb2+)、c(Co2+)、 2 ]与
2 c(HNO )
2
pH关系如图。平衡常数K大于或等于105时认为反应不可逆(即完全反应)。
下列叙述正确的是( )
A.L 直线代表pPb和pH的关系
2
B.常温下,K [Co(OH) ]=1.0×10-15
sp 2
c(Co2+)
C.当Pb(OH) 、Co(OH) 共存时, =1×10-5
2 2 c(Pb2+)
D.Co(OH) 、Pb(OH) 都能完全溶于亚硝酸溶液中
2 2
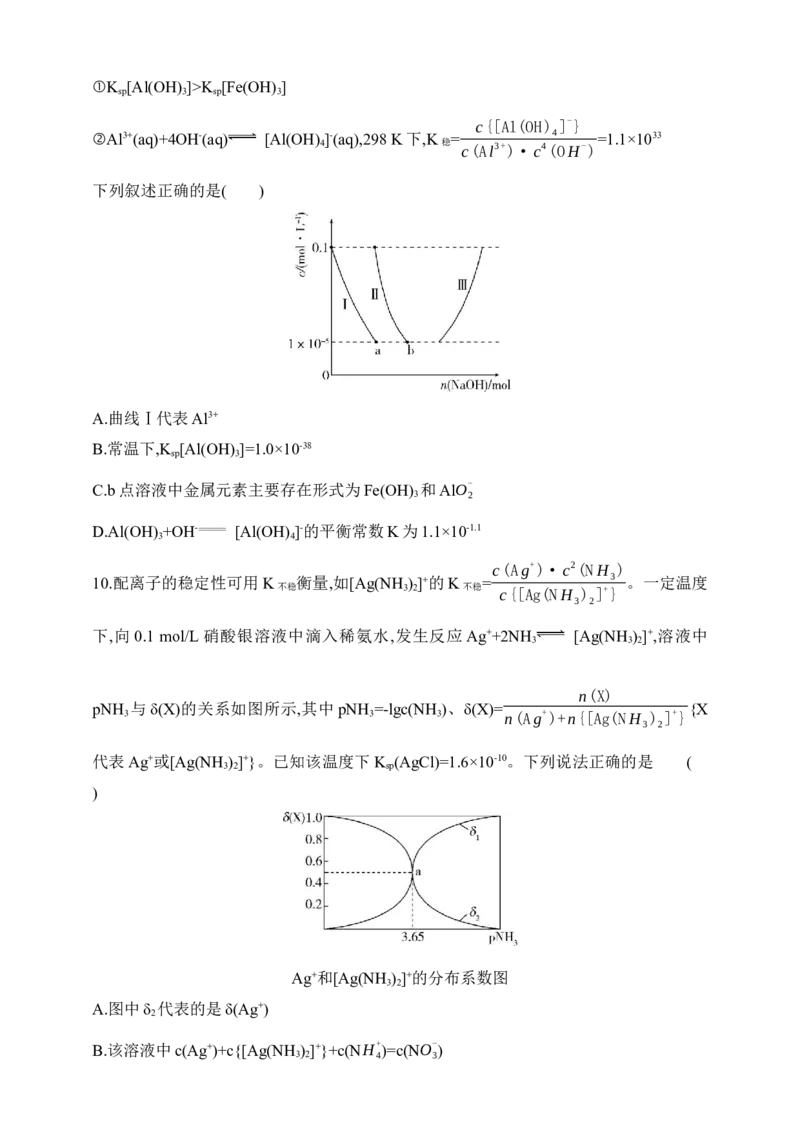
9.常温下,向10.0 mL浓度均为0.1 mol·L-1的AlCl 和FeCl 混合溶液中加入NaOH固体,溶
3 3
液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,
测得a、b点溶液pH分别为3.0、4.3。
已知:①K [Al(OH) ]>K [Fe(OH) ]
sp 3 sp 3
c{[Al(OH) ]-}
②Al3+(aq)+4OH-(aq) [Al(OH)
4
]-(aq),298 K下,K
稳
=
c(Al3+)·c4(
4
OH-)
=1.1×1033
下列叙述正确的是( )
A.曲线Ⅰ代表Al3+
B.常温下,K [Al(OH) ]=1.0×10-38
sp 3
C.b点溶液中金属元素主要存在形式为Fe(OH) 和AlO-
3 2
D.Al(OH) +OH- [Al(OH) ]-的平衡常数K为1.1×10-1.1
3 4
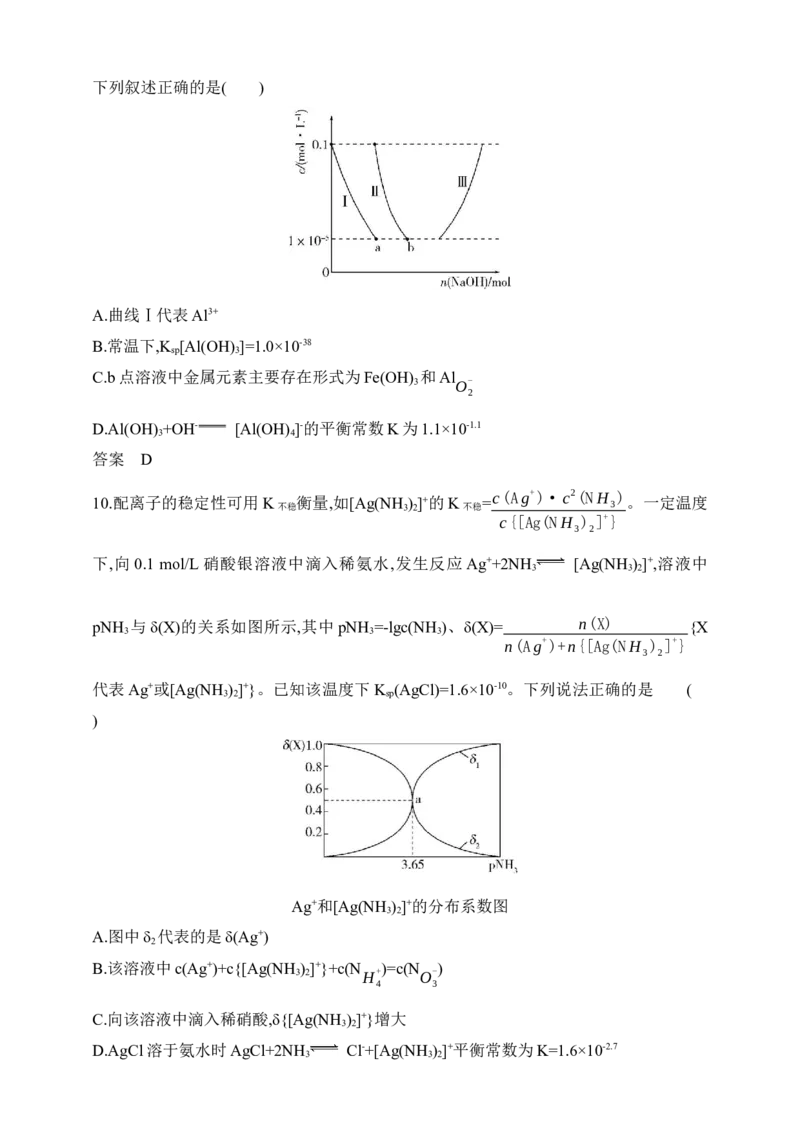
c(Ag+)·c2(NH )
10.配离子的稳定性可用K 衡量,如[Ag(NH ) ]+的K = 3 。一定温度
不稳 3 2 不稳 c{[Ag(NH ) ]+}
3 2
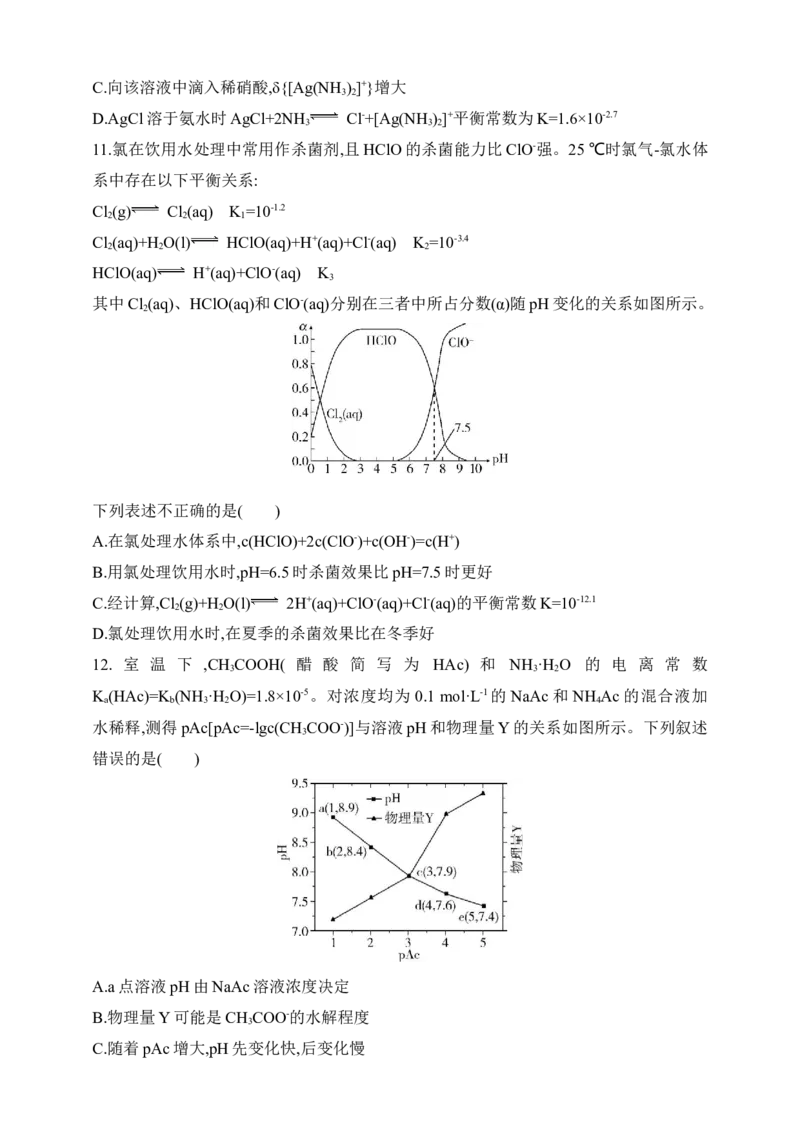
下,向 0.1 mol/L 硝酸银溶液中滴入稀氨水,发生反应 Ag++2NH [Ag(NH ) ]+,溶液中
3 3 2
n(X)
pNH 与δ(X)的关系如图所示,其中pNH =-lgc(NH )、δ(X)= {X
3 3 3 n(Ag+)+n{[Ag(NH ) ]+}
3 2
代表Ag+或[Ag(NH ) ]+}。已知该温度下K (AgCl)=1.6×10-10。下列说法正确的是 (
3 2 sp
)
Ag+和[Ag(NH ) ]+的分布系数图
3 2
A.图中δ 代表的是δ(Ag+)
2
B.该溶液中c(Ag+)+c{[Ag(NH ) ]+}+c(NH+ )=c(NO- )
3 2 4 3C.向该溶液中滴入稀硝酸,δ{[Ag(NH ) ]+}增大
3 2
D.AgCl溶于氨水时AgCl+2NH Cl-+[Ag(NH ) ]+平衡常数为K=1.6×10-2.7
3 3 2
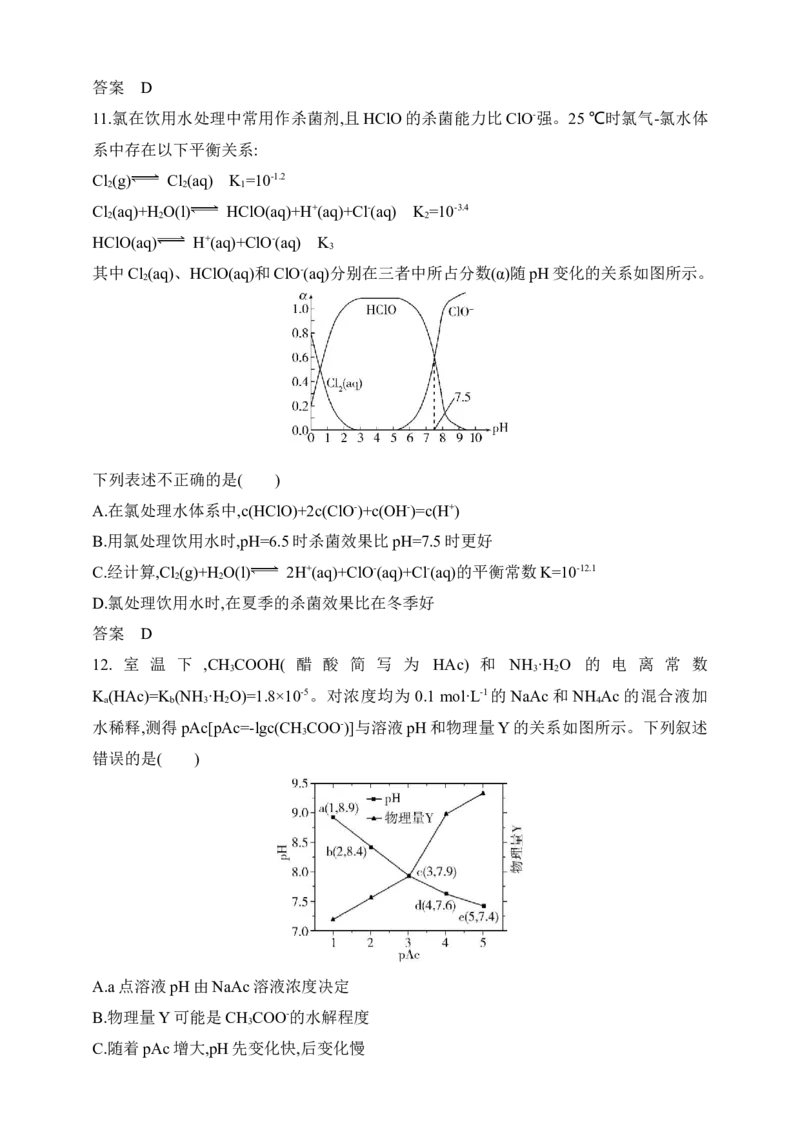
11.氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25 ℃时氯气-氯水体
系中存在以下平衡关系:
Cl (g) Cl (aq) K =10-1.2
2 2 1
Cl (aq)+H O(l) HClO(aq)+H+(aq)+Cl-(aq) K =10-3.4
2 2 2
HClO(aq) H+(aq)+ClO-(aq) K
3
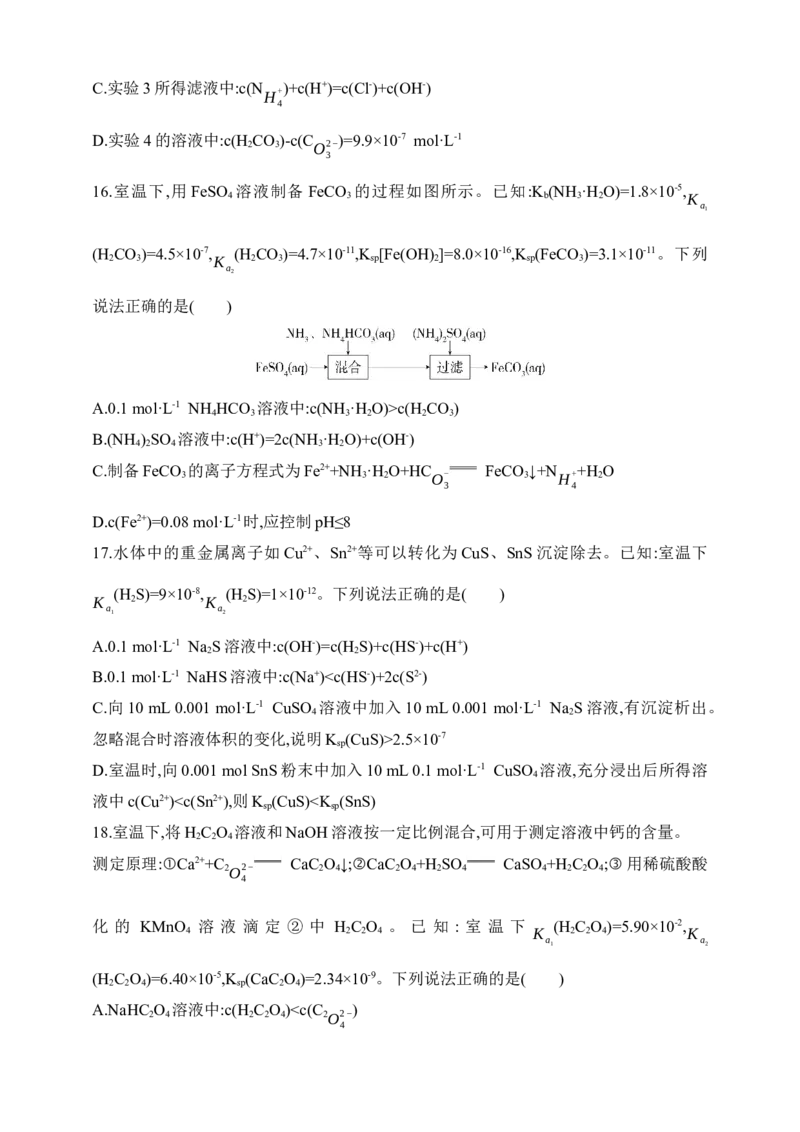
其中Cl (aq)、HClO(aq)和ClO-(aq)分别在三者中所占分数(α)随pH变化的关系如图所示。
2
下列表述不正确的是( )
A.在氯处理水体系中,c(HClO)+2c(ClO-)+c(OH-)=c(H+)
B.用氯处理饮用水时,pH=6.5时杀菌效果比pH=7.5时更好
C.经计算,Cl (g)+H O(l) 2H+(aq)+ClO-(aq)+Cl-(aq)的平衡常数K=10-12.1
2 2
D.氯处理饮用水时,在夏季的杀菌效果比在冬季好
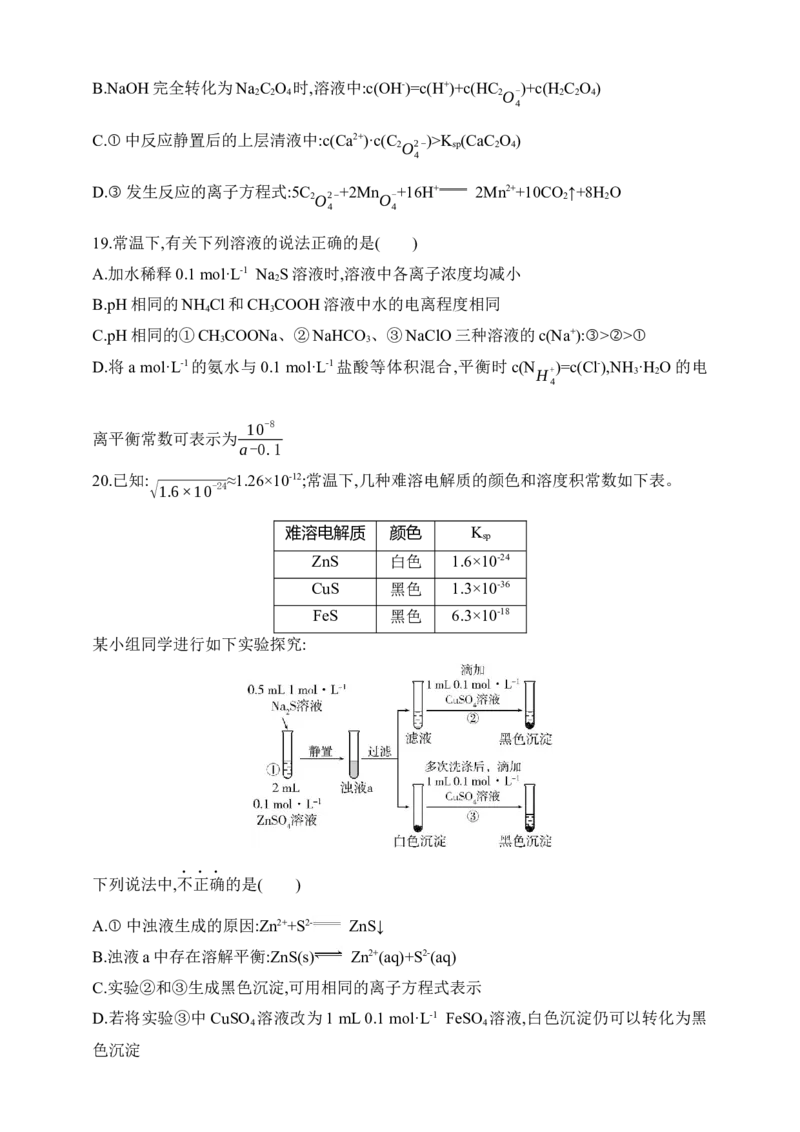
12. 室 温 下 ,CH COOH( 醋 酸 简 写 为 HAc) 和 NH ·H O 的 电 离 常 数
3 3 2
K (HAc)=K (NH ·H O)=1.8×10-5。对浓度均为 0.1 mol·L-1的 NaAc 和 NH Ac 的混合液加
a b 3 2 4
水稀释,测得pAc[pAc=-lgc(CH COO-)]与溶液pH和物理量Y的关系如图所示。下列叙述
3
错误的是( )
A.a点溶液pH由NaAc溶液浓度决定
B.物理量Y可能是CH COO-的水解程度
3
C.随着pAc增大,pH先变化快,后变化慢D.随着pAc无限增大,混合溶液pH可小于7
13.室温下,用0.1 mol·L-1Na SO 溶液吸收废气中的SO ,并获得BaSO 的过程如图所示。
2 3 2 3
忽略吸收废气所引起的溶液体积变化和 H O 的挥发,溶液中含硫物种的浓度 c
2 总
=c(H SO )+c(HS )+c(S )。已知: (H SO )=1.54×10-2, (H SO )=1.02×10-7。下列说
2 3 O- O2− K 2 3 K 2 3
3 3 a 1 a 2
法正确的是 ( )
A.0.1 mol·L-1 Na SO 溶液吸收SO 至pH=7的溶液:c(HS )
sp 3
c(SO2−)
3
D.沉淀后的上层清液久置:2c(Ba2+)+c(Na+)+c(H+)=c(OH-)+2c(S )+c(HS )
O2− O-
3 3
14.用一定浓度 NaOH溶液吸收H S可制备Na S或NaHS。若通入H S所引起的溶液体
2 2 2
积变化和H O挥发可忽略,溶液中含硫物种的浓度c =c(H S)+c(HS-)+c(S2-)。室温下,H S
2 总 2 2
的电离常数分别为 =1.1×10-7、 =1.3×10-13。下列说法正确的是( )
K K
a a
1 2
A.Na S溶液显碱性的原因:S2-+2H O H S+2OH-
2 2 2
B.NaOH恰好转化为Na S的溶液中:c(OH-)=c(H+)+c(HS-)+c(S2-)
2
C.吸收所得c =c(Na+)的溶液中:c(H S)>c(S2-)
总 2
D.NaOH溶液吸收H S过程中,溶液的温度下降
2
15.室温下,某兴趣小组通过下列实验制备少量NaHCO 并探究其性质。
3
实验1:测得100 mL 14 mol·L-1氨水的pH约为12。
实验2:向上述氨水中加NaCl粉末至饱和,通入足量CO 后析出晶体。
2
实验3:将所得混合物静置后过滤、洗涤、干燥,得到NaHCO 。
3
实验4:配制100 mL一定浓度的NaHCO 溶液,测得pH为8.0。
3
下列说法正确的是( )
A.依据实验1推测K (NH ·H O)约为7×10-26
b 3 2
B.依据实验2推测溶解度:NaHCO >NaCl
3C.实验3所得滤液中:c(N )+c(H+)=c(Cl-)+c(OH-)
H+
4
D.实验4的溶液中:c(H CO )-c(C )=9.9×10-7 mol·L-1
2 3 O2−
3
16.室温下,用 FeSO 溶液制备 FeCO 的过程如图所示。已知:K (NH ·H O)=1.8×10-5,
4 3 b 3 2 K
a
1
(H CO )=4.5×10-7, (H CO )=4.7×10-11,K [Fe(OH) ]=8.0×10-16,K (FeCO )=3.1×10-11。下列
2 3 K 2 3 sp 2 sp 3
a
2
说法正确的是( )
A.0.1 mol·L-1 NH HCO 溶液中:c(NH ·H O)>c(H CO )
4 3 3 2 2 3
B.(NH ) SO 溶液中:c(H+)=2c(NH ·H O)+c(OH-)
4 2 4 3 2
C.制备FeCO 的离子方程式为Fe2++NH ·H O+HC FeCO ↓+N +H O
3 3 2 O- 3 H+ 2
3 4
D.c(Fe2+)=0.08 mol·L-1时,应控制pH≤8
17.水体中的重金属离子如 Cu2+、Sn2+等可以转化为CuS、SnS沉淀除去。已知:室温下
(H S)=9×10-8, (H S)=1×10-12。下列说法正确的是( )
K 2 K 2
a a
1 2
A.0.1 mol·L-1 Na S溶液中:c(OH-)=c(H S)+c(HS-)+c(H+)
2 2
B.0.1 mol·L-1 NaHS溶液中:c(Na+)2.5×10-7
sp
D.室温时,向0.001 mol SnS粉末中加入10 mL 0.1 mol·L-1 CuSO 溶液,充分浸出后所得溶
4
液中c(Cu2+)K (CaC O )
2O2− sp 2 4
4
D.③发生反应的离子方程式:5C
2O2−
+2Mn
O-
+16H+ 2Mn2++10CO
2
↑+8H
2
O
4 4
19.常温下,有关下列溶液的说法正确的是( )
A.加水稀释0.1 mol·L-1 Na S溶液时,溶液中各离子浓度均减小
2
B.pH相同的NH Cl和CH COOH溶液中水的电离程度相同
4 3
C.pH相同的①CH COONa、②NaHCO 、③NaClO三种溶液的c(Na+):③>②>①
3 3
D.将a mol·L-1的氨水与0.1 mol·L-1盐酸等体积混合,平衡时c(N )=c(Cl-),NH ·H O的电
H+ 3 2
4
10-8
离平衡常数可表示为
a-0.1
20.已知: ≈1.26×10-12;常温下,几种难溶电解质的颜色和溶度积常数如下表。
√1.6×10-24
难溶电解质 颜色 K
sp
ZnS 白色 1.6×10-24
CuS 黑色 1.3×10-36
FeS 黑色 6.3×10-18
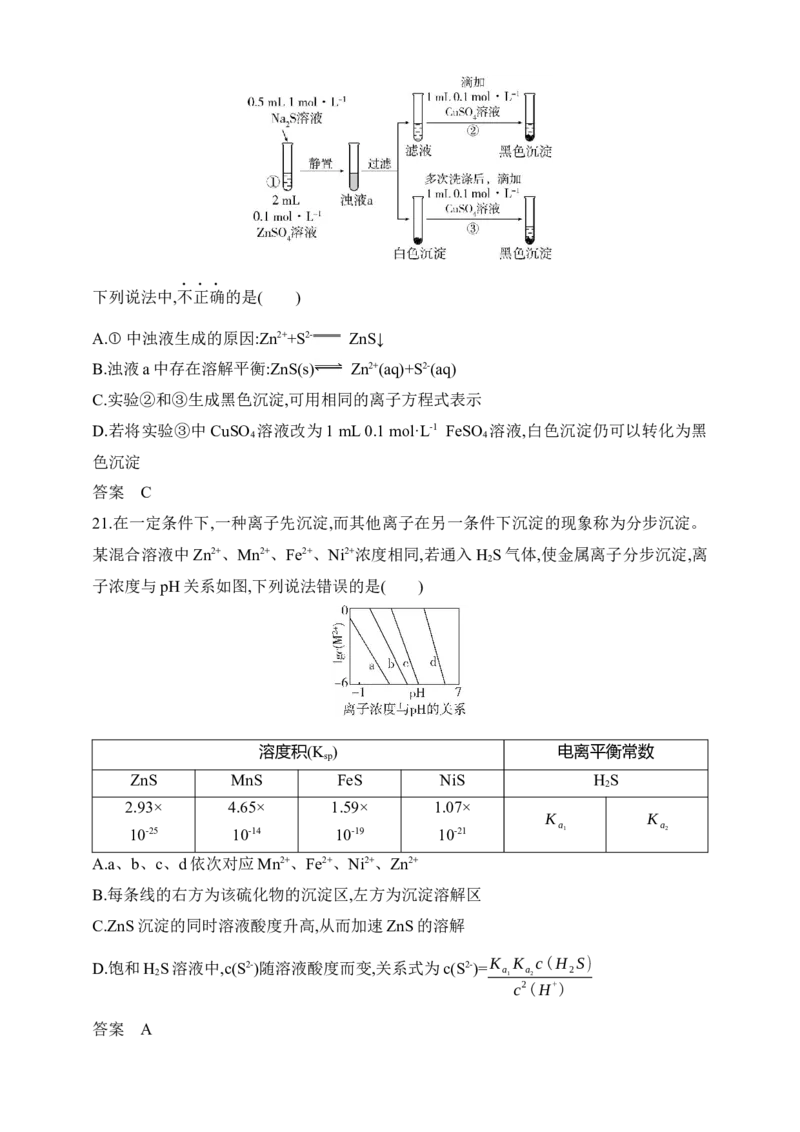
某小组同学进行如下实验探究:
下列说法中,不正确的是( )
A.①中浊液生成的原因:Zn2++S2- ZnS↓
B.浊液a中存在溶解平衡:ZnS(s) Zn2+(aq)+S2-(aq)
C.实验②和③生成黑色沉淀,可用相同的离子方程式表示
D.若将实验③中CuSO 溶液改为1 mL 0.1 mol·L-1 FeSO 溶液,白色沉淀仍可以转化为黑
4 4
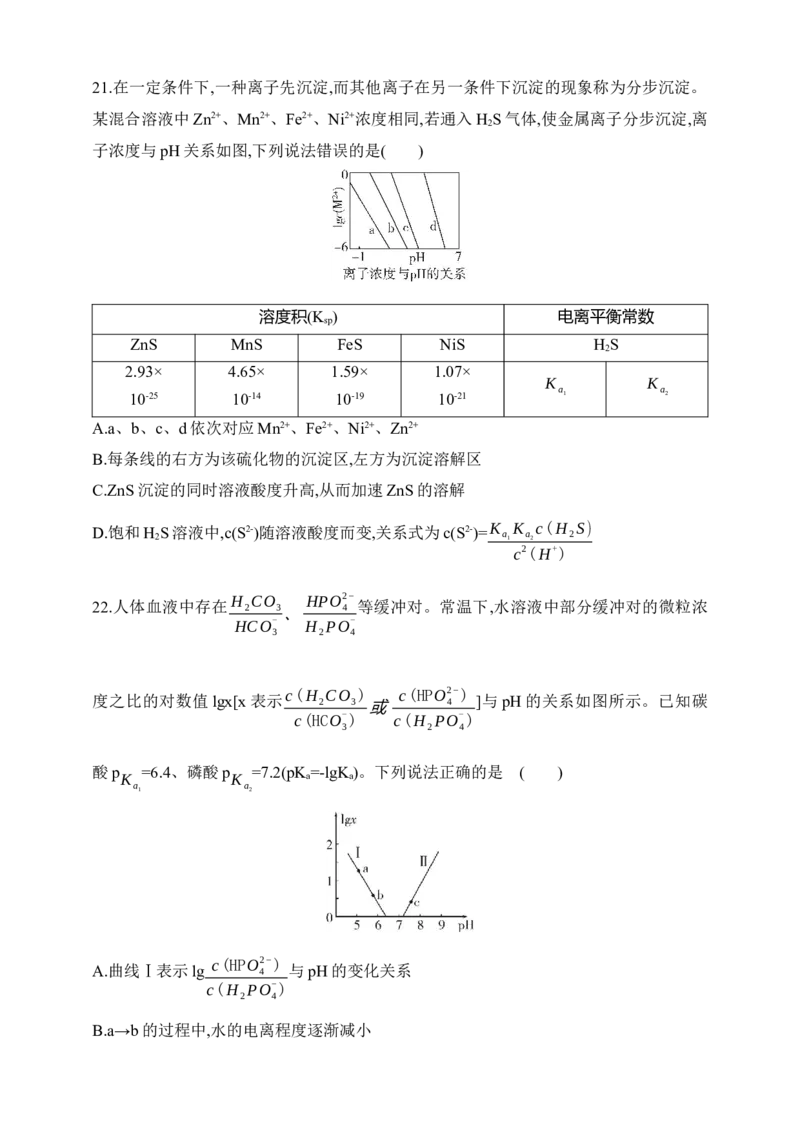
色沉淀21.在一定条件下,一种离子先沉淀,而其他离子在另一条件下沉淀的现象称为分步沉淀。
某混合溶液中Zn2+、Mn2+、Fe2+、Ni2+浓度相同,若通入H S气体,使金属离子分步沉淀,离
2
子浓度与pH关系如图,下列说法错误的是( )
溶度积(K ) 电离平衡常数
sp
ZnS MnS FeS NiS H S
2
2.93× 4.65× 1.59× 1.07×
K K
a a
10-25 10-14 10-19 10-21 1 2
A.a、b、c、d依次对应Mn2+、Fe2+、Ni2+、Zn2+
B.每条线的右方为该硫化物的沉淀区,左方为沉淀溶解区
C.ZnS沉淀的同时溶液酸度升高,从而加速ZnS的溶解
D.饱和H S溶液中,c(S2-)随溶液酸度而变,关系式为c(S2-)= K K c(H S)
2 a 1 a 2 2
c2(H+)
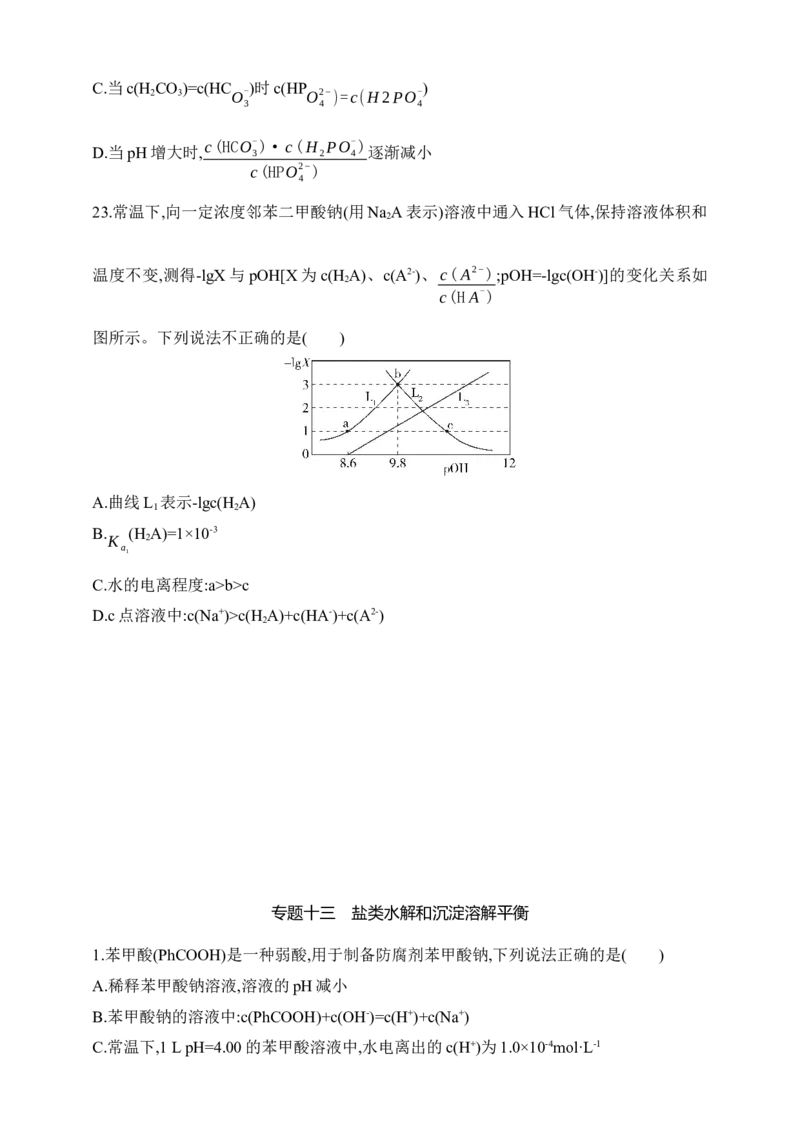
H CO HPO2−
22.人体血液中存在
2 3、 4
等缓冲对。常温下,水溶液中部分缓冲对的微粒浓
HCO- H PO-
3 2 4
c(H CO ) c(HPO2−)
度之比的对数值lgx[x表示
2 3 或 4
]与pH的关系如图所示。已知碳
c(HCO-) c(H PO-)
3 2 4
酸p =6.4、磷酸p =7.2(pK =-lgK )。下列说法正确的是 ( )
K K a a
a a
1 2
c(HPO2−)
A.曲线Ⅰ表示lg
4
与pH的变化关系
c(H PO-)
2 4
B.a→b的过程中,水的电离程度逐渐减小C.当c(H CO )=c(HC )时c(HP )
2 3 O- O2− )=c(H2PO-
3 4 4
c(HCO-)·c(H PO-)
D.当pH增大时,
3 2 4
逐渐减小
c(HPO2−)
4
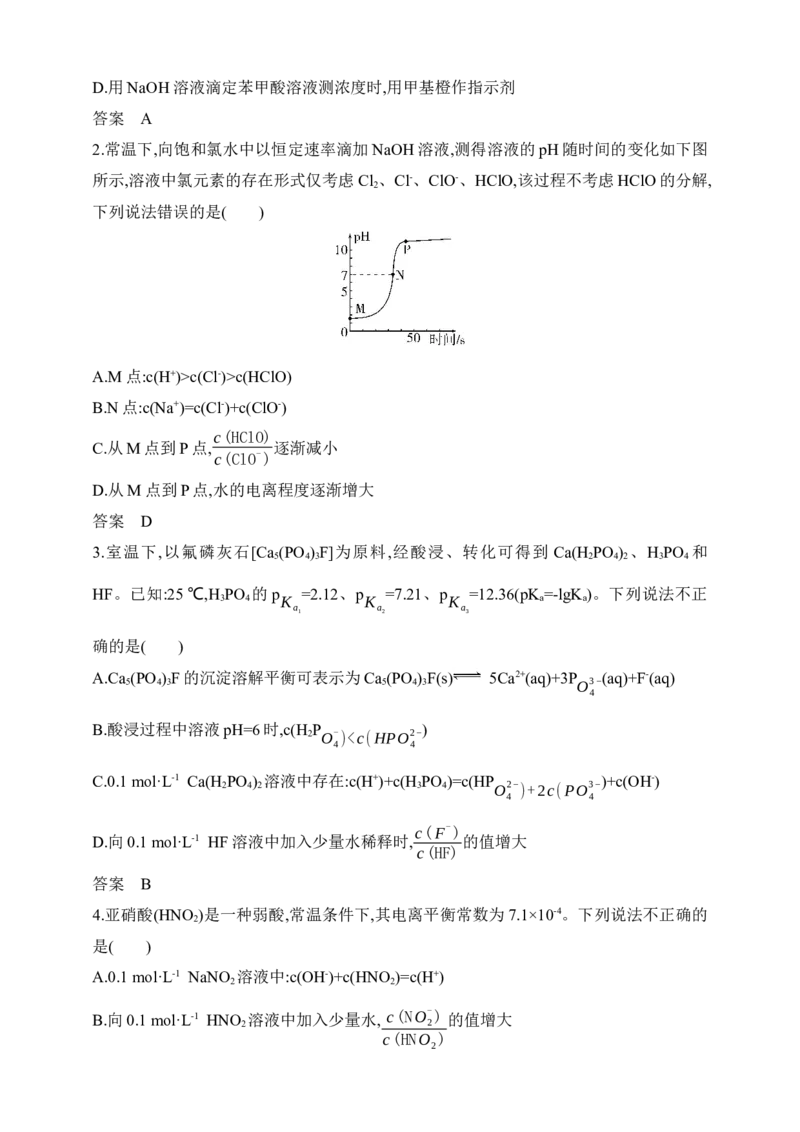
23.常温下,向一定浓度邻苯二甲酸钠(用Na A表示)溶液中通入HCl气体,保持溶液体积和
2
温度不变,测得-lgX与pOH[X为c(H A)、c(A2-)、c(A2−);pOH=-lgc(OH-)]的变化关系如
2
c(HA-)
图所示。下列说法不正确的是( )
A.曲线L 表示-lgc(H A)
1 2
B. (H A)=1×10-3
K 2
a
1
C.水的电离程度:a>b>c
D.c点溶液中:c(Na+)>c(H A)+c(HA-)+c(A2-)
2
专题十三 盐类水解和沉淀溶解平衡
1.苯甲酸(PhCOOH)是一种弱酸,用于制备防腐剂苯甲酸钠,下列说法正确的是( )
A.稀释苯甲酸钠溶液,溶液的pH减小
B.苯甲酸钠的溶液中:c(PhCOOH)+c(OH-)=c(H+)+c(Na+)
C.常温下,1 L pH=4.00的苯甲酸溶液中,水电离出的c(H+)为1.0×10-4mol·L-1D.用NaOH溶液滴定苯甲酸溶液测浓度时,用甲基橙作指示剂
答案 A
2.常温下,向饱和氯水中以恒定速率滴加NaOH溶液,测得溶液的pH随时间的变化如下图
所示,溶液中氯元素的存在形式仅考虑Cl 、Cl-、ClO-、HClO,该过程不考虑HClO的分解,
2
下列说法错误的是( )
A.M点:c(H+)>c(Cl-)>c(HClO)
B.N点:c(Na+)=c(Cl-)+c(ClO-)
c(HClO)
C.从M点到P点, 逐渐减小
c(ClO-)
D.从M点到P点,水的电离程度逐渐增大
答案 D
3.室温下,以氟磷灰石[Ca (PO ) F]为原料,经酸浸、转化可得到 Ca(H PO ) 、H PO 和
5 4 3 2 4 2 3 4
HF。已知:25 ℃,H PO 的p =2.12、p =7.21、p =12.36(pK =-lgK )。下列说法不正
3 4 K K K a a
a a a
1 2 3
确的是( )
A.Ca (PO ) F的沉淀溶解平衡可表示为Ca (PO ) F(s) 5Ca2+(aq)+3P (aq)+F-(aq)
5 4 3 5 4 3 O3−
4
B.酸浸过程中溶液pH=6时,c(H P )
2 O- )c(N )>c(OH-)>c(H+)
2 O-
2
答案 A
5.常温下,用0.01 mol·L-1的NaOH溶液滴定10 mL HX和HY的混合酸,测得溶液的导电能
力随滴入NaOH溶液体积V的关系如图所示。已知HX为强酸,HY为弱酸,N点和P点可
分别看作HX和HY恰好与NaOH完全反应的点(忽略溶液混合时引起的体积变化)。下
列叙述正确的是( )
A.M点溶液中HX和HY的浓度均为0.005 mol·L-1
B.P点溶液中存在:c(Na+)=c(X-)+c(Y-)+c(OH-)
C.Q点溶液中存在:c(Na+)>c(X-)>c(Y-)
D.水的电离程度:Q>P>N>M
答案 C
6.聚合硫酸铁[Fe(OH)SO ] 能用作净水剂(絮凝剂),可由绿矾(FeSO ·7H O)和KClO 在水溶
4 n 4 2 3
液中反应得到。下列说法不正确的是( )
6
A.KClO 作氧化剂,每生成1 mol [Fe(OH)SO ] 消耗 mol KClO
3 4 n 3
n
B.生成聚合硫酸铁后,水溶液的pH增大
C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强
答案 A
7.某中学化学社进行沉淀溶解平衡相关实验,操作流程如下。下列说法正确的是( )
已知:常温下,K (AgCl)=1.8×10-10,K (AgBr)=5.4×10-13,K (AgI)=8.5×10-17
sp sp spA.悬浊液a中c(Br-)与悬浊液d中c(Br-)相等
B.步骤③可以证明K (AgBr)>K (AgI)
sp sp
C.向悬浊液e中滴加几滴0.1 mol·L-1 NaCl溶液,观察到黄色沉淀转化为白色沉淀
D.向悬浊液d中加入少量NaI溶液,沉淀颜色不变时, c(I-) =8.5×10-4
c(Br-) 5.4
答案 D
8.已知:常温下,K [Co(OH) ]>K [Pb(OH) ],lg2≈0.3。常温下在含大量Co(OH) 和Pb(OH)
sp 2 sp 2 2 2
的浊液中滴加 HNO 溶液,浊液中 pX[pX=-lgc(X),c(X)为 c(Pb2+)、c(Co2+)、
c(NO-)
]与
2 2
c(HNO )
2
pH关系如图。平衡常数K大于或等于105时认为反应不可逆(即完全反应)。
下列叙述正确的是( )
A.L 直线代表pPb和pH的关系
2
B.常温下,K [Co(OH) ]=1.0×10-15
sp 2
C.当Pb(OH) 、Co(OH) 共存时,c(Co2+)=1×10-5
2 2
c(Pb2+)
D.Co(OH) 、Pb(OH) 都能完全溶于亚硝酸溶液中
2 2
答案 B
9.常温下,向10.0 mL浓度均为0.1 mol·L-1的AlCl 和FeCl 混合溶液中加入NaOH固体,溶
3 3
液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,
测得a、b点溶液pH分别为3.0、4.3。
已知:
①K [Al(OH) ]>K [Fe(OH) ]
sp 3 sp 3
②Al3+(aq)+4OH-(aq) [Al(OH)
4
]-(aq),298 K下,K
稳
= c{[Al(OH)
4
]-} =1.1×1033
c(Al3+)·c4(OH-)下列叙述正确的是( )
A.曲线Ⅰ代表Al3+
B.常温下,K [Al(OH) ]=1.0×10-38
sp 3
C.b点溶液中金属元素主要存在形式为Fe(OH) 和Al
3 O-
2
D.Al(OH) +OH- [Al(OH) ]-的平衡常数K为1.1×10-1.1
3 4
答案 D
c(Ag+)·c2(NH )
10.配离子的稳定性可用K 不稳 衡量,如[Ag(NH 3 ) 2 ]+的K 不稳 = 3 。一定温度
c{[Ag(NH ) ]+}
3 2
下,向 0.1 mol/L 硝酸银溶液中滴入稀氨水,发生反应 Ag++2NH [Ag(NH ) ]+,溶液中
3 3 2
pNH 与δ(X)的关系如图所示,其中pNH =-lgc(NH )、δ(X)= n(X) {X
3 3 3
n(Ag+)+n{[Ag(NH ) ]+}
3 2
代表Ag+或[Ag(NH ) ]+}。已知该温度下K (AgCl)=1.6×10-10。下列说法正确的是 (
3 2 sp
)
Ag+和[Ag(NH ) ]+的分布系数图
3 2
A.图中δ 代表的是δ(Ag+)
2
B.该溶液中c(Ag+)+c{[Ag(NH ) ]+}+c(N )=c(N )
3 2 H+ O-
4 3
C.向该溶液中滴入稀硝酸,δ{[Ag(NH ) ]+}增大
3 2
D.AgCl溶于氨水时AgCl+2NH Cl-+[Ag(NH ) ]+平衡常数为K=1.6×10-2.7
3 3 2答案 D
11.氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25 ℃时氯气-氯水体
系中存在以下平衡关系:
Cl (g) Cl (aq) K =10-1.2
2 2 1
Cl (aq)+H O(l) HClO(aq)+H+(aq)+Cl-(aq) K =10-3.4
2 2 2
HClO(aq) H+(aq)+ClO-(aq) K
3
其中Cl (aq)、HClO(aq)和ClO-(aq)分别在三者中所占分数(α)随pH变化的关系如图所示。
2
下列表述不正确的是( )
A.在氯处理水体系中,c(HClO)+2c(ClO-)+c(OH-)=c(H+)
B.用氯处理饮用水时,pH=6.5时杀菌效果比pH=7.5时更好
C.经计算,Cl (g)+H O(l) 2H+(aq)+ClO-(aq)+Cl-(aq)的平衡常数K=10-12.1
2 2
D.氯处理饮用水时,在夏季的杀菌效果比在冬季好
答案 D
12. 室 温 下 ,CH COOH( 醋 酸 简 写 为 HAc) 和 NH ·H O 的 电 离 常 数
3 3 2
K (HAc)=K (NH ·H O)=1.8×10-5。对浓度均为 0.1 mol·L-1的 NaAc 和 NH Ac 的混合液加
a b 3 2 4
水稀释,测得pAc[pAc=-lgc(CH COO-)]与溶液pH和物理量Y的关系如图所示。下列叙述
3
错误的是( )
A.a点溶液pH由NaAc溶液浓度决定
B.物理量Y可能是CH COO-的水解程度
3
C.随着pAc增大,pH先变化快,后变化慢D.随着pAc无限增大,混合溶液pH可小于7
答案 D
13.室温下,用0.1 mol·L-1Na SO 溶液吸收废气中的SO ,并获得BaSO 的过程如图所示。
2 3 2 3
忽略吸收废气所引起的溶液体积变化和 H O 的挥发,溶液中含硫物种的浓度 c
2 总
=c(H SO )+c(HS )+c(S )。已知: (H SO )=1.54×10-2, (H SO )=1.02×10-7。下列说
2 3 O- O2− K 2 3 K 2 3
3 3 a 1 a 2
法正确的是 ( )
A.0.1 mol·L-1 Na SO 溶液吸收SO 至pH=7的溶液:c(HS )
sp 3
c(SO2−)
3
D.沉淀后的上层清液久置:2c(Ba2+)+c(Na+)+c(H+)=c(OH-)+2c(S )+c(HS )
O2− O-
3 3
答案 A
14.用一定浓度 NaOH溶液吸收H S可制备Na S或NaHS。若通入H S所引起的溶液体
2 2 2
积变化和H O挥发可忽略,溶液中含硫物种的浓度c =c(H S)+c(HS-)+c(S2-)。室温下,H S
2 总 2 2
的电离常数分别为 =1.1×10-7、 =1.3×10-13。下列说法正确的是( )
K K
a a
1 2
A.Na S溶液显碱性的原因:S2-+2H O H S+2OH-
2 2 2
B.NaOH恰好转化为Na S的溶液中:c(OH-)=c(H+)+c(HS-)+c(S2-)
2
C.吸收所得c =c(Na+)的溶液中:c(H S)>c(S2-)
总 2
D.NaOH溶液吸收H S过程中,溶液的温度下降
2
答案 C
15.室温下,某兴趣小组通过下列实验制备少量NaHCO 并探究其性质。
3
实验1:测得100 mL 14 mol·L-1氨水的pH约为12。
实验2:向上述氨水中加NaCl粉末至饱和,通入足量CO 后析出晶体。
2
实验3:将所得混合物静置后过滤、洗涤、干燥,得到NaHCO 。
3
实验4:配制100 mL一定浓度的NaHCO 溶液,测得pH为8.0。
3下列说法正确的是( )
A.依据实验1推测K (NH ·H O)约为7×10-26
b 3 2
B.依据实验2推测溶解度:NaHCO >NaCl
3
C.实验3所得滤液中:c(N )+c(H+)=c(Cl-)+c(OH-)
H+
4
D.实验4的溶液中:c(H CO )-c(C )=9.9×10-7 mol·L-1
2 3 O2−
3
答案 D
16.室温下,用 FeSO 溶液制备 FeCO 的过程如图所示。已知:K (NH ·H O)=1.8×10-5,
4 3 b 3 2 K
a
1
(H CO )=4.5×10-7, (H CO )=4.7×10-11,K [Fe(OH) ]=8.0×10-16,K (FeCO )=3.1×10-11。下列
2 3 K 2 3 sp 2 sp 3
a
2
说法正确的是( )
A.0.1 mol·L-1 NH HCO 溶液中:c(NH ·H O)>c(H CO )
4 3 3 2 2 3
B.(NH ) SO 溶液中:c(H+)=2c(NH ·H O)+c(OH-)
4 2 4 3 2
C.制备FeCO 的离子方程式为Fe2++NH ·H O+HC FeCO ↓+N +H O
3 3 2 O- 3 H+ 2
3 4
D.c(Fe2+)=0.08 mol·L-1时,应控制pH≤8
答案 C
17.水体中的重金属离子如 Cu2+、Sn2+等可以转化为CuS、SnS沉淀除去。已知:室温下
(H S)=9×10-8, (H S)=1×10-12。下列说法正确的是( )
K 2 K 2
a a
1 2
A.0.1 mol·L-1 Na S溶液中:c(OH-)=c(H S)+c(HS-)+c(H+)
2 2
B.0.1 mol·L-1 NaHS溶液中:c(Na+)2.5×10-7
sp
D.室温时,向0.001 mol SnS粉末中加入10 mL 0.1 mol·L-1 CuSO 溶液,充分浸出后所得溶
4
液中c(Cu2+)K (CaC O )
2O2− sp 2 4
4
D.③发生反应的离子方程式:5C
2O2−
+2Mn
O-
+16H+ 2Mn2++10CO
2
↑+8H
2
O
4 4
答案 A
19.常温下,有关下列溶液的说法正确的是( )
A.加水稀释0.1 mol·L-1 Na S溶液时,溶液中各离子浓度均减小
2
B.pH相同的NH Cl和CH COOH溶液中水的电离程度相同
4 3
C.pH相同的①CH COONa、②NaHCO 、③NaClO三种溶液的c(Na+):③>②>①
3 3
D.将a mol·L-1的氨水与0.1 mol·L-1盐酸等体积混合,平衡时c(N )=c(Cl-),NH ·H O的电
H+ 3 2
4
10-8
离平衡常数可表示为
a-0.1
答案 D
20.已知: ≈1.26×10-12;常温下,几种难溶电解质的颜色和溶度积常数如下表。
√1.6×10-24
难溶电解质 颜色 K
sp
ZnS 白色 1.6×10-24
CuS 黑色 1.3×10-36
FeS 黑色 6.3×10-18
某小组同学进行如下实验探究:下列说法中,不正确的是( )
A.①中浊液生成的原因:Zn2++S2- ZnS↓
B.浊液a中存在溶解平衡:ZnS(s) Zn2+(aq)+S2-(aq)
C.实验②和③生成黑色沉淀,可用相同的离子方程式表示
D.若将实验③中CuSO 溶液改为1 mL 0.1 mol·L-1 FeSO 溶液,白色沉淀仍可以转化为黑
4 4
色沉淀
答案 C
21.在一定条件下,一种离子先沉淀,而其他离子在另一条件下沉淀的现象称为分步沉淀。
某混合溶液中Zn2+、Mn2+、Fe2+、Ni2+浓度相同,若通入H S气体,使金属离子分步沉淀,离
2
子浓度与pH关系如图,下列说法错误的是( )
溶度积(K ) 电离平衡常数
sp
ZnS MnS FeS NiS H S
2
2.93× 4.65× 1.59× 1.07×
K K
a a
10-25 10-14 10-19 10-21 1 2
A.a、b、c、d依次对应Mn2+、Fe2+、Ni2+、Zn2+
B.每条线的右方为该硫化物的沉淀区,左方为沉淀溶解区
C.ZnS沉淀的同时溶液酸度升高,从而加速ZnS的溶解
D.饱和H S溶液中,c(S2-)随溶液酸度而变,关系式为c(S2-)= K K c(H S)
2 a 1 a 2 2
c2(H+)
答案 AH CO HPO2−
22.人体血液中存在
2 3、 4
等缓冲对。常温下,水溶液中部分缓冲对的微粒浓
HCO- H PO-
3 2 4
c(H CO ) c(HPO2−)
度之比的对数值lgx[x表示
2 3 或 4
]与pH的关系如图所示。已知碳
c(HCO-) c(H PO-)
3 2 4
酸p =6.4、磷酸p =7.2(pK =-lgK )。下列说法正确的是 ( )
K K a a
a a
1 2
c(HPO2−)
A.曲线Ⅰ表示lg
4
与pH的变化关系
c(H PO-)
2 4
B.a→b的过程中,水的电离程度逐渐减小
C.当c(H CO )=c(HC )时c(HP )
2 3 O- O2− )=c(H2PO-
3 4 4
c(HCO-)·c(H PO-)
D.当pH增大时,
3 2 4
逐渐减小
c(HPO2−)
4
答案 D
23.常温下,向一定浓度邻苯二甲酸钠(用Na A表示)溶液中通入HCl气体,保持溶液体积和
2
温度不变,测得-lgX与pOH[X为c(H A)、c(A2-)、c(A2−);pOH=-lgc(OH-)]的变化关系如
2
c(HA-)
图所示。下列说法不正确的是( )
A.曲线L 表示-lgc(H A)
1 2
B. (H A)=1×10-3
K 2
a
1C.水的电离程度:a>b>c
D.c点溶液中:c(Na+)>c(H A)+c(HA-)+c(A2-)
2
答案 A