文档内容
电化学中的多室、多池装置
(选择题1~5题,每小题3分,6~12题,每小题5分,共50分)
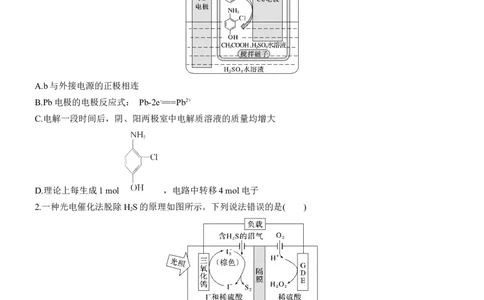
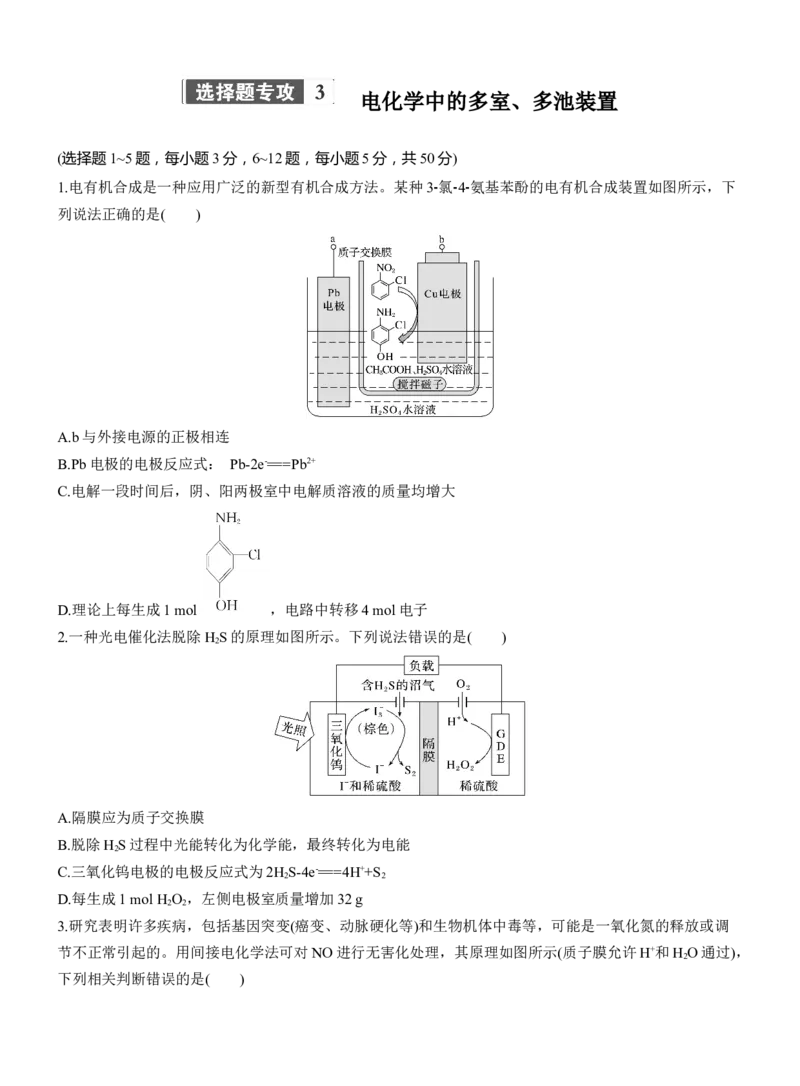
1.电有机合成是一种应用广泛的新型有机合成方法。某种3⁃ 氯 ⁃4⁃ 氨基苯酚的电有机合成装置如图所示,下
列说法正确的是( )
A.b与外接电源的正极相连
B.Pb电极的电极反应式: Pb-2e-===Pb2+
C.电解一段时间后,阴、阳两极室中电解质溶液的质量均增大
D.理论上每生成1 mol ,电路中转移4 mol电子
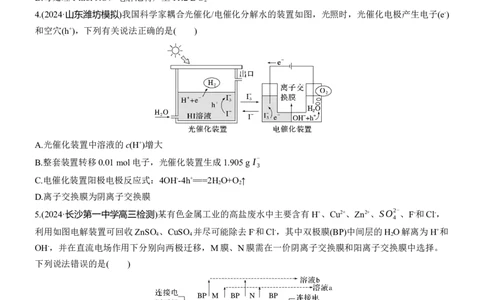
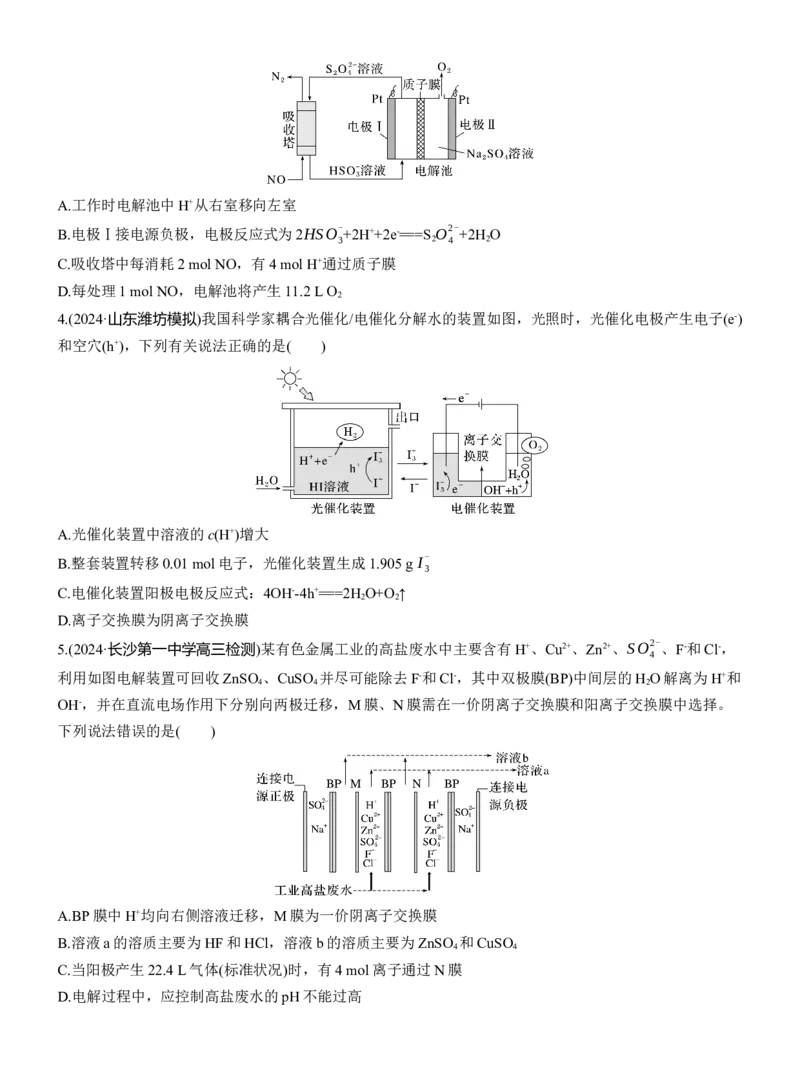
2.一种光电催化法脱除H S的原理如图所示。下列说法错误的是( )
2
A.隔膜应为质子交换膜
B.脱除H S过程中光能转化为化学能,最终转化为电能
2
C.三氧化钨电极的电极反应式为2H S-4e-===4H++S
2 2
D.每生成1 mol H O ,左侧电极室质量增加32 g
2 2
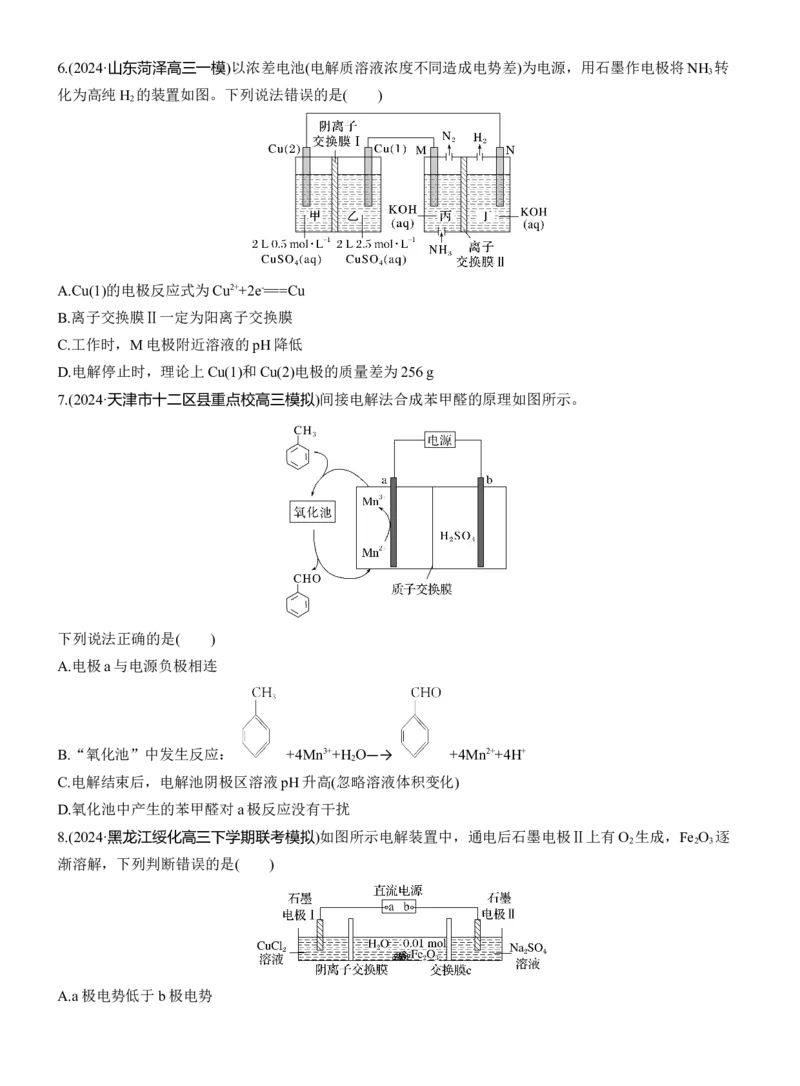
3.研究表明许多疾病,包括基因突变(癌变、动脉硬化等)和生物机体中毒等,可能是一氧化氮的释放或调
节不正常引起的。用间接电化学法可对NO进行无害化处理,其原理如图所示(质子膜允许H+和H O通过),
2
下列相关判断错误的是( )A.工作时电解池中H+从右室移向左室
B.电极Ⅰ接电源负极,电极反应式为2HSO-
+2H++2e-===S
O2-
+2H O
3 2 4 2
C.吸收塔中每消耗2 mol NO,有4 mol H+通过质子膜
D.每处理1 mol NO,电解池将产生11.2 L O
2
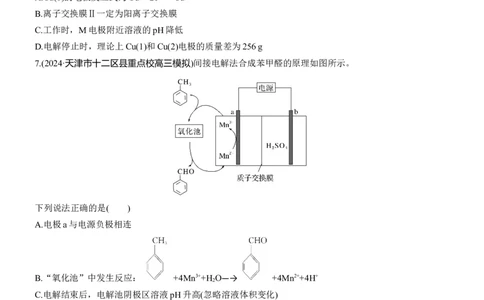
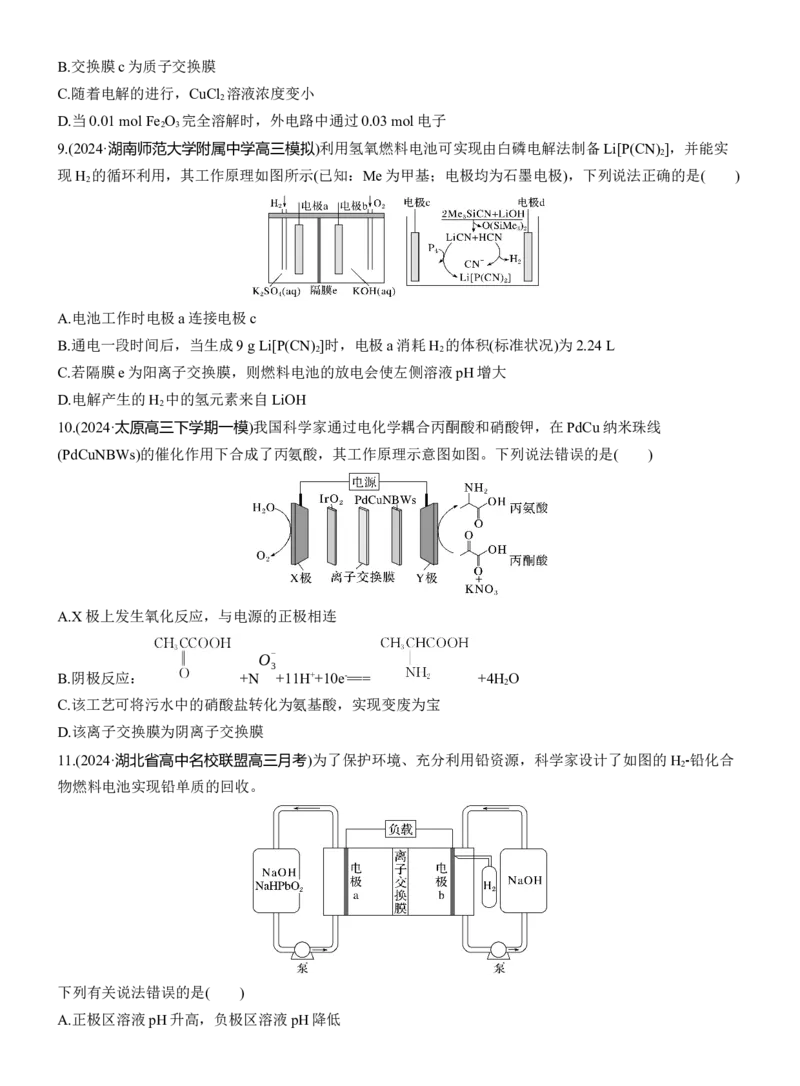
4.(2024·山东潍坊模拟)我国科学家耦合光催化/电催化分解水的装置如图,光照时,光催化电极产生电子(e-)
和空穴(h+),下列有关说法正确的是( )
A.光催化装置中溶液的c(H+)增大
B.整套装置转移0.01 mol电子,光催化装置生成1.905 g
I-
3
C.电催化装置阳极电极反应式:4OH--4h+===2H O+O ↑
2 2
D.离子交换膜为阴离子交换膜
5.(2024·长沙第一中学高三检测)某有色金属工业的高盐废水中主要含有H+、Cu2+、Zn2+、SO2-
、F-和Cl-,
4
利用如图电解装置可回收ZnSO 、CuSO 并尽可能除去F-和Cl-,其中双极膜(BP)中间层的H O解离为H+和
4 4 2
OH-,并在直流电场作用下分别向两极迁移,M膜、N膜需在一价阴离子交换膜和阳离子交换膜中选择。
下列说法错误的是( )
A.BP膜中H+均向右侧溶液迁移,M膜为一价阴离子交换膜
B.溶液a的溶质主要为HF和HCl,溶液b的溶质主要为ZnSO 和CuSO
4 4
C.当阳极产生22.4 L气体(标准状况)时,有4 mol离子通过N膜
D.电解过程中,应控制高盐废水的pH不能过高6.(2024·山东菏泽高三一模)以浓差电池(电解质溶液浓度不同造成电势差)为电源,用石墨作电极将NH 转
3
化为高纯H 的装置如图。下列说法错误的是( )
2
A.Cu(1)的电极反应式为Cu2++2e-===Cu
B.离子交换膜Ⅱ一定为阳离子交换膜
C.工作时,M电极附近溶液的pH降低
D.电解停止时,理论上Cu(1)和Cu(2)电极的质量差为256 g
7.(2024·天津市十二区县重点校高三模拟)间接电解法合成苯甲醛的原理如图所示。
下列说法正确的是( )
A.电极a与电源负极相连
B.“氧化池”中发生反应: +4Mn3++H O―→ +4Mn2++4H+
2
C.电解结束后,电解池阴极区溶液pH升高(忽略溶液体积变化)
D.氧化池中产生的苯甲醛对a极反应没有干扰
8.(2024·黑龙江绥化高三下学期联考模拟)如图所示电解装置中,通电后石墨电极Ⅱ上有O 生成,Fe O 逐
2 2 3
渐溶解,下列判断错误的是( )
A.a极电势低于b极电势B.交换膜c为质子交换膜
C.随着电解的进行,CuCl 溶液浓度变小
2
D.当0.01 mol Fe O 完全溶解时,外电路中通过0.03 mol电子
2 3
9.(2024·湖南师范大学附属中学高三模拟)利用氢氧燃料电池可实现由白磷电解法制备Li[P(CN) ],并能实
2
现H 的循环利用,其工作原理如图所示(已知:Me为甲基;电极均为石墨电极),下列说法正确的是( )
2
A.电池工作时电极a连接电极c
B.通电一段时间后,当生成9 g Li[P(CN) ]时,电极a消耗H 的体积(标准状况)为2.24 L
2 2
C.若隔膜e为阳离子交换膜,则燃料电池的放电会使左侧溶液pH增大
D.电解产生的H 中的氢元素来自LiOH
2
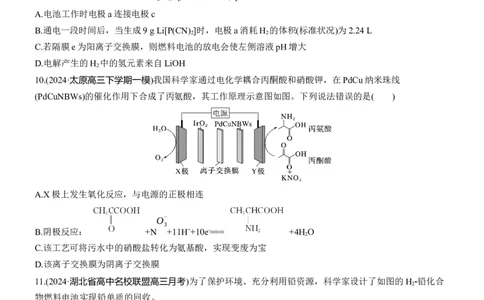
10.(2024·太原高三下学期一模)我国科学家通过电化学耦合丙酮酸和硝酸钾,在PdCu纳米珠线
(PdCuNBWs)的催化作用下合成了丙氨酸,其工作原理示意图如图。下列说法错误的是( )
A.X极上发生氧化反应,与电源的正极相连
O-
3
B.阴极反应: +N +11H++10e-=== +4H O
2
C.该工艺可将污水中的硝酸盐转化为氨基酸,实现变废为宝
D.该离子交换膜为阴离子交换膜
11.(2024·湖北省高中名校联盟高三月考)为了保护环境、充分利用铅资源,科学家设计了如图的H
2⁃
铅化合
物燃料电池实现铅单质的回收。
下列有关说法错误的是( )
A.正极区溶液pH升高,负极区溶液pH降低B.电子流向:电极b→负载→电极a
C.正极区电极反应式为HPbO-
+H O+2e-===Pb+3OH-
2 2
D.为了提高Pb的回收率,离子交换膜为阴离子交换膜
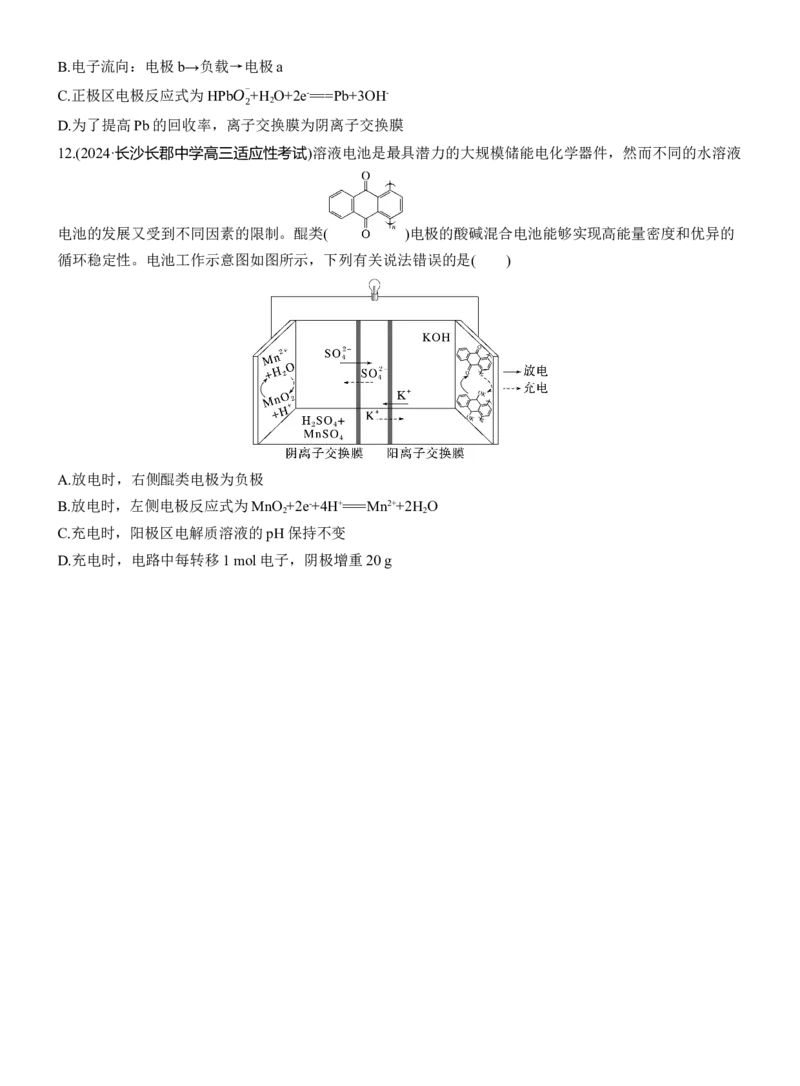
12.(2024·长沙长郡中学高三适应性考试)溶液电池是最具潜力的大规模储能电化学器件,然而不同的水溶液
电池的发展又受到不同因素的限制。醌类( )电极的酸碱混合电池能够实现高能量密度和优异的
循环稳定性。电池工作示意图如图所示,下列有关说法错误的是( )
A.放电时,右侧醌类电极为负极
B.放电时,左侧电极反应式为MnO +2e-+4H+===Mn2++2H O
2 2
C.充电时,阳极区电解质溶液的pH保持不变
D.充电时,电路中每转移1 mol电子,阴极增重20 g答案精析
1.D
2.C
[由图分析可知,三氧化钨电极上I-转化为I- ,失电子,为负极,I-
与H S反应生成S 和I-,从而碘元
3 3 2 2
素相关物质实现循环反应,并将H S转化为S ,GDE电极上H+和O 参与电极反应生成H O ,得电子,为
2 2 2 2 2
正极。左侧酸性条件下H S生成S 时有H+产生,而右侧电极反应消耗H+,故隔膜应为质子交换膜,A正
2 2
确;三氧化钨电极的电极反应式为3I--2e-===I-
,H
S和I-
发生化学反应生成S 和I-,C错误;正极每生成1
3 2 3 2
mol H O ,得2 mol电子,故负极失去2 mol电子,生成1 mol
I- ,由反应2I-
+2H S===S +6I-+4H+可知生成
2 2 3 3 2 2
0.5 mol S ,0.5 mol S 为32 g,且生成的H+迁移到右侧电极室,左侧电极室质量增加32 g,D正确。]
2 2
3.D [从图中可以看出,电极Ⅱ中H O失去电子生成O 和H+,连接电源正极,为阳极;电极Ⅰ得到电子,
2 2
将HSO-
转化为S
O2- ,连接电源负极为阴极。电极Ⅰ为阴极,其电极反应式为2HSO-
+2H++2e-===S
O2-
3 2 4 3 2 4
+2H O,B正确;吸收塔中发生反应的离子方程式为2S
O2-
+2NO+2H O===N
+4HSO-
,吸收塔中每消耗2
2 2 4 2 2 3
mol NO,转移4 mol电子,有4 mol H+通过质子膜,C正确;未说明气体所处状态,无法计算氧气体积,D
错误。]
4.B [光催化装置中,氢离子得到电子发生还原反应生成氢气,溶液中的氢离子浓度减小,I-得到空穴发生
氧化反应生成I- ,电极反应式为3I-+2h+===I-
,由得失电子守恒可知,整套装置转移0.01
mol电子时,I-
的
3 3 3
1
质量为0.01 mol× ×381 g·mol-1=1.905 g,故A错误、B正确;电催化装置中,右侧电极为阳极,氢氧根离
2
子在阳极得到空穴生成氧气和水,电极反应式为4OH-+4h+===2H O+O ↑,破坏水的电离平衡产生的氢离
2 2
子透过阳离子交换膜移向阴极,故C、D错误。]
5.B [由图可知,最左侧为阳极室,水放电生成氧气和氢离子;最右侧为阴极室,水放电生成氢气和氢氧
根离子;电解池中阳离子向阴极移动,BP膜中H+均向右侧溶液迁移;氟离子、氯离子通过M膜向左侧迁
移,故M膜为一价阴离子交换膜,A正确;溶液a中氟离子、氯离子通过M膜向左侧迁移,氢离子与右侧
双极膜迁移出来的OH-中和,故反应后溶液a的溶质主要为ZnSO 和CuSO ,溶液b的溶质主要为右侧迁
4 4
移过来的氟离子、氯离子与左侧迁移过来的氢离子生成HF和HCl,B错误;阳极反应为2H O-4e-===4H+
2
+O ↑,当阳极产生22.4 L气体,标准状况下为1 mol,根据电子守恒可知,有4 mol离子通过N膜,C正
2
确;电解过程中,若pH过高,则会导致锌离子、铜离子转化为沉淀,故应控制高盐废水的pH不能过高,
D正确。]
6.B [以浓差电池为电源,以石墨为电极将NH 转化为高纯H ,M电极上NH 转化为N ,N元素化合价升
3 2 3 2
高,发生氧化反应,M电极为阳极,则N电极为阴极,Cu(1)为正极,电极反应式为Cu2++2e-===Cu,故A
正确;M电极为阳极,电极反应式为2NH -6e-+6OH-===N ↑+6H O,消耗了OH-,碱性减弱,pH减小,则
3 2 2
丙室内阴离子浓度降低,N电极为阴极,电极反应式为2H O+2e-===H ↑+2OH-,丁室内阴离子浓度增大,
2 2为保持两侧电荷守恒,可以是丙室中钾离子进入乙室,则离子交换膜为阳离子交换膜,也可以是乙中氢氧
根离子进入丙室,则离子交换膜可以为阴离子交换膜,故B错误、C正确;电池从开始工作到停止放电,
正极区硫酸铜溶液的浓度由2.5 mol·L-1降低到1.5 mol·L-1,负极区硫酸铜溶液由0.5 mol·L-1升高到1.5
mol·L-1,正极反应可还原Cu2+的物质的量为2 L×(2.5-1.5) mol·L-1=2 mol,正极质量增加128 g,电路中转移
4 mol电子,负极反应:Cu-2e-===Cu2+,转移4 mol电子时,负极消耗2 mol Cu单质,质量减少128 g,理
论上Cu(1)和Cu(2)电极的质量差为256 g,故D正确。]
7.B [根据图中信息可知,左侧a电极反应为Mn2+-e-===Mn3+,为阳极,则b电极为阴极,电极反应为2H+
+2e-===H ↑,阳极生成的Mn3+进入“氧化池”将甲苯氧化为苯甲醛,发生的反应为 +4Mn3++H O
2 2
+4Mn2++4H+。据分析可知电极a是阳极,与电源正极相连,故A错误;电解过程中阴极电极b
发生反应:2H++2e-===H ↑,同时电解质溶液中有等量的H+通过质子交换膜进入阴极区,从而使电解池阴
2
极区溶液的pH几乎不变(忽略溶液体积变化),故C错误;苯甲醛有强还原性容易在电解池阳极上放电引起
干扰,故D错误。]
8.D [由题意可知,石墨电极Ⅱ为电解池的阳极,水在阳极失去电子发生氧化反应生成氧气和氢离子,氢
离子通过质子交换膜c进入中间室,与氧化铁反应生成铁离子和水,则a为直流电源的负极,b为正极,石
墨电极Ⅰ为阴极,铜离子在阴极得到电子发生还原反应生成铜,氯离子通过阴离子交换膜进入中间室。由
分析可知,a为直流电源的负极、b为正极,则a极电势低于b极电势,故A正确;由分析可知,石墨电极
Ⅰ为阴极,铜离子在阴极得到电子发生还原反应生成铜,氯离子通过阴离子交换膜进入中间室,所以随着
电解的进行,氯化铜溶液浓度变小,故C正确;氧化铁与氢离子反应生成铁离子和水,0.01 mol氧化铁溶
解消耗氢离子的物质的量为0.06 mol,则0.01 mol氧化铁溶解,外电路中通过0.06 mol电子,故D错误。]
9.D [由图可知,左侧装置为氢氧燃料电池装置,电极a为负极,电极反应为H -2e-===2H+,电极b为正极,
2
电极反应为O +4e-+2H O===4OH-;右侧装置为电解池,与电极a连接的电极d为阴极,电极反应为
2 2
2HCN+2e-===H ↑+2CN-,与电极b连接的电极c为阳极,电极反应为P -4e-+8LiCN===4Li[P(CN) ]+4Li+。
2 4 2
9 g 1
由得失电子守恒可知,标准状况下,生成9 g Li[P(CN) ]时,电极a消耗氢气的体积为 ×
2 90 g·mol-1 2
×22.4 L·mol-1=1.12 L,故B错误;负极发生反应:H -2e-===2H+,若隔膜e为阳离子交换膜,氢离子和
2
K+通过阳离子交换膜进入正极区,但负极区溶液中氢离子浓度增加,pH减小,故C错误;氢氰酸在阴极
得到电子发生还原反应生成氰酸根离子和氢气,而由图可知HCN中的H来自LiOH,故D正确。]10.D [X电极H O生成氧气发生氧化反应,为阳极,电极反应式为2H O-4e-===O ↑+4H+,Y为阴极,发
2 2 2
NO-
3
生还原反应,电极反应式为 + +11H++10e-=== +4H O,A、B正确;该离子
2
交换膜为阳离子交换膜,H+可以通过,D错误。]
11.D
[根据题干信息,通过电化学装置实现铅单质的回收,正极区电极反应式为HPbO-
+H O+2e-
2 2
===Pb+3OH-,C正确;该装置为H 2⁃铅化合物燃料电池,通入燃料氢气的电极b为负极,电极a为正极,
负极氢气失电子、产生氢离子消耗氢氧根离子,溶液pH降低,正极产生氢氧根离子,溶液pH升高,A正
确;电极b为负极,电极a为正极,电子流向:电极b→负载→电极a,B正确;离子交换膜应使用阳离子
交换膜,防止HPbO-
移动至电极b,D错误。]
2
12.C [由图可知放电时为原电池,左侧电极反应式为MnO +2e-+4H+===Mn2++2H O,为原电池的正极,则
2 2
右侧醌类电极为负极;充电时,电源正极连接原电池正极,作电解池的阳极,电源负极连接原电池负极,
作电解池的阴极,电极反应为 +2nH O+2nK++4ne-=== +2nOH-,据此分析判断。充电时,
2
阳极电极反应式为Mn2++2H O-2e-===MnO +4H+,阳极区电解质溶液的pH减小,故C错误;由阴极电极反
2 2
应可知,电路中每转移4 mol电子,阴极增重质量为80 g,则电路中每转移1 mol电子,阴极增重20 g,故
D正确。]