文档内容
绝密★启用前
2025 年高考考前信息必刷卷 01(江苏专用)
化 学
考情速递
高考·新动向:本卷化学试题紧扣“一核四层四翼”高考评价体系,突出学科核心素养与关键能力的综
合考查。例如,第4题以元素周期表分区为切入点,要求学生结合电子排布式分析ds区元素,既考查
基础知识的掌握(如Cu的电子构型),又体现对“证据推理与模型认知”素养的要求。第10题通过
电解苯制备环己烷的装置分析,要求学生理解电极反应机理,综合运用氧化还原与电化学原理,凸显
对“科学探究与创新意识”的考查。此外,第17题围绕碳中和目标设计CO₂捕集与转化问题,将学科
前沿与社会热点融入试题,体现了“科学态度与社会责任”的育人导向。
高考·新考法:试题注重教材知识的深化与迁移,强调“源于教材,高于教材”。例如:
1. 第3题通过实验装置正误判断(如NaHCO₃热稳定性实验的试管方向),考查学生对教材实验细节的
掌握程度,同时要求其结合物质性质分析错误原因,体现了对实验操作能力和逻辑思维的考查。
2. 第8题以有机合成为背景,涉及糖类与醛基的显色反应(如麦芽糖与新制氢氧化铜反应),将教材中
的基础反应(斐林试剂检验还原糖)迁移到新情境中,检验学生灵活应用知识的能力。
3. 第13题通过多步反应的热力学分析(盖斯定律与平衡移动),要求学生整合反应机理、平衡常数及
图像信息,体现了对“知识综合与迁移能力”的高阶要求。
高考·新情境:试题情境紧密联系生产生活实际与科技发展,强化“学以致用”。例如:
第14题以陶瓷工业中钴系色釉的制备为背景,设计从含钴废料中回收碳酸钴的工艺流程,涉及碱浸、
酸溶、萃取等化工操作,将实际工业流程与化学原理(如氧化还原、萃取平衡)结合,考查学生解决
真实问题的能力。
第16题以甾类药物的合成为主线,通过反应类型判断、同分异构体推断等任务,模拟药物研发中的有
机合成路径,体现化学在医药领域的应用价值。
第17题聚焦碳捕集与人工合成淀粉技术,将CO₂还原为甲醛的反应机理与电催化装置分析相结合,既
呼应“双碳”战略,又展示化学在解决环境与能源问题中的核心作用。
命题·大预测:未来高考化学试题将进一步强化以下趋势:
核心素养导向:如第7题通过二茂铁结构分析(σ键数目计算),考查“宏观辨识与微观探析”素养,
预测类似题目将更注重物质结构与性质的深度关联。
实验探究特色:第11题以实验现象反推结论(如电离常数比较),要求基于证据链推理,未来实验题
可能更侧重“假设-验证”的科学思维模式。
综合性与开放性:第15题合成路线的设计(乙炔与A制备目标产物),需自主选择试剂并设计路径,
体现“创新思维”,预计此类开放性设问将增多,鼓励创造性解决方案。
(考试时间:90分钟 试卷满分:100分)注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 P 31 S 32 K 39
一、选择题:本题共13小题,每小题3分,共39分。每小题只有一个选项符合题目要求。
1. 古代壁画中常用的蓝色颜料是石青[2CuCO Cu(OH) ],黑色颜料是铁黑(Fe O)。下列元素位于元素周
3 2 3 4
期表中 ds区的是
∙
A. Cu B. C C. Fe D. O
【答案】A
【解析】A.Cu的价电子排布式为3d104s1,其属于ds区元素,A符合题意;
B.C的价电子排布式为2s22p2,其属于p区元素,B不符合题意;
C.Fe的价电子排布式为3d64s2,其属于d区元素,C不符合题意;
D.O的价电子排布式为2s22p4,其属于p区元素,D不符合题意;
故选A。
2. 主要用作玻璃和搪瓷乳白剂。下列说法正确的是
A. 中仅含离子键 B. 灼烧 时火焰呈黄色
C. 原子半径: D. 热稳定性:
【答案】B
【解析】A. 中,硅与氟原子形成共价键,A错误;
B. 含有钠元素,其焰色为黄色,B正确;
C.钠与硅均为第三周期元素,从左到右,随着核电荷数增加,原子半价逐渐减小,C错误;
D.根据元素周期表递变规律,氟的氧化性强于硅,所以热稳定性是 ,D错误;
故选B。
3. 下列实验原理及装置均正确的是
A. 图甲:分离乙酸乙酯与饱和碳酸钠溶液
B. 图乙:探究NaHCO 固体的热稳定性
3C. 图丙:用标准酸性KMnO 溶液滴定未知浓度的FeSO 溶液
4 4
D. 图丁:采用如图装置蒸干FeSO 溶液获得FeSO ·7H O
4 4 2
【答案】A
【解析】A.分离乙酸乙酯与饱和碳酸钠溶液不互溶,出现分层,故可用分液将其分离,A正确;
B.NaHCO 固体分解时会生成水,故试管口应向下倾斜,B错误;
3
C.高锰酸钾腐蚀橡胶管,标准酸性KMnO 溶液应装在酸式滴定管中,C错误;
4
D.FeSO 溶液中 加热过程中会被氧化,故不能蒸干FeSO 溶液获得FeSO ·7H O,D错误;
4 4 4 2
故选A。
4. X、Y、Z、M四种主族元素,原子序数依次增大,分别位于三个不同短周期,Y与M同主族,Y与Z
核电荷数相差2,Z的原子最外层电子数是内层电子数的3倍。下列说法不正确的是
A. 键角: B. 分子的极性:
C. 共价晶体熔点: D. 热稳定性:
【答案】B
【解析】X、Y、Z、M四种主族元素,原子序数依次增大,分别位于三个不同短周期,Y与M同主
族,Y与Z核电荷数相差2,Z的原子最外层电子数是内层电子数的3倍,则Z为O元素,Y为C元
素,X为H元素,M为Si元素。
A. 为 ,其中C原子的杂化类型为 , 的空间构型为平面正三角形,键角为120°;
为 ,其中C原子的杂化类型为 , 的空间构型为三角锥形,由于C原子还有1个孤电
子对,故键角小于109°28´,因此,键角的大小关系为 ,A正确;
B. 为 ,其为直线形分子,分子结构对称,分子中正负电荷的重心是重合的,故其为百极
性分子; 分子结构不对称,分子中正负电荷的重心是不重合的,故其为极性分子,因此,两者极
性的大小关系为 ,B不正确;
C.金则石和晶体硅均为共价晶体,但是由于C的原子半径小于Si,因此,C—C键的键能大于Si—Si
键的,故共价晶体熔点较高的是金刚石,C正确;
D.元素的非金属性越强,其气态氢化物的热稳定性越强;C的非金属性强于Si,因此,甲烷的稳定热
稳定性较高,D正确;
故选B。
阅读材料,回答5-7题。
有机金属化合物是一类含有金属—碳键的化合物。蔡斯盐K[PtCl (C H)∙H O] 由乙烯和K[PtCl ]溶液在
3 2 4 2 2 4
催化剂作用下制得; 二茂铁 Fe(C H) 常被用作燃料的催化剂和抗爆剂,熔点为 172℃; 三甲基铝
5 5 2
(CH)Al可用作许多反应的催化剂;[RhI(CO) ]−可催化(CHOH与CO反应生成乙酸; Ni能与CO在
3 3 2 2 3
50~60℃条件下反应生成 Ni(CO) ,其在220~250℃下迅速分解生成金属 Ni,可用于 Ni、Co分离。完
4
成问题。5. 对于反应 下列说法正确的是
A. 该反应的△H<0
B. CO在反应过程中共价键未断裂
C. [RhI(CO) ]−提高该反应的活化能
2 2
D. 及时分离CHCOOH 能加快化学反应速率
3
6. 下列化学反应表示正确的是
A. 溴乙烷制备乙烯的反应:CHCHBr CH=CH ↑+HBr
3 2 2 2
B. 过量铁与氯气反应:
C. 合成蔡斯盐的反应:
D. 生成 Ni(CO) 的反应:
4
7. 下列说法正确的是
A. (CH)Al中 Al 原子轨道的杂化类型为 sp3
3 3
B. K[PtCl (C H)]中 Pt的化合价为+3
3 2 4
C. Fe(C H) 属于离子化合物
5 5 2
D. 1mol Ni(CO) 中 σ 键数目为 8 mol
4
【答案】5. A 6. C 7. D
【解析】【5题详解】
A.该反应可以理解为醇的氧化反应生成乙酸,为放热反应,则△H<0,A正确;
B.CO结构 为,反应生成乙酸中存在碳氧双键和碳氧单键,则CO在反应过程中共价键发生断
裂,B错误;
C.[RhI(CO) ]−为反应的催化剂,降低该反应的活化能,加快反应速率,C错误;
2 2
D.及时分离CHCOOH ,促使平衡正向移动,但是物质浓度减小,减慢了反应速率,D错误;
3
故选A;
【6题详解】
A.溴乙烷在氢氧化钠醇溶液条件下加热生成乙烯,反应:CHCHBr+NaOH
3 2
CH=CH ↑+NaBr+H O,A错误;
2 2 2
B.过量铁与氯气反应生成氯化铁: ,B错误;
C.乙烯和K[PtCl ]溶液在催化剂作用下制得蔡斯盐,反应为:
2 4,C正确;
D.Ni能与CO在50~60℃条件下反应生成 Ni(CO) ,: ,D错误;
4
故选C;
【7题详解】
A.(CH)Al中 Al 原子形成3个共价键,且无孤电子对,轨道的杂化类型为 sp2,A错误;
3 3
B.K[PtCl (C H)]中钾为+1价、氯为-1价, C H 整体化合价为0,则Pt的化合价为+2,B错误;
3 2 4 2 4
C.二茂铁 Fe(C H) 熔点为 172℃,属于分子晶体,不存在离子键,C错误;
5 5 2
D.1个CO中存在1个σ键,镍和4个CO形成4个配位键,则1mol Ni(CO) 中含8mol σ 键,数目为
4
8 mol,D正确;
故选D。
8. 在给定条件下,下列选项所示的物质间转化能实现的是
A.
B.
C.
D.
【答案】A
【解析】A. 与NaOH反应生成新制氢氧化铜悬浊液,新制氢氧化铜可与还原性糖麦芽糖反应
生成 ,故A正确;
B.铁与氯气反应只能生成FeCl ,故B错误;
3
C. 与CO 不能反应,故C错误;
2
D. 为共价化合物,不能电解制取Al,故D错误;
故选:A。
9. 合成抗肿瘤药氟他胺的部分流程如下。已知吡啶的结构简式为( )。下列说法正确的是A. 甲分子中所有原子共平面
B. 乙在水中的溶解度小于甲
C. 1 mol丙最多与4 mol H 发生加成反应
2
D. 乙→丙过程中加入吡啶是为了结合反应中产生的HCl
【答案】D
【解析】A.甲分子中—CF 的C原子是饱和C原子,采用sp3杂化,为四面体结构,因此该物质分子
3
中所有原子不可能共平面,A错误;
B.物质乙分子中的氨基—NH 是亲水基,导致物质乙在水中的溶解度大于物质甲,B错误;
2
C.苯环能够与H 发生加成反应,但是酰胺基中的羰基具有特殊的稳定性,不能与H 发生加成反应,
2 2
故1 mol丙最多只能与3 mol H 发生加成反应,C错误;
2
D.根据物质乙、丙结构简式的不同,可知反应时,物质乙分子中—NH 上的H原子与 中
2
的除Cl原子之外的基团发生取代反应产生丙,同时H与Cl原子结合产生HCl,D正确;
故选D。
10.利用电解可以将气态苯( )转化为环己烷( ),其电解装置如图所示。下列有关说法正确
的是
A. 电解时,电极A与电源的正极相连
B. 电解时,电极B上产生的气体为
C. 反应中每生成 ,转移电子数为
D. 电解的总反应方程式:【答案】C
【解析】由图可知, 在电极A发生还原反应生成 ,电极方程式为: +6H++6e-=
,电极A为阴极,电极B为阳极,HO在阳极失去电子生成O ,电极方程式为:2HO-4e-=O
2 2 2 2
+4H+,以此解答。
A.由分析可知,电解时,电极A为阴极,与电源的负极相连,A错误;
B.由分析可知,电解时,电极B为阳极,HO在阳极失去电子生成O,B错误;
2 2
C.由分析可知,电极A的电极方程式为: +6H++6e-= ,每生成 ,转移电
子数为 ,C正确;
D.电极A的电极方程式为: +6H++6e-= ,电极B的电极方程式为:2HO-4e-=O
2 2
+4H+,则电解的总反应方程式:2 +6H O 2 +3O ,D错误;
2 2
故选C。
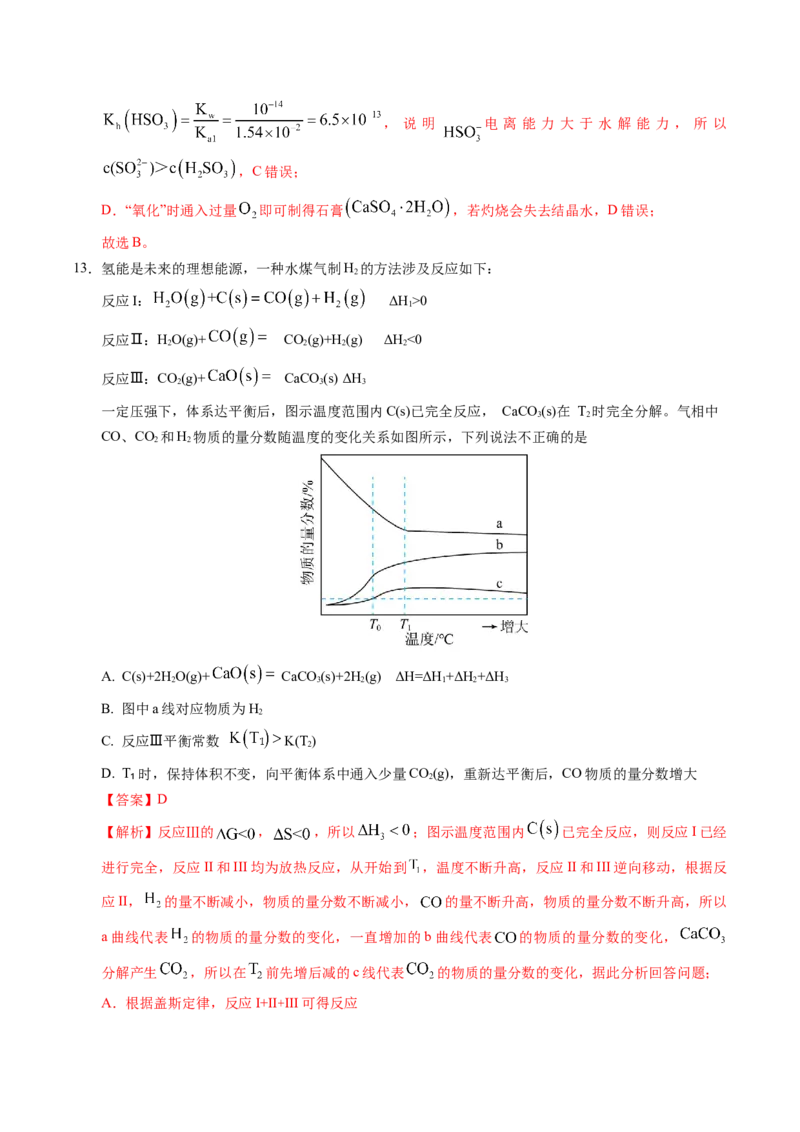
11.室温下,下列实验过程和现象能验证相应实验结论的是
选
实验方案过程和现象 实验结论
项
用玻璃棒分别蘸取0.1 HCl和 溶液滴到pH试纸上,
A 酸性:HCl>
溶液pH(HCl)<pH( )
向2mL 溶液中加入Mg条,产生无色气体,并有红褐色沉
B 金属活动性:Mg>Fe
淀生成
电离平衡常数:
C 向2mL饱和 溶液中通入 ,出现白色沉淀
向2mL浓度均为0.1 的 和 混合溶液中滴加 溶度积常数:
D
少量0.1 溶液,振荡,产生白色沉淀
【答案】A
【解析】A.用玻璃棒分别蘸取0.1 HCl和 溶液滴到pH试纸上,溶液pH(HCl)<pH():说明HCl的电离程度大于 ,溶液中 :HCl大于 溶液,则酸性: ,
A正确;
B.向2mL 溶液中加入Mg条,产生无色气体,并有红褐色沉淀生成:是因为Mg与水反应生
成了 ,再与 反应得到 后最终被氧化为红褐色 ,整个反应过程
没有体现金属性的关系,所以无法比较Mg 和Fe的金属性大小,B错误;
C.向2mL饱和 溶液中通入 ,出现白色沉淀:是因为发生反应
,属于沉淀的生成,无法比较电离平衡常数,C错误;
D.向2mL浓度均为0.1 的 和 混合溶液中滴加少量0.1 溶液,
振荡,产生白色沉淀:不管是 与 或 生成沉淀,都只涉及沉淀的生成,不涉及沉淀的
转化,无法比较溶度积,D错误;
故选A。
12.室温下,用 溶液吸收 的过程如图所示。
已知: , ,下列说法正确的是
A. 溶液中:
B. 充分吸收烟气后的溶液中:
C. 完全转化为 时:
D. “氧化”时通入过量 并灼烧制得石膏
【答案】B
【解析】NaSO 溶液吸收烟气后得到NaSO 和NaHSO 的混合溶液,然后加入碳酸钙得到亚硫酸钙沉
2 3 2 3 3
淀,过滤分离,最后经氧气氧化为石膏,据此回答。
A.根据质子守恒, 溶液中 ,A错误;
B.当未吸收烟气时, 溶液中存在物料守恒
,当吸收 后,硫元素质量增加,即 ,B正确;
C . 溶 液 中 存 在 的 电 离 平 衡 和 水 解 平 衡 , ,, 说 明 电 离 能 力 大 于 水 解 能 力 , 所 以
,C错误;
D.“氧化”时通入过量 即可制得石膏 ,若灼烧会失去结晶水,D错误;
故选B。
13.氢能是未来的理想能源,一种水煤气制H 的方法涉及反应如下:
2
反应I: ΔH>0
1
反应Ⅱ:HO(g)+ CO(g)+H(g) ΔH <0
2 2 2 2
反应Ⅲ:CO(g)+ CaCO (s) ΔH
2 3 3
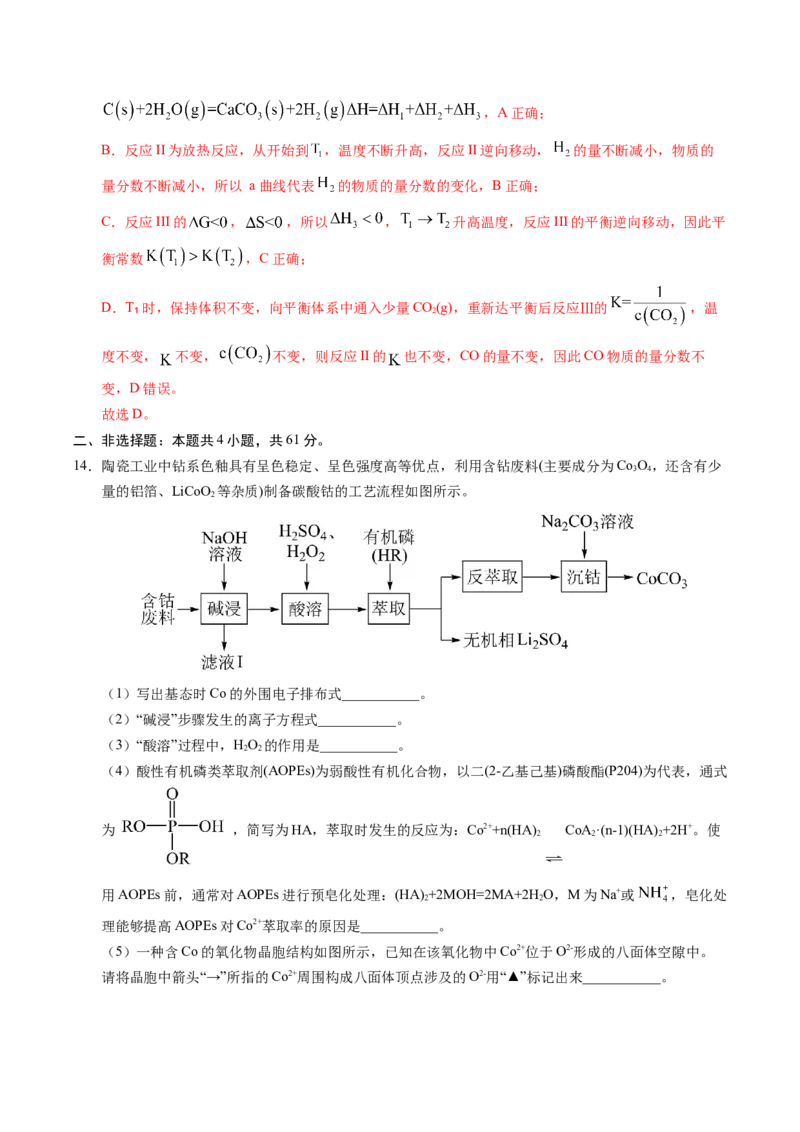
一定压强下,体系达平衡后,图示温度范围内C(s)已完全反应, CaCO (s)在 T 时完全分解。气相中
3 2
CO、CO 和H 物质的量分数随温度的变化关系如图所示,下列说法不正确的是
2 2
A. C(s)+2HO(g)+ CaCO (s)+2H(g) ΔH=ΔH +ΔH +ΔH
2 3 2 1 2 3
B. 图中a线对应物质为H
2
C. 反应Ⅲ平衡常数 K(T)
2
D. T₁时,保持体积不变,向平衡体系中通入少量CO(g),重新达平衡后,CO物质的量分数增大
2
【答案】D
【解析】反应Ⅲ的 , ,所以 ;图示温度范围内 已完全反应,则反应I已经
进行完全,反应II和III均为放热反应,从开始到 ,温度不断升高,反应II和III逆向移动,根据反
应II, 的量不断减小,物质的量分数不断减小, 的量不断升高,物质的量分数不断升高,所以
a曲线代表 的物质的量分数的变化,一直增加的b曲线代表 的物质的量分数的变化,
分解产生 ,所以在 前先增后减的c线代表 的物质的量分数的变化,据此分析回答问题;
A.根据盖斯定律,反应I+II+III可得反应,A正确;
B.反应II为放热反应,从开始到 ,温度不断升高,反应II逆向移动, 的量不断减小,物质的
量分数不断减小,所以 a曲线代表 的物质的量分数的变化,B正确;
C.反应III的 , ,所以 , 升高温度,反应III的平衡逆向移动,因此平
衡常数 ,C正确;
D.T₁时,保持体积不变,向平衡体系中通入少量CO(g),重新达平衡后反应Ⅲ的 ,温
2
度不变, 不变, 不变,则反应II的 也不变,CO的量不变,因此CO物质的量分数不
变,D错误。
故选D。
二、非选择题:本题共4小题,共61分。
14.陶瓷工业中钻系色釉具有呈色稳定、呈色强度高等优点,利用含钻废料(主要成分为Co O,还含有少
3 4
量的铝箔、LiCoO 等杂质)制备碳酸钴的工艺流程如图所示。
2
(1)写出基态时Co的外围电子排布式___________。
(2)“碱浸”步骤发生的离子方程式___________。
(3)“酸溶”过程中,HO 的作用是___________。
2 2
(4)酸性有机磷类萃取剂(AOPEs)为弱酸性有机化合物,以二(2-乙基己基)磷酸酯(P204)为代表,通式
为 ,简写为HA,萃取时发生的反应为:Co2++n(HA) CoA·(n-1)(HA) +2H+。使
2 2 2
用AOPEs前,通常对AOPEs进行预皂化处理:(HA) +2MOH=2MA+2H O,M为Na+或 ,皂化处
2 2
理能够提高AOPEs对Co2+萃取率的原因是___________。
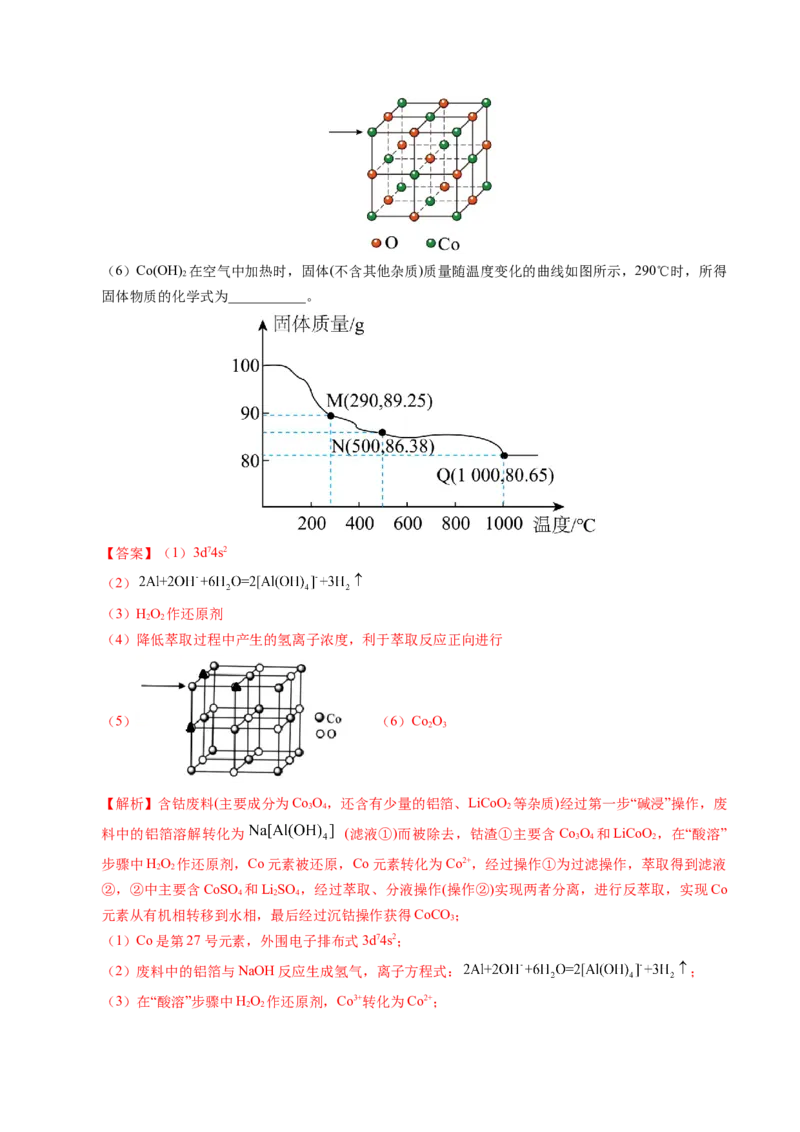
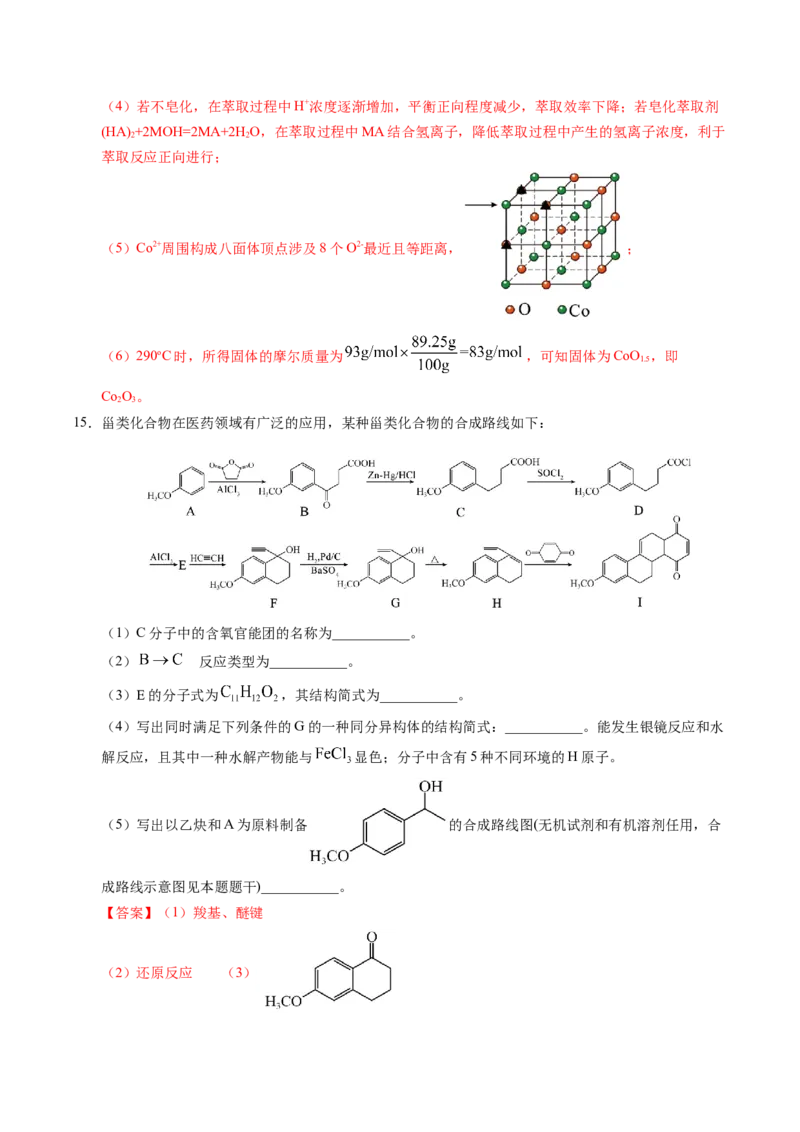
(5)一种含Co的氧化物晶胞结构如图所示,已知在该氧化物中Co2+位于O2-形成的八面体空隙中。
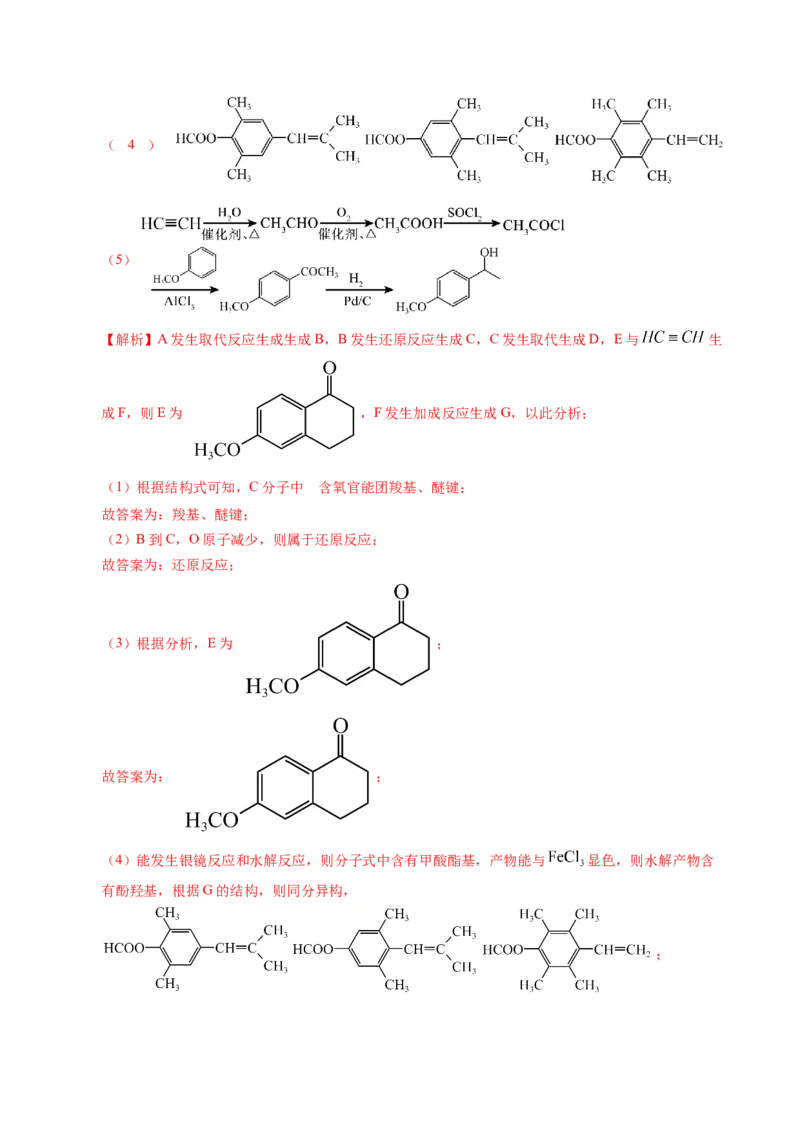
请将晶胞中箭头“→”所指的Co2+周围构成八面体顶点涉及的O2-用“▲”标记出来___________。(6)Co(OH) 在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,290℃时,所得
2
固体物质的化学式为___________。
【答案】(1)3d74s2
(2)
(3)HO 作还原剂
2 2
(4)降低萃取过程中产生的氢离子浓度,利于萃取反应正向进行
(5) (6)Co O
2 3
【解析】含钴废料(主要成分为Co O,还含有少量的铝箔、LiCoO 等杂质)经过第一步“碱浸”操作,废
3 4 2
料中的铝箔溶解转化为 (滤液①)而被除去,钴渣①主要含Co O 和LiCoO ,在“酸溶”
3 4 2
步骤中HO 作还原剂,Co元素被还原,Co元素转化为Co2+,经过操作①为过滤操作,萃取得到滤液
2 2
②,②中主要含CoSO 和LiSO ,经过萃取、分液操作(操作②)实现两者分离,进行反萃取,实现Co
4 2 4
元素从有机相转移到水相,最后经过沉钴操作获得CoCO;
3
(1)Co是第27号元素,外围电子排布式3d74s2;
(2)废料中的铝箔与NaOH反应生成氢气,离子方程式: ;
(3)在“酸溶”步骤中HO 作还原剂,Co3+转化为Co2+;
2 2(4)若不皂化,在萃取过程中H+浓度逐渐增加,平衡正向程度减少,萃取效率下降;若皂化萃取剂
(HA) +2MOH=2MA+2H O,在萃取过程中MA结合氢离子,降低萃取过程中产生的氢离子浓度,利于
2 2
萃取反应正向进行;
(5)Co2+周围构成八面体顶点涉及8个O2-最近且等距离, ;
(6)290oC时,所得固体的摩尔质量为 ,可知固体为CoO ,即
1.5
Co O。
2 3
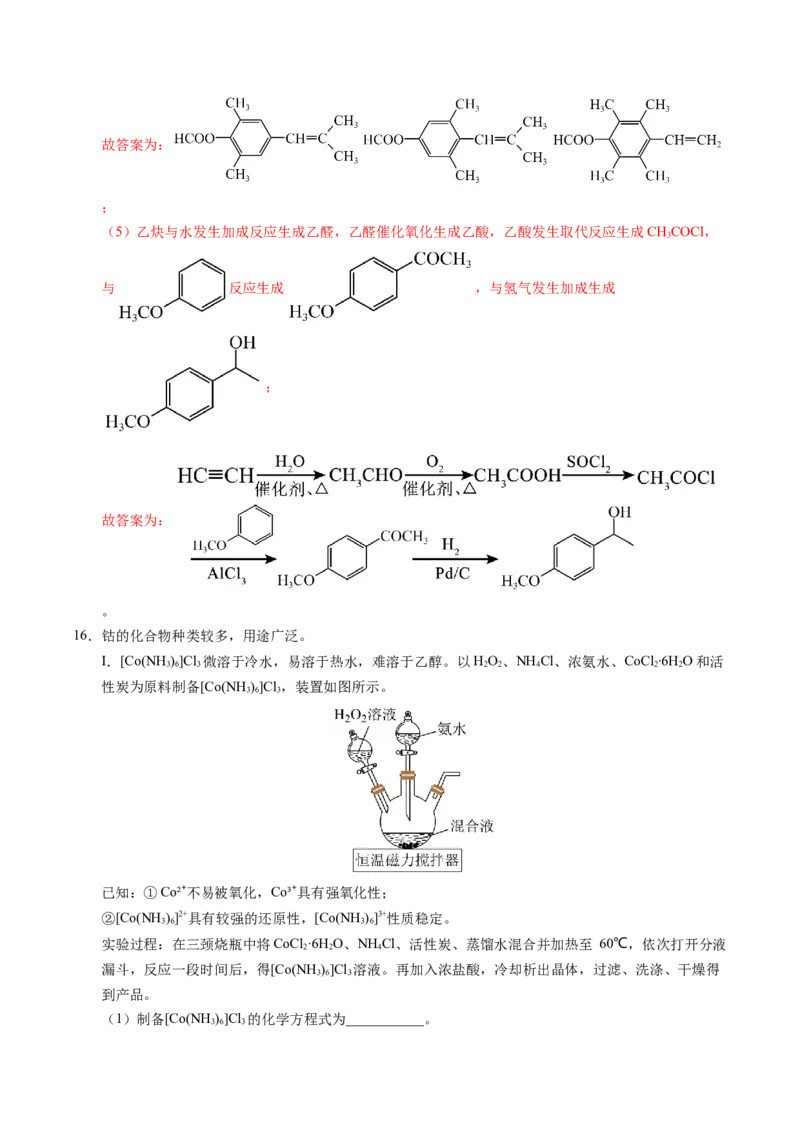
15.甾类化合物在医药领域有广泛的应用,某种甾类化合物的合成路线如下:
(1)C分子中的含氧官能团的名称为___________。
(2) 的反应类型为___________。
(3)E的分子式为 ,其结构简式为___________。
(4)写出同时满足下列条件的G的一种同分异构体的结构简式:___________。能发生银镜反应和水
解反应,且其中一种水解产物能与 显色;分子中含有5种不同环境的H原子。
(5)写出以乙炔和A为原料制备 的合成路线图(无机试剂和有机溶剂任用,合
成路线示意图见本题题干)___________。
【答案】(1)羧基、醚键
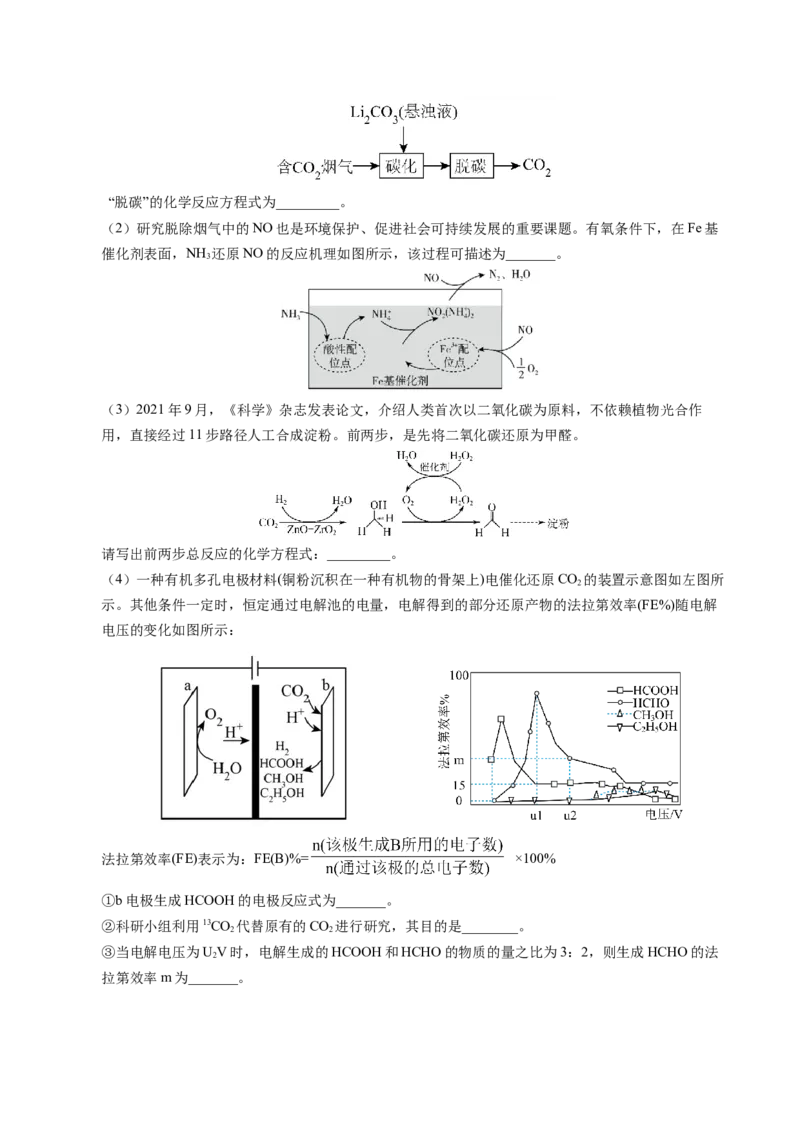
(2)还原反应 (3)( 4 )
(5)
【解析】A发生取代反应生成生成B,B发生还原反应生成C,C发生取代生成D,E与 生
成F,则E为 ,F发生加成反应生成G,以此分析;
(1)根据结构式可知,C分子中 含的氧官能团羧基、醚键;
故答案为:羧基、醚键;
(2)B到C,O原子减少,则属于还原反应;
故答案为:还原反应;
(3)根据分析,E为 ;
故答案为: ;
(4)能发生银镜反应和水解反应,则分子式中含有甲酸酯基,产物能与 显色,则水解产物含
有酚羟基,根据G的结构,则同分异构,
;故答案为:
;
(5)乙炔与水发生加成反应生成乙醛,乙醛催化氧化生成乙酸,乙酸发生取代反应生成CHCOCl,
3
与 反应生成 ,与氢气发生加成生成
;
故答案为:
。
16.钴的化合物种类较多,用途广泛。
I.[Co(NH )]Cl 微溶于冷水,易溶于热水,难溶于乙醇。以HO、NH Cl、浓氨水、CoCl ∙6H O和活
3 6 3 2 2 4 2 2
性炭为原料制备[Co(NH )]Cl ,装置如图所示。
3 6 3
已知:①Co²⁺不易被氧化,Co³⁺具有强氧化性;
②[Co(NH )]2+具有较强的还原性,[Co(NH )]3+性质稳定。
3 6 3 6
实验过程:在三颈烧瓶中将CoCl ·6H O、NH Cl、活性炭、蒸馏水混合并加热至 60℃,依次打开分液
2 2 4
漏斗,反应一段时间后,得[Co(NH )]Cl 溶液。再加入浓盐酸,冷却析出晶体,过滤、洗涤、干燥得
3 6 3
到产品。
(1)制备[Co(NH )]Cl 的化学方程式为___________。
3 6 3(2)分液漏斗中液体加入三颈烧瓶中的顺序为___________。
(3)活性炭是该反应的催化剂,实验室有粒状和粉末状两种形态的活性炭,从比表面积和吸附性的
角度分析,本实验选择粉末状活性炭的优缺点是___________。
(4)洗涤时使用的试剂有冰水、乙醇、冷的盐酸,最后洗涤使用的洗涤剂为___________。
(5)测定产品纯度。取一定量产品溶于水,以KCrO 溶液作指示剂,用AgNO 标准溶液进行滴定,
2 4 3
测量溶液中Cl⁻含量。为使滴定终点时 Cl⁻沉淀完全(浓度小于1.8×10-5 mol∙L-1加入指示剂后溶液中
浓度不应超过 (忽略滴加过程的体积增加)___________。[已知: K (AgCl)= 1.8×10-10,
sp
K (Ag CrO)=2.0×10-12]
sp 2 4
Ⅱ.实验室还可以用废旧锂电池正极材料 (含LiCoO ,以及少量 Fe)为原料制备Co(OH) ,已知:酸
2 2
性条件下的氧化性强弱顺序为Co3+>HO>Fe3+;LiOH可溶于水; 下表是部分金属离子生成氢氧化
2 2
物沉淀的pH。
金属离子 Co2+ Fe2+ Fe3+
开始沉淀的
7.6 7.6 2.7
pH
沉淀完全的
9.2 9.6 3.7
pH
(6)请补充完整实验方案:取一定量废旧锂电池正极材料,粉碎后与足量NaSO 溶液配成悬浊液,
2 3
___________,过滤、洗涤、真空烘干得到Co(OH) 。(实验中必须使用的试剂:1 mol∙L-1HSO 溶液、
2 2 4
5 mol∙L-1NaOH溶液、30%H O 溶液)
2 2
【答案】(1) 或
(2)先滴加氨水再滴加HO 溶液
2 2
(3)粉末状活性炭比表面积较粒状活性炭大,催化效果更好,但对产物的吸附性也强,不利于反应
的进一步进行
(4)乙醇 (5)2.0×10-2molL-1
(6)在搅拌下,先加入1 molL-1HSO 溶液至固体完全溶解;继续向其中加入30% H O 溶液至溶液
∙ 2 4 2 2
颜色不再加深(或开始产生大量气泡或加入适量30% H O 溶液),再向其中加入5molL-1NaOH溶液至
∙ 2 2
溶液pH至3.7~7.6之间,过滤,向滤液中继续加入5molL-1NaOH溶液调节pH至9.2
∙
【解析】以HO、NH Cl、浓氨水、CoCl ∙6H O和活性炭为原料制备[Co(NH )]Cl 时,考虑到Co2+不
2 2 4 2 2 ∙ 3 6 3
易被氧化,[Co(NH )]2+具有较强的还原性,则应先将Co2+与氨水反应转化为[Co(NH )]Cl ,再加入
3 6 3 6 2
HO,将[Co(NH )]Cl 氧化为[Co(NH )]Cl 。所以向盛有NH Cl、CoCl ∙6H O和活性炭的混合物中先
2 2 3 6 2 3 6 3 4 2 2
加入氨水,然后加入HO 溶液。
2 2
(1)由分析可知,制备[Co(NH )]Cl 时,应往CoCl ·6H O、NH Cl中先加入氨水,生成
3 6 3 2 2 4
[Co(NH )]Cl ,再加入HO,将[Co(NH )]Cl 氧化为[Co(NH )]Cl ,依据得失电子守恒可得出HO
3 6 2 2 2 3 6 2 3 6 3 2 2——2CoCl ,再依据质量守恒,便可得出配平的化学方程式为
2
或
。
(2)由于Co2+不易被氧化,而[Co(NH )]2+具有较强的还原性,所以应将Co2+先转化为[Co(NH )]2+,
3 6 3 6
再用HO 氧化,从而得出分液漏斗中液体加入三颈烧瓶中的顺序为:先滴加氨水再滴加HO 溶液。
2 2 2 2
(3)活性炭是该反应的催化剂,催化剂的表面积越大,催化效果越好,但吸附产品能力强,不利于
产品脱离催化剂表面,会影响反应物与活性炭的接触,从而影响反应物的转化率。实验室有粒状和粉
末状两种形态的活性炭,从比表面积和吸附性的角度分析,本实验选择粉末状活性炭的优缺点是:粉
末状活性炭比表面积较粒状活性炭大,催化效果更好,但对产物的吸附性也强,不利于反应的进一步
进行。
(4)[Co(NH )]Cl 微溶于冷水,易溶于热水,难溶于乙醇,由此得出[Co(NH )]Cl 在乙醇中的溶解度
3 6 3 3 6 3
最小,且乙醇易挥发,容易干燥处理,则洗涤时使用的试剂有冰水、乙醇、冷的盐酸,最后洗涤使用
的洗涤剂为:乙醇。
(5)滴定终点时Cl⁻沉淀完全,其浓度小于1.8×10-5 mol∙L-1,此时溶液中c(Ag+)= =
mol∙L-1=1.0×10-5mol∙L-1,加入指示剂后溶液中 浓度不应超过 =
mol∙L-1=2.0×10-2mol∙L-1。
(6)实验室用废旧锂电池正极材料(含LiCoO ,以及少量 Fe)为原料制备Co(OH) ,此时先加酸溶
2 2
解,由于酸性条件下的氧化性强弱顺序为Co3+>HO>Fe3+,则应先加入还原剂将Co3+还原为Co2+,
2 2
再加HO 将Fe2+氧化为Fe3+,然后加入NaOH调节pH在3.7~7.6之间,使Fe3+全部转化为Fe(OH) 沉
2 2 3
淀;过滤后继续加入NaOH溶液,调节pH至9.2,将Co2+全部转化为Co(OH) 沉淀,过滤、洗涤、干
2
燥。所以实验方案为:取一定量废旧锂电池正极材料,粉碎后与足量NaSO 溶液配成悬浊液,在搅拌
2 3
下,先加入1 mol∙L-1HSO 溶液至固体完全溶解;继续向其中加入30% H O 溶液至溶液颜色不再加深
2 4 2 2
(或开始产生大量气泡或加入适量30% H O 溶液),再向其中加入5mol∙L-1NaOH溶液至溶液pH至
2 2
3.7~7.6之间,过滤,向滤液中继续加入5mol∙L-1NaOH溶液调节pH至9.2,过滤、洗涤、真空烘干得
到Co(OH) 。
2
【点睛】Fe3+是HO 分解的催化剂,往含Fe2+的溶液中加入HO 时,有气泡(O )产生。
2 2 2 2 2
17.我国对世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和,而研发CO 的碳捕捉和碳利用
2
技术则是关键。
(1)烟气中CO 的捕集可通过如下所示的物质转化实现。
2“脱碳”的化学反应方程式为_________。
(2)研究脱除烟气中的NO也是环境保护、促进社会可持续发展的重要课题。有氧条件下,在Fe基
催化剂表面,NH 还原NO的反应机理如图所示,该过程可描述为_______。
3
(3)2021年9月,《科学》杂志发表论文,介绍人类首次以二氧化碳为原料,不依赖植物光合作
用,直接经过11步路径人工合成淀粉。前两步,是先将二氧化碳还原为甲醛。
请写出前两步总反应的化学方程式:_________。
(4)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO 的装置示意图如左图所
2
示。其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解
电压的变化如图所示:
法拉第效率(FE)表示为:FE(B)%= ×100%
①b电极生成HCOOH的电极反应式为_______。
②科研小组利用13CO 代替原有的CO 进行研究,其目的是________。
2 2
③当电解电压为UV时,电解生成的HCOOH和HCHO的物质的量之比为3:2,则生成HCHO的法
2
拉第效率m为_______。【答案】(1)
(2)在Fe基催化剂表面, 吸附在酸性配位点上形成 , 与 吸附在 配位点上形
成 ,然后 与 结合生成 ,最后 与 反应生成
,并从催化剂表面逸出
(3)
.
(4)① CO+2e- +2H+= HCOOH ②. 确定阴极上生成含碳化合物源自二氧化碳而非有机多孔电极
2
材料 ③. 20%
【解析】(1)碳酸锂和二氧化碳反应生成碳酸氢锂,碳酸氢锂受热分解为碳酸锂并释放出二氧化碳
气体,反应为: ;
(2)由图可知,在Fe基催化剂表面, 吸附在酸性配位点上形成 , 与 吸附在
配位点上形成 ,然后 与 结合生成 ,最后 与 反应生成
,并从催化剂表面逸出,使得污染物NO被还原为无毒的氮气;
(3)由图可知,前两步反应为二氧化碳、氢气在催化剂表面转化为甲醇和水,甲醇和过氧化氢生成
的氧气发生氧化还原反应被氧化为甲醛,总反应为二氧化碳、氢气、过氧化氢生成甲醛和水:
;
(4)①b电极为阴极,酸性条件下二氧化碳在阴极得到电子被还原为甲酸,反应为CO+2e- +2H+=
2
HCOOH。
②有机多孔电极材中含有碳元素,利用13CO 代替原有的CO 进行研究,可以对反应中的碳原子进行
2 2
跟踪定位,确定阴极上生成含碳化合物源自二氧化碳而非有机多孔电极材料。
③ 、 ,电解电压为UV时,放电生成1mol
2
甲酸转移2mol,生成1mol甲醛转移4mol电子,由图可知,生成甲酸的FE%为15%,则由电解生成
的甲酸和甲醛的物质的量之比为3:2,可得 ,解得m=20。