文档内容
绝密★启用前
2025 年高考考前信息必刷卷 02(云南专用)
化 学
考情速递
高考·新动向:2025年云南八省联考化学科目考试就是云南省自主命题的体现,单项选择题本大题有16
小题,每小题3分,共48分;非选择题本大题有4小题,每小题13分,共52分。新高考下的化学试
卷在结构上可能会与其他新高考省份有更多的一致性或者相互借鉴之处,朝着体现高考公平性、普适
性和人才选拔准确性的方向完善结构设置。
高考·新考法:2025年高考化学题型向着更加综合化、融合多知识模块方向发展,这对于考生来说首先
在知识整合方面带来了巨大挑战。化学试题会打破化学学科内各知识板块的界限,如无机化学、有机
化学、物理化学等板块不再孤立考查。在一道题目中可能同时融合多方面知识进行综合考查。。
高考·新情境:新高考体系基本形成,云南从老高考转为新高考。这使得化学学科在整个高考体系中的
定位发生了变化,其教学方式和学生的学习策略也需要相应调整。例如,在新高考模式下,化学学科
的学习可能更注重与其他学科的联系,以及在实际生活中的应用。学生需要培养综合运用知识的能力,
而不仅仅是对化学知识的死记硬背。
命题·大预测:2025年高考人数可能增多,考生增多意味着竞争加剧,在化学学科上也不例外。学生需
要更加努力提高化学成绩,以在众多考生中脱颖而出。这就要求学生在日常学习中提高学习效率,注
重知识的掌握和应用能力的提升。云南省在借鉴其他省份新高考经验的过程中,可能会在题型的创新、
题目情境的设置等方面有所借鉴。比如一些先行新高考改革省份中出现的开放性化学试题(如实验方案
设计与评价的开放性问题)、以真实科研成果或工业生产流程为背景的综合应用题等题型,有可能会逐
渐出现在云南高考化学试卷中。这有助于选拔具有创新思维和实际应用能力的学生,适应现代社会对
人才的需求。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 Na-23 Mg-24 Al-27 S-32 Cl-35.5
K-39 Ca-40 Ti-48 V-51 Mn-55 Fe-56 Cu-64 Zn-65 Br-80 I-127 Ag-108 Ba-137 Bi-209
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题
目要求。
1.下列有关我国传统文化和现代科技的说法正确的是( )A.《本草纲目》中对酿酒有如下记载:“以大麦蒸热,和曲酿瓮中七日,以甑蒸取,其清如水,味
极浓烈”。其中用到的操作为蒸馏和过滤
B.《天工开物》记载“凡火药,硫为纯阳,硝为纯阴”,“硫”指的是硫酸
C.唐代三彩釉陶中,黄色釉、褐色釉是利用赭石来着色的,赭石的主要成分为
D.“试玉要烧三日满,辨才须待七年期”,此文中“玉”的主要成分为硅酸盐,该诗句表明玉的硬
度很大
【答案】C
【解析】A项,《本草纲目》中记载的酿酒操作为蒸馏,没有过滤,故A错误;B项,“硝”是
KNO,“硫”指的是单质硫,故B错误;C项,利用赭石的颜色可知其主要成分为Fe O,故C正确;D
3 2 3
项,玉的主要成分是SiO、Al O 等耐高温物质,此句话说明玉的熔点高,而不是硬度大,故D错误;故
2 2 3
选C。
2.科学、安全、有效、合理地使用化学品是每位生产者和消费者的责任,下列有关说法错误的是(
)
A.碳酸氢钠和氢氧化铝均可用于治疗胃酸过多
B.FeCl 溶液可腐蚀覆铜板制作印刷电路板
3
C.75%的乙醇与84消毒液的消毒原理相同
D.Al与NaOH混合固体可用于疏通厨房管道
【答案】C
【解析】A项,碳酸氢钠和氢氧化铝都可以和胃酸反应,均可用于治疗胃酸过多,A正确;B项,
FeCl 溶液可用作覆铜板制作印刷电路板的“腐蚀液”,铁离子将铜氧化,化学方程式为
3
2FeCl +Cu=CuCl +2FeCl ,B正确;C项,75%酒精可以进行消毒的原理是酒精可以使蛋白质凝固而变性,
3 2 2
从而达到杀菌消毒的效果,84消毒液的主要成分是次氯酸钠,具有强氧化性,在水中能够生成次氯酸,从
而起到消毒的作用,二者原理不同,C错误;D项,Al与NaOH溶液反应会产生氢气,增加管道内的气压,
从而疏通厨房管道,同时反应放热加快氢氧化钠对毛发等淤积物的腐蚀,D正确;故选C。
3.下列解释实验事实的反应方程式不正确的是( )
A.盛放烧碱的试剂瓶不能用玻璃塞:SiO+2NaOH=Na SiO+H O
2 2 3 2
B.用烧碱溶液吸收氯气:Cl+2OH-=Cl-+ClO-+H O
2 2
C.用KSCN溶液检验Fe3+:Fe3++3SCN- Fe(SCN)
3
D.酸性KI淀粉溶液久置后变蓝:4I-+O +2H O=2I +4OH-
2 2 2
【答案】D【解析】A项,氢氧化钠溶液能和二氧化硅反应生成黏性较强的硅酸钠,所以盛放烧碱的试剂瓶不能
用玻璃塞,A正确;B项,氯气能被氢氧化钠溶液吸收生成氯化钠、次氯酸钠和水,B正确;C项,铁离
子能和KSCN溶液反应显红色,据此可以鉴别铁离子, C正确;D项,溶液显酸性,不可能生成OH-,应
该是4I-+O +4H+=2I +2H O ,D不正确;故选D。
2 2 2
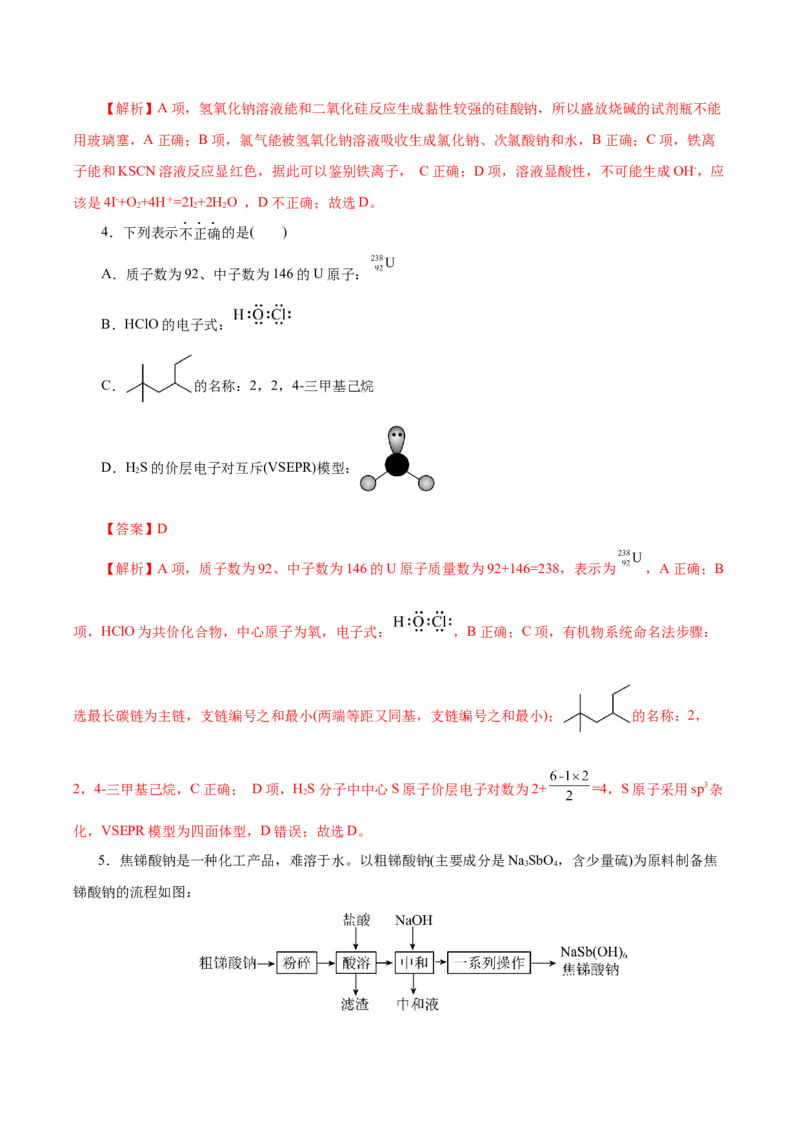
4.下列表示不正确的是( )
A.质子数为92、中子数为146的U原子:
B.HClO的电子式:
C. 的名称:2,2,4-三甲基己烷
D.HS的价层电子对互斥(VSEPR)模型:
2
【答案】D
【解析】A项,质子数为92、中子数为146的U原子质量数为92+146=238,表示为 ,A正确;B
项,HClO为共价化合物,中心原子为氧,电子式: ,B正确;C项,有机物系统命名法步骤:
选最长碳链为主链,支链编号之和最小(两端等距又同基,支链编号之和最小); 的名称:2,
2,4-三甲基己烷,C正确; D项,HS分子中中心S原子价层电子对数为2+ =4,S原子采用sp3杂
2
化,VSEPR模型为四面体型,D错误;故选D。
5.焦锑酸钠是一种化工产品,难溶于水。以粗锑酸钠(主要成分是NaSbO ,含少量硫)为原料制备焦
3 4
锑酸钠的流程如图:下列说法正确的是( )
A.锑元素位于元素周期表的第六周期第VA族
B.为了加快“酸溶”速率,可采用高温条件
C.“中和”时,反应之一为SbCl +6NaOH=NaSb(OH) ↓+5NaCl
5 6
D.“一系列操作”包括蒸发浓缩、冷却结晶
【答案】C
【解析】A项,锑元素位于元素周期表第五周期第VA族元素,A错误;B项,温度过高,盐酸挥发加
快,盐酸损失过多,B错误;C项,“中和”反应为盐酸和氢氧化钠生成氯化钠和水,SbCl 和氢氧化钠反
5
应生成难溶于水的焦锑酸钠沉淀,反应之一为SbCl + 6NaOH=NaSb(OH) ↓+5NaCl,C正确;D项,焦锑酸
5 6
钠难溶于水,“一系列操作”是过滤、洗涤、干燥,D错误;故选C。
6.下列实验能达成预期目的的是( )
实验
A.制备银 B.滴定未知浓度的 C.铁制镀件电
目的 D.制备乙酸乙酯
氨溶液 溶液 镀铜
【答案】B
【解析】A项,制备银氨溶液是在洁净的试管中加入2%AgNO 溶液,然后边振荡试管边逐滴滴入2%
3
氨水至沉淀恰好溶解,图中滴加试剂顺序错误,不能制得银氨溶液,A错误;B项,滴定管分酸式和碱式
两种,通常碱用碱式滴定管,酸用酸式滴定管,使用聚四氟乙烯的(耐酸碱腐蚀)活塞可以任意选择酸碱滴
定管,B正确;C项,在铁表面镀铜,应该用铁制镀件作阴极,铜片作阳极,C错误;D项,制备乙酸乙
酯,除图中反应物和催化剂,还需加入碎瓷片防止暴沸,同时产物应用饱和NaCO 溶液收集除杂,D错误;
2 3
故选B。
7.设N 为阿伏伽德罗常数的值,下列说法正确的是( )
A
A.10g的2H18O中含有的质子数与中子数均为5 N
2 A
B.32g硫在足量的氧气中充分燃烧,转移电子数为6 N
A
C.N(g)+3H(g) 2NH (g) ΔH=−92.4kJ/mol,1mol N 被还原,放出92.4kJ能量
2 2 3 2
D.pH=4的盐酸和pH=4的醋酸溶液等体积混合后,溶液中 的数目仍为10-4 N
A
【答案】C【解析】A项,2H18O中有10个质子,12个中子,相对分子量为22,10g2H18O物质的量为 mol,
2 2
质子数为 N ,中子数为 N ,A错误;B项,32g硫物质的量为1mol,在足量氧气中充分燃烧,生成
A A
1molSO ,转移电子数为4N ,B错误;C项,N(g)+3H(g) 2NH (g) ΔH=−92.4kJ/mol,根据热化学方
2 A 2 2 3
程式的含义,1mol N 参与反应被还原,放出92.4kJ能量,C正确;D项,没有说明体积具体是多少,无法
2
计算氢离子数目,D错误;故选C。
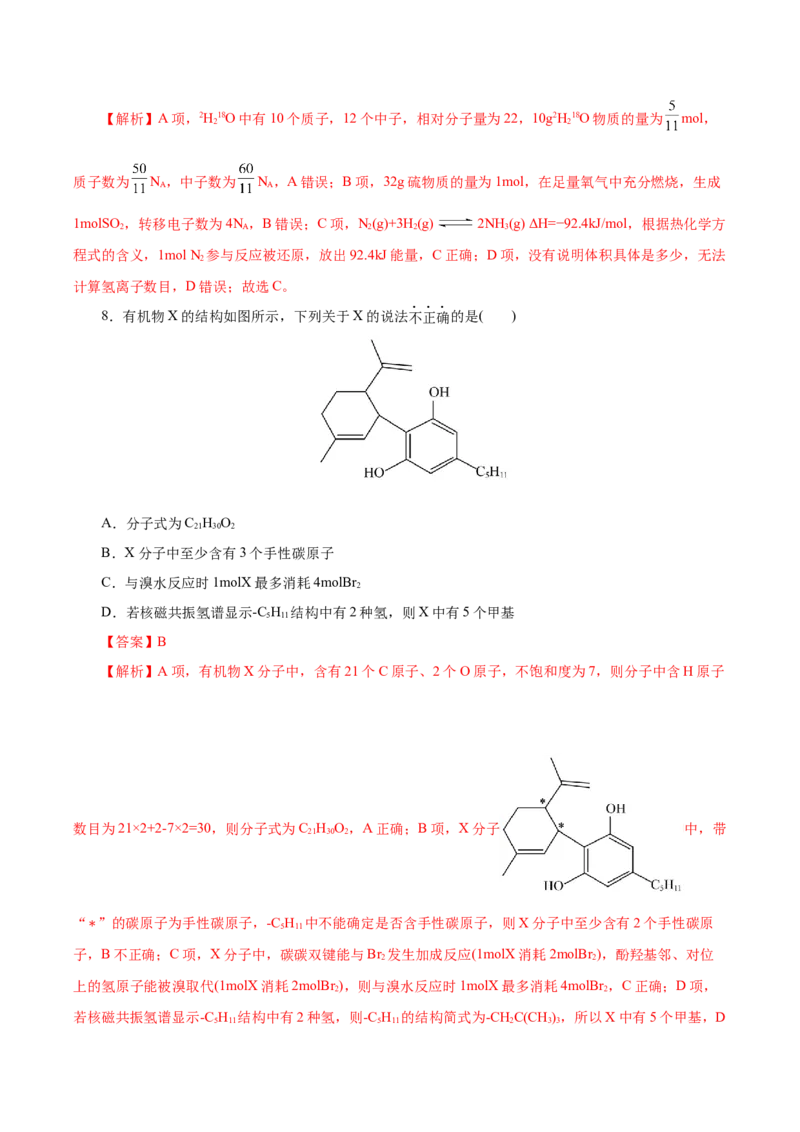
8.有机物X的结构如图所示,下列关于X的说法不正确的是( )
A.分子式为C H O
21 30 2
B.X分子中至少含有3个手性碳原子
C.与溴水反应时1molX最多消耗4molBr
2
D.若核磁共振氢谱显示-C H 结构中有2种氢,则X中有5个甲基
5 11
【答案】B
【解析】A项,有机物X分子中,含有21个C原子、2个O原子,不饱和度为7,则分子中含H原子
数目为21×2+2-7×2=30,则分子式为C H O,A正确;B项,X分子 中,带
21 30 2
“∗”的碳原子为手性碳原子,-C H 中不能确定是否含手性碳原子,则X分子中至少含有2个手性碳原
5 11
子,B不正确;C项,X分子中,碳碳双键能与Br 发生加成反应(1molX消耗2molBr ),酚羟基邻、对位
2 2
上的氢原子能被溴取代(1molX消耗2molBr ),则与溴水反应时1molX最多消耗4molBr ,C正确;D项,
2 2
若核磁共振氢谱显示-C H 结构中有2种氢,则-C H 的结构简式为-CHC(CH),所以X中有5个甲基,D
5 11 5 11 2 3 3正确;故选B。
9.W、X、Y、Z四种短周期元素,原子序数依次增大。四种元素形成的盐(XW )ZY 是强氧化剂,
4 2 2 8
常用于测定钢中锰的含量。(XW )ZY 中阴离子的结构如图所示,图中各原子最外层都达到8电子稳定结
4 2 2 8
构。下列说法正确的是( )
A.简单离子半径:W<X<Y<Z
B.氢化物的沸点:X<Y
C.(XW )ZY 中Z的杂化方式是dsp2
4 2 2 8
D.(XW )ZY 用于测定钢中锰的含量时,Y元素被还原
4 2 2 8
【答案】D
【解析】阴离子为 ,根据阴离子的结构和各原子最外层都达到8
电子稳定结构可知,Y连接2根共价键,结合(XW )ZY 是强氧化剂,可知,推出Y是O元素,含有过氧
4 2 2 8
键即具有强氧化性,由此阴离子结构可知ZY2-中含有2个-1价的氧、剩余的6个氧为-2价,因此Z的化
2 8
合价为+6价,结合题中所给原子序数关系,Z的原子序数最大,可知Z为S元素;阴离子呈-2价,故阳离
子呈+1价,W的原子序数最小,由XW+可知,XW+即为NH +,因此W为H元素,X为N元素,综合可
4 4 4
知,W、X、Y、Z分别为H、N、O、S元素。A项,核外电子层数越多,则离子半径越大,具有相同核外
电子结构时,核电荷数越大则离子半径越小,S2-核外有3个电子层,离子半径最大,由此可知简单离子的
半径:H-<O2-<N3-<S2-,故A错误;B项,X为N元素、Y是O元素,X的氢化物可能是NH 、NH,Y
3 2 4
的氢化物可能是HO、HO,未说明形成的是哪种氢化物,无法进行比较,故B错误;C项,在SO2-中
2 2 2 2 8
的中心原子S原子形成4个σ键,因此σ键电子对数为4,观察阴离子结构可知,S原子上没有孤电子对,
因此中心原子S原子的价层电子对数为4,硫原子并没有用到d轨道,因此采取的是sp3杂化,故C错误;
D项,在测定钢中锰的含量时,一般会将锰氧化为较高的价态,而(NH )SO 的强氧化性是阴离子结构中-
4 2 2 8
O-O-的-1价O体现的,在反应中化合价降低,被还原,作为氧化剂,故D正确;故选D。
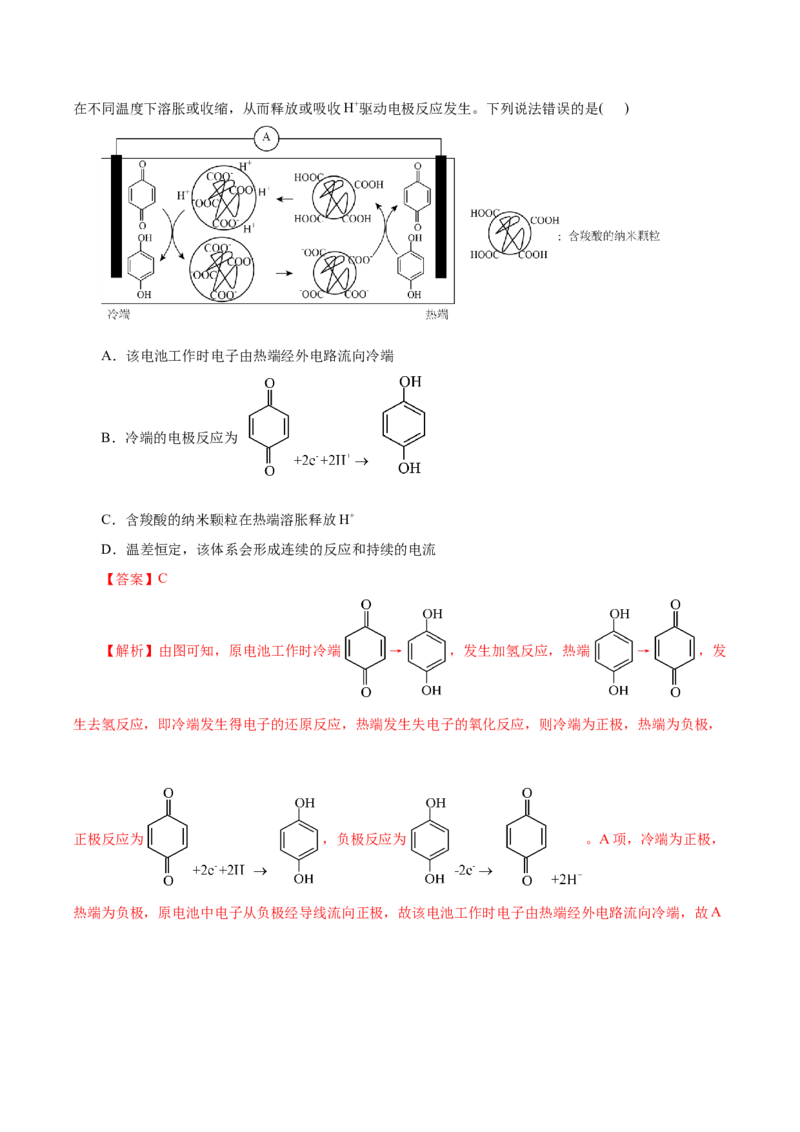
10.热电化学电池是一种新型的低成本低品位热富集体系,工作原理如下图所示,含羧酸的纳米颗粒在不同温度下溶胀或收缩,从而释放或吸收H+驱动电极反应发生。下列说法错误的是( )
A.该电池工作时电子由热端经外电路流向冷端
B.冷端的电极反应为
C.含羧酸的纳米颗粒在热端溶胀释放H+
D.温差恒定,该体系会形成连续的反应和持续的电流
【答案】C
【解析】由图可知,原电池工作时冷端 → ,发生加氢反应,热端 → ,发
生去氢反应,即冷端发生得电子的还原反应,热端发生失电子的氧化反应,则冷端为正极,热端为负极,
正极反应为 ,负极反应为 。A项,冷端为正极,
热端为负极,原电池中电子从负极经导线流向正极,故该电池工作时电子由热端经外电路流向冷端,故A正确;B项,冷端为正极,正极上 得电子生成 ,正极反应式为为
,故B正确;C项,热端为负极,负极反应为 ,则含羧酸的纳米颗粒
在热端溶胀吸收H+驱动电极反应发生,故C错误;D项,含羧酸的纳米颗粒在不同温度下溶胀或收缩,从
而释放或吸收H+驱动电极反应发生,则温差恒定时该电池能持续工作,形成连续的反应和持续的电流,故
D正确;故选C。
11.根据下列实验操作和现象能得到相应结论的是( )
选项 实验操作和现象 结论
向NaS溶液中通入足量CO,然后再将产生的
A 2 2 K (H CO)>K (H S)
气体导入CuSO 溶液中,产生黑色沉淀 a1 2 3 a1 2
4
向FeCl 和KSCN的混合溶液中滴入硝酸酸化
B 2 氧化性:Fe3+<Ag+
的AgNO 溶液,溶液变红
3
常温下,用pH计分别测定等体积
同温下,不同浓度的CHCOONH 溶液中水
C 1mol·L-1CHCOONH 溶液和 3 4
3 4 的电离程度相同
0.1mol·L-1CHCOONH 溶液的pH,pH都等于7
3 4
向盛有2mL一定浓度的Na[Ag(S O)]溶液的
3 2 3 2
D 试管中,滴入5滴2mol·L-1的KI溶液,产生黄 [Ag(S O)]3-发生了水解
2 3 2
色沉淀
【答案】A
【解析】A项,产生黑色沉淀,说明向NaS溶液中通入足量CO 生成了HS气体,强酸制弱酸,所以
2 2 2
K (H CO)>K (H S),A正确;B项,亚铁离子被硝酸氧化为铁离子,生成硫氰化铁,氧化性
a1 2 3 a1 2
HNO>Fe3+,无法比较铁离子和银离子的氧化性,B错误;C项,同温下,不同浓度的醋酸铵溶液中,两溶
3
液的水解程度不同,但同一溶液中的醋酸根离子和铵根离子的水解程度相同,故水的电离程度不相同,但
两溶液均呈中性,C错误;D项,黄色沉淀的成分为AgI,说明Na[Ag(S O)]溶液含有Ag+,即
3 2 3 2
[Ag(S O)]3-发生电离,而不是水解,D错误;故选A。
2 3 2
12.配合物间的结构转变是一种有趣的现象。配合物1经过加热可转变为配合物2,如图所示。下列说法错误的是( )
A.配合物1中含有2种配体 B.配合物2中N原子采取sp2杂化
C.转变过程中涉及配位键的断裂和形成 D.转变前后,Co的化合价由 价变为0价
【答案】D
【解析】A项,配合物1中,HO中氧原子提供孤对电子,Co2+提供空轨道形成配位键;配合物1右
2
侧N、O分别提供一对孤电子,与Co2+形成配位键,则配合物1中含有2种配体,A正确;B项,由配合
物2的结构可知,N形成2个σ键,一个配位键,故采取sp2杂化,B正确;C项,转变过程中,配合物1
中断裂2个HO与Co2+形成的配位键,配合物2中,SO 2-中的O与Co2+形成2个配位键,涉及配位键的断
2 4
裂和形成,C正确;D项,配合物1、2中Co都为+2价,Co的化合价没有发生变化,D错误;故选D。
13.钛酸钡(BTTO)是一种新型太阳能电池材料,其制备原理为:BaCO +X BTTO+ CO ↑。已知
3 2
钛酸钡的晶胞结构(Ti4+、Ba2+均与O2-接触)和元素周期表中钛的数据如图所示,晶胞参数为 为阿伏
加德罗常数的值。下列有关叙述正确的是( )
A.Ti元素的质量数为47.87 B.晶体中与Ti4+紧邻的O2-有12个
C.X的化学式为TiO D.钛酸钡的密度约为
2
【答案】C
【解析】A项,Ti元素的相对原子质量为47.87,故A错误;B项,根据晶胞结构图,晶体中与Ti4+紧
邻的O2-有6个,故B错误;C项,根据均摊原则,晶胞中Ti4+数 、Ba2+数1、O2-数为 ,钛酸钡的化学式为BaTiO ,根据元素守恒,X的化学式为TiO,故C正确;D项,根据均摊原则,晶胞中
3 2
Ti4+数1、Ba2+数1、O2-数为3,钛酸钡的密度约为 ,故D错误;故选
C。
14.分布系数 在处理平衡浓度时,应用广泛。图为草酸的分布系数与pH的关系图。其中,草酸
K =5.9×10-2,K =6.4×10-5下列说法不正确的是( )
a1 a2
A.忽略第二步水解,0.1mol·L-1的NaC O 中C O2-的水解率约为
2 2 4 2 4
B.当cC O2-=cHC O-,有
2 4 2 4
C.草酸氢钠溶液的 介于2.5~3之间
D.此图像不可以完全根据 滴定NaC O 的实验数据绘出
2 2 4
【答案】A
【解析】pH较小时,草酸主要以草酸分子形式存在,随着pH的逐渐增大,草酸分子的分布系数减小,
草酸氢根的分布系数逐渐增大,则δ 表示HC O 的分布系数,δ 表示HC O-的分布系数,随着pH值的继
2 2 2 4 1 2 4
续增大,草酸氢根的分布系数减小,草酸根的分布系数增大,则δ 表示C O2-的分布系数。且K =
0 2 4 al
,K = ,则图像中的两条竖线分别代表pK 和pK 。A项,C O2-的水
a2 a1 a2 2 4
解平衡常数K = =1.6×10-10,即cHC O-
h1 2 4=4.0×10-6 mol/L,则忽略第二步水解,0.1mol/L的NaC O 中的水解率约为 4.0×10-
2 2 4
3%<12%,A错误;B项, , ,由图可知,当 c(H C O)
2 2 4
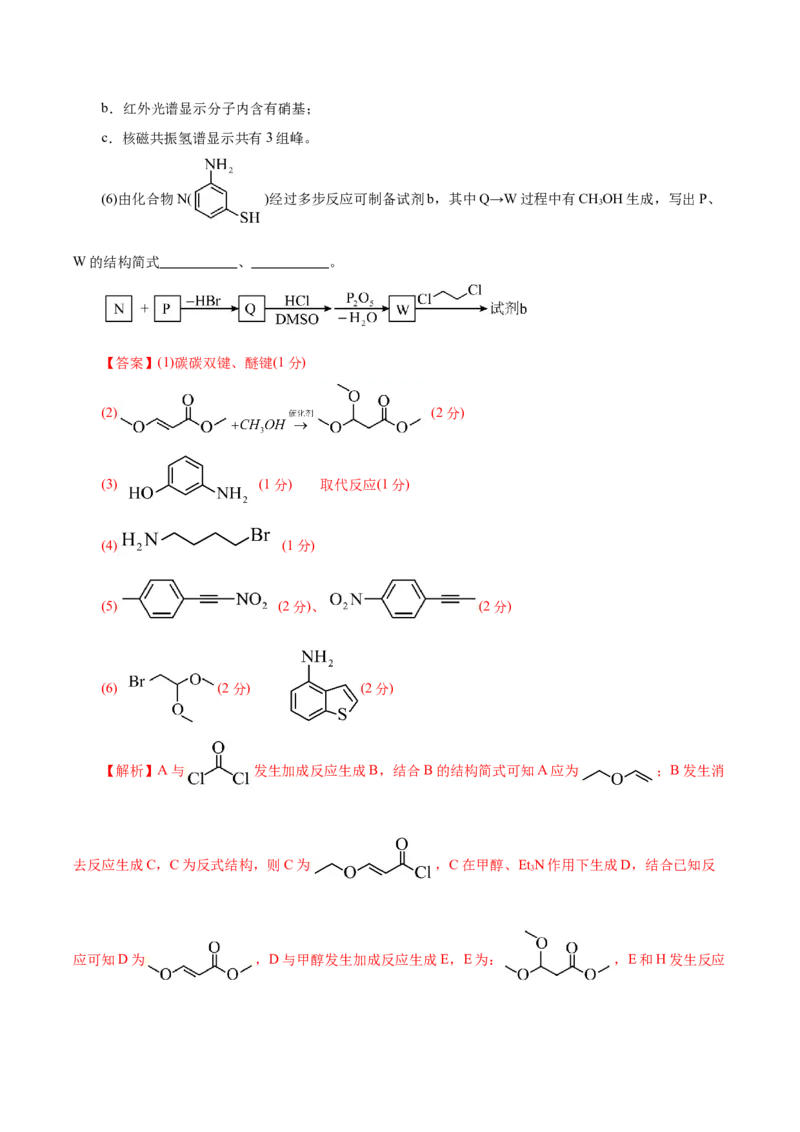
=c(C O2-) 时,2”、“=”或“<”)。
2
(2)根据盖斯定律,反应d的ΔH= (用含 的代数式表示)。
4
(3)以CO和HS反应制取COS的反应(a、b、c、d)体系在一定条件下建立平衡后,下列说法正确的是
2
_______(填选项字母)。
A.恒容条件下增大CO与HS的浓度,反应a、b、c、d的正反应速率都增加
2
B.升高温度,CO 的浓度增大,表明反应d为吸热反应
2
C.加入作用于反应a的催化剂,可增大ΔH 的值
1
D.降低反应温度,反应a~d的正、逆反应速率都减小
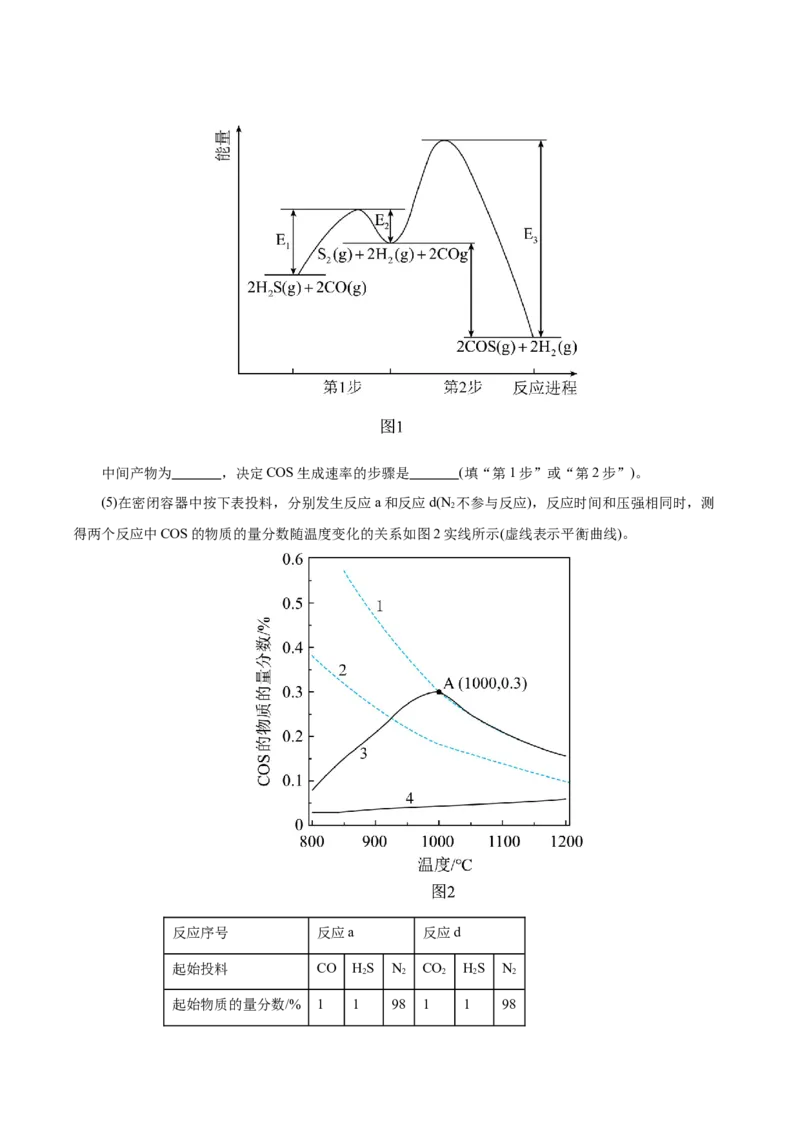
(4)反应a分两步进行,其反应过程中的能量变化如图1所示。中间产物为 ,决定COS生成速率的步骤是 (填“第1步”或“第2步”)。
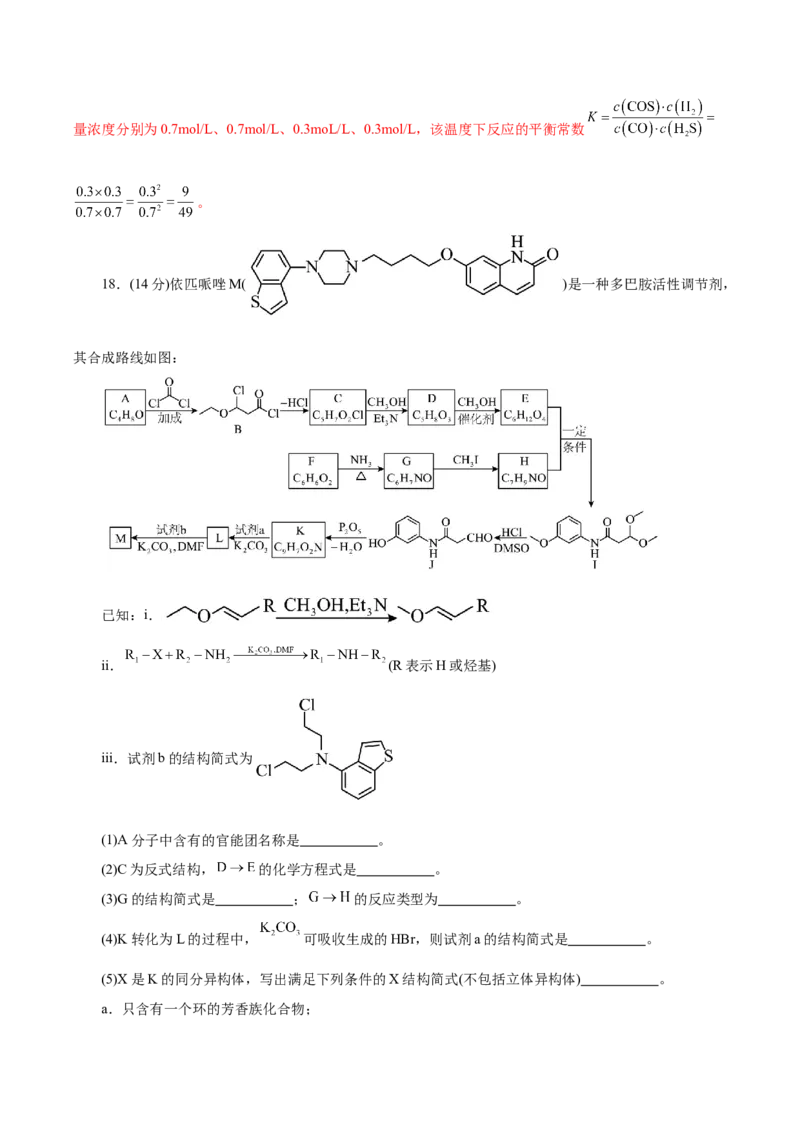
(5)在密闭容器中按下表投料,分别发生反应a和反应d(N 不参与反应),反应时间和压强相同时,测
2
得两个反应中COS的物质的量分数随温度变化的关系如图2实线所示(虚线表示平衡曲线)。
反应序号 反应a 反应d
起始投料 CO HS N CO HS N
2 2 2 2 2
起始物质的量分数/% 1 1 98 1 1 98①实验测得反应d的速率方程为 , ,k为速率常数,则
反应d达到平衡后,仅升高温度, 增大的倍数 (填“>”、“<”或“=”) 增大的倍数。
②已知相同条件下,反应a速率比反应d快,1000℃时,反应a的平衡常数。 (用分数表示,
写出分析与计算过程)。
【答案】(1)极性(1分) >(2分) (2)ΔH -ΔH (2分) (3)AD(2分)
1 3
(4)S (2分) 第2步(2分) (5)< (2分) (2分)
2
【解析】(1)COS的结构式为O=C=S,为直线形分子,但由于C=O与C=S键键长不同,正负电中心不
重合,故为极性分子;COS与CO 均为分子晶体,COS的相对分子质量更大,范德华力更大,沸点更高;
2
(2)根据盖斯定律,可知反应d=反应a-反应c,即ΔH=ΔH -ΔH ;(3)A项,恒容条件下增大CO和HS的浓
4 1 3 2
度,对于反应a、b、c、d来说,均增大了反应物的浓度,反应的正反应速率增大,A项正确;B项,升高
温度,CO 的浓度增大,可能为反应c正向移动导致,也可能是反应d逆向移动导致,所以无法判断反应d
2
吸热还是放热,B项错误;C项,催化剂可以同等程度增大正、逆反应速率,不能改变反应的焓变,C项
错误;D项,降低温度,体系的总能量降低,正、逆反应速率均减小,D项正确;故选AD;(4)由图可知,
中间产物为S,两步反应中,慢反应速率决定总反应速率,活化能越大,反应速率越慢,所以决定COS生
2
成速率的步骤是第2步;(5)①反应d中随温度的升高,生成物COS的物质的量分数减小,说明升高温度,
化学平衡逆向移动, ,则 增大的倍数 增大的倍数。②已知相同条件下,反应a速率比反应d
快,从图像可以看出,反应时间和压强相同时,相同温度下,曲线3的生成物COS物质的量分数大,所以
曲线3表示反应a,A点对应的平衡体系中,COS的物质的量分数为0.3%,假设容器体积为1L,起始时反
应的总物质的量为100mol,则CO、HS、N 的物质的量分别为1mol、1mol和98mol,该反应前后总物质
2 2
的量不变,所以平衡时总物质的量也为100mol,则平衡时COS的物质的量为0.3mol,设HS的转化量为x
2
mol,列三段式:
则 ,平衡时CO、HS、COS、H 的物质的量分别为0.7mol、0.7mol、0.3mol、0.3mol,物质的
2 2量浓度分别为0.7mol/L、0.7mol/L、0.3moL/L、0.3mol/L,该温度下反应的平衡常数
。
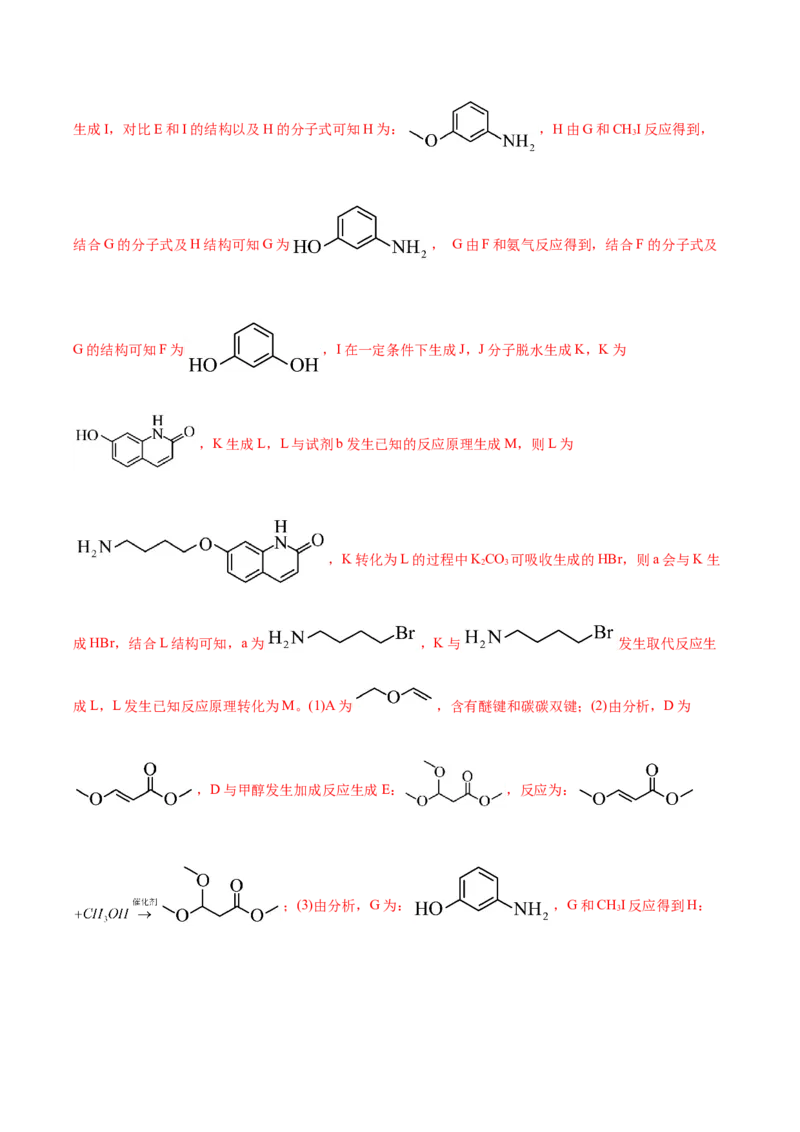
18.(14分)依匹哌唑M( )是一种多巴胺活性调节剂,
其合成路线如图:
已知:i.
ii. (R表示H或烃基)
iii.试剂b的结构简式为
(1)A分子中含有的官能团名称是 。
(2)C为反式结构, 的化学方程式是 。
(3)G的结构简式是 ; 的反应类型为 。
(4)K转化为L的过程中, 可吸收生成的HBr,则试剂a的结构简式是 。
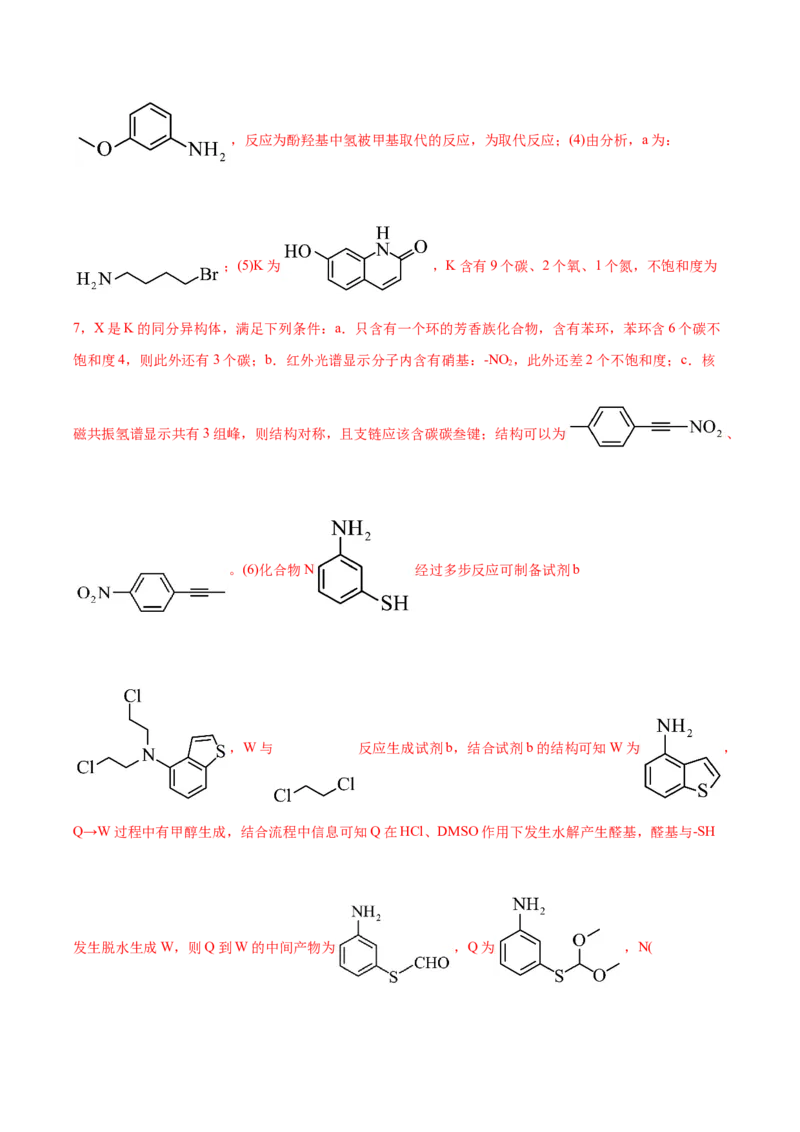
(5)X是K的同分异构体,写出满足下列条件的X结构简式(不包括立体异构体) 。
a.只含有一个环的芳香族化合物;b.红外光谱显示分子内含有硝基;
c.核磁共振氢谱显示共有3组峰。
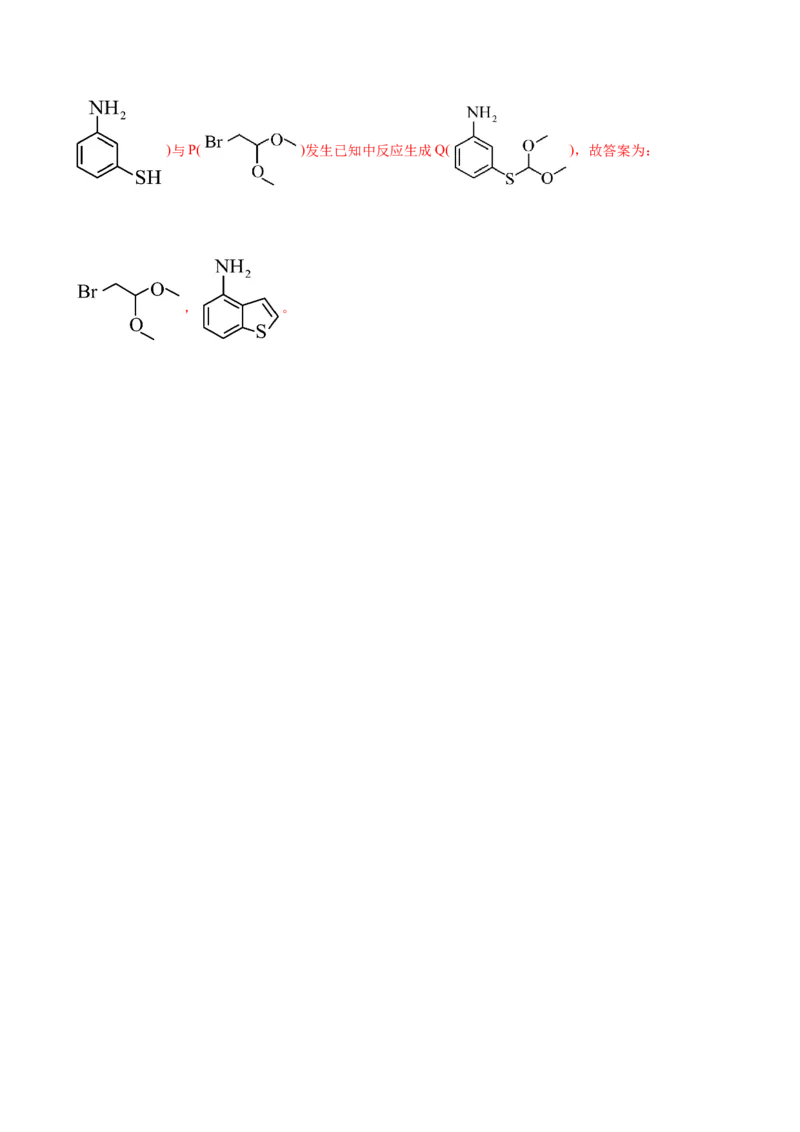
(6)由化合物N( )经过多步反应可制备试剂b,其中Q→W过程中有CHOH生成,写出P、
3
W的结构简式 、 。
【答案】(1)碳碳双键、醚键(1分)
(2) (2分)
(3) (1分) 取代反应(1分)
(4) (1分)
(5) (2分)、 (2分)
(6) (2分) (2分)
【解析】A与 发生加成反应生成B,结合B的结构简式可知A应为 ;B发生消
去反应生成C,C为反式结构,则C为 ,C在甲醇、EtN作用下生成D,结合已知反
3
应可知D为 ,D与甲醇发生加成反应生成E,E为: ,E和H发生反应生成I,对比E和I的结构以及H的分子式可知H为: ,H由G和CHI反应得到,
3
结合G的分子式及H结构可知G为 , G由F和氨气反应得到,结合F的分子式及
G的结构可知F为 ,I在一定条件下生成J,J分子脱水生成K,K为
,K生成L,L与试剂b发生已知的反应原理生成M,则L为
,K转化为L的过程中KCO 可吸收生成的HBr,则a会与K生
2 3
成HBr,结合L结构可知,a为 ,K与 发生取代反应生
成L,L发生已知反应原理转化为M。(1)A为 ,含有醚键和碳碳双键;(2)由分析,D为
,D与甲醇发生加成反应生成E: ,反应为:
;(3)由分析,G为: ,G和CHI反应得到H:
3,反应为酚羟基中氢被甲基取代的反应,为取代反应;(4)由分析,a为:
;(5)K为 ,K含有9个碳、2个氧、1个氮,不饱和度为
7,X是K的同分异构体,满足下列条件:a.只含有一个环的芳香族化合物,含有苯环,苯环含6个碳不
饱和度4,则此外还有3个碳;b.红外光谱显示分子内含有硝基:-NO ,此外还差2个不饱和度;c.核
2
磁共振氢谱显示共有3组峰,则结构对称,且支链应该含碳碳叁键;结构可以为 、
。(6)化合物N 经过多步反应可制备试剂b
,W与 反应生成试剂b,结合试剂b的结构可知W为 ,
Q→W过程中有甲醇生成,结合流程中信息可知Q在HCl、DMSO作用下发生水解产生醛基,醛基与-SH
发生脱水生成W,则Q到W的中间产物为 ,Q为 ,N()与P( )发生已知中反应生成Q( ),故答案为:
, 。