文档内容
绝密★启用前
2025 年高考考前信息必刷卷 03(浙江专用)
化 学
考情速递
高考·新动向:部分考生认为化学简单到离谱,甚至觉得不需要动脑子就能做对题目,这些考生平日里
知识积累扎实,在这次考试中做题得心应手。然而,对于那些化学基础稍薄弱或者对新题型预估不足
的考生,情况则不太乐观。新的大题题型打乱了他们的解题节奏,在考场上花费大量时间理解题意和
摸索解题思路,导致时间紧张。
高考·新考法:非选择题由原来的5道精简为4道。在分值分配上,第一大题16分,第二大题12分,
第三大题12分,第四大题12分。这种变化对考生的知识综合运用能力和思维转换能力提出了更高要求。
例如物质结构和无机流程融合成了16分的第一道大题,考生不仅要熟知物质结构的微观奥秘,还要能
将其与宏观的无机流程顺畅对接,增加了答题的难度和对知识综合运用的要求。题型布局打乱,一直
以来考生习惯的大题数量和出题套路被彻底打破,出题人改变了原有的题型布局。这种变化让考生失
去了熟悉题型带来的优势,需要在考场上重新适应新的题型结构,增加了考试的挑战性。
命题·大预测:在2025浙江化学第二次考试中,难度比首考略有增加。物质分类可能会给出一些特殊的
新材料或者新型化合物,要求依据物质分类的基础定义和特殊情况进行判断。在反应分类中,可能会
出现一些新的化学反应类型组合或者特殊反应条件下的反应分类。随着新能源的发展,2025年的化学
情景可能更多涉及新能源相关化学知识。例如在氢能的利用方面。在环境方面,可能会涉及到新型的
环境治理化学方法或者污染物检测的化学原理。
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 Na-23 Mg-24 Al-27 S-32 Cl-35.5
K-39 Ca-40 Mn-55 Fe-56 Cu-64 Zn-65 Br-80 I-127 Ag-108 Ba-137 Hg-201 Bi-209
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有一项是符合题
目要求的,不选、多选、错选均不得分)
1.下列分子属于极性分子的是( )
A.CH B.CO C.SO D.NH
4 2 3 3
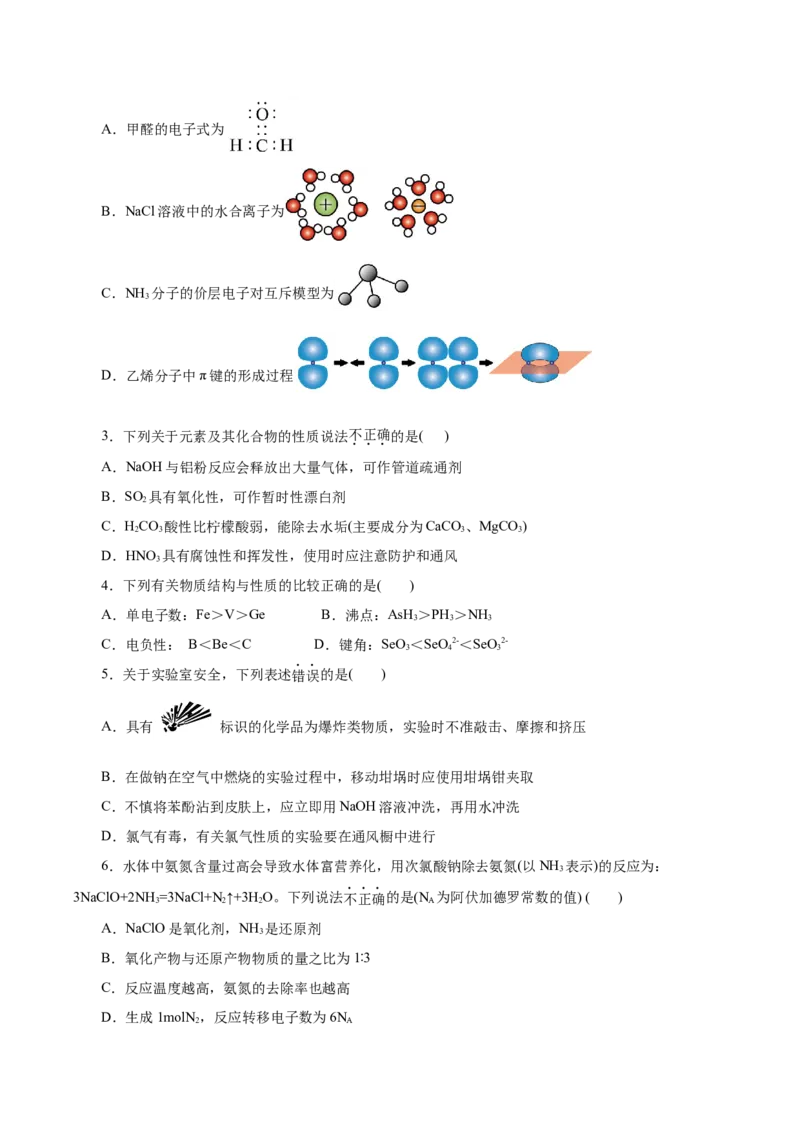
2.下列化学用语或图示正确的是( )A.甲醛的电子式为
B.NaCl溶液中的水合离子为
C.NH 分子的价层电子对互斥模型为
3
D.乙烯分子中π键的形成过程
3.下列关于元素及其化合物的性质说法不正确的是( )
A.NaOH与铝粉反应会释放出大量气体,可作管道疏通剂
B.SO 具有氧化性,可作暂时性漂白剂
2
C.HCO 酸性比柠檬酸弱,能除去水垢(主要成分为CaCO 、MgCO )
2 3 3 3
D.HNO 具有腐蚀性和挥发性,使用时应注意防护和通风
3
4.下列有关物质结构与性质的比较正确的是( )
A.单电子数:Fe>V>Ge B.沸点:AsH >PH >NH
3 3 3
C.电负性: B<Be<C D.键角:SeO<SeO2-<SeO2-
3 4 3
5.关于实验室安全,下列表述错误的是( )
A.具有 标识的化学品为爆炸类物质,实验时不准敲击、摩擦和挤压
B.在做钠在空气中燃烧的实验过程中,移动坩埚时应使用坩埚钳夹取
C.不慎将苯酚沾到皮肤上,应立即用NaOH溶液冲洗,再用水冲洗
D.氯气有毒,有关氯气性质的实验要在通风橱中进行
6.水体中氨氮含量过高会导致水体富营养化,用次氯酸钠除去氨氮(以NH 表示)的反应为:
3
3NaClO+2NH =3NaCl+N↑+3H O。下列说法不正确的是(N 为阿伏加德罗常数的值) ( )
3 2 2 A
A.NaClO是氧化剂,NH 是还原剂
3
B.氧化产物与还原产物物质的量之比为1∶3
C.反应温度越高,氨氮的去除率也越高
D.生成1molN ,反应转移电子数为6N
2 A7.从结构探析物质性质和用途是学习化学的有效方法。下列实例与解释不相符的是( )
选项 实例 解释
将95%乙醇加入[Cu(NH )]SO 溶液中 乙醇极性较小,降低了[Cu(NH )]SO 的溶
A 3 4 4 3 4 4
析出深蓝色晶体 解
铁丝在酒精喷灯上灼烧,焰色无明显变
B 铁原子核外电子在灼烧时没有发生跃迁
化
DNA中碱基A与T、G与C的互补配
C 分子间氢键作用实现了超分子的分子识别
对
D 熔点:C HNH NO <NH NO 引入乙基减弱了离子间的相互作用
2 5 3 3 4 3
8.下列离子方程式或电极反应式正确的是( )
A.用足量酸性KMnO 溶液除甲醛:5HCHO+2MnO -+6H+=5HCOOH+2Mn2++3H O
4 4 2
B.用铁电极电解饱和食盐水,阳极的电极反应为:2Cl-―2e-=Cl↑
2
C.NaSO 溶液中通入少量Cl:3SO 2-+Cl+H O=SO 2-+2Cl-+2HSO -
2 3 2 3 2 2 4 3
D.NH Cl固体溶于重水:NH ++D O NH ·D O+H+
4 4 2 3 2
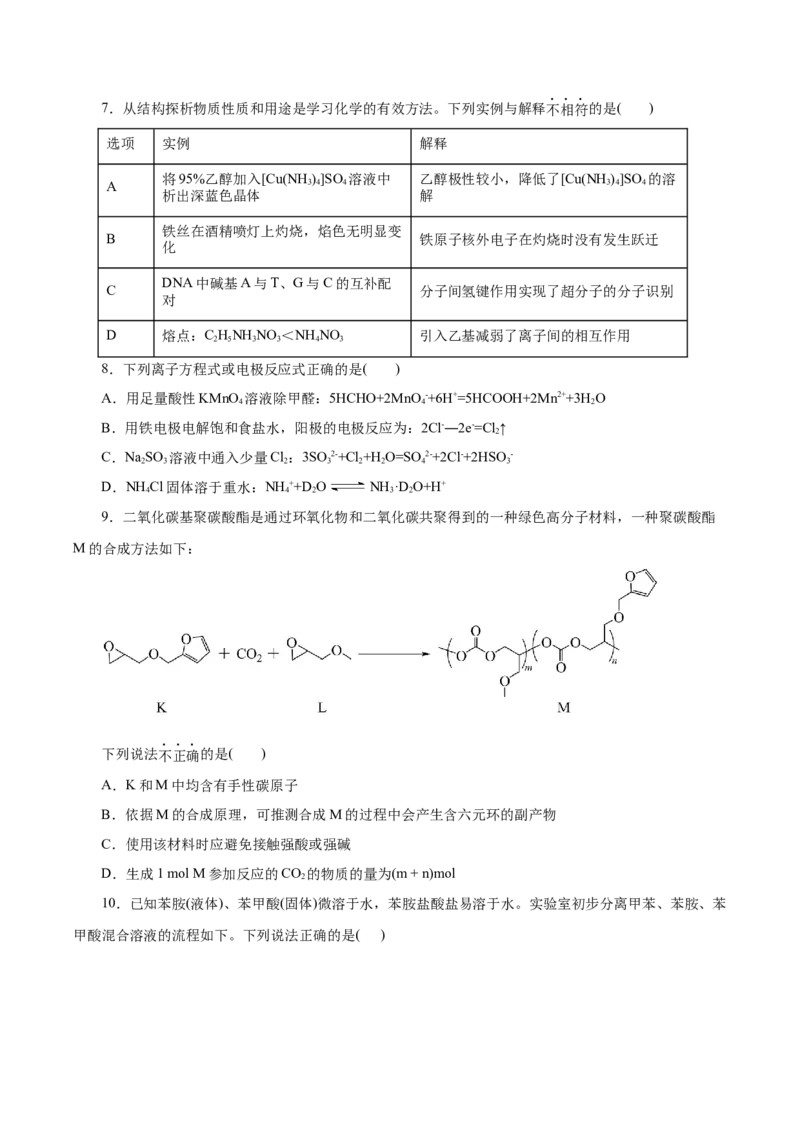
9.二氧化碳基聚碳酸酯是通过环氧化物和二氧化碳共聚得到的一种绿色高分子材料,一种聚碳酸酯
M的合成方法如下:
下列说法不正确的是( )
A.K和M中均含有手性碳原子
B.依据M的合成原理,可推测合成M的过程中会产生含六元环的副产物
C.使用该材料时应避免接触强酸或强碱
D.生成1 mol M参加反应的CO 的物质的量为(m + n)mol
2
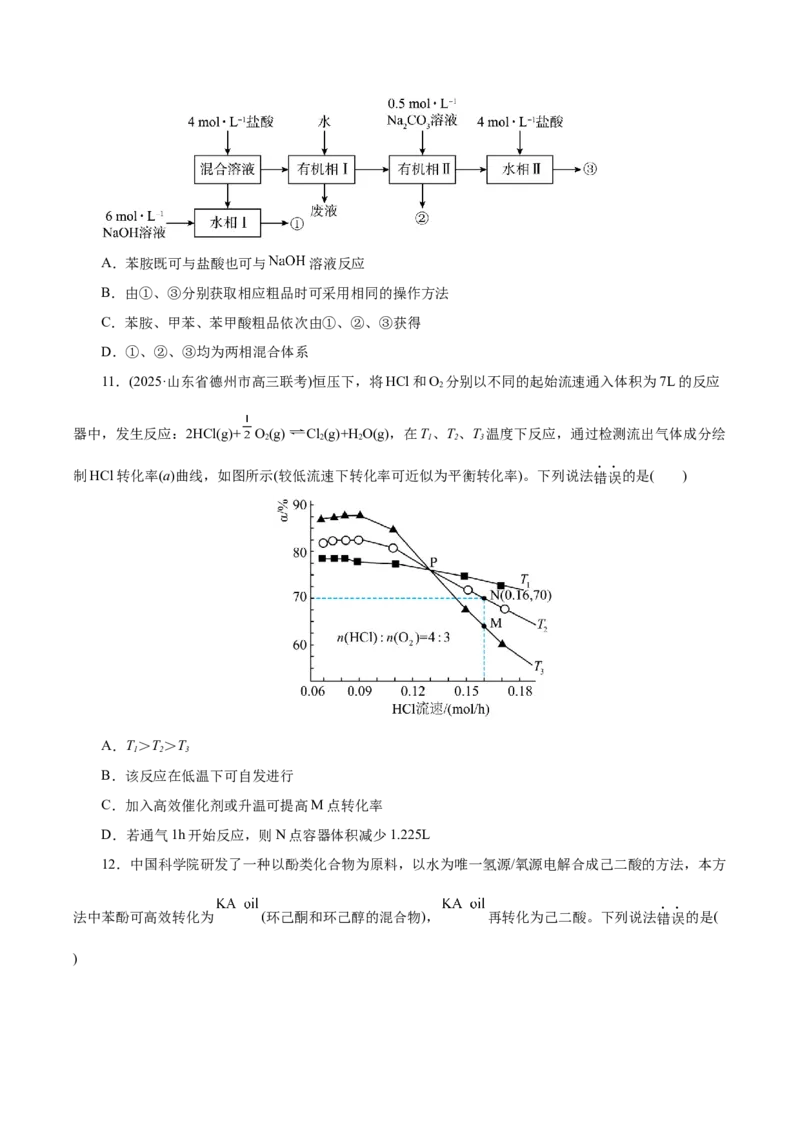
10.已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲苯、苯胺、苯
甲酸混合溶液的流程如下。下列说法正确的是( )A.苯胺既可与盐酸也可与 溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
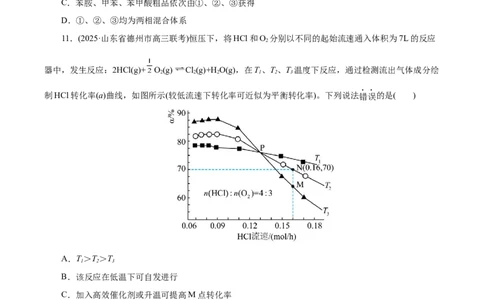
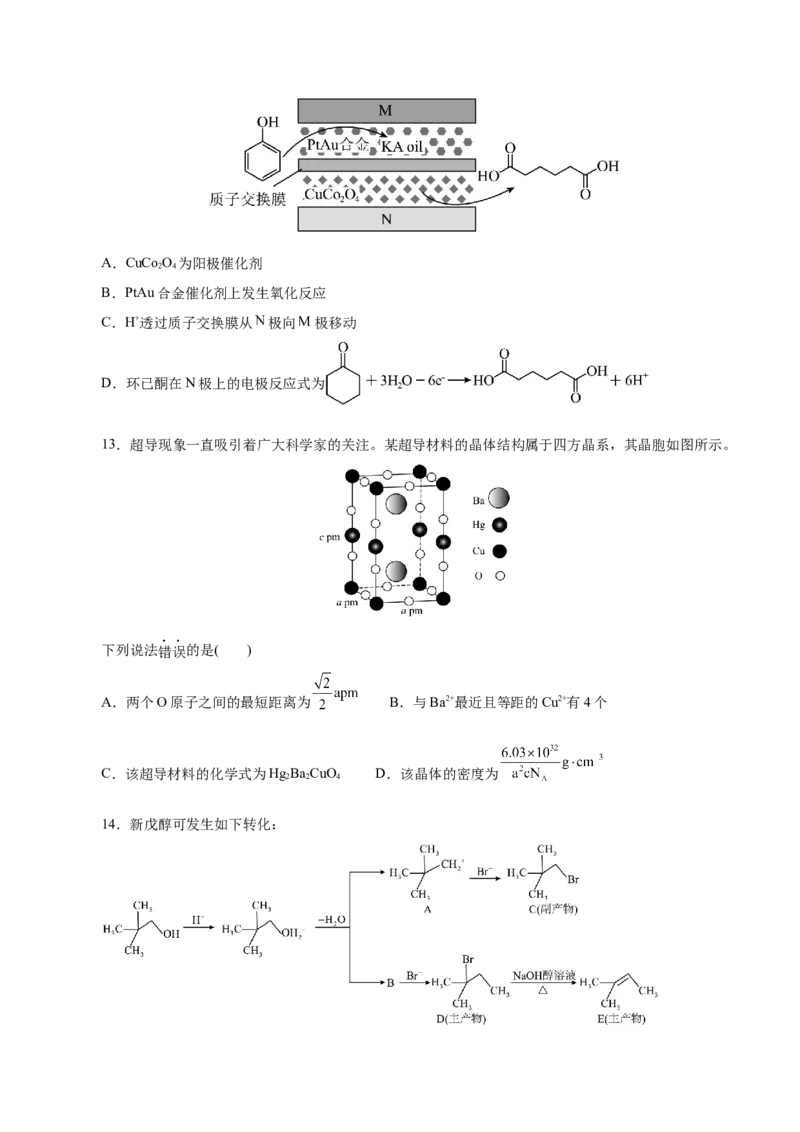
11.(2025·山东省德州市高三联考)恒压下,将HCl和O 分别以不同的起始流速通入体积为7L的反应
2
器中,发生反应:2HCl(g)+ O(g) Cl(g)+HO(g),在T、T、T 温度下反应,通过检测流出气体成分绘
2 2 2 1 2 3
制HCl转化率(a)曲线,如图所示(较低流速下转化率可近似为平衡转化率)。下列说法错误的是( )
A.T>T>T
1 2 3
B.该反应在低温下可自发进行
C.加入高效催化剂或升温可提高M点转化率
D.若通气1h开始反应,则N点容器体积减少1.225L
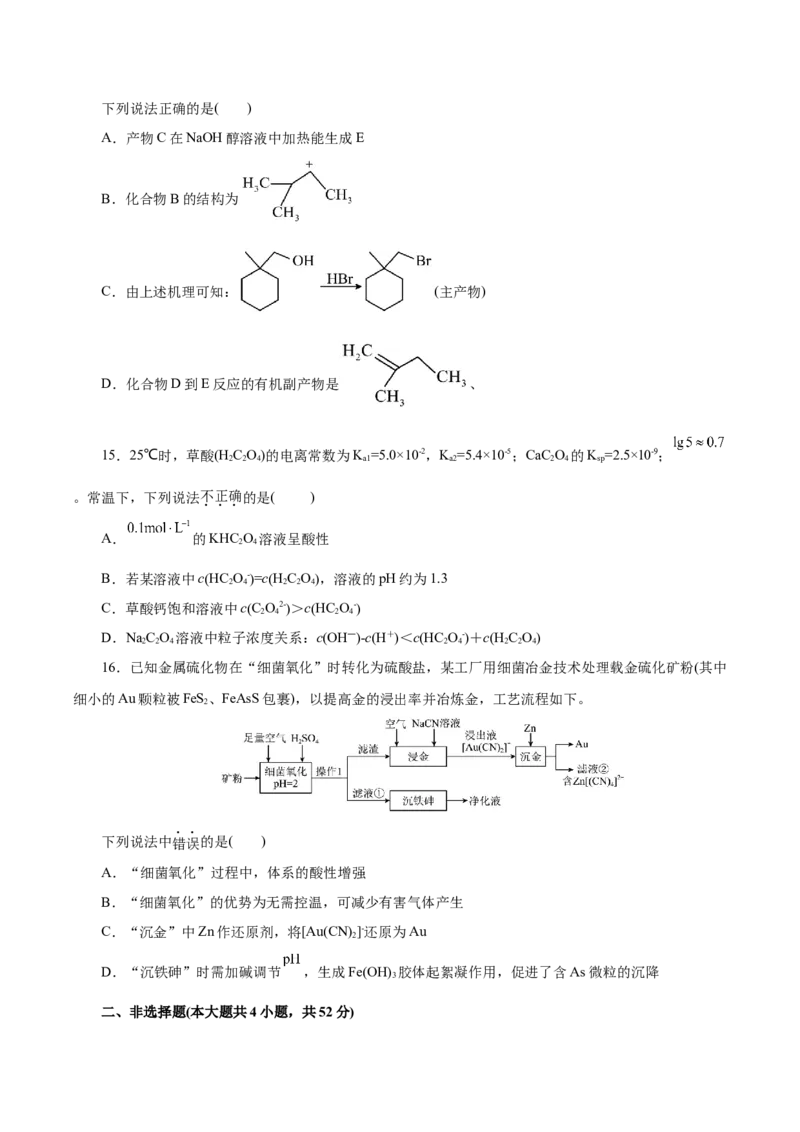
12.中国科学院研发了一种以酚类化合物为原料,以水为唯一氢源/氧源电解合成己二酸的方法,本方
法中苯酚可高效转化为 (环己酮和环己醇的混合物), 再转化为己二酸。下列说法错误的是(
)A.CuCo O 为阳极催化剂
2 4
B.PtAu合金催化剂上发生氧化反应
C.H+透过质子交换膜从 极向 极移动
D.环已酮在N极上的电极反应式为
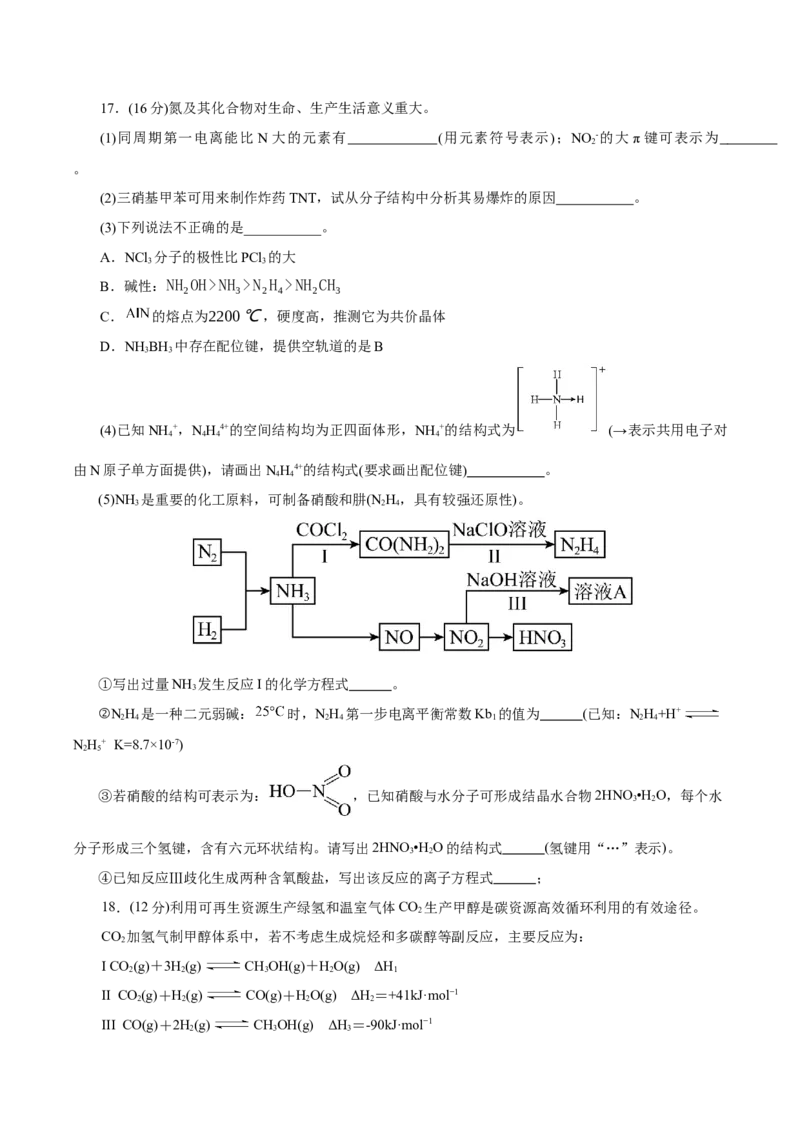
13.超导现象一直吸引着广大科学家的关注。某超导材料的晶体结构属于四方晶系,其晶胞如图所示。
下列说法错误的是( )
A.两个O原子之间的最短距离为 B.与Ba2+最近且等距的Cu2+有4个
C.该超导材料的化学式为HgBa CuO D.该晶体的密度为
2 2 4
14.新戊醇可发生如下转化:下列说法正确的是( )
A.产物C在NaOH醇溶液中加热能生成E
B.化合物B的结构为
C.由上述机理可知: (主产物)
D.化合物D到E反应的有机副产物是 、
15.25℃时,草酸(H C O)的电离常数为K =5.0×10-2,K =5.4×10-5;CaC O 的K =2.5×10-9;
2 2 4 a1 a2 2 4 sp
。常温下,下列说法不正确的是( )
A. 的KHC O 溶液呈酸性
2 4
B.若某溶液中cHC O-=cHC O,溶液的pH约为1.3
2 4 2 2 4
C.草酸钙饱和溶液中cC O2->cHC O-
2 4 2 4
D.NaC O 溶液中粒子浓度关系:c(OH―)-c(H+)<cHC O-+cHC O
2 2 4 2 4 2 2 4
16.已知金属硫化物在“细菌氧化”时转化为硫酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中
细小的Au颗粒被FeS、FeAsS包裹),以提高金的浸出率并冶炼金,工艺流程如下。
2
下列说法中错误的是( )
A.“细菌氧化”过程中,体系的酸性增强
B.“细菌氧化”的优势为无需控温,可减少有害气体产生
C.“沉金”中Zn作还原剂,将[Au(CN) ]-还原为Au
2
D.“沉铁砷”时需加碱调节 ,生成Fe(OH) 胶体起絮凝作用,促进了含As微粒的沉降
3
二、非选择题(本大题共4小题,共52分)17.(16分)氮及其化合物对生命、生产生活意义重大。
(1)同周期第一电离能比 N大的元素有 (用元素符号表示);NO -的大π键可表示为
2
。
(2)三硝基甲苯可用来制作炸药TNT,试从分子结构中分析其易爆炸的原因 。
(3)下列说法不正确的是___________。
A.NCl 分子的极性比PCl 的大
3 3
B.碱性:NH OH>NH >N H >NH CH
2 3 2 4 2 3
C. 的熔点为2200℃,硬度高,推测它为共价晶体
D.NH BH 中存在配位键,提供空轨道的是B
3 3
(4)已知NH +,NH4+的空间结构均为正四面体形,NH +的结构式为 (→表示共用电子对
4 4 4 4
由N原子单方面提供),请画出NH4+的结构式(要求画出配位键) 。
4 4
(5)NH 是重要的化工原料,可制备硝酸和肼(N H,具有较强还原性)。
3 2 4
①写出过量NH 发生反应I的化学方程式 。
3
②NH 是一种二元弱碱: 时,NH 第一步电离平衡常数Kb 的值为 (已知:NH+H+
2 4 2 4 1 2 4
NH+ K=8.7×10-7)
2 5
③若硝酸的结构可表示为: ,已知硝酸与水分子可形成结晶水合物2HNO•H O,每个水
3 2
分子形成三个氢键,含有六元环状结构。请写出2HNO•H O的结构式 (氢键用“…”表示)。
3 2
④已知反应Ⅲ歧化生成两种含氧酸盐,写出该反应的离子方程式 ;
18.(12分)利用可再生资源生产绿氢和温室气体CO 生产甲醇是碳资源高效循环利用的有效途径。
2
CO 加氢气制甲醇体系中,若不考虑生成烷烃和多碳醇等副反应,主要反应为:
2
I CO (g)+3H(g) CHOH(g)+HO(g) ΔH
2 2 3 2 1
II CO(g)+H(g) CO(g)+HO(g) ΔH =+41kJ·mol−1
2 2 2 2
III CO(g)+2H(g) CHOH(g) ΔH =-90kJ·mol−1
2 3 3(1)计算反应I的焓变 。
(2)以250℃、5Mpa、n(H ):n(CO)=3的平衡为基础,探讨温度,压强和原料气组成对平衡的影响,
2 2
以下说法错误的是___________。
A.随着温度升高,甲醇的百分含量将降低
B.随着压强增大,甲醇的产率将增大
C.随着n(H ):n(CO)的增加,CO的转化率将下降
2 2
D.若在原料气里加入CO,则CO 转化率将增大
2
(3)若只关注反应I,氢气和甲醇的燃烧热分别为285 kJ·mol−1和726 kJ·mol−1,则绿氢生产绿甲醇的理
论能量转化效率为 (保留一位小数)。
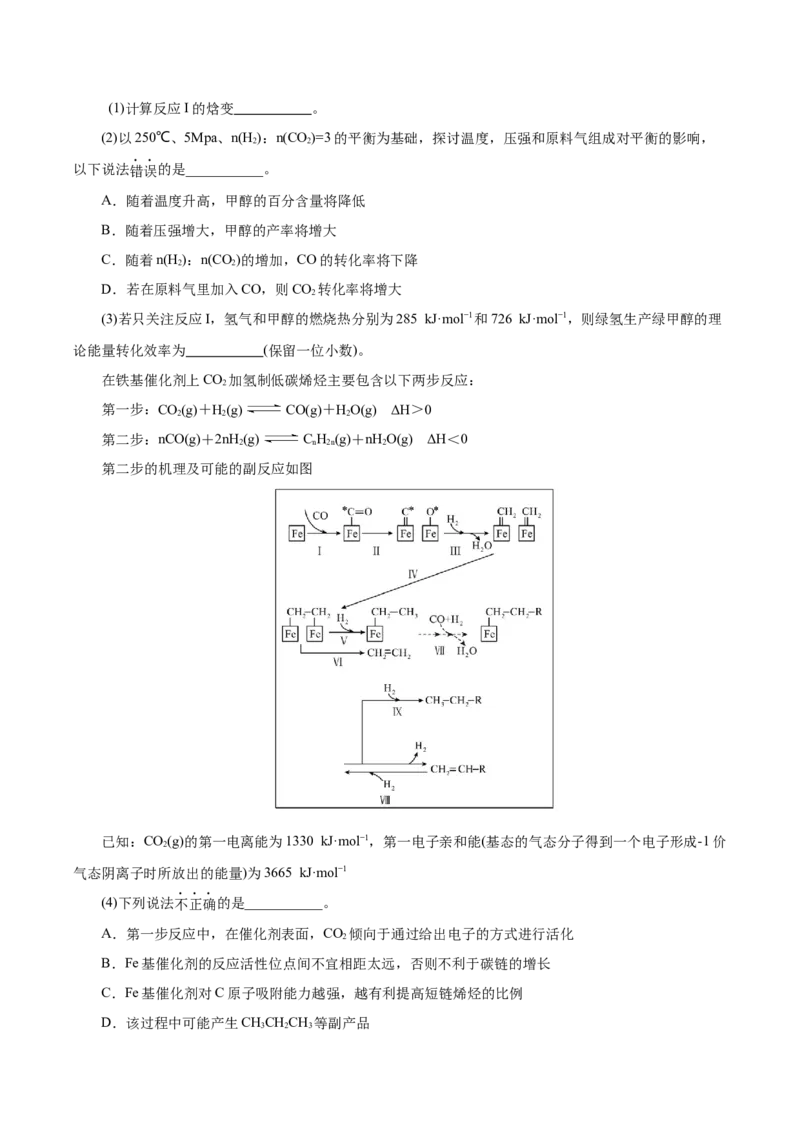
在铁基催化剂上CO 加氢制低碳烯烃主要包含以下两步反应:
2
第一步:CO(g)+H(g) CO(g)+HO(g) ΔH>0
2 2 2
第二步:nCO(g)+2nH(g) C H (g)+nHO(g) ΔH<0
2 n 2n 2
第二步的机理及可能的副反应如图
已知:CO(g)的第一电离能为1330 kJ·mol−1,第一电子亲和能(基态的气态分子得到一个电子形成-1价
2
气态阴离子时所放出的能量)为3665 kJ·mol−1
(4)下列说法不正确的是___________。
A.第一步反应中,在催化剂表面,CO 倾向于通过给出电子的方式进行活化
2
B.Fe基催化剂的反应活性位点间不宜相距太远,否则不利于碳链的增长
C.Fe基催化剂对C原子吸附能力越强,越有利提高短链烯烃的比例
D.该过程中可能产生CHCHCH 等副产品
3 2 3(5)在其他条件恒定的情况下,适当降低原料气的流速,CO 的转化率将 (填“增大”或
2
“减小”),原因为 ,产物中 将 ,原因为 (结合反应机理中的
步骤来回答)。
19.(12分)某小组采用如下实验流程制备难溶于水的白色BiOCl:
已知:Bi(NO) 极易水解产生难溶的BiONO 固体, 。
3 3 3
(1)下图为步骤Ⅰ的实验装置图(夹持仪器和尾气处理装置已省略),仪器A的名称是 。
(2)下列说法正确的是_______。
A.步骤Ⅰ:加热温度越高,溶解速率越快,产率越高
B.步骤Ⅱ:可加适量的NaOH溶液调节pH
C.步骤Ⅲ:在通风橱中浓缩至蒸发皿中大量晶体析出
D.步骤Ⅳ:试剂X选用HCl、NaCl,组合使用更有利于制备BiOCl
(3)写出Bi(NO) 水解离子方程式 。
3 3
①简述实验室配制 溶液方法 。
②请结合浓度商和平衡常数解释HNO 可抑制Bi(NO) 的水解 。
3 3 3
(4)利用HNO 溶液与NaOH溶液测定中和反应反应热,从下列选项中选择合适的操作补全测定步骤(有
3
些步骤可重复使用): 。
用量筒量取50mL0.50mol·L-1HNO→(_______)→(_______)→(_______)→(_______)→用另一个量筒量取
3
50mL0.55mol·L-1NaOH溶液→(_______)→(_______)→(_______)→打开杯盖,将NaOH溶液倒入量热计的
内筒,盖上杯盖→(a)→(e)→测量并记录温度→重复上述步骤两次。
a.插入温度计
b.测量并记录温度c.打开杯盖,将硝酸倒入量热计的内筒,盖上杯盖
d.用蒸馏水把温度计上的溶液冲洗干净,擦干备用
e.搅拌器匀速搅拌
(5)测定产品的纯度:称取产品0.1200g于锥形瓶中,加盐酸溶解,加入饱和硫脲(简写为TU)与Bi3+形
成黄色溶液,再用0.0200mol·L-1的EDTA滴定至终点,三次滴定消耗EDTA溶液的平均体积为20.50 mL,
则产品的纯度为 (已知形成无色[Bi(EDTA)]-远比形成黄色[Bi(TU) ]3+容易,M=260.5 g·mol-1)。
2
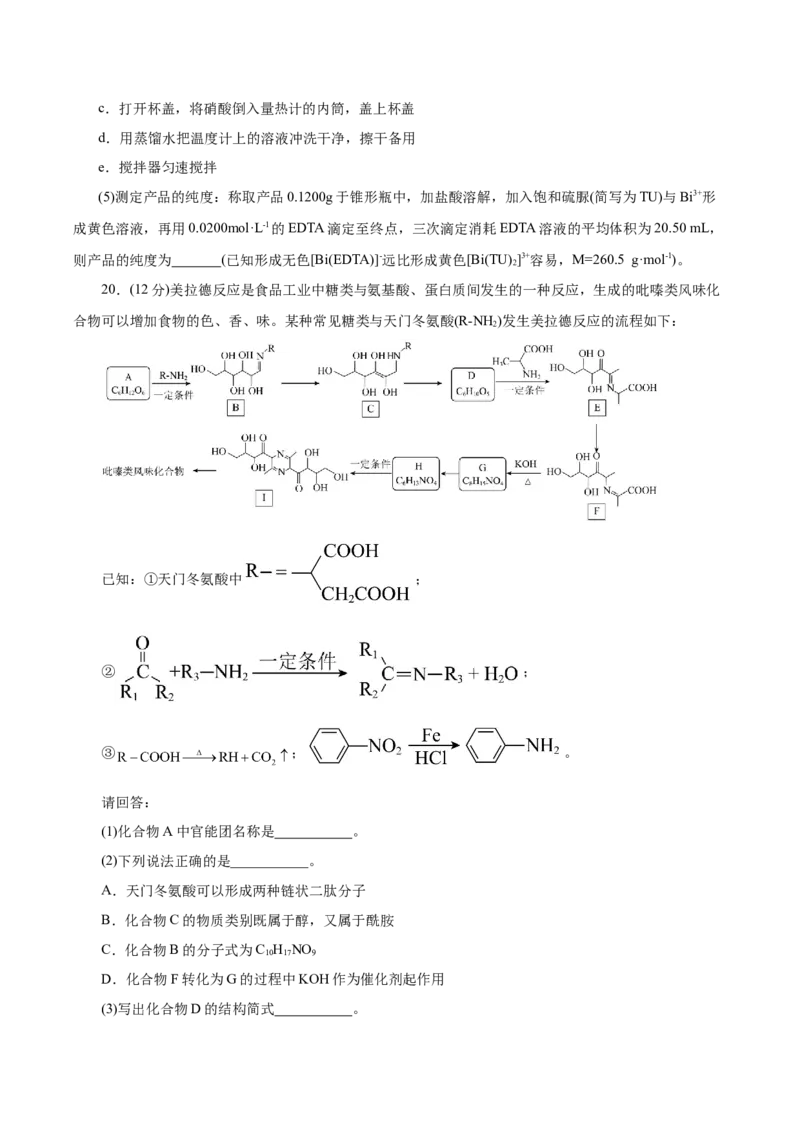
20.(12分)美拉德反应是食品工业中糖类与氨基酸、蛋白质间发生的一种反应,生成的吡嗪类风味化
合物可以增加食物的色、香、味。某种常见糖类与天门冬氨酸(R-NH )发生美拉德反应的流程如下:
2
已知:①天门冬氨酸中 ;
② ;
③ ; 。
请回答:
(1)化合物A中官能团名称是 。
(2)下列说法正确的是___________。
A.天门冬氨酸可以形成两种链状二肽分子
B.化合物C的物质类别既属于醇,又属于酰胺
C.化合物B的分子式为C H NO
10 17 9
D.化合物F转化为G的过程中KOH作为催化剂起作用
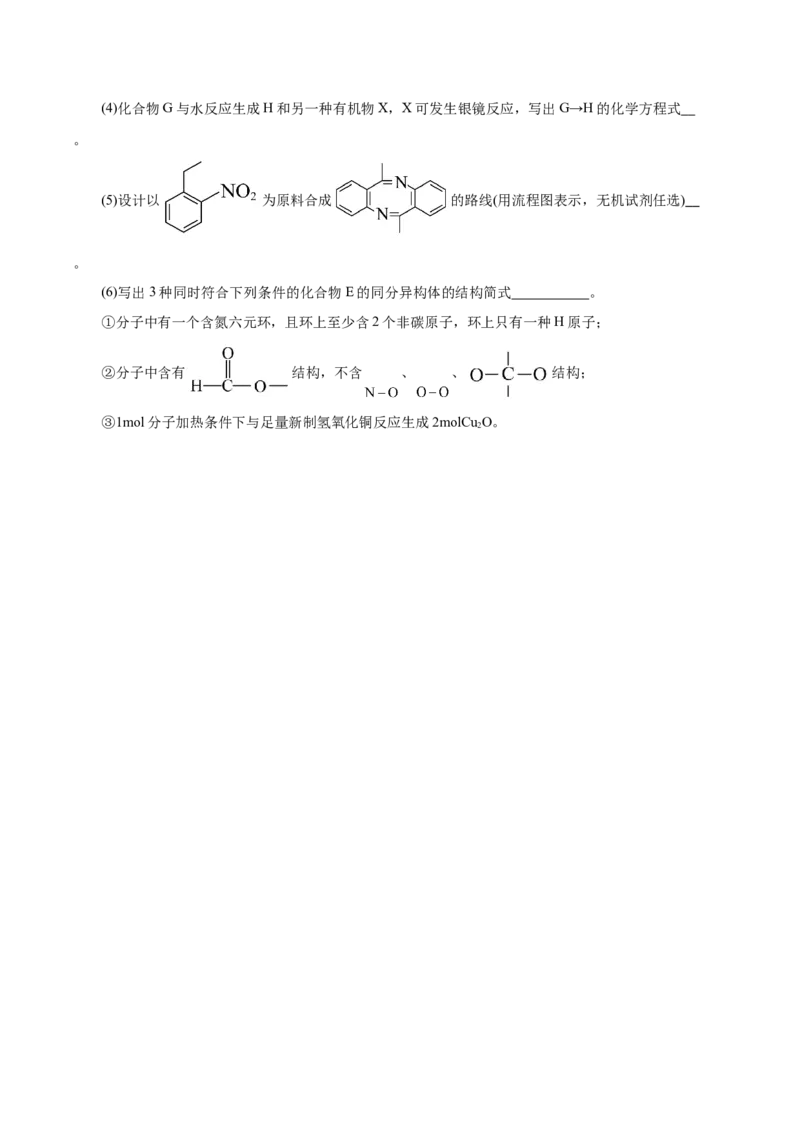
(3)写出化合物D的结构简式 。(4)化合物G与水反应生成H和另一种有机物X,X可发生银镜反应,写出G→H的化学方程式
。
(5)设计以 为原料合成 的路线(用流程图表示,无机试剂任选)
。
(6)写出3种同时符合下列条件的化合物E的同分异构体的结构简式 。
①分子中有一个含氮六元环,且环上至少含2个非碳原子,环上只有一种H原子;
②分子中含有 结构,不含 、 、 结构;
③1mol分子加热条件下与足量新制氢氧化铜反应生成2molCu O。
2