文档内容
微专题39 水溶液中平衡图像的拓展与探析
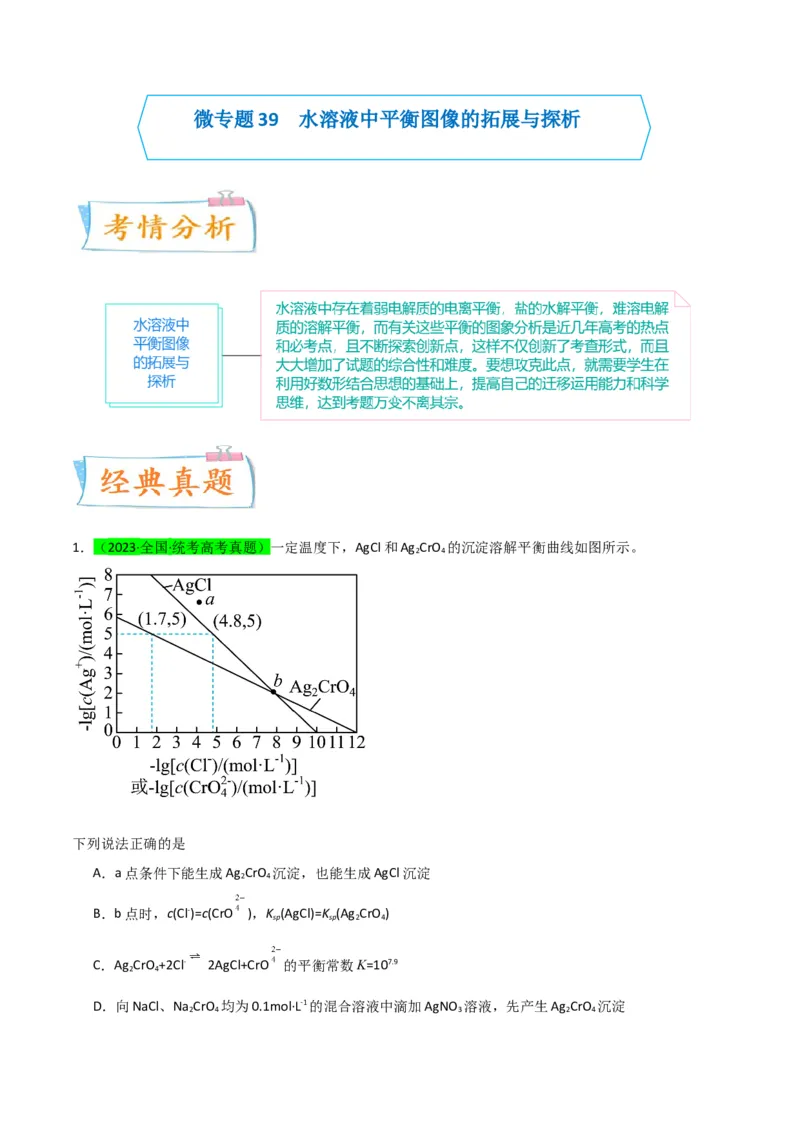
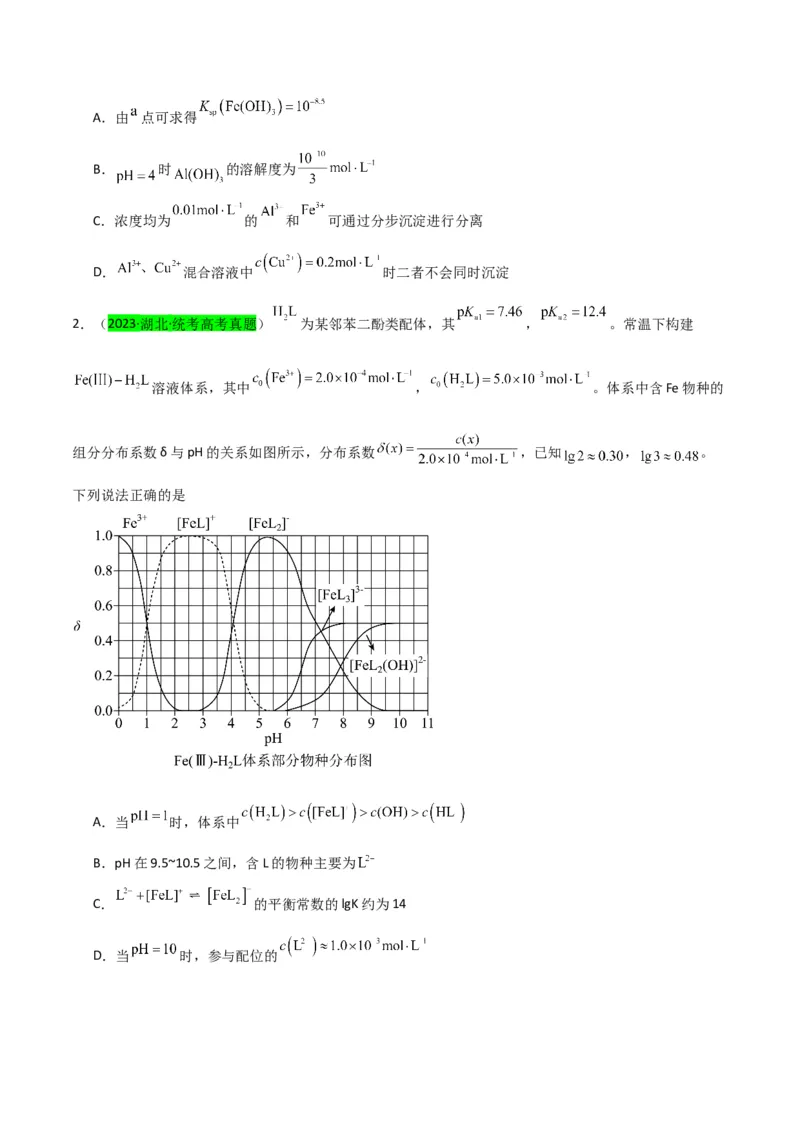
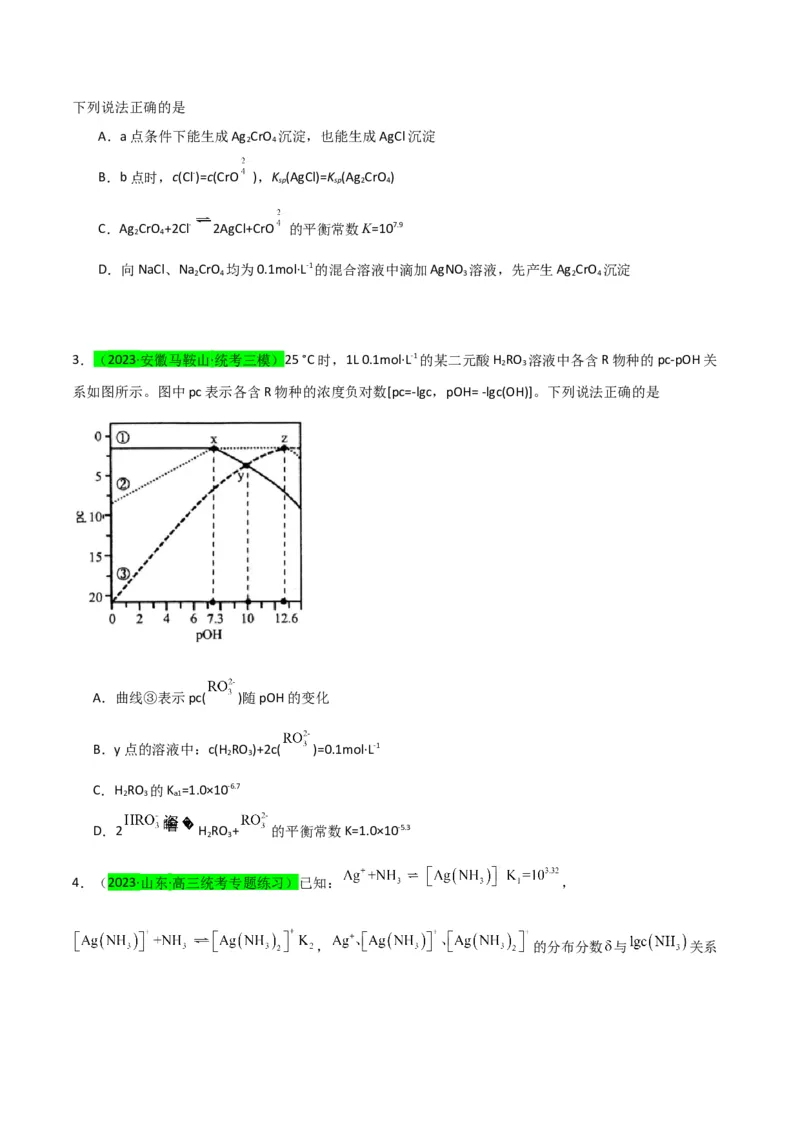
1.(2023·全国·统考高考真题)一定温度下,AgCl和Ag CrO 的沉淀溶解平衡曲线如图所示。
2 4
下列说法正确的是
A.a点条件下能生成Ag CrO 沉淀,也能生成AgCl沉淀
2 4
B.b点时,c(Cl-)=c(CrO ),K (AgCl)=K (Ag CrO )
sp sp 2 4
C.Ag CrO +2Cl- 2AgCl+CrO 的平衡常数K=107.9
2 4
D.向NaCl、Na CrO 均为0.1mol·L-1的混合溶液中滴加AgNO 溶液,先产生Ag CrO 沉淀
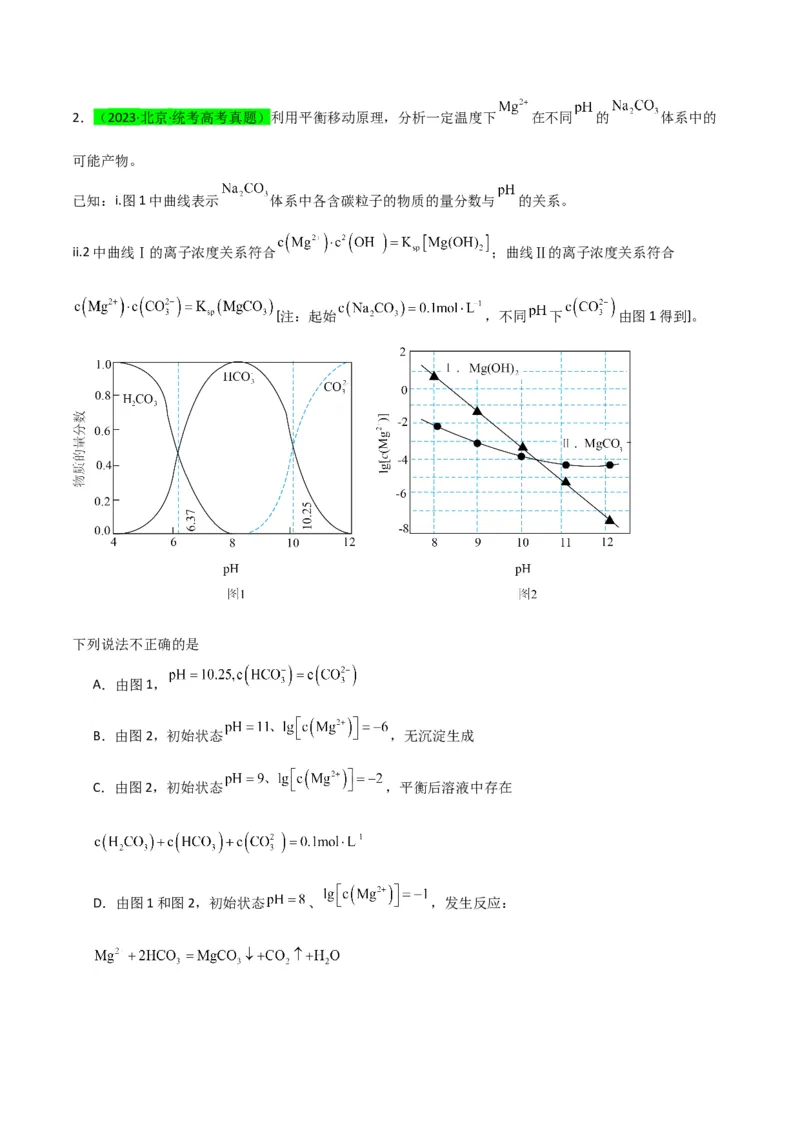
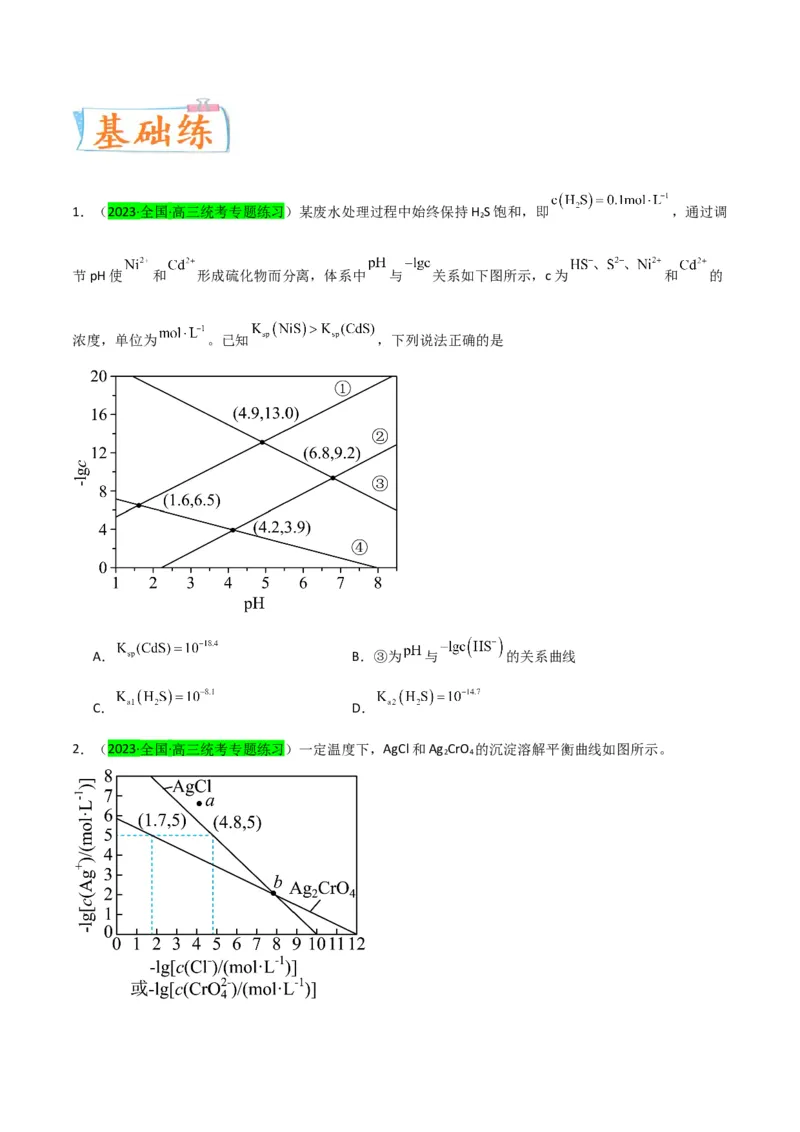
2 4 3 2 42.(2023·北京·统考高考真题)利用平衡移动原理,分析一定温度下 在不同 的 体系中的
可能产物。
已知:i.图1中曲线表示 体系中各含碳粒子的物质的量分数与 的关系。
ii.2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 ,不同 下 由图1得到]。
下列说法不正确的是
A.由图1,
B.由图2,初始状态 ,无沉淀生成
C.由图2,初始状态 ,平衡后溶液中存在
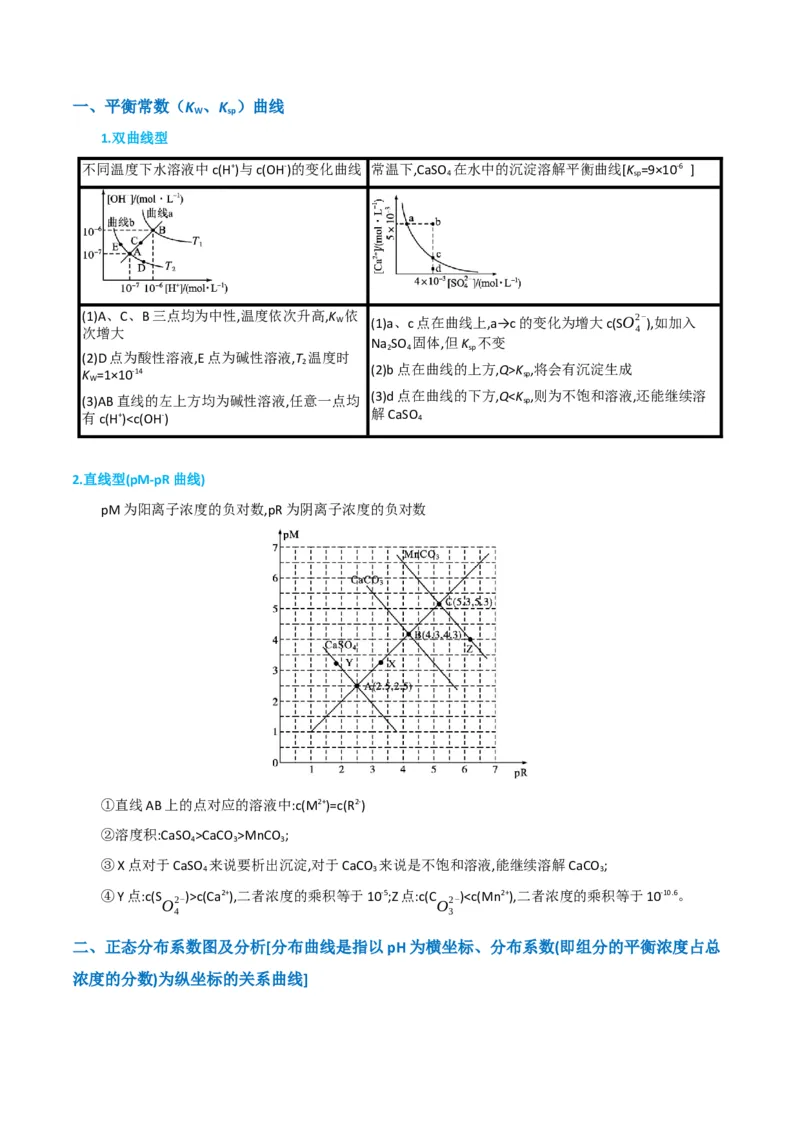
D.由图1和图2,初始状态 、 ,发生反应:一、分布系数图像题应注意的三点
1.明标:要想理清溶液中粒子浓度关系,首先看各纵、横坐标表示的含义,尤其多维坐标图像更应注意。
2.理线:根据坐标内曲线的变化趋势,理清每曲线、每部分表示的含义,判断曲线所代表的粒子。
3.求点:要注意图像内的各种交点,通过交点建立不同粒子间的等量关系,由已知量代替未知量,简化求
解过程。
二、解沉淀溶解平衡图像题三步骤
第一步:明确图像中纵、横坐标的含义。
纵、横坐标通常是难溶物溶解后电离出的离子浓度。
第二步:理解图像中线上点、线外点的含义。
(1)曲线上任意一点都达到了沉淀溶解平衡状态,此时Q=Ksp。在
c
温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能在曲
线上变化,不会出现在曲线以外。
(2)曲线上方区域的点均为过饱和溶液,此时Q>Ksp。
c
(3)曲线下方区域的点均为不饱和溶液,此时QK
sp
,将会有沉淀生成
W
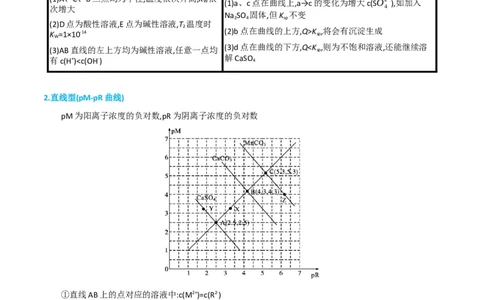
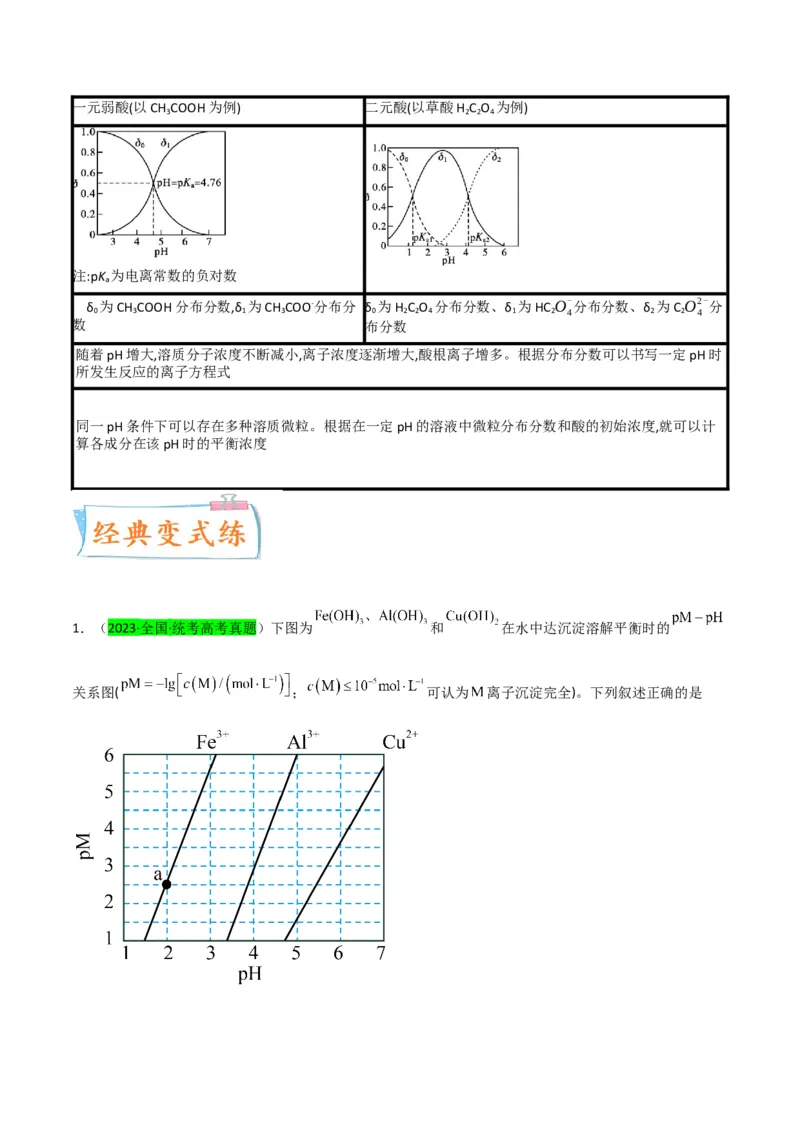
(3)AB直线的左上方均为碱性溶液,任意一点均
(3)d点在曲线的下方,QCaCO >MnCO ;
4 3 3
③X点对于CaSO 来说要析出沉淀,对于CaCO 来说是不饱和溶液,能继续溶解CaCO ;
4 3 3
④Y点:c(S )>c(Ca2+),二者浓度的乘积等于10-5;Z点:c(C )c>b>a
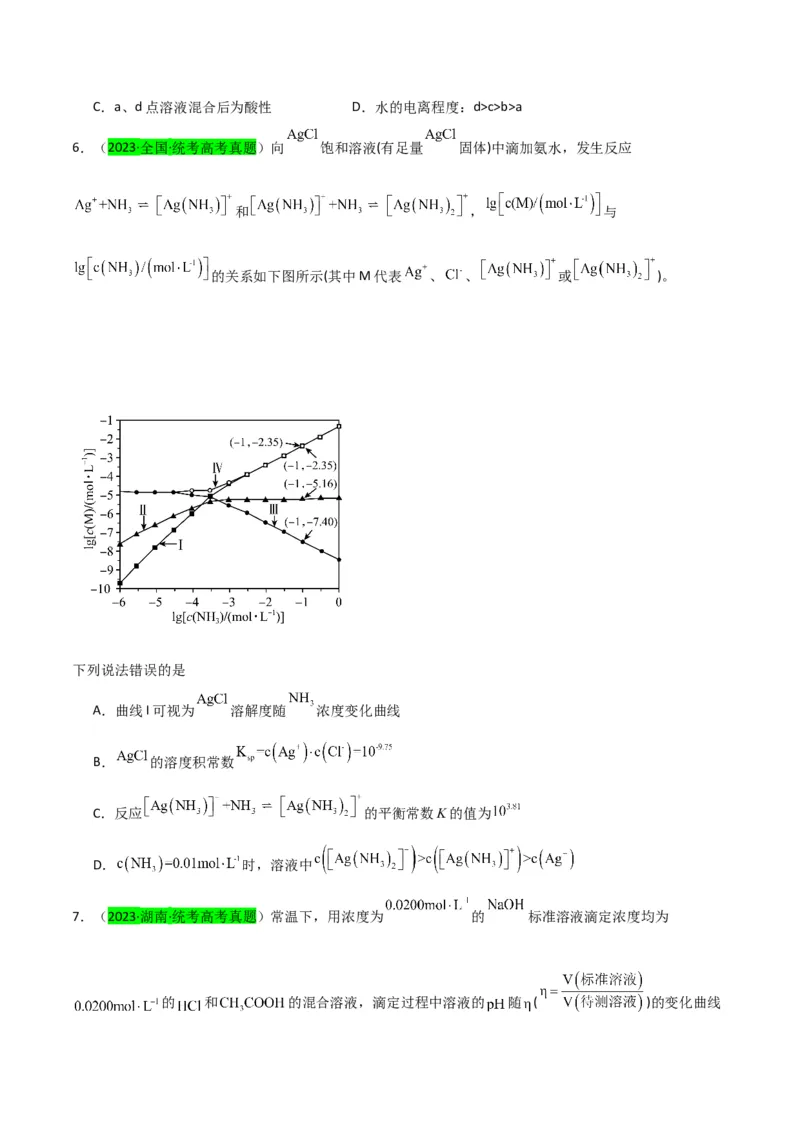
6.(2023·全国·统考高考真题)向 饱和溶液(有足量 固体)中滴加氨水,发生反应
和 , 与
的关系如下图所示(其中M代表 、 、 或 )。
下列说法错误的是
A.曲线I可视为 溶解度随 浓度变化曲线
B. 的溶度积常数
C.反应 的平衡常数K的值为
D. 时,溶液中
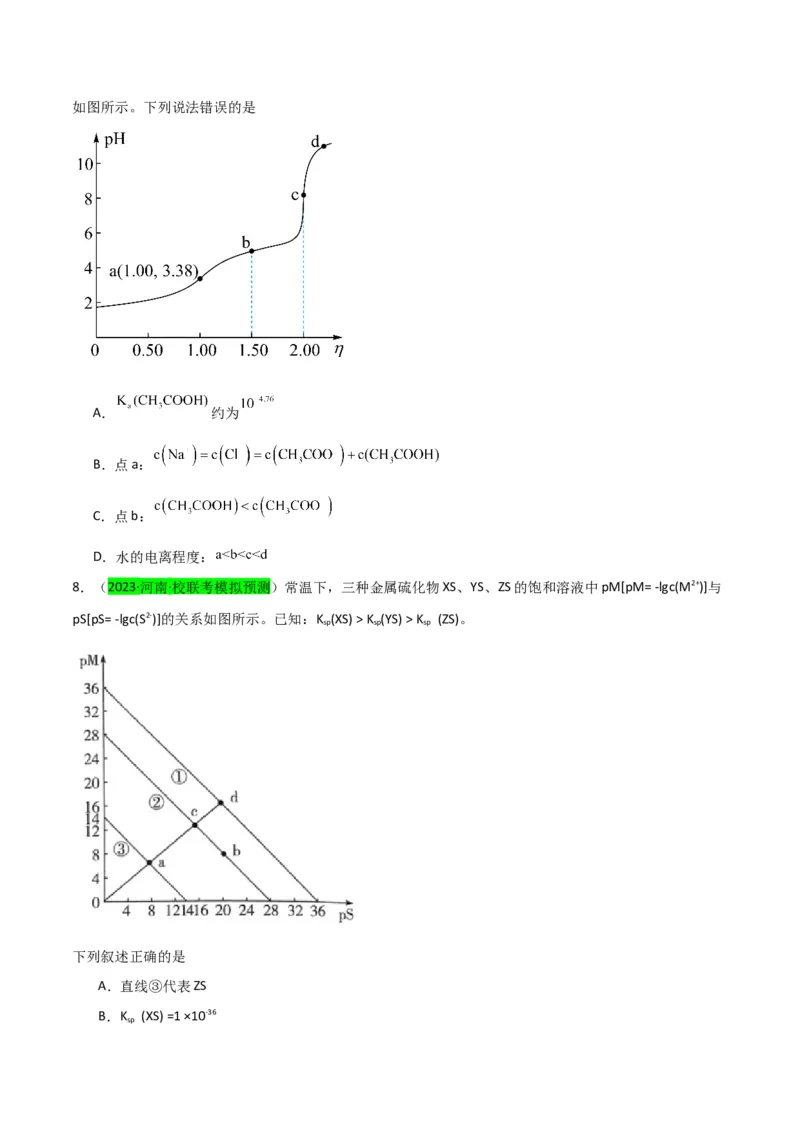
7.(2023·湖南·统考高考真题)常温下,用浓度为 的 标准溶液滴定浓度均为
的 和 的混合溶液,滴定过程中溶液的 随 ( )的变化曲线如图所示。下列说法错误的是
A. 约为
B.点a:
C.点b:
D.水的电离程度:
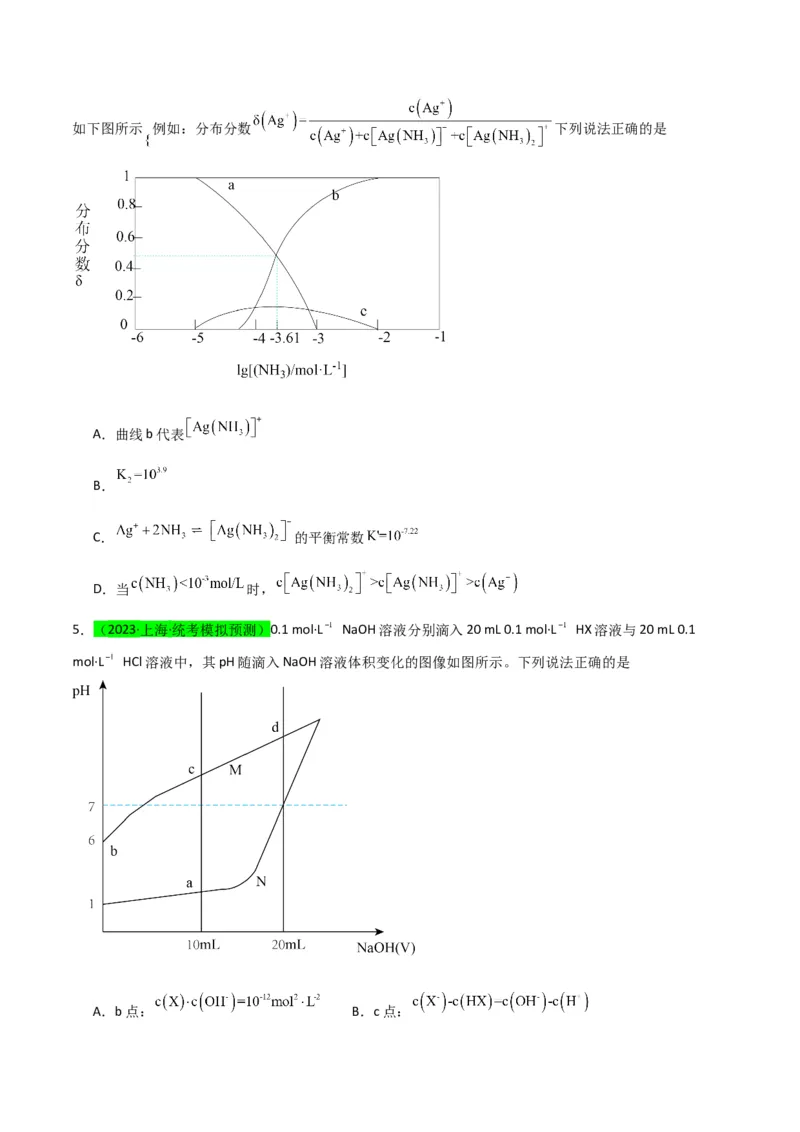
8.(2023·河南·校联考模拟预测)常温下,三种金属硫化物XS、YS、ZS的饱和溶液中pM[pM= -lgc(M2+)]与
pS[pS= -lgc(S2-)]的关系如图所示。已知:K (XS) > K (YS) > K (ZS)。
sp sp sp
下列叙述正确的是
A.直线③代表ZS
B.K (XS) =1 ×10-36
spC.向c点饱和溶液中加少量Na S,c点向b点迁移
2
D.YS(s) +Z2+(aq) ZS(s) +Y2+ (aq) K=1 ×108
1.(2023·山东·统考高考真题)在含HgI (g)的溶液中,一定c(I-)范围内,存在平衡关系:
2
; ; ; ;
,平衡常数依次为 。已知 、 , 、
随 的变化关系如图所示,下列说法错误的是
A.线 表示 的变化情况
B.随 增大, 先增大后减小
C.
D.溶液中I元素与 元素的物质的量之比始终为
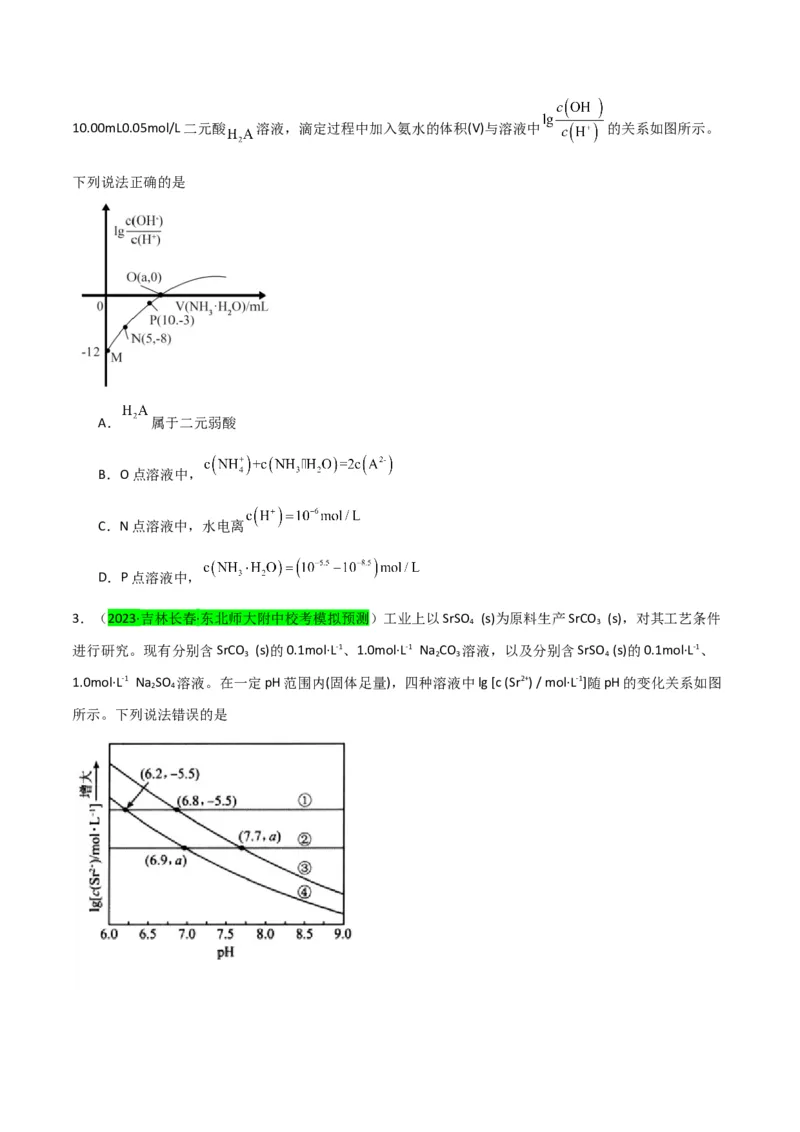
2.(2023·福建泉州·福建省泉州第一中学校考模拟预测)25℃时,用0.10mol/L的氨水滴定10.00mL0.05mol/L二元酸 溶液,滴定过程中加入氨水的体积(V)与溶液中 的关系如图所示。
下列说法正确的是
A. 属于二元弱酸
B.O点溶液中,
C.N点溶液中,水电离
D.P点溶液中,
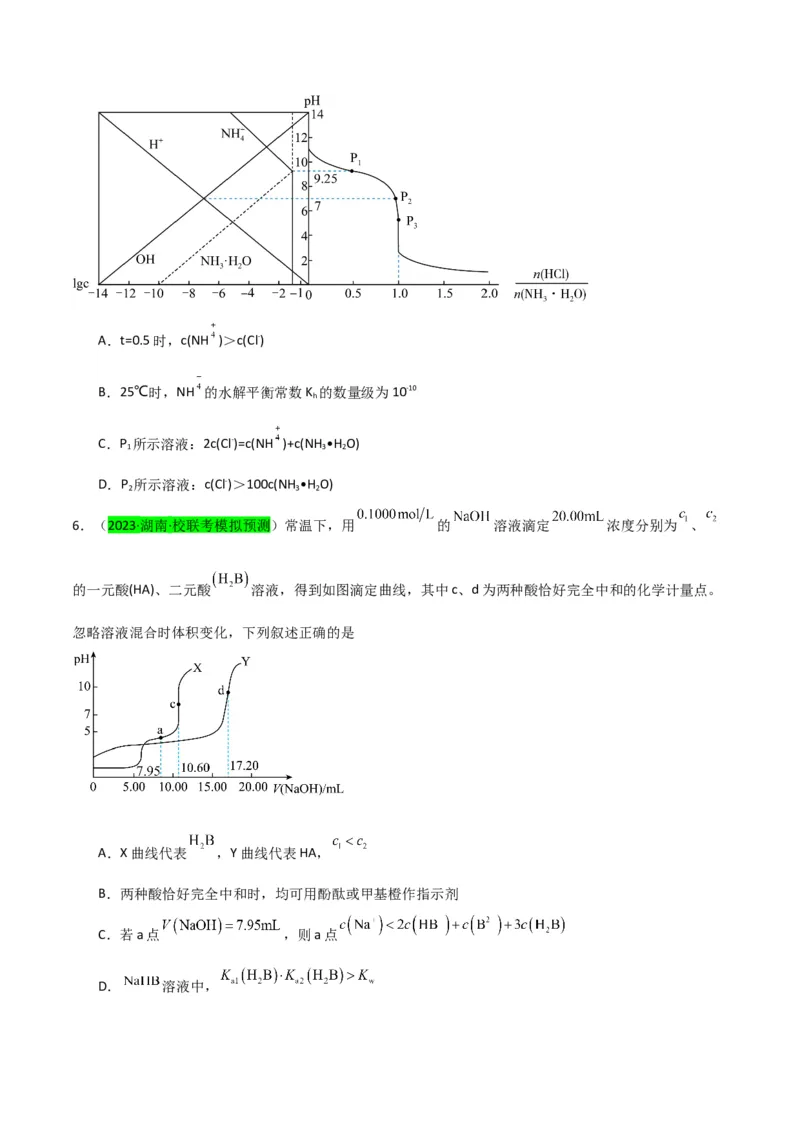
3.(2023·吉林长春·东北师大附中校考模拟预测)工业上以SrSO (s)为原料生产SrCO (s),对其工艺条件
4 3
进行研究。现有分别含SrCO (s)的0.1mol·L-1、1.0mol·L-1 Na CO 溶液,以及分别含SrSO (s)的0.1mol·L-1、
3 2 3 4
1.0mol·L-1 Na SO 溶液。在一定pH范围内(固体足量),四种溶液中lg [c (Sr2+) / mol·L-1]随pH的变化关系如图
2 4
所示。下列说法错误的是A.反应SrSO (s) + (aq) SrCO (s) + (aq) 的平衡常数K=
4 3
B.a=−6.5
C.曲线④代表含SrCO (s)的1.0mol/L Na CO 溶液的变化曲线
3 2 3
D.将pH=6.8状态下的①、③两物料等体积混合后,溶液中lgc(Sr2+)小于−5.5
4.(2023·山西·校联考模拟预测)25℃时,用同一较高浓度的NaOH溶液分别滴定酸HA和CuSO 溶液,
4
pM[p 表示负对数, M表示 、c(Cu2+)]与溶液pH的变化关系如图。已知; CuA 易溶于水,一般认
2
为反应的平衡常数为K> 105时反应进行完全。下列说法错误的是
A.HA为一元弱酸,25℃时 K=10-7.4
a
B.①表示滴定CuSO 溶液时pM与溶液pH的关系
4
C.滴定HA溶液至x点时,溶液中c(HA)> c(A-)> c(Na+)
D.滴定CuSO 溶液至x点时,若改为滴加HA溶液,沉淀会逐渐完全溶解
4
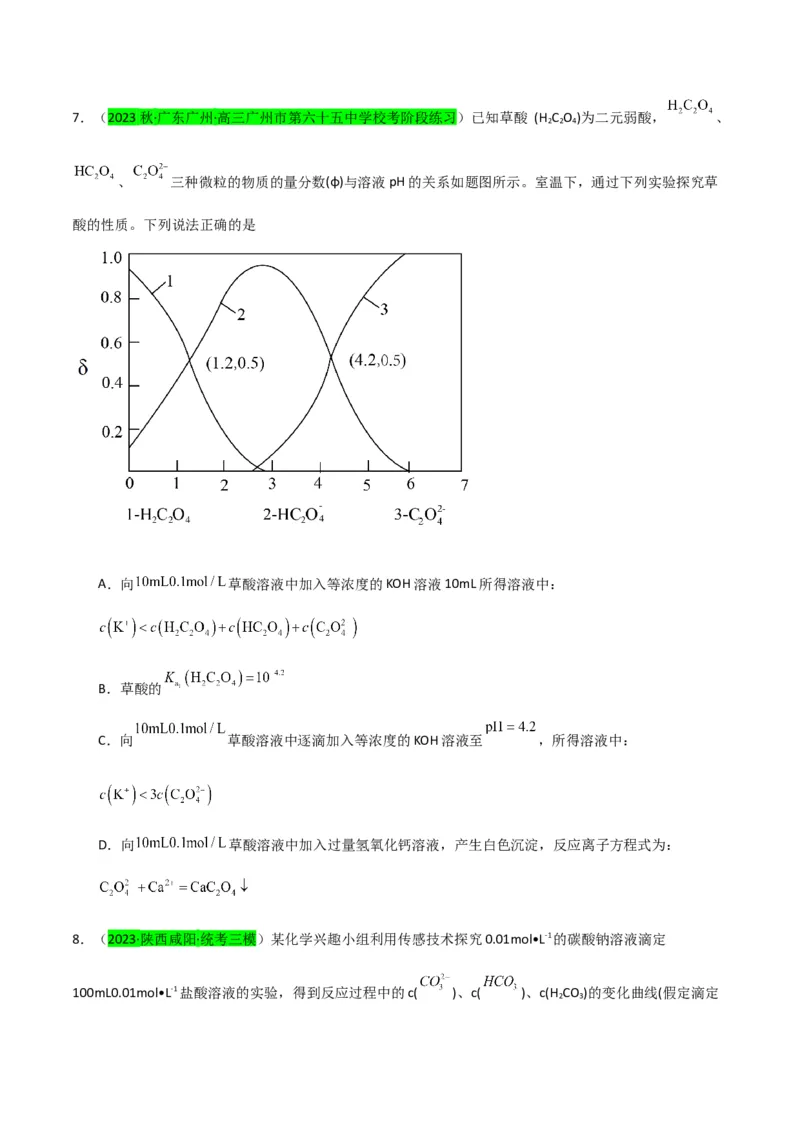
5.(2023·陕西西安·统考一模)25℃时,将HCl气体缓慢通入0.1mol•L-1的氨水中,溶液的pH、体系中粒
子浓度的对数值(lgc)与反应物的物质的量之比[t= ]的关系如图所示。若忽略溶液体积变化,下
列有关说法错误的是A.t=0.5时,c(NH )>c(Cl-)
B.25℃时,NH 的水解平衡常数K 的数量级为10-10
h
C.P 所示溶液:2c(Cl-)=c(NH )+c(NH •H O)
1 3 2
D.P 所示溶液:c(Cl-)>100c(NH •H O)
2 3 2
6.(2023·湖南·校联考模拟预测)常温下,用 的 溶液滴定 浓度分别为 、
的一元酸(HA)、二元酸 溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点。
忽略溶液混合时体积变化,下列叙述正确的是
A.X曲线代表 ,Y曲线代表HA,
B.两种酸恰好完全中和时,均可用酚酞或甲基橙作指示剂
C.若a点 ,则a点
D. 溶液中,7.(2023秋·广东广州·高三广州市第六十五中学校考阶段练习)已知草酸 (H C O )为二元弱酸, 、
2 2 4
、 三种微粒的物质的量分数(φ)与溶液pH的关系如题图所示。室温下,通过下列实验探究草
酸的性质。下列说法正确的是
A.向 草酸溶液中加入等浓度的KOH溶液10mL所得溶液中:
B.草酸的
C.向 草酸溶液中逐滴加入等浓度的KOH溶液至 ,所得溶液中:
D.向 草酸溶液中加入过量氢氧化钙溶液,产生白色沉淀,反应离子方程式为:
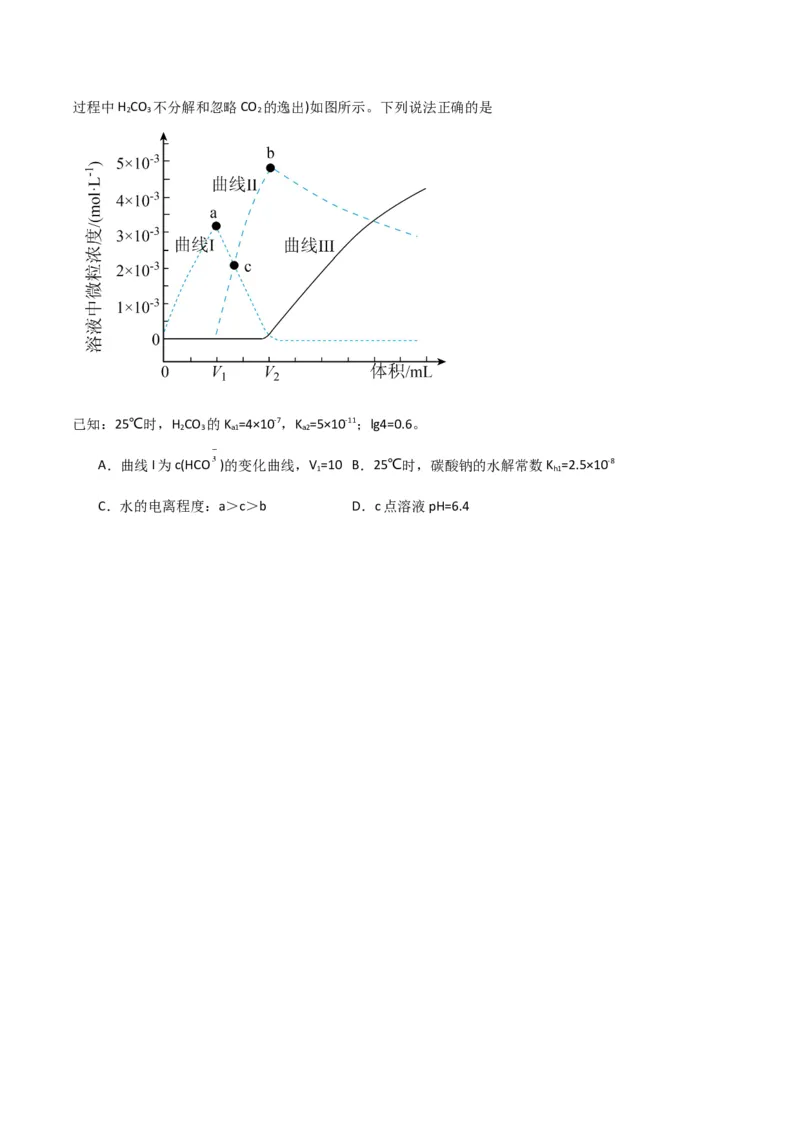
8.(2023·陕西咸阳·统考三模)某化学兴趣小组利用传感技术探究0.01mol•L-1的碳酸钠溶液滴定
100mL0.01mol•L-1盐酸溶液的实验,得到反应过程中的c( )、c( )、c(H CO )的变化曲线(假定滴定
2 3过程中H CO 不分解和忽略CO 的逸出)如图所示。下列说法正确的是
2 3 2
已知:25℃时,H CO 的K =4×10-7,K =5×10-11;lg4=0.6。
2 3 a1 a2
A.曲线I为c(HCO )的变化曲线,V =10 B.25℃时,碳酸钠的水解常数K =2.5×10-8
1 h1
C.水的电离程度:a>c>b D.c点溶液pH=6.4