文档内容
微专题41 水溶液中的三大守恒和浓度大小比较
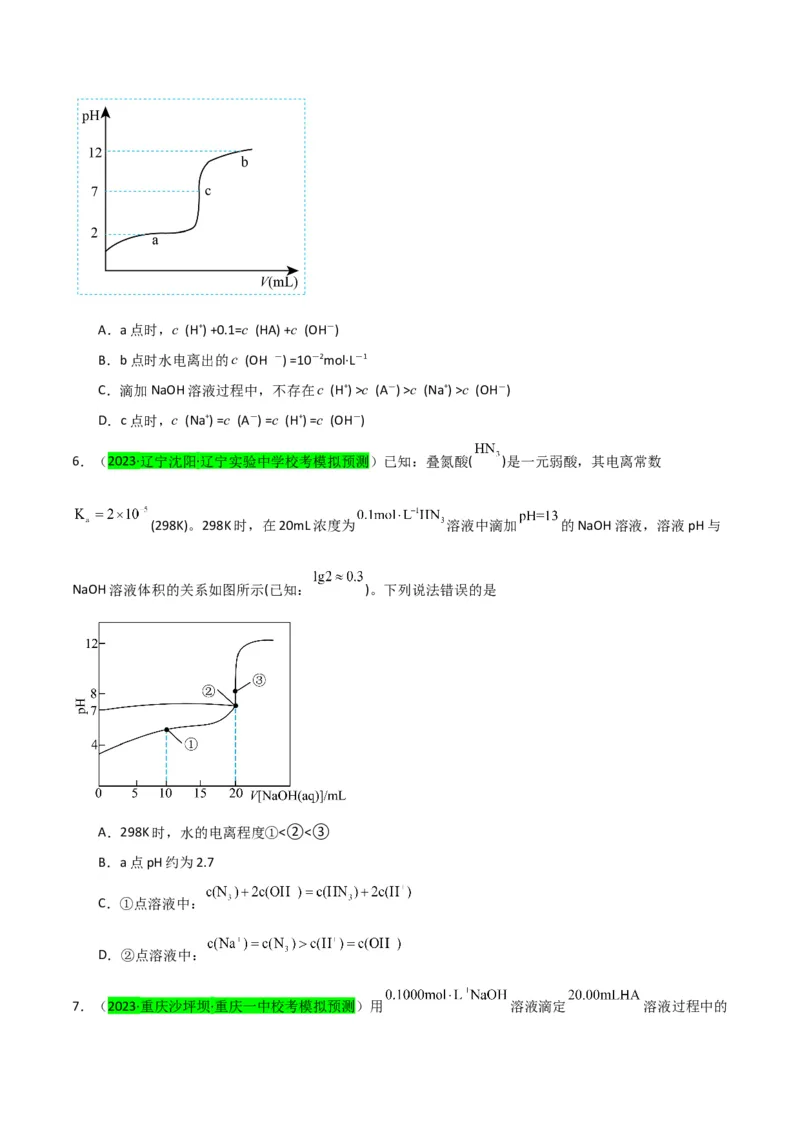
1.(2023·湖南·统考高考真题)常温下,用浓度为 的 标准溶液滴定浓度均为
的 和 的混合溶液,滴定过程中溶液的 随 ( )的变化曲线
如图所示。下列说法错误的是A. 约为
B.点a:
C.点b:
D.水的电离程度:
2.(2023·浙江·统考高考真题)草酸( )是二元弱酸。某小组做如下两组实验:
实验I:往 溶液中滴加 溶液。
实验Ⅱ:往 溶液中滴加 溶液。
[已知: 的电离常数 ,溶液混合后体积变化忽略不
计],下列说法正确的是
A.实验I可选用甲基橙作指示剂,指示反应终点
B.实验I中 时,存在
C.实验Ⅱ中发生反应
D.实验Ⅱ中 时,溶液中
掌握微粒浓度大小比较的常见类型及分析方法一、微粒浓度的大小比较理论依据
(1)电离理论——弱电解质的电离是微弱的
①弱电解质的电离是微弱的,电离产生的微粒都非常少,同时还要考虑水的电离。
如氨水中:NH ·H O、NH、OH-浓度的大小关系是c(NH ·H O)>c(OH-)>c(NH)。
3 2 3 2
②多元弱酸的电离是分步进行的,其主要是第一步电离(第一步电离程度远大于第二步电离)。
如在HS溶液中:HS、HS-、S2-、H+的浓度大小关系是 c (H S) > c (H + ) > c (HS - ) > c (S 2 - ) 。
2 2 2
(2)水解理论——弱电解质离子的水解过程一般是微弱的
①弱电解质离子的水解是微弱的(水解相互促进的除外),但由于水的电离,故水解后酸性溶液中c(H+)或碱
性溶液中c(OH-)总是大于水解产生的弱电解质的浓度。
如NH Cl溶液中:NH、Cl-、NH ·H O、H+的浓度大小关系是c(Cl-)>c(NH)>c(H+)>c(NH ·H O)。
4 3 2 3 2
②多元弱酸酸根离子的水解是分步进行的,其主要是第一步水解。如在 NaCO 溶液中:CO、HCO、
2 3
HCO 的浓度大小关系应是c(CO)>c(HCO)>c(H CO)。
2 3 2 3
二、溶液中微粒种类的判断
我们在判断溶液中微粒浓度大小时,首先要判断溶液中微粒的种类,然后再进行比较。判断溶液中微粒种
类的方法是正确写出溶液中所有的电离方程式、水解方程式,然后结合溶液中的溶质即可判断溶液中的微
粒种类。
注意:在书写电离方程式时,不要丢掉水的电离方程式。
如:NaHCO 溶液中存在三种电离:NaHCO ===Na++HCO、HCO H++CO、HO H++OH-;
3 3 2
一种水解:HCO+HO HCO +OH-所以溶液中的离子为Na+、CO、HCO、OH-、H+,分子为
2 2 3
HCO、HO。
2 3 2三、离子浓度大小比较的方法
(1)考虑水解因素:如NaCO 溶液。
2 3
CO+HO HCO+OH-
2
HCO+HO HCO+OH-
2 2 3
所以c(Na+)>c(CO)>c(OH-)>c(HCO)。
(2)不同溶液中同一离子浓度的比较要看溶液中其他离子对它的影响。如相同浓度的 a.NH Cl、
4
b.CH COONH、c.NH HSO 三种溶液中c(NH)由大到小的顺序是c>a>b。
3 4 4 4
(3)混合液中各离子浓度的比较要综合分析水解因素、电离因素,如相同浓度的NH Cl和氨水混合液中,因
4
NH ·H O的电离>NH的水解,故离子浓度顺序为c(NH)>c(Cl-)>c(OH-)>c(H+)。
3 2
四、三个守恒
1.电荷守恒规律
电解质溶液中,无论存在多少种离子,溶液均呈电中性,即阴离子所带负电荷总数一定等于阳离子所带正
电荷总数。如NaHCO 溶液中的离子有Na+、H+、HCO、CO、OH-,其存在如下关系:c(Na+)+c(H+)=
3
c(HCO)+c(OH-)+2c(CO)。
2.物料守恒规律
电解质溶液中,由于某些离子能够水解,离子种类增多,但元素总是守恒的。如 K S溶液中S2-、HS-都能
2
水解,故S元素以S2-、HS-、H S三种形式存在,它们之间有如下守恒关系:c(K+)=2c(S2-)+2c(HS-)+
2
2c(H S)。
2
3.质子守恒规律
电解质溶液中,电离、水解等过程中得到的质子(H+)数等于失去的质子(H+)数。如NaHCO 溶液中:
3
即c(H CO )+c(H+)===c(CO)+c(OH-)。
2 3
如Na S水溶液中的质子转移情况如图所示:
2
由图可得Na S水溶液中质子守恒式:c(OH-)=c(H+)+2c(H S)+c(HS-)。
2 2
质子守恒式也可以由电荷守恒式与物料守恒式推导得到。NaS水溶液中电荷守恒式为
2
c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)①,物料守恒式为c(Na+)=2[c(HS-)+c(S2-)+c(H S)]②,
2
由①式-②式,消去没有参与变化的Na+,即可得到质子守恒式:
c(OH-)=c(H+)+2c(H S)+c(HS-)。
2
五、常见几种物质的微粒浓度比较(溶液中水分子除外)。
项目 0.1 mol·L-1CH COOH溶液 0.1 mol·L-1CH COONa溶液
3 3
粒子
CH COO-、CH COOH 、OH-、H+ Na+、CH COO-、CH COOH 、、OH-、H+
种类 3 3 3 3
离子浓
c(CH COOH)>c(CH COO-)>c(H+)>c(OH-) c(Na+)>c(CH COO-)>c(OH-)>c(CH COOH)>c(H+)
度比较 3 3 3 3
电荷
c(H+)=c(CH COO-)+c(OH-) c(Na+)+c(H+)=c(CH COO-)+c(OH-)
守恒 3 3
物料
c(CH COO-)+c(CH COOH)=0.1 mol·L-1 c(CH COO-)+c(CH COOH)=c(Na+)=0.1 mol·L-1
守恒 3 3 3 3
0.1 mol·L-1的 0.1 mol·L-1的
项目
NaHCO 溶液 Na CO 溶液
3 2 3
粒子
Na+、CO、HCO、H CO 、OH-、H+ Na+、CO、HCO、H CO 、OH-、H+
2 3 2 3
种类
离子浓
c(Na+)>c(HCO)>c(OH-)>c(H+)>c(CO) c(Na+)>c(CO)>c(OH-)>c(HCO)>c(H+)
度比较
电荷
c(Na+)+c(H+)=c(HCO)+2c(CO)+c(OH-) c(Na+)=2[c(CO)+c(HCO)+c(H CO )]
2 3
守恒
物料
c(Na+)=c(HCO)+c(CO)+c(H CO ) c(Na+)+c(H+)=c(HCO)+c(OH-)+2c(CO)
2 3
守恒
质子
c(OH-)=c(H CO )+c(H+)-c(CO) c(OH-)=c(H+)+2c(H CO )+c(HCO)
2 3 2 3
守恒
易错提醒:选好参照物
不同溶液中同一离子浓度的大小比较要选好参照物,分组比较各个击破。如25 ℃时,相同物质的量浓度的
下列溶液中:①NH Cl、②CH COONH 、③NH HSO 、④(NH ) SO 、⑤(NH ) Fe(SO ) ,c(NH)由大到小的顺序
4 3 4 4 4 4 2 4 4 2 4 2
为⑤>④>③>①>②。分析流程为:
分组――→④⑤中c(NH)要大于①②③1.(2022·全国·统考高考真题)常温下,一元酸 的 。在某体系中, 与 离子不能
穿过隔膜,未电离的 可自由穿过该膜(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是
A.溶液Ⅰ中
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的 不相等
D.溶液Ⅰ和Ⅱ中的 之比为
2.(2022·浙江·统考高考真题) 时,向 浓度均为 的盐酸和醋酸的混合溶液中逐滴加入
的 溶液(醋酸的 ;用 的 溶液滴定 等浓度的盐酸,滴定
终点的 突跃范围4.3~9.7)。下列说法不正确的是
A.恰好中和时,溶液呈碱性
B.滴加 溶液至 的过程中,发生反应的离子方程式为:
C.滴定过程中,D. 时,
1.(2023秋·天津红桥·高三统考期末)下列判断不正确的是
A.在 的 溶液中
B. 溶液和 溶液中所含微粒种类相同
C.氨水和 溶液混合,形成 的溶液中
D. 的 溶液中
2.(2023·浙江温州·乐清市知临中学校考一模)在常温下,下列说法正确的是
A. 溶液中商加稀盐酸至溶液呈中性时:
B. 的氨水与 的盐酸等体积互混, ,则 的电离常数为
C.等浓度的 与 溶液,前者 大于后者(已知, 的 , 的
, )
D.浓度均为 的 和 混合溶液,滴加 的 溶液,最先产
生的沉淀为 ( , )
3.(2023·河南·校联考模拟预测)用强碱滴定某一元弱酸时,弱酸被强碱部分中和后得到“弱pH酸盐和弱酸”组成的缓冲溶液,其中存在pH=pK 一lg 。25°C时0.1mol·L-1的NaOH溶液滴定16.00mL某未知
a
浓度的HA溶液,滴定过程中消耗NaOH溶液的体积与混合溶液pH之间的关系如图所示(已知:pK=-lgK,
a a
100.48=3,酸性HA>HCN)。下列说法错误的是
A.25℃时,HA电离常数的数量级为10-5
B.b点溶液中存在c(HA)+c(H+)>c(A-)+c(OH-)
C.c点溶液中离子浓度的大小关系为c(HA)>c(A-)>c(H+)>c(OH-)
D.若将HA改为等体积、等浓度的HCN,则pH随NaOH溶液体积的变化曲线竖直上移
4.(2023·河南·校联考模拟预测)食用级NaHSO 产品用作防腐剂、抗氧化剂等。根据常温时下列实验得
3
到的粒子浓度关系正确的是
实
实验操作和现象 粒子浓度的关系
验
向蓝色石蕊试纸上滴入2滴0.1 mol ·L-1NaHSO 溶液,试纸
① 3 c(Na+) >c( ) >c( ) >c(H SO )
变红 2 3
向10 mL0.1 mol ·L-1NaHSO 溶液中加入等体积等浓度的 c(Na+)-c( ) -c( ) -c(H SO ) =0.05
② 3 2 3
NaOH溶液 mol ·L-1
向0.1 mol ·L-1NaHSO 溶液中加入等浓度的NaOH溶液至
③ 3 c( ) +c( )=c(Na+)
pH=7
A.①③ B.②③ C.①② D.①②③
5.(2023·江西上饶·校联考二模)25°C时,向20mL 0.10mol·L-1的一元酸HA (K =1.0×10-2) 中逐滴加入
a
0.10mol·L-1NaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如图所示,下列说法正确的是A.a点时,c (H+) +0.1=c (HA) +c (OH-)
B.b点时水电离出的c (OH -) =10-2mol·L-1
C.滴加NaOH溶液过程中,不存在c (H+) >c (A-) >c (Na+) >c (OH-)
D.c点时,c (Na+) =c (A-) =c (H+) =c (OH-)
6.(2023·辽宁沈阳·辽宁实验中学校考模拟预测)已知:叠氮酸( )是一元弱酸,其电离常数
(298K)。298K时,在20mL浓度为 溶液中滴加 的NaOH溶液,溶液pH与
NaOH溶液体积的关系如图所示(已知: )。下列说法错误的是
A.298K时,水的电离程度①<②<③
B.a点pH约为2.7
C.①点溶液中:
D.②点溶液中:
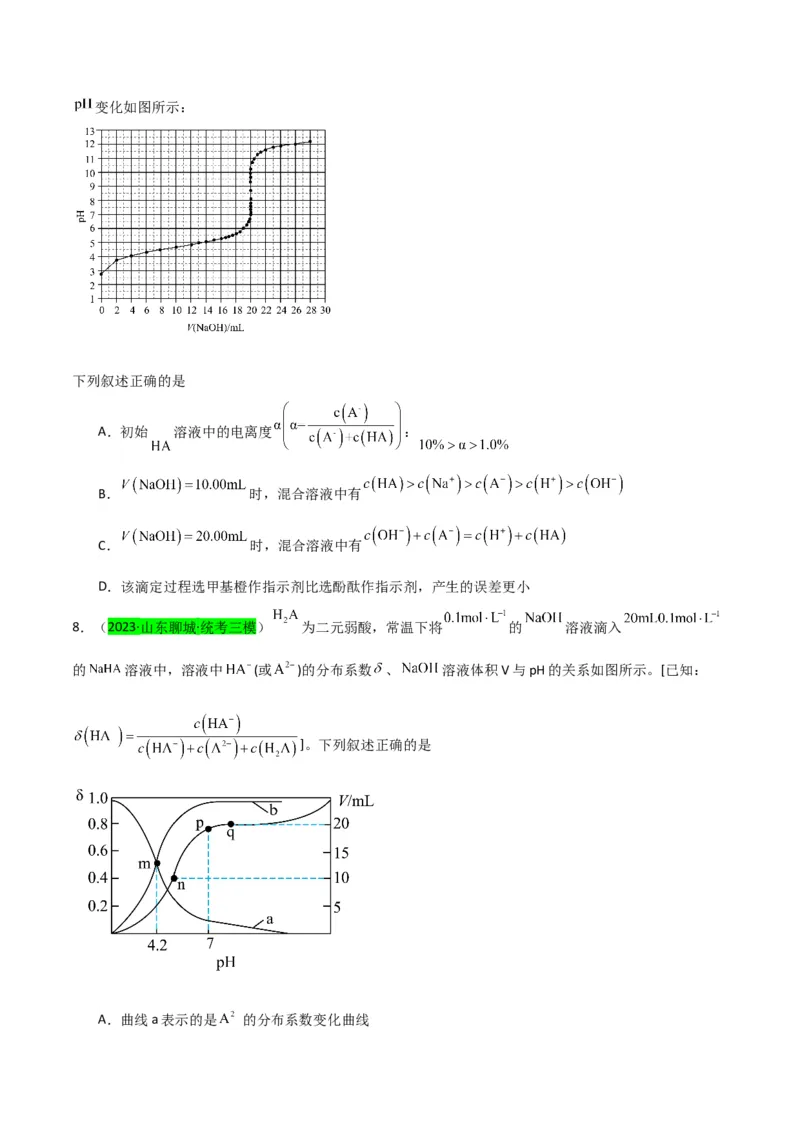
7.(2023·重庆沙坪坝·重庆一中校考模拟预测)用 溶液滴定 溶液过程中的变化如图所示:
下列叙述正确的是
A.初始 溶液中的电离度 :
B. 时,混合溶液中有
C. 时,混合溶液中有
D.该滴定过程选甲基橙作指示剂比选酚酞作指示剂,产生的误差更小
8.(2023·山东聊城·统考三模) 为二元弱酸,常温下将 的 溶液滴入
的 溶液中,溶液中 (或 )的分布系数 、 溶液体积V与pH的关系如图所示。[已知:
]。下列叙述正确的是
A.曲线a表示的是 的分布系数变化曲线B.滴定时,可用甲基橙做指示剂
C. 的第二步电离平衡常数的数量级为
D.n点对应的溶液中,
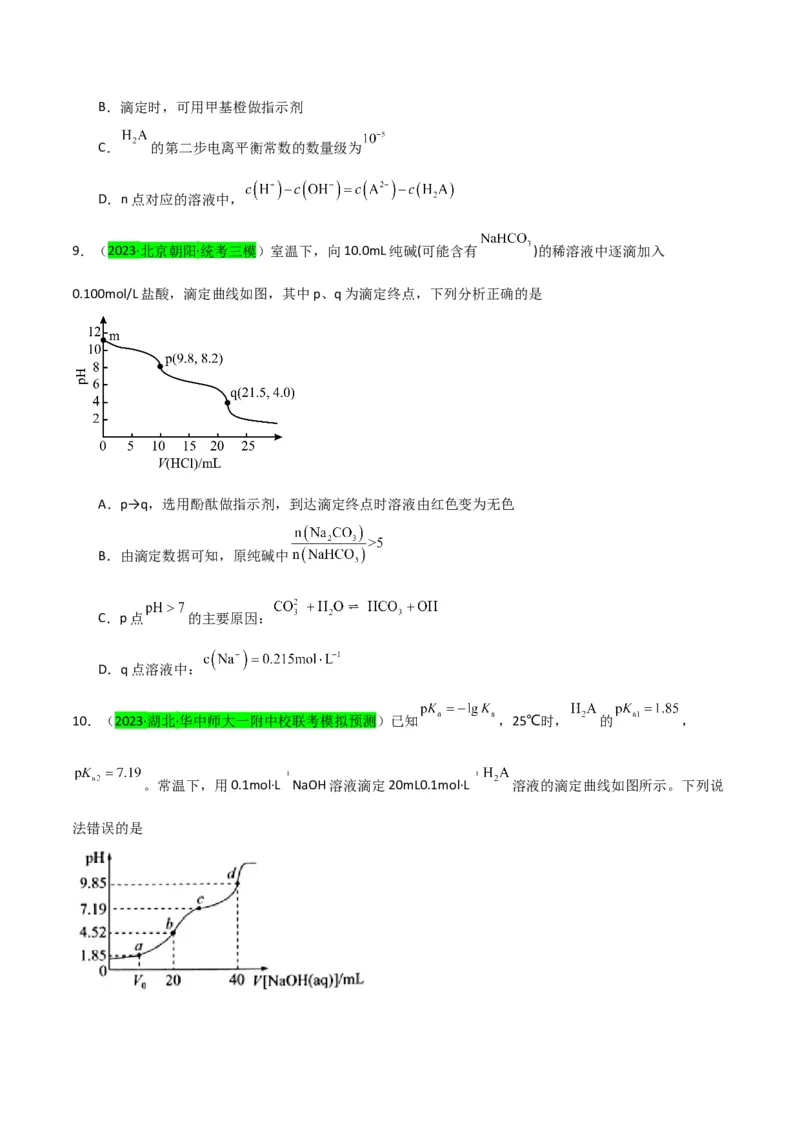
9.(2023·北京朝阳·统考三模)室温下,向10.0mL纯碱(可能含有 )的稀溶液中逐滴加入
0.100mol/L盐酸,滴定曲线如图,其中p、q为滴定终点,下列分析正确的是
A.p→q,选用酚酞做指示剂,到达滴定终点时溶液由红色变为无色
B.由滴定数据可知,原纯碱中
C.p点 的主要原因:
D.q点溶液中:
10.(2023·湖北·华中师大一附中校联考模拟预测)已知 ,25℃时, 的 ,
。常温下,用0.1mol·L NaOH溶液滴定20mL0.1mol·L 溶液的滴定曲线如图所示。下列说
法错误的是A.a点加入NaOH溶液的体积 mL
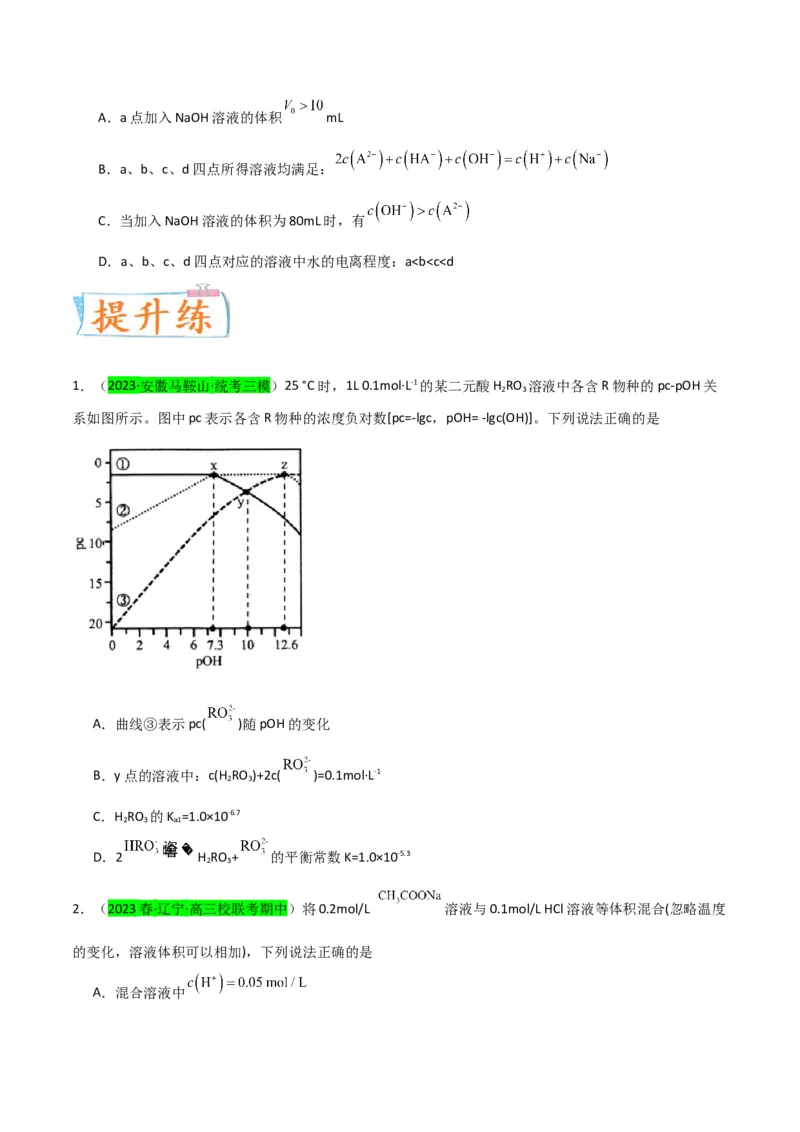
B.a、b、c、d四点所得溶液均满足:
C.当加入NaOH溶液的体积为80mL时,有
D.a、b、c、d四点对应的溶液中水的电离程度:ac(Na+)>c(H+)>c(OH-)
2 2
D.向0.1 mol/L的HCN溶液中通入HCl气体至pH=4,则HCN的电离度为0.049%
4.(2023·上海·统考模拟预测)0.1 mol·L NaOH溶液分别滴入20 mL 0.1 mol·L HX溶液与20 mL 0.1
mol·L HCl溶液中,其pH随滴入NaOH溶液体积变化的图像如图所示。下列说法正确的是
A.b点: B.c点:
C.a、d点溶液混合后为酸性 D.水的电离程度:d>c>b>a5.(2022·广东·统考模拟预测)测定 溶液升温过程中的pH(不考虑水的蒸发、溶液体积
的变化),数据如下。
温度/℃ 25 40 60 80
pH 11.90 11.68 11.54 11.42
下列说法错误的是
A.25℃时, 的一级水解常数 的数量级为
B.温度升高后 溶液碱性减弱
C.溶液中
D.温度升高pH变小是K 增大与水解平衡移动共同作用的结果
w
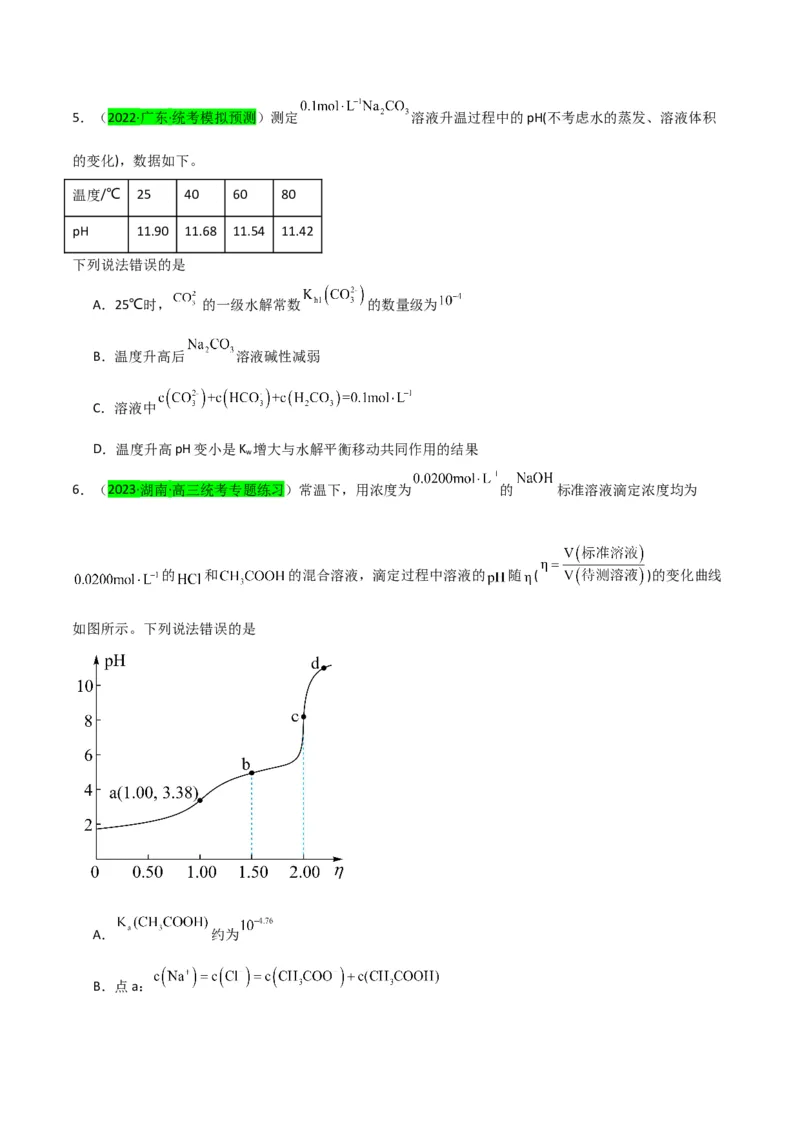
6.(2023·湖南·高三统考专题练习)常温下,用浓度为 的 标准溶液滴定浓度均为
的 和 的混合溶液,滴定过程中溶液的 随 ( )的变化曲线
如图所示。下列说法错误的是
A. 约为
B.点a:C.点b:
D.水的电离程度:
7.(2023·浙江·高三统考专题练习)常温下,通过下列实验探究H S、Na S溶液的性质。
2 2
实验1:向 溶液中通入一定体积NH ,测得溶液pH为7
3
实验2:向 溶液中滴加等体积同浓度的NaOH溶液,充分反应后再滴入2滴酚酞,溶液呈红
色
实验3:向 溶液中滴入 溶液,产生白色溶沉淀;再滴入几滴
溶液,立即出现黑色沉淀
实验4:向 溶液中逐滴滴加等体积同浓度的盐酸,无明显现象
下列说法正确的是
A.实验1得到的溶液中存在
B.由实验2可得出:
C.由实验3可得出:
D.实验4得到的溶液中存在
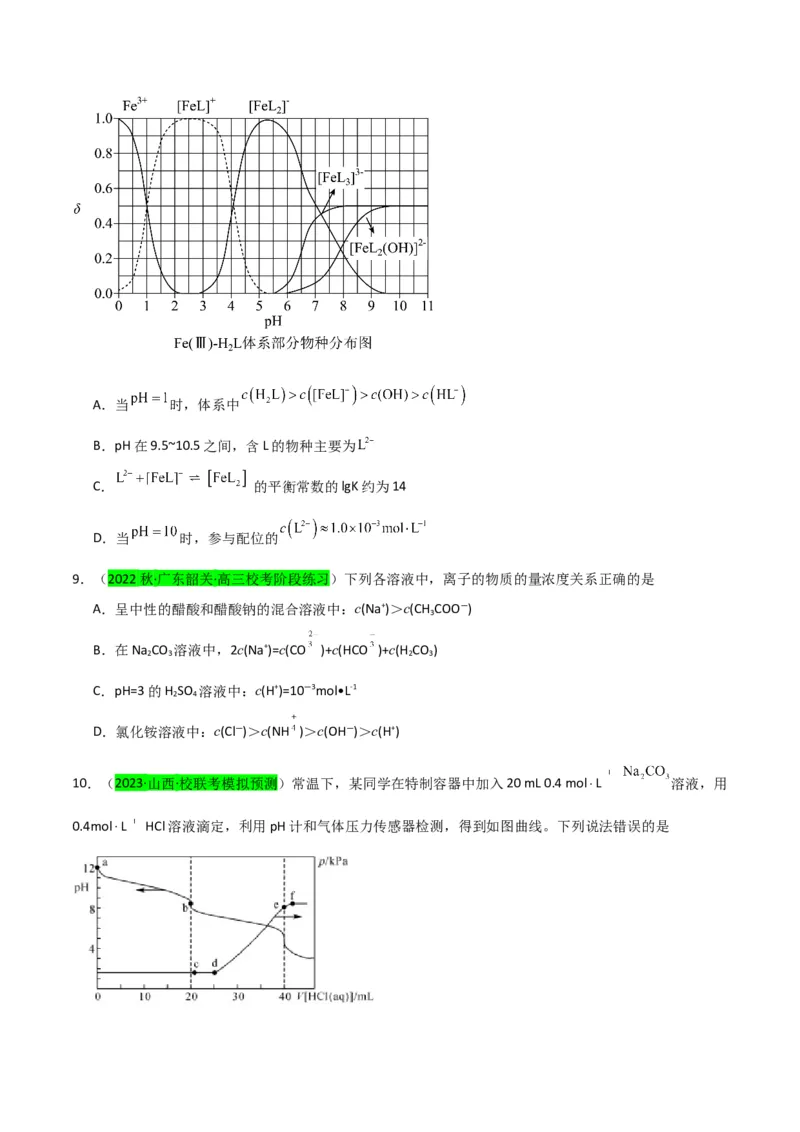
8.(2023·全国·高三统考专题练习) 为某邻苯二酚类配体,其 , 。常温下构建
溶液体系,其中 , 。体系中含Fe物种的
组分分布系数δ与pH的关系如图所示,分布系数 ,已知 , 。
下列说法正确的是A.当 时,体系中
B.pH在9.5~10.5之间,含L的物种主要为
C. 的平衡常数的lgK约为14
D.当 时,参与配位的
9.(2022秋·广东韶关·高三校考阶段练习)下列各溶液中,离子的物质的量浓度关系正确的是
A.呈中性的醋酸和醋酸钠的混合溶液中:c(Na+)>c(CH COO—)
3
B.在Na CO 溶液中,2c(Na+)=c(CO )+c(HCO )+c(H CO )
2 3 2 3
C.pH=3的H SO 溶液中:c(H+)=10—3mol•L-1
2 4
D.氯化铵溶液中:c(Cl—)>c(NH )>c(OH—)>c(H+)
10.(2023·山西·校联考模拟预测)常温下,某同学在特制容器中加入20 mL 0.4 mol⋅L 溶液,用
0.4mol⋅L HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是A.整个滴定过程中应先用酚酞溶液、后用甲基橙溶液作指示剂
B.a→f点对应的溶液中,水的电离程度一直在减小
C.
D.f点对应的溶液中存在: