文档内容
大题优练 1 无机制备类实验设计
优 选 例 题
例1:2020年初,突如其来的新型冠状肺炎在全世界肆虐,依据研究,含氯消毒剂可以有效灭活新冠病毒,
为阻断疫情做出了巨大贡献。二氧化氯(ClO )就是其中一种高效消毒灭菌剂。氯酸钠还原法是目前使用较
2
为广泛的ClO 制备方法,其中一种是用NaClO 与 在催化剂、 时,发生反应得到ClO ,下
2 3 2
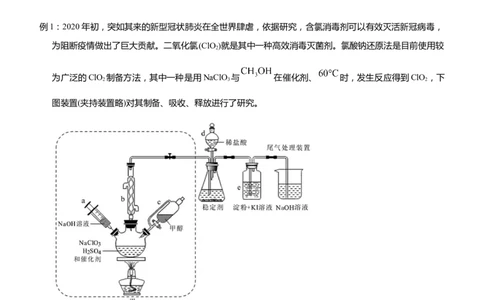
图装置(夹持装置略)对其制备、吸收、释放进行了研究。
已知:①ClO 的浓度较大时易分解爆炸,一般用CO 或空气稀释到 以下,实验室也常用稳定剂吸收
2 2
ClO ,生成NaClO,使用时加酸只释放出ClO 一种气体;
2 2 2
②ClO 与 反应的离子方程式为: ;
2
③有关物质沸点如下表:物质 ClO
2
沸点
请回答:
(1)仪器d的名称是_______,仪器b的作用是_______。
(2)反应中甲醇被氧化为甲酸,写出制备ClO 的化学方程式_______。
2
(3)在ClO 释放实验中,发生的离子反应方程式是_______。
2
(4)根据反应条件判断制备装置甲中需改进的一项措施是_______。
(5)NaOH吸收ClO 尾气,生成物质的量为1∶1的两种阴离子,一种为ClO,则另一种为_______。
2
(6)自来水厂用碘量法检测水中ClO 的浓度,其实验操作如下:取 的水样,加入足量的碘化钾,
2
再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用 标准溶液滴定碘单质
,达到滴定终点时用去 标准溶液,测得该水样中ClO 的含量
2
为_______ (保留一位小数)。
【答案】(1)分液漏斗 导出ClO 气体,冷凝回流
2
(2) =====
(3)
(4)水浴加热
(5)
(6)135.0
【解析】装置甲中甲醇、NaClO 、硫酸反应生成ClO ,加入氢氧化钠后硫酸被中和反应即停止,稳定剂
3 2用于吸收ClO ,加入盐酸释放ClO ,淀粉碘化钾溶液用于检验ClO ,氢氧化钠溶液用于尾气吸收。(1)仪器d
2 2 2
的名称是分液漏斗;b是球形冷凝管,由于甲醇易挥发,则作用是对甲中的甲醇蒸汽具有冷凝回流的作用,
同时让产生的气体逸出:(2)甲醇被氧化为甲酸 还原生成 ,硫酸生成硫酸钠,
反应方程式为 ===== ;(3)稳定剂吸收
,生成 NaClO ,加盐酸后 发生歧化反应释放 ,发生的离子反应方程式是:
2
;(4)生成的 要在 反应,温度不能过高,裝置甲直接加热,
无法控制温度,故用水浴加热;(5) 吸收 尾气,生成物质的量之比为1∶1的两种阴离子,一种为
,氯元素由 价得电子降低到 价,那么还有一部分氯元素由 价失电子升高到 价,则另一种
为 ;(6)根据题目信息, , 的物质的量为 ,故
的物质的量为0.0004mol,质量为: ,水样中 的含
量为 。
模 拟 优 练
1.次硫酸氢钠甲醛(NaHSO·HCHO·2H O)在印染、医药以及原子能工业中应用广泛。以 NaSO 、SO 、
2 2 2 3 2
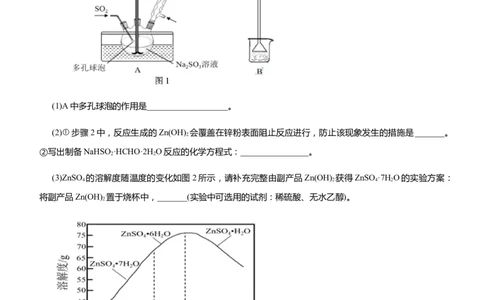
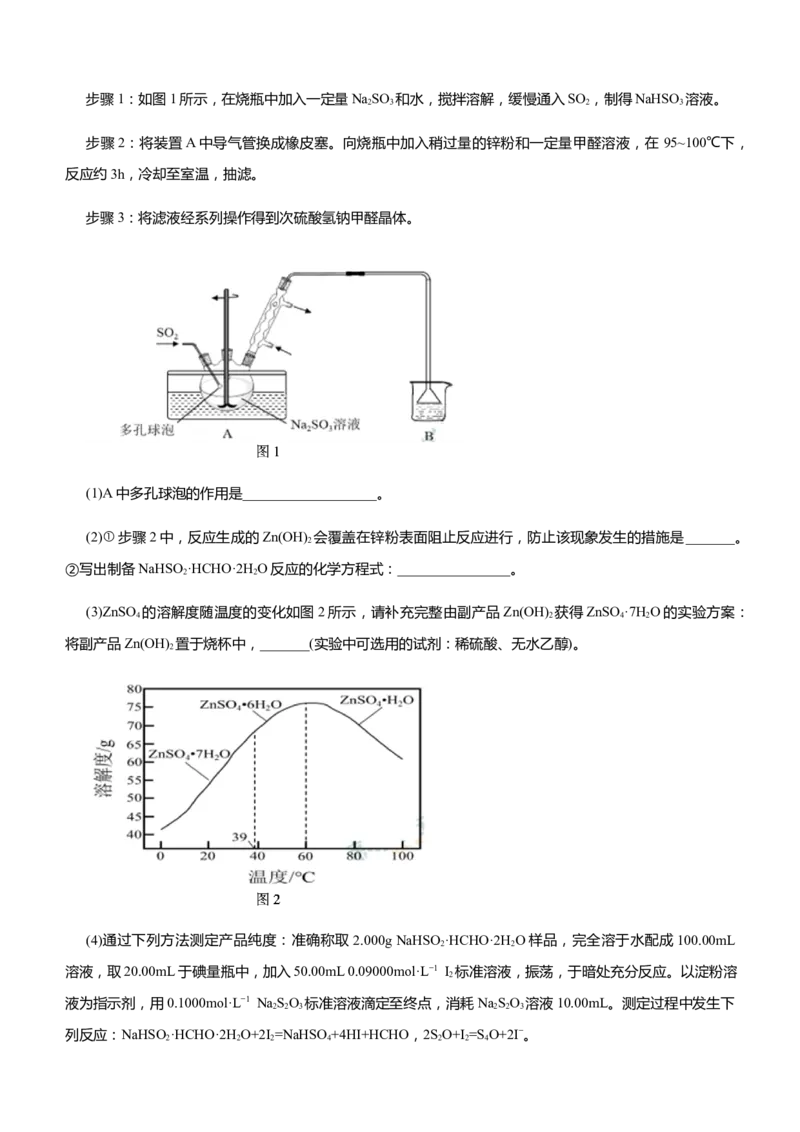
HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:步骤1:如图1所示,在烧瓶中加入一定量NaSO 和水,搅拌溶解,缓慢通入SO ,制得NaHSO 溶液。
2 3 2 3
步骤2:将装置A中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在 95~100℃下,
反应约3h,冷却至室温,抽滤。
步骤3:将滤液经系列操作得到次硫酸氢钠甲醛晶体。
(1)A中多孔球泡的作用是___________________。
(2)①步骤2中,反应生成的Zn(OH) 会覆盖在锌粉表面阻止反应进行,防止该现象发生的措施是_______。
2
②写出制备NaHSO·HCHO·2H O反应的化学方程式:________________。
2 2
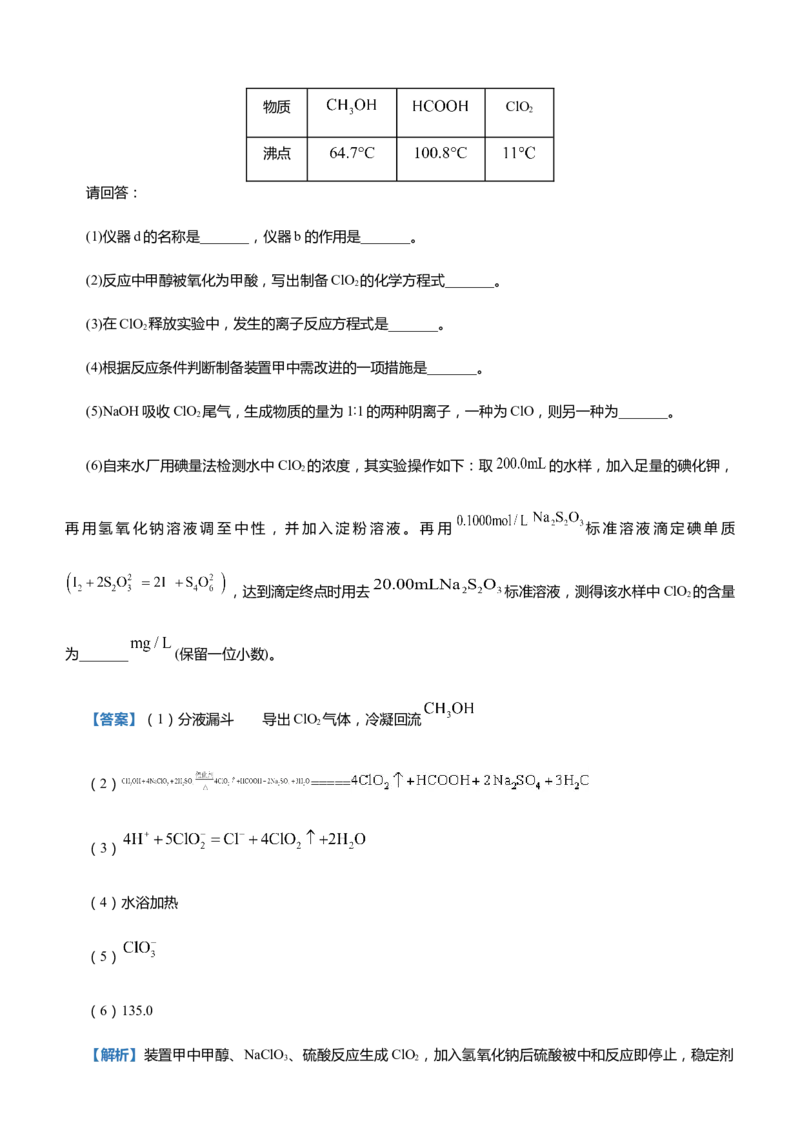
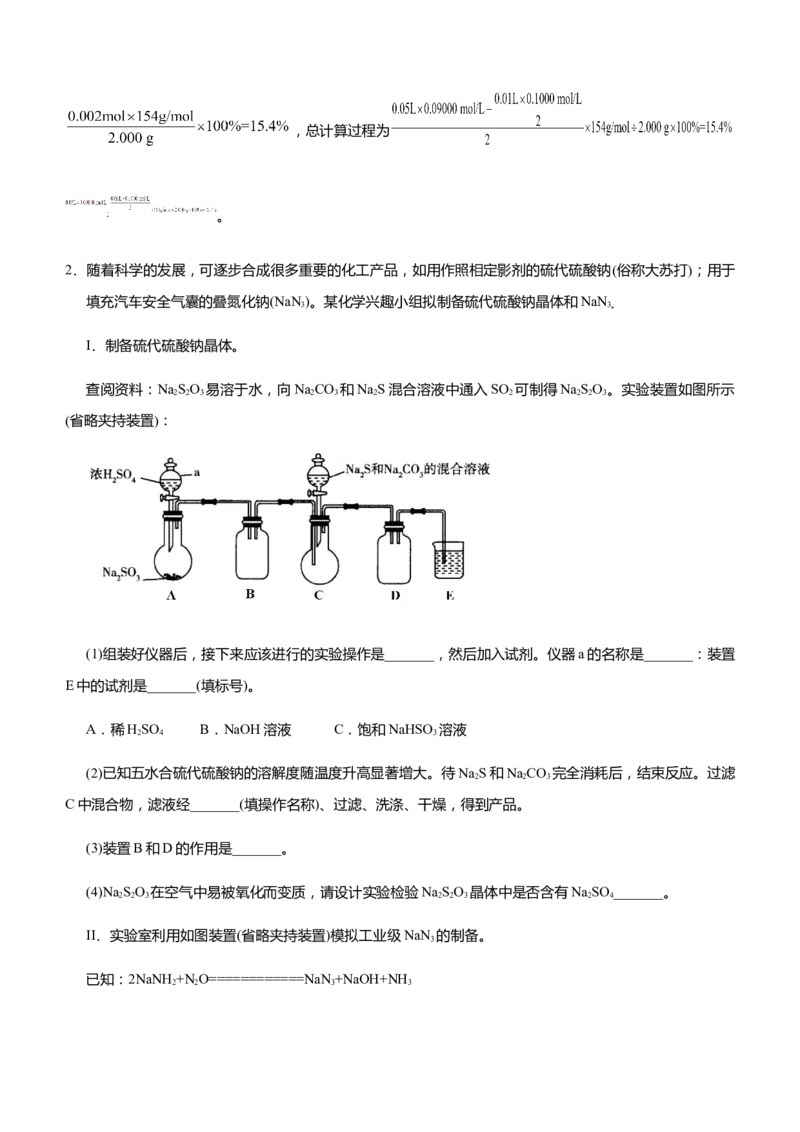
(3)ZnSO 的溶解度随温度的变化如图2所示,请补充完整由副产品Zn(OH) 获得ZnSO·7H O的实验方案:
4 2 4 2
将副产品Zn(OH) 置于烧杯中,_______(实验中可选用的试剂:稀硫酸、无水乙醇)。
2
(4)通过下列方法测定产品纯度:准确称取2.000g NaHSO ·HCHO·2H O样品,完全溶于水配成100.00mL
2 2
溶液,取20.00mL于碘量瓶中,加入50.00mL 0.09000mol·L−1 I 标准溶液,振荡,于暗处充分反应。以淀粉溶
2
液为指示剂,用0.1000mol·L−1 Na SO 标准溶液滴定至终点,消耗NaSO 溶液10.00mL。测定过程中发生下
2 2 3 2 2 3
列反应:NaHSO·HCHO·2H O+2I =NaHSO +4HI+HCHO,2SO+I =S O+2I−。
2 2 2 4 2 2 4计算NaHSO·HCHO·2H O样品的纯度(写出计算过程)_______。
2 2
【答案】(1)增大接触面积,使SO 充分反应
2
(2)快速搅拌
(3)加入适量稀硫酸使沉淀溶解,通过蒸发浓缩,冷却结晶,控制温度在 20℃~39℃之间,使
ZnSO·7H O析出,用乙醇进行洗涤,干燥后得到ZnSO·7H O晶体
4 2 4 2
(4)15.4%
【解析】步骤1:在烧瓶中加入一定量NaSO 和水,搅拌溶解,缓慢通入SO ,NaSO 、HO、SO 反应
2 3 2 2 3 2 2
生成NaHSO ,A中多孔球泡的是为了增大接触面积,使SO 充分反应;步骤2:将装置A中导气管换成橡皮
3 2
塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在 95~100℃下,反应约3h,NaHSO 溶液、锌粉和甲醛
3
反 应 生 成 NaHSO·HCHO·2H O 和 Zn(OH) , 化 学 方 程 式 为
2 2 2
。(1)A中多孔球泡的作用是可以增大接触面
积,使SO 充分反应;(2)①通过快速搅拌可防止Zn(OH) 会覆盖在锌粉的表面;②NaHSO 溶液、锌粉和甲
2 2 3
醛 反 应 生 成 NaHSO·HCHO·2H O 和 Zn(OH) , 化 学 方 程 式 为
2 2 2
;(3)由副产品Zn(OH) 获得ZnSO·7H O的
2 4 2
实验方案:将副产品Zn(OH) 置于烧杯中,加入适量稀硫酸使沉淀溶解,通过蒸发浓缩,冷却结晶,控制温
2
度在 20℃~39℃之间,使 ZnSO·7H O 析出,用乙醇进行洗涤,干燥后得到 ZnSO·7H O 晶体。(4)用
4 2 4 2
0.1000mol·L−1 NaSO 标准溶液滴定至终点,消耗NaSO 溶液10.00mL,根据离子方程式2SO+I =S O+2I−可
2 2 3 2 2 3 2 2 4
知,与NaHSO·HCHO·2H O反应后剩余的I 的物质的量为 ,反应前加入
2 2 2
50.00mL 0.09000mol·L−1 I 标准溶液,由此可计算出与 NaHSO·HCHO·2H O 反应消耗 I 的物质的量为
2 2 2 2
,根据化学方程式NaHSO·HCHO·2H O+2I =NaHSO +4HI+
2 2 2 4
HCHO , 算 出 NaHSO·HCHO·2H O 的 物 质 的 量 为 , 其 纯 度 为
2 2,总计算过程为
。
2.随着科学的发展,可逐步合成很多重要的化工产品,如用作照相定影剂的硫代硫酸钠(俗称大苏打);用于
填充汽车安全气囊的叠氮化钠(NaN )。某化学兴趣小组拟制备硫代硫酸钠晶体和NaN
3 3。
I.制备硫代硫酸钠晶体。
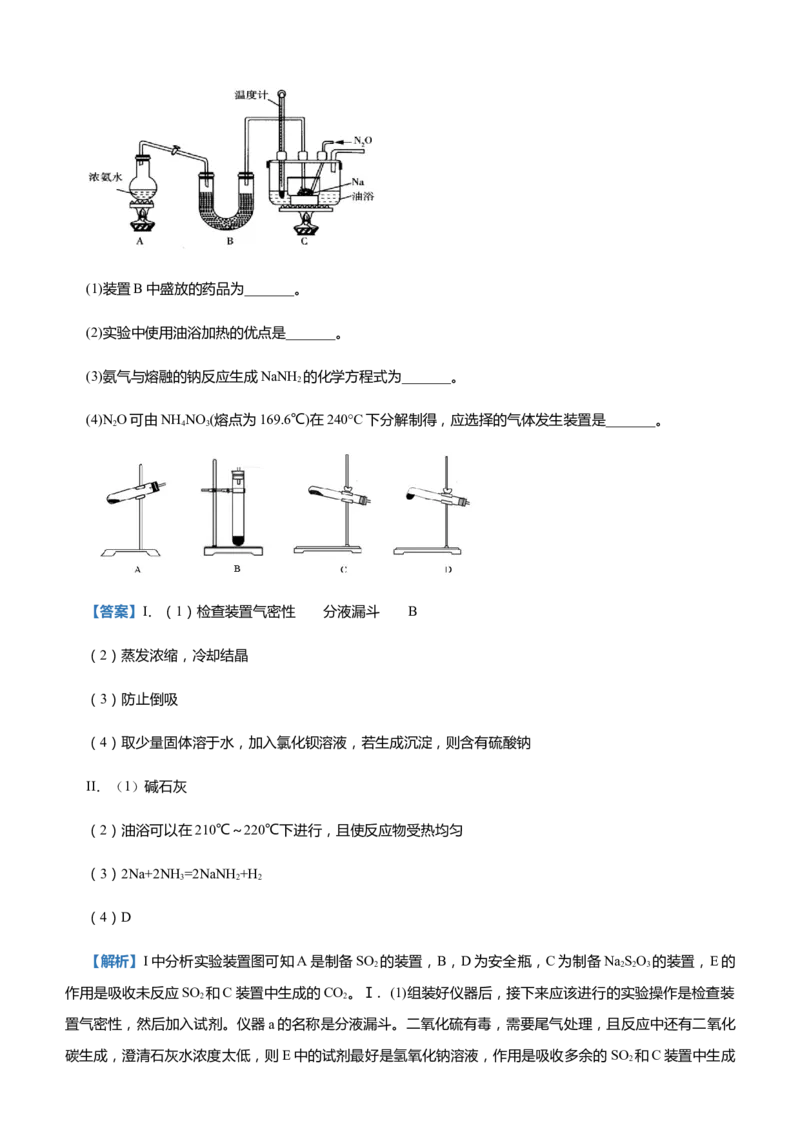
查阅资料:NaSO 易溶于水,向NaCO 和NaS混合溶液中通入SO 可制得NaSO 。实验装置如图所示
2 2 3 2 3 2 2 2 2 3
(省略夹持装置):
(1)组装好仪器后,接下来应该进行的实验操作是_______,然后加入试剂。仪器a的名称是_______:装置
E中的试剂是_______(填标号)。
A.稀HSO B.NaOH溶液 C.饱和NaHSO 溶液
2 4 3
(2)已知五水合硫代硫酸钠的溶解度随温度升高显著增大。待NaS和NaCO 完全消耗后,结束反应。过滤
2 2 3
C中混合物,滤液经_______(填操作名称)、过滤、洗涤、干燥,得到产品。
(3)装置B和D的作用是_______。
(4)Na SO 在空气中易被氧化而变质,请设计实验检验NaSO 晶体中是否含有NaSO _______。
2 2 3 2 2 3 2 4
II.实验室利用如图装置(省略夹持装置)模拟工业级NaN 的制备。
3
已知:2NaNH +N O============NaN +NaOH+NH
2 2 3 3(1)装置B中盛放的药品为_______。
(2)实验中使用油浴加热的优点是_______。
(3)氨气与熔融的钠反应生成NaNH 的化学方程式为_______。
2
(4)N O可由NH NO (熔点为169.6℃)在240°C下分解制得,应选择的气体发生装置是_______。
2 4 3
【答案】I.(1)检查装置气密性 分液漏斗 B
(2)蒸发浓缩,冷却结晶
(3)防止倒吸
(4)取少量固体溶于水,加入氯化钡溶液,若生成沉淀,则含有硫酸钠
II.(1)碱石灰
(2)油浴可以在210℃~220℃下进行,且使反应物受热均匀
(3)2Na+2NH =2NaNH +H
3 2 2
(4)D
【解析】I中分析实验装置图可知A是制备SO 的装置,B,D为安全瓶,C为制备NaSO 的装置,E的
2 2 2 3
作用是吸收未反应SO 和C装置中生成的CO 。Ⅰ.(1)组装好仪器后,接下来应该进行的实验操作是检查装
2 2
置气密性,然后加入试剂。仪器a的名称是分液漏斗。二氧化硫有毒,需要尾气处理,且反应中还有二氧化
碳生成,澄清石灰水浓度太低,则E中的试剂最好是氢氧化钠溶液,作用是吸收多余的SO 和C装置中生成
2的CO 气体。(2)由于五水合硫代硫酸钠的溶解度随温度升高显著增大。待 NaS和NaCO 完全消耗后,结束
2 2 2 3
反应。过滤C中混合物,滤液经蒸发浓缩,冷却结晶、过滤、洗涤、干燥,得到产品。(3)B和D为安全瓶,
防止倒吸。(4)取少量固体溶于水,加入氯化钡溶液,若生成沉淀,则含有硫酸钠。Ⅱ.(1)生成的氨气中含有
水蒸气,需要干燥,则装置B中盛放的药品为碱石灰。(2)由于制备NaN 的反应需要在210℃~220℃下进行,
3
水浴不能达到这样的温度,所以实验中使用油浴而不用水浴。(3)氨气与熔融的钠反应生成NaNH ,根据原子
2
守恒可知还有氢气生成,反应的化学方程式为2Na+2NH =2NaNH +H 。(4)N O可由NH NO (熔点为169.6℃)
3 2 2 2 4 3
在240℃下分解制得,由于在该温度下硝酸铵已熔化,同时为避免液体倒流引起试管炸裂,因此选择的气体
发生装置是装置D。
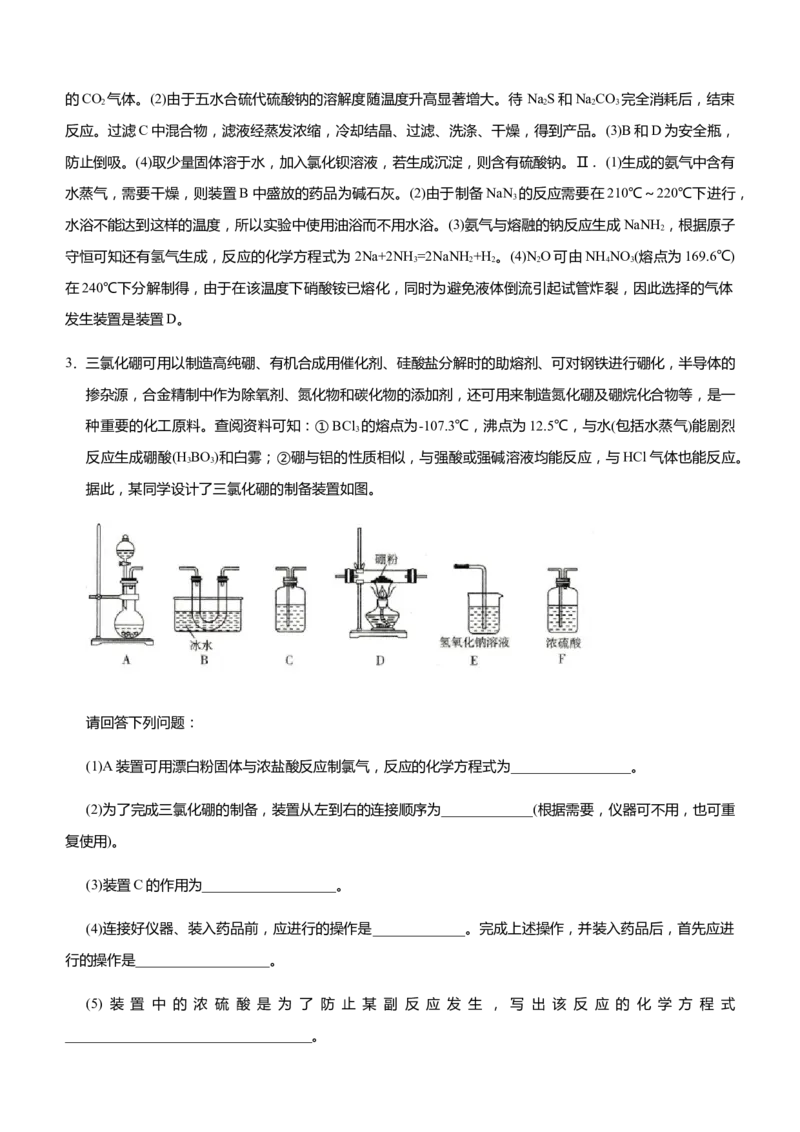
3.三氯化硼可用以制造高纯硼、有机合成用催化剂、硅酸盐分解时的助熔剂、可对钢铁进行硼化,半导体的
掺杂源,合金精制中作为除氧剂、氮化物和碳化物的添加剂,还可用来制造氮化硼及硼烷化合物等,是一
种重要的化工原料。查阅资料可知:①BCl 的熔点为-107.3℃,沸点为12.5℃,与水(包括水蒸气)能剧烈
3
反应生成硼酸(H BO)和白雾;②硼与铝的性质相似,与强酸或强碱溶液均能反应,与HCl气体也能反应。
3 3
据此,某同学设计了三氯化硼的制备装置如图。
请回答下列问题:
(1)A装置可用漂白粉固体与浓盐酸反应制氯气,反应的化学方程式为_________________。
(2)为了完成三氯化硼的制备,装置从左到右的连接顺序为_____________(根据需要,仪器可不用,也可重
复使用)。
(3)装置C的作用为___________________。
(4)连接好仪器、装入药品前,应进行的操作是_____________。完成上述操作,并装入药品后,首先应进
行的操作是___________________。
(5) 装 置 中 的 浓 硫 酸 是 为 了 防 止 某 副 反 应 发 生 , 写 出 该 反 应 的 化 学 方 程 式
___________________________________。(6)实验结束后,取E中溶液适量于试管中,滴加几滴酚酞试液,现象为_______________,产生该现象的
原因为_______________________________。
【答案】(1)Ca(ClO) +4HCl(浓)=CaCl +2Cl↑+2H O
2 2 2 2
(2)ACFDBFE
(3)除去Cl 中混有的HCl气体,防止其与硼发生副反应(生成H 与Cl 混合共热有爆炸危险)
2 2 2
(4)检查装置气密性 打开分液漏斗活塞,通一段时间Cl
2
(5)BCl +3H O=HBO+3HCl↑
3 2 3 3
(6)溶液先变红后褪色 NaOH溶液呈碱性使酚酞变红,NaClO有漂白性使酚酞褪色
【解析】根据装置制备 BCl :由 A 中用漂白粉固体与浓盐酸反应制氯气,反应的化学方程式为
3
Ca(ClO) +4HCl(浓)=CaCl +2Cl↑+2H O,制得的氯气混有HCl和水蒸气,由C中饱和食盐水吸收HCl气体,
2 2 2 2
由F中浓硫酸吸水干燥,发生反应前先通入一段时间的氯气,排尽装置中的空气,干燥纯净的氯气与硼粉在
D中发发生反应,用B中冰水冷凝产物BCl 并收集,E中NaOH吸收尾气,防止污染空气,三氯化硼与水能
3
剧烈反应生成硼酸(HBO )和HCl:BCl +3H O=HBO+3HCl↑,为防止E中的水蒸气进入B装置,在B和
3 3 3 2 3 3
E 之间连接一个 F 干燥装置,(1)用漂白粉固体与浓盐酸反应制氯气,反应的化学方程式为
Ca(ClO) +4HCl(浓)=CaCl +2Cl↑+2H O;(2)根据分析,A制备氯气,C中饱和食盐水吸收HCl气体,F中浓硫
2 2 2 2
酸吸水干燥,为保证除杂充分,导气管均长进短出,干燥纯净的氯气与硼粉在 D中发发生反应,用B中冰水
冷凝产物BCl 并收集,E中NaOH吸收尾气,防止污染空气,为防止E中的水蒸气进入B装置,在B和E之
3
间连接一个F干燥装置,故连接顺序为:ACFDBFE;(3)装置C中为饱和食盐水,作用为除去Cl 中混有的
2
HCl气体,防止其与硼发生副反应(生成H 与Cl 混合共热有爆炸危险);(4)装入药品前,应检查装置气密性,
2 2
装入药品后,先打开分液漏斗活塞,通入一段时间的氯气,排尽装置中的空气;(5)三氯化硼与水能剧烈反应
生成 硼酸 (H BO)和白雾 ,白雾 为 HCl ,反应为: BCl +3H O=HBO+3HCl↑ ;(6)E 中发生反应
3 3 3 2 3 3
Cl+2NaOH=NaClO+NaCl+H O,溶液中存在具有漂白性的NaClO和过量的NaOH,滴加几滴酚酞试液,溶液
2 2
先变红后褪色,原因是NaOH溶液呈碱性使酚酞变红,NaClO有漂白性使酚酞褪色。
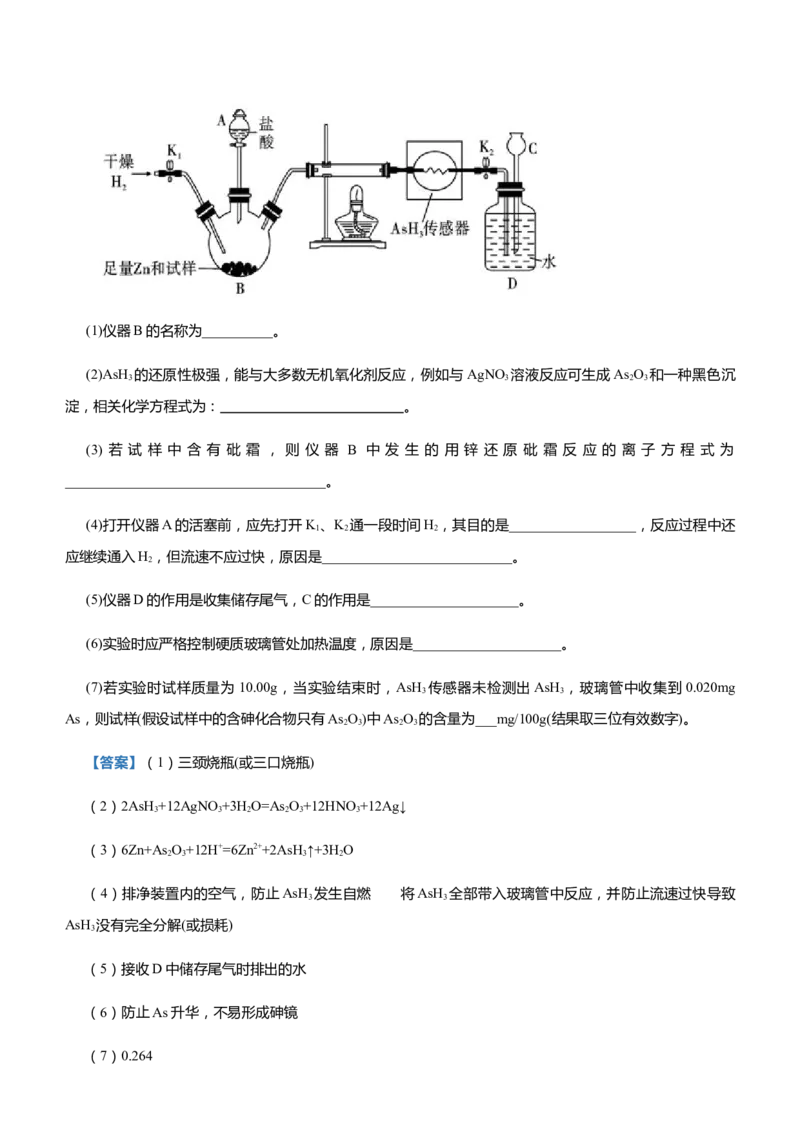
4.As O 为白色霜状粉末,俗称砒霜,为剧毒物质,对人的致死量为 0.1g,法医学中可采用马氏(Marsh)试砷
2 3
法验证砒霜中毒。某实验室使用马氏试砷法检验某待测试样中As O 的含量,如图所示。马氏试砷法的原
2 3
理是将Zn、盐酸和待测试样混合,若试样中含砒霜,则可反应生成 AsH ,将其导入硬质玻璃试管中,在
3
250℃~300℃时AsH 分解,会在玻璃管壁上生成黑色的“砷镜”。
3
已知:AsH 是一种有大蒜味的有毒气体,易自燃,As的熔点为817℃,在6149℃时升华。
3(1)仪器B的名称为__________。
(2)AsH 的还原性极强,能与大多数无机氧化剂反应,例如与 AgNO 溶液反应可生成As O 和一种黑色沉
3 3 2 3
淀,相关化学方程式为: 。
(3) 若 试 样 中 含 有 砒 霜 , 则 仪 器 B 中 发 生 的 用 锌 还 原 砒 霜 反 应 的 离 子 方 程 式 为
_____________________________________。
(4)打开仪器A的活塞前,应先打开K 、K 通一段时间H ,其目的是__________________,反应过程中还
1 2 2
应继续通入H,但流速不应过快,原因是___________________________。
2
(5)仪器D的作用是收集储存尾气,C的作用是_____________________。
(6)实验时应严格控制硬质玻璃管处加热温度,原因是_____________________。
(7)若实验时试样质量为10.00g,当实验结束时,AsH 传感器未检测出AsH ,玻璃管中收集到0.020mg
3 3
As,则试样(假设试样中的含砷化合物只有As O)中As O 的含量为___mg/100g(结果取三位有效数字)。
2 3 2 3
【答案】(1)三颈烧瓶(或三口烧瓶)
(2)2AsH +12AgNO +3H O=As O+12HNO +12Ag↓
3 3 2 2 3 3
(3)6Zn+As O+12H+=6Zn2++2AsH ↑+3H O
2 3 3 2
(4)排净装置内的空气,防止AsH 发生自燃 将AsH 全部带入玻璃管中反应,并防止流速过快导致
3 3
AsH 没有完全分解(或损耗)
3
(5)接收D中储存尾气时排出的水
(6)防止As升华,不易形成砷镜
(7)0.264【解析】(1)仪器B的名称为三颈圆底烧瓶(或三口烧瓶);(2)AsH 的还原性极强,能与大多数无机氧化剂
3
反应,例如与AgNO 溶液反应可生成As O 和一种黑色沉淀,As的化合价升高,则Ag化合价降低,黑色沉
3 2 3
淀为:Ag。相关化学方程式为:2AsH +12AgNO +3H O=As O+12HNO +12Ag↓;(3) 在酸性溶液中,锌还原
3 3 2 2 3 3
砒霜,锌氧化为锌离子,As O 还原为AsH ,反应的离子方程式为:6Zn+As O+12H+=6Zn2++2AsH ↑+3H O;
2 3 3 2 3 3 2
(4)打开仪器A的活塞前,应先打开K 、K 通一段时间H ,其目的是排净装置内的空气,防止AsH 发生自燃。
1 2 2 3
反应过程中还应继续通入H ,但流速不应过快,原因是:将AsH 全部带入玻璃管中反应,并防止流速过快
2 3
导致AsH 没有完全分解(或损耗);(5)仪器D的作用是收集储存尾气,C的作用是接收D中储存尾气时排出的
3
水;(6)实验时应严格控制硬质玻璃管处加热温度,原因是防止As升华,不易形成砷镜;(7)实验所用试样为
10.00g当实验结束时,AsH 传感器未检测出AsH ,说明AsH 全部在玻璃管中受热分解为0.020mg As,则试
3 3 3
样中As O 的含量为 =0.264mg/100g。
2 3
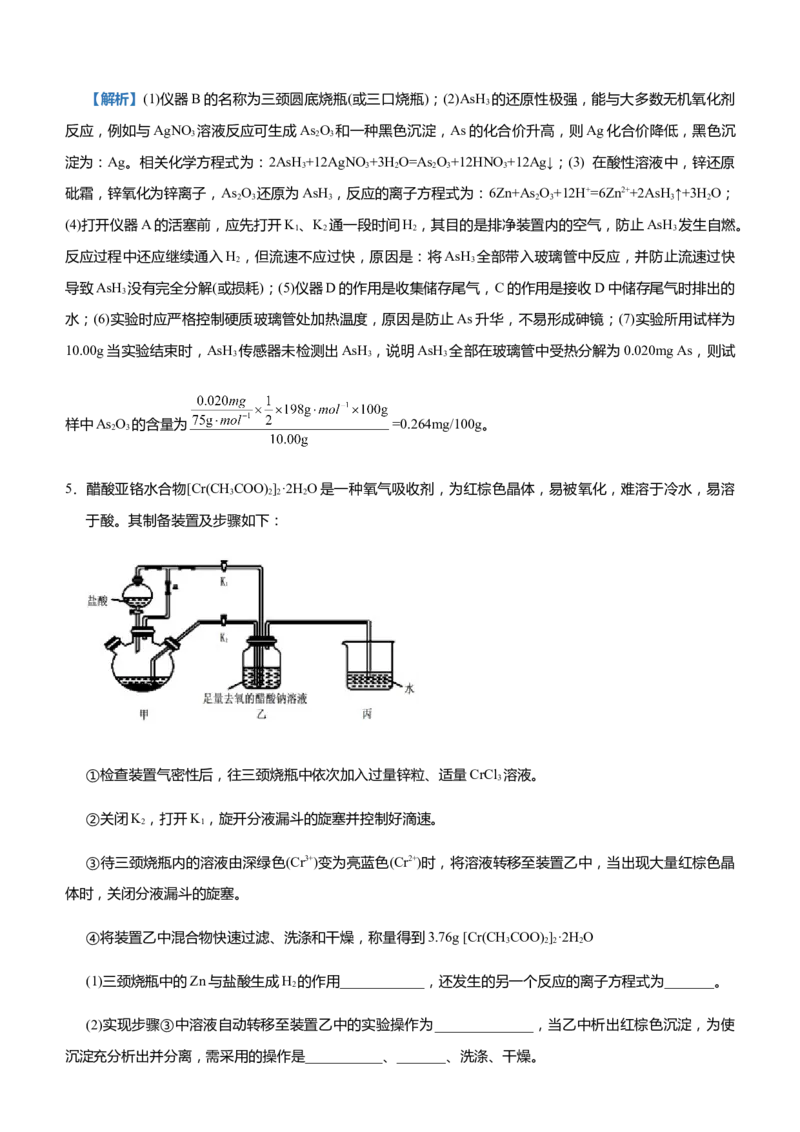
5.醋酸亚铬水合物[Cr(CH COO) ]·2H O是一种氧气吸收剂,为红棕色晶体,易被氧化,难溶于冷水,易溶
3 2 2 2
于酸。其制备装置及步骤如下:
①检查装置气密性后,往三颈烧瓶中依次加入过量锌粒、适量CrCl 溶液。
3
②关闭K,打开K,旋开分液漏斗的旋塞并控制好滴速。
2 1
③待三颈烧瓶内的溶液由深绿色(Cr3+)变为亮蓝色(Cr2+)时,将溶液转移至装置乙中,当出现大量红棕色晶
体时,关闭分液漏斗的旋塞。
④将装置乙中混合物快速过滤、洗涤和干燥,称量得到3.76g [Cr(CH COO) ]·2H O
3 2 2 2
(1)三颈烧瓶中的Zn与盐酸生成H 的作用____________,还发生的另一个反应的离子方程式为_______。
2
(2)实现步骤③中溶液自动转移至装置乙中的实验操作为______________,当乙中析出红棕色沉淀,为使
沉淀充分析出并分离,需采用的操作是___________、_______、洗涤、干燥。(3)装置丙中导管口水封的目的是______________。
(4)铬的离子会污染水,常温下要除去上述实验中多余的Cr2+,最好往废液中通入足量的空气,再加入碱液,
调节pH至少为___才能使铬的离子沉淀完全。[已知Cr(OH) 的溶度积为1×10−32]
3
(5)若实验所取用的CrCl 溶液中含溶质6.34g,则[Cr(CH COO) ]·2H O(相对分子质量为376)的产率是____。
3 3 2 2 2
【答案】(1)排除装置中的空气 2Cr3++Zn=2Cr2++Zn2+
(2)关闭k,打开k 冷却 过滤
1 2
(3)防止空气进入装置乙中氧化Cr2+
(4)5
(5)50%
【解析】(1)产品易被氧化,因此生成H 的作用是排除装置中空气,防止醋酸亚铬水合物被氧化;锌为
2
活泼金属,与Cr3+发生:Zn+2Cr3+=Zn2++2Cr2+;(2)实现步骤③中溶液自动转移至装置乙中,利用三颈烧瓶
的压强大,把液体压入装置乙中,即打开k ,关闭k ;根据信息,醋酸亚铬水合物难溶于冷水,因此采用操
2 1
作是冷却、过滤、洗涤、干燥;(3)醋酸亚铬水合物易被氧化,因此装置丙中导管口水封的目的是防止空气
进 入 装 置 乙 中 氧 化 Cr2+ ; ( 4 ) Cr3+ 完 全 转 化 成 沉 淀 , c(Cr3+)≤10−5mol/L , 因 此 有 c(OH−)≥
=10−9
mol·L−1 , 即 pH 至 少 为 5 , 才 能 使 Cr3+ 全 部 转 化 成 沉 淀 ; ( 5 ) CrCl 的 物 质 的 量 为 6.34g/
3
158.5g·mol−1=0.04mol,根据 Cr 元素守恒,[Cr(CH COO) ]·2H O 的物质的量为 0.04mol/2=0.02mol,
3 2 2 2
[Cr(CH COO) ]·2H O的质量为0.02mol×376g·mol−1=7.52g,即产率为3.76g/7.52g×100%=50%。
3 2 2 2