文档内容
培优训练13:物质结构与性质
1.钛的很多化合物受到广泛关注,请回答下列问题:
(1)Cr掺杂能够显著提高TiO 薄膜的光催化活性。基态Cr原子中,占据最高能层
2
的核外电子的电子云轮廓图形状为________,其价层电子的轨道表达式(电子排布
图)为______________________________________________________________。
(2)四乙醇钛能增加橡胶在金属表面的粘附性。其制备原理如下:
TiCl +4CH CH OH+4NH ===Ti(OCH CH ) +4NH Cl
4 3 2 3 2 3 4 4
①TiCl 的熔点为-25 ℃,沸点为136.45 ℃,常温下是无色液体,则TiCl 的晶体类
4 4
型为________。
②N和O位于同一周期,且O的核电荷数比N的多,但N的第一电离能比O高,
原因是______________________________________________________________。
③NH 的立体构型为________,CH CH OH 分子中 C 原子的杂化轨道类型为
3 3 2
________。
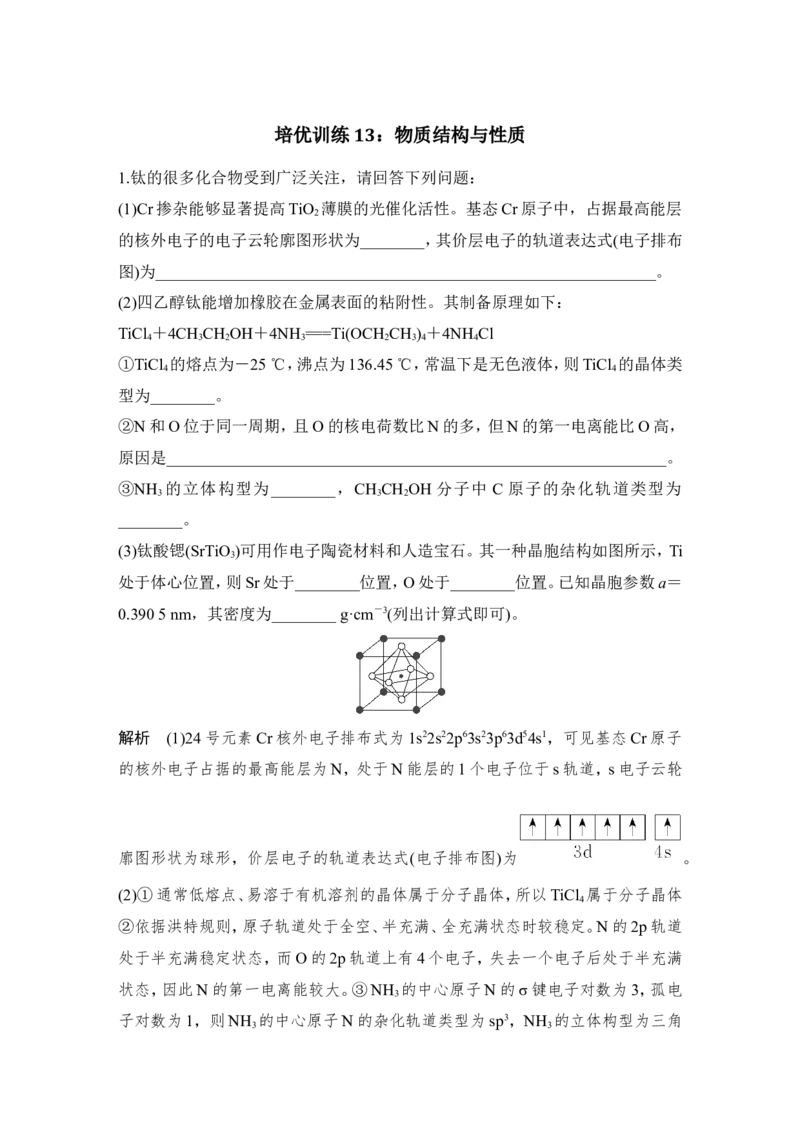
(3)钛酸锶(SrTiO )可用作电子陶瓷材料和人造宝石。其一种晶胞结构如图所示,Ti
3
处于体心位置,则Sr处于________位置,O处于________位置。已知晶胞参数a=
0.390 5 nm,其密度为________ g·cm-3(列出计算式即可)。
解析 (1)24号元素Cr核外电子排布式为1s22s22p63s23p63d54s1,可见基态Cr原子
的核外电子占据的最高能层为N,处于N能层的1个电子位于s轨道,s电子云轮
廓图形状为球形,价层电子的轨道表达式(电子排布图)为 。
(2)①通常低熔点、易溶于有机溶剂的晶体属于分子晶体,所以TiCl 属于分子晶体
4
②依据洪特规则,原子轨道处于全空、半充满、全充满状态时较稳定。N的2p轨道
处于半充满稳定状态,而O的2p轨道上有4个电子,失去一个电子后处于半充满
状态,因此N的第一电离能较大。③NH 的中心原子N的σ键电子对数为3,孤电
3
子对数为1,则NH 的中心原子N的杂化轨道类型为sp3,NH 的立体构型为三角
3 3锥形。乙醇分子中两个C原子形成的σ键数均为4,因此两个碳原子均采用sp3杂
化。(3)已知钛酸锶的化学式为SrTiO ,Sr、Ti、O三种粒子的个数比为1∶1∶3,既
3
然Ti处于体心位置,根据均摊法,晶胞中Ti的数目为1,处于面心位置的属于一个
晶胞的粒子数为3,所以,处于面心位置的为O,那么,处于顶角位置的就是Sr。因
为该晶胞是立方晶系,且在一个晶胞中含有1个SrTiO ,则ρ== g·cm-3。
3
答案 (1)球形
(2)①分子晶体 ②N的2p轨道处于半充满稳定状态,而O的2p轨道有4个电子
失去一个电子后处于半充满状态,因此N的第一电离能较大 ③三角锥形 sp3
(3)顶角 面心
2.2017年4月26日,中国首艘国产航母在大连正式下水,标志着我国自主设计建
造航空母舰取得重大阶段性成果。请回答下列问题:
(1)航母用钢可由低硅生铁冶炼而成。
①硅原子价层电子的轨道表示式(电子排布图)为________。
②Fe3+比Fe2+稳定的原因是______________________________________________
____________________________________________________________________。
③FeO、NiO的晶体结构与NaCl的晶体结构相同。其中Fe2+与Ni2+的离子半径分
别为7.8×10-2 nm、6.9×10-2 nm。则熔点FeO________(填“<”“>”或“=”)NiO,
原因是_____________________________________________________________
__________________________________________________________________。
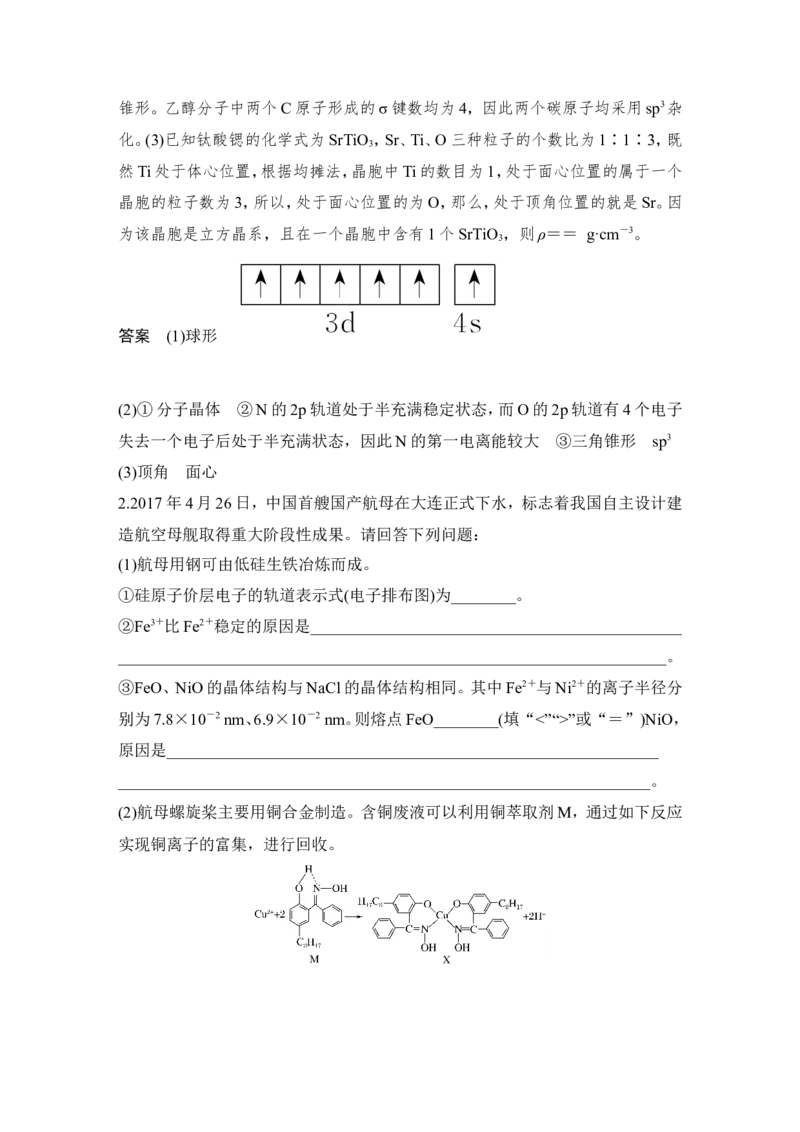
(2)航母螺旋桨主要用铜合金制造。含铜废液可以利用铜萃取剂M,通过如下反应
实现铜离子的富集,进行回收。①M所含元素的电负性由大到小的顺序为________(用元素符号表示)。
②上述反应中断裂和生成的化学键有________(填序号)。
A.共价键 B.配位键
C.金属键 D.范德华力
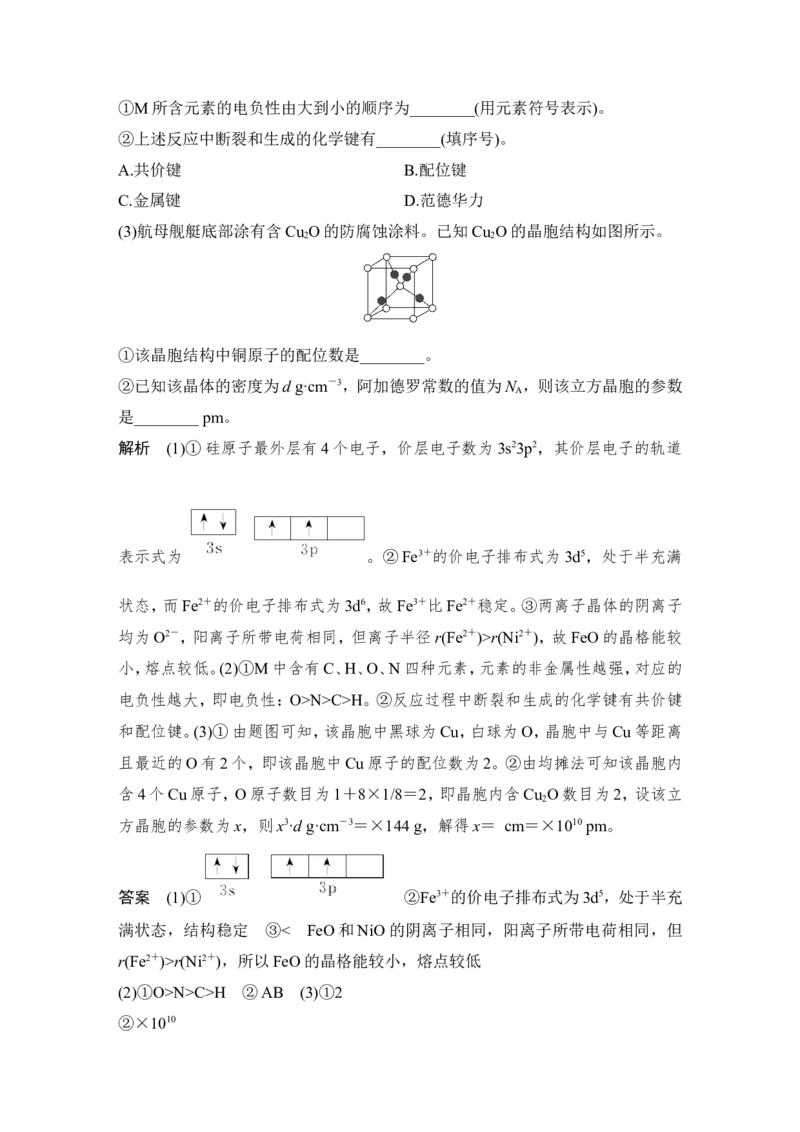
(3)航母舰艇底部涂有含Cu O的防腐蚀涂料。已知Cu O的晶胞结构如图所示。
2 2
①该晶胞结构中铜原子的配位数是________。
②已知该晶体的密度为d g·cm-3,阿加德罗常数的值为N ,则该立方晶胞的参数
A
是________ pm。
解析 (1)①硅原子最外层有4个电子,价层电子数为3s23p2,其价层电子的轨道
表示式为 。②Fe3+的价电子排布式为3d5,处于半充满
状态,而Fe2+的价电子排布式为3d6,故Fe3+比Fe2+稳定。③两离子晶体的阴离子
均为O2-,阳离子所带电荷相同,但离子半径r(Fe2+)>r(Ni2+),故FeO的晶格能较
小,熔点较低。(2)①M中含有C、H、O、N四种元素,元素的非金属性越强,对应的
电负性越大,即电负性:O>N>C>H。②反应过程中断裂和生成的化学键有共价键
和配位键。(3)①由题图可知,该晶胞中黑球为Cu,白球为O,晶胞中与Cu等距离
且最近的O有2个,即该晶胞中Cu原子的配位数为2。②由均摊法可知该晶胞内
含4个Cu原子,O原子数目为1+8×1/8=2,即晶胞内含Cu O数目为2,设该立
2
方晶胞的参数为x,则x3·d g·cm-3=×144 g,解得x= cm=×1010 pm。
答案 (1)① ②Fe3+的价电子排布式为3d5,处于半充
满状态,结构稳定 ③< FeO和NiO的阴离子相同,阳离子所带电荷相同,但
r(Fe2+)>r(Ni2+),所以FeO的晶格能较小,熔点较低
(2)①O>N>C>H ②AB (3)①2
②×10103.[2018·陕西省高三教学质检(一),35]钛( Ti)铝合金在航空领域应用广泛。回答下
22
列问题:
(1)基态Ti原子的核外电子排布式为[Ar]________,其中s轨道上总共有________
个电子。
(2)六氟合钛酸钾(K TiF )中存在[TiF ]2-配离子,则钛元素的化合价是________,配
2 6 6
体是________。
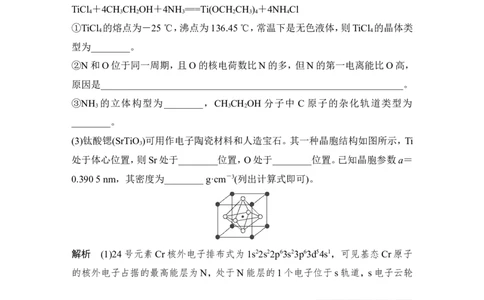
(3)TiCl 可用作烯烃定向聚合的催化剂,例如,丙烯用三乙基铝和三氯化钛作催化
3
剂时,可以发生下列聚合反应:
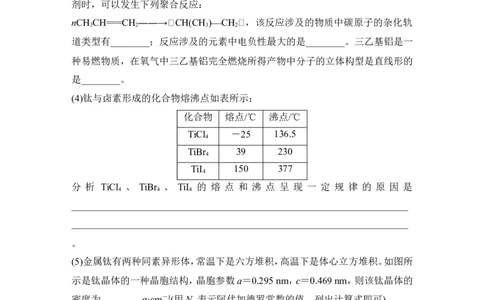
nCH CH===CH ――→CH(CH )—CH ,该反应涉及的物质中碳原子的杂化轨
3 2 3 2
道类型有________;反应涉及的元素中电负性最大的是________。三乙基铝是一
种易燃物质,在氧气中三乙基铝完全燃烧所得产物中分子的立体构型是直线形的
是________。
(4)钛与卤素形成的化合物熔沸点如表所示:
化合物 熔点/℃ 沸点/℃
TiCl -25 136.5
4
TiBr 39 230
4
TiI 150 377
4
分 析 TiCl 、 TiBr 、 TiI 的 熔 点 和 沸 点 呈 现 一 定 规 律 的 原 因 是
4 4 4
_____________________________________________________________________
_____________________________________________________________________
。
(5)金属钛有两种同素异形体,常温下是六方堆积,高温下是体心立方堆积。如图所
示是钛晶体的一种晶胞结构,晶胞参数a=0.295 nm,c=0.469 nm,则该钛晶体的
密度为________ g·cm-1(用N 表示阿伏加德罗常数的值,列出计算式即可)。
A
解析 (1)Ti 为 22 号元素,基态 Ti 原子的核外电子排布式为[Ar]3d24s2 或
1s22s22p63s23p63d24s2,其中s轨道上共有8个电子。(2)由化合物中正、负化合价的
代数和为0,知钛元素的化合价为+4,配体是F-。(3)该反应涉及的物质中碳原子的杂化轨道类型有sp3杂化、sp2杂化。同一周期主族元素,从左到右元素的电负性
递增,同一主族元素,自上而下元素的电负性递减,故涉及的元素中电负性最大的
是Cl。三乙基铝在O 中燃烧生成Al O 、CO 和H O,其中分子的立体构型是直线
2 2 3 2 2
形的是CO 。(4)三者都是分子晶体,对于组成和结构相似的分子晶体,相对分子质
2
量越大,分子间作用力越大,熔、沸点越高。(5)该晶胞的底面正六边形的面积S=
a2,则该晶胞的体积为a2c=×(2.95×10-8)2×(4.69×10-8)cm3,又该晶胞中含有的
钛原子的数目为2×+3+12×=6,则该晶胞的质量为 g,故该钛晶体的密度为
g·cm-3。
答案 (1)3d24s2 8 (2)+4 F- (3)sp2、sp3 Cl CO (4)TiCl 、TiBr 、TiI 都是
2 4 4 4
分子晶体,而且组成和结构相似,其相对分子质量依次增大,分子间作用力逐渐增
大,因而三者的熔点和沸点依次升高
(5)
4.2013年诺贝尔化学奖授予三位美国科学家,以表彰他们在开发多尺度复杂化学
系统模型方面所做的贡献。这种模型可以用量子化学计算小区间内(如生物固氮时
固氮酶中)的化学反应。
(1)固氮酶有铁蛋白和钼铁蛋白两种,它们不仅能够催化N 还原成NH ,还能将环
2 3
境底物乙炔(HC≡CH)催化还原成乙烯。
①乙炔是________(填“非极性”或“极性”)分子。
②碳负离子CH的立体构型为________。
③根据等电子原理,NO+的电子式为________。
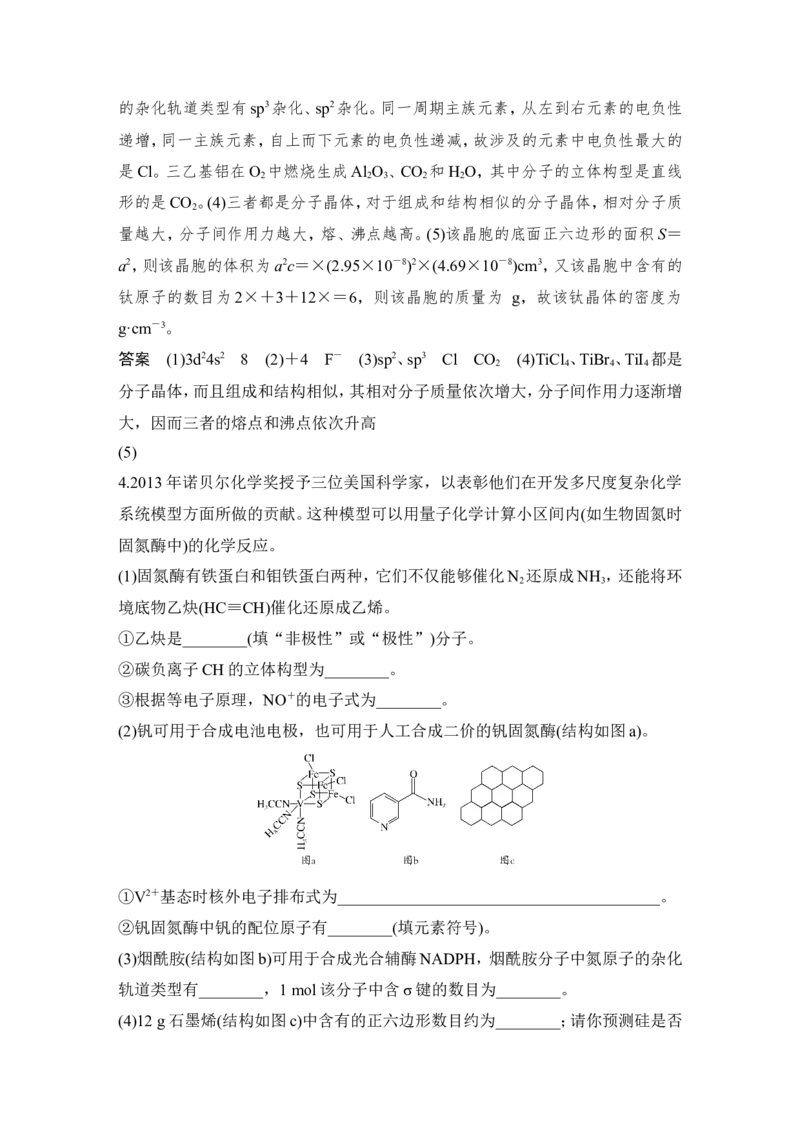
(2)钒可用于合成电池电极,也可用于人工合成二价的钒固氮酶(结构如图a)。
①V2+基态时核外电子排布式为________________________________________。
②钒固氮酶中钒的配位原子有________(填元素符号)。
(3)烟酰胺(结构如图b)可用于合成光合辅酶NADPH,烟酰胺分子中氮原子的杂化
轨道类型有________,1 mol该分子中含σ键的数目为________。
(4)12 g石墨烯(结构如图c)中含有的正六边形数目约为________;请你预测硅是否容易形成类似石墨烯的结构,并说明理由:_______________________________
_____________________________________________________________________
。
解析 (1)①乙炔的结构简式为CH≡CH,为四原子直线对称结构,为非极性分子
②CH的价层电子对数为3+×(4+1-3×1)=4,故CH的立体构型为三角锥形。
③NO+与N 为等电子体,故电子式为[∶N⋮⋮O∶]+。
2
(2)②根据图a可知V的配位原子为N和S。
(3)根据图b可知—N===为sp2杂化, 为sp3杂化。
(4)石墨烯中形成大π键成正六边形结构,而Si的原子半径较大,较难成π键,故不
易形成类似石墨烯的结构。
答案 (1)①非极性 ②三角锥形 ③[∶N⋮⋮O∶]+
(2)①1s22s22p63s23p63d3 (或[Ar]3d3) ②S、N
(3)sp2、sp3 15N
A
(4)0.5N 不容易,硅原子半径大,3p轨道不易形成π键
A