文档内容
1.化学与传统文化、STSE、阿伏加德罗常数的应用
题组一 化学与传统文化 、STSE
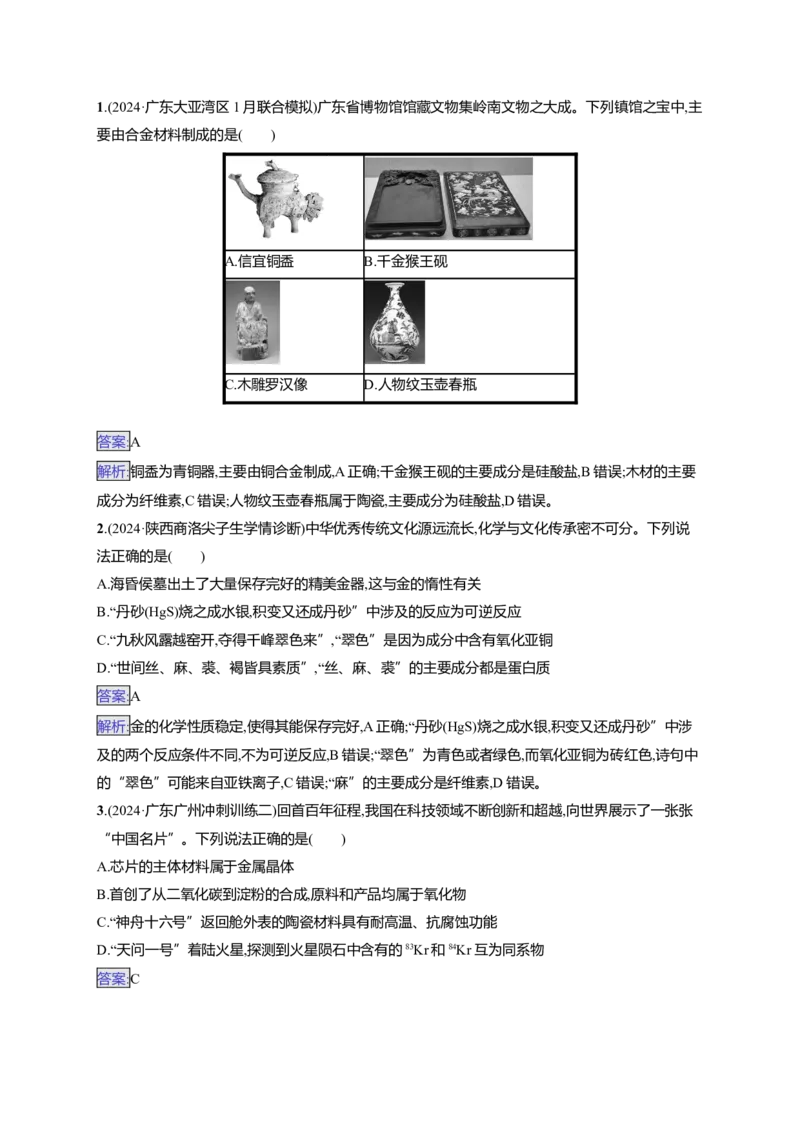
1.(2024·广东大亚湾区1月联合模拟)广东省博物馆馆藏文物集岭南文物之大成。下列镇馆之宝中,主
要由合金材料制成的是( )
A.信宜铜盉 B.千金猴王砚
C.木雕罗汉像 D.人物纹玉壶春瓶
2.(2024·陕西商洛尖子生学情诊断)中华优秀传统文化源远流长,化学与文化传承密不可分。下列说
法正确的是( )
A.海昏侯墓出土了大量保存完好的精美金器,这与金的惰性有关
B.“丹砂(HgS)烧之成水银,积变又还成丹砂”中涉及的反应为可逆反应
C.“九秋风露越窑开,夺得千峰翠色来”,“翠色”是因为成分中含有氧化亚铜
D.“世间丝、麻、裘、褐皆具素质”,“丝、麻、裘”的主要成分都是蛋白质
3.(2024·广东广州冲刺训练二)回首百年征程,我国在科技领域不断创新和超越,向世界展示了一张张
“中国名片”。下列说法正确的是( )
A.芯片的主体材料属于金属晶体
B.首创了从二氧化碳到淀粉的合成,原料和产品均属于氧化物
C.“神舟十六号”返回舱外表的陶瓷材料具有耐高温、抗腐蚀功能
D.“天问一号”着陆火星,探测到火星陨石中含有的83Kr和84Kr互为同系物
4.(2024·广东韶关综合测试二)劳动创造美好生活。下列生活、生产活动中,没有运用相应化学原理
的是 ( )
选项 生活、生产活动 化学原理
A 施肥时草木灰和铵态氮肥不能混合使用 KCO 溶液与铵盐发生相互促进的水解
2 3
B 葡萄糖与银氨溶液制银镜 葡萄糖具有还原性
C 液氨常用作制冷剂 液氨汽化时吸收大量的热
D 漂白粉漂白有色物质放置一段时间后效果更好 HCO 酸性强于HClO
2 35.(2024·安徽黄山二模)下列古诗文中蕴含着一定的化学知识或原理,下列有关说法错误的是( )
A.“榆荚只能随柳絮,等闲撩乱走空园”中柳絮的主要成分和棉花相同
B.《物理小识·金石类》:“有硇水(硝酸)者,剪银块投之,则旋而为水”,该过程涉及氧化还原反应
C.“雨过天青云破处,这般颜色做将来”中所描述瓷器的青色不是来自氧化铁
D.“纷纷灿烂如星陨,赫赫喧豗似火攻”中烟花是某些金属的焰色试验,属于化学变化
6.(2024·广东湛江二模)化学渗透在社会生活的各个方面。下列叙述错误的是( )
A.“九章三号”光量子计算原型机所用芯片的主要成分Si能溶于NaOH溶液
B.用于制作飞机轴承的氮化硅陶瓷材料具有耐高温、耐磨蚀等优良性能
C.航天员餐食中的油脂属于天然高分子化合物
D.稀土永磁材料是电子技术通信中的重要材料,稀土元素均为金属元素
题组二 阿伏加德罗常数的应用
7.(2024·黑龙江大庆实验中学模拟)氮化硅陶瓷,被誉为“先进陶瓷材料皇冠上的明珠”。氮化硅
(Si N)可由石英与焦炭在高温的氮气气流中通过以下反应制备:3SiO +6C+2N Si N+6CO。设
3 4 2 2 3 4
N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1 mol SiO 中含2 mol Si—O
2
B.每生成11.2 L CO转移电子数目为N
A
C.2.8 g N 中含有的π键数目为0.2N
2 A
D.0.1 mol Na SiO 晶体中含离子数目小于0.3N
2 3 A
8.(2024·广东佛山质检一)氯碱工业涉及Cl、H、NaOH、NaClO等物质。设N 为阿伏加德罗常数
2 2 A
的值,下列说法错误的是( )
A.1 mol NaOH固体中的离子数目为2N
A
B.1 L 1 mol·L-1的NaClO溶液中,ClO-的数目小于N
A
C.标准状况下,22.4 L的H 和Cl 混合气体,共价键数目为N
2 2 A
D.1 mol Cl 与足量NaOH溶液反应生成NaClO转移电子数为2N
2 A
9.(2024·浙江温州一模)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.18 g H 18 O中含有的中子数为10N
2 A
B.42 g环己烷( )中含有σ键的数目为9N
A
C.标准状况下,22.4 L CHCl 中含有的分子数为N
3 A
D.6.0 g SiO
与足量NaOH溶液反应,所得溶液中SiO2-
的个数为0.1N
2 3 A10.(2024·吉林白山二模)AlN是一种半导体材料,一种制备方法是Al O+N +3C 2AlN+3CO。设
2 3 2
N 为阿伏加德罗常数的值。下列叙述正确的是 ( )
A
A.标准状况下,11.2 L N 含π键数目为0.5N
2 A
B.12 g C(金刚石)含非极性键数目为2N
A
C.每生成1 mol AlN时转移电子数目为6N
A
D.0.1 mol Al O 溶于足量盐酸,溶液中含Al3+数目为0.2N
2 3 A
11.(2024·辽宁沈阳一模)N 表示阿伏加德罗常数,关于硫代硫酸钠和稀硫酸的反应,下列说法中错误的
A
是( )
A.1 mol硫代硫酸钠固体中阴阳离子总数为3N
A
B.100 mL pH=2的HSO 溶液中H+数目为0.002N
2 4 A
C.32 g S 和S 混合物中硫原子数目为N
6 8 A
D.标准状况下,生成22.4 L SO 时,理论上转移的电子数为2N
2 A
12.(2024·安徽安庆二模)苹果醋主要成分有苹果酸(2-羟基丁二酸)、乙酸、二氧化碳和氯化钠等多种
成分。若N 表示阿伏加德罗常数,下列说法正确的是( )
A
A.0.1 mol苹果酸与足量的Na反应,产生0.15 mol氢气
B.60 g乙酸中σ键有8N
A
C.CO
的电子式为O··C··
O
2 ·· ··
D.1 L 1 mol·L-1的NaCl溶液中含有粒子数目为2N
A
13.(2024·陕西渭南质检Ⅰ)高效率和高选择性地将CO 转化为CH 是CO 资源利用的途径之一。有
2 4 2
科研人员通过催化将CO 转化为CH,最高选择性达99.4%。其原理如图所示:
2 4
设N 为阿伏加德罗常数的值,下列说法正确的是 ( )
A
A.44 g CO 中所含非极性键的数目为4N
2 A
B.1 mol CH 中所含电子数和中子数均为10N
4 A
C.途径2生成标准状况下11.2 L CH 时转移电子数为4N
4 A
D.途径1所得产物物质的量之比为1∶1,形成共价键数目为6N
A
1.化学与传统文化、STSE、阿伏加德罗常数的应用
题组一 化学与传统文化 、STSE1.(2024·广东大亚湾区1月联合模拟)广东省博物馆馆藏文物集岭南文物之大成。下列镇馆之宝中,主
要由合金材料制成的是( )
A.信宜铜盉 B.千金猴王砚
C.木雕罗汉像 D.人物纹玉壶春瓶
答案:A
解析:铜盉为青铜器,主要由铜合金制成,A正确;千金猴王砚的主要成分是硅酸盐,B错误;木材的主要
成分为纤维素,C错误;人物纹玉壶春瓶属于陶瓷,主要成分为硅酸盐,D错误。
2.(2024·陕西商洛尖子生学情诊断)中华优秀传统文化源远流长,化学与文化传承密不可分。下列说
法正确的是( )
A.海昏侯墓出土了大量保存完好的精美金器,这与金的惰性有关
B.“丹砂(HgS)烧之成水银,积变又还成丹砂”中涉及的反应为可逆反应
C.“九秋风露越窑开,夺得千峰翠色来”,“翠色”是因为成分中含有氧化亚铜
D.“世间丝、麻、裘、褐皆具素质”,“丝、麻、裘”的主要成分都是蛋白质
答案:A
解析:金的化学性质稳定,使得其能保存完好,A正确;“丹砂(HgS)烧之成水银,积变又还成丹砂”中涉
及的两个反应条件不同,不为可逆反应,B错误;“翠色”为青色或者绿色,而氧化亚铜为砖红色,诗句中
的“翠色”可能来自亚铁离子,C错误;“麻”的主要成分是纤维素,D错误。
3.(2024·广东广州冲刺训练二)回首百年征程,我国在科技领域不断创新和超越,向世界展示了一张张
“中国名片”。下列说法正确的是( )
A.芯片的主体材料属于金属晶体
B.首创了从二氧化碳到淀粉的合成,原料和产品均属于氧化物
C.“神舟十六号”返回舱外表的陶瓷材料具有耐高温、抗腐蚀功能
D.“天问一号”着陆火星,探测到火星陨石中含有的83Kr和84Kr互为同系物
答案:C解析:芯片的主体材料为单质硅,不属于金属晶体,A错误;淀粉属于糖类,不是氧化物,B错误;“神舟十
六号”返回舱外表的陶瓷材料具有耐高温、抗腐蚀的功能,这样才能保证返回舱顺利返回,C正确;
83Kr和84Kr是同种元素的不同核素,互为同位素,D错误。
4.(2024·广东韶关综合测试二)劳动创造美好生活。下列生活、生产活动中,没有运用相应化学原理
的是 ( )
选项 生活、生产活动 化学原理
A 施肥时草木灰和铵态氮肥不能混合使用 KCO 溶液与铵盐发生相互促进的水解
2 3
B 葡萄糖与银氨溶液制银镜 葡萄糖具有还原性
C 液氨常用作制冷剂 液氨汽化时吸收大量的热
D 漂白粉漂白有色物质放置一段时间后效果更好 HCO 酸性强于HClO
2 3
答案:C
解析:A项,施肥时草木灰和铵态氮肥不能混合使用,是因为草木灰中的碳酸根和铵根发生相互促进的
水解,会使氮肥肥效降低;B项,葡萄糖与银氨溶液制银镜,是因为葡萄糖结构中含有醛基,具有还原
性;C项,液氨常用作制冷剂是因为液氨中存在大量的分子间氢键,汽化时需吸收大量的热;D项,漂白
粉漂白有色物质放置一段时间后效果更好,是因为一段时间后,空气中的二氧化碳与漂白粉溶液发生
了反应,溶液中的HClO浓度更大,漂白效果更好;答案选C。
5.(2024·安徽黄山二模)下列古诗文中蕴含着一定的化学知识或原理,下列有关说法错误的是( )
A.“榆荚只能随柳絮,等闲撩乱走空园”中柳絮的主要成分和棉花相同
B.《物理小识·金石类》:“有硇水(硝酸)者,剪银块投之,则旋而为水”,该过程涉及氧化还原反应
C.“雨过天青云破处,这般颜色做将来”中所描述瓷器的青色不是来自氧化铁
D.“纷纷灿烂如星陨,赫赫喧豗似火攻”中烟花是某些金属的焰色试验,属于化学变化
答案:D
解析:柳絮和棉花的主要成分都是纤维素,A正确;“有硇水(硝酸)者,剪银块投之,则旋而为水”,说明硝
酸和银反应,该反应属于氧化还原反应,B正确;瓷器的青色不是来自氧化铁,因为氧化铁是红棕色,不
是青色,C正确;焰色试验属于物理变化,D错误。
6.(2024·广东湛江二模)化学渗透在社会生活的各个方面。下列叙述错误的是( )
A.“九章三号”光量子计算原型机所用芯片的主要成分Si能溶于NaOH溶液
B.用于制作飞机轴承的氮化硅陶瓷材料具有耐高温、耐磨蚀等优良性能
C.航天员餐食中的油脂属于天然高分子化合物
D.稀土永磁材料是电子技术通信中的重要材料,稀土元素均为金属元素
答案:C解析:计算原型机所用芯片的主要成分Si能溶于NaOH溶液,反应原理为Si+2NaOH+H O
2
NaSiO+2H ↑,A正确;用于制作飞机轴承的氮化硅陶瓷材料是耐高温结构陶瓷,属于新型无机非金属
2 3 2
材料,B正确;油脂相对分子质量不是很大,不是高分子化合物,C错误;稀土元素位于过渡金属区,均为
金属元素,D正确。
题组二 阿伏加德罗常数的应用
7.(2024·黑龙江大庆实验中学模拟)氮化硅陶瓷,被誉为“先进陶瓷材料皇冠上的明珠”。氮化硅
(Si N)可由石英与焦炭在高温的氮气气流中通过以下反应制备:3SiO +6C+2N Si N+6CO。设
3 4 2 2 3 4
N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1 mol SiO 中含2 mol Si—O
2
B.每生成11.2 L CO转移电子数目为N
A
C.2.8 g N 中含有的π键数目为0.2N
2 A
D.0.1 mol Na SiO 晶体中含离子数目小于0.3N
2 3 A
答案:C
解析:SiO 中每个Si原子形成4个Si—O,1 mol SiO 中含4 mol Si—O,A错误;未说明气体所处的温度
2 2
和压强,无法计算11.2 L CO的物质的量,B错误;N 中含有氮氮三键,一个三键含有2个π键,2.8 g N
2 2
2.8 g
的物质的量为 =0.1 mol,含有π键数目为0.2N ,C正确;Na SiO 晶体中含有2个Na+和
28 g·mol-1 A 2 3
1个SiO2-
,0.1 mol Na SiO 晶体中含离子数目等于0.3N ,D错误。
3 2 3 A
8.(2024·广东佛山质检一)氯碱工业涉及Cl、H、NaOH、NaClO等物质。设N 为阿伏加德罗常数
2 2 A
的值,下列说法错误的是( )
A.1 mol NaOH固体中的离子数目为2N
A
B.1 L 1 mol·L-1的NaClO溶液中,ClO-的数目小于N
A
C.标准状况下,22.4 L的H 和Cl 混合气体,共价键数目为N
2 2 A
D.1 mol Cl 与足量NaOH溶液反应生成NaClO转移电子数为2N
2 A
答案:D
解析:1 mol NaOH固体中含有1 mol Na+和1 mol OH-,所以离子数目为2N ,A正确;1 L 1 mol·L-1的
A
NaClO溶液中含有1 mol NaClO,但是ClO-会发生水解反应生成HClO,所以ClO-的数目小于N ,B正
A
确;标准状况下,22.4 L的H 和Cl 混合气体为1 mol,H 和Cl 都是双原子分子,所以共价键数目为
2 2 2 2
N ,C正确;Cl 与足量NaOH溶液反应的化学方程式为Cl+2NaOH NaCl+NaClO+H O,反应中Cl
A 2 2 2 2
既是氧化剂又是还原剂,1 mol Cl 参与反应转移1 mol电子,所以转移电子数为N ,D错误。
2 A
9.(2024·浙江温州一模)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.18 g H 18 O中含有的中子数为10N
2 AB.42 g环己烷( )中含有σ键的数目为9N
A
C.标准状况下,22.4 L CHCl 中含有的分子数为N
3 A
D.6.0 g SiO
与足量NaOH溶液反应,所得溶液中SiO2-
的个数为0.1N
2 3 A
答案:B
m 18 g m 42 g
= =
解析:n= =0.9 mol,则中子数为9N ,A错误;n= =0.5 mol,1个
M 20 g·mol-1 A M 84 g·mol-1
环己烷中含有18个σ键,则42 g环己烷中含有σ键的数目为9N ,B正确;标准状况下,CHCl 为液体,
A 3
无法根据体积计算物质的量,C错误;二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,硅酸钠在溶液中
m 6.0 g
发生水解反应,根据原子守恒,n(Si)=
=
=0.1
mol,则SiO2-
个数小于0.1N ,D错误。
M 60 g·mol-1 3 A
10.(2024·吉林白山二模)AlN是一种半导体材料,一种制备方法是Al O+N +3C 2AlN+3CO。设
2 3 2
N 为阿伏加德罗常数的值。下列叙述正确的是 ( )
A
A.标准状况下,11.2 L N 含π键数目为0.5N
2 A
B.12 g C(金刚石)含非极性键数目为2N
A
C.每生成1 mol AlN时转移电子数目为6N
A
D.0.1 mol Al O 溶于足量盐酸,溶液中含Al3+数目为0.2N
2 3 A
答案:B
解析:1个N 分子含2个π键,标准状况下,11.2 L N 的物质的量为0.5 mol,含1N π键,A错误;12 g C的
2 2 A
1
物质的量为1 mol,含1 mol×4× =2 mol非极性键,即非极性键数目为2N ,B正确;根据反应式可知,生
2 A
成1 mol AlN时转移3 mol电子,转移电子数目为3N ,C错误;Al3+会水解,0.1 mol Al O 溶于足量盐酸,
A 2 3
溶液中含Al3+数目小于0.2N ,D错误。
A
11.(2024·辽宁沈阳一模)N 表示阿伏加德罗常数,关于硫代硫酸钠和稀硫酸的反应,下列说法中错误的
A
是( )
A.1 mol硫代硫酸钠固体中阴阳离子总数为3N
A
B.100 mL pH=2的HSO 溶液中H+数目为0.002N
2 4 A
C.32 g S 和S 混合物中硫原子数目为N
6 8 A
D.标准状况下,生成22.4 L SO 时,理论上转移的电子数为2N
2 A
答案:B
解析:NaSO
中阳离子为Na+、阴离子为SO2-
,1 mol Na SO 中含2 mol Na+和1 mol
SO2-
,1 mol硫
2 2 3 2 3 2 2 3 2 3
代硫酸钠固体中阴阳离子总物质的量为3 mol,总数为3N ,A项正确;100 mL pH=2的HSO 溶液中
A 2 4
n(H+)=0.01 mol·L-1×0.1 L=0.001 mol,H+数目为0.001N ,B项错误;32 g S 和S 混合物中n(S)=
A 6 832 g
=1 mol,含硫原子数目为N ,C项正确;硫代硫酸钠与稀硫酸的反应为NaSO+H SO
32 g·mol-1 A 2 2 3 2 4
NaSO +S↓+SO ↑+H O,反应中生成1 mol SO 转移2 mol电子,标准状况下22.4 L SO 物质的量为
2 4 2 2 2 2
1 mol,则理论上转移电子数为2N ,D项正确。
A
12.(2024·安徽安庆二模)苹果醋主要成分有苹果酸(2-羟基丁二酸)、乙酸、二氧化碳和氯化钠等多种
成分。若N 表示阿伏加德罗常数,下列说法正确的是( )
A
A.0.1 mol苹果酸与足量的Na反应,产生0.15 mol氢气
B.60 g乙酸中σ键有8N
A
C.CO
的电子式为O··C··
O
2 ·· ··
D.1 L 1 mol·L-1的NaCl溶液中含有粒子数目为2N
A
答案:A
解析:已知苹果酸(2-羟基丁二酸)中含有一个羟基和两个羧基,故0.1 mol苹果酸与足量的Na反应,产
3×0.1
生 mol=0.15 mol氢气,A正确;一分子乙酸中含有7个σ键,故60 g乙酸中σ键有
2
60 g ·· ··
×7×N mol-1=7N ,B错误;CO 为共价化合物,故CO 的电子式为O ··C·· O ,C错
60 g·mol-1 A A 2 2 ·· ··
·· ··
误;由于NaCl溶液中含有水分子、H+、Na+、Cl-和OH-等微粒,故1 L 1 mol·L-1的NaCl溶液中含有粒
子数目大于2N ,D错误。
A
13.(2024·陕西渭南质检Ⅰ)高效率和高选择性地将CO 转化为CH 是CO 资源利用的途径之一。有
2 4 2
科研人员通过催化将CO 转化为CH,最高选择性达99.4%。其原理如图所示:
2 4
设N 为阿伏加德罗常数的值,下列说法正确的是 ( )
A
A.44 g CO 中所含非极性键的数目为4N
2 A
B.1 mol CH 中所含电子数和中子数均为10N
4 A
C.途径2生成标准状况下11.2 L CH 时转移电子数为4N
4 A
D.途径1所得产物物质的量之比为1∶1,形成共价键数目为6N
A
答案:C
解析:CO 的结构式为O C O,44 g CO 物质的量为1 mol,所含极性键的数目为4N ,A错误;1 mol
2 2 A
CH 中所含电子数为10N ,所含中子数为6N ,B错误;途径2中CO~CH ~8e-,生成标准状况下11.2 L
4 A A 2 4
CH 时转移电子数为0.5N ×8=4N ,C正确;不知道所得产物物质的量,无法计算共价键数目,D错误。
4 A A