文档内容
第 2 讲 离子反应 离子方程式
[复习目标] 1.了解电解质及其分类,掌握强弱电解质的本质区别。2.理解电解质在水溶液
中的电离以及电解质溶液的导电性。3.了解离子反应的概念、离子反应发生的条件,并能正
确书写离子方程式以及判断离子能否大量共存。
考点一 离子反应与离子大量共存的判断
1.电解质的概念
(1)概念
在____________或____________能够导电的化合物,称为电解质,二者情况下均不导电的化
合物称为非电解质。
(2)分类
电解质
[应用举例]
现有11种物质:①锂 ②纯HPO ③氨水 ④NH ⑤BaSO ⑥NaCl固体 ⑦NaCl溶
3 4 3 4
液 ⑧乙醇 ⑨Al O ⑩AlCl ⑪CuSO ·5H O
2 3 3 4 2
按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
序号 符合的条件 物质的序号
(1) 本身能导电
(2) 电解质,熔融状态能导电
(3) 电解质,水溶液中能导电
(4) 非电解质
(5) 强电解质
(6) 弱电解质
2.电离方程式
强电解质在水溶液中完全电离,用“===”连接。
弱电解质在水溶液中部分电离,用“”连接,多元弱酸分步电离,一般以第一步电离为
主;多元弱碱,分步电离,一步完成。
[应用举例]
按要求书写下列电解质的电离方程式:
①Ba(OH) :_____________________________________________________________;
2②KAl(SO ):___________________________________________________________;
4 2
③CHCOOH:___________________________________________________________;
3
④HCO:_______________________________________________________________;
2 3
⑤Cu(OH) :_____________________________________________________________;
2
⑥NaHSO 溶于水:_______________________________________________________;
4
⑦NaHSO 熔融:_________________________________________________________;
4
⑧NaHCO :_____________________________________________________________
3
________________________________________________________________________。
3.离子反应
(1)概念:有离子参加或有离子生成的反应统称为离子反应。
(2)本质:离子反应的本质是溶液中某些离子的物质的量的减少。
(3)常见离子反应的类型
一、离子共存判断集锦
1.几种离子在同一溶液中能发生上述任何一种类型的离子反应,都不能大量共存。
判断下列溶液中离子一定能大量共存的有哪些?
(1)使酚酞溶液变红的溶液:Na+、Cl-、SO、Fe3+
(2)使紫色石蕊溶液变红的溶液:Fe2+、Mg2+、NO、Cl-
(3)常温下,c(H+)=1×10-13 mol·L-1的溶液中:NH、Al3+、SO、NO
(4)碳酸氢钠溶液:K+、SO、Cl-、H+
(5)含大量Fe3+的溶液:NH、Na+、Cl-、SCN-
(6)强碱溶液:Na+、K+、AlO、CO
(7)常温下,pH=1的溶液:K+、Fe2+、Cl-、NO
(8)加入铝粉有氢气产生的溶液:K+、Na+、CO、SO
(9)由水电离出的c (H+)=1×10-12 mol·L-1的溶液:Na+、K+、Cl-、NO
水(10)c(H+)∶c(OH-)=1∶10-2的溶液:K+、Ba2+、ClO-、CO
(11)澄清透明的溶液:Fe3+、Mg2+、Br-、Cl-
2.强氧化性与强还原性的离子(或分子)在溶液中会发生氧化还原反应不能大量共存。
判断下表中所列离子能否发生氧化还原反应,能反应的打“√”,不能反应的打“×”。
S2- SO I- Fe2+ Br- Cl-
MnO(H+)
ClO- __(酸性)
NO(H+) — —
Fe3+
3.(1)判断下列几组离子能否大量共存,不能大量共存的说明理由。
①Na+、Fe2+、NO、SO:_______________________________________________。
②H+、Fe2+、NO、SO:________________________________________________
________________________________________________________________________。
③向含有Fe2+、Cl-、Na+、H+的溶液中滴入HO:__________________________
2 2
________________________________________________________________________。
(2)S2-与SO,Cl—与ClO-在碱性条件下能否大量共存:________(填“能”或“不能”)。写
出上述两组离子在酸性条件下反应的离子方程式:__________________________、
________________________________________________________________________。
二、离子反应过程中溶液导电性变化分析
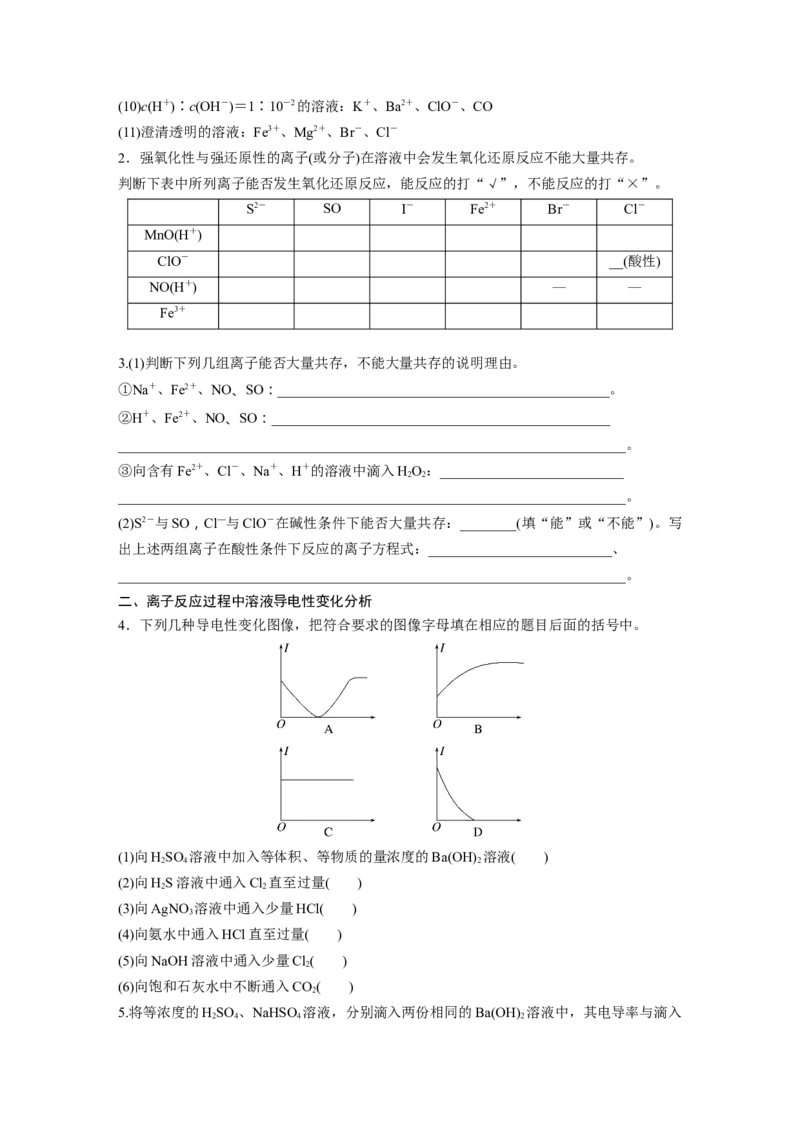
4.下列几种导电性变化图像,把符合要求的图像字母填在相应的题目后面的括号中。
(1)向HSO 溶液中加入等体积、等物质的量浓度的Ba(OH) 溶液( )
2 4 2
(2)向HS溶液中通入Cl 直至过量( )
2 2
(3)向AgNO 溶液中通入少量HCl( )
3
(4)向氨水中通入HCl直至过量( )
(5)向NaOH溶液中通入少量Cl( )
2
(6)向饱和石灰水中不断通入CO( )
2
5.将等浓度的HSO 、NaHSO 溶液,分别滴入两份相同的Ba(OH) 溶液中,其电导率与滴入
2 4 4 2溶液体积变化的曲线如图所示。下列分析正确的是( )
A.b→d反应的离子方程式为H++OH-===HO
2
B.d点溶液中,Na+与SO的物质的量之比为1∶1
C.c点导电能力相同,所以两溶液中含有相同量的OH-
D.a、b两点Ba2+均沉淀完全,所以对应的溶液均显中性
电解质溶液导电原理及影响因素
(1)导电原理
电解质电离出的阴、阳离子在外加电场的作用下,发生定向移动实现导电过程。
(2)影响因素
①离子浓度:一般情况下,自由移动的离子浓度越大,所带电荷数越多,电解质溶液导电能
力越强。
②离子种类:离子浓度相同时,不同离子导电能力不同。
③溶液温度:一般情况下,温度升高,电解质溶液导电能力增强。
考点二 离子方程式的书写及正误判断
1.离子方程式
(1)概念:用________________________来表示反应的式子。
(2)意义:离子方程式不仅可以表示____________________________,还可以表示
________________________。
2.离子方程式中物质的“拆分”原则
(1)一般原则:能拆分写成离子形式的物质是易溶的强电解质,包括________、________、
大多数____________。除此之外的物质不能拆分。
(2)酸式酸根的拆分
①强酸的酸式酸根如硫酸氢根离子(HSO)在水溶液中拆分成“H+”和“SO”。
②多元弱酸的酸式酸根不能拆分,如HCO、HSO、HC O等。
2
(3)微溶物的拆分①微溶物作为产物视为沉淀,不拆分。
②作反应物时,澄清溶液中,微溶物拆分为离子,浑浊液中微溶物不拆分,如Ca(OH) 。
2
(4)产物NH ·H O的拆分
3 2
①不加热或稀溶液中,写成“NH ·H O”。
3 2
②加热或浓溶液中,写成“NH ↑”和“HO”。
3 2
3.离子方程式规范书写的基本要求
(1)符合事实:离子反应要符合客观事实,不可臆造产物及反应。
(2)方程式正确:化学式与离子使用正确合理。
(3)符号正确:“===” “↑”“↓”等使用正确。
(4)三个守恒:两边原子数、电荷数必须守恒,氧化还原反应离子方程式中氧化剂得电子总
数与还原剂失电子总数要相等。
一、常见离子方程式的书写
1.完成下列反应的离子方程式:
(1)注意氧化物、难溶物质、气体、难电离物质的书写形式。
①过氧化钠溶于水
________________________________________________________________________。
②向AlCl 溶液中滴加过量的氨水
3
________________________________________________________________________。
③Cl 溶于水
2
________________________________________________________________________。
④向NaHSO 溶液中加入过量NaHSO 溶液
3 4
________________________________________________________________________。
(2)注意微溶物质、NH与碱反应的条件。
①向澄清石灰水中加入稀盐酸
________________________________________________________________________。
②NaSO 溶液与AgNO 溶液混合
2 4 3
________________________________________________________________________。
③铵盐溶液与强碱溶液混合加热检测NH
________________________________________________________________________。
(3)注意单质、浓酸的拆分(浓硫酸、浓磷酸不拆分)。
①用MnO 与浓盐酸共热制Cl
2 2
________________________________________________________________________。
②铜溶于浓硝酸
________________________________________________________________________。二、多重反应离子方程式的书写
2.完成下列反应的离子方程式。
(1)Ba(OH) 溶液与HSO 溶液混合
2 2 4
________________________________________________________________________。
(2)Ba(OH) 溶液与(NH )SO 溶液混合
2 4 2 4
________________________________________________________________________。
(3)CuSO 溶液与Ba(OH) 溶液混合
4 2
________________________________________________________________________。
三、“四角度”判断离子方程式的正误
3.能正确表示下列反应的离子方程式的打“√”,不能的打“×”。
(1)从“拆分”视角判断
①食醋去除水垢中的CaCO :CaCO +2H+===Ca2++HO+CO↑(2023·北京,6B)( )
3 3 2 2
②HSO 溶液中滴入氯化钙溶液:SO+Ca2+===CaSO↓(2023·浙江1月选考,7D)( )
2 3 3
③向氢氧化钡溶液中加入盐酸:H++OH-===HO(2021·湖北,4A)( )
2
④向硝酸银溶液中滴加少量碘化钾溶液:Ag++I-===AgI↓(2021·湖北,4B)( )
⑤过氧化物转化为碱:2O+2HO===4OH-+O↑(2022·广东,14C)( )
2 2
⑥电解饱和食盐水:2Cl-+2H+=====Cl↑+H↑(2018·江苏,7D)( )
2 2
(2)从原理的视角
①Cl 制备84消毒液(主要成分是NaClO):Cl +2OH-===Cl-+ClO-+HO(2023·北京,6A)(
2 2 2
)
②SO 与KClO溶液反应:SO +2ClO-+HO===2HClO+SO(2021·辽宁,4D)( )
2 2 2
③乙醇与KCr O 酸性溶液反应:3CHCHOH+2Cr O+16H+―→3CHCOOH+4Cr3++
2 2 7 3 2 2 3
11HO(2022·浙江6月选考,13C)( )
2
④向0.1 mol·L-1NaCO 溶液中通入CO,溶液pH从12下降到约为9,反应的离子方程式为:
2 3 2
CO+HO+CO===2HCO(2021·江苏,11C)( )
2 2
⑤溴与冷的NaOH溶液反应:Br +OH-===Br-+BrO-+H+(2022·浙江6月选考,13D)(
2
)
(3)从是否符合“三守恒”的视角
①利用覆铜板制作印刷电路板:2Fe3++Cu===2Fe2++Cu2+(2023·北京,6C)( )
②用铝粉和NaOH溶液反应制取少量H:Al+2OH-===AlO+H↑(2019·江苏,7B)( )
2 2
③NaOH溶液与I 反应的离子方程式:I+2OH-===I-+IO+HO(2021·江苏,9A)( )
2 2 2
④酸性硫酸亚铁溶液在空气中被氧化:4Fe2++O +4H+===4Fe3++2HO(2017·浙江11月选
2 2
考,12C)( )
⑤高锰酸钾与浓盐酸制氯气的反应:MnO+4Cl-+8H+===Mn2++2Cl↑+4HO(2018·浙江
2 2
4月选考,13B)( )⑥钠与水反应:Na+2HO===Na++2OH-+H↑(2017·江苏,6A)( )
2 2
(4)从是否符合指定用量关系的视角
①氢氧化钠溶液与过量的碳酸氢钙溶液反应:OH-+Ca2++HCO===CaCO ↓+HO(2018·浙
3 2
江4月选考,13D)( )
②0.1 mol·L-1 NaAlO 溶液中通入过量CO :AlO+CO +2HO===Al(OH) ↓+HCO(2020·江
2 2 2 2 3
苏,7C)( )
③0.1 mol·L-1 AgNO 溶液中加入过量浓氨水:Ag++NH +HO===AgOH↓+NH(2020·江
3 3 2
苏,7D)( )
④NaHCO 溶液与少量的Ba(OH) 溶液混合:HCO+Ba2++OH-===BaCO ↓+HO(2022·湖
3 2 3 2
南,11D)( )