文档内容
第 43 讲 电解原理应用新拓展
[复习目标] 1.深化对电解原理及规律的理解,提升应用电解原理综合分析解决实际问题的
能力。2.熟知电解原理创新试题的呈现方式及问题设置,总结解答此类问题的一般方法及规
律。
1.电解原理常见的考查点
电解原理及应用是高考高频考点,该类试题往往与生产、生活及新科技等相联系,以装置图
或流程图为载体呈现,题材广、信息新,题目具有一定难度。主要考查阴、阳极的判断、电
极反应式及电解反应方程式的书写、溶液离子浓度变化及有关计算等。
2.“5点”突破电解综合应用题
(1)分清阴、阳极,与电源正极相连的为阳极,与电源负极相连的为阴极,两极反应为“阳
氧阴还”。
(2)剖析离子移向,阳离子移向阴极,阴离子移向阳极。(注意离子交换膜会限制某些离子的
移动方向)
(3)注意放电顺序,正确判断放电的微粒或物质。
(4)注意介质,正确判断反应产物,酸性介质不出现OH-,碱性介质不出现H+;不能想当然
地认为金属作阳极,电极产物为金属阳离子。
(5)注意得失电子守恒和电荷守恒,正确书写电极反应式。
类型一 电解与物质制备
1.(2023·浙江1月选考,11)在熔融盐体系中,通过电解TiO 和SiO 获得电池材料(TiSi),
2 2
电解装置如图,下列说法正确的是( )
A.石墨电极为阴极,发生氧化反应
B.电极A的电极反应:8H++TiO+SiO+8e-===TiSi+4HO
2 2 2
C.该体系中,石墨优先于Cl-参与反应
D.电解时,阳离子向石墨电极移动
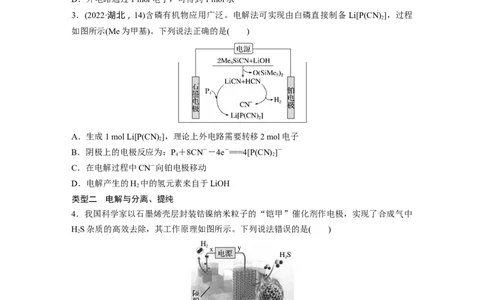
2.(2022·重庆,12)硝酮是重要的有机合成中间体,可采用“成对间接电氧化”法合成。电
解槽中水溶液的主要成分及反应过程如图所示。下列说法错误的是( )
A.惰性电极2为阳极
B.反应前后WO、WO数量不变
C.消耗1 mol氧气,可得到1 mol硝酮
D.外电路通过1 mol电子,可得到1 mol水
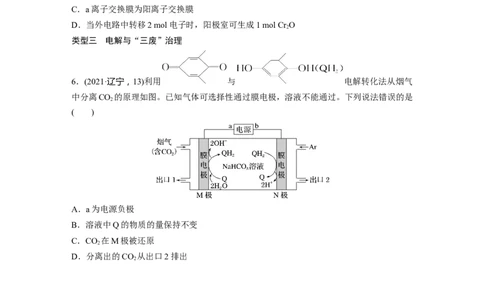
3.(2022·湖北,14)含磷有机物应用广泛。电解法可实现由白磷直接制备 Li[P(CN)],过程
2
如图所示(Me为甲基)。下列说法正确的是( )
A.生成1 mol Li[P(CN) ],理论上外电路需要转移2 mol电子
2
B.阴极上的电极反应为:P+8CN--4e-===4[P(CN) ]-
4 2
C.在电解过程中CN-向铂电极移动
D.电解产生的H 中的氢元素来自于LiOH
2
类型二 电解与分离、提纯
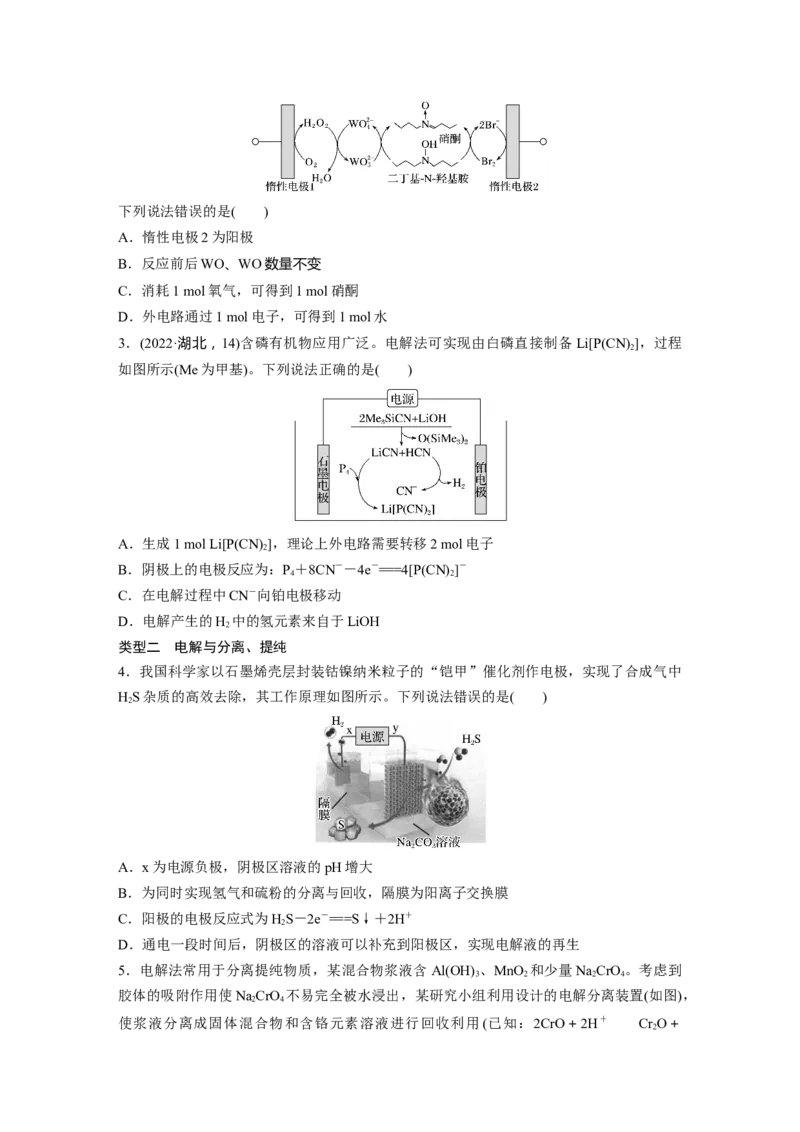
4.我国科学家以石墨烯壳层封装钴镍纳米粒子的“铠甲”催化剂作电极,实现了合成气中
HS杂质的高效去除,其工作原理如图所示。下列说法错误的是( )
2
A.x为电源负极,阴极区溶液的pH增大
B.为同时实现氢气和硫粉的分离与回收,隔膜为阳离子交换膜
C.阳极的电极反应式为HS-2e-===S↓+2H+
2
D.通电一段时间后,阴极区的溶液可以补充到阳极区,实现电解液的再生
5.电解法常用于分离提纯物质,某混合物浆液含 Al(OH) 、MnO 和少量NaCrO 。考虑到
3 2 2 4
胶体的吸附作用使NaCrO 不易完全被水浸出,某研究小组利用设计的电解分离装置(如图),
2 4
使浆液分离成固体混合物和含铬元素溶液进行回收利用(已知:2CrO+2H+Cr O+
2HO),下列说法不正确的是( )
2
A.阴极室生成的物质为NaOH和H
2
B.阳极发生的电极反应是2HO-4e-===4H++O↑
2 2
C.a离子交换膜为阳离子交换膜
D.当外电路中转移2 mol电子时,阳极室可生成1 mol Cr O
2
类型三 电解与“三废”治理
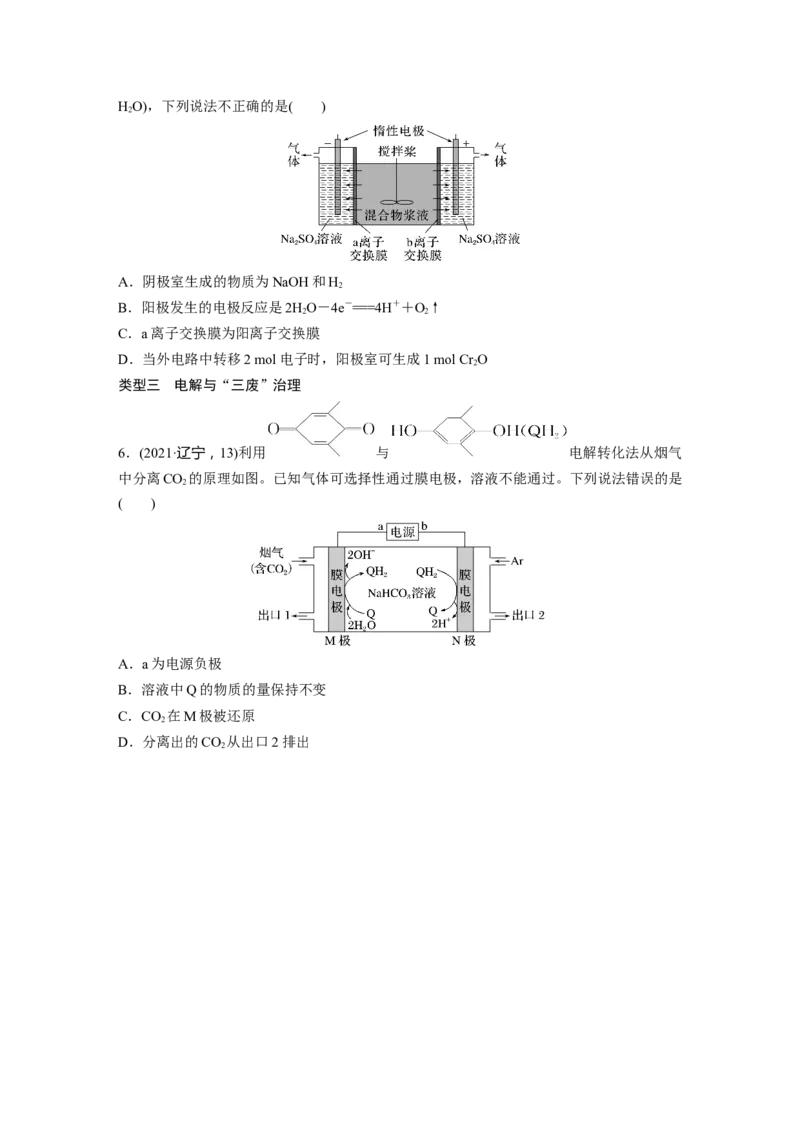
6.(2021·辽宁,13)利用 与 电解转化法从烟气
中分离CO 的原理如图。已知气体可选择性通过膜电极,溶液不能通过。下列说法错误的是
2
( )
A.a为电源负极
B.溶液中Q的物质的量保持不变
C.CO 在M极被还原
2
D.分离出的CO 从出口2排出
2