文档内容
微专题 09 “守恒法”在氧化还原反应计算中的应用
一、在高中化学计算中通常要遵循三大守恒规律:
1.得失电子守恒
2.质量守恒
3.电荷守恒
二、守恒思想在氧化还原反应计算中的应用
1.对于氧化还原反应的计算,要根据氧化还原反应的实质——反应中氧化剂得到的电子
总数与还原剂失去的电子总数相等,即得失电子守恒。利用守恒的思想,可以抛开繁琐
的反应过程,可不写化学方程式,不追究中间反应过程,只要把物质分为始态和终态,
从得电子和失电子两个方面进行整体思维,便可迅速获得正确结果。
2.守恒法解题的思维流程
(1)找出氧化剂、还原剂及相应的还原产物和氧化产物。
(2)找准一个原子或离子得失电子数(注意化学式中粒子的个数)。
(3)根据题中物质的物质的量和得失电子守恒列出等式。n(氧化剂) 变价原子个数 化
合价变化值(高价-低价)= n(还原剂) 变价原子个数 化合价变化值(高价-低价)
三、考查角度
(1)考查两元素之间得失电子守恒计算
【典型精析】
1.关于反应 ,
下列说法正确的是
A. 中C的化合价为
B.反应中 和 表现氧化性
C.氧化剂与还原剂的物质的量之为5∶2
D.氧化产物与还原产物的物质的量之为5∶12.在标准状况下将3.84g铜粉投入一定量浓HNO 中,随着铜粉的溶解,反应生成的气体
3
颜色逐渐变浅,当铜粉完全溶解后共收集到由NO 和NO组成的混合气体1.12L,则反应
2
消耗HNO 的物质的量为
3
A.0.17mol B.0.15mol C.0.12mol D.无法计算
(2)考查多步反应得失电子守恒计算
3.硫代硫酸钠(Na SO 是一种解毒药,用于氟化物、砷、汞、铅、锡、碘等中毒,临床
2 2 3)
常用于治疗荨麻疹,皮肤瘙痒等病症.硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液
中分解产生S和SO
2
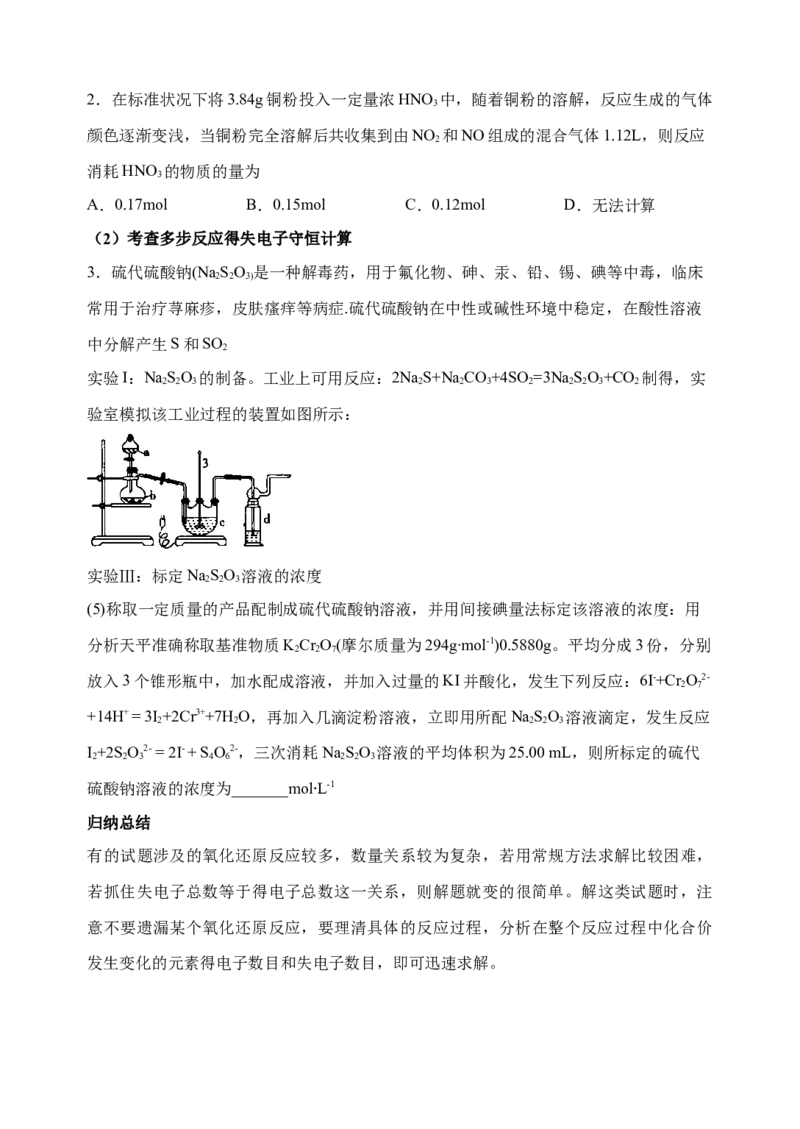
实验I:NaSO 的制备。工业上可用反应:2NaS+Na CO+4SO=3Na SO+CO 制得,实
2 2 3 2 2 3 2 2 2 3 2
验室模拟该工业过程的装置如图所示:
实验Ⅲ:标定NaSO 溶液的浓度
2 2 3
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用
分析天平准确称取基准物质KCr O(摩尔质量为294g∙mol-1)0.5880g。平均分成3份,分别
2 2 7
放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr O2-
2 7
+14H+ = 3I+2Cr3++7H O,再加入几滴淀粉溶液,立即用所配NaSO 溶液滴定,发生反应
2 2 2 2 3
I+2S O2- = 2I- + S O2-,三次消耗 NaSO 溶液的平均体积为25.00 mL,则所标定的硫代
2 2 3 4 6 2 2 3
硫酸钠溶液的浓度为_______molL-1
归纳总结 ∙
有的试题涉及的氧化还原反应较多,数量关系较为复杂,若用常规方法求解比较困难,
若抓住失电子总数等于得电子总数这一关系,则解题就变的很简单。解这类试题时,注
意不要遗漏某个氧化还原反应,要理清具体的反应过程,分析在整个反应过程中化合价
发生变化的元素得电子数目和失电子数目,即可迅速求解。【实战演练】
1.关于反应8NH +6NO =7N +12H O,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为4:3
D.氧化产物与还原产物的质量之比为3:4
2.已知KMnO +8HCl(浓) 2KCl+MnCl +2Cl↑+4H O,下列说法正确的是
2 4 2 2 2
A.KMnO 发生氧化反应
2 4
B.还原剂为MnCl
2
C.氧化剂与还原剂的物质的量之比为1∶8
D.当有0.4molHCl被氧化时,产生Cl 的体积(标准状况下)为4.48L
2
3.Cu在稀硝酸中可以发生反应:3Cu +8HNO(稀)=3Cu(NO) +2NO↑+4H O,下列叙述正
3 3 2 2
确的是
A.HNO 在反应中失去电子
3
B.氧化产物与还原产物的物质的量之比为2∶3
C.发生氧化反应的硝酸占参加反应的硝酸的
D.每1molHNO 参加反应,有 mol电子转移
3
4.关于反应 ,下列说法不正确的是
A.硫元素既被氧化又被还原
B.氧化剂与还原剂的物质的量之比为2:1
C.每生成1mol ,转移8mol电子
D.相同条件下,每吸收5 就会放出1.255.FeS与一定量的稀硝酸反应,生成的Fe(NO )、Fe (SO )、NO和HO,当反应完全时,
3 3 2 4 3 2
实际参加的硝酸与生成的NO的物质的量之比为
A. B. C. D.
6.将标准状况下44.8 L仅含NO和NO 混合气体的尾气通入NaCO 溶液中,发生的反应
2 2 3
为:NO +NO+Na CO=2NaNO +CO ;2NO +2Na CO=NaNO +NaNO +CO 。气体被完全
2 2 3 2 2 2 2 3 2 3 2
吸收,则消耗的NaCO 的物质的量为
2 3
A.2 mol B.3 mol C.1.5 mol D.1 mol
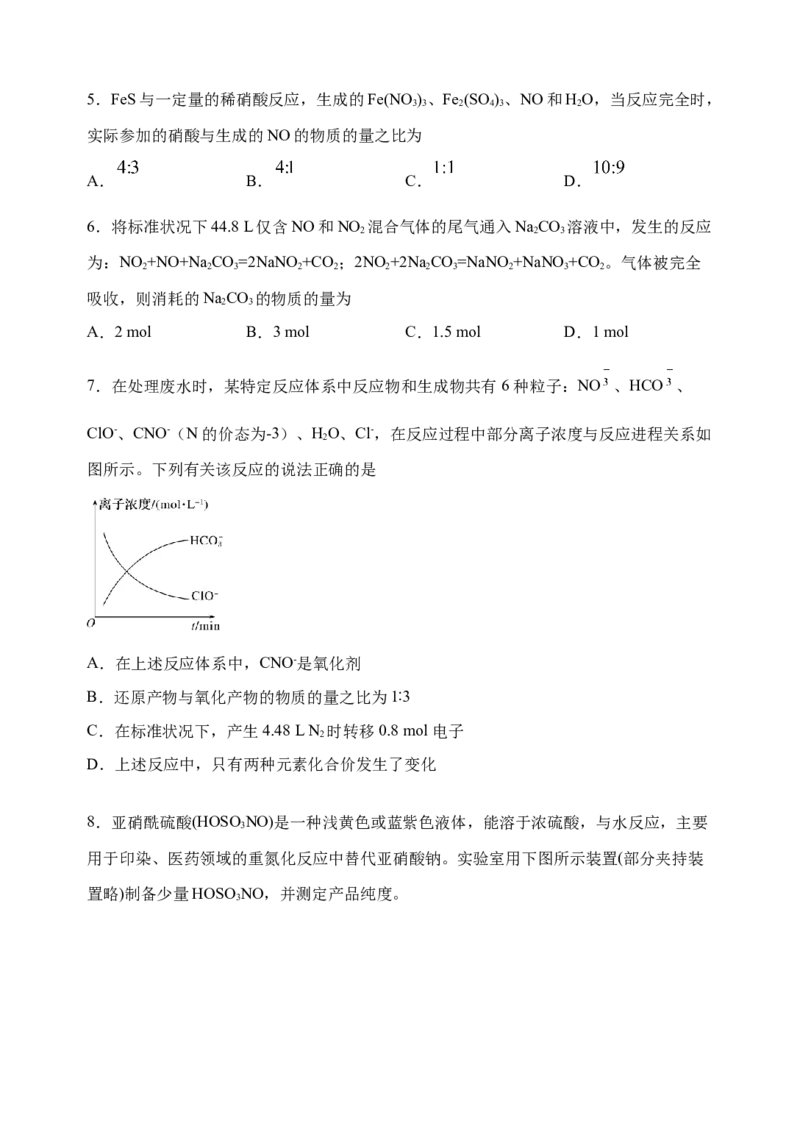
7.在处理废水时,某特定反应体系中反应物和生成物共有 6 种粒子:NO 、HCO 、
ClO-、CNO-(N 的价态为-3)、HO、Cl-,在反应过程中部分离子浓度与反应进程关系如
2
图所示。下列有关该反应的说法正确的是
A.在上述反应体系中,CNO-是氧化剂
B.还原产物与氧化产物的物质的量之比为1∶3
C.在标准状况下,产生 4.48 L N 时转移 0.8 mol 电子
2
D.上述反应中,只有两种元素化合价发生了变化
8.亚硝酰硫酸(HOSONO)是一种浅黄色或蓝紫色液体,能溶于浓硫酸,与水反应,主要
3
用于印染、医药领域的重氮化反应中替代亚硝酸钠。实验室用下图所示装置(部分夹持装
置略)制备少量HOSONO,并测定产品纯度。
3(5)测定HOSONO的纯度:准确称取1.350 g产品放入250 mL碘量瓶中,加入60.00 mL
3
0.1000 mol•L-1 KMnO 标准溶液和10 mL 25%硫酸溶液,摇匀(过程中无气体产生);用
4
0.2500 mol•L-1草酸钠标准溶液滴定,平均消耗草酸钠标准溶液的体积为20.00 mL。已知:
2KMnO +5HOSONO+2HO=KSO +2MnSO +5HNO+2HSO 。
4 3 2 2 4 4 3 2 4
①上述反应中,HOSONO体现了_______(填“氧化”或“还原”)性。
3
②亚硝酰硫酸的纯度为_______(计算结果保留4位有效数字)。