文档内容
微专题24 H O 性质“四重性”探究及应用
2 2
1.过氧化氢
(1)结构
(2)化学式:HO
2 2
(3)电子式:
(4)结构式:H—O—O—H
H、O原子个数比为1∶1,HO 是既含极性键,又含非极性键的共价化合物。
2 2
(5)物理性质
水溶液为无色透明液体,溶于水、醇、乙醚,不溶于苯、石油醚。
纯过氧化氢是淡蓝色的粘稠液体,熔点-0.43 °C,沸点 150.2 °C,纯的过氧化氢其分子构
型会改变,所以熔沸点也会发生变化。凝固点时固体密度为1.71g/,密度随温度升高而减
小。它的缔合程度比H₂O大,所以它的介电常数和沸点比水高。纯过氧化氢比较稳定,
加热到153 °C便猛烈的分解为水和氧气,值得注意的是,过氧化氢中不存在分子间氢键。
(6)化学性质
Ⅰ.不稳定性:2HO=====2HO+O↑。
2 2 2 2
加热、光照或加催化剂都能使分解加快,因此HO 应保存在棕色瓶中并放置在阴凉处。
2 2
Ⅱ.弱还原性:遇强氧化剂时,显还原性, HO 中-1价的氧遇强氧化剂可失去电子转化
2 2
成0价氧而被氧化。
2KMnO +5HO+3HSO ===K SO +2MnSO +5O↑+8HO
4 2 2 2 4 2 4 4 2 2
Ⅲ.强氧化性:遇较强还原剂时,显氧化性。
①在工业上用10%的HO 漂白羽毛及丝织品,在医疗上用3%的HO 做为消毒杀菌剂;
2 2 2 2
②氧化Fe2+、SO等还原性物质:
HO+2Fe2++2H+===2Fe3++2HO,HO+NaSO ===Na SO +HO;
2 2 2 2 2 2 3 2 4 2③使湿润的淀粉KI试纸变蓝:HO+2I-+2H+===I +2HO
2 2 2 2
Ⅳ.弱酸性:相当于二元弱酸
过氧化氢是一种极弱的酸:HO H++HO (Ka=2.4×10-12);
2 2
HO H+ + O
【专题精练】
1.过氧化氢( )俗称双氧水,其分子结构如图所示。医疗上常用3%的双氧水进行
伤口或中耳炎消毒。过氧化氢能与 反应生成 .下列有关过氧化氢的说法中错误
的是( )
A. 的结构式为
B.过氧化氢与 的化合反应,不是氧化还原反应
C. 为既含有极性键又含有非极性键的共价化合物
D.过氧化氢与 反应的离子方程式为
2.为探究过氧化氢分解反应快慢的影响因素,某学习小组设计了下列实验:
实验① 实验② 实验③下列说法不正确的是
A.对比实验①和②,可研究催化剂对化学反应快慢的影响
B.对比实验①和③,可研究升温对过氧化氢分解反应快慢的影响
C.综合实验②和③,可得出过氧化氢分解制氧气的最佳反应条件
D.综合实验①、②和③,可得出5%的过氧化氢溶液最适合用于分解制氧气
3.100℃时,在不同金属离子存在下,过氧化氢经过24h的分解率如下表所示:
加入量(mg·L- 加入量(mg·L-
离子 分解率/% 离子 分解率/%
1) 1)
无 2 Fe2+ 1.0 15
Cu2
Al3+ 10 2 0.1 86
+
Zn2+ 10 10 Cr3+ 0.1 96
下列有关说法正确的是
A.能使过氧化氢分解反应活化能降低最多的离子是Al3+
B.催化剂可以使平衡移动,提高过氧化氢的分解率
C.若向过氧化氢中加入水,过氧化氢的分解速率加快
D.用等量HO 制O 时,与自身分解相比,加入足量酸性KMnO 溶液可得到更多O
2 2 2 4 2
4.以下四个反应均有过氧化氢参与(未配平),请填写下列空格
A.NaO+HCl——H O+NaCl B.Ag O+HO——Ag+O+H O
2 2 2 2 2 2 2 2 2
C.HO+Cr (SO )+KOH——K CrO+K SO +H O D.HO——HO+O
2 2 2 4 3 2 4 2 4 2 2 2 2 2
(1)过氧化氢仅体现氧化性的反应是__________
(2)过氧化氢既体现氧化性又体现还原性的反应是__________________(3)过氧化氢体现弱酸性的反应是______,其理由是__________________。
5.过氧化物是一类非常重要的化合物,从人们制得第一种过氧化物距今已有200多年的
历史了,在众多的过氧化物中过氧化氢迄今为止仍然得到广泛的应用。
(1)与HO 具有相同的电子总数的双原子分子有_______(写两种);
2 2
(2)若从海水中提取碘,需将碘化物变成单质碘。写出在酸性条件下HO 氧化I-离子的离
2 2
子方程式_______;
(3)NaO、KO、CaO 和BaO 都能与酸作用生成HO,目前实验室制取HO 可通过上述
2 2 2 2 2 2 2 2 2 2
某种过氧化物与适量的稀HSO 作用并过滤后获得,其中最适合的过氧化物是_______(填
2 4
化学式);
(4)纯HO 可用作火箭燃料的氧化剂,已知0.4mol液态肼(N H)与足量的液态HO 反应,
2 2 2 4 2 2
生成N(g)和HO(g),放出256.6kJ的热量,则该反应的热化学方程式是_______。
2 2
6.HO 是在医疗、化工方面应用广泛的化学试剂。
2 2
⑴ NaO、CaO 以及BaO 都可与酸发生复分解反应生成过氧化氢。实验室通过上述某种
2 2 2 2
过氧化物与适量稀硫酸作用,过滤后即可制得较纯净的HO 溶液,则应选择的过氧化物
2 2
是__________;发生反应的化学方程式为:_______________________。
⑵ 双氧水可消除采矿业废液中的氰化物(如KCN,其中N为-3价),反应的化学方程
式为:KCN + H O + H O===A + NH↑
2 2 2 3
① 生成物A的化学式为_________。
② 在标准状况下有0.448 L氨气生成,则转移的电子数为______________。
⑶ HO 中氧元素的化合价处于中间价,既有氧化性又有还原性。
2 2
酸化的HO 溶液中滴入KI淀粉溶液,溶液变蓝,发生反应的离子方程式为__________。
2 2
向NaClO溶液中滴入HO,可产生O,发生反应的离子方程式为:_______________。
2 2 2
⑷ 用酸性KMnO 溶液滴定法可测定双氧水中HO 的含量,有两位同学分别用以下化学
4 2 2
方程式表示其中的反应原理:
① 5HO + 2KMnO + 3H SO ===2MnSO + K SO + 5O ↑ + 8H O
2 2 4 2 4 4 2 4 2 2
② 3HO + 2KMnO + 3H SO ===2MnSO + K SO + 4O ↑ + 6H O
2 2 4 2 4 4 2 4 2 2
你认为其中错误的是__________(若认为没有,本小题的两个空可以不填),简述理由_____________________________________________________________。
7.过氧化氢的水溶液俗称双氧水,它的用途很广,常用于消毒、杀菌、漂白等。试回答
下列问题:
(1)过氧化氢属于________(极性/非极性)分子。
(2)NaO,KO 以及BaO 都可与酸作用生成过氧化氢,目前实验室制取过氧化氢溶液
2 2 2 2 2
可取上述某种过氧化物与适量稀硫酸作用,然后经_______操作即可制得,则上述最适合
的过氧化物是________。
(3)几乎所有古代艺术家的油画都是以铅白2PbCO ·Pb(OH) 为底色,但若空气中含HS
3 2 2
气体,铅白就会变黑,可以用HO 将黑色物氧化成颜色相近的PbSO 而修复,写出铅白
2 2 4
在空气中变黑的化学方程式________。
(4)甲酸钙[Ca(HCOO) ]广泛用于食品工业生产上,实验室制取甲酸钙的方法之一是将
2
氢氧化钙和甲醛溶液依次加入到质量分数为30%-70%的过氧化氢溶液中,
①则该反应的化学方程式为____________________,
②过氧化氢比理论用量稍多,其目的是_____。
③反应温度最好控制在30 -70℃,温度不易过高,其主要原因是_____________________。
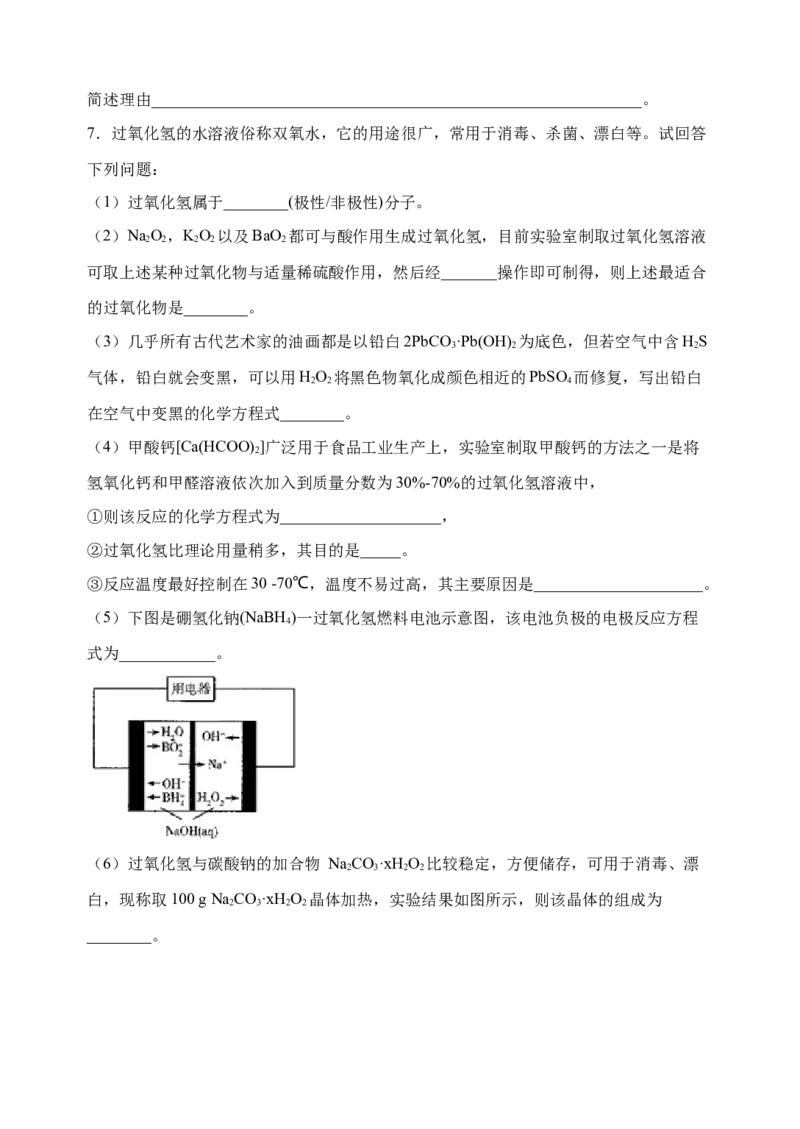
(5)下图是硼氢化钠(NaBH )一过氧化氢燃料电池示意图,该电池负极的电极反应方程
4
式为____________。
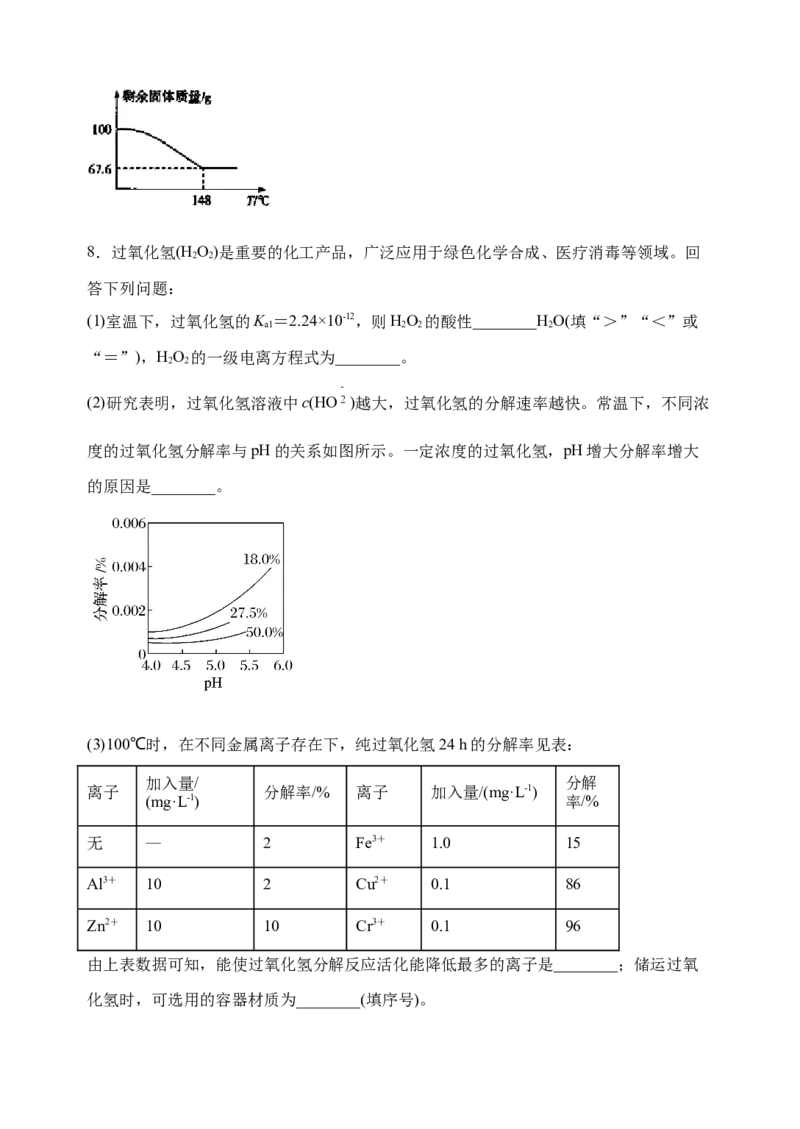
(6)过氧化氢与碳酸钠的加合物 NaCO·xH O 比较稳定,方便储存,可用于消毒、漂
2 3 2 2
白,现称取100 g Na CO·xH O 晶体加热,实验结果如图所示,则该晶体的组成为
2 3 2 2
________。8.过氧化氢(H O)是重要的化工产品,广泛应用于绿色化学合成、医疗消毒等领域。回
2 2
答下列问题:
(1)室温下,过氧化氢的K =2.24×10-12,则HO 的酸性________HO(填“>”“<”或
a1 2 2 2
“=”),HO 的一级电离方程式为________。
2 2
(2)研究表明,过氧化氢溶液中c(HO )越大,过氧化氢的分解速率越快。常温下,不同浓
度的过氧化氢分解率与pH的关系如图所示。一定浓度的过氧化氢,pH增大分解率增大
的原因是________。
(3)100℃时,在不同金属离子存在下,纯过氧化氢24 h的分解率见表:
加入量/ 分解
离子 分解率/% 离子 加入量/(mg·L-1)
(mg·L-1) 率/%
无 — 2 Fe3+ 1.0 15
Al3+ 10 2 Cu2+ 0.1 86
Zn2+ 10 10 Cr3+ 0.1 96
由上表数据可知,能使过氧化氢分解反应活化能降低最多的离子是________;储运过氧
化氢时,可选用的容器材质为________(填序号)。A.不锈钢 B.黄铜 C.纯铝 D.铸铁
9.某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过
氧化氢的性质。请填写下列空白:
Ⅰ.测定过氧化氢的含量
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL_______(填仪器名称)中,
加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫
酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为________。
(3)判断滴定到达终点的现象是_________________________。
(4)重复滴定三次,平均耗用c mol/L KMnO 标准溶液V mL,则原过氧化氢溶液中过氧
4
化氢的质量分数为____________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏
高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性
和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化
氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
实验内容 实验方法 实验现象
验证氧化性 ____________ ____________
验证不稳定性 ____________ ____________
10.HO 是重要的化学试剂,在实验室和生产实际中应用广泛。
2 2
(1)写出HO 的结构式:,HO 在MnO 催化下分解的化学方程式:
2 2 2 2 2
_____________________________________________________。
(2)①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入HO 后,则可使铜顺利溶解,写
2 2
出该反应的离子方程式:_____________________________________________________。②在“海带提碘”的实验中,利用酸性HO 得到碘单质的离子方程式是
2 2
_____________________________________________________。
③你认为HO 被称为绿色氧化剂的主要原因是
2 2
_____________________________________________________。
(3)H O 还有一定的还原性,能使酸性KMnO 溶液褪色。
2 2 4
①写出反应的离子方程式:_____________________________________________________。
②实验室常用酸性KMnO 标准液测定溶液中HO 的浓度,酸性KMnO 溶液应盛放在
4 2 2 4
__________________________(填“酸式”或“碱式”)滴定管中,判断到达滴定终点的
现象是。
(4)H O 是一种二元弱酸,写出其第一步电离的方程式:它与过量的Ba(OH) 反应的化学
2 2 2
方程式为_____________________________________________________。