文档内容
微专题30 无机框图推断题常见突破口
一、题型特点
无机推断题具有明显的化学学科特点,是现在每年高考理综卷的必考题型,是将基本概
念、基本理论、元素单质及其重要化合物知识与化学实验及简单计算有机结合起来的综
合题型。在高三复习中抓住无机推断题,不仅能进一步加深元素及其化合物的有关知识,
还能培养分析推理、观察思维、获取信息及综合应用的能力。
二、解题策略
无论推断题属于哪种形式,均遵循这样的推断思路:迅速浏览、整体扫描、产生印象、
寻找“突破口”,突破点由点到面、随时检验,注意联系、大胆假设、全面分析(正推或
逆推),验证确认。解题的关键是仔细审题,依物质的特性或特征转化来确定“突破口”,
顺藤摸瓜,进而完成全部未知物的推断。我们可以将推断题的解题方法及推理过程表示
如下:
推断题――→――→――→结论―→验证
三、解题“突破口”
1.以“物质的特殊颜色”为突破口
相关知识:
(1)有色固体
①红色:Cu、Cu O、Fe O;
2 2 3
②红褐色:Fe(OH) ;
3
③黄色:AgI、Ag PO ;
3 4
④浅黄色:S、NaO 或AgBr;
2 2
⑤蓝色:Cu(OH) ;
2
⑥黑色:炭粉、CuO、FeO、FeS、CuS、Ag S、PbS;
2
⑦紫黑色:KMnO 、I;
4 2
⑧白色:Fe(OH) 、CaCO 、BaSO、AgCl、BaSO。
2 3 4 3
(2)有色溶液:
Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)、MnO(紫红色)、Fe3+与苯酚(紫色)、Fe3+与SCN-
(红色)、I 与淀粉(蓝色)等。
2
水(溶剂) 苯(溶剂) CCl (溶剂)
4
Br 黄→橙 黄→红棕
2I 深黄→褐 淡紫→紫红 紫→深紫
2
(3)有色气体:
Cl(黄绿色)、Br (g)(红棕色)、NO (红棕色)、I(g)(紫色)、O(淡蓝色)等。
2 2 2 2 3
(4)火焰颜色:
①焰色反应:Na+(黄色)、K+(紫色)、Ca2+(砖红色)等;②蓝色:CO在空气中燃烧;
③淡蓝色:S、H、HS、CH 等在空气中燃烧;④苍白色:H 在Cl 中燃烧。
2 2 4 2 2
2.以“物质的特征性质”为突破口
相关知识
(1)能使品红溶液褪色的气体:
SO (加热后又恢复红色)、Cl(加热后不恢复红色)。
2 2
(2)沉淀特殊的颜色变化:
①白色沉淀先变灰绿色,再变红褐色:Fe(OH) ――→Fe(OH) ;
2 3
②白色沉淀迅速变棕褐色:AgOH→Ag O。
2
(3)在空气中变为红棕色:NO(无色)――→NO (红棕色)。
2
(4)能使澄清石灰水变浑浊的气体:CO、SO 。
2 2
(5)通入CO 气体变浑浊的溶液:石灰水(过量则变澄清)、NaSiO 溶液、饱和NaCO 溶液、
2 2 3 2 3
浓苯酚钠溶液、NaAlO 溶液等。
2
(6)使湿润的红色石蕊试纸变蓝的气体:NH 。
3
(7)使湿润的淀粉碘化钾试纸变蓝:NO 、Cl、Br 、FeCl 等。
2 2 2 3
(8)能与SO 、Cl 、O 等氧化性较强的气体(或其水溶液)反应析出淡黄色沉淀:HS。
2 2 2 2
(9)在一定条件下具有漂白性的物质:NaO、HO、SO 、氯水、O、活性炭等。
2 2 2 2 2 3
(10)能溶解SiO 固体的物质:氢氟酸和NaOH溶液。
2
(11)能与浓硫酸、铜片共热产生红棕色气体(NO)的溶液:硝酸盐(或硝酸)溶液。
2
(12)滴入沸水中可得到红褐色胶体的溶液:含Fe3+的盐溶液。
(13)烟雾现象:
①棕(黄)色的烟:Cu或Fe在Cl 中燃烧;
2
②白烟:Na在Cl 或P在空气中燃烧;NH 遇到HCl气体;
2 3
③白雾:由HX等极易溶于水的气体产生;
④白色烟雾:P在Cl 燃烧。
2
3.以“物质之间的特征转化关系”为突破口
相关知识:
(1)连续氧化反应:A――→B――→C――→D(酸或碱)。①NH (g)――→N――→NO――→NO ――→HNO;
3 2 2 3
②HS(g)――→S――→SO ――→SO ――→HSO ;
2 2 3 2 4
③CH(g)――→C――→CO――→CO――→HCO;
4 2 2 3
④Na(s)――→NaO――→NaO――→2NaOH。
2 2 2
(2)
X可能为弱酸的铵盐:(NH )CO 或NH HCO ;(NH )S或NH HS;(NH )SO 或NH HSO
4 2 3 4 3 4 2 4 4 2 3 4 3
等。
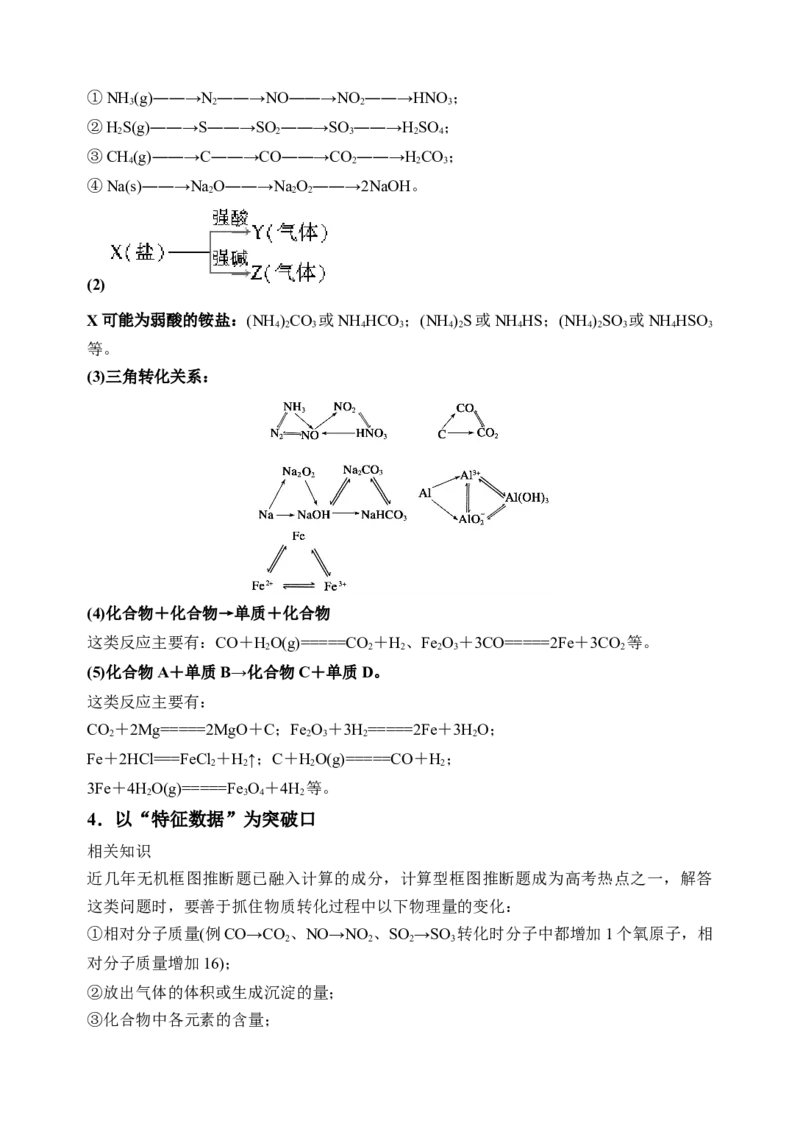
(3)三角转化关系:
(4)化合物+化合物→单质+化合物
这类反应主要有:CO+HO(g)=====CO+H、Fe O+3CO=====2Fe+3CO 等。
2 2 2 2 3 2
(5)化合物A+单质B→化合物C+单质D。
这类反应主要有:
CO+2Mg=====2MgO+C;Fe O+3H=====2Fe+3HO;
2 2 3 2 2
Fe+2HCl===FeCl +H↑;C+HO(g)=====CO+H;
2 2 2 2
3Fe+4HO(g)=====Fe O+4H 等。
2 3 4 2
4.以“特征数据”为突破口
相关知识
近几年无机框图推断题已融入计算的成分,计算型框图推断题成为高考热点之一,解答
这类问题时,要善于抓住物质转化过程中以下物理量的变化:
①相对分子质量(例CO→CO 、NO→NO 、SO →SO 转化时分子中都增加1个氧原子,相
2 2 2 3
对分子质量增加16);
②放出气体的体积或生成沉淀的量;
③化合物中各元素的含量;④气体的相对密度;
⑤离子化合物中离子个数之比;
⑥反应物之间的物质的量之比;
⑦电子总数;
⑧质子总数等。
(1)常见10电子微粒及相互转化关系:
①分子:Ne、HF、HO、NH 、CH;
2 3 4
②阳离子:Na+、Mg2+、Al3+、NH、HO+;
3
③阴离子:F-、O2-、N3-、OH-、NH等。其相互转化关系为NH+OH-=====NH ↑+
3
HO;HO++OH-===2H O等。
2 3 2
(2)常见18电子微粒
①分子:Ar、HCl、HS、PH、SiH、HO;
2 3 4 2 2
②阳离子:K+、Ca2+;
③阴离子:Cl-、S2-、P3-、O;
④有机物:CHOH、CHNH 、CHF、CHCH 等。
3 3 2 3 3 3
(3)常见物质的相对分子质量:
①相对分子质量为28的物质:CO、N、C H 等;
2 2 4
②相对分子质量为26的物质:C H 等;
2 2
③相对分子质量为32的物质:S、O 等;
2
④相对分子质量为78的物质:NaS、NaO、Al(OH) 等;
2 2 2 3
⑤相对分子质量为100的物质:CaCO 、KHCO 、MgN 等。
3 3 3 2
5.以“特征的分子结构”为突破口
相关知识
中学教材中涉及的一些典型物质的分子结构:
①直线形:三原子分子(如CO、CS);多原子分子(如C H 等);
2 2 2 2
②平面形:C H(苯)、C H(乙烯)等;
6 6 2 4
③三角锥形:NH 、PH 、HO+等;
3 3 3
④正四面体形:CH、CX(X=F、Cl、Br、I)、P(白磷)、NH等;
4 4 4
6.以“特殊的工业生产”为突破口
相关知识
中学教材中涉及的重要工业生产反应:
①煅烧石灰石;②工业制水煤气;③工业生产硫酸;④合成氨工业;⑤硝酸的生产工业;⑥氯碱工业(电解饱和食盐水);⑦工业制盐酸;⑧高炉炼铁;⑨工业制取漂粉精;⑩硅酸
盐工业等。
【专题精练】
1.A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组
成空气的成分。化合物F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个
数比为1∶2。在一定条件下,各物质之间的相互转化关系如下图(图中部分产物未列出):
请填写下列空白:
(1)A是__________,C是________。
(2)H与盐酸反应生成E的化学方程式是______________________________________。
(3)E与F反应的化学方程式是_____________________________________________。
(4)F与G的水溶液反应生成I和D的离子方程式是___________________________
________________________________________________________________________。
【答案】
(1)碳(或C) 钠(或Na)
(2)Na CO+2HCl===2NaCl+HO+CO↑
2 3 2 2
(3)2CO +2NaO===2Na CO+O
2 2 2 2 3 2
(4)Na O+S2-+2HO===4OH-+S↓+2Na+
2 2 2
【解析】
本题的突破口为“化合物F的焰色反应呈黄色”,则F含有Na+,从而可知单质B、C中
有一种为Na,结合B、E均为组成空气的成分,可确定C为Na,B为O ,E为CO ,那
2 2
么F为NaO 。E(CO)与F(Na O)反应生成H和B(O),则H为NaCO 。由C(Na)和D反
2 2 2 2 2 2 2 3
应生成化合物G,G中非金属元素与金属元素的原子个数比为1∶2,则G中D元素显-2
价,应为ⅥA族,由原子序数的大小关系确定D为S,G为NaS。利用氧化还原反应知
2
识,可推测F(Na O)能将G(Na S)氧化成D(S)。
2 2 2
2.中学化学中几种常见物质的转化关系如下:将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:[来源:学,科,
网]
(1)红褐色胶体中F粒子直径大小的范围:_____________________________________。
(2)写出A、B、H的化学式:A______、B________、H________。
(3)①HO 分子的电子式:_________________________________________________。
2 2
②写出C的酸性溶液与双氧水反应的离子方程式:
________________________________________________________________________。
(4)写出鉴定E中阳离子的实验方法和现象:__________________________________
________________________________________________________________________
________________________________________________________________________。
(5)在C溶液中加入与C等物质的量的NaO,恰好使C转化为F,写出该反应的离子方程
2 2
式:_____________________________________________________________________。
【答案】
(1)1 nm~100 nm (2)Fe FeS HSO (稀)
2 4
(3)① ②2Fe2++HO+2H+===2Fe3++2HO
2 2 2
(4)取少量E于试管中,用胶头滴管滴入NaOH溶液,加热试管,可观察到试管口处湿润
的红色石蕊试纸变蓝(或其他合理答案)
(5)4Fe2++4NaO+6HO===4Fe(OH) ↓+O↑+8Na+
2 2 2 3 2
【解析】
本题的突破口为“D溶液滴入沸水中可得到以F为分散质的红褐色胶体”,可推断D溶
液中含有Fe3+,进而推知A为Fe,B为FeS,C为FeSO ,D为Fe (SO ),F为Fe(OH) ,
4 2 4 3 3
H为HSO 。因为F为胶体分散系,则其粒子直径大小为1nm~100nm。C为FeSO ,具
2 4 4
有还原性,与双氧水发生氧化还原反应:2Fe2++HO +2H+===2Fe3++2HO。E中阳离
2 2 2
子为NH,其检验方法为利用NH与OH-在加热条件下产生的NH ,然后利用湿润的红色
3
石蕊试纸检验(变蓝色)或用蘸有浓盐酸的玻璃棒靠近试管口,看是否有白烟产生。
3.已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图
所示:(1)D的化学式是____________,E的化学式是________。
(2)A和B反应生成C的化学方程式是_______________________________________。
(3)E和F反应生成D、H和G的化学方程式是_______________________________
________________________________________________________________________。
【答案】
(1)NH NH Cl (2)H +Cl=====2HCl
3 4 2 2
(3)2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO
4 2 2 3 2
【解析】
本题的突破口为“D(气体)→E(固体)→D(气体)”这一系列转化过程,可联想到中学化学中
“氨气→铵盐→氨气”这一转化过程,据此可推测D为NH ,结合G为CaCl ,可知E为
3 2
NH Cl,F为Ca(OH) 。其余物质可以逐一确定:A为H(或Cl),B为Cl(或H),C为
4 2 2 2 2 2
HCl,H为HO。
2
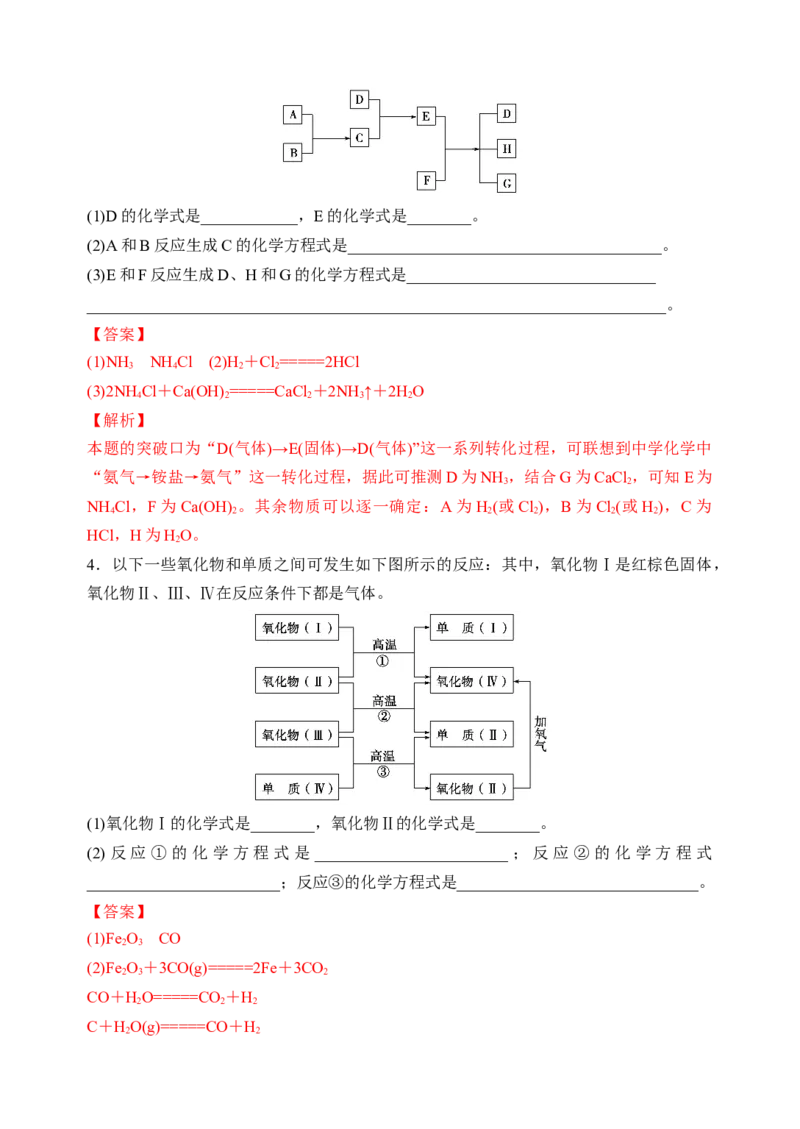
4.以下一些氧化物和单质之间可发生如下图所示的反应:其中,氧化物Ⅰ是红棕色固体,
氧化物Ⅱ、Ⅲ、Ⅳ在反应条件下都是气体。
(1)氧化物Ⅰ的化学式是________,氧化物Ⅱ的化学式是________。
(2)反应①的化学方程式是 ________________________;反应②的化学方程式
________________________;反应③的化学方程式是______________________________。
【答案】
(1)Fe O CO
2 3
(2)Fe O+3CO(g)=====2Fe+3CO
2 3 2
CO+HO=====CO+H
2 2 2
C+HO(g)=====CO+H
2 2【解析】
本题的突破口为①特殊反应条件——均在高温条件下进行;②氧化物Ⅰ是红棕色固体,
即Fe O 固体。中学阶段涉及物质在高温条件下进行的反应有:CaCO 的分解,C、CO与
2 3 3
HO(g),SiO 与C,硅酸盐工业,热还原法冶炼金属等。由氧化物Ⅱ加氧气可得氧化物Ⅳ
2 2
知,氧化物Ⅱ为还原性气体,结合上述分析可推测氧化物Ⅱ为 CO,氧化物Ⅳ为CO ,由
2
反应③为高温置换反应推测该反应为C+HO(g)=====CO+H。
2 2
5.下图中每一方框的字母代表一种反应物或生成物:
已知气态烃D(其密度在同温同压下是氢气密度的13倍)跟物质F反应时产生明亮而带浓
烟的火焰。请写出下列字母代表的物质的化学式(分子式):
A________、B________、C________、D__________、
E__________、H__________。
【答案】
CaC HO Ca(OH) C H CO Ca(HCO )
2 2 2 2 2 2 3 2
【解析】
据同温同压下,两气体的密度之比等于其相对分子质量之比,可计算出气态烃 D的相对
分子质量为26,即D为C H 。根据D与F反应时产生明亮而带浓烟的火焰,可推断F为
2 2
O 。由D+F→E+B(C H +O→CO +HO)、A+B→C+D[CaC +HO→Ca(OH) +C H]
2 2 2 2 2 2 2 2 2 2 2
可确定A、B、C、E分别为CaC 、HO、Ca(OH) 、CO 。进而可确定G为CaCO 、H为
2 2 2 2 3
Ca(HCO )。
3 2
6.下图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,
H、G是正四面体结构的非极性分子,H是一种重要的能源,J是一种耐高温材料,K是
由两种常见元素组成的化合物(图中部分反应物或生成物没有列出)。
请按要求回答:(1)写出B的化学式____________________,G的电子式________________。
(2)反应①的离子方程式为__________________________________________________。
(3)反应②进行的条件是____________、______________________________________。
(4)反应③的化学方程式为_________________________________________________。
【答案】
(1)Al
(2)Al3++3AlO+6HO===4Al(OH) ↓
2 3
(3)光照 过量Cl
2
(4)AlC +12HO===3CH ↑+4Al(OH) ↓
4 3 2 4 3
【解析】
由H、G是正四面体形结构的非极性分子,H是一种重要的能源,可确定H为CH,再结
4
合H+Cl→G,推断G为CCl ,则A为HCl。日常生活中常见的金属主要有Fe、Al等,
2 4
再结合化学课本上介绍过的一种耐高温材料Al O ,可大胆推测B可能是Al。把Al带入
2 3
框图分析,便可逐一推出其他物质。反应①的离子方程式为Al3++3AlO+6HO===4Al
2
(OH) ↓;反应②进行的条件是光照、过量 Cl ;反应③的化学方程式为 Al C +
3 2 4 3
12HO===4Al(OH) ↓+3CH↑。
2 3 4
7.下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的HO
2
已略去),已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。
(b)反应①、②是化工生产中的重要反应。
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。
(d)化合物L具有漂白性,可由Cl 与NaOH溶液反应而制得。
2
(e)化合物J由两种元素组成,其相对分子质量为32。请按要求填空:
(1)反应③的化学方程式为_________________________________________________。
(2)C的结构式为________________;H的化学式为________________。
(3)L的溶液与化合物E反应的离子方程式为_________________________________
________________________________________________________________________。
(4)化合物J的化学式为__________________________________________________。
【答案】
(1)2NH +HSO ===(NH)SO
3 2 4 4 2 4
(2) (NH )SO 或NH HSO
4 2 3 4 3
(3)ClO-+SO +2OH-===Cl-+SO+HO
2 2
(4)N H
2 4
【解析】
本题的突破口为(1)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体,且
反应①②是化工生产中的重要反应;(2)化合物E是形成酸雨的污染物之一。考虑中学教
材中涉及的化工生产原理,可知反应①为硫酸工业的基础反应(S+O 的反应),从而推断,
2
A为S,B为O ,E为SO 。化合物的K是常用的氮肥,应为铵盐,则K为(NH )SO ,F
2 2 4 2 4
为NH ,反应②为合成氨反应。化合物L具有漂白性,可由Cl 与NaOH溶液反应制得,
3 2
则L为NaClO,与NH 反应生成相对分子质量为32的化合物J,J能被B(O)氧化为C,
3 2
前后联系可推测C为N,D为H,J为NH。
2 2 2 4