文档内容
微专题突破3 新情景方程式的书写
一、选择题
1.(2024·湖北卷)过量SO 与以下0.1 mol·L-1的溶液反应,下列总反应方程式错误的是
2
溶液 现象 化学方程式
A NaS 产生淡黄色沉淀 3SO +2NaS=3S↓+2NaSO
2 2 2 2 3
B FeCl 溶液由棕黄色变浅绿色 2FeCl +SO +2HO=2FeCl +HSO +2HCl
3 3 2 2 2 2 4
SO +2CuCl +2HO=2CuCl↓+HSO +
C CuCl 溶液褪色,产生白色沉淀 2 2 2 2 4
2 2HCl
D NaCO(含酚酞) 溶液由红色变无色 2SO +NaCO+HO=CO+2NaHSO
2 3 2 2 3 2 2 3
A.A B.B C.C D.D
2.(2024·江苏镇江市高三开学考)ⅤA族氮、磷、砷(As)、锑(Sb)元素及其化合物应用广泛。氨
是重要的化工原料,广泛用于生产铵盐、硝酸、纯碱、医药等;肼(NH)的燃烧热为624 kJ·mol-1,是
2 4
常用的火箭燃料。白磷(P)晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸(HPO )为一元弱酸,
4 3 2
HPO 为三元中强酸。锑是带有银色光泽的灰色金属,铅锑合金一般用作铅蓄电池的负极材料。
3 4
下列化学反应表示正确的是
A.肼燃烧的热化学方程式:NH(l)+O(g)=N(g)+2HO(g) ∆H=-624 kJ·mol-1
2 4 2 2 2
B.NO 与水反应:3NO +HO=2H++2NO -+NO
2 2 2 3
C.次磷酸与足量NaOH溶液反应:HPO +3NaOH=NaPO +3HO
3 2 3 2 2
D.铅蓄电池放电时的负极反应:Pb-2e—=Pb2+
3.(2024·连云港一模)周期表中ⅡA族元素及其化合物应用广泛。铍的化合物性质与铝相似,
BeO的熔点为2 575℃,熔融时BeF 能导电,而BeCl 不能导电;Mg的燃烧热为610 kJ·mol-1,实验室
2 2
中常用酸性KMnO 测定物品中不溶性CaC O 的含量。铍镍合金可用于制造弹簧秤的弹簧,BaSO 可用作
4 2 4 4
隔音材料,CaO可用作工业废气脱硫剂。下列化学反应表示正确的是
A.BeO与NaOH溶液反应:BeO+NaOH=NaBeO+HO
2 2
B.镁的燃烧:2Mg(s)+O(g)=2MgO(s) ∆H=-610 kJ·mol-1
2
C.向Mg(HCO ) 溶液中滴加足量NaOH溶液:Mg2++2HCO -+4OH-=Mg(OH)↓+2CO2-+
3 2 3 2 3
2HO
2
D.用酸性KMnO 测定CaC O 的含量:5C O2-+2MnO -+16H+=2Mn2++10CO↑8HO
4 2 4 2 4 4 2 2
4.(2024·徐州上学期期中)NaSO-Co O 可作为光催化水生产物质X的高效催化剂,反应部分
2 2 8 3 4
机理如题图所示。下列说法正确的是
A.Co元素位于元素周期表IB族
B.在激光作用下,NaSO 发生氧化反应
2 2 8
C.物质X为H
2
D.工业上煅烧CoCO 制备Co O 的反应:6CoCO+O====2Co O+6CO
3 3 4 3 2 3 4 2
二、填空题
5.(2024·安徽卷)精炼铜产生的铜阳极泥富含Cu、Ag、Au等多种元素。研究人员设计了一种从第3讲 新情境方程式的书写
铜阳极泥中分离提收金和银的流程,如下图所示。
(3)“浸取2”步骤中,单质金转化为HAuCl 的化学方程式为
4
___________________________________________________________________。
(5)“浸取3”步骤中,“浸渣2”中的AgCl转化为[Ag(SO)]3-。“电沉积”步骤中阴极的电极
2 3 2
反应式为________________________________________。“电沉积”步骤完成后,阴极区溶液中可循环
利用的物质为_____________(填化学式)。
6.(2024·江苏卷)Ag的抗菌性能。纳米Ag表面能产生Ag+杀死细菌(如图所示),其抗菌性能受
溶解氧浓度影响。
的
①纳米Ag溶解产生Ag+ 离子方程式为__________________________________________。
②实验表明溶解氧浓度过高,纳米Ag的抗菌性能下降,主要原因是
______________________________________________________________________。
7.(2024·无锡上学期期中)还原吸附法
(3)纳米磁性Fe O 的制备
3 4
以FeSO 和Fe (SO ) 为原料,在氨水存在的条件下反应可生成纳米磁性Fe O,发生反应的化学方
4 2 4 3 3 4
程式为________________________________________________________________________。
8.(2025·扬州开学考)钴及其化合物用途广泛。如:LiCoO 做锂电池的正极材料;草酸钴可用于
2
催化剂(Co O)制备。
3 4
LiCO 和Co O 混合后,在空气中高温加热可以制备锂电池的正极材料LiCoO ,写出反应方程式
2 3 3 4 2
___________________________________________________________。
9.(2024·镇江市丹阳市上学期开学考)MnO 在电池中有重要应用。以软锰矿(含MnO 及少量
2 2
Fe、Al的氧化物)为原料制备粗二氧化锰颗粒的过程如下:
浸出。用HSO 和FeSO 可溶解软锰矿,生成Mn2+的离子方程式为
2 4 4
________________________________________________。
10.(2024·南外、金陵中学、海安中学三校最后一卷节选)钴、镍是重要的战略金属,在工业中
占据重要地位。以湿法炼锌过程中产出的钴渣为原料,分离回收钴渣中钴、镍的工艺流程如下。
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找已知:①酸浸液主要含有Zn2+、Co2+、Fe2+、Ni2+、Mn2+等金属阳离子;
(3)除锰。在酸性条件下,向除镍后的溶液中加入NaSO 溶液选择性氧化Mn2+,反应生成MnO
2 2 8 2
和SO 2-的离子方程式为_______________________________________________________________。
4
(4)沉钴。向除锰后的溶液中加入NaSO 溶液并控制溶液pH氧化沉Co2+。将Co(OH) 隔绝空气
2 2 8 3
灼烧会生成Co O;如果控制温度不当,Co(OH) 会生成CoO杂质,反应的化学方程式是
2 3 3
________________________________________________。
11.(2024·泰州市期中)由菱锰矿(主要成分为MnCO,还含有少量Si、Fe、Ni等元素)制备一种
3
新型锂电池正极材料LiMn O 的工艺流程如下:
2 4
煅烧时,生成LiMn O 的化学方程式为
2 4
_________________________________________________________________________。
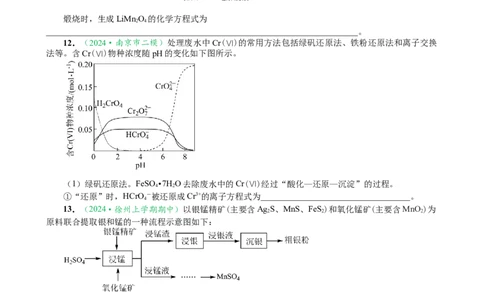
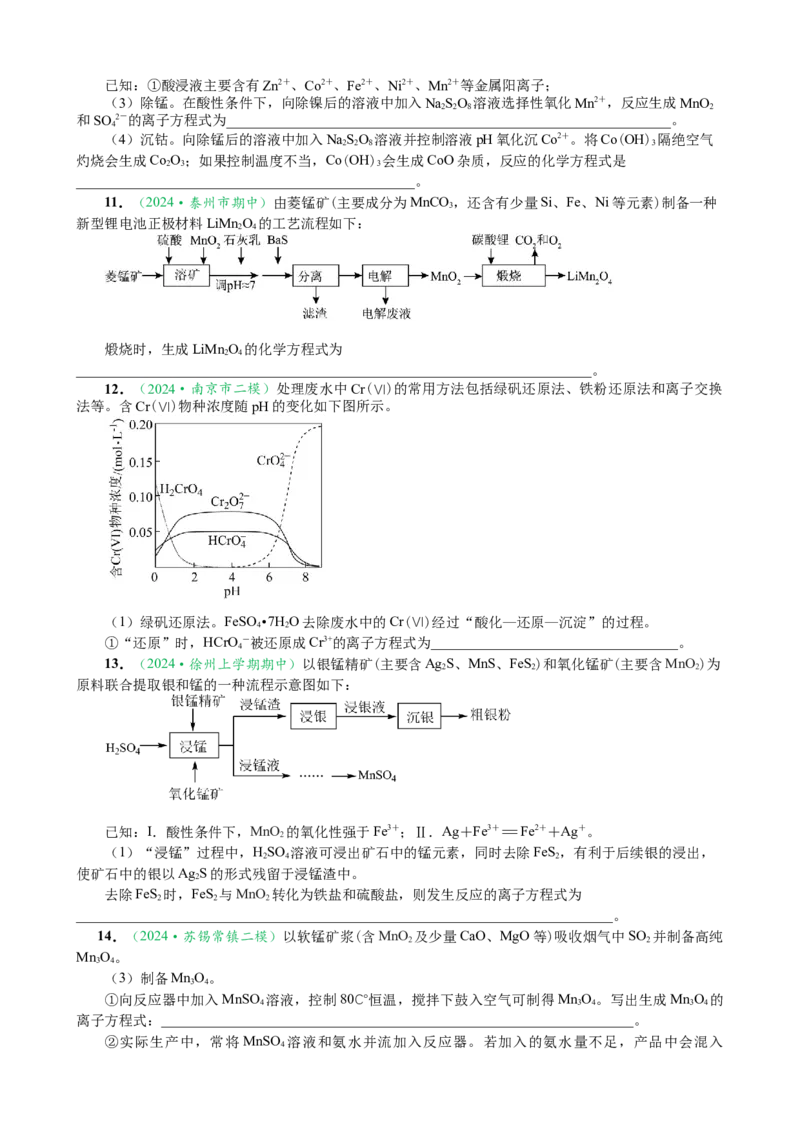
12.(2024·南京市二模)处理废水中Cr(Ⅵ)的常用方法包括绿矾还原法、铁粉还原法和离子交换
法等。含Cr(Ⅵ)物种浓度随pH的变化如下图所示。
(1)绿矾还原法。FeSO •7HO去除废水中的Cr(Ⅵ)经过“酸化—还原—沉淀”的过程。
4 2
①“还原”时,HCrO -被还原成Cr3+的离子方程式为___________________________________。
4
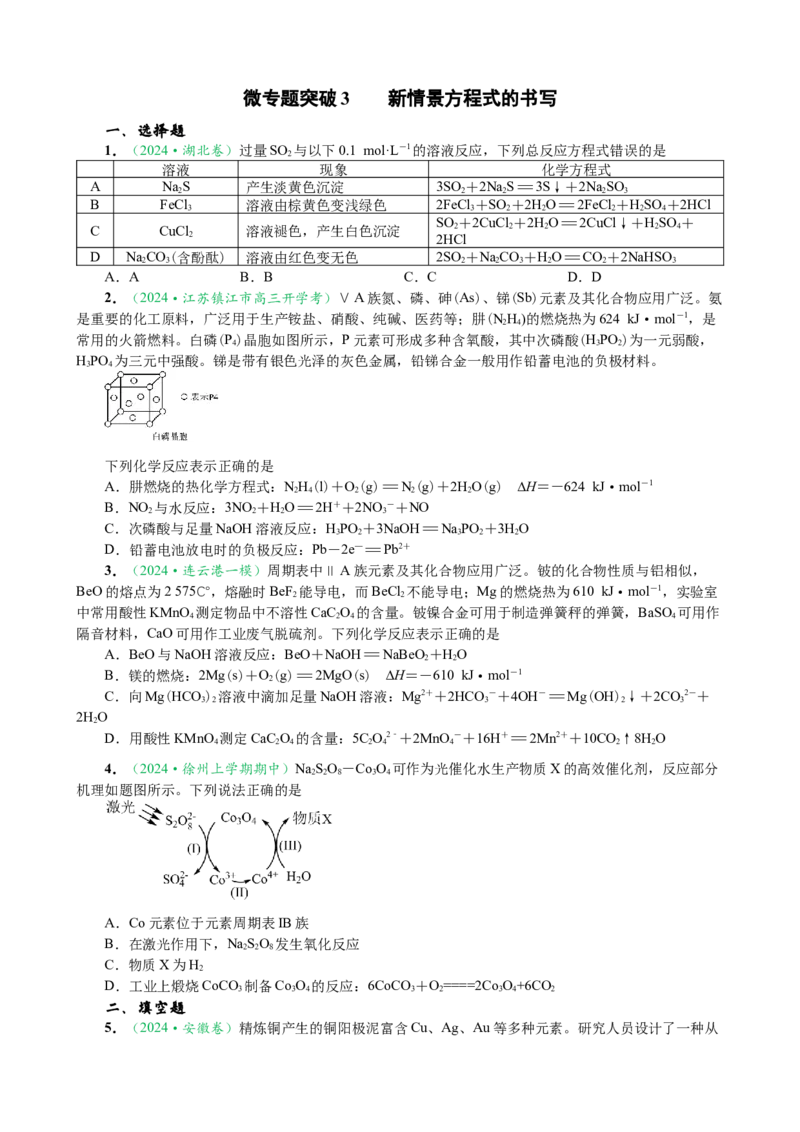
13.(2024·徐州上学期期中)以银锰精矿(主要含Ag S、MnS、FeS)和氧化锰矿(主要含MnO )为
2 2 2
原料联合提取银和锰的一种流程示意图如下:
已知:I.酸性条件下,MnO 的氧化性强于Fe3+;Ⅱ.Ag+Fe3+=Fe2++Ag+。
2
(1)“浸锰”过程中,HSO 溶液可浸出矿石中的锰元素,同时去除FeS,有利于后续银的浸出,
2 4 2
使矿石中的银以Ag S的形式残留于浸锰渣中。
2
去除FeS 时,FeS 与MnO 转化为铁盐和硫酸盐,则发生反应的离子方程式为
2 2 2
____________________________________________________________________________。
14.(2024·苏锡常镇二模)以软锰矿浆(含MnO 及少量CaO、MgO等)吸收烟气中SO 并制备高纯
2 2
MnO。
3 4
(3)制备MnO。
3 4
①向反应器中加入MnSO 溶液,控制80℃恒温,搅拌下鼓入空气可制得MnO 。写出生成MnO 的
4 3 4 3 4
离子方程式:___________________________________________________________________。
②实际生产中,常将MnSO 溶液和氨水并流加入反应器。若加入的氨水量不足,产品中会混入
4第3讲 新情境方程式的书写
MnO 、 MnO 等 , 其 原 因 是
2 3 2
___________________________________________________________________________
____________________________________________________________________。
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找