文档内容
微专题突破8 化学反应速率与化学平衡
一、选择题
1.(2024·泰州市期中)反应Si(s)+3HCl(g) SiHCl (g)+H(g) ∆H=-225 kJ·mol-1 。下
3 2
列说法不正确的是
A.该反应在低温下能自发进行是由于∆H<0的影响
B.该反应的平衡常数K=
C.实际生产中选择高温是因为高温时Si的平衡转化率比低温时大
D.其他条件不变时,可通过缩小体积增大压强提高Si的转化率
【答案】C
【解析】A项,反应自发进行应满足∆G=∆H-T∆H<0,该反应∆S>0,所以该反应在低温下能自发
进行是由于ΔH<0的影响,正确;B项,硅为固体,不能体现在平衡常数中,根据平衡常数的定义,可
知平衡常数表示正确,正确;C项,该反应为放热反应,升温会使平衡逆向移动,Si的平衡转化率会减
小,错误;D项,该反应是气体系数减小的反应,缩小体积增大压强会使反应平衡向正向进行,提高 Si
的转化率,正确。
2.(2024·江苏镇江市高三开学考)HS和CO 反应生成的羰基硫(COS)用于粮食熏蒸,能防止某
2 2
些昆虫、线虫和真菌的危害。CO(g)+HS(g) COS(g)+HO(g);∆H>0。下列说法正确的是
2 2 2
A.上述反应的平衡常数K=
B.上述反应中消耗1 mol HS,生成22.4 L水蒸气
2
C.已知该反应在加热条件下能自发进行,则其∆S>0
D.及时分离出HO,可加快该反应到达平衡状态
2
【答案】C
【解析】A项,该反应中水为气态,要带入平衡常数表达式,上述反应的平衡常数K=,错误;B项,
上述反应中消耗1 mol HS,生成1 mol水蒸气,由于缺少是否为标准状况下,因此无法计算水蒸气的体
2
积,错误;C项,该反应是∆H>0,已知该反应在加热条件下能自发进行,则∆S>0,正确;D项,及时
分离出HO,反应速率降低,可增大反应物的转化率,但不能加快该反应到达平衡状态,错误。
2
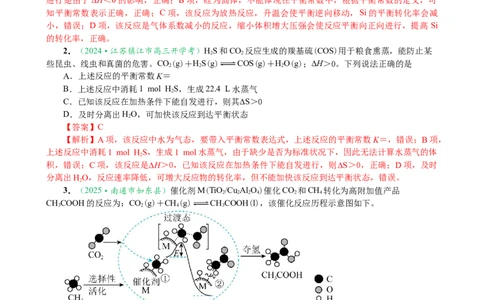
3.(2025·南通市如东县)催化剂M(TiO/Cu Al O)催化CO 和CH 转化为高附加值产品
2 2 2 4 2 4
CHCOOH的反应为:CO(g)+CH(g) CHCOOH(l),该催化反应历程示意图如下。
3 2 4 3
下列说法不正确的是
A.该反应的∆S<0
B.①→②过程放出能量并形成了C-C键
C.所示的反应机理中,步骤①可理解为CH 中带部分负电荷的C与催化剂M之间发生作用
4
D.该反应中每消耗1 mol CO,转移电子的数目约为2×6.02×1023
2
【答案】D
【解析】A项,根据反应方程式CO(g)+CH(g) CHCOOH(l)可知:该步反应的正反应是气体
2 4 3
体积减小的反应,所以该反应的∆S<0,正确;B项,①→②过程是放热反应,放出能量,并在 CH 和
4
CO 之间形成了C-C键,正确;C项,由题图所示的反应机理可知,CH 中C显负价,H显正价,步骤
2 4
①可理解为CH 中带部分负电荷的C与催化剂M之间发生作用,使C-H键断裂,正确;
4微专题突破8 化学反应速率与化学平衡
D项,该反应中每消耗l mol CO,则消耗1 mol CH,CH 中C元素的化合价由CH 中的-4价变为
2 4 4 4
CHCOOH中的0价,化合价升高4价,根据反应过程中电子转移总数等于元素化合价升降总数,可知反
3
应过程中转移电子的数目约为1 mol×4×6.02×l023/mo1=4×6.02×1023,错误。
4.(2024·南通市如皋二模)氯气在生产、生活中应用广泛。实验室用KMnO 和浓盐酸常温下反
4
应制取Cl,工业上用电解饱和食盐水制备Cl,也可用地康法制备Cl。450℃,以CuCl 作催化剂,地康
2 2 2 2
法原理如图所示。氨气可以检验Cl 是否发生泄露,遇Cl 泄漏时反应有白烟生成;Cl 可用于制备氯水或
2 2 2
含KClO等成分的消毒剂,也可用于处理含氰(CN-)废水。
关于地康法制Cl,下列说法正确的是
2
A.反应的平衡常数可表示为K=
B.其他条件不变,升高温度HCl的平衡转化率降低说明该反应∆H<0
C.CuCl 的使用可以增大反应的活化能
2
D.每生成22.4L Cl 时,转移电子的数目为2×6.02×1023
2
【答案】B
【解析】由图知,450℃,以CuCl 作催化剂,地康法制备氯气的总反应为4HCl(g)+O(g)
2 2
2HO(g)+2Cl(g)。
2 2
A项,结合分析可知,该反应的平衡常数可表示为K=,错误;B项,其他条件不变,升高温度HCl
的平衡转化率降低,说明升温平衡左移,则说明该反应正向放热,即∆H<0,正确;C项,地康法制备氯
气时CuCl 作催化剂,CuCl 的使用可以降低反应的活化能,错误;D项,未指明标准状况,气体摩尔体
2 2
积不确定,则无法计算每生成22.4 L Cl 时转移的电子数目,错误。
2
5.(2024·扬州市高三下学期开学考)羟胺(NH OH)能与水反应:NH OH+HO NH OH++
2 2 2 3
OH-。下列说法不正确的是
A.反应的平衡常数K=
B.NH OH能与水反应是因为分子中氮原子存在孤电子对
2
C.NH OH溶液能吸收CO 气体
2 2
D.向羟胺溶液中滴加过量稀HSO ,可生成(NH OH)SO
2 4 3 2 4
【答案】D
【解析】A项,反应的平衡常数为:K=,正确;B项,NH OH能与水反应是因为分子中氮原子存在
2
孤电子对,能和H+离子形成配位键,正确;C项,NH OH溶液呈碱性,能吸收酸性气体CO ,正确;D
2 2
项,向羟胺溶液中滴加过量稀 HSO ,生成硫酸氢盐,反应的化学方程式为:NH OH+HSO =
2 4 2 2 4
(NH OH)HSO ,错误。
3 4
6.(2024·徐州上学期期中)汽车安装尾气净化装置也可除去NO,反应方程式为2NO (g)+
x 2
4CO(g) N(g)+4CO(g),关于反应2NO (g)+4CO(g) N(g)+4CO(g),下列说法正确的是
2 2 2 2 2
A.该反应的∆S>0
B.选择合适的催化剂,可以使NO 完全转化成N
2 2
C.及时移除N、CO,正反应速率增大,平衡向正反应方向移动
2 2
D.上述反应中每生成0.1 mol N,转移电子的数目约为0.8×6.02×1023
2
【答案】D
【解析】A项,根据气体的化学计量数可知此反应的正反应是气体分子个数减小的反应,所以该反
应的∆S<0,错误;B项,催化剂只能改变反应速率不能改变转化率,错误;C项,及时移除N 、CO ,
2 2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找逆反应速率减小,正反应速率开始不变,平衡向正反应方向移动,导致反应物浓度减小,正反应速率随
之减小,错误;D项,上述反应中当生成1 mol N 时,转移电子为8 mol,所以每生成0.1 mol N,转移
2 2
电子的数目约为0.8×6.02×1023,正确。
7.(2024·苏锡常镇一模)对于反应2SO(g)+O(g) 2SO(g),下列有关说法正确的是
2 2 3
A.该反应的∆S>0
B.该反应平衡常数的表达式为K=
C.反应中每消耗22.4 L O(标准状况),转移电子数约为2×6.02×1023
2
D.温度不变,提高c (O)或增大反应压强,均能提高反应速率和SO 的转化率
起始 2 2
【答案】D
【解析】A项,该反应前后气体分子数减少,则∆S<0,错误;B项,该反应平衡常数的表达式为K
=,错误;C项,每消耗22.4 L O (标准状况),即1 mol O 时,转移4 mol电子,转移电子数为
2 2
4×6.02×1023,错误;D项,增大浓度或增大压强均能提高化学反应速率,增大氧气的浓度或增大压强均
有利于该反应正向移动,从而提高二氧化硫的转化率,正确。
8.(2024·南通市二模)CuO-TiO 可用于低温下催化氧化HCHO:HCHO(g)+
x 2
O(g)==========CO(g)+HO(l)。下列关于CuO-TiO 催化氧化甲醛的反应说法正确的是
2 2 2 x 2
A.该反应∆H<0,∆S<0
B.HCHO、CO、HO均为极性分子
2 2
C.升高温度,υ 增大,υ 减小
逆 正
D.使用CuO-TiO 催化剂降低了该反应的焓变
x 2
【答案】A
【解析】A项,根据方程式可知,该反应∆S<0,根据∆G=∆H-T∆S<0反应可自发进行,放热的熵
减反应低温可自发进行,由此可判断∆H<0,正确;B项,CO 为直线形分子,属于非极性分子,错误;
2
C项,升高温度,正、逆反应速率均增大,错误;D项,催化剂可以改变反应活化能,不能改变反应焓变,
错误。
9.(2024·南京市二模)制备光电子功能材料ZnS可通过自发反应ZnO(s)+HS(g)=ZnS(s)+
2
HO(g) ∆H>0。下列说法正确的是
2
A.该反应的ΔS<0
B.其他条件相同,缩小容器体积,达到新平衡时减小
C.其他条件相同,升高体系温度,HS的平衡转化率增大
2
D.其他条件相同,使用催化剂加快正反应速率,减慢逆反应速率
【答案】C
【解析】A项,反应ZnO(s)+HS(g)=ZnS(s)+HO(g)能自发进行,其ΔH>0,则ΔS>0,不正
2 2
确;B项,反应前后气体分子数相等,其他条件相同,缩小容器体积,相当于加压,平衡不发生移动,则
不变,不正确;C项,其他条件相同,升高体系温度,由于正反应为吸热反应,则平衡正向移动,HS的
2
平衡转化率增大,正确;D项,其他条件相同,使用催化剂,可降低反应的活化能,加快正反应速率,
同时加快逆反应速率,不正确。
10.(2025·南通市海安市开学考)工业上由粗硅制备高纯晶体硅流程中的一步反应为SiHCl(g)+
3
H(g) Si(s)+3HCl(g)。下列说法正确的是
2
A.该反应∆S<0
B.该反应的平衡常数K=
C.用E表示键能,该反应∆H=3E(Si-Cl)+E(Si-H)+E(H-H)-3E(H-Cl)-2E(Si-Si)
D.该过程需要在无水条件下进行的原因:SiHCl 与水反应生成HSiO 和HCl两种物质
3 2 3
【答案】C
【解析】A项,该反应是气体分子总数增加的反应,∆S>0,错误;B项,Si为固体,不能出现在平
衡常数表达式中,该反应K=,错误;C项,SiHCl 中含3个Si-Cl键和1个Si-H,H 中含1个H-
3 2
H,HCl中含1个H-Cl键,Si中含2个Si-Si键,根据∆H=反应物总键能-生成物总键能,可知∆H=微专题突破8 化学反应速率与化学平衡
3E(Si-Cl)+E(Si-H)+E(H-H)-3E(H-Cl)-2E(Si-Si),正确;D项,SiHCl 中Si为+4价,H、
3
Cl为-1价,根据氧化还原反应规律和质量守恒可知SiHCl 与水反应生成HSiO、HCl、H 三种物质,错
3 2 3 2
误。
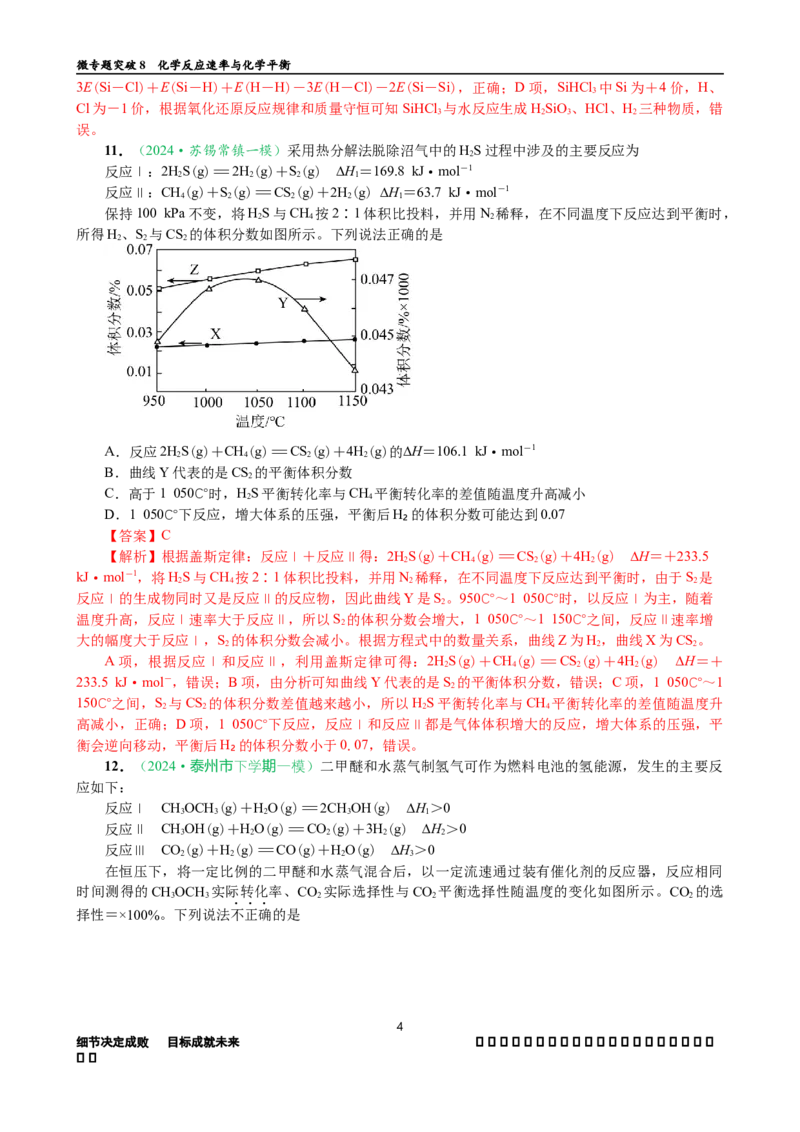
11.(2024·苏锡常镇一模)采用热分解法脱除沼气中的HS过程中涉及的主要反应为
2
反应Ⅰ:2HS(g)=2H(g)+S(g) ∆H=169.8 kJ·mol-1
2 2 2 1
反应Ⅱ:CH(g)+S(g)=CS(g)+2H(g) ∆H=63.7 kJ·mol-1
4 2 2 2 1
保持100 kPa不变,将HS与CH 按2∶1体积比投料,并用N 稀释,在不同温度下反应达到平衡时,
2 4 2
所得H、S 与CS 的体积分数如图所示。下列说法正确的是
2 2 2
A.反应2HS(g)+CH(g)=CS(g)+4H(g)的∆H=106.1 kJ·mol-1
2 4 2 2
B.曲线Y代表的是CS 的平衡体积分数
2
C.高于1 050℃时,HS平衡转化率与CH 平衡转化率的差值随温度升高减小
2 4
D.1 050℃下反应,增大体系的压强,平衡后H₂的体积分数可能达到0.07
【答案】C
【解析】根据盖斯定律:反应Ⅰ+反应Ⅱ得:2HS(g)+CH(g)=CS(g)+4H(g) ∆H=+233.5
2 4 2 2
kJ·mol-1,将HS与CH 按2∶1体积比投料,并用N 稀释,在不同温度下反应达到平衡时,由于S 是
2 4 2 2
反应Ⅰ的生成物同时又是反应Ⅱ的反应物,因此曲线Y是S。950℃~1 050℃时,以反应Ⅰ为主,随着
2
温度升高,反应Ⅰ速率大于反应Ⅱ,所以S 的体积分数会增大,1 050℃~1 150℃之间,反应Ⅱ速率增
2
大的幅度大于反应Ⅰ,S 的体积分数会减小。根据方程式中的数量关系,曲线Z为H,曲线X为CS。
2 2 2
A项,根据反应Ⅰ和反应Ⅱ,利用盖斯定律可得:2HS(g)+CH(g)=CS(g)+4H(g) ∆H=+
2 4 2 2
233.5 kJ·mol-,错误;B项,由分析可知曲线Y代表的是S 的平衡体积分数,错误;C项,1 050℃~1
2
150℃之间,S 与CS 的体积分数差值越来越小,所以HS平衡转化率与CH 平衡转化率的差值随温度升
2 2 2 4
高减小,正确;D项,1 050℃下反应,反应Ⅰ和反应Ⅱ都是气体体积增大的反应,增大体系的压强,平
衡会逆向移动,平衡后H₂的体积分数小于0.07,错误。
12.(2024·泰州市下学期一模)二甲醚和水蒸气制氢气可作为燃料电池的氢能源,发生的主要反
应如下:
反应Ⅰ CHOCH (g)+HO(g)=2CHOH(g) ∆H>0
3 3 2 3 1
反应Ⅱ CHOH(g)+HO(g)=CO(g)+3H(g) ∆H>0
3 2 2 2 2
反应Ⅲ CO(g)+H(g)=CO(g)+HO(g) ∆H>0
2 2 2 3
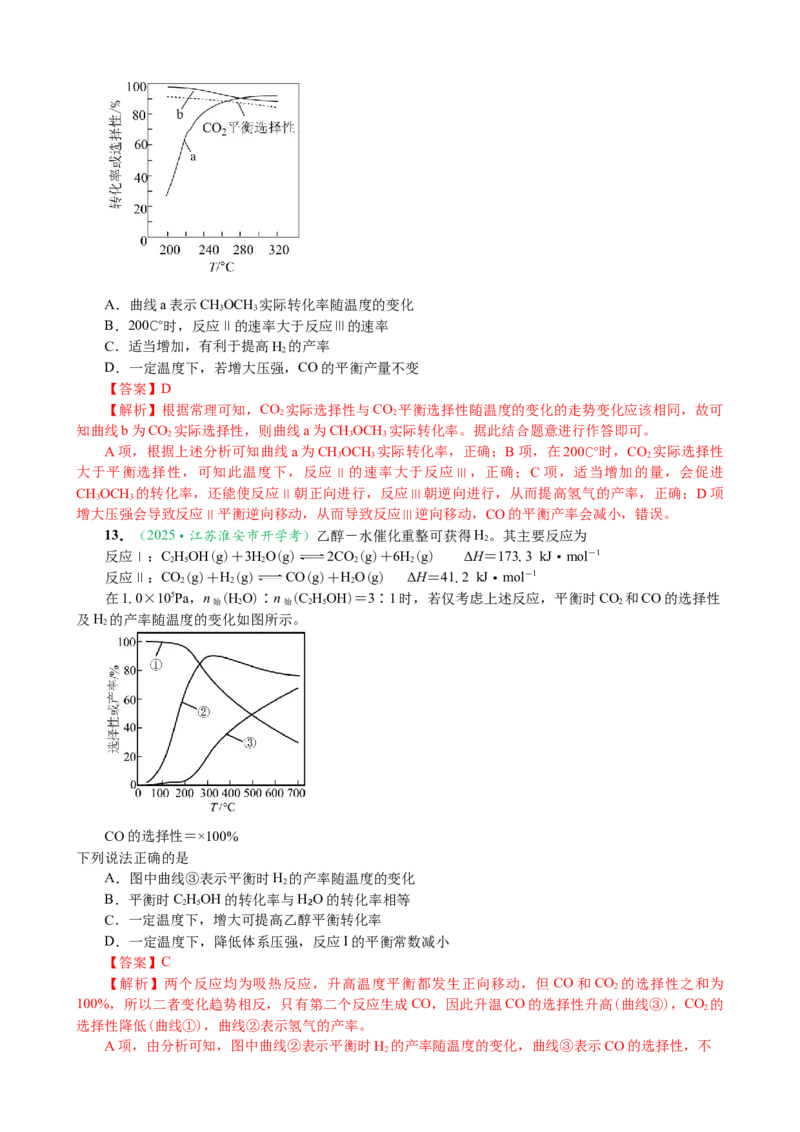
在恒压下,将一定比例的二甲醚和水蒸气混合后,以一定流速通过装有催化剂的反应器,反应相同
时间测得的CHOCH 实际转化率、CO 实际选择性与CO 平衡选择性随温度的变化如图所示。CO 的选
3 3 2 2 2
择性=×100%。下列说法不正确的是
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找A.曲线a表示CHOCH 实际转化率随温度的变化
3 3
B.200℃时,反应Ⅱ的速率大于反应Ⅲ的速率
C.适当增加,有利于提高H 的产率
2
D.一定温度下,若增大压强,CO的平衡产量不变
【答案】D
【解析】根据常理可知,CO 实际选择性与CO 平衡选择性随温度的变化的走势变化应该相同,故可
2 2
知曲线b为CO 实际选择性,则曲线a为CHOCH 实际转化率。据此结合题意进行作答即可。
2 3 3
A项,根据上述分析可知曲线a为CHOCH 实际转化率,正确;B项,在200℃时,CO 实际选择性
3 3 2
大于平衡选择性,可知此温度下,反应Ⅱ的速率大于反应Ⅲ,正确;C项,适当增加的量,会促进
CHOCH 的转化率,还能使反应Ⅱ朝正向进行,反应Ⅲ朝逆向进行,从而提高氢气的产率,正确;D项
3 3
增大压强会导致反应Ⅱ平衡逆向移动,从而导致反应Ⅲ逆向移动,CO的平衡产率会减小,错误。
13.(2025·江苏淮安市开学考)乙醇-水催化重整可获得H。其主要反应为
2
反应Ⅰ:C HOH(g)+3HO(g) 2CO(g)+6H(g) ΔH=173.3 kJ·mol-1
2 5 2 2 2
反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH=41.2 kJ·mol-1
2 2 2
在1.0×105Pa,n (HO)∶n (C HOH)=3∶1时,若仅考虑上述反应,平衡时CO 和CO的选择性
始 2 始 2 5 2
及H 的产率随温度的变化如图所示。
2
CO的选择性=×100%
下列说法正确的是
A.图中曲线③表示平衡时H 的产率随温度的变化
2
B.平衡时C HOH的转化率与H₂O的转化率相等
2 5
C.一定温度下,增大可提高乙醇平衡转化率
D.一定温度下,降低体系压强,反应I的平衡常数减小
【答案】C
【解析】两个反应均为吸热反应,升高温度平衡都发生正向移动,但 CO和CO 的选择性之和为
2
100%,所以二者变化趋势相反,只有第二个反应生成CO,因此升温CO的选择性升高(曲线③),CO 的
2
选择性降低(曲线①),曲线②表示氢气的产率。
A项,由分析可知,图中曲线②表示平衡时H 的产率随温度的变化,曲线③表示CO的选择性,不
2微专题突破8 化学反应速率与化学平衡
正确;B项,n (HO)∶n (C HOH)=3∶1,若第二个反应不生成HO,则平衡时C HOH的转化率与
始 2 始 2 5 2 2 5
H₂O的转化率相等,但第二个反应生成HO,所以平衡时C HOH的转化率与H₂O的转化率不相等,不
2 2 5
正确;C项,一定温度下,增大,相当于C HOH的物质的量不变时增大HO的物质的量,平衡正向移动,
2 5 2
乙醇的平衡转化率增大,正确;D项,平衡常数只受温度变化的影响,一定温度下,降低体系压强,虽
然平衡发生移动,但反应I的平衡常数不变,不正确。
二、填空题
14.(2024·泰州市下学期一模)空气中CO 含量的控制和CO 资源利用具有重要意义。
2 2
(2)利用铟氧化物催化CO、H 制取CHOH的可能机理如图2所示,InO 无催化活性,形成氧空
2 2 3 2 3
位后具有较强催化活性,将固定比例的CO、H 混合气体以不同流速通过装有催化剂的反应管,CHOH
2 2 3
选择性、CO 转化率随气体流速变化曲线如图3所示,
2
①图2中的反应每生成1 mol CHOH(g)放出49 kJ的热量,其热化学方程式为
3
_______________________________________________________________________。
② 若 原 料 气 中 H 比 例 过 低 、 过 高 均 会 减 弱 催 化 剂 活 性 , 原 因 是
2
___________________________________
______________________________________________________________________。
③制取CHOH时,同时发生反应CO(g)+H(g) CO(g)+HO(g) ∆H>0,气体流速分别为15
3 2 2 2
000 mL·h-1和21 000 mL·h-1,相同时间内生成CHOH的质量,前者_________后者(选填“>”、
3
“="或“<”);保持气体流速不变,反应管内温度从300℃升高到320℃,测得出口处CO 和
2
CHOH的物质的量均减小,可能的原因是__________________________________________________
3
__________________________________________________________________________。
【答案】(2)①CO(g)+3H(g) CHOH(g)+HO(g) ∆H=-49 kJ·mol-1 ②H 比例过低,
2 2 3 2 2
不利于催化剂形成氧空位,导致催化剂失活;H 比例过高,反应①生成过多的水会积累在具有活性的催
2
化剂表面,导致催化剂失活 ③< ④升高温度,生成甲醇的反应左移,生成一氧化碳的反应右移,且反
应以生成一氧化碳的反应为主
【解析】①由图可知,催化剂作用下,二氧化碳与氢气反应生成甲醇和水,反应的方程式为CO(g)
2
+3H(g) CHOH(g)+HO(g),由反应生成1 mol甲醇放出49 kJ的热量可知,反应的焓变∆H=-
2 3 2
49 kJ·mol-1,则反应的热化学方程式为CO(g)+3H(g) CHOH(g)+HO(g) ∆H=—49 kJ·mol
2 2 3 2
-1,故答案为:CO(g)+3H(g) CHOH(g)+HO(g) ∆H=—49 kJ·mol-1;②由图2可知,若原
2 2 3 2
料气中氢气的比例过低不利于催化剂形成氧空位,导致催化剂失活;若氢气的比例过高,反应①生成过
多的水积累在具有活性的催化剂表面,导致催化剂失活,故答案为:H 比例过低,不利于催化剂形成氧
2
空位,导致催化剂失活;H 比例过高,反应①生成过多的水会积累在具有活性的催化剂表面,导致催化
2
剂失活;③设混合气体中二氧化碳的比例分数为x,由图可知,气体流速由15 000 mL·h-1和21 000
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找mL·h-1时,二氧化碳的转化率分别为5%和4%,则转化的二氧化碳分别为15 000x mL·h-1×5%=750x
mL·h-1、21 000x mL·h-1×4%=840x mL·h-1,而甲醇选择性增大,所以相同时间内生成流速为15 000
mL·h-1时生成甲醇的质量小于21 000 mL·h-1;二氧化碳与氢气反应生成甲醇的反应为放热反应,升高
温度,平衡向逆反应方向移动,生成甲醇的物质的量减小,二氧化碳与氢气反应生成甲醇的反应为吸热
反应,升高温度,平衡向正反应方向移动,消耗二氧化碳的物质的量增大,反应管内温度从300℃升高到
320℃时,出口处甲醇和二氧化碳的物质的量均减小说明反应以生成一氧化碳的反应为主,故答案为:<;
升高温度,生成甲醇的反应左移,生成一氧化碳的反应右移,且反应以生成一氧化碳的反应为主。
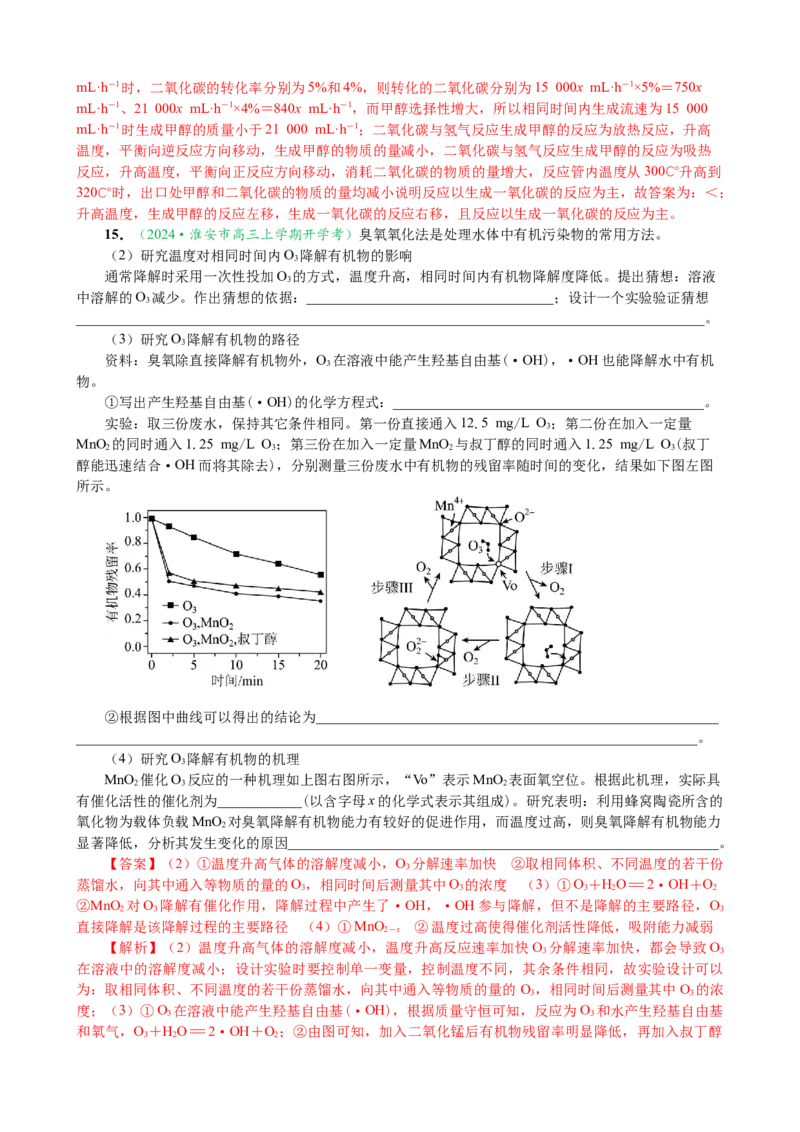
15.(2024·淮安市高三上学期开学考)臭氧氧化法是处理水体中有机污染物的常用方法。
(2)研究温度对相同时间内O 降解有机物的影响
3
通常降解时采用一次性投加O 的方式,温度升高,相同时间内有机物降解度降低。提出猜想:溶液
3
中溶解的O 减少。作出猜想的依据:___________________________________;设计一个实验验证猜想
3
_________________________________________________________________________________________。
(3)研究O 降解有机物的路径
3
资料:臭氧除直接降解有机物外,O 在溶液中能产生羟基自由基(·OH),·OH也能降解水中有机
3
物。
①写出产生羟基自由基(·OH)的化学方程式:____________________________________________。
实验:取三份废水,保持其它条件相同。第一份直接通入12.5 mg/L O;第二份在加入一定量
3
MnO 的同时通入1.25 mg/L O;第三份在加入一定量MnO 与叔丁醇的同时通入1.25 mg/L O(叔丁
2 3 2 3
醇能迅速结合·OH而将其除去),分别测量三份废水中有机物的残留率随时间的变化,结果如下图左图
所示。
②根据图中曲线可以得出的结论为_________________________________________________________
________________________________________________________________________________________。
(4)研究O 降解有机物的机理
3
MnO 催化O 反应的一种机理如上图右图所示,“Vo”表示MnO 表面氧空位。根据此机理,实际具
2 3 2
有催化活性的催化剂为____________(以含字母x的化学式表示其组成)。研究表明:利用蜂窝陶瓷所含的
氧化物为载体负载MnO 对臭氧降解有机物能力有较好的促进作用,而温度过高,则臭氧降解有机物能力
2
显著降低,分析其发生变化的原因_____________________________________________________________。
【答案】(2)①温度升高气体的溶解度减小,O 分解速率加快 ②取相同体积、不同温度的若干份
3
蒸馏水,向其中通入等物质的量的O,相同时间后测量其中O 的浓度 (3)①O+HO=2·OH+O
3 3 3 2 2
②MnO 对O 降解有催化作用,降解过程中产生了·OH,·OH参与降解,但不是降解的主要路径,O
2 3 3
直接降解是该降解过程的主要路径 (4)①MnO ②温度过高使得催化剂活性降低,吸附能力减弱
2-x
【解析】(2)温度升高气体的溶解度减小,温度升高反应速率加快O 分解速率加快,都会导致O
3 3
在溶液中的溶解度减小;设计实验时要控制单一变量,控制温度不同,其余条件相同,故实验设计可以
为:取相同体积、不同温度的若干份蒸馏水,向其中通入等物质的量的 O ,相同时间后测量其中O 的浓
3 3
度;(3)①O 在溶液中能产生羟基自由基(·OH),根据质量守恒可知,反应为O 和水产生羟基自由基
3 3
和氧气,O +HO=2·OH+O ;②由图可知,加入二氧化锰后有机物残留率明显降低,再加入叔丁醇
3 2 2微专题突破8 化学反应速率与化学平衡
有机物残留率有所降低,但不太明显。因此MnO 对O 降解有催化作用,降解过程中产生了·OH,
2 3
·OH参与降解,但不是降解的主要路径,O 直接降解是该降解过程的主要路径;(4)由图可知,步骤
3
Ⅰ二氧化锰放出氧气生成MnO ,步骤ⅡMnO 与结合O 放出氧气生成O2-,步骤ⅢO2-放出氧气同
2-x 2-x 3 2 2
时生成二氧化锰,因此实际具有催化活性的催化剂为MnO 。若温度过高使得催化剂活性降低,吸附能
2-x
力减弱,导致臭氧降解有机物能力显著降低。
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找