文档内容
微专题突破15 化学计算考点透视一
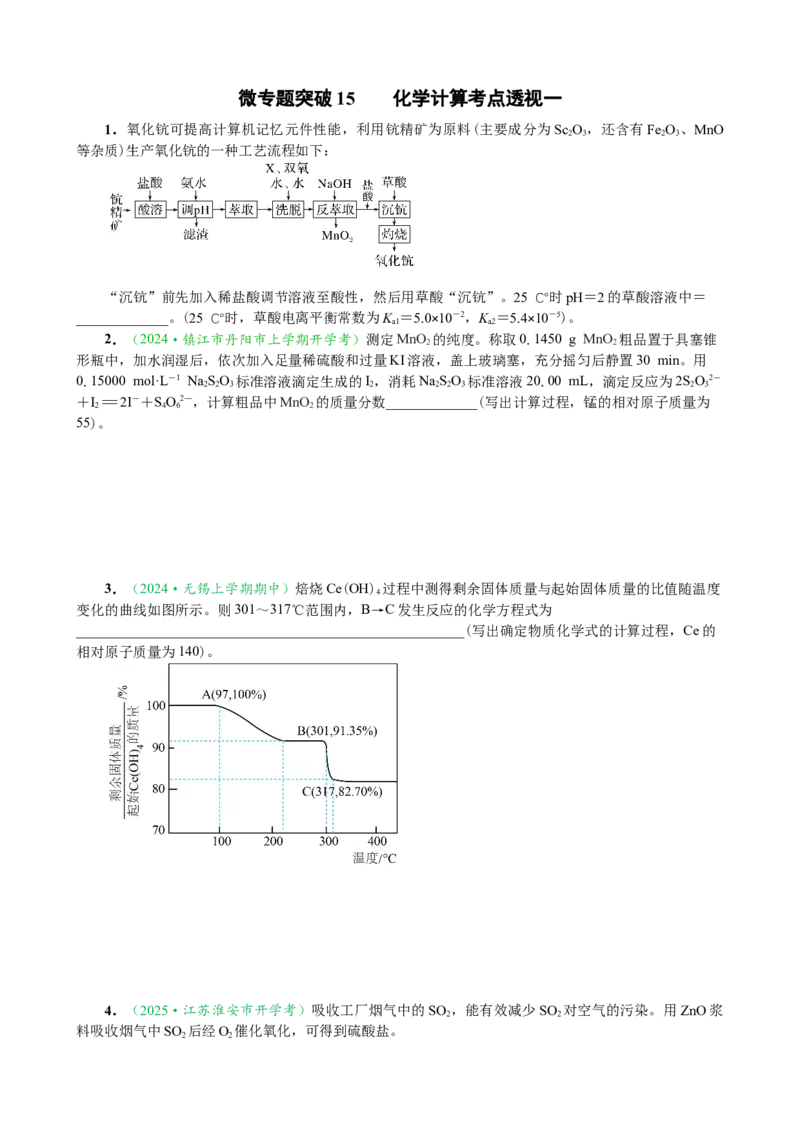
1.氧化钪可提高计算机记忆元件性能,利用钪精矿为原料(主要成分为Sc O ,还含有Fe O 、MnO
2 3 2 3
等杂质)生产氧化钪的一种工艺流程如下:
“沉钪”前先加入稀盐酸调节溶液至酸性,然后用草酸“沉钪”。25 ℃时pH=2的草酸溶液中=
_____________。(25 ℃时,草酸电离平衡常数为K =5.0×10-2,K =5.4×10-5)。
a1 a2
2.(2024·镇江市丹阳市上学期开学考)测定MnO 的纯度。称取0.1450 g MnO 粗品置于具塞锥
2 2
形瓶中,加水润湿后,依次加入足量稀硫酸和过量KI溶液,盖上玻璃塞,充分摇匀后静置30 min。用
0.15000 mol·L-1 NaSO 标准溶液滴定生成的I,消耗NaSO 标准溶液20.00 mL,滴定反应为2SO2-
2 2 3 2 2 2 3 2 3
+I=2I-+SO2—,计算粗品中MnO 的质量分数_____________(写出计算过程,锰的相对原子质量为
2 4 6 2
55)。
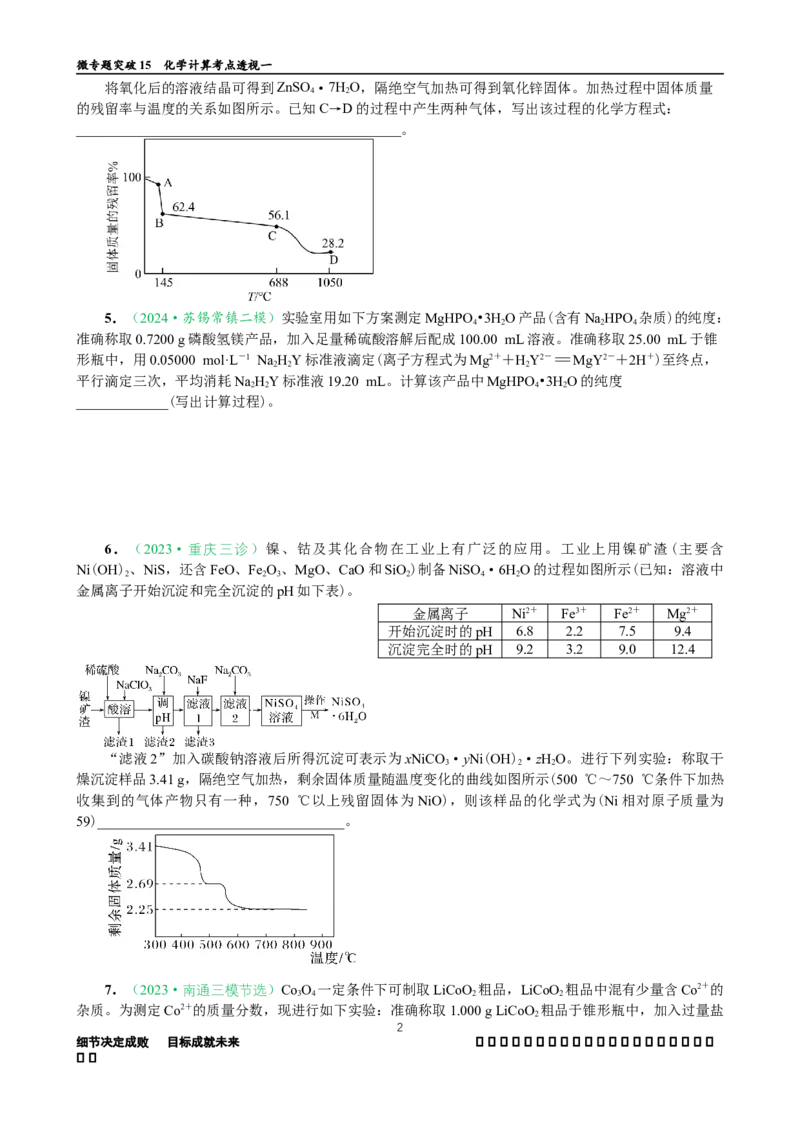
3.(2024·无锡上学期期中)焙烧Ce(OH) 过程中测得剩余固体质量与起始固体质量的比值随温度
4
变化的曲线如图所示。则301~317℃范围内,B→C发生反应的化学方程式为
_______________________________________________________(写出确定物质化学式的计算过程,Ce的
相对原子质量为140)。
4.(2025·江苏淮安市开学考)吸收工厂烟气中的SO ,能有效减少SO 对空气的污染。用ZnO浆
2 2
料吸收烟气中SO 后经O 催化氧化,可得到硫酸盐。
2 2微专题突破15 化学计算考点透视一
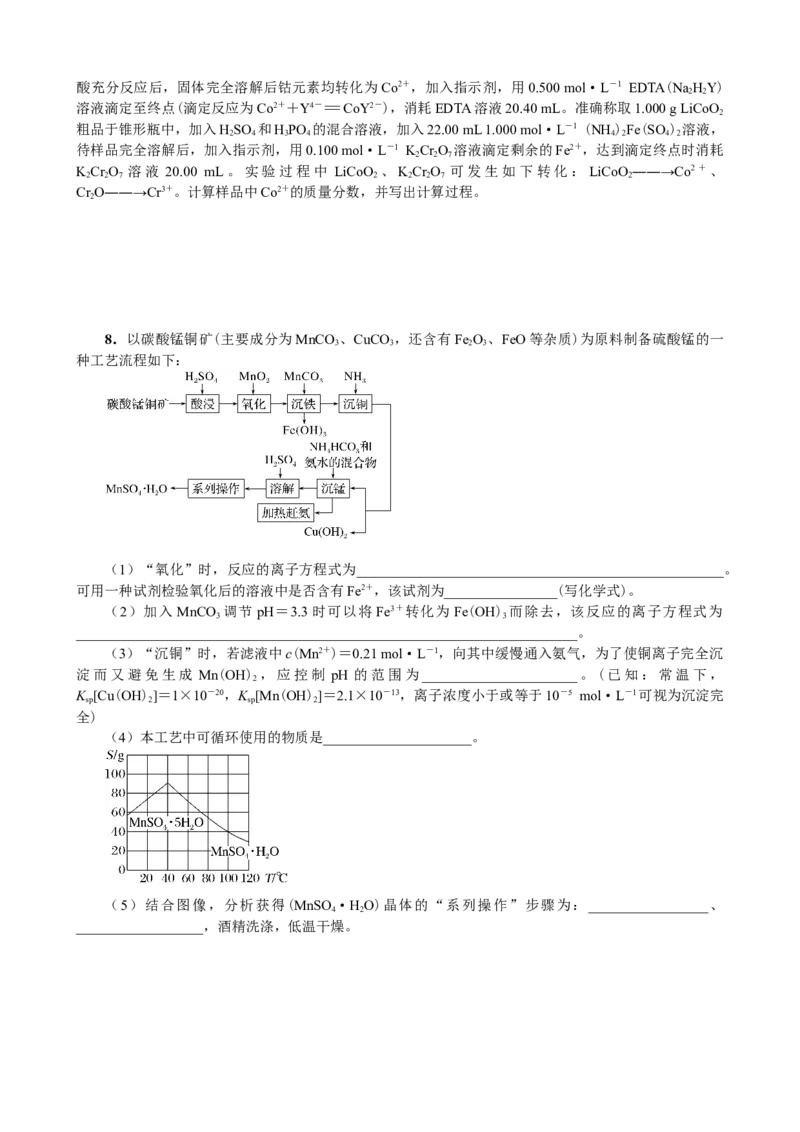
将氧化后的溶液结晶可得到ZnSO·7HO,隔绝空气加热可得到氧化锌固体。加热过程中固体质量
4 2
的残留率与温度的关系如图所示。已知C→D的过程中产生两种气体,写出该过程的化学方程式:
______________________________________________。
5.(2024·苏锡常镇二模)实验室用如下方案测定MgHPO•3HO产品(含有NaHPO 杂质)的纯度:
4 2 2 4
准确称取0.7200 g磷酸氢镁产品,加入足量稀硫酸溶解后配成100.00 mL溶液。准确移取25.00 mL于锥
形瓶中,用0.05000 mol·L-1 NaHY标准液滴定(离子方程式为Mg2++HY2-=MgY2-+2H+)至终点,
2 2 2
平行滴定三次,平均消耗NaHY标准液19.20 mL。计算该产品中MgHPO•3HO的纯度
2 2 4 2
_____________(写出计算过程)。
6.(2023·重庆三诊)镍、钴及其化合物在工业上有广泛的应用。工业上用镍矿渣(主要含
Ni(OH)、NiS,还含FeO、Fe O、MgO、CaO和SiO)制备NiSO ·6HO的过程如图所示(已知:溶液中
2 2 3 2 4 2
金属离子开始沉淀和完全沉淀的pH如下表)。
金属离子 Ni2+ Fe3+ Fe2+ Mg2+
开始沉淀时的pH 6.8 2.2 7.5 9.4
沉淀完全时的pH 9.2 3.2 9.0 12.4
“滤液2”加入碳酸钠溶液后所得沉淀可表示为xNiCO·yNi(OH)·zHO。进行下列实验:称取干
3 2 2
燥沉淀样品3.41 g,隔绝空气加热,剩余固体质量随温度变化的曲线如图所示(500 ℃~750 ℃条件下加热
收集到的气体产物只有一种,750 ℃以上残留固体为NiO),则该样品的化学式为(Ni相对原子质量为
59)___________________________________。
7.(2023·南通三模节选)Co O 一定条件下可制取LiCoO 粗品,LiCoO 粗品中混有少量含Co2+的
3 4 2 2
杂质。为测定Co2+的质量分数,现进行如下实验:准确称取1.000 g LiCoO 粗品于锥形瓶中,加入过量盐
2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找酸充分反应后,固体完全溶解后钴元素均转化为Co2+,加入指示剂,用0.500 mol·L-1 EDTA(NaHY)
2 2
溶液滴定至终点(滴定反应为Co2++Y4-=CoY2-),消耗EDTA溶液20.40 mL。准确称取1.000 g LiCoO
2
粗品于锥形瓶中,加入HSO 和HPO 的混合溶液,加入22.00 mL 1.000 mol·L-1 (NH )Fe(SO ) 溶液,
2 4 3 4 4 2 4 2
待样品完全溶解后,加入指示剂,用0.100 mol·L-1 KCr O 溶液滴定剩余的Fe2+,达到滴定终点时消耗
2 2 7
KCr O 溶液 20.00 mL。实验过程中 LiCoO 、KCr O 可发生如下转化:LiCoO ――→Co2+、
2 2 7 2 2 2 7 2
Cr O――→Cr3+。计算样品中Co2+的质量分数,并写出计算过程。
2
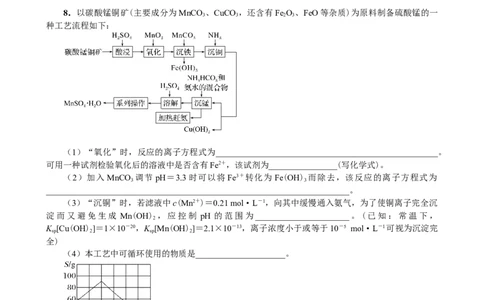
8.以碳酸锰铜矿(主要成分为MnCO 、CuCO ,还含有Fe O 、FeO等杂质)为原料制备硫酸锰的一
3 3 2 3
种工艺流程如下:
(1)“氧化”时,反应的离子方程式为____________________________________________________。
可用一种试剂检验氧化后的溶液中是否含有Fe2+,该试剂为________________(写化学式)。
(2)加入 MnCO 调节 pH=3.3时可以将 Fe3+转化为 Fe(OH) 而除去,该反应的离子方程式为
3 3
_______________________________________________________________________。
(3)“沉铜”时,若滤液中c(Mn2+)=0.21 mol·L-1,向其中缓慢通入氨气,为了使铜离子完全沉
淀而又避免生成 Mn(OH) ,应控制 pH 的范围为______________________。(已知:常温下,
2
K [Cu(OH)]=1×10-20,K [Mn(OH)]=2.1×10-13,离子浓度小于或等于10-5 mol·L-1可视为沉淀完
sp 2 sp 2
全)
(4)本工艺中可循环使用的物质是_____________________。
(5)结合图像,分析获得(MnSO ·HO)晶体的“系列操作”步骤为:_________________、
4 2
__________________,酒精洗涤,低温干燥。