文档内容
微专题突破5 无机物的性质、转化与应用
千里之行,始于足下。——老子(学习注意积累)
目标定位
1.知道常见无机物的用途与物质之间的关系。
2.根据物质的性质判断给定的转化能否实现。
3.根据信息结合已有知识判断方程式是否正确。
4.根据化工微流程判断有关说法是否正确。
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
1.常见金属及其化合物的性质与应用
重要性质 应用
(1)钠具有较强的还原性 可用于冶炼钛、锆、铌等金属
(2)Na O 与HO、CO 反应均生成O 用作供氧剂
2 2 2 2 2
(3)Na CO 水解使溶液显碱性 用热的纯碱溶液洗去油污
2 3
(4)NaHCO 受热分解生成CO、能与酸反应 用作焙制糕点的膨松剂、胃酸中和剂
3 2
(5)肥皂水显碱性 肥皂水作蚊虫叮咬处的清洗剂
(6)锂密度小、比能量大 可用作电池负极材料
(7)Al具有良好的延展性和抗腐蚀性 常用铝箔包装物品
(8)常温下,铝、铁遇浓硫酸、浓硝酸钝化 用铝制或铁制容器盛装、运输浓硫酸、浓硝酸
(9)铝与氧化铁反应放出大量的热 用于焊接铁轨
(10)MgO、Al O 熔点高 用作耐高温材料
2 3
(11)小苏打溶液和硫酸铝溶液反应生成CO 用于泡沫灭火器
2
(12)明矾溶液显酸性 用于清除铜器表面的铜锈
(13)Al(OH) 有弱碱性 用于中和胃酸
3
(14)Fe具有还原性 防止食品氧化变质
(15)Fe O 是红棕色粉末 用作红色颜料
2 3
(16)FeCl 溶液具有较强氧化性 腐蚀Cu刻制印刷电路板
3
(17)CuSO 能使蛋白质变性 配制成波尔多液用于树木杀虫
4
(18)BaSO 不溶于水,不与胃酸反应 在医疗上进行胃部造影前,用作患者服用的“钡餐”
4
2.常见非金属及其化合物的性质与应用
重要性质 应用
(1)浓硫酸具有吸水性 用作干燥剂(不能干燥NH 、HS、HI)
3 2
(2)生石灰、无水氯化钙能与水反应 用作(食品)干燥剂
(3)P O 能与水反应 用作干燥剂(不可干燥食品)
2 5
(4)硅具有半导体性能 制作芯片和太阳能电池
(5)SiO 存在光的全反射,且有硬度和柔韧度 制作光导纤维
2
(6)2C+SiO=====Si+2CO↑ 碳还原二氧化硅制备粗硅
2
(7)4HF+SiO=2HO+SiF↑ 用氢氟酸刻蚀玻璃
2 2 4
(8)ClO 具有较强的氧化性 用于自来水的杀菌消毒
2
(9)次氯酸盐具有强氧化性 用作杀菌消毒剂、漂白剂
(10)碘酸钾在常温下稳定 食盐中的加碘物质
(11)氮气的化学性质稳定 作保护气
(12)氦气化学性质稳定、密度小 可用于填充飞艇、气球
(13)草木灰和硫酸铵反应生成氨气 草木灰和硫酸铵不能混合施用
(14)NH HCO 、NH NO 是可溶的含氮化合物 用作氮肥
4 3 4 3
(15)浓氨水具有挥发性和还原性 检验输送Cl 的管道是否漏气
2
(16)SO 具有漂白性 用来漂白纸浆、毛、丝等
2
(17)硅酸钠的水溶液黏结力强、不易燃烧 用作黏合剂、防火剂
(18)干冰升华吸收大量的热 用于人工降雨
(19)液氨汽化吸收大量的热 用作制冷剂
3.常考原料预处理阶段各操作的目的微专题突破5 无机物的性质、转化与应用 问题的态度:问则少;辩则明
研磨、粉碎等 增大反应物的接触面积,增大反应速率,提高原料转化率、利用率、浸取率
灼烧(煅烧、焙烧) 除去有机物;使无机物分解为金属氧化物等,便于后续浸取、溶解
水浸 分离水溶性和非水溶性的物质
浸取 酸浸 溶解金属、金属氧化物、调节pH促进某离子的水解而转化为沉淀
碱浸 除去油污、溶解酸性氧化物、溶解铝及其化合物、调节pH等
考考位位位
1.(2024·江苏卷)下列化学反应表示正确的是
A.汽车尾气处理:2NO+4CO=====N+4CO
2 2
B.NO -电催化为N 的阳极反应:2NO -+12H++10e—=N↑+6HO
3 2 3 2 2
C.硝酸工业中NH 的氧化反应:4NH +3O=====2N+6HO
3 3 2 2 2
D.CO 和H 催化制二甲醚:2CO+6H催化剂高温、CHOCH +3HO
2 2 2 2———高压 3 3 2
2.(2024·江苏卷)在给定条件下,下列制备过程涉及的物质转化均可实现的是
A.HCl制备:NaCl溶液电解—\s\up 4()H 和Cl 点燃—\s\up 4()HCl
—→ 2 2 —→
B.金属Mg制备:Mg(OH) 盐酸—\s\up 4()MgCl 溶液电解—\s\up 4()Mg
2 —→ 2 —→
C.纯碱工业:NaCl溶液C —— O → 2\s\up 4()NaHCO 3Δ — — → \s\up 4()Na 2 CO 3
D.硫酸工业:FeS O2—高 SO H2O\s\up 4()HSO
2—→ 温 2——→ 2 4
【问题解决1】
(2023·江苏卷)下列物质结构与性质或物质性质与用途具有对应关系的是
A.H 具有还原性,可作为氢氧燃料电池的燃料
2
B.氨极易溶于水,液氨可用作制冷剂
C.HO分子之间形成氢键,HO(g)的热稳定性比HS(g)的高
2 2 2
D.NH 中的N原子与H+形成配位键,NH 具有还原性
2 4 2 4
物质的性质与应用
1.常见杀菌剂、消毒剂、净水剂的性质及用途
性质 用途 物质
吸附性 作净水剂(混凝剂) 明矾、_______(水解生成胶体)
杀菌消毒 次氯酸钠、________、二氧化氯
氧化性
漂白剂 漂白粉、____________
氧化性、吸附性 杀菌消毒、新型净水剂 ___________
2.常见干燥剂、还原剂与食品安全
性质 用途 物质
化学性质稳定 作食品保护气 _______
吸水 可作(食品)干燥剂 ________、无水氯化钙、硅胶
还原性 食品的抗氧化剂 Fe、_________盐、酚类
既可以杀菌又具有还原性 在葡萄酒中可以微量添加 _______
3.生活、生产中物质的性质与用途
性质 用途 物质
化学性质稳定 治疗胃酸过多 Al(OH)
3
不稳定性 作焙制糕点的膨松剂 ___________
能与酸反应 胃酸中和剂 NaHCO 、___________
3
颜色 作红色颜料 ________
4HF+SiO=2HO+SiF↑ 刻蚀玻璃 _______
2 2 4
不燃不爆 可用作耐火材料、防腐剂 水玻璃(______钠)
质量轻、比能量大 可用作电池____极材料 锂
锌的活泼性大于铁 以减缓船体腐蚀 ____块
考点精练
1.(2023·海安高级中学高三下学期3月月考)硫及其化合物在生产、生活和科学研究中有着广泛的作用。
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找下列硫酸盐性质与用途具有对应关系的是
A.CuSO 水溶液呈酸性,可用作杀菌剂
4
B.FeSO 具有还原性,可用作治疗贫血药剂
4
C.BaSO 具有氧化性,可用于制取BaS
4
D.Al (SO ) 易溶于水,可用作净水剂
2 4 3
2.(2023·淮阴中学高三下学期最后一模)已知:BF 极易水解生成HBF 和硼酸(HBO);硼酸和甲醇在
3 4 3 3
浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH )],硼酸甲酯主要用作热稳定剂、木材防腐剂等;GaN的结构与
3 3
晶体硅类似,是第三代半导体研究的热点。下列物质性质与用途具有对应关系的是
A.BF 极易水解,可用作催化剂
3
B.硼酸甲酯具有挥发性,可用作木材防腐剂
C.GaN硬度大,可用作半导体材料
D.Al O 熔点高,可用作耐火材料
2 3
3.(2024·泰州市下学期一模)下列物质的结构、性质、用途具有对应关系的是
A.浓硫酸具有脱水性,可用于干燥Cl
2
B.ClF 具有强氧化性,可用作火箭助燃剂
3
C.冰晶石微溶于水,可用作电解铝工业的助熔剂
D.HF分子之间形成氢键,HF(g)的热稳定性比HCl(g)的高
【问题解决2】
(2023·江苏南通市模拟)在给定条件下,下列选项所示的物质间转化能实现的是
A.MnO ――→Cl B.FeCl (aq)――→FeCl (s)
2 2 3 3
C.KFeO――→O D.MgCl (aq)――→Mg
2 4 2 2
无机物的性质与转化
1.课本中金属与非金属及其化合物的转化
①金属——钠的、镁、铝、铁、铜及其化合物
②非金属——氯、硫、氮、碳与硅及其化合物
③化工生产——以海水为资源:候氏制碱法、氯碱工业、溴水提溴、提碘;以空气为资源:硝酸制备;以
矿石为资源:硫酸制备、铝、硅制备、硅酸盐工业(玻璃生产)
2.关注以下转化中的易错点
①反应原理——反应产物是否符合事实:如S与O 产物不是SO ,N 与O 不是NO ,I 与铁是FeI 而Cl、
2 3 2 2 2 2 2 2
Br 与Fe则是FeCl 、FeBr ;Al O、SiO 等与HO是不反应的;SO 、CO 与BaCl 溶液是不反应的。
2 3 3 2 3 2 2 2 2 2
②反应条件:如N 与O 是放电而不是加热,MnO 只与浓的盐酸反应且需加热。
2 2 2
③某些易水解的挥发酸盐或结晶水合物:如 FeCl (aq)加热得不到FeCl ,MgCl •6HO直接加热得不到
3 3 2 2
MgCl (应HCl气流中加热)。
2
考点精练
1.(2023·海安高级中学高三下学期3月月考)硫及其化合物在生产、生活和科学研究中有着广泛的作用。
可以用CuSO 溶液除去HS气体,生成黑色CuS沉淀。在给定条件下,下列物质间所示的转化可以实现的是
4 2
A.CaS(s)――――→HS(g) B.CuS(s)――――→HS(g)
2 2
C.SO (g)―――→HSO (aq) D.Cu(s)―――→SO (g)
2 2 4 2
2.(2024·江苏徐州模拟预测)在给定条件下,下列选项所示的物质间转化能实现的是
A.MgCl (aq)石灰乳\s\up 4()Mg(OH) 煅烧—\s\up 4()MgO B.Ca(OH) Cl2\s\up 4()Ca(ClO) 过量S\s\up
2 ——— 2 —→ 2——→ 2O2—
4()HClO
C.Fe
2
O
3
盐
—
酸
→
—\s\up 4()FeCl
3
(aq)蒸
—
发
→
—\s\up 4()FeCl
3
(s) D.CuSO
4
N
H
a
(
O
a
\s\up 4()Cu(OH)
2
悬浊液蔗
—
糖
→
—Δ
Cu O
2
【问题解决3】
(2023·江苏)下列化学反应表示正确的是
A.水煤气法制氢:C(s)+HO(g)=H(g)+CO(g) ΔH=-131.3 kJ·mol-1
2 2
B.HCO催化加氢生成HCOO-的反应:HCO+H=====HCOO-+HO
2 2
C.电解水制氢的阳极反应:2HO-2e-=H↑+2OH-
2 2
D.CaH 与水反应:CaH+2HO=Ca(OH)+H↑
2 2 2 2 2微专题突破5 无机物的性质、转化与应用 问题的态度:问则少;辩则明
化学反应表达式
1.熟记课本上的方程式。
2.据题中所给的信息结合有关原理,判断方程式正确否。
考点精练
1.(2024·江苏南通二模)下列化学反应表示正确的是
A.电解饱和食盐水制备Cl 的离子方程式:2Cl-+2H+====Cl↑+H↑
2 2 2
B.将氯水在强光下照射的化学方程式:2HClO====Cl↑+2HO
2 2
C.氨气检验Cl 泄露的化学方程式:3Cl+8NH =N+6NH Cl
2 2 3 2 4
D.Cl 处理含氰碱性废水的离子方程式:5Cl+2CN-+4HO=10Cl-+N↑+2CO↑+8H+
2 2 2 2 2
2.(2024·南通市海门市第一次调研)周期表中VIA族元素及其化合物应用广泛。 O、 O、 O是氧元素
186 187 188
的3种核素,可以形成多种重要的化合物。亚硫酰氯(SOCl )为黄色液体,其结构式为( ),遇水发生
2
水解。工业上可电解HSO 与(NH )SO 混合溶液制备过二硫酸铵[(NH )SO],过二硫酸铵与双氧水中都含有
2 4 4 2 4 4 2 2 8
过氧键(-O-O-)。硝化法制硫酸的主要反应为:NO (g)+SO (g)=SO (g)+NO(g) ∆H=+41.8 kJ·mol-
2 2 3
1。SO 和SO 都是酸性氧化物,是制备硫酸的中间产物。下列化学反应表示正确的是
2 3
A.HO 氧化酸性废水中的Fe2+离子方程式:2Fe2++HO=2Fe3++2OH-
2 2 2 2
B.氢氧化钠吸收足量二氧化硫的离子方程式:2OH-+SO =SO2-+HO
2 3 2
C.亚硫酰氯水解的反应方程式:SOCl +2HO=HSO +2HCl
2 2 2 4
D.电解法制备(NH )SO 时的阳极反应:2SO 2--2e—=SO2-
4 2 2 8 4 2 8
3.(2024•南通市海安市高三上学期开学考)B、Al、Ga位于元素周期表中ⅢA族。BF 为无色气体,主
3
要用作有机合成中的催化剂,极易水解生成HBF (HBF 在水中完全电离为H+和BF-)和硼酸(HBO)。硼酸是
4 4 4 3 3
一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH )],硼酸甲酯主要用作热稳
3 3
定剂、木材防腐剂等。高温下Al O 和焦炭在氯气的氛围中获得AlCl 。GaN的结构与晶体硅类似,是第三代半
2 3 3
导体研究的热点。下列化学反应表示不正确的是
A.制备B(OCH ):HBO+3CHOH========B(OCH )↑+3HO
3 3 3 3 3 3 3 2
B.BF 和NaOH溶液反应:4BF+6OH-=3BF-+BO3-+3HO
3 3 4 3 2
C.高温下Al O、焦炭在氯气中反应:2Al O+3C+3Cl====2AlCl +3CO
2 3 2 3 2 3
D.电解Al O(熔融)制备Al的阳极反应:2O2--4e—=O↑
2 3 2
【问题解决4】
某工厂采用辉铋矿(主要成分为BiS ,含有FeS 、SiO 杂质)与软锰矿(主要成分为MnO )联合焙烧法制备
2 3 2 2 2
BiOCl,工艺流程如图所示。焙烧时过量的MnO 分解为MnO ,金属活动性:Fe>(H)>Bi>Cu。下列说法错
2 2 3
误的是
A.通过“联合焙烧”BiS 和FeS 分别转化为BiO、Fe O
2 3 2 2 3 2 3
B.“水浸”所得滤液的主要溶质是MnSO
4
C.“酸浸”所得滤渣的主要成分是SiO,气体A为Cl
2 2
D.向“酸浸”所得滤液中加入金属Bi的目的是消耗H+,促进Bi3+水解
无机化工微流程图
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找四线分析法
试剂线 分清各步加入试剂的作用,一般是为了除去杂质或进行目标元素及其化合物间的转化等
操作线 分离杂质和产品需要进行的分离、提纯操作等
杂质线 分清各步去除杂质的种类,杂质的去除顺序、方法及条件等
关注目标元素及其化合物在各步发生的反应或进行分离、提纯的操作方法,实质是目标
产品线
元素及其化合物的转化
考点精练
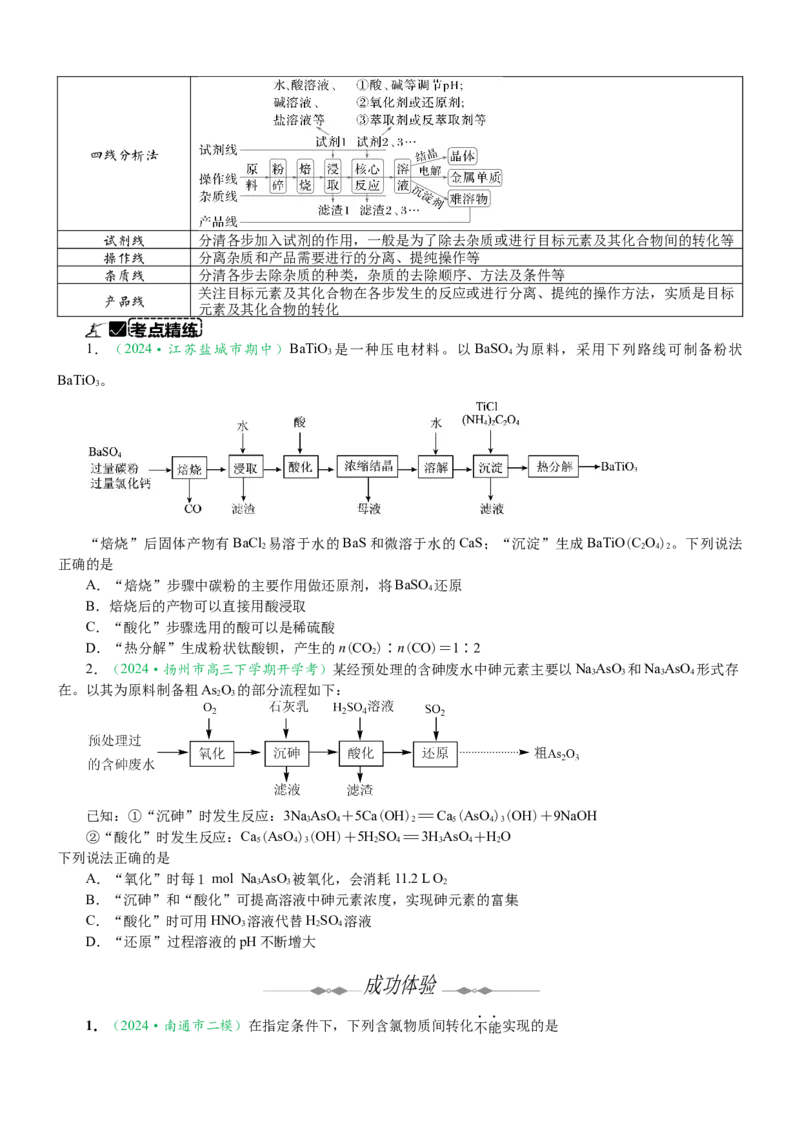
1.(2024·江苏盐城市期中)BaTiO 是一种压电材料。以BaSO 为原料,采用下列路线可制备粉状
3 4
BaTiO 。
3
“焙烧”后固体产物有BaCl 易溶于水的BaS和微溶于水的CaS;“沉淀”生成BaTiO(C O) 。下列说法
2 2 4 2
正确的是
A.“焙烧”步骤中碳粉的主要作用做还原剂,将BaSO 还原
4
B.焙烧后的产物可以直接用酸浸取
C.“酸化”步骤选用的酸可以是稀硫酸
D.“热分解”生成粉状钛酸钡,产生的n(CO)∶n(CO)=1∶2
2
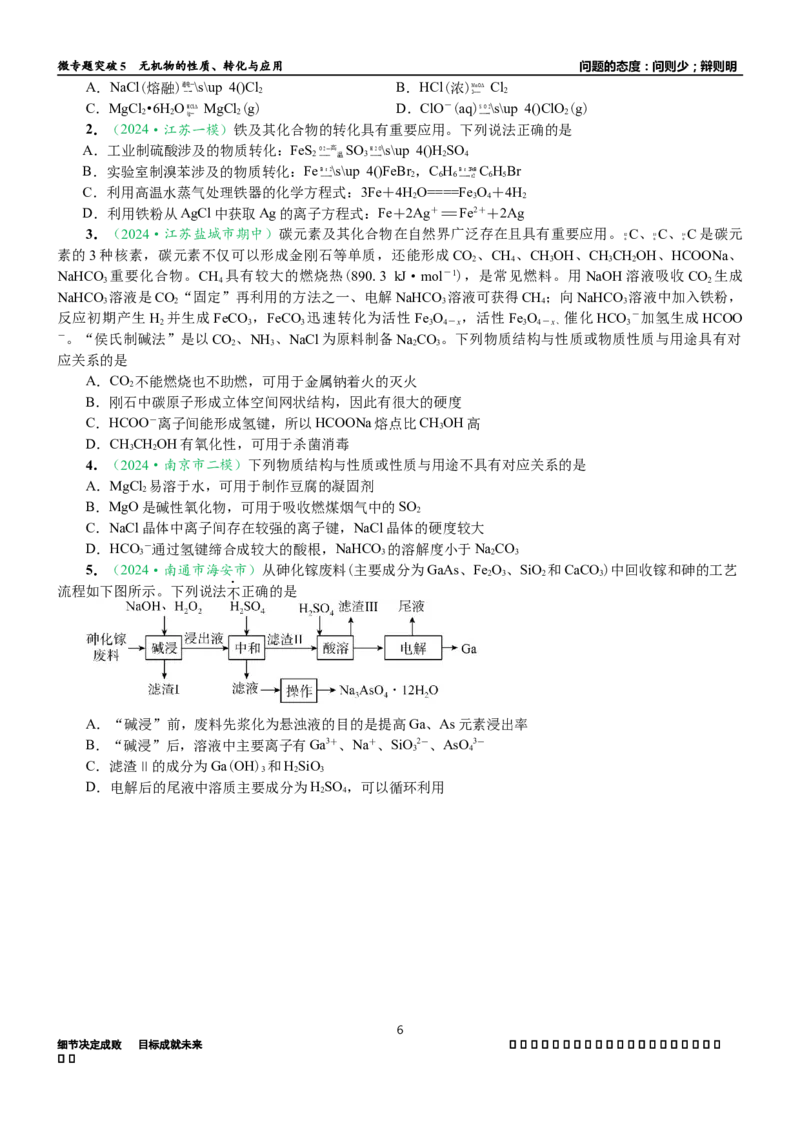
2.(2024·扬州市高三下学期开学考)某经预处理的含砷废水中砷元素主要以NaAsO 和NaAsO 形式存
3 3 3 4
在。以其为原料制备粗As O 的部分流程如下:
2 3
已知:①“沉砷”时发生反应:3NaAsO+5Ca(OH)=Ca (AsO )(OH)+9NaOH
3 4 2 5 4 3
②“酸化”时发生反应:Ca (AsO )(OH)+5HSO =3HAsO+HO
5 4 3 2 4 3 4 2
下列说法正确的是
A.“氧化”时每1 mol NaAsO 被氧化,会消耗11.2 L O
3 3 2
B.“沉砷”和“酸化”可提高溶液中砷元素浓度,实现砷元素的富集
C.“酸化”时可用HNO 溶液代替HSO 溶液
3 2 4
D.“还原”过程溶液的pH不断增大
成功体验
1.(2024·南通市二模)在指定条件下,下列含氯物质间转化不能实现的是微专题突破5 无机物的性质、转化与应用 问题的态度:问则少;辩则明
A.NaCl(熔融)通 — 电 → —\s\up 4()Cl 2 B.HCl(浓)M 2— n — OΔ Cl 2
C.MgCl 2 •6H 2 OH (g C — lΔ MgCl 2 (g) D.ClO-(aq)S —— O → 2\s\up 4()ClO 2 (g)
2.(2024·江苏一模)铁及其化合物的转化具有重要应用。下列说法正确的是
A.工业制硫酸涉及的物质转化:FeS 2O —— 2— — 高 温 SO 3H —— 2 → O\s\up 4()H 2 SO 4
B.实验室制溴苯涉及的物质转化:FeB —— r → 2\s\up 4()FeBr 2 ,C 6 H 6B —— r → 2F r e 2 BC 6 H 5 Br
C.利用高温水蒸气处理铁器的化学方程式:3Fe+4HO====Fe O+4H
2 3 4 2
D.利用铁粉从AgCl中获取Ag的离子方程式:Fe+2Ag+=Fe2++2Ag
3.(2024·江苏盐城市期中)碳元素及其化合物在自然界广泛存在且具有重要应用。 C、 C、 C是碳元
162 163 164
素的3种核素,碳元素不仅可以形成金刚石等单质,还能形成CO 、CH 、CHOH、CHCHOH、HCOONa、
2 4 3 3 2
NaHCO 重要化合物。CH 具有较大的燃烧热(890.3 kJ·mol-1),是常见燃料。用NaOH溶液吸收CO 生成
3 4 2
NaHCO 溶液是CO“固定”再利用的方法之一、电解NaHCO 溶液可获得CH ;向NaHCO 溶液中加入铁粉,
3 2 3 4 3
反应初期产生H 并生成FeCO ,FeCO 迅速转化为活性Fe O ,活性Fe O 催化HCO -加氢生成HCOO
2 3 3 3 4-x 3 4-x、 3
-。“侯氏制碱法”是以CO 、NH 、NaCl为原料制备NaCO 。下列物质结构与性质或物质性质与用途具有对
2 3 2 3
应关系的是
A.CO 不能燃烧也不助燃,可用于金属钠着火的灭火
2
B.刚石中碳原子形成立体空间网状结构,因此有很大的硬度
C.HCOO-离子间能形成氢键,所以HCOONa熔点比CHOH高
3
D.CHCHOH有氧化性,可用于杀菌消毒
3 2
4.(2024·南京市二模)下列物质结构与性质或性质与用途不具有对应关系的是
A.MgCl 易溶于水,可用于制作豆腐的凝固剂
2
B.MgO是碱性氧化物,可用于吸收燃煤烟气中的SO
2
C.NaCl晶体中离子间存在较强的离子键,NaCl晶体的硬度较大
D.HCO -通过氢键缔合成较大的酸根,NaHCO 的溶解度小于NaCO
3 3 2 3
5.(2024·南通市海安市)从砷化镓废料(主要成分为GaAs、Fe O、SiO 和CaCO)中回收镓和砷的工艺
2 3 2 3
流程如下图所示。下列说法不正确的是
A.“碱浸”前,废料先浆化为悬浊液的目的是提高Ga、As元素浸出率
B.“碱浸”后,溶液中主要离子有Ga3+、Na+、SiO2-、AsO3-
3 4
C.滤渣Ⅱ的成分为Ga(OH) 和HSiO
3 2 3
D.电解后的尾液中溶质主要成分为HSO ,可以循环利用
2 4
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找