文档内容
押江苏卷第 3、11 题
化学实验基础
核心考点 考情统计 考向预测 备考策略
2023·江苏卷,3 1.重点关注实验室常用化学仪器
实验装置图与
的主要用途和使用方法。掌握化学
基本操作、物 2022·江苏卷,4
实验的基本操作。能综合运用物质
质制备
2021·江苏卷,3 主要有实验装置的使用,气体制备 的不同性质对常见的物质进行分离
和收集,表格型与实验操作、现象 和提纯。
表格型实验方 与结论相关实验方案的设计与评价 2.掌握评价检验类化学实验方案
案的设计---实
2023·江苏卷,11
设计的一般思路。掌握评价性质探
验操作、现象 2022·江苏卷,11 究类化学实验方案设计的一般思
与结论 路。
1.(2023·江苏卷,3)实验室制取 的实验原理及装置均正确的是
A.制取 B.除去 中的HCl C.收集 D.吸收尾气中的
2.(2023·江苏卷,11)室温下,探究 溶液的性质,下列实验方案能达到探究目的的是选
探究目的 实验方案
项
向 溶液中滴加几滴新制氯水,再滴加KSCN溶液,观察溶液颜
A 溶液中是否含有
色变化
B 是否有还原性 向 溶液中滴加几滴酸性 溶液,观察溶液颜色变化
C 是否水解 向 溶液中滴加2~3滴酚酞试液,观察溶液颜色变化
能否催化 分
D 向 溶液中滴加几滴 溶液,观察气泡产生情况
解
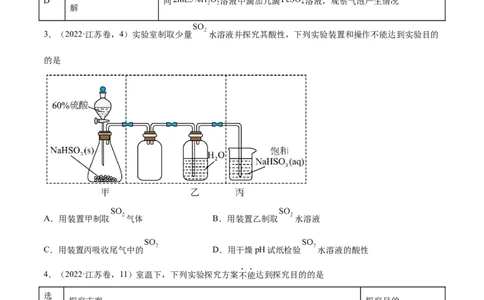
3.(2022·江苏卷,4)实验室制取少量 水溶液并探究其酸性,下列实验装置和操作不能达到实验目的
的是
A.用装置甲制取 气体 B.用装置乙制取 水溶液
C.用装置丙吸收尾气中的 D.用干燥pH试纸检验 水溶液的酸性
4.(2022·江苏卷,11)室温下,下列实验探究方案不能达到探究目的的是
选
探究方案 探究目的
项
A 向盛有 溶液的试管中滴加几滴 溶液,振荡,再滴加几滴新制氯 具有还原性
水,观察溶液颜色变化
向盛有 水溶液的试管中滴加几滴品红溶液,振荡,加热试管,观察溶液
B 具有漂白性
颜色变化
C 向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 的氧化性比 的
强D 用pH计测量醋酸、盐酸的pH,比较溶液pH大小 是弱电
解质
5.(2021·江苏卷,3)下列由废铜屑制取CuSO ·5H O的实验原理与装置不能达到实验目的的是
4 2
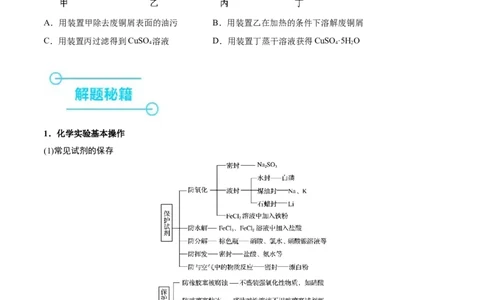
A.用装置甲除去废铜屑表面的油污 B.用装置乙在加热的条件下溶解废铜屑
C.用装置丙过滤得到CuSO 溶液 D.用装置丁蒸干溶液获得CuSO ·5H O
4 4 2
1.化学实验基本操作
(1)常见试剂的保存
(2)熟记典型的实验操作
①测定溶液pH的操作
将一小块pH试纸放在干燥洁净的表面皿上,用洁净干燥的玻璃棒蘸取少量待测液点到 pH试纸中央,待变
色稳定后再和标准比色卡对照,读出对应的pH。
②滴定管赶气泡的操作
a酸式滴定管:右手将滴定管倾斜30°左右,左手迅速打开活塞使溶液冲出,从而使溶液充满尖嘴。b碱式滴定管:将胶管弯曲使玻璃尖嘴向上倾斜,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出,
即可赶出碱式滴定管中的气泡。
③萃取分离操作
关闭分液漏斗活塞,将混合液倒入分液漏斗中,塞上塞子,用右手食指顶住塞子,左手握住活塞部分,将
分液漏斗倒置振荡,振荡后打开活塞,使漏斗内气体放出,静置、分层,在漏斗下面放一个小烧杯,先打
开上口塞子再打开分液漏斗活塞,使下层液体从下口沿烧杯壁流下,下层液体流出后,关闭活塞,上层液
体从上口倒出。
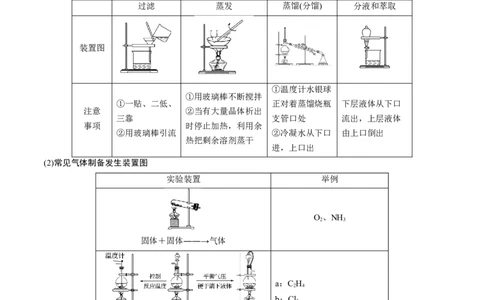
2.典型气体制备、净化、收集、尾气处理装置
(1)常见的物质分离装置
过滤 蒸发 蒸馏(分馏) 分液和萃取
装置图
①温度计水银球
①用玻璃棒不断搅拌
①一贴、二低、 正对着蒸馏烧瓶 下层液体从下口
注意 ②当有大量晶体析出
三靠 支管口处 流出,上层液体
事项 时停止加热,利用余
②用玻璃棒引流 ②冷凝水从下口 由上口倒出
热把剩余溶剂蒸干
进,上口出
(2)常见气体制备发生装置图
实验装置 举例
O、NH
2 3
固体+固体――→气体
a:C H
2 4
b:Cl
2
固体+液体(或液体+液体)――→气体
a:H、O、CO、Cl、NH
2 2 2 2 3
b:H、CO
2 2
固体+液体(不加热)―→气体
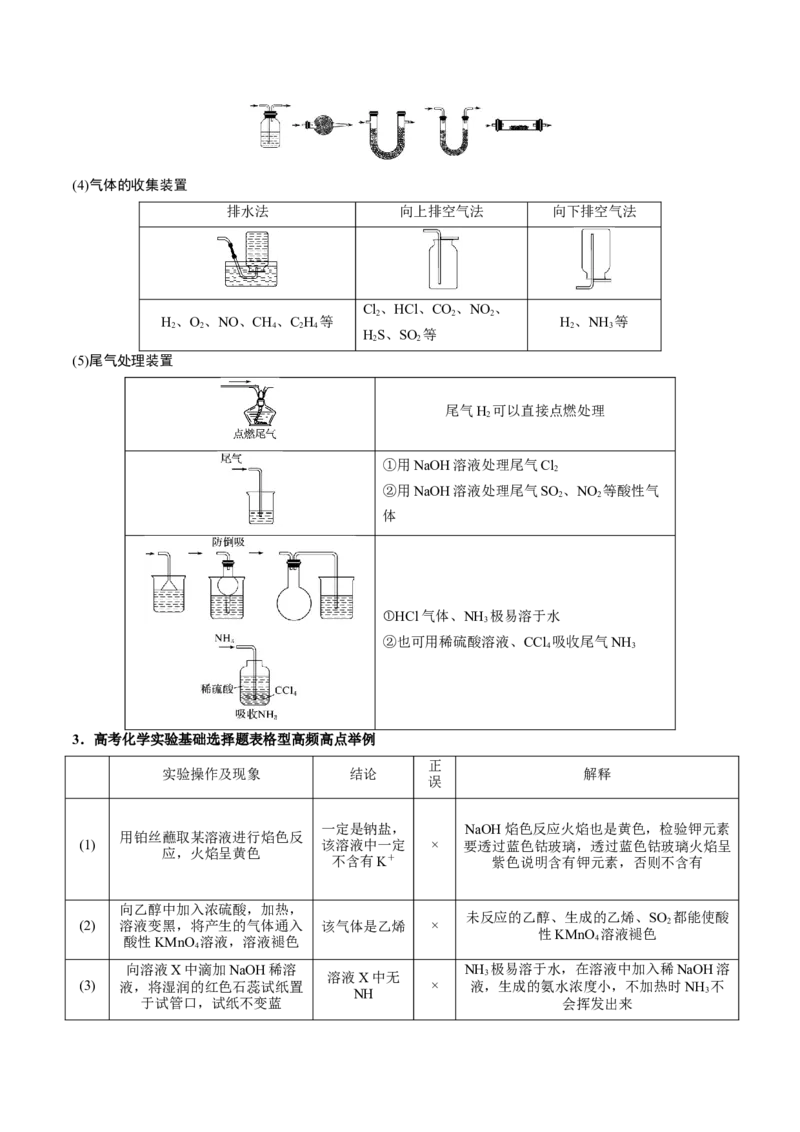
(3)常见的净化装置——用于除去气体中的杂质气体(4)气体的收集装置
排水法 向上排空气法 向下排空气法
Cl、HCl、CO、NO 、
2 2 2
H、O、NO、CH、C H 等 H、NH 等
2 2 4 2 4 2 3
HS、SO 等
2 2
(5)尾气处理装置
尾气H 可以直接点燃处理
2
①用NaOH溶液处理尾气Cl
2
②用NaOH溶液处理尾气SO 、NO 等酸性气
2 2
体
①HCl气体、NH 极易溶于水
3
②也可用稀硫酸溶液、CCl 吸收尾气NH
4 3
3.高考化学实验基础选择题表格型高频高点举例
正
实验操作及现象 结论 解释
误
一定是钠盐, NaOH焰色反应火焰也是黄色,检验钾元素
用铂丝蘸取某溶液进行焰色反
(1) 该溶液中一定 × 要透过蓝色钴玻璃,透过蓝色钴玻璃火焰呈
应,火焰呈黄色
不含有K+ 紫色说明含有钾元素,否则不含有
向乙醇中加入浓硫酸,加热,
未反应的乙醇、生成的乙烯、SO 都能使酸
(2) 溶液变黑,将产生的气体通入 该气体是乙烯 × 2
性KMnO 溶液褪色
酸性KMnO 溶液,溶液褪色 4
4
向溶液X中滴加NaOH稀溶 NH 极易溶于水,在溶液中加入稀NaOH溶
溶液X中无 3
(3) 液,将湿润的红色石蕊试纸置 × 液,生成的氨水浓度小,不加热时NH 不
NH 3
于试管口,试纸不变蓝 会挥发出来淀粉碘化钾试纸检验的是具有强氧化性的气
用湿润的淀粉碘化钾试纸检验
(4) 该气体是Cl × 体,Y可能是Cl,也可能是O、NO 等气
气体Y,试纸变蓝 2 2 3 2
体
将某气体通入品红溶液中,品 该气体一定是
(5) × O、Cl 也能使品红溶液褪色
红溶液褪色 SO 3 2
2
向溶液Y中滴加硝酸,再滴加 Y中一定含有 若溶液Y中含有SO,滴加硝酸时能被氧化
(6) ×
BaCl 溶液,有白色沉淀生成 SO 成SO,加入BaCl 也会有白色沉淀产生
2 2
蘸有浓氨水的玻璃棒靠近溶液 X一定是浓盐 只要是挥发性的浓酸遇蘸有浓氨水的玻璃棒
(7) ×
X,有白烟产生 酸 都能产生白烟,浓盐酸、浓硝酸都符合
稀硫酸在淀粉水解中作催化剂,在未中和硫
在淀粉溶液中加入适量稀硫酸
酸的情况下加入的新制Cu(OH) 悬浊液会与
微热,向水解后的溶液中加入 说明淀粉未水 2
(8) × 硫酸反应生成CuSO ,在加热时得不到沉
新制Cu(OH) 悬浊液并加热, 解 4
2 淀,应该先加氢氧化钠中和硫酸后再加新制
无砖红色沉淀
Cu(OH) 悬浊液
2
向某溶液中滴加KSCN溶液,
该溶液中一定
(9) 溶液不变色,滴加氯水后溶液 √ Fe2+的检验方法正确
含Fe2+
显红色
说明 溶解度大的物质容易向溶解度小的转化;但
在硫酸钡沉淀中加入浓碳酸钠
K 相近时,溶解度小的物质也能向溶解度
(10) 溶液充分搅拌后,取沉淀(洗 K (BaCO) < × sp
sp 3 大的转化,如K (BaSO) 挥发出的CH3COOH,变浑浊可能是因为
(14) 酸,将产生的气体直接通入苯 ×
碳酸>苯酚 CO,也可能是因为CHCOOH,无法比较
酚钠溶液中,产生白色浑浊 2 3
碳酸与苯酚的酸性强弱
将Fe(NO ) 样品溶于稀硫酸 在Fe(NO ) 中加入稀硫酸后,Fe2+能被H
3 2 Fe(NO ) 晶体 3 2
(15) 后,滴加KSCN溶液,溶液变 3 2 × +、NO(两者同时存在相当于HNO)氧化成
已氧化变质 3
红 Fe3+而干扰实验
SO 通入溴水(或碘水或酸性高 SO 在反应中作还原剂,体现的是还原性而
(16) 2 SO 有漂白性 × 2
锰酸钾溶液)中,溴水褪色 2 不是漂白性向某溶液中加入稀盐酸,产生
该溶液一定是 碳酸氢盐、亚硫酸盐、亚硫酸氢盐溶液也有
(17) 的气体通入澄清石灰水中,石 ×
碳酸盐溶液 相同现象
灰水变浑浊
乙酸与乙酸乙酯互溶,不能用分液的方法分
(18) 分离乙酸和乙酸乙酯 用分液法 ×
离
制备Fe(OH) 胶体:0.1 mol·L-
3
(19) 1 FeCl 3 溶液与0.3 mol·L-1 有胶体生成 × 将饱和FeCl 3 溶液滴入沸水中,继续煮沸至
液体呈透明的红褐色,即得到Fe(OH 胶体
)3
NaOH溶液等体积混合
向两份蛋白质溶液中分别滴加
蛋白质均发生 向蛋白质溶液中加入饱和氯化钠溶液,发生
(20) 饱和NaCl溶液和CuSO 溶 ×
4 变性 盐析
液,均有固体析出
考点一 实验装置图与基本操作、物质制备
1.(2024·江苏百师联盟开学摸底)下列实验中,所选用的实验仪器(夹持装置略)正确的是
A.灼烧干海带:选用①、⑦
B.NaCl溶液的蒸发结晶:选用①、⑥、⑦
C.配制100mL 的NaOH溶液:选用③、⑤、⑥
D.分离苯和 的混合液:选用③、④、⑥
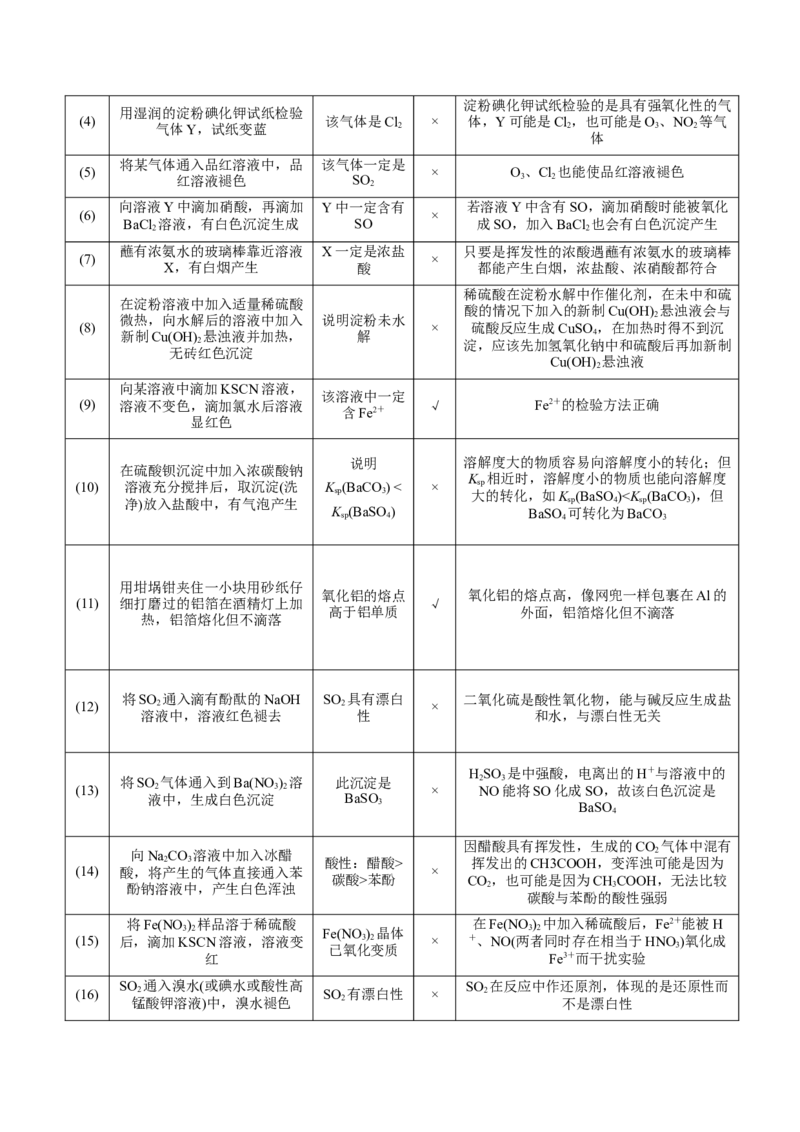
2.(2024·江苏扬州期末)PH 气体微溶于水,有强还原性,可由反应P+3KOH+3HO=====PH ↑+
3 4 2 3
3KHPO 制得。实验室制取少量PH 的原理及装置均正确的是
2 2 3A.制取PH B.干燥PH C.收集PH D.吸收尾气中的PH
3 3 3 3
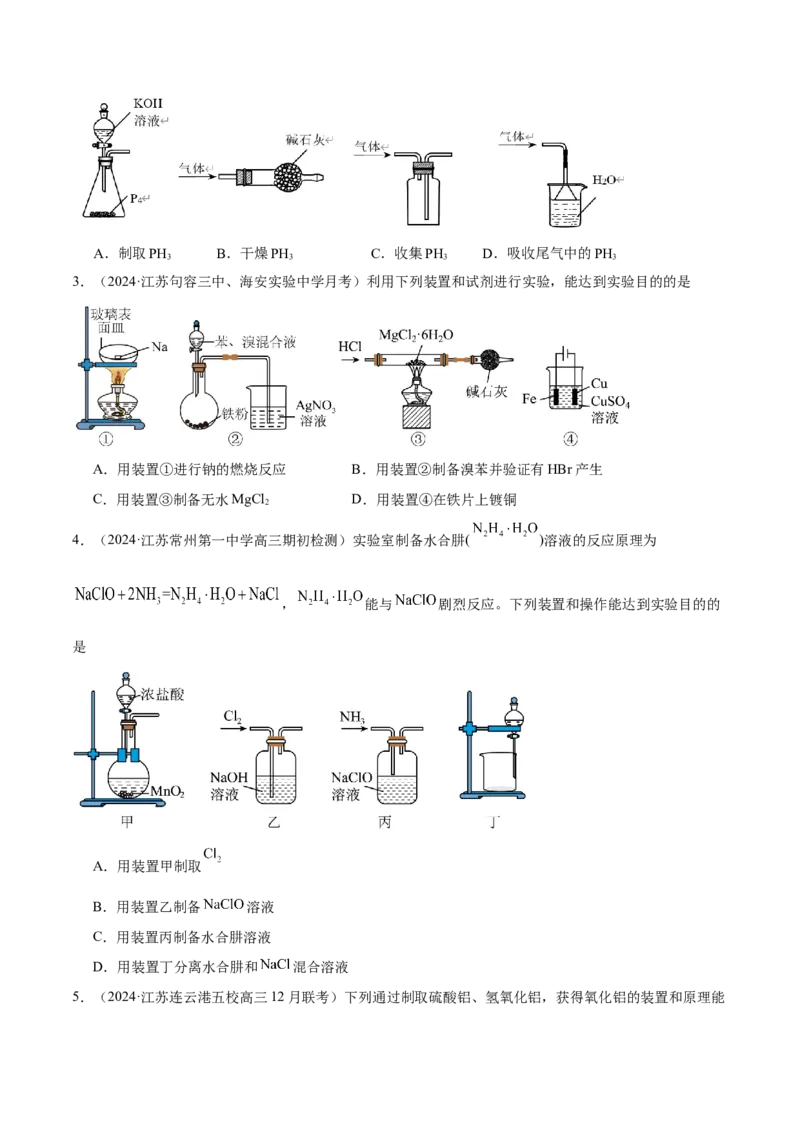
3.(2024·江苏句容三中、海安实验中学月考)利用下列装置和试剂进行实验,能达到实验目的的是
A.用装置①进行钠的燃烧反应 B.用装置②制备溴苯并验证有HBr产生
C.用装置③制备无水MgCl D.用装置④在铁片上镀铜
2
4.(2024·江苏常州第一中学高三期初检测)实验室制备水合肼( )溶液的反应原理为
, 能与 剧烈反应。下列装置和操作能达到实验目的的
是
A.用装置甲制取
B.用装置乙制备 溶液
C.用装置丙制备水合肼溶液
D.用装置丁分离水合肼和 混合溶液
5.(2024·江苏连云港五校高三12月联考)下列通过制取硫酸铝、氢氧化铝,获得氧化铝的装置和原理能达到实验目的的是
A B C D
制硫酸铝 制氢氧化铝 过滤氢氧化铝 灼烧制氧化铝
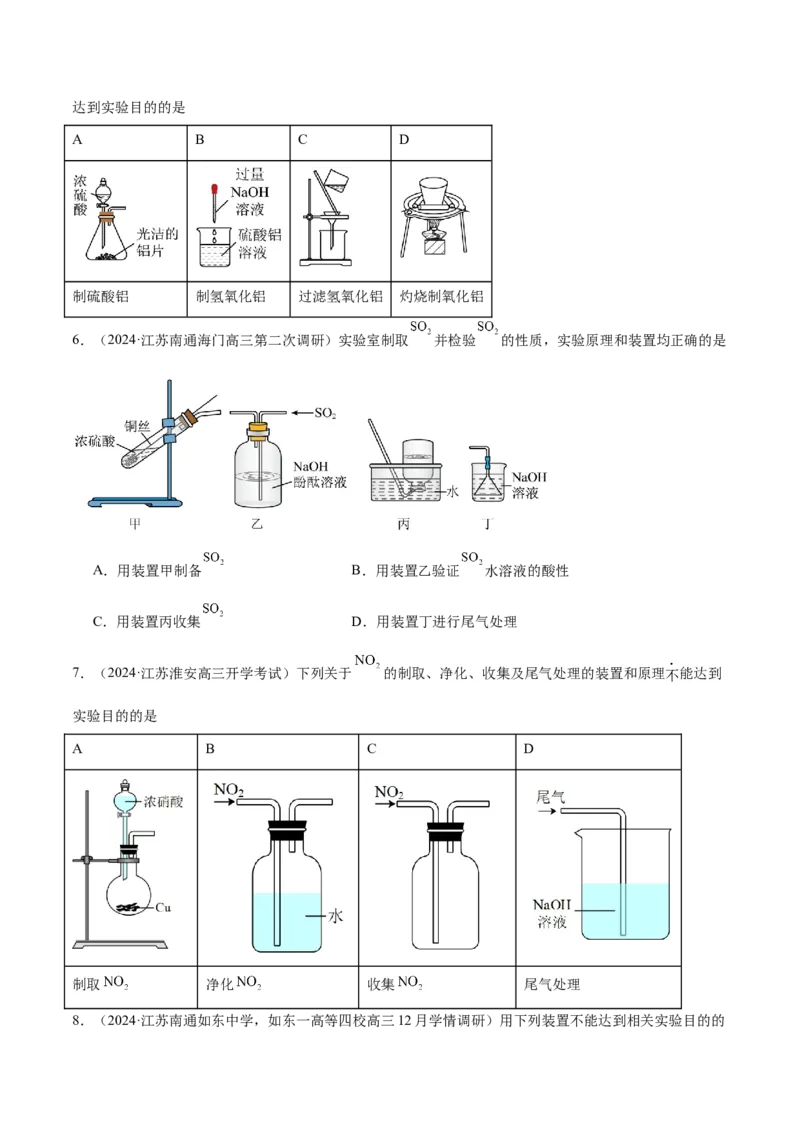
6.(2024·江苏南通海门高三第二次调研)实验室制取 并检验 的性质,实验原理和装置均正确的是
A.用装置甲制备 B.用装置乙验证 水溶液的酸性
C.用装置丙收集 D.用装置丁进行尾气处理
7.(2024·江苏淮安高三开学考试)下列关于 的制取、净化、收集及尾气处理的装置和原理不能达到
实验目的的是
A B C D
制取 净化 收集 尾气处理
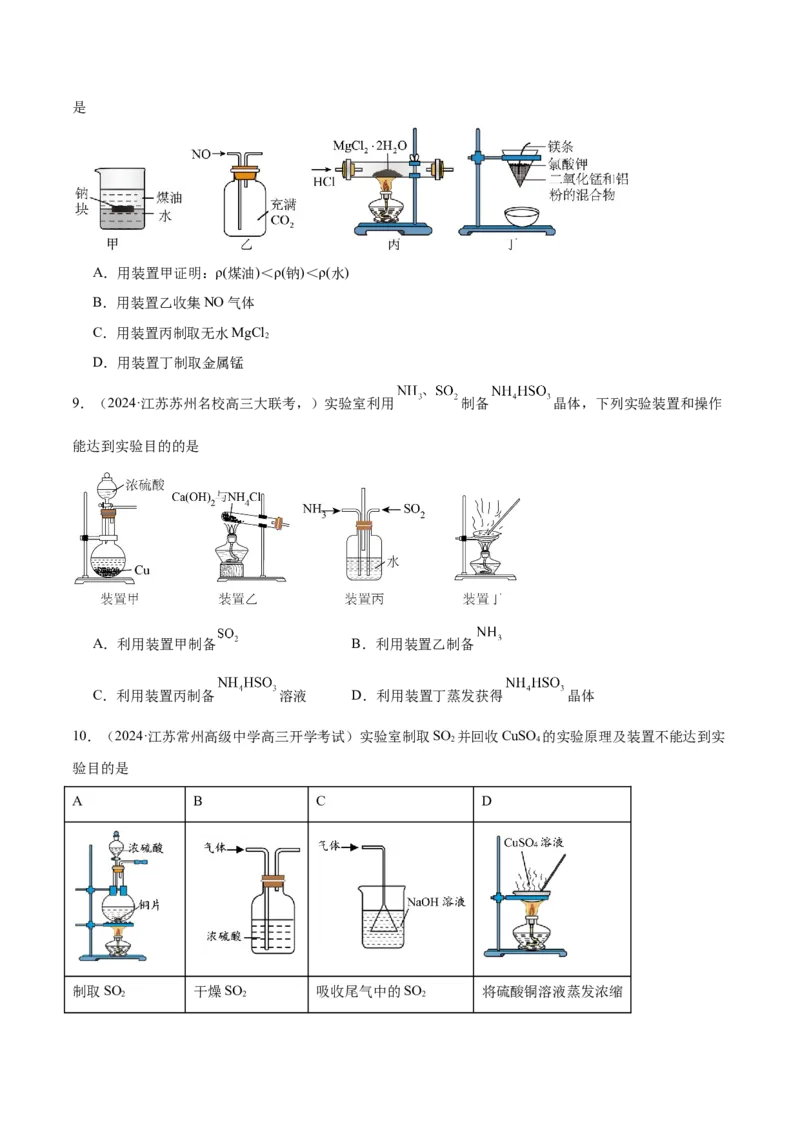
8.(2024·江苏南通如东中学,如东一高等四校高三12月学情调研)用下列装置不能达到相关实验目的的是
A.用装置甲证明:ρ(煤油)<ρ(钠)<ρ(水)
B.用装置乙收集NO气体
C.用装置丙制取无水MgCl
2
D.用装置丁制取金属锰
9.(2024·江苏苏州名校高三大联考,)实验室利用 制备 晶体,下列实验装置和操作
能达到实验目的的是
A.利用装置甲制备 B.利用装置乙制备
C.利用装置丙制备 溶液 D.利用装置丁蒸发获得 晶体
10.(2024·江苏常州高级中学高三开学考试)实验室制取SO 并回收CuSO 的实验原理及装置不能达到实
2 4
验目的是
A B C D
制取SO 干燥SO 吸收尾气中的SO 将硫酸铜溶液蒸发浓缩
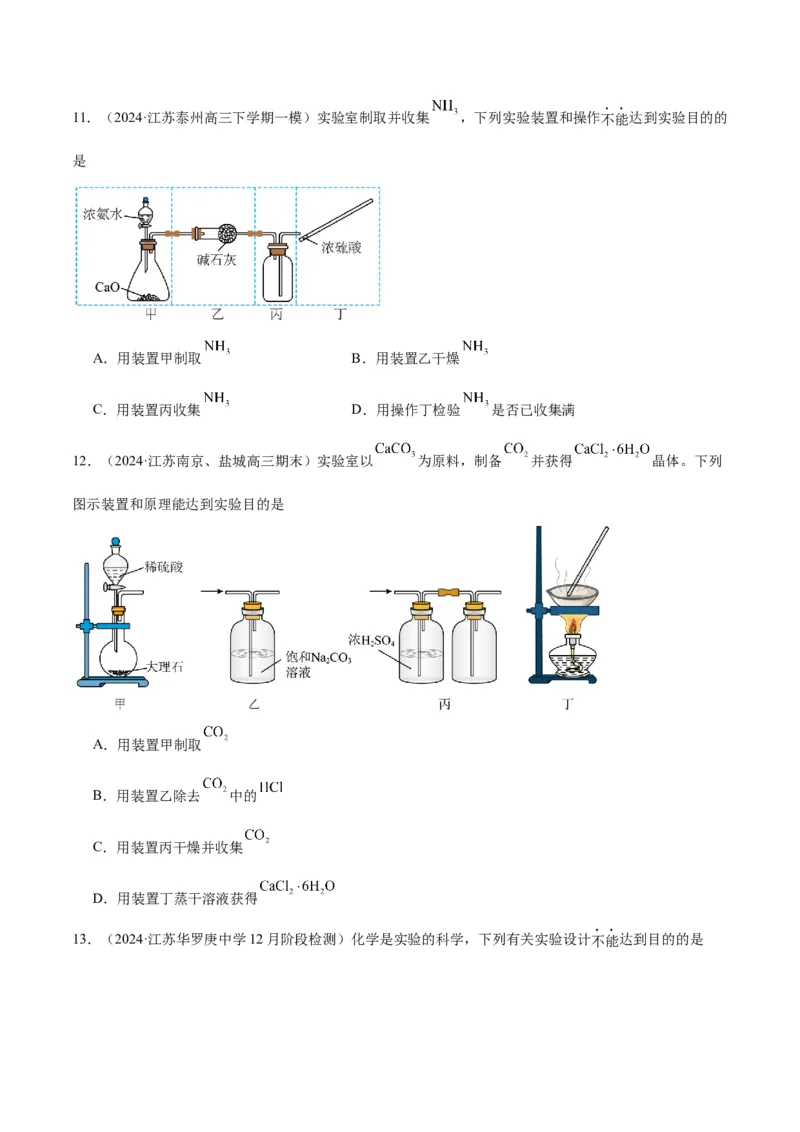
2 2 211.(2024·江苏泰州高三下学期一模)实验室制取并收集 ,下列实验装置和操作不能达到实验目的的
是
A.用装置甲制取 B.用装置乙干燥
C.用装置丙收集 D.用操作丁检验 是否已收集满
12.(2024·江苏南京、盐城高三期末)实验室以 为原料,制备 并获得 晶体。下列
图示装置和原理能达到实验目的是
A.用装置甲制取
B.用装置乙除去 中的
C.用装置丙干燥并收集
D.用装置丁蒸干溶液获得
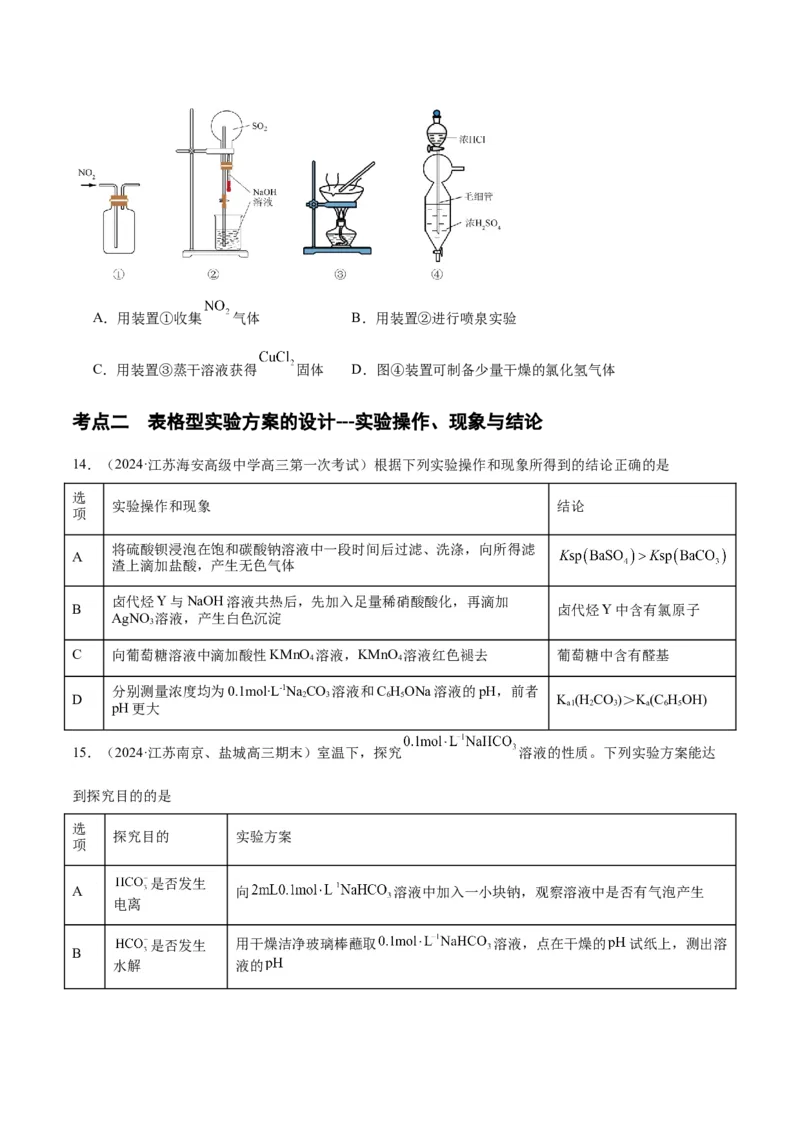
13.(2024·江苏华罗庚中学12月阶段检测)化学是实验的科学,下列有关实验设计不能达到目的的是A.用装置①收集 气体 B.用装置②进行喷泉实验
C.用装置③蒸干溶液获得 固体 D.图④装置可制备少量干燥的氯化氢气体
考点二 表格型实验方案的设计---实验操作、现象与结论
14.(2024·江苏海安高级中学高三第一次考试)根据下列实验操作和现象所得到的结论正确的是
选
实验操作和现象 结论
项
将硫酸钡浸泡在饱和碳酸钠溶液中一段时间后过滤、洗涤,向所得滤
A
渣上滴加盐酸,产生无色气体
卤代烃Y与NaOH溶液共热后,先加入足量稀硝酸酸化,再滴加
B 卤代烃Y中含有氯原子
AgNO 溶液,产生白色沉淀
3
C 向葡萄糖溶液中滴加酸性KMnO 溶液,KMnO 溶液红色褪去 葡萄糖中含有醛基
4 4
分别测量浓度均为0.1mol∙L-1NaCO 溶液和C HONa溶液的pH,前者
D 2 3 6 5 K (H CO)>K(C HOH)
pH更大 a1 2 3 a 6 5
15.(2024·江苏南京、盐城高三期末)室温下,探究 溶液的性质。下列实验方案能达
到探究目的的是
选
探究目的 实验方案
项
是否发生
A 向 溶液中加入一小块钠,观察溶液中是否有气泡产生
电离
是否发生 用干燥洁净玻璃棒蘸取 溶液,点在干燥的 试纸上,测出溶
B
水解 液的溶液中是否存在 取一支洁净的铂丝,蘸取 溶液后在煤气灯上灼烧,透过蓝色
C
钴玻璃观察火焰颜色
溶液中是否存在
D 向 溶液中滴入几滴澄清石灰水,观察溶液是否变浑浊
16.(2024·江苏泰州高三下学期一模)室温下,下列实验探究方案能够边到探究目的的是
选
探究方案 探究目的
项
将 溴丁烷与 的乙醇溶液混合后加热,生成的气体通入 溴丁烷能否发生消去反应生
A
的 溶液中,观察现象 成烯烃
B 将 气体通入紫色石蕊溶液中,观察溶液颜色变化 是否具有漂白性
比较 与 在水中
C 向饱和 溶液中通入足量 气体,观察现象
溶解度的大小
比较 与 氧化性的强弱
D 向 溶液中滴加淀粉,再通入 气体,观察现象
17.(2024·江苏扬州期末)25 ℃,探究0.1 mol·L−1 KHC O 溶液的性质。下列实验方案能达到探究目的
2 4
的是
选项 探究目的 实验方案
用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰
A 钾元素的焰色试验
的颜色
向2 mL KHC O 溶液中滴加氯水,再滴入AgNO 溶
2 4 3
B HC O是否有还原性 液,
2
观察是否有白色沉淀产生
向2 mL KHC O 溶液中滴加2~3滴酚酞试液,观察溶
2 4
C HC O是否水解
2
液颜色的变化
比较溶液中c(H C O)
2 2 4
D 用pH计测量0.1 mol·L−1 KHC O 溶液的pH
2 4
与c(C O)的大小
2
18.(2024·江苏句容三中、海安实验中学月考)下列实验的方案设计、现象和结论都正确的是
选
实验目的 实验方案设计 实验现象和结论
项
检验某固体试样中 取少量固体试样完全溶于盐酸,再滴加 没有出现血红色,说明该固体试样
A
是否存在三价铁 KSCN溶液 中不存在三价铁
检验溴乙烷中溴元 溴乙烷和NaOH溶液混合,振荡后加 若有淡黄色沉淀产生,则说明溴乙
B
素 烷中含溴元素
热,静置分层后,取少量上层清液,移入另一支试管中,加入2滴 溶液
比较 与 向饱和 溶液中滴加相同浓度的 产生白色沉淀,说明
C
的大小 溶液
探究电石与水的反 将电石与饱和食盐水反应产生的气体通 若酸性高锰酸钾溶液褪色,说明电
D
应 入酸性高锰酸钾溶液 石与水反应生成了乙炔
19.(2024·江苏常州第一中学高三期初检测)下列实验操作、实验现象和结论对应均正确的是
选
实验操作 实验现象 结论
项
向 溶液中通入 ,再滴加 稀溶 产生白色沉淀, 白色沉淀为 ,后转化成
A
液 白色沉淀不溶解
B 向 溶液中滴入 溶液 有白色沉淀生成 发生了相互促进的水解反应
向盛有 固体的试管中加入 溶
C 产生无色气体
液,充分搅拌后,取沉淀(洗净)放入稀盐酸中
层无色,水
D 向 溶液中加入少量氯水,再加 振荡 说明 的还原性强于 的
层变为棕黄色
20.(2024·江苏连云港五校高三12月联考)室温下,下列实验研究方案能达到探究目的的是
选
探究方案 探究目的
项
向香茅醛( )中加入少量酸性 溶液,观察溶液颜色变
A 香茅醛中是否含碳碳双键
化
向 溶液中加入 溶液,充分反应后用 与 的反应有一定限
B
苯萃取2~3次,取水层滴加KSCN溶液观察溶液颜色变化 度
用pH试纸测定浓度均为 的 溶液和 溶液的 比较HClO、CHCOOH
C 3
pH 酸性相对强弱
向两支盛有5mL4%的HO 溶液的试管中分别加入2滴0.1mol·L-1的 比较Fe3+、Cu2+对HO 分
D 2 2 2 2
CuSO 溶液和2滴0.1mol·L-1的Fe (SO ) 溶液,观察气泡生成的快慢 解反应的催化效果
4 2 4 3
21.(2024·江苏百师联盟开学摸底)下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
选
陈述Ⅰ 陈述Ⅱ
项
A 向 溶液中通入足量 ,无明显现象 弱酸不能制强酸B 向酸性 溶液中滴加 溶液,紫色褪去 具有氧化性
将等物质的量的 和单质溴混 可以发生1,2-加
C
合,在一定条件下发生加成反应,可生成3种有机物 成、3,4-加成和1,4-加成
用毛皮摩擦过的橡胶棒靠近从酸式滴定管管中流出的
D 是非极性分子
,液流方向改变
22.(2024·江苏盐城联盟校10月第一次学情调研)室温下,下列实验探究方案及现象能达到探究目的的
是
选
探究方案及现象 探究目的
项
A 用pH计测量醋酸、盐酸的pH,比较溶液pH大小 醋酸是弱电解质
向久置的 溶液中加入足量 溶液,出现白色沉淀;再加入足量稀 不能被空气
B
盐酸,部分沉淀溶解 氧化
向NaBr溶液中滴加过量氯水,溶液变橙色,再加入淀粉KI溶液,溶液变蓝
C 氧化性:
色
向盛有 溶液的试管中滴加几滴KSCN溶液,振荡,再滴加几滴新制氯
D 具有还原性
水,观察溶液颜色变化
23.(20241·江苏无锡高三期中教学质量调研)室温下,下列实验方案不能达到探究目的的是
选
实验方案 探究目的
项
A 向 溶液中滴入淀粉,再滴加HI溶液,观察溶液颜色变化 探究 与 氧化性强弱
用pH计分别测定等物质的量浓度的 溶液和 溶 探究键的极性对羧酸酸性的
B
影响
液的pH
向大小形状完全相同的打磨过的镁条和铝条中加入2mL3 盐
C 探究镁、铝金属性的强弱
酸,观察反应剧烈程度
向 溶液中先加入少量氢氧化钠溶液,充分反应后再加入少量 探究 与 溶
D
溶液,观察沉淀颜色的变化 度积的大小
24.(2024·江苏南通海门高三第二次调研)下列实验方案能达到探究目的的是
选
实验方案 探究目的
项苯酚的酸性与 酸性
A 向苯酚浊液中滴加 溶液,观察溶液是否变澄清
的强弱
比较 与
B 向NaCl和NaI混合溶液中滴加少量 溶液,观察产生沉淀的颜色
的大小
向 溶液中加入 溶液,再加入 与KI能否发生氧化
C
苯,振荡,观察苯层的颜色 还原反应
向 稀溶液中加入稍过量的 氧化,再向溶液中加入酸性高锰
D 溶液中是否还残留有
酸钾溶液,观察溶液是否褪色
25.(2024·江苏宿迁3月学情调研)室温下,探究0.1 mol·L-1 FeCl 溶液的性质,下列实验方案能达到探
3
究目的的是( )
选项 探究方案 探究目的
向两支试管中分别加入5 mL 5%的HO
2 2
溶液,再向两支试管中滴入3滴浓度均
A 比较Fe3+和Cu2+的催化效率
为0.1 mol·L-1 FeCl 和CuSO ,观察
3 4
产生气体的速率
向2 mL 0.1 mol·L-1 FeCl 溶液中加入1
3
B mL 0.1 mol·L-1 KI溶液,充分振荡后滴 2Fe3++2I-===2Fe2++I 是否为可逆反应
2
加KSCN溶液,观察颜色变化
向苯酚溶液中滴加几滴0.1 mol·L-1
C FeCl 与苯酚发生了氧化还原反应
FeCl 溶液,溶液呈紫色 3
3
将5 mL 0.1 mol·L-1 FeCl 溶液和15
3
D mL 0.1 mol·L-1 NaHCO 溶液混合,生 Fe3+与HCO发生了双水解反应
3
成红褐色沉淀和气体