文档内容
易错点 16 分子结构与性质
易错题【01】VSEPR模型和空间构型
①VSEPR模型反映中心原子的价层电子对的空间结构,而分子(或离子)的空间结构是指
σ键电子对的空间构型,不包括孤电子对。
②VSEPR模型和分子的空间构型不一定相同,还要看中心原子是否有孤电子对,若不含孤
电子对,二者空间构型相同,否则,不相同。
③根据VSEPR模型判断分子(或离子)的空间结构时,要略去孤电子对。
易错题【02】判断中心原子杂化轨道类型的方法
(1)根据杂化轨道的空间分布构型:①直线形—sp,②平面三角形—sp2,③四面体形—
sp3。
(2)根据杂化轨道间的夹角:①109.28°—sp3,②120°—sp2,③180°—sp。
(3)利用价层电子对数确定三种杂化类型(适用于中心粒子):2对—sp杂化,3对—sp2杂化,
4对—sp3杂化。
(4)根据σ键数与孤电子对数(适用于结构式已知的粒子):①含C有机物:2个σ—sp,3个σ
—sp2,4个σ—sp3。②含N化合物:2个σ—sp2,3个σ—sp3。③含O(S)化合物:2个σ—sp3。
(5)根据等电子原理:如CO 是直线形分子,CNS-、N与CO 是等电子体,所以分子构型
2 2
均为直线形,中心原子均采用sp杂化。
易错题【03】共价键的极性与分子极性的关系
易错题【04】共价键和分子间作用力的比较
分子间作用力 共价键
氢键(包括分子内氢 极性共价键、非极性
分类 范德华力
键、分子间氢键) 共价键
分子或原子(稀有气 氢原子与氧原子、
作用粒子 原子
体) 氮原子或氟原子
特征 无方向性、饱和性 有方向性、饱和性 有方向性、饱和性
强度比较 共价键>氢键>范德华力
影响其强度的因 随着分子极性和相对 对于A—H…B, 成键原子半径越小,A、B的电负性越
分子质量的增大而增 键长越短,键能越
素 大,B原子的半径
大 大,共价键越稳定
越小,作用力越大
①影响物质的熔、沸
点和溶解度等物理性 分子间氢键的存
质; 在,使物质的熔、
②组成和结构相似的 沸点升高,在水中 影响分子的稳定性,
对物质性质的影
物质,随相对分子质 的溶解度增大,如 共价键键能越大,分
响
量的增大,物质熔、 熔、沸点: 子稳定性越强
沸点升高,如熔、沸 HO>HS,
2 2
点:FHCl,NH >PH
2 2 2 2 3 3
CFHS>CH。
2 2 4
(4)OF 和ClO都是分子晶体,二者结构相似,ClO的相对分子质量大,其范德华力大,
2 2 2
故ClO的熔、沸点高。
2
【答案】(1)甲硫醇不能形成分子间氢键,而水和甲醇均能,且水比甲醇的氢键多
(2)高 NH 形成分子间氢键
3
(3)HO>HS>CH
2 2 4
(4)低 OF 和ClO都是分子晶体,结构相似,ClO的相对分子质量大,ClO的熔、
2 2 2 2
沸点高
1.(2022·东莞中学松山湖学校高三月考)用价层电子对互斥理论预测HS和BF 的立体
2 3
结构,两个结论都正确的是
A.直线形;三角锥形 B.V形;三角锥形
C.直线形;平面三角形 D.V形;平面三角形
2.(2021·湖北·高考真题)“碳中和”有利于全球气候改善。下列有关CO 的说法错误的
2
是
A.CO 是Ⅴ形的极性分子 B.CO 可催化还原为甲酸
2 2
C.CO 晶体可用于人工增雨 D.CO 是侯氏制碱法的原料之一
2 23.(2021·湖北·高考真题)下列有关N、P及其化合物的说法错误的是
A.N的电负性比P的大,可推断NCl 分子的极性比PCl 的大
3 3
B.N与N的π键比P与P的强,可推断N≡N的稳定性比P≡P的高
C.NH 的成键电子对间排斥力较大,可推断NH 的键角比PH 的大
3 3 3
D.HNO 的分子间作用力较小,可推断HNO 的熔点比HPO 的低
3 3 3 4
4.(2021·山东·高考真题)关于CHOH、NH 和(CH)NNH 的结构与性质,下列说法错
3 2 4 3 2 2
误的是
A.CHOH为极性分子 B.NH 空间结构为平面形
3 2 4
C.NH 的沸点高于(CH)NNH D.CHOH和(CH)NNH 中C、O、N杂化方
2 4 3 2 2 3 3 2 2
式均相同
5.(2022·湖北·高考真题)磷酰三叠氮是一种高能分子,结构简式为 。下列关
于该分子的说法正确的是
A.为非极性分子 B.立体构型为正四面体形
C.加热条件下会分解并放出 D.分解产物 的电子式为
6.(2021·江苏·高考真题)N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过
2 3
催化氧化生产HNO;HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在
3 3
高温或放电条件下,N 与O 反应生成NO,NO进一步氧化生成NO 。2NO(g)
2 2 2
+O (g)=2NO (g) ΔH=-116.4kJ·mol-1。大气中过量的NO 和水体中过量的NH 、NO 均是
2 2 x
污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N,也可将水体中
2
的NO -转化为N。下列有关NH 、NH 、NO 的说法正确的是
3 2 3
A.NH 能形成分子间氢键
3
B.NO 的空间构型为三角锥形
C.NH 与NH 中的键角相等
3
D.NH 与Ag+形成的[Ag(NH)]+中有6个配位键
3 3 2
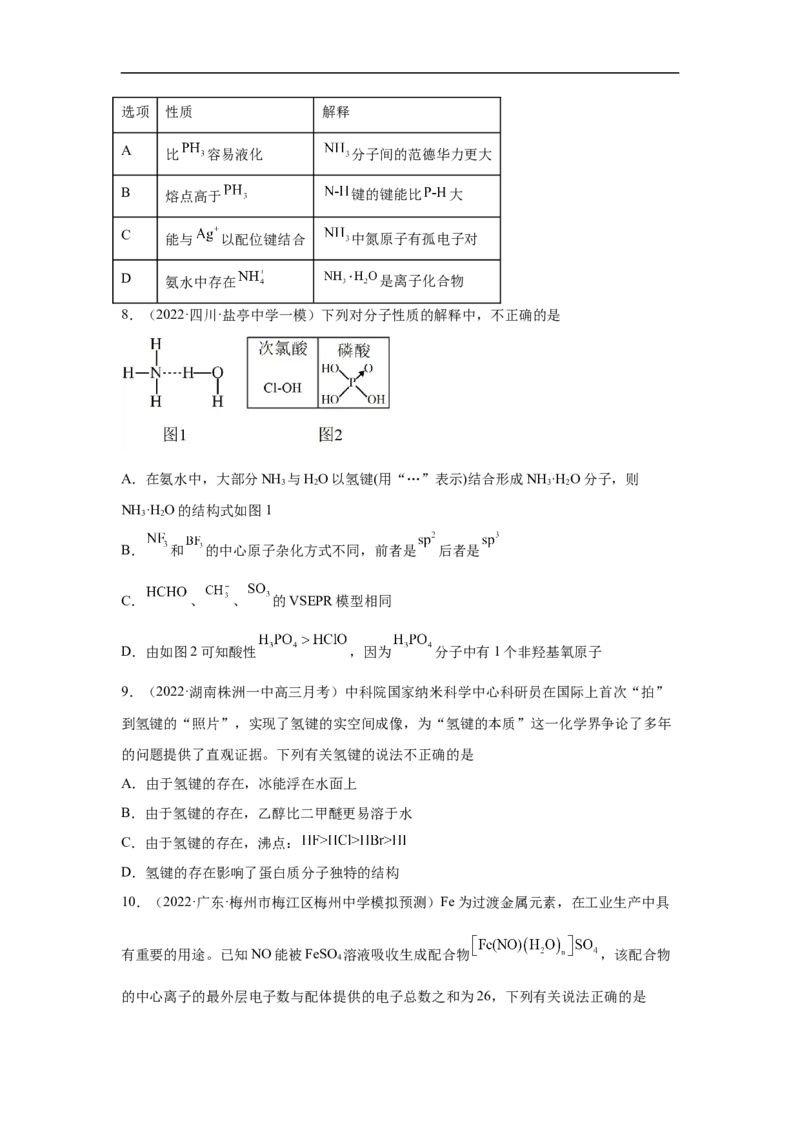
7.(2021·海南·高考真题)关于 性质的解释合理的是选项 性质 解释
A 比 容易液化 分子间的范德华力更大
B 熔点高于 键的键能比 大
C 能与 以配位键结合 中氮原子有孤电子对
D 氨水中存在 是离子化合物
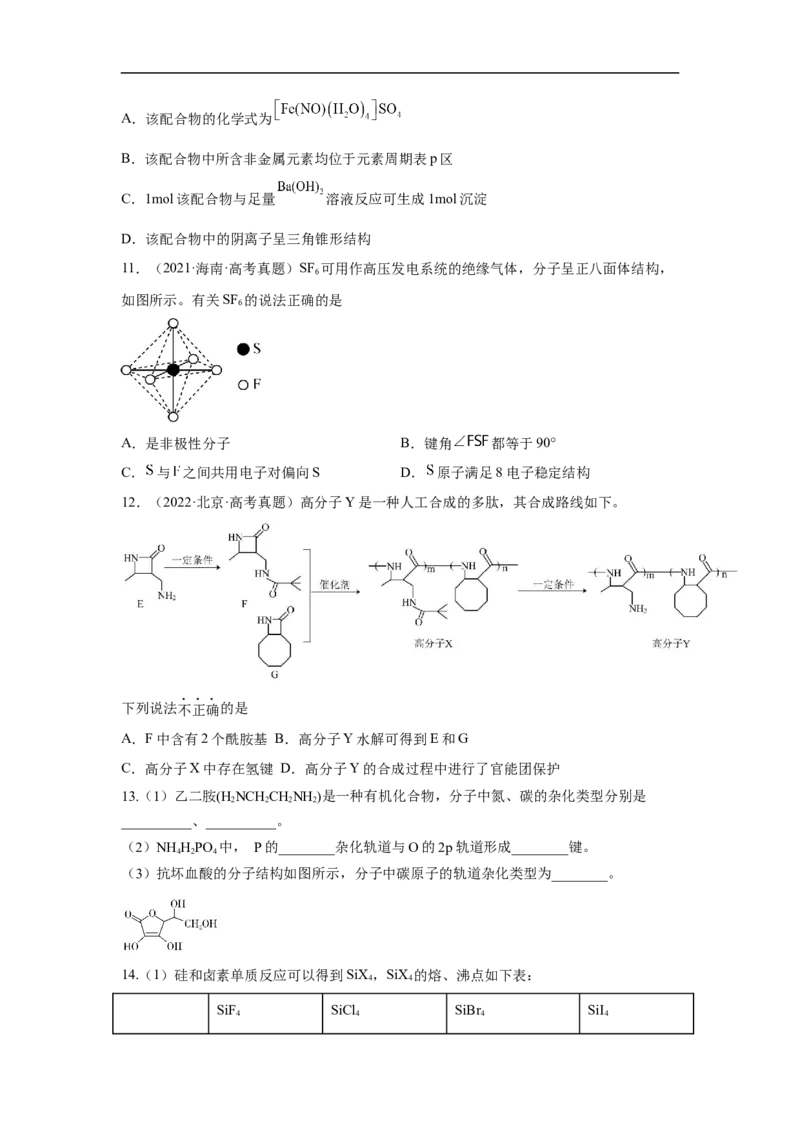
8.(2022·四川·盐亭中学一模)下列对分子性质的解释中,不正确的是
A.在氨水中,大部分NH 与HO以氢键(用“…”表示)结合形成NH ·H O分子,则
3 2 3 2
NH ·H O的结构式如图1
3 2
B. 和 的中心原子杂化方式不同,前者是 后者是
C. 、 、 的VSEPR模型相同
D.由如图2可知酸性 ,因为 分子中有1个非羟基氧原子
9.(2022·湖南株洲一中高三月考)中科院国家纳米科学中心科研员在国际上首次“拍”
到氢键的“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了多年
的问题提供了直观证据。下列有关氢键的说法不正确的是
A.由于氢键的存在,冰能浮在水面上
B.由于氢键的存在,乙醇比二甲醚更易溶于水
C.由于氢键的存在,沸点:
D.氢键的存在影响了蛋白质分子独特的结构
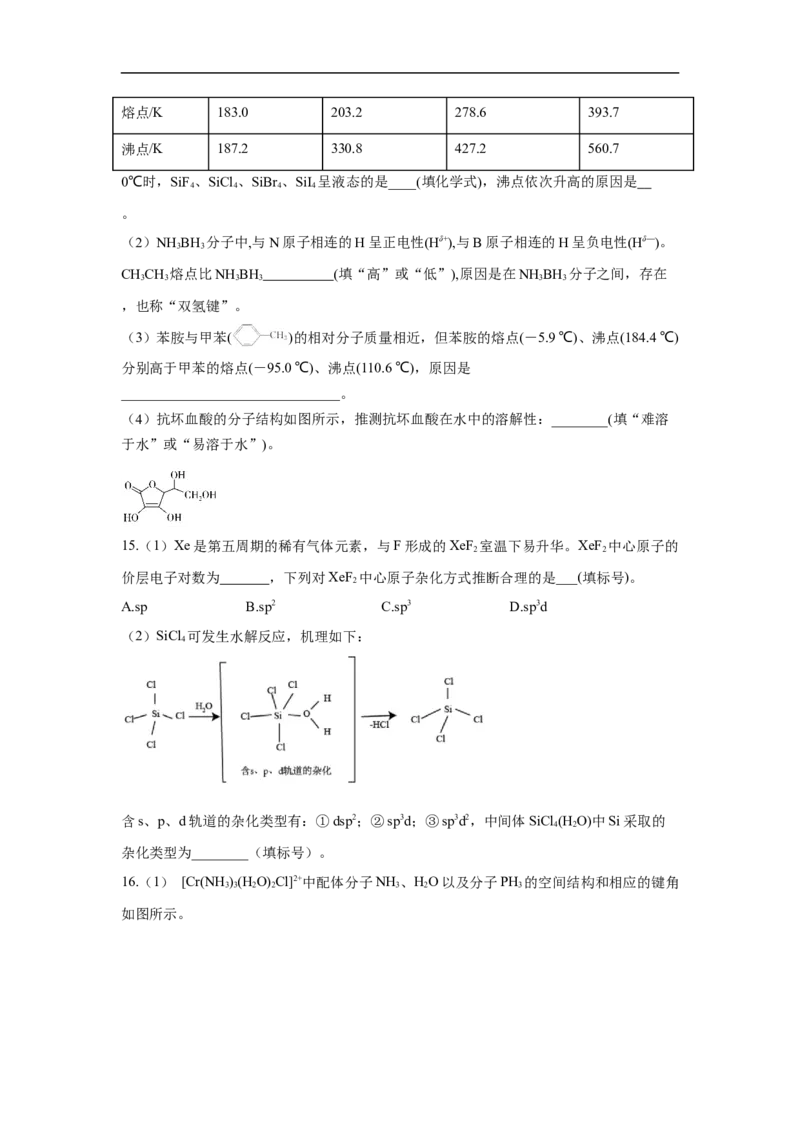
10.(2022·广东·梅州市梅江区梅州中学模拟预测)Fe为过渡金属元素,在工业生产中具
有重要的用途。已知NO能被FeSO 溶液吸收生成配合物 ,该配合物
4
的中心离子的最外层电子数与配体提供的电子总数之和为26,下列有关说法正确的是A.该配合物的化学式为
B.该配合物中所含非金属元素均位于元素周期表p区
C.1mol该配合物与足量 溶液反应可生成1mol沉淀
D.该配合物中的阴离子呈三角锥形结构
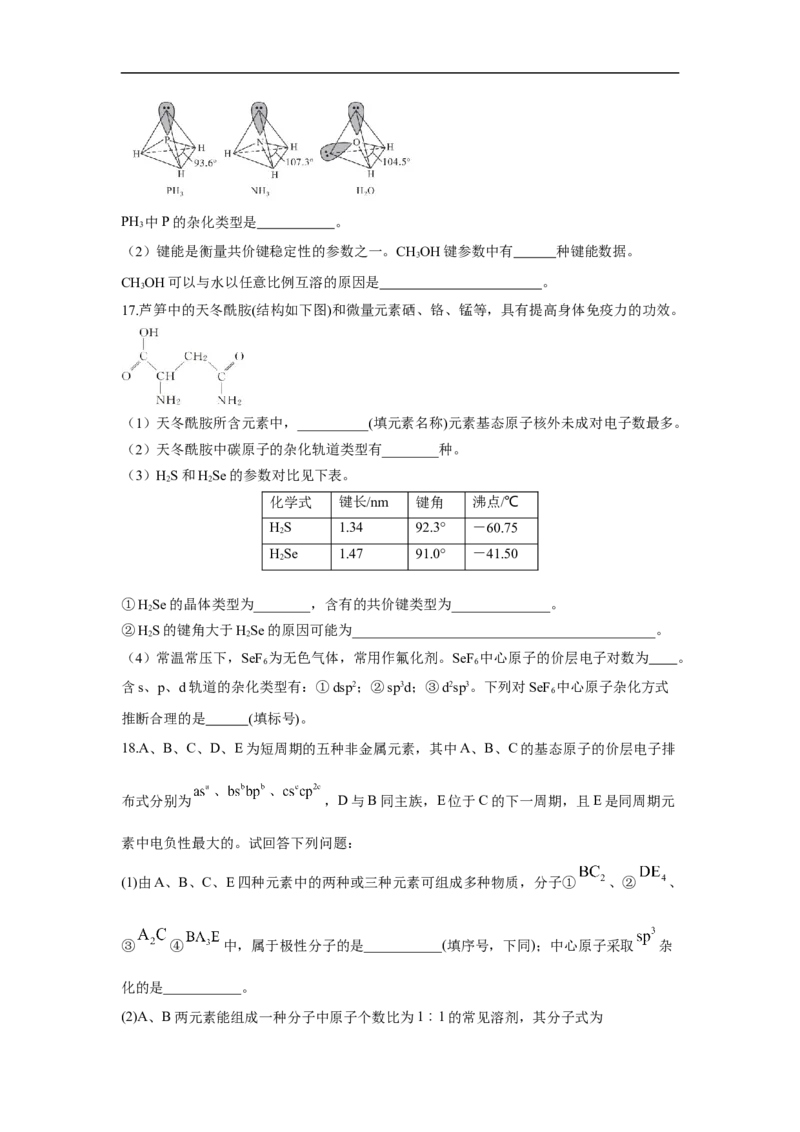
11.(2021·海南·高考真题)SF 可用作高压发电系统的绝缘气体,分子呈正八面体结构,
6
如图所示。有关SF 的说法正确的是
6
A.是非极性分子 B.键角 都等于90°
C. 与 之间共用电子对偏向S D. 原子满足8电子稳定结构
12.(2022·北京·高考真题)高分子Y是一种人工合成的多肽,其合成路线如下。
下列说法不正确的是
A.F中含有2个酰胺基 B.高分子Y水解可得到E和G
C.高分子X中存在氢键 D.高分子Y的合成过程中进行了官能团保护
13.(1)乙二胺(H NCH CHNH )是一种有机化合物,分子中氮、碳的杂化类型分别是
2 2 2 2
__________、__________。
(2)NH HPO 中, P的________杂化轨道与O的2p轨道形成________键。
4 2 4
(3)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为________。
14.(1)硅和卤素单质反应可以得到SiX,SiX 的熔、沸点如下表:
4 4
SiF SiCl SiBr SiI
4 4 4 4熔点/K 183.0 203.2 278.6 393.7
沸点/K 187.2 330.8 427.2 560.7
0℃时,SiF、SiCl 、SiBr 、SiI 呈液态的是____(填化学式),沸点依次升高的原因是
4 4 4 4
。
(2)NH BH 分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ—)。
3 3
CHCH 熔点比NH BH (填“高”或“低”),原因是在NH BH 分子之间,存在
3 3 3 3 3 3
,也称“双氢键”。
(3)苯胺与甲苯( )的相对分子质量相近,但苯胺的熔点(-5.9 ℃)、沸点(184.4 ℃)
分别高于甲苯的熔点(-95.0 ℃)、沸点(110.6 ℃),原因是
_______________________________。
(4)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性:________(填“难溶
于水”或“易溶于水”)。
15.(1)Xe是第五周期的稀有气体元素,与F形成的XeF 室温下易升华。XeF 中心原子的
2 2
价层电子对数为 ,下列对XeF 中心原子杂化方式推断合理的是___(填标号)。
2
A.sp B.sp2 C.sp3 D.sp3d
(2)SiCl 可发生水解反应,机理如下:
4
含s、p、d轨道的杂化类型有:①dsp2;②sp3d;③sp3d2,中间体SiCl (H O)中Si采取的
4 2
杂化类型为________(填标号)。
16.(1) [Cr(NH )(H O) Cl]2+中配体分子NH 、HO以及分子PH 的空间结构和相应的键角
3 3 2 2 3 2 3
如图所示。PH 中P的杂化类型是 。
3
(2)键能是衡量共价键稳定性的参数之一。CHOH键参数中有 种键能数据。
3
CHOH可以与水以任意比例互溶的原因是 。
3
17.芦笋中的天冬酰胺(结构如下图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。
(1)天冬酰胺所含元素中,__________(填元素名称)元素基态原子核外未成对电子数最多。
(2)天冬酰胺中碳原子的杂化轨道类型有________种。
(3)HS和HSe的参数对比见下表。
2 2
化学式 键长/nm 键角 沸点/℃
HS 1.34 92.3° -60.75
2
HSe 1.47 91.0° -41.50
2
①HSe的晶体类型为________,含有的共价键类型为______________。
2
②HS的键角大于HSe的原因可能为___________________________________________。
2 2
(4)常温常压下,SeF 为无色气体,常用作氟化剂。SeF 中心原子的价层电子对数为 。
6 6
含s、p、d轨道的杂化类型有:①dsp2;②sp3d;③d2sp3。下列对SeF 中心原子杂化方式
6
推断合理的是 (填标号)。
18.A、B、C、D、E为短周期的五种非金属元素,其中A、B、C的基态原子的价层电子排
布式分别为 ,D与B同主族,E位于C的下一周期,且E是同周期元
素中电负性最大的。试回答下列问题:
(1)由A、B、C、E四种元素中的两种或三种元素可组成多种物质,分子① 、② 、
③ ④ 中,属于极性分子的是___________(填序号,下同);中心原子采取 杂
化的是___________。
(2)A、B两元素能组成一种分子中原子个数比为1︰1的常见溶剂,其分子式为___________;相同条件下,该物质在 中的溶解度___________(填“大于”或“小
于”)其在 中的溶解度。
(3)阴离子 与 的VSEPR模型名称分别为___________、___________,其VSEPR
模型与空间结构不一致的是___________(填离子符号)。
(4) 、 和 的沸点由高到低的顺序为___________(用化学式表示)。
参考答案
1.D【详解】HS中S的孤电子对数为 ×(6-2×1)=2,σ键电子对数为2,S的价层电子
2
对数为4,VSEPR模型为四面体型,去掉孤电子对,HS的立体构型为V形;BF 中B的
2 3
孤电子对数为 ×(3-3×1)=0,σ键电子对数为3,B的价层电子对数为3,VSEPR模型为
平面三角形,由于B上没有孤电子对,BF 的立体构型为平面三角形;答案选D。
3
2.A【详解】A.CO 的中心原子C的价层电子对数为2,无孤电子对,CO 的空间构型为
2 2
直线形,其正负电荷中心重合,为非极性分子,A项错误;
B.CO 可以被H 在催化剂作用下还原为甲酸,B项正确;
2 2
C.固态二氧化碳(干冰)升华时吸热,可用于人工增雨,C项正确;
D.侯氏制碱法中发生反应: NaC1 + H O + NH +CO = NaHCO ↓+NHC1,CO 是生产原
2 3 2 3 4 2
料之一,D项正确;
故选A。
3.A【详解】A.P和Cl的电负性差值比N和Cl的电负性差值大,因此PCl 分子的极性
3
比NCl 分子极性大,A项错误;
3
B.N与N的 键比P与P的强,故 的稳定性比 的高,B项正确;
C.N的电负性比P大,NH 中成键电子对距离N比PH 中成键电子对距离P近,NH 中成
3 3 3
键电子对间的斥力大,因此NH 的键角比PH 的大,C项正确;
3 3
D.相对分子质量:HNO