文档内容
邵阳市第二中学高三第二次化学月考试题
制卷审题:
可能用到的相对原子质量 H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 K-39 Fe-56 Cu-64
一、选择题:本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.古医典富载化学知识 ,下述之物见其氧化性者为
A.金(Au) :“虽被火亦未熟”B.石灰(CaO) :“以水沃之 , 即热蒸而解”
C.石硫黄(S) :“能化……银、铜、铁,奇物”
D.石钟乳(CaCO ) :“色黄,以苦酒(醋) 洗刷则白”
3
2.下列试剂实验室保存方法错误的是
A.浓硝酸保存在棕色细口瓶中B.氢氧化钠固体保存在广口塑料瓶中
C.四氯化碳保存在广口塑料瓶中D.高锰酸钾固体保存在棕色广口瓶中
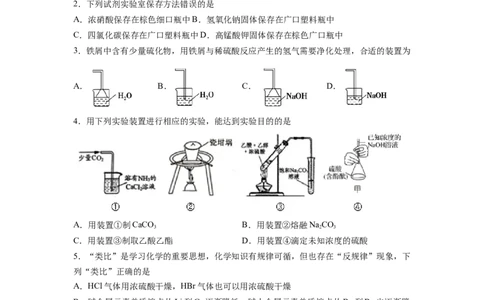
3.铁屑中含有少量硫化物,用铁屑与稀硫酸反应产生的氢气需要净化处理,合适的装置为
A. B. C. D.
4.用下列实验装置进行相应的实验,能达到实验目的的是
A.用装置①制CaCO B.用装置②熔融NaCO
3 2 3
C.用装置③制取乙酸乙酯 D.用装置④滴定未知浓度的硫酸
5.“类比”是学习化学的重要思想,化学知识有规律可循,但也存在“反规律”现象,下
列“类比”正确的是
A.HCl气体用浓硫酸干燥,HBr气体也可以用浓硫酸干燥
B.碱金属元素单质熔点从Li到Cs逐渐降低,碱土金属元素单质熔点从Be到Ba也逐渐降
低
C. 是两性氧化物, 也是两性氧化物
D.实验室用FeS与稀盐酸反应制 ,也可用CuS与稀盐酸反应制
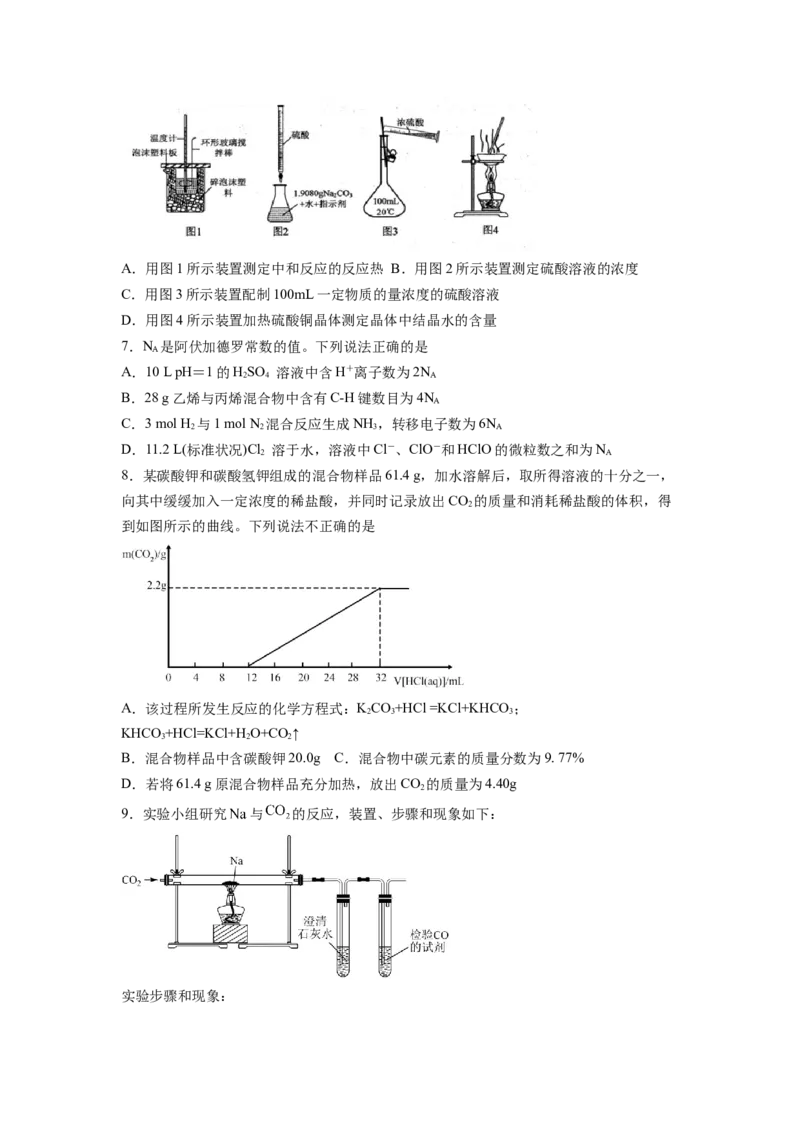
6.定量实验是学习化学的重要途径,下列操作规范且能达到定量实验目的的是A.用图1所示装置测定中和反应的反应热 B.用图2所示装置测定硫酸溶液的浓度
C.用图3所示装置配制100mL一定物质的量浓度的硫酸溶液
D.用图4所示装置加热硫酸铜晶体测定晶体中结晶水的含量
7.N 是阿伏加德罗常数的值。下列说法正确的是
A
A.10 L pH=1的HSO 溶液中含H+离子数为2N
2 4 A
B.28 g乙烯与丙烯混合物中含有C-H键数目为4N
A
C.3 mol H 与1 mol N 混合反应生成NH ,转移电子数为6N
2 2 3 A
D.11.2 L(标准状况)Cl 溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为N
2 A
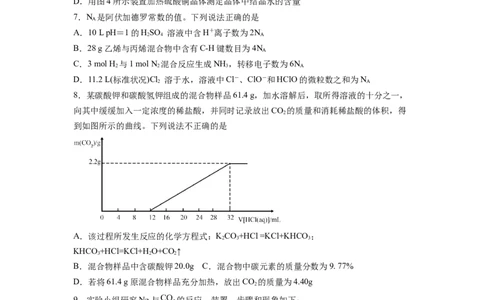
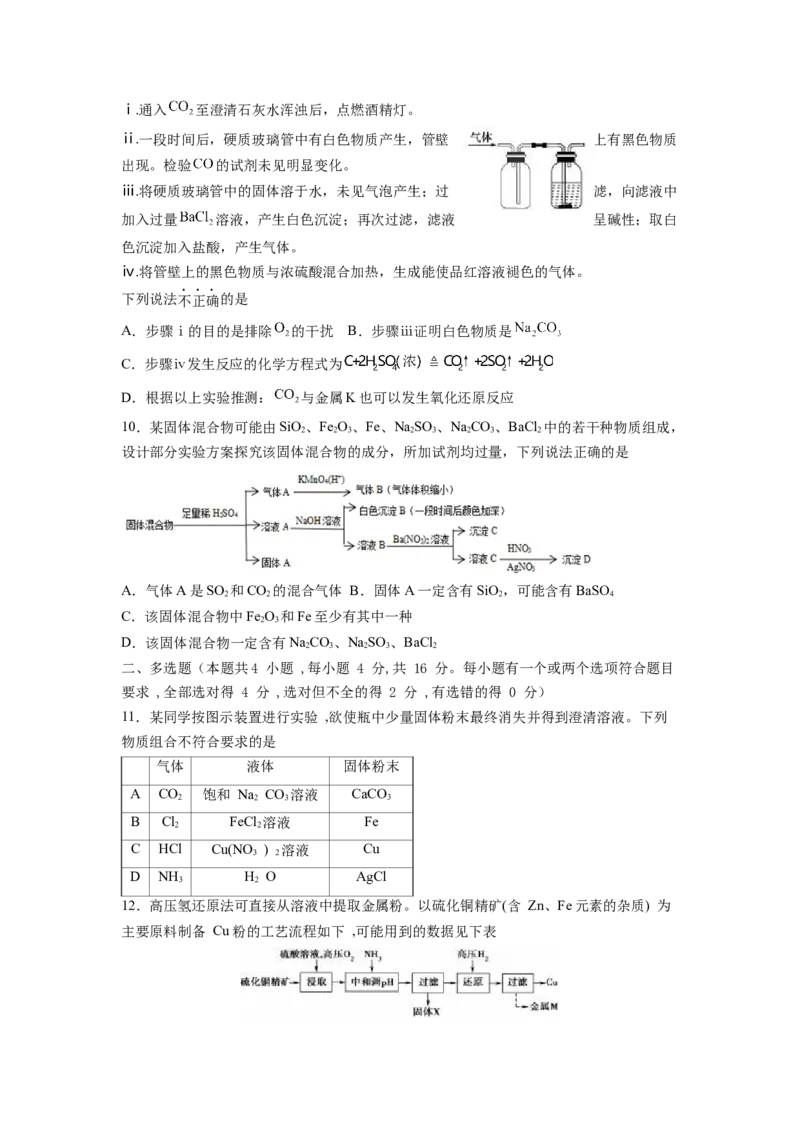
8.某碳酸钾和碳酸氢钾组成的混合物样品61.4 g,加水溶解后,取所得溶液的十分之一,
向其中缓缓加入一定浓度的稀盐酸,并同时记录放出CO 的质量和消耗稀盐酸的体积,得
2
到如图所示的曲线。下列说法不正确的是
A.该过程所发生反应的化学方程式:KCO+HCl =KCl+KHCO ;
2 3 3
KHCO +HCl=KCl+H O+CO↑
3 2 2
B.混合物样品中含碳酸钾20.0g C.混合物中碳元素的质量分数为9. 77%
D.若将61.4 g原混合物样品充分加热,放出CO 的质量为4.40g
2
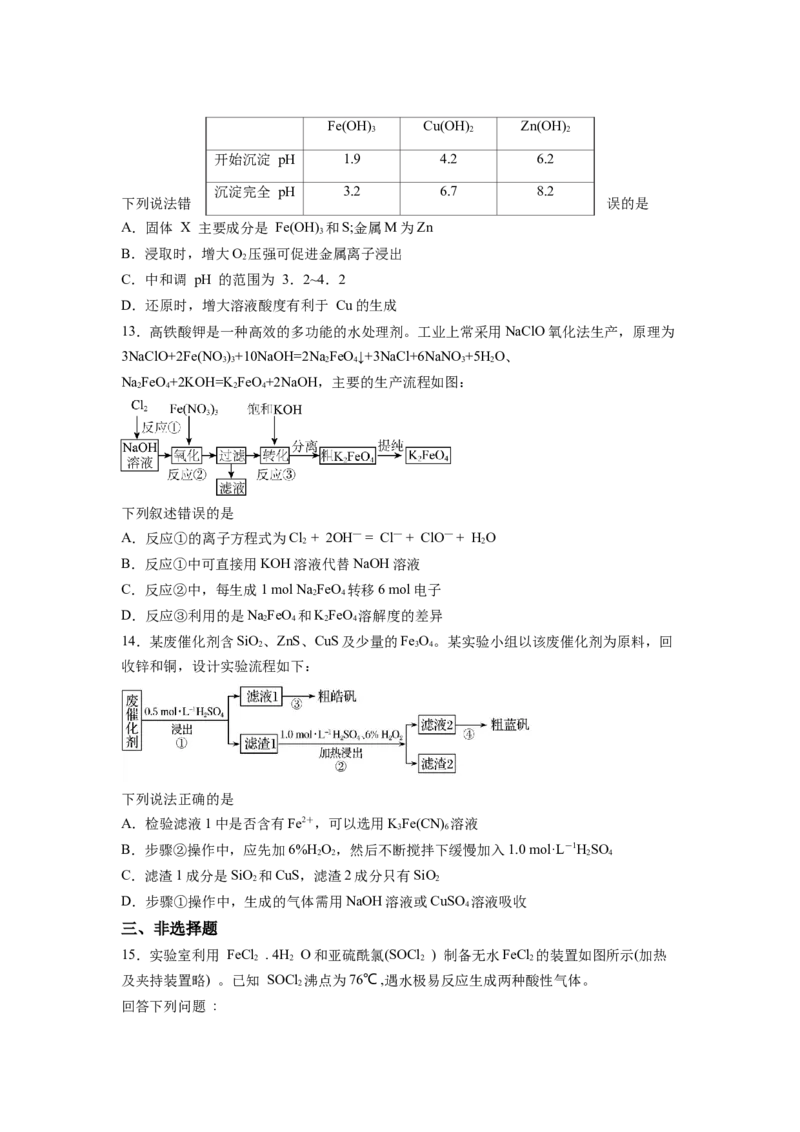
9.实验小组研究 与 的反应,装置、步骤和现象如下:
实验步骤和现象:ⅰ.通入 至澄清石灰水浑浊后,点燃酒精灯。
ⅱ.一段时间后,硬质玻璃管中有白色物质产生,管壁 上有黑色物质
出现。检验 的试剂未见明显变化。
ⅲ.将硬质玻璃管中的固体溶于水,未见气泡产生;过 滤,向滤液中
加入过量 溶液,产生白色沉淀;再次过滤,滤液 呈碱性;取白
色沉淀加入盐酸,产生气体。
ⅳ.将管壁上的黑色物质与浓硫酸混合加热,生成能使品红溶液褪色的气体。
下列说法不正确的是
A.步骤ⅰ的目的是排除 的干扰 B.步骤ⅲ证明白色物质是
C.步骤ⅳ发生反应的化学方程式为
D.根据以上实验推测: 与金属K也可以发生氧化还原反应
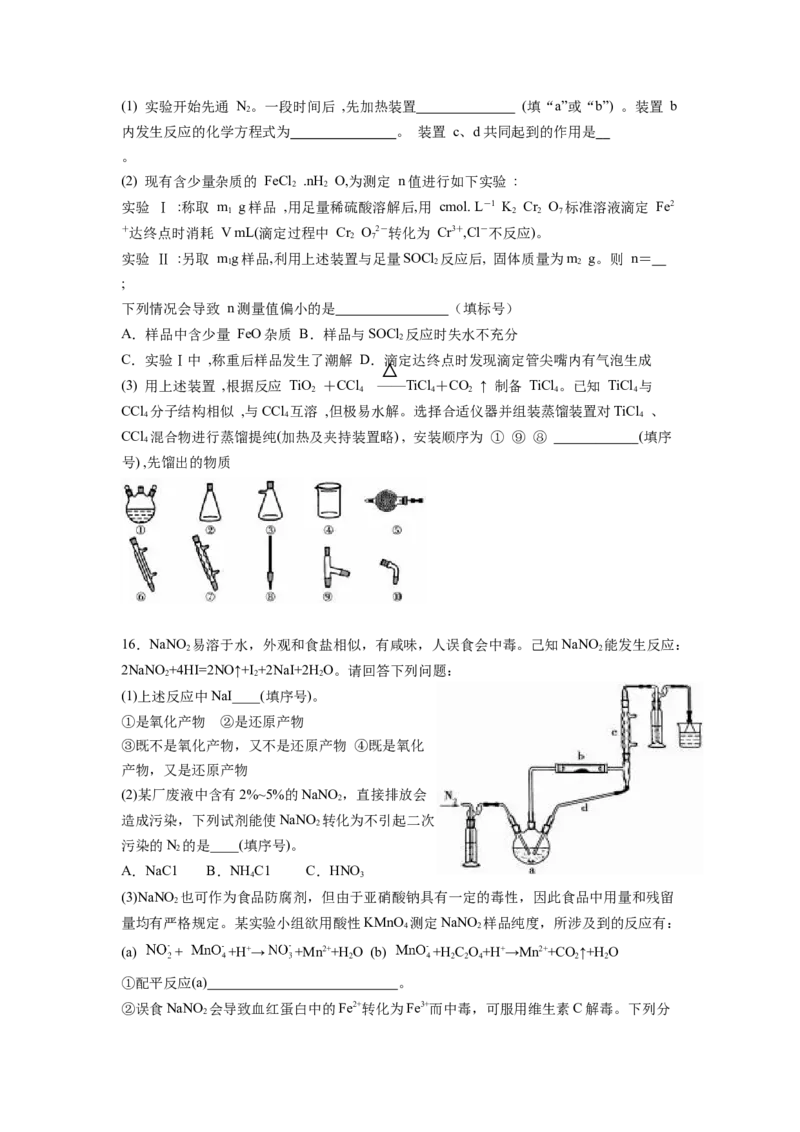
10.某固体混合物可能由SiO、Fe O、Fe、NaSO 、NaCO、BaCl 中的若干种物质组成,
2 2 3 2 3 2 3 2
设计部分实验方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
A.气体A是SO 和CO 的混合气体 B.固体A一定含有SiO,可能含有BaSO
2 2 2 4
C.该固体混合物中Fe O 和Fe至少有其中一种
2 3
D.该固体混合物一定含有NaCO、NaSO 、BaCl
2 3 2 3 2
二、多选题(本题共4 小题 ,每小题 4 分,共 16 分。每小题有一个或两个选项符合题目
要求 ,全部选对得 4 分 ,选对但不全的得 2 分 ,有选错的得 0 分)
11.某同学按图示装置进行实验 ,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列
物质组合不符合要求的是
气体 液体 固体粉末
A CO 饱和 Na CO 溶液 CaCO
2 2 3 3
B Cl FeCl 溶液 Fe
2 2
C HCl Cu(NO ) 溶液 Cu
3 2
D NH H O AgCl
3 2
12.高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含 Zn、Fe元素的杂质) 为
主要原料制备 Cu粉的工艺流程如下 ,可能用到的数据见下表Fe(OH) Cu(OH) Zn(OH)
3 2 2
开始沉淀 pH 1.9 4.2 6.2
沉淀完全 pH 3.2 6.7 8.2
下列说法错 误的是
A.固体 X 主要成分是 Fe(OH) 和S;金属M为Zn
3
B.浸取时,增大O 压强可促进金属离子浸出
2
C.中和调 pH 的范围为 3.2~4.2
D.还原时,增大溶液酸度有利于 Cu的生成
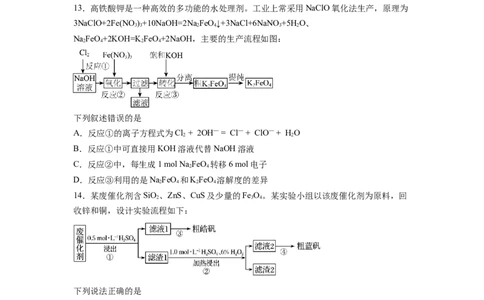
13.高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为
3NaClO+2Fe(NO )+10NaOH=2Na FeO↓+3NaCl+6NaNO +5H O、
3 3 2 4 3 2
NaFeO+2KOH=K FeO+2NaOH,主要的生产流程如图:
2 4 2 4
下列叙述错误的是
A.反应①的离子方程式为Cl + 2OH— = Cl— + ClO— + HO
2 2
B.反应①中可直接用KOH溶液代替NaOH溶液
C.反应②中,每生成1 mol Na FeO 转移6 mol电子
2 4
D.反应③利用的是NaFeO 和KFeO 溶解度的差异
2 4 2 4
14.某废催化剂含SiO、ZnS、CuS及少量的Fe O。某实验小组以该废催化剂为原料,回
2 3 4
收锌和铜,设计实验流程如下:
下列说法正确的是
A.检验滤液1中是否含有Fe2+,可以选用KFe(CN) 溶液
3 6
B.步骤②操作中,应先加6%H O,然后不断搅拌下缓慢加入1.0 mol·L-1HSO
2 2 2 4
C.滤渣1成分是SiO 和CuS,滤渣2成分只有SiO
2 2
D.步骤①操作中,生成的气体需用NaOH溶液或CuSO 溶液吸收
4
三、非选择题
15.实验室利用 FeCl . 4H O和亚硫酰氯(SOCl ) 制备无水FeCl 的装置如图所示(加热
2 2 2 2
及夹持装置略) 。已知 SOCl 沸点为76℃ ,遇水极易反应生成两种酸性气体。
2
回答下列问题 :(1) 实验开始先通 N。一段时间后 ,先加热装置 (填“a”或“b”) 。装置 b
2
内发生反应的化学方程式为 。 装置 c、d共同起到的作用是
。
(2) 现有含少量杂质的 FeCl .nH O,为测定 n值进行如下实验 :
2 2
实验 Ⅰ :称取 m g样品 ,用足量稀硫酸溶解后,用 cmol. L-1 K Cr O 标准溶液滴定 Fe2
1 2 2 7
+达终点时消耗 V mL(滴定过程中 Cr O2-转化为 Cr3+,Cl-不反应)。
2 7
实验 Ⅱ :另取 mg样品,利用上述装置与足量SOCl 反应后, 固体质量为m g。则 n=
1 2 2
;
下列情况会导致 n测量值偏小的是 (填标号)
A.样品中含少量 FeO杂质 B.样品与SOCl 反应时失水不充分
2
C.实验Ⅰ中 ,称重后样品发生了潮解 D.滴定达终点时发现滴定管尖嘴内有气泡生成
△
(3) 用上述装置 ,根据反应 TiO +CCl ——TiCl +CO ↑ 制备 TiCl 。已知 TiCl 与
2 4 4 2 4 4
CCl 分子结构相似 ,与CCl 互溶 ,但极易水解。选择合适仪器并组装蒸馏装置对TiCl 、
4 4 4
CCl 混合物进行蒸馏提纯(加热及夹持装置略) , 安装顺序为 ① ⑨ ⑧ (填序
4
号) ,先馏出的物质
16.NaNO 易溶于水,外观和食盐相似,有咸味,人误食会中毒。己知NaNO 能发生反应:
2 2
2NaNO +4HI=2NO↑+I +2NaI+2H O。请回答下列问题:
2 2 2
(1)上述反应中NaI____(填序号)。
①是氧化产物 ②是还原产物
③既不是氧化产物,又不是还原产物 ④既是氧化
产物,又是还原产物
(2)某厂废液中含有2%~5%的NaNO ,直接排放会
2
造成污染,下列试剂能使NaNO 转化为不引起二次
2
污染的N 的是____(填序号)。
2
A.NaC1 B.NH C1 C.HNO
4 3
(3)NaNO 也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留
2
量均有严格规定。某实验小组欲用酸性KMnO 测定NaNO 样品纯度,所涉及到的反应有:
4 2
(a) + +H+→ +Mn2++H O (b) +H C O+H+→Mn2++CO ↑+H O
2 2 2 4 2 2
①配平反应(a) 。
②误食NaNO 会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列分
2析错误的是____(填序号)。
A.NaNO 被氧化 B.维生素C具有还原性
2
C.还原性:维生素C>Fe2+ D.NaNO 是氧化剂
2
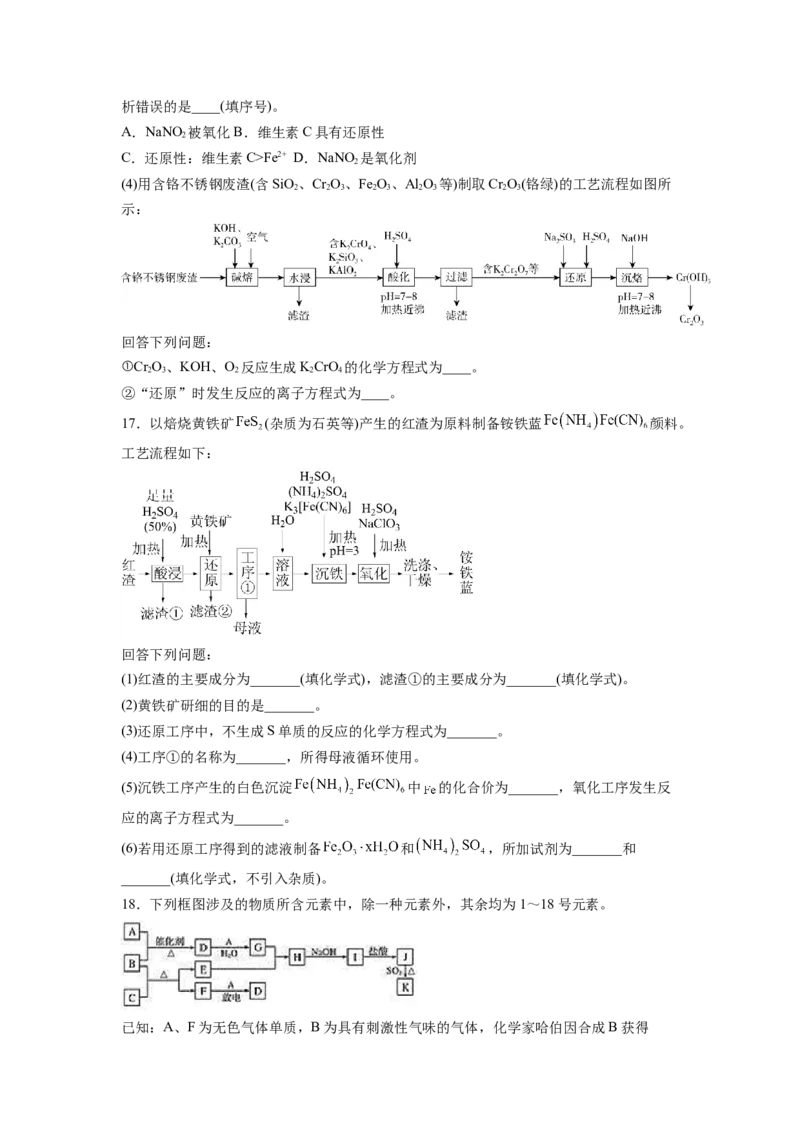
(4)用含铬不锈钢废渣(含SiO、Cr O、Fe O、Al O 等)制取Cr O(铬绿)的工艺流程如图所
2 2 3 2 3 2 3 2 3
示:
回答下列问题:
①Cr O、KOH、O 反应生成KCrO 的化学方程式为____。
2 3 2 2 4
②“还原”时发生反应的离子方程式为____。
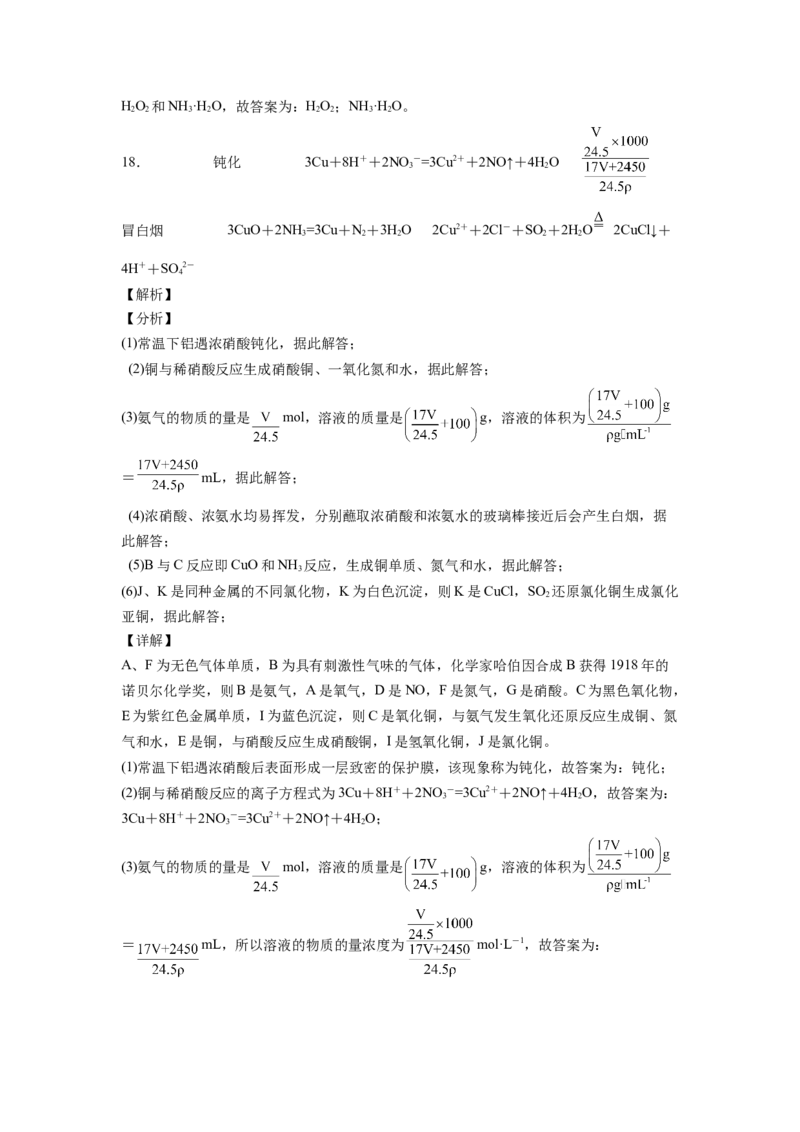
17.以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝 颜料。
工艺流程如下:
回答下列问题:
(1)红渣的主要成分为_______(填化学式),滤渣①的主要成分为_______(填化学式)。
(2)黄铁矿研细的目的是_______。
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(4)工序①的名称为_______,所得母液循环使用。
(5)沉铁工序产生的白色沉淀 中 的化合价为_______,氧化工序发生反
应的离子方程式为_______。
(6)若用还原工序得到的滤液制备 和 ,所加试剂为_______和
_______(填化学式,不引入杂质)。
18.下列框图涉及的物质所含元素中,除一种元素外,其余均为1~18号元素。
已知:A、F为无色气体单质,B为具有刺激性气味的气体,化学家哈伯因合成B获得1918年的诺贝尔化学奖。C为黑色氧化物,E为紫红色金属单质,I为蓝色沉淀(部分反应
的产物未列出)。请回答下列问题:
(1)常温下铝遇到G的浓溶液后表面形成一层致密的保护膜,该现象称为___________。
(2)E与G的稀溶液反应的离子方程式为_________。
(3)在25 ℃和101 kPa的条件下,将VL的B气体溶于100 mL水中,得到密度为ρg·mL-1
的溶液M,则M溶液的物质的量浓度为________ mol·L-1。(已知25 ℃、101 kPa条件下
气体摩尔体积为24.5 L·mol-1,不必化简)
(4)分别蘸取B的浓溶液和G的浓溶液的玻璃棒,接近后的现象是_________。
(5)B和C反应的化学方程式为__________。
(6)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO 还原J生成K的离子方程式:
2
______。邵阳市第二中学高三第二次化学月考
参考答案:
1. C
2. C
3.C
【解析】
【详解】
含少量硫化物的铁屑与稀硫酸反应有HS生成;氢气不与碱溶液反应,而硫化氢能与碱溶
2
液反应,HS在水中溶解度小,故氢气中混有的硫化氢用烧碱溶液除去,又因为硫化氢与
2
碱反应较快,容易引起倒吸,C装置倒置漏斗能防倒吸,故宜选择C装置吸收硫化氢;
故选C。
4.A
【解析】
【详解】
A.用装置①制CaCO ,发生反应为CO+CaCl +HO+2NH =CaCO ↓+2NH Cl,故A符
3 2 2 2 3 3 4
合题意;
B.不能用坩埚熔融NaCO,坩埚含有SiO,因此坩埚与碳酸钠高温下反应生成硅酸钠,
2 3 2
故B不符合题意;
C.用装置③制取乙酸乙酯,右侧收集装置不能伸入到溶液液面以下,易发生倒吸,故C
不符合题意;
D.用装置④滴定未知浓度的硫酸,NaOH溶液应该装在碱式滴定管里,故D不符合题意。
综上所述,答案为A。
5.B
【解析】
【详解】
A. HBr具有较强的还原性,可被浓硫酸氧化为溴单质,故A错误;
B. 碱金属元素和碱土金属元素都属于金属晶体,从上到下,原子半径依次增大,金属键依
次减弱,熔沸点依次降低,故B正确;
C. 是酸性氧化物,故C错误;
D. CuS不与盐酸反应,故D错误。
6 .A
【解析】
【详解】
A.用图1所示装置可测定中和反应的反应热,故A正确;
B.利用中和滴定测定稀硫酸的浓度,一般用氢氧化钠溶液滴定,不能将碳酸钠固体放在
锥形瓶中,用稀硫酸滴定碳酸钠,故B错误;
C.浓硫酸应该在烧杯中稀释并冷却后在转移至容量瓶中,故C错误;D.加热固体应在坩埚中进行,不能用蒸发皿,故D错误。
故选A。
7.B
【解析】
【分析】
A. pH=1的HSO 溶液中c(H+)=0.1mol/L,n(H+)=0.1mol/L 10 L=1mol,含H+离
2 4
子数为N ;
A ×
B. 2乙烯与丙烯的最简式为CH,28 g乙烯与丙烯混合物中含有2mol的CH,C-H键数目
2 2
为4N ;
A
C. 氢气与氮气反应为可逆反应,3 mol H 与1 mol N 混合反应生成n(NH )<2mol,转移
2 2 3
电子数小于6N ;
A
D. 11.2 L(标准状况)Cl 溶于水,部分氯气发生反应,溶液中2Cl、Cl-、ClO-和HClO的
2 2
微粒数之和为N ;
A
【详解】
A. pH=1的HSO 溶液中c(H+)=0.1mol/L,n(H+)=0.1mol/L 10 L=1mol,含H+离
2 4
子数为N ,A错误;
A ×
B. 2乙烯与丙烯的最简式为CH,28 g乙烯与丙烯混合物中含有2mol的CH,C-H键数目
2 2
为4N ,B正确;
A
C. 氢气与氮气反应为可逆反应,3 mol H 与1 mol N 混合反应生成n(NH )<2mol,转移
2 2 3
电子数小于6N ,C错误;
A
D. 11.2 L(标准状况)Cl 溶于水,部分氯气发生反应,溶液中2Cl、Cl-、ClO-和HClO的
2 2
微粒数之和为N ,D错误;
A
答案为B
【点睛】
氯气溶于水,部分发生化学反应,部分为分子形式存在。
8.B
【解析】
【详解】
A. 由图可知,开始没有气体生成,发生反应:KCO+HCl=KCl+KHCO ,加入12mL盐
2 3 3
酸时,开始有气体生成,此时发生反应:KHCO +HCl=KCl+H O+CO↑,故A正确;
3 2 2
B.溶液中碳酸钾转化为碳酸氢钾,消耗盐酸为12mL,KHCO 与HCl反应消耗盐酸的体积
3
为32mL-12mL=20mL,反应都按1:1进行,故样品中碳酸钾与碳酸氢钾的物质的量之比
=12mL:(20-12)mL=3:2,根据碳元素守恒可知,碳酸钾的物质的量=
×10=0.3mol,故样品中碳酸钾的质量=0.3mol×138g/mol=41.4g,故B错误;
C. 当加入32mL盐酸时,生成的气体达最大值,根据碳元素守恒,可知样品中碳元素的质量=2.2g× ×10=6g,故样品中碳元素质量分数= ×100%≈9.77%,故C正确;
D. 碳酸氢钾的物质的量为0.3mol× =0.2mol,根据方程式2KHCO
3
KCO+H O+CO↑,可知生成二氧化碳的物质的量为0.2mol× =0.1mol,二氧化碳的质量
2 3 2 2
=0.1mol×44g/mol=4.4g,故D正确;
故选B。
9.B
【解析】
【详解】
A.通入CO 至澄清石灰水浑浊后,可以排除试管内原有氧气的干扰,A项正确;
2
B.将硬质玻璃管中的固体溶于水,未见气泡产生,说明不存在NaO,向滤液中加入过量
2 2
BaCl 溶液,产生白色沉淀,加入盐酸,产生气体说明白色固体中存在NaCO,再次过滤,
2 2 3
滤液呈碱性,说明白色固体中也存在NaO,B项错误;
2
C.黑色物质是C,C和浓硫酸在加热条件下发生反应: ,
C项正确;
D.K和Na都是IA族的碱金属,化学性质相似,且K比Na更加活泼,根据以上实验推测:
与金属K也可以发生氧化还原反应,D项正确;
答案选B。
10.C
【解析】
【分析】
固体混合物可能由SiO、Fe O、Fe、NaSO 、NaCO、BaCl 中的两种或两种以上的物质
2 2 3 2 3 2 2
组成,实验可知,气体A与高锰酸钾反应后得到气体B,且气体体积比原来减小,说明有
气体能够与酸性高锰酸钾溶液发生氧化还原反应,则A中一定含SO ,可能含CO、H;
2 2 2
则混合物中一定含有NaSO ,可能含有NaCO 和Fe。混合物与足量硫酸反应后的固体A
2 3 2 3
可能为SiO 或BaSO,或二者均存在;溶液A与NaOH反应后生成白色沉淀B,B的颜色
2 4
一段时间后加深,则B为Fe(OH) ,溶液B与Ba(NO ) 反应生成沉淀C为BaSO,溶液C
2 3 2 4
与硝酸、硝酸银反应生成沉淀D为AgCl,则原混合物中Fe O 和Fe至少有其中一种,一定
2 3
含BaCl 。
2
【详解】
A.A气体能与高锰酸钾反应,但仍有气体剩余,说明气体A一定含有SO ,可能含CO、
2 2
H 的一种或两种,A错误;
2
B.溶液A中加入足量氢氧化钠得到白色沉淀,一段时间后颜色变深,说明白色沉淀中含
有Fe(OH) ,溶液C转化为沉淀D,说明是AgCl,则一定含有BaCl ,则固体A中一定存
2 2
在BaSO,可能含SiO,B错误;
4 2C.溶液A中加入足量氢氧化钠得到白色沉淀,一段时间后颜色变深,说明溶液A中含有
Fe2+,可能来源于Fe3+与SO 2-的反应,也可能来源于Fe和HSO 反应,则该固体混合物
3 2 4
中Fe O 和Fe至少有其中一种,C正确;
2 3
D.根据以上分析,固体混合物一定含有NaSO 、BaCl ,可能含Fe,D错误;
2 3 2
答案选C。
11.A 12.D
13.BC
【解析】
【分析】
由题给流程可知,氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,向反应后的溶液
中加入硝酸铁溶液发生反应生成高铁酸钠沉淀,过滤得到高铁酸钠和滤液;向高铁酸钠固
体中加入饱和氢氧化钾溶液将高铁酸钠转化为高铁酸钾,过滤得到粗高铁酸钾,粗高铁酸
钾经提纯得到高铁酸钾。
【详解】
A.由分析可知,反应①为氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的
离子方程式为Cl+2OH—=Cl—+ClO—+H O,故A正确;
2 2
B.高铁酸钠和高铁酸钾都溶于水,若反应①中直接用氢氧化钾溶液代替氢氧化钠溶液,
反应制得的粗高铁酸钾中的可溶性杂质多,提纯得到的高铁酸钾中还会有可溶性杂质无法
除去,故B错误;
C.反应②中铁离子被氧化生成高铁酸根离子,则生成1 mol 高铁酸钠转移电子的物质的
量为3mol,故C错误;
D.反应③是利用高铁酸钾的溶解度小于高铁酸钠,将高铁酸钠转化为高铁酸钾,故D正
确;
故选BC。
14.AD
【解析】
【分析】
废催化剂加入稀硫酸,第一次浸出主要发生反应ZnS+H SO =ZnSO +H S↑、
2 4 4 2
Fe O+4H SO =FeSO+Fe (SO )+4H O,过滤后滤液中ZnSO、FeSO 、Fe (SO ),浓缩结晶
3 4 2 4 4 2 4 3 2 4 4 2 4 3
得到粗ZnSO·7H O,滤渣1含有SiO、CuS,向盛有滤渣1的反应器中加HSO 和HO 溶
4 2 2 2 4 2 2
液,发生氧化还原反应,生成硫酸铜、硫,滤渣2含有硫和二氧化硅,滤液含有硫酸铜,
经结晶可得到硫酸铜晶体,以此解答该题。
【详解】
A.若检验滤液中滤液1中是否含有Fe2+,可以选用KFe(CN) 溶液,在KFe(CN) 溶液的
3 6 3 6
作用下,Fe2+可以反应生成蓝色沉淀,故A正确;
B.过氧化氢在酸性条件下可氧化CuS,应先加入稀硫酸,再加入过氧化氢,故B错误;
C.根据分析,滤渣2含有硫和二氧化硅,故C错误;D.根据分析,步骤①操作中生成的气体为硫化氢,直接排放易污染空气,需用NaOH溶
液或CuSO 溶液吸收,故D正确;
4
故答案选AD。
15.解析 : (1) 实验开 始 时 先 通 N ,排 尽 装 置 中 的 空 气 , 一 段 时 间后 ,先
2
加热装置a, 产生 SOCl 气体充满b装置后再加热b装置 ,装置 b 中 发 生 反 应 的 化
2
学 方 程 式 为 FeCl . 4H O+4SOCl — △ — FeCl +4SO ↑+8HCl↑ ; 装 置 c、d 的
2 2 2 2 2
共 同
作用是冷凝回流 SOCl ; 答案为 :a; FeCl . 4H O+4SOCl △ FeCl +4SO ↑ +8HCl↑ ;
2 2 2 2 2 2
冷凝回流 SOCl 。
2
(2) 滴定过 程 中 Cr O2 - 将 Fe2 + 氧 化 成 Fe3 + , 自 身 被 还 原 成 Cr3 + ,反
2 7
应的离子方程式为 6Fe2 ++Cr O2△ -+14H+ —— 6Fe3 ++ 2Cr3 ++ 7H O, 则 m g 样
2 7 2 1
品 中 n(FeCl ) = 6n (Cr O2 - )=6cV×10 -3 mol;m g样品中结晶水的质量为(m
2 2 7 1 1
-m )g,结晶水物质的量为 mol,n(FeCl )∶ n( H O) = 1∶ n = ( 6cV × 10-3 mol) :
2 2 2
mol, 解 得 n=1000(m -m )/108cV;A.样品中含少量FeO杂质,溶于稀硫酸
1 2
生成 Fe2 + ,导致消耗的 K Cr O 溶 液 的 体 积 V 偏 大 ,使 n 的测量值偏小 ,A 选
2 2 7
;B.样品 与 SOCl 反 应 时 失 水 不 充 分 , 则 m 偏大 ,使 n 的测量值 偏 小 ,B 选
2 2
;C.实 验 Ⅰ 称 重 后 ,样品发生了潮解 , 样 品 的 质 量 不变 , 消 耗 的 K Cr O
2 2 7
溶液的体积V不变 ,使 n 的测量值不变 ,C 不选 ;D.滴定 达 到 终 点 时发现滴定管尖
嘴内有气泡生成 , 导致消耗的K Cr O 溶液的体积V 偏 小 , 使 n 的 测 量 值 偏 大 ,
2 2 7
D 项 不 选 ; 答 案 选 AB. (3) 组装 蒸 馏 装 置 对 TiCl 、CCl 混合物进行蒸馏提
4 4
纯 ,按由下而上 、从左到右的顺序组装 ,安装顺序为①⑨⑧ , 然后连接冷凝管 ,蒸馏装置
中应选择直形冷凝管 ⑥ 、不选用球形冷凝管 ⑦ , 接 着 连 接 尾 接 管 ⑩ , TiCl 极易
4
水 解 , 为 防 止外界水蒸气进入 , 最后连接 ③⑤ ,安装顺序为①⑨⑧⑥⑩ ③⑤ ; 由于
TiCl 、CCl 分子结构相似 ,TiCl 的相对分子质量大于CCl ,TiCl 分子间的范德华力较
4 4 4 4 4
大 , TiCl 的沸点高于CCl , 故先蒸出的物质为CCl ; 答案为 : ⑥ ⑩ ③⑤ ;CCl 。
4 4 4 4
16.(1)③
(2)A
(3) 5 +2 +6H+=5 +2Mn2++3H O D
2
(4) 2 +8KOH+3O =4 +4H O
2 2
【解析】
【分析】
制取 (铬绿)的工艺流程中,含铬不锈钢废渣加入氢氧化钾、碳酸钾、通入氧气反应将
转化为 ,水浸过滤后滤液加入硫酸酸化调节pH,除去硅、铝元素,得到含
滤液,加入亚硫酸钠还原得到三价铬,加入氢氧化钠得到三价铬沉淀,最终生成。
(1)
述反应中NaI中钠元素、碘元素化合价反应前后没有发生改变,NaI既不是氧化产物,又
不是还原产物,故选③;
(2)
使NaNO 转化为不引起二次污染的N,NaNO 中氮元素化合价降低发生还原反应,为氧化
2 2 2
剂,则反应中需要加入还原性物质,氯化铵中氮元素化合价可以升高,具有还原性,可以
转化为氮气,答案选B;
(3)
①反应中 和 发生氧化还原反应,根据电子守恒配平,反应为:5 +2
+6H+=5 +2Mn2++3H O;
2
②NaNO 会导致Fe2+转化为Fe3+,说明亚硝酸钠具有氧化性,可服用维生素C解毒,维生
2
素C和亚硝酸钠反应,说明维生素C具有还原性;
A.亚硝酸钠具有氧化性,发生还原反应,被还原,选项A错误;
B.维生素C具有还原性,选项B正确;
C.可服用维生素C解毒,说明维生素C首先和亚硝酸钠反应,则还原性:维生素C>Fe2+
,选项C正确;
D.NaNO 具有氧化性,是氧化剂,选项D正确;
2
答案选A;
(4)
①由流程可知,在碱性条件下, 、KOH、O 反应生成 ,反应中氧气为氧化剂、
2
为还原剂,根据电子守恒配平,化学方程式为:2 +8KOH+3O =4
2
+4H O;
2
②由流程可知,“还原”时 中加入亚硫酸钠、稀硫酸反应后 发生还原反应
生成三价铬,则亚硫酸钠发生氧化反应生成硫酸钠,发生反应的离子方程式为
。
17.(1) Fe O SiO
2 3 2
(2)增大固液接触面积,加快反应速率,提高黄铁矿的利用率
(3)7Fe (SO )+FeS +8H O=15FeSO +8H SO
2 4 3 2 2 4 2 4
(4)蒸发浓缩、冷却结晶、过滤洗涤
(5) +2; 6Fe(NH )Fe(CN) +ClO -+6H+=6Fe(NH )Fe(CN) +H O+Cl-+6 +3H O
4 2 6 3 4 6 2 2
(6) HO NH ·H O
2 2 3 2
【解析】
【分析】已知黄铁矿高温煅烧生成Fe O,反应原理为:4FeS+11O 2Fe O+8SO,故产生的红
2 3 2 2 2 3 2
渣主要成分为Fe O 和SiO,将红渣粉碎后加入足量的50%的HSO 溶液加热充酸浸,反应
2 3 2 2 4
原理为:Fe O+3H SO =Fe (SO )+3H O,过滤出滤渣①,主要成分为SiO,向滤液中加入
2 3 2 4 2 4 3 2 2
黄铁矿进行还原,将Fe3+还原为Fe2+,由(3)小问可知不生成S沉淀,则硫元素被氧化为
,反应原理为:14Fe3++FeS +8H O=15Fe2++2 +16H+,然后进行工序①为蒸发浓缩、
2 2
冷却结晶,得到FeSO 晶体和母液主要含有FeSO 溶液和HSO ,加水溶解FeSO 晶体,向
4 4 2 4 4
所得溶液中加入(NH )SO 、K[Fe(CN) ]并用HSO 调节溶液的pH为3,进行沉铁过程,反
4 2 4 4 6 2 4
应原理为:Fe2++2 +[Fe(CN)]3-=Fe(NH)Fe(CN) ↓,然后过滤出沉淀,洗涤后加入
6 4 2 6
HSO 和NaClO 进行氧化步骤,反应原理为:6Fe(NH )Fe(CN) +
2 4 3 4 2 6
+6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 ,过滤、洗涤干燥即制得Fe(NH )Fe(CN) ,据此
4 6 2 4 6
分析解题。
(1)
由分析可知,红渣的主要成分为:Fe O,滤渣①的主要成分为:SiO,故答案为:Fe O;
2 3 2 2 3
SiO;
2
(2)
黄铁矿研细的主要目的是增大固液接触面积,加快反应速率,提高黄铁矿的利用率,故答
案为:增大固液接触面积,加快反应速率,提高黄铁矿的利用率;
(3)
由分析可知,还原工序中,不产生S单质沉淀,则硫元素被氧化为 ,反应原理为:
14Fe3++FeS +8H O=15Fe2++2 +16H+,故化学方程式为:
2 2
7Fe (SO )+FeS +8H O=15FeSO +8H SO ,故答案为:
2 4 3 2 2 4 2 4
7Fe (SO )+FeS +8H O=15FeSO +8H SO ;
2 4 3 2 2 4 2 4
(4)
由分析可知,工序①的名称为蒸发浓缩、冷却结晶、过滤洗涤,所得母液主要含有FeSO
4
溶液和HSO 可以循环利用,故答案为:蒸发浓缩、冷却结晶、过滤洗涤;
2 4
(5)
沉铁工序中产生的白色沉淀Fe(NH )Fe(CN) 中Fe的化合价为+2价和[Fe(CN) ]4-中的+3价,
4 2 6 6
由分析可知,氧化工序所发生的离子方程式为:6Fe(NH )Fe(CN) +
4 2 6
+6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 ,故答案为:+2;6Fe(NH )Fe(CN) +
4 6 2 4 2 6
+6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 ;
4 6 2
(6)
由分析可知,还原工序所得的滤液中主要含有FeSO 溶液和HSO ,向滤液中先加入一定
4 2 4
量的HO 溶液将Fe2+完全氧化为Fe3+,在向氧化后的溶液中加入氨水至不再产生沉淀为止,
2 2
过滤洗涤,对沉淀进行灼烧,即可制得Fe O·x H O和(NH )SO ,故所需要加入的试剂为
2 3 2 4 2 4HO 和NH ·H O,故答案为:HO;NH ·H O。
2 2 3 2 2 2 3 2
18. 钝化 3Cu+8H++2NO -=3Cu2++2NO↑+4HO
3 2
冒白烟 3CuO+2NH =3Cu+N+3HO 2Cu2++2Cl-+SO +2HO 2CuCl↓+
3 2 2 2 2
4H++SO 2-
4
【解析】
【分析】
(1)常温下铝遇浓硝酸钝化,据此解答;
(2)铜与稀硝酸反应生成硝酸铜、一氧化氮和水,据此解答;
(3)氨气的物质的量是 mol,溶液的质量是 g,溶液的体积为
= mL,据此解答;
(4)浓硝酸、浓氨水均易挥发,分别蘸取浓硝酸和浓氨水的玻璃棒接近后会产生白烟,据
此解答;
(5)B与C反应即CuO和NH 反应,生成铜单质、氮气和水,据此解答;
3
(6)J、K是同种金属的不同氯化物,K为白色沉淀,则K是CuCl,SO 还原氯化铜生成氯化
2
亚铜,据此解答;
【详解】
A、F为无色气体单质,B为具有刺激性气味的气体,化学家哈伯因合成B获得1918年的
诺贝尔化学奖,则B是氨气,A是氧气,D是NO,F是氮气,G是硝酸。C为黑色氧化物,
E为紫红色金属单质,I为蓝色沉淀,则C是氧化铜,与氨气发生氧化还原反应生成铜、氮
气和水,E是铜,与硝酸反应生成硝酸铜,I是氢氧化铜,J是氯化铜。
(1)常温下铝遇浓硝酸后表面形成一层致密的保护膜,该现象称为钝化,故答案为:钝化;
(2)铜与稀硝酸反应的离子方程式为3Cu+8H++2NO -=3Cu2++2NO↑+4HO,故答案为:
3 2
3Cu+8H++2NO -=3Cu2++2NO↑+4HO;
3 2
(3)氨气的物质的量是 mol,溶液的质量是 g,溶液的体积为
= mL,所以溶液的物质的量浓度为 mol·L-1,故答案为:;
(4)浓硝酸、浓氨水均易挥发,分别蘸取浓硝酸和浓氨水的玻璃棒接近后会产生硝酸铵,实
验现象是冒白烟,故答案为:冒白烟;
(5)B与C反应的化学方程式为3CuO+2NH =3Cu+N+3HO,故答案为:3CuO+
3 2 2
2NH =3Cu+N+3HO;
3 2 2
(6)J、K是同种金属的不同氯化物,K为白色沉淀,则K是CuCl,SO 还原氯化铜生成氯化
2
亚铜的离子方程式为2Cu2++2Cl-+SO +2HO 2CuCl↓+4H++SO 2-,故答案为:2Cu2
2 2 4
++2Cl-+SO +2HO 2CuCl↓+4H++SO 2-。
2 2 4