文档内容
第 03 讲 物质的量在化学方程式计算中的应用
目录
01 模拟基础练
【题型一】根据方程式进行计算
【题型二】关系式法在化学计算中的应用
【题型三】差量法在化学计算中的应用
【题型四】守恒法在化学计算中的应用
02 重难创新练
03 真题实战练
题型一 根据化学方程式进行计算
1.向500 mL氢氧化钠溶液中投入10.8 g铝,二者恰好完全反应,计算回答:
(1)铝的物质的量是 。
(2)氢氧化钠溶液的物质的量浓度是 。
(3)在标准状况下生成氢气的体积是 。
2.把10.2 g镁铝合金的粉末放入过量的烧碱溶液中,在标准状况下生成6.72 L氢气。试计算:
(1)该合金中铝的质量分数是 。
(2)该合金中镁与铝的物质的量之比是 。
3.把1.1 g铁、铝混合物溶于200 mL 5 mol·L-1盐酸中,反应后盐酸的浓度变为4.6 mol·L-1(溶液体积
变化忽略不计)。求:
(1)反应中消耗HCl的物质的量。
(2)该混合物中铝、铁的物质的量。
4.已知MnO 与浓盐酸反应的化学方程式为MnO + 4HCl(浓) MnCl +Cl↑+2H O,回答下列问题:
2 2 2 2 2
(1)该反应的离子方程式为___________________________。
(2)被氧化的HCl占HCl总量的________。
(3)当标准状况下有11.2 L氯气生成时,该反应转移的电子数为________(设N 为阿伏加德罗常数的值)。
A
(4)1.74 g MnO 与100 mL 12 mol·L-1的过量浓盐酸完全反应(假设HCl无挥发),在反应后的溶液中加入
2
足量的AgNO 溶液,可生成________g沉淀。
35.钢铁制品经常进行烤蓝处理,即在铁制品的表面生成一层致密的Fe O 。某学习小组为了研究烤蓝
3 4
铁片,分别进行了以下实验操作:
①把一定量烤蓝铁片加工成均匀粉末。
②取m g该粉末,放入28.00 mL 1 mol·L-1的盐酸中,恰好完全反应,生成标准状况下的气体134.4
mL,向溶液中滴入KSCN溶液,无明显现象。
完成下列各题:
(1)将反应后的溶液稀释至100 mL,则溶液中c(Fe2+) = 。
(2)样品中n(Fe)∶n(Fe O) = 。
3 4
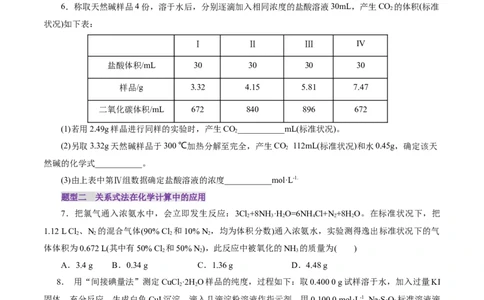
6.称取天然碱样品4份,溶于水后,分别逐滴加入相同浓度的盐酸溶液30mL,产生CO 的体积(标准
2
状况)如下表:
Ⅰ Ⅱ Ⅲ IV
盐酸体积/mL 30 30 30 30
样品/g 3.32 4.15 5.81 7.47
二氧化碳体积/mL 672 840 896 672
(1)若用2.49g样晶进行同样的实验时,产生CO___________mL(标准状况)。
2
(2)另取3.32g天然碱样品于300 ℃加热分解至完全,产生CO 112mL(标准状况)和水0.45g,确定该天
2
然碱的化学式___________。
(3)由上表中第Ⅳ组数据确定盐酸溶液的浓度___________mol·L-1.
题型二 关系式法在化学计算中的应用
7.把氯气通入浓氨水中,会立即发生反应:3Cl+8NH·H O=6NH Cl+N +8H O。在标准状况下,把
2 3 2 4 2 2
1.12 L Cl 、N 的混合气体(90% Cl 和10% N ,均为体积分数)通入浓氨水,实验测得逸出标准状况下的气
2 2 2 2
体体积为0.672 L(其中有50% Cl 和50% N ),此反应中被氧化的NH 的质量为( )
2 2 3
A.3.4 g B.0.34 g C.1.36 g D.4.48 g
8. 用“间接碘量法”测定CuCl ·2H O样品的纯度,过程如下:取0.400 0 g试样溶于水,加入过量KI
2 2
固体,充分反应,生成白色CuI沉淀,滴入几滴淀粉溶液作指示剂,用0.100 0 mol·L-1 Na SO 标准溶液滴
2 2 3
定,到达滴定终点时,消耗Na
2
S
2
O
3
标准溶液20.00 mL。(滴定反应为I
2
+2S 2O2-=S 4O2-+2I-)
3 6
(1)写出生成白色CuI沉淀的离子方程式:____________________________。
(2)该样品中CuCl ·2H O的质量分数为______________。
2 2
9.化学需氧量(COD)是衡量水质的重要指标之一,COD 是指在特定条件下用一种强氧化剂(如
KMnO )定量地氧化水体中的还原性物质所消耗的氧化剂的量(折算为氧化能力相当的O 质量,单位:
4 2
mg·L-1)。某水样的COD测定过程如下:取100.0 mL水样,用硫酸酸化,加入10.00 mL 0.002 000 mol·L-1KMnO 溶液,充分作用后,再加入10.00 mL 0.005 000 mol·L-1 Na C O 溶液。用0.002 000 mol·L-1 KMnO
4 2 2 4 4
溶液滴定,滴定终点时消耗6.50 mL。
已知:2Mn O-+5C 2O2-+16H+=2Mn2++10CO
2
↑+8H
2
O。
4 4
(1)1 mol KMnO 的氧化能力与_____________g O 的氧化能力相当(作氧化剂时转移的电子数相同)。
4 2
(2)该水样的COD值是_____________mg·L-1。(写出计算过程,结果保留小数点后一位)
10.金属锡的纯度可以通过下述方法分析:将试样溶于盐酸,反应的化学方程式为
Sn+2HCl=SnCl +H ↑,再加入过量的FeCl 溶液,发生反应SnCl +2FeCl =SnCl +2FeCl ,最后用已知浓度的
2 2 3 2 3 4 2
KCr O 溶液滴定生成的Fe2+,反应的化学方程式为6FeCl +K Cr O+14HCl=6FeCl +2KCl+2CrCl +7H O。现
2 2 7 2 2 2 7 3 3 2
有金属锡试样0.613 g,经上述反应后,共用去0.100 mol·L-1 KCr O 溶液16.00 mL。求试样中锡的质量分
2 2 7
数_____________ (假定杂质不参加反应,锡的相对原子质量为119)。
11.一定条件下,将TiO 溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH Fe(SO ) 标准溶液滴定
2 4 4 2
Ti3+至全部生成Ti4+。称取TiO 样品0.60 g,消耗0.20 mol·L-1的NH Fe(SO ) 溶液36.75 mL,则样品中TiO
2 4 4 2 2
的质量分数是 98% 。
题型三 差量法在化学计算中的应用
12.工业纯碱中常含有少量的NaCl杂质,某化学兴趣小组取m g纯碱样品与足量稀盐酸充分反应,加
热、蒸干、灼烧,得n g固体.则该样品中纯碱的质量分数为 ( A)
106(n-m) 168(m-n) 84(n-m)
A. ×100% B. ×100% C. ×100% D.
11m 56m 11m
n-m
×100%
m
13.200℃时将 16.0g NaOH 和 NaHCO 的混合物放在密闭容器中加热到质量不再减少为止,称得剩
3
余固体质量为 14.8g,试回答:
(1)剩余固体的化学式是__________。
(2)原混合物中 NaOH 的质量分数__________。
14.臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来
制取臭氧:3O 2O。
2 3
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为_____________g·mol-1(保留
一位小数)。
(2)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为_____________L。
题型四 守恒法在化学计算中的应用
15.(2024•云南省大理市期末)有200mlMgCl 和AlCl 的混合物,其中c(Mg2+)为0.2mol/L,c(C1-)为
2 3
1.3mol/L。为使Mg2+全部转化为沉淀分离出来,至少需加4mol/L溶液的NaOH体积为( )A.40ml B.72ml C.80ml D.128ml
16.14 g铜金合金与足量的某浓度硝酸反应,将产生的气体与 2.24 L(标准状况)O 混合,通入水中,
2
气体恰好被完全吸收,则合金中铜的质量为( )
A.9.6 g B.6.4 g C.12.8 g D.1.6 g
17.碳酸铜和碱式碳酸铜[Cu (OH) CO]均可溶于盐酸,转化为氯化铜。在高温下这两种化合物均能分
2 2 3
解成氧化铜。溶解28.4 g上述混合物,消耗1 mol·L-1盐酸500 mL。煅烧等质量的上述混合物,得到氧化铜
的质量是 ( )
A.35 g B.30 g C.20 g D.15 g
18.向500 mL稀硝酸中加入一定量的铁粉,铁粉完全溶解后,放出NO 6.272 L(标准状况下),同时溶
液质量增加11.2 g。下列判断不正确的是 ( )
A.原HNO 的物质的量浓度为2.24 mol·L-1
3
B.原溶液中投入铁粉的物质的量是0.2 mol
C.反应后溶液中c(Fe3+)∶c(Fe2+)=2∶3
D.反应后的溶液还可以溶解铜粉4.48 g
19.将13.6 g Fe、Fe O 和CuO的混合粉末加入100 mL一定物质的量浓度的盐酸中,充分反应,生成
2 3
标准状况下的氢气896 mL,过滤,滤渣经洗涤、干燥后得到1.28 g固体纯净物,经检验滤液中只含有一种
溶质。请回答:
(1)固体混合物中CuO的质量为_____________。
(2)盐酸的浓度为_____________。
20. 取1.77 g镁铝合金投入100 mL 2.00 mol·L-1的盐酸中,合金完全溶解,放出氢气1.904 L(已折算
成标准状况)。请计算:
(1)镁铝合金中镁的质量分数=_____________%(保留三位有效数字)。
(2)上述溶液中继续滴加 V mL 1.00 mol·L-1的 NaOH 溶液,得到沉淀 3.10 g。则 V 的最大值
=____________。
21.已知一定量的氢气在氯气中燃饶,所得混合物用 500mL 6.0 mol·L-1的KOH溶液恰好完全吸收,测
得溶液中含有ClO- 0.20 mol、ClO -0.30 mol(忽略氯气与水反应、盐类水解及溶液体积变化)。回答下列问题。
3
(1)所得溶液中c(Cl-)为________mol·L-1。
(2)所用氯气和参加反应的氢气的物质的量之比n(Cl )∶n(H )=________。
2 2
1.(2024•安徽省合肥市期中)某稀溶液中含有4mol KNO 和2mol HSO ,向其中加入1.2mol Fe,充分
3 2 4
反应(已知NO -被还原为NO),最终溶液体积为1L,下列说法正确的是( )
3A.所得溶液中c(NO -)=2.75mol·L-1 B.所得溶液中c(Fe2+):c(Fe3+)=1:1
3
C.反应后生成NO的体积为28L(标准状况下) D.所得溶液中的溶质只有FeSO
4
2.(2024•湖南省名校联考期中)将2.56 gCu投入12mL10mol·L-1硝酸中,恰好完全反应,向反应后的溶
液中加入40mLamol·L-1NaOH溶液,Cu2+恰好完全沉淀,将生成的气体与bmol O 一起通入足量NaOH溶液
2
中,气体恰好被完全吸收生成c mol NaNO 。下列判断正确的是( )
3
A.生成的气体中只有NO B.
C. D.
3.(2024•湖北省云学名校新高考联盟期中联考)将13.6g Cu和Cu O组成的混合物加入250 mL一定浓
2
度的稀硝酸中,固体完全溶解生成Cu(NO ) 和NO,向所得溶液中加入1.0 L 0.5 mol/LNaOH溶液时,金属
3 2
离子恰好沉淀完全,生成沉淀的质量为19.6 g,下列说法错误的是( )
A.原稀硝酸的浓度为2 mol/L
B.Cu和Cu O的物质的量之比为2:1
2
C.反应后剩余硝酸的物质的量为0.1 mol
D.产生的NO在标准状况下的体积为2.24L
4.(2024•安徽省淮北市期中)将1.76g镁铜合金投入20mL一定浓度的硝酸中,合金完全溶解,产生
NO和NO 混合气体896mL(不考虑其他气体,体积折算为标准状况下),反应结束后向溶液中加入
2
120mL1mol·L-1NaOH溶液,恰好使溶液中的金属阳离子全部转化为沉淀3.12g。若将盛有896mL该混合气
体的容器倒扣在水中,通入一定体积的氧气,恰好可将该混合气体完全转化。下列说法错误的是( )
A.Mg与Cu的物质的量比值为3:1 B.NO和NO 的体积比为1:1
2
C.原硝酸的浓度为8mol·L-1 D.通入的O 的体积(标准状况下)V=448Ml
2
5.(2024•上海省浦东新区期中)某学生用 NaHCO 和 KHCO 组成的某混合物与盐酸进行实验,测得下
3 3
表数据(盐酸的物质的量浓度相等,体积均为 50 mL)。
实验编号 I II III
盐酸的体积 50.0mL 50.0mL 50.0mL
m(混合物) 13.56g 21.88g 25.36g
V(CO )(标准状况) 3.36L 5.04L 5.04L
2
(1)则该学生所用盐酸的物质的量浓度是 mol/L;
(2)50 mL 该盐酸恰好能溶解上述组成的混合物的质量是 g;
(3)上述固体混合物中 KHCO 的质量分数是 (用小数表示,保留 2 位小数)。
3
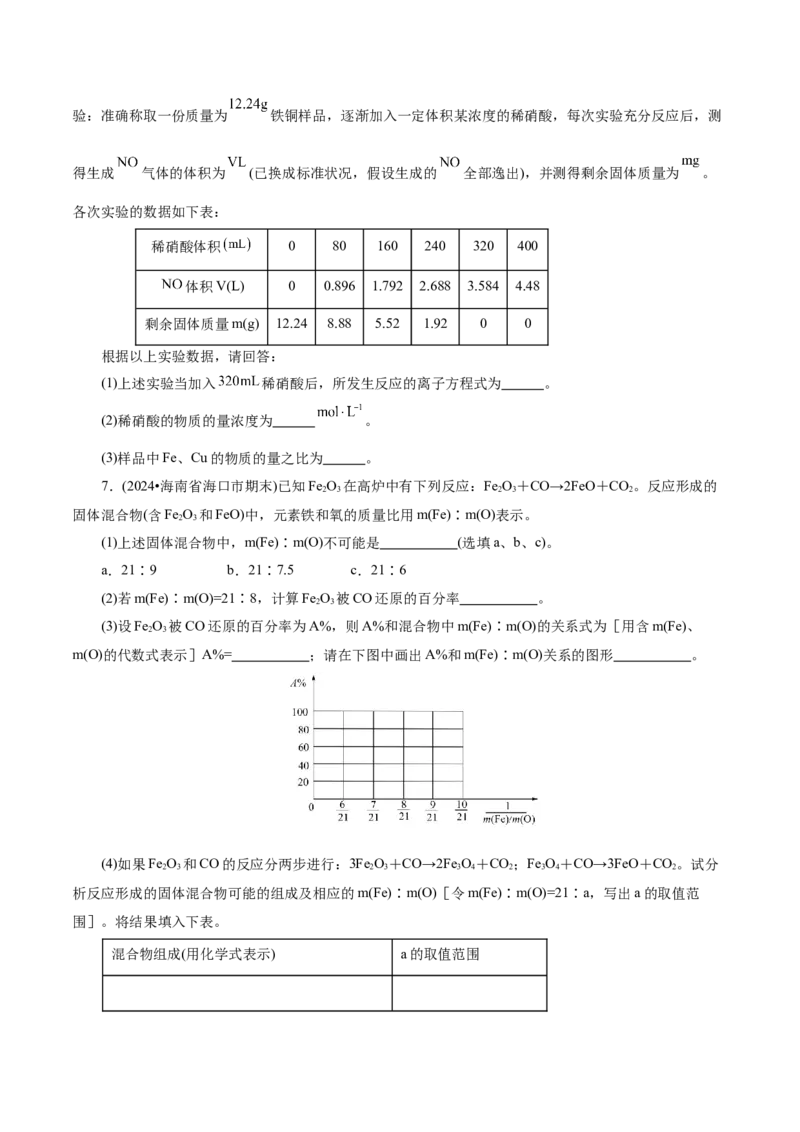
6.(2024•浙江省浙南名校联盟开学考试)为确定某一铁铜样品中各成份的含量,某同学进行了如下实验:准确称取一份质量为 铁铜样品,逐渐加入一定体积某浓度的稀硝酸,每次实验充分反应后,测
得生成 气体的体积为 (已换成标准状况,假设生成的 全部逸出),并测得剩余固体质量为 。
各次实验的数据如下表:
稀硝酸体积 0 80 160 240 320 400
体积V(L) 0 0.896 1.792 2.688 3.584 4.48
剩余固体质量m(g) 12.24 8.88 5.52 1.92 0 0
根据以上实验数据,请回答:
(1)上述实验当加入 稀硝酸后,所发生反应的离子方程式为 。
(2)稀硝酸的物质的量浓度为 。
(3)样品中Fe、Cu的物质的量之比为 。
7.(2024•海南省海口市期末)已知Fe O 在高炉中有下列反应:Fe O+CO→2FeO+CO。反应形成的
2 3 2 3 2
固体混合物(含Fe O 和FeO)中,元素铁和氧的质量比用m(Fe)∶m(O)表示。
2 3
(1)上述固体混合物中,m(Fe)∶m(O)不可能是 (选填a、b、c)。
a.21∶9 b.21∶7.5 c.21∶6
(2)若m(Fe)∶m(O)=21∶8,计算Fe O 被CO还原的百分率 。
2 3
(3)设Fe O 被CO还原的百分率为A%,则A%和混合物中m(Fe)∶m(O)的关系式为[用含m(Fe)、
2 3
m(O)的代数式表示]A%= ;请在下图中画出A%和m(Fe)∶m(O)关系的图形 。
(4)如果Fe O 和CO的反应分两步进行:3Fe O+CO→2Fe O+CO;Fe O+CO→3FeO+CO。试分
2 3 2 3 3 4 2 3 4 2
析反应形成的固体混合物可能的组成及相应的m(Fe)∶m(O)[令m(Fe)∶m(O)=21∶a,写出a的取值范
围]。将结果填入下表。
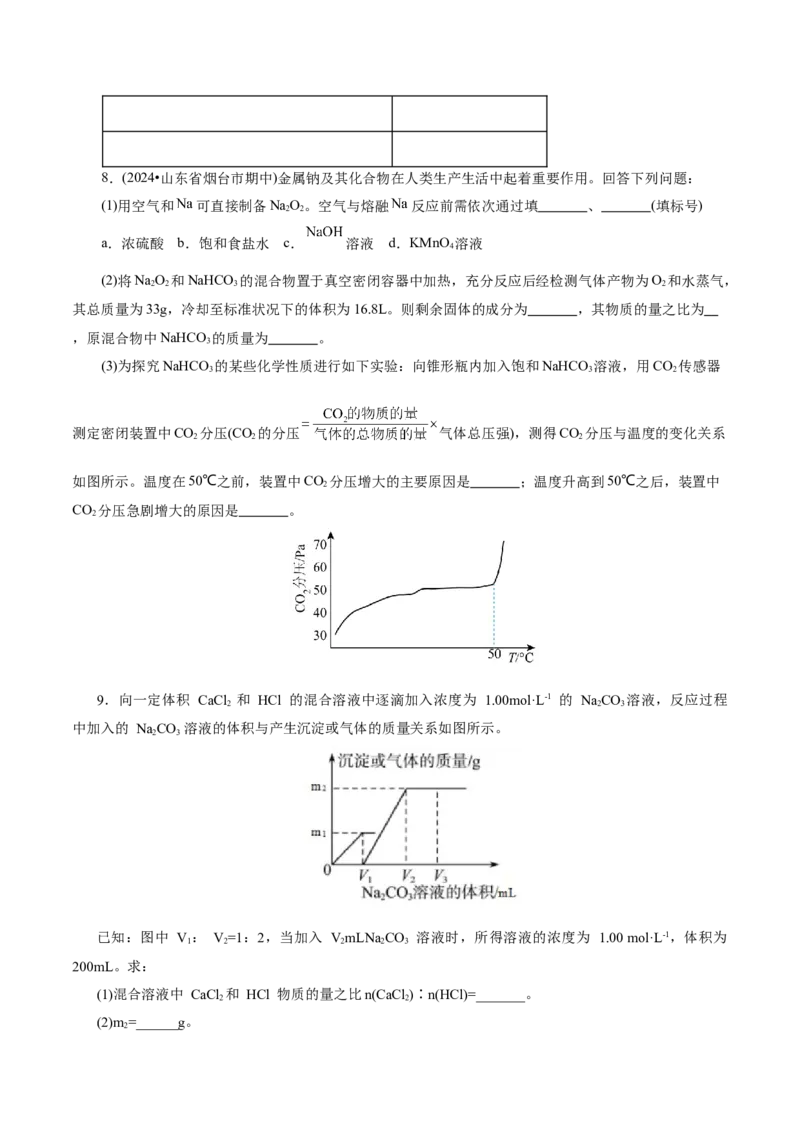
混合物组成(用化学式表示) a的取值范围8.(2024•山东省烟台市期中)金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)用空气和 可直接制备NaO。空气与熔融 反应前需依次通过填 、 (填标号)
2 2
a.浓硫酸 b.饱和食盐水 c. 溶液 d.KMnO 溶液
4
(2)将NaO 和NaHCO 的混合物置于真空密闭容器中加热,充分反应后经检测气体产物为O 和水蒸气,
2 2 3 2
其总质量为33g,冷却至标准状况下的体积为16.8L。则剩余固体的成分为 ,其物质的量之比为
,原混合物中NaHCO 的质量为 。
3
(3)为探究NaHCO 的某些化学性质进行如下实验:向锥形瓶内加入饱和NaHCO 溶液,用CO 传感器
3 3 2
测定密闭装置中CO 分压(CO 的分压 气体总压强),测得CO 分压与温度的变化关系
2 2 2
如图所示。温度在50℃之前,装置中CO 分压增大的主要原因是 ;温度升高到50℃之后,装置中
2
CO 分压急剧增大的原因是 。
2
9.向一定体积 CaCl 和 HCl 的混合溶液中逐滴加入浓度为 1.00mol·L-1 的 NaCO 溶液,反应过程
2 2 3
中加入的 NaCO 溶液的体积与产生沉淀或气体的质量关系如图所示。
2 3
已知:图中 V : V=1:2,当加入 VmLNa CO 溶液时,所得溶液的浓度为 1.00 mol·L-1,体积为
1 2 2 2 3
200mL。求:
(1)混合溶液中 CaCl 和 HCl 物质的量之比n(CaCl )∶n(HCl)=_______。
2 2
(2)m =______g。
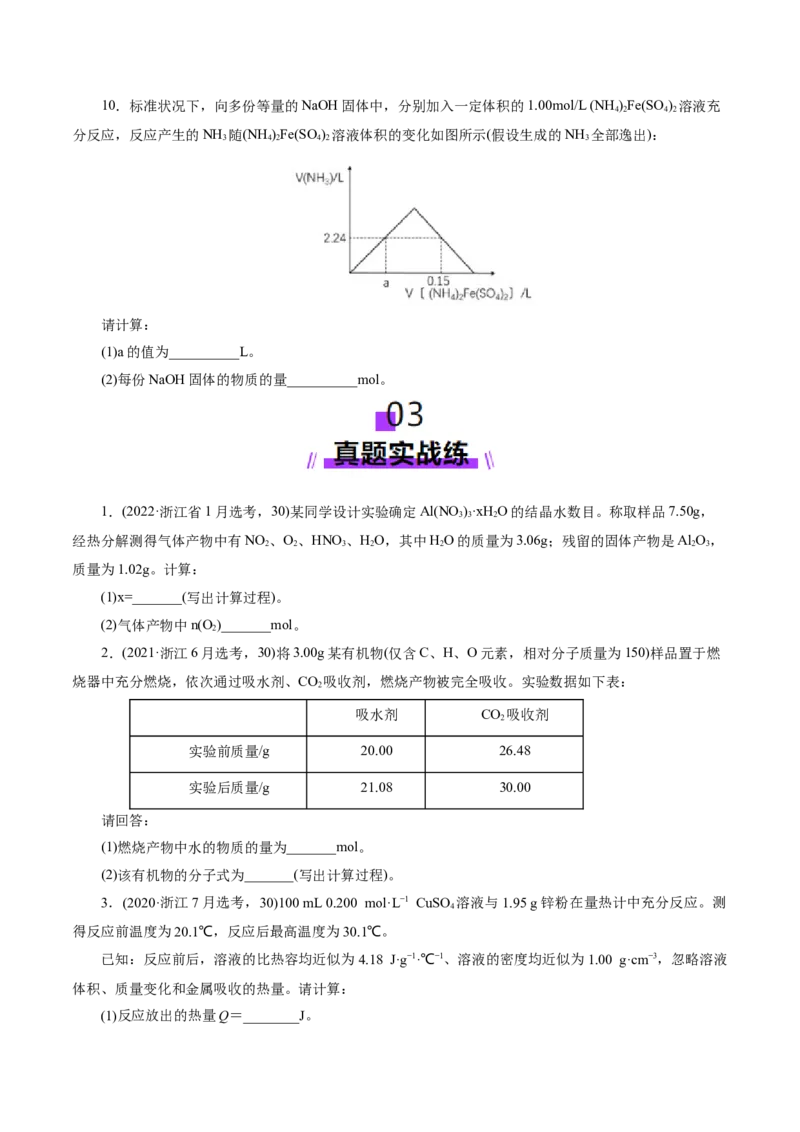
210.标准状况下,向多份等量的NaOH固体中,分别加入一定体积的1.00mol/L (NH)Fe(SO ) 溶液充
4 2 4 2
分反应,反应产生的NH 随(NH )Fe(SO ) 溶液体积的变化如图所示(假设生成的NH 全部逸出):
3 4 2 4 2 3
请计算:
(1)a的值为__________L。
(2)每份NaOH固体的物质的量__________mol。
1.(2022·浙江省1月选考,30)某同学设计实验确定Al(NO )·xH O的结晶水数目。称取样品7.50g,
3 3 2
经热分解测得气体产物中有NO 、O、HNO、HO,其中HO的质量为3.06g;残留的固体产物是Al O,
2 2 3 2 2 2 3
质量为1.02g。计算:
(1)x=_______(写出计算过程)。
(2)气体产物中n(O )_______mol。
2
2.(2021·浙江6月选考,30)将3.00g某有机物(仅含C、H、O元素,相对分子质量为150)样品置于燃
烧器中充分燃烧,依次通过吸水剂、CO 吸收剂,燃烧产物被完全吸收。实验数据如下表:
2
吸水剂 CO 吸收剂
2
实验前质量/g 20.00 26.48
实验后质量/g 21.08 30.00
请回答:
(1)燃烧产物中水的物质的量为_______mol。
(2)该有机物的分子式为_______(写出计算过程)。
3.(2020·浙江7月选考,30)100 mL 0.200 mol·L−1 CuSO 溶液与1.95 g锌粉在量热计中充分反应。测
4
得反应前温度为20.1℃,反应后最高温度为30.1℃。
已知:反应前后,溶液的比热容均近似为4.18 J·g−1·℃−1、溶液的密度均近似为1.00 g·cm−3,忽略溶液
体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量Q=________J。(2)反应Zn(s)+CuSO (aq)===ZnSO(aq)+Cu(s)的ΔH=________kJ·mol−1(列式计算)。
4 4
4.(2019·浙江4月选考,30)由C、H、O三种元素组成的链状有机化合物X,只含有羟基和羧基两种
官能团,且羟基数目大于羧基数目。称取2.04 g纯净的X,与足量金属钠充分反应,生成672 mL氢气(标
准状况)。请确定摩尔质量最小的X分子中羟基、羧基数目及该X的相对分子质量(要求写出简要推理过程)。