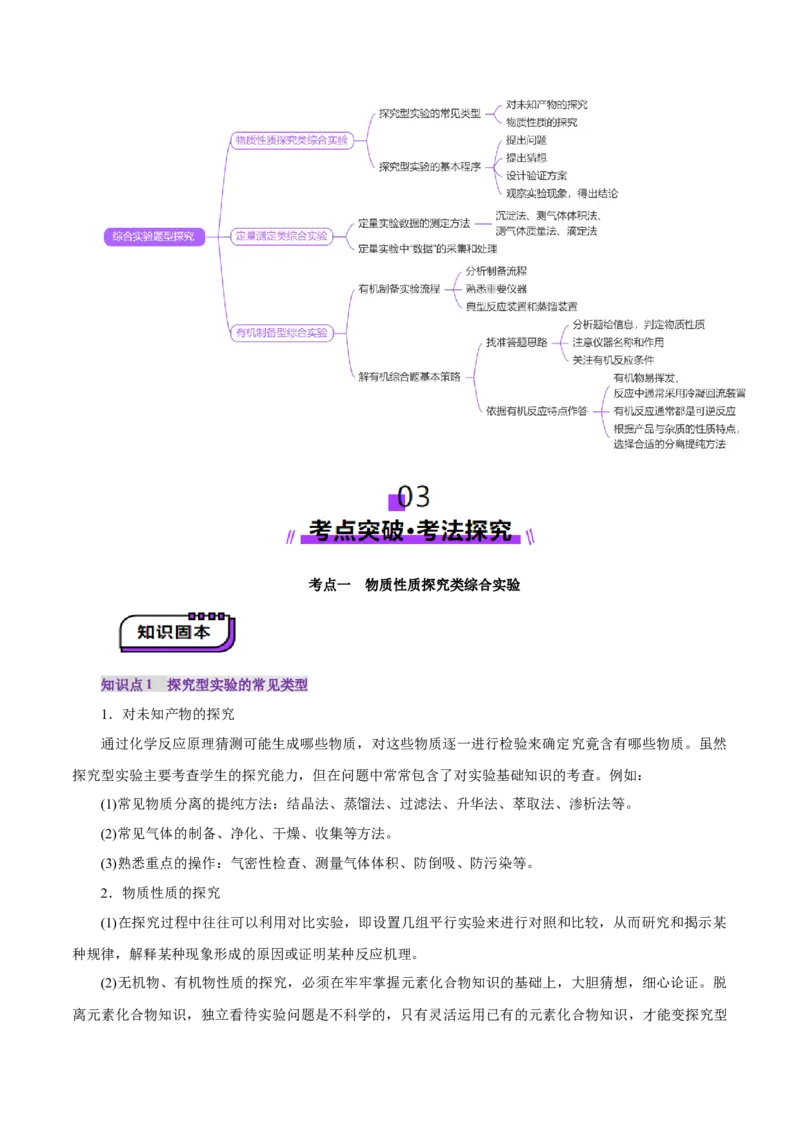
文档内容
第 04 讲 综合实验题型探究
目录
01
考情透视·目标导航
02 知识导图·思维引航...................................................................................................................
03考点突破·考法探究....................................................................................................................
考点一 物质性质探究类综合实验........................................................................................
知识点1探究型实验的常见类型..........................................................................................
知识点2探究型实验的基本程序..........................................................................................
考向1 验证型综合实验........................................................................................................
考向2 猜想型综合实验........................................................................................................
考点二 定量测定类综合实验................................................................................................
知识点1 定量实验数据的测定方法....................................................................................
知识点2 定量实验中“数据”的采集和处理......................................................................
考向1 滴定操作型在定量测定实验中的应用......................................................................
考向2 气体关联型在定量测定实验中的应用......................................................................
考点三 有机制备型实验题....................................................................................................
知识点1 有机制备实验流程.............................................................................................
知识点2 解有机综合题基本策略.......................................................................................
考向 有机物的制备............................................................................................................
04真题练习·命题洞见....................................................................................................................考点要
考题统计 考情分析
求
2023•湖南卷18题,15分;2023山东卷18
常见物质的 题,12分;2023辽宁卷17题,14分;2022
制备 山东卷18题,12分;2022全国乙卷27题,
14分;2021辽宁卷18题,13分
综合实验题是每年考查能力的综合
2023浙江1月选考20题,10分;2022全国甲
化学实验条 压轴题,其综合性强、难度大,是一道
卷27题,15分;2022湖北卷18题,14分;
件的控制 拉分的主要试题。本讲试题将以元素化
2021湖北卷18题,14分
合物知识为依托,以陌生物质制备为背
景,充分体现了“源于教材,又不拘泥
于教材”的命题指导思想,把化学实验
基础知识和基本操作技能准确迁移到类
化学实验方 2023全国甲卷28题,14分;2023北京卷19
似的实验中去,题目类型主要有物质制
案的设计与 题,14分;2022湖南卷15题,12分;2022
备类、实验探究类、定量测定类等,但
评价 北京卷19题,14分
并不拘泥于固定的形式,但由于物质陌
生、设问巧妙,在解题中,往往让考生
感到“老虎吃天、无从下口”的畏惧
感。备考中要注意有机物的涉入,理清
探究型实验 2023•广东卷17题,14分;2021广东卷17 关系,熟记切入点——从安全、环保、
方案 题,14分 可行、简约等角度进行评价分析。
2023全国乙卷26题,14分;2023山东卷18
题,12分;2023湖北卷18题,14分;2023
定量测定实 浙江6月选考20题,10分;2022山东卷18
验 题,12分;2022广东卷17题,14分;2022
河北卷14题,14分;2021山东卷18题,12
分;2021全国甲卷27题,14分
复习目标:
1.设计、评价、改进实验方案;
2.正确选用实验装置;
3.掌握控制实验条件的方法;
4.预测或描述实验现象、分析或处理实验数据、得出合理结论。考点一 物质性质探究类综合实验
知识点1 探究型实验的常见类型
1.对未知产物的探究
通过化学反应原理猜测可能生成哪些物质,对这些物质逐一进行检验来确定究竟含有哪些物质。虽然
探究型实验主要考查学生的探究能力,但在问题中常常包含了对实验基础知识的考查。例如:
(1)常见物质分离的提纯方法:结晶法、蒸馏法、过滤法、升华法、萃取法、渗析法等。
(2)常见气体的制备、净化、干燥、收集等方法。
(3)熟悉重点的操作:气密性检查、测量气体体积、防倒吸、防污染等。
2.物质性质的探究
(1)在探究过程中往往可以利用对比实验,即设置几组平行实验来进行对照和比较,从而研究和揭示某
种规律,解释某种现象形成的原因或证明某种反应机理。
(2)无机物、有机物性质的探究,必须在牢牢掌握元素化合物知识的基础上,大胆猜想,细心论证。脱
离元素化合物知识,独立看待实验问题是不科学的,只有灵活运用已有的元素化合物知识,才能变探究型实验为验证型实验,使复杂问题简单化。
【名师提醒】
1.物质氧化性、还原性的判断。如探究SO 具有还原性的方法是将气体通入酸性KMnO 溶液中,通
2 4
过酸性KMnO 溶液褪色或变浅来说明SO 的还原性;验证Fe3+的氧化性强于I 时,可利用FeCl 与淀粉-KI
4 2 2 3
溶液反应,通过溶液变为蓝色的现象来说明Fe3+的氧化性强于I。
2
2.同周期、同主族元素性质递变规律的验证,一般通过设计比较元素金属性、非金属性强弱的实验
来完成。如通过比较Mg、Al与同浓度盐酸反应产生H 的快慢来比较Mg、Al的金属活动性。
2
3.电解质强弱的判断。如探究一元酸 HA 是弱酸的方法是常温下配制 NaA 溶液,测其 pH,若
pH>7,说明HA为弱酸。
4.物质酸性强弱的判断。如探究碳酸和硅酸的酸性强弱,可利用相对强的酸制备相对弱的酸的反应
原理,将CO 气体通入NaSiO 溶液,看是否有白色胶状沉淀生成来判断HCO 与HSiO 酸性的强弱。
2 2 3 2 3 2 3
5.钢铁发生电化学腐蚀的规律探究。可以通过控制钢铁是否与空气接触、所接触的电解质溶液的酸
碱度、钢铁在腐蚀过程中体系内的气压变化等设计实验,找出规律。
知识点2 探究型实验的基本程序
解答探究型实验题的基本程序可用以下流程图表示:
1.提出问题
要提出问题,首先得发现问题,对题给信息进行对比、质疑,通过思考提出值得探究的问题。此外,
实验中出现的特殊现象也是发现问题、提出问题的重要契机。
2.提出猜想
所谓猜想就是根据已有知识对问题的解决提出的几种可能的情况。有一些问题,结论有多种可能(这就
是猜想),只能通过实验进行验证。
3.设计验证方案
提出猜想后,就要结合题给条件,设计出科学、合理、安全的实验方案,对可能的情况进行探究。实
验设计中,关键点是对试剂的选择和实验条件的调控。
4.观察实验现象,得出结论
考向1 验证型综合实验
【例1】某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。(1)浓盐酸与MnO 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO 。
2 2
①反应的离子方程式是 。
②电极反应:
ⅰ.还原反应:MnO +2e-+4H+=Mn2++2H O
2 2
ⅱ.氧化反应: 。
③根据电极反应,分析A中仍存在盐酸和MnO 的原因。
2
ⅰ.随着c(H+)降低或c(Mn2+)升高,MnO 氧化性减弱。
2
ⅱ.随着c(Cl-)降低, 。
④补充实验证实③中的分析。
实验操作 试剂 产物
Ⅰ 较浓HSO 有氯气
2 4
Ⅱ a 有氯气
Ⅲ a+b 无氯气
a是 ,b是 。
(2)利用c(H+)对MnO 氧化性的影响,探究卤素离子的还原性。相同浓度的 KCl、KBr、KI溶液与
2
MnO 反应所需的最低c(H+)由大到小的顺序是 ,从原子结构角度说明理由: 。
2
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以增强溴的氧化性,将 Mn2+氧化为MnO 。经
2
实验证实了推测,该化合物是 。
(4)Ag分别与1 mol·L-1的盐酸、氢溴酸和氢碘酸混合,Ag只与氢碘酸发生置换反应,试解释原因:
。
(5)总结:物质氧化性和还原性变化的一般规律是 。
【思维建模】【变式训练】某研究性学习小组通过下列实验验证AgI沉淀的生成会使I 的氧化能力增强而将Fe2+氧
2
化。
回答下列问题:
(1)由AgNO 固体配制50 mL 0.1 mol·L-1的AgNO 溶液,配制好的溶液应转移到 试剂瓶中
3 3
保存。
(2)步骤1的实验现象是 ;步骤2无明显现象;步骤3最终的实验现象是溶液中生成黄色
沉淀, 。由此可知,步骤3反应的离子方程式为 。
(3)某同学在实验时漏掉步骤2,直接加入过量AgNO 溶液,也观察到与步骤3相同的实验现象。该同
3
学推测溶液中还有I-
生成,并由此对I 氧化Fe2+的结论产生了质疑。
3 2(4)为了确证AgI的生成使I 的氧化能力增强而将Fe2+氧化,学习小组在上述实验基础上进行补充实验:
2
分别取少量的 和步骤3试管中的上层清液于试管a和试管b中,往两支试管中加入过量的
,观察到的现象为 。
考向2 猜想型综合实验
【例2】为更好地利用化学变化中的物质变化和能量变化,在化学研究和工业生产中还需要关注化学
反应的快慢和进行程度等。
(1)研究小组向4.5mL1mol·L-1KCl溶液中加入0.50mL0.2mol·L-1 AgNO 溶液,产生AgCl沉淀,静置,
3
得到AgCl滤液;在AgCl滤液中放入5cm长的镁条后,立即有无色气泡产生,气体可燃,滤液中逐渐出现
白色浑浊。
【发现问题】对比发现,Mg+AgCl滤液反应比Mg+HO反应速率快。研究小组对此实验现象产生的原
2
因进行了探究。
【查阅资料】Cl-类体积较小的阴离子,能够“钻入” Mg(OH) 膜,达到使其溶解的效果,称作“离
2
子钻入效应”,
【提出猜想】
猜想一:Cl-钻入Mg(OH) 膜形成孔径,增大了Mg和HO的接触面积,加快了Mg+HO的反应速率;
2 2 2
猜想二:在“离子钻入效应”基础上, 置换Ag+形成许多微小的Mg-Ag原电池,使Mg+HO反应
2
速率进一步加快。
【实验设计】用砂纸擦去镁条表面氧化膜,取表面积和质量相同的镁条(5cm),用浓度分别为1
mol·L-1KCl、0.2 mol·L-1 AgNO、0.2 mol·L-1 KNO 溶液,按照下表进行系列实验,若有沉淀,先将沉淀过
3 3
滤后,将滤液加入装Mg条的试管,并观察Mg条表面实验现象。
实验序 V(KCl) V(AgNO ) V(KNO ) V(H O)
3 3 2 实验现象
号
1 / / / 5.00 微小气泡附着
2 4.50 0.50 / / 大量气泡放出
3 4.50 / / 0.50 少量气泡放出
4 a / b / 少量气泡放出
①根据表中信息,补充数据:a=_______,b=_______。
②由实验1和实验3对比可知: 有加快Mg+HO反应速率的作用。
2③由实验_______和实验_______对比可知:Ag+有加快Mg+HO反应速率的作用。
2
【实验结论】猜想一和猜想二成立。
(2)为了进一步证明 原电池能加快Mg+HO+ Cl-体系中Mg+HO的反应速率,研究小组利用数
2 2
字化实验进行了验证。
【实验设计】选取实验2和实验4两个实验方案,将各实验Mg条、溶液量等比例放大至30cm,
,采集两个实验的 时间、温度-时间变化数据(先采集约10s时溶液的 时间、温度-时间数据,
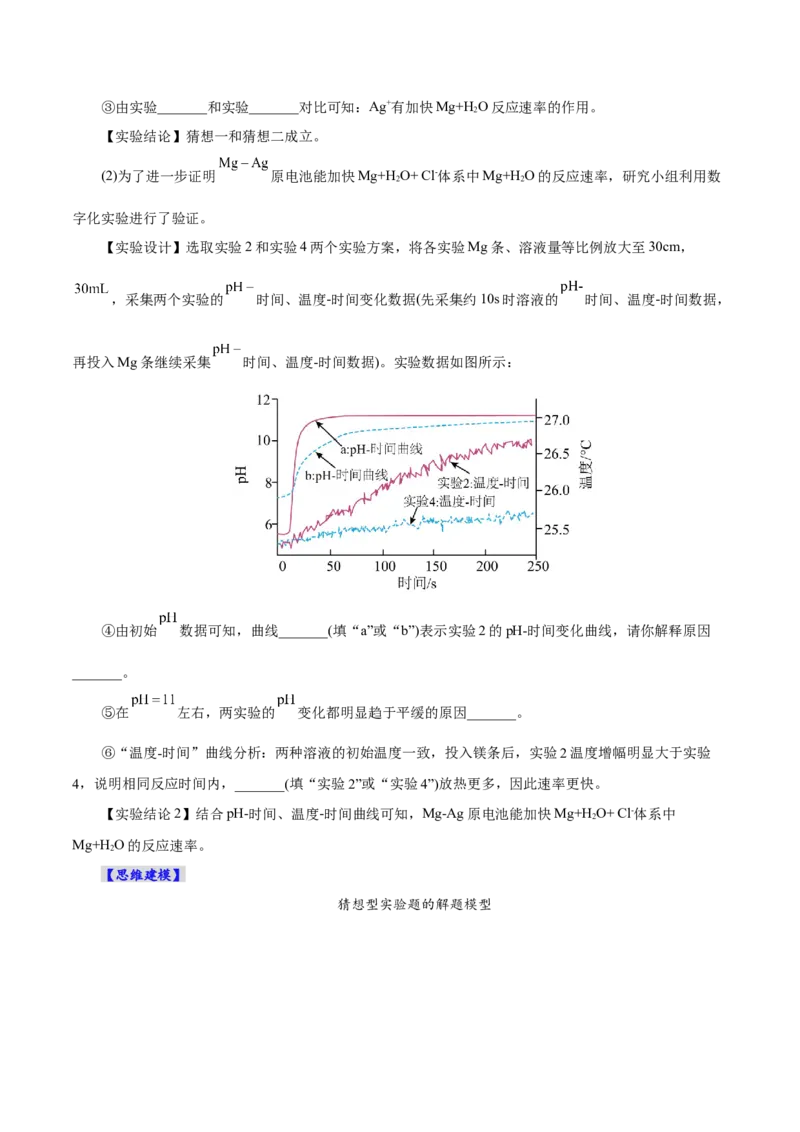
再投入Mg条继续采集 时间、温度-时间数据)。实验数据如图所示:
④由初始 数据可知,曲线_______(填“a”或“b”)表示实验2的pH-时间变化曲线,请你解释原因
_______。
⑤在 左右,两实验的 变化都明显趋于平缓的原因_______。
⑥“温度-时间”曲线分析:两种溶液的初始温度一致,投入镁条后,实验2温度增幅明显大于实验
4,说明相同反应时间内,_______(填“实验2”或“实验4”)放热更多,因此速率更快。
【实验结论2】结合pH-时间、温度-时间曲线可知,Mg-Ag原电池能加快Mg+HO+ Cl-体系中
2
Mg+HO的反应速率。
2
【思维建模】
猜想型实验题的解题模型【变式训练】(2024·浙江省杭州学军中学高三调研考试)某学习小组对Cu与HNO 的反应进行了研究。
3
(1)铜与稀硝酸反应的化学方程式是_______。
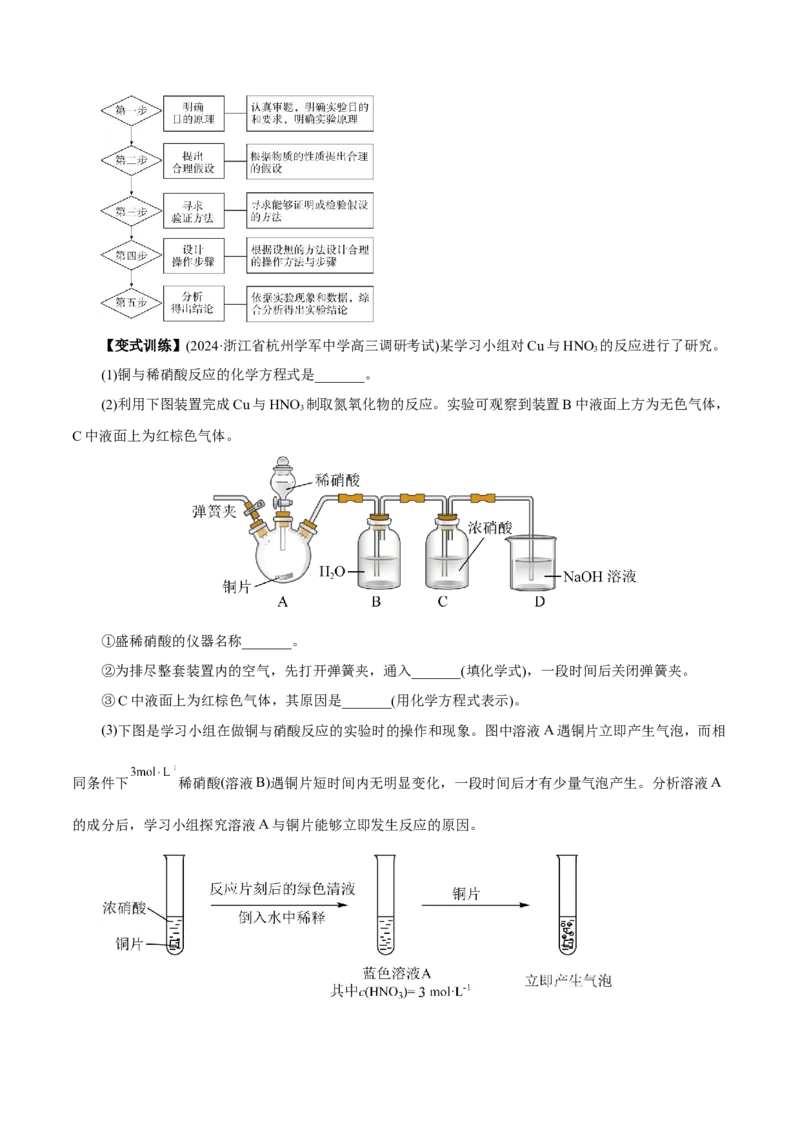
(2)利用下图装置完成Cu与HNO 制取氮氧化物的反应。实验可观察到装置B中液面上方为无色气体,
3
C中液面上为红棕色气体。
①盛稀硝酸的仪器名称_______。
②为排尽整套装置内的空气,先打开弹簧夹,通入_______(填化学式),一段时间后关闭弹簧夹。
③C中液面上为红棕色气体,其原因是_______(用化学方程式表示)。
(3)下图是学习小组在做铜与硝酸反应的实验时的操作和现象。图中溶液A遇铜片立即产生气泡,而相
同条件下 稀硝酸(溶液B)遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。分析溶液A
的成分后,学习小组探究溶液A与铜片能够立即发生反应的原因。①假设1:_______(填化学式)对该反应有催化作用。
实验验证:向溶液B中加入少量硝酸铜固体,溶液呈浅蓝色,放入铜片,没有明显变化。
结论:假设1不成立。
②假设2:NO 对该反应有催化作用。
2
方案1:向放有铜片的溶液B中通入少量NO ,铜片表面立即产生气泡,反应持续进行。有同学认为
2
应补充对比实验:另取一份放有铜片的溶液B,向其中加入数滴5mol·L—1硝酸,无明显变化。补充该实验
的目的是_______。
方案2:向A中鼓入N 数分钟得溶液C.相同条件下,铜片与A、C溶液的反应速率分别为 、
2
,当 _______ 。(填“>”、“=”、“<”)时,实验能够证明假设2成立。
③经检验,A溶液中还含有少量亚硝酸HNO。
2
设计实验证明HNO 也对该反应有催化作用。操作和预期现象是:向含有铜片的B溶液中_______。
2
最后结论:NO 和HNO 对铜与硝酸的反应都有催化作用。
2 2
考点二 定量测定类综合实验
知识点1 定量实验数据的测定方法
知识点2 定量实验中“数据”的采集和处理
1.称量固体质量时,中学一般用托盘天平,可估读到0.1 g,精确度要求高的实验中可以用电子天平。
2.测量液体体积时,一般实验中选用适当规格的量筒,可估读到0.1 mL,精确度要求高的定量实验,
如中和滴定中选用滴定管(酸式或碱式),可估读到0.01 mL。容量瓶作为精密的定容仪器,用于配制一定物
质的量浓度的溶液,一般不用于量取液体的体积。3.气体除了量取外,还可以称量。称气体的质量时一般有两种方法:一种方法是称反应装置在放出
气体前后的质量减小值;另一种方法是称吸收装置前后的质量增大值。
4.用pH试纸(测得整数值)或pH计(精密测量溶液的pH)直接测出溶液的pH,经过计算可以得到溶液
中H+或OH-的物质的量浓度。
5.为了数据的准确性,要进行平行实验,重复测定。如中和滴定实验中要平行做 2~3次滴定实验,
求算未知溶液的浓度再取平均值,但对于“离群”数据(指与其他数据有很大差异的数据)要舍弃,因为数
据“离群”的原因可能是操作中出现了较大的误差。
名师提醒】
实验数据处理时的“五看”
一看数据是否符合测量仪器的精度特点,如用托盘天平测得的质量的精度为 0.1 g,若精度值超过了这
个范围,说明所得数据是无效的;
二看数据是否在误差允许范围内,若所得的数据明显超出误差允许范围,要舍去;
三看反应是否完全,是否是过量反应物作用下所得的数据,只有完全反应时所得的数据,才能进行有
效处理和应用;
四看所得数据的测试环境是否一致,特别是气体体积数据,只有在温度、压强一致的情况下才能进行
比较、运算;
五看数据测量过程是否规范、合理,错误和违反测量规则的数据需要舍去。
考向1 滴定操作型在定量测定实验中的应用
【例1】(2024·天津市第七中学高三模拟)在科研和工农业生产中,氮、氯、砷(As)、铁、铜等元素形成
的单质及其化合物有着广泛的应用。请回答下列问题:
(1)As和N同族,基态砷原子的价层电子排布式为 。
(2) ClO -的空间结构名称为 。
3
(3)氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO 溶液的浓度,现用
3
0.1000mol/L的酸性KMnO 溶液进行滴定,反应原理为:5HSO -+2 MnO -+H+=2Mn2++3H O+5SO 2-。请回答
4 3 4 2 4
下列问题:
①用KMnO 进行滴定时,判断滴定终点的现象是 。
4
②下列操作会导致测定结果偏低的是 (填序号)。
A.酸式滴定管水洗后未用待测液润洗
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗C.滴定管尖嘴部分有气泡,滴定后消失
D.观察读数时,滴定前仰视,滴定后俯视
③根据下表中测定的实验数据,计算NaHSO 溶液的物质的量浓度 (写出计算过程,结果保
3
留4位有效数字)。
实验编号 待测NaHSO 溶液的体积/mL KMnO 溶液的体积/mL
3 4
1 20.00 15.98
2 20.00 17.00
3 20.00 16.02
【变式训练】 (2024·河北沧州高三联考)植物可滴定酸度是影响果实风味品质的重要因素,实验室用
滴定法测定葡萄可滴定酸度(以酒石酸计)。实验步骤如下:
Ⅰ.配制标准NaOH溶液并标定:用托盘天平称取mgNaOH固体,配成 溶液,
并用易于保存的基准物质邻苯二甲酸氢钾溶液标定,测得标准NaOH溶液的准确浓度为 。
Ⅱ.葡萄中有机酸含量的测定:剔除葡萄非可食用部分,切碎混匀,称取250g放入高速组织捣碎机,
并加入等质量的水,捣碎1~2min。称取匀浆50g并用水洗入250mL容量瓶,加水至刻度线。用标准NaOH
溶液滴定样液,计算葡萄可滴定酸度。
已知:①酒石酸是弱酸,结构简式为 。
②酒石酸的电离平衡常数为K =9.1×10-4,K =4.3×10-5。
a1 a2
回答下列问题:
(1) g。NaOH溶液使用前需标定的原因是 。
(2)酒石酸与足量NaOH溶液反应的离子方程式为 。
(3)实验过程中用不到的仪器有 (填标号),还需要用到的硅酸盐制品有 。
(4)用标准NaOH溶液滴定样液的操作步骤为①标准量取 样液,以酚酞为指示剂,用标准NaOH
溶液滴定,滴定终点的现象为 ,平行测定三组,平均消耗标准NaOH溶液V mL。
1②葡萄可滴定酸度(质量分数,以酒石酸计)为 (用含c、V、V 的代数式表示)。
0 1
考向2 气体关联型在定量测定实验中的应用
【例2】(2024·浙江省绍兴市高三下学期第二次模拟考试)氢化钙可作为轻便的氢气发生剂,也可用作
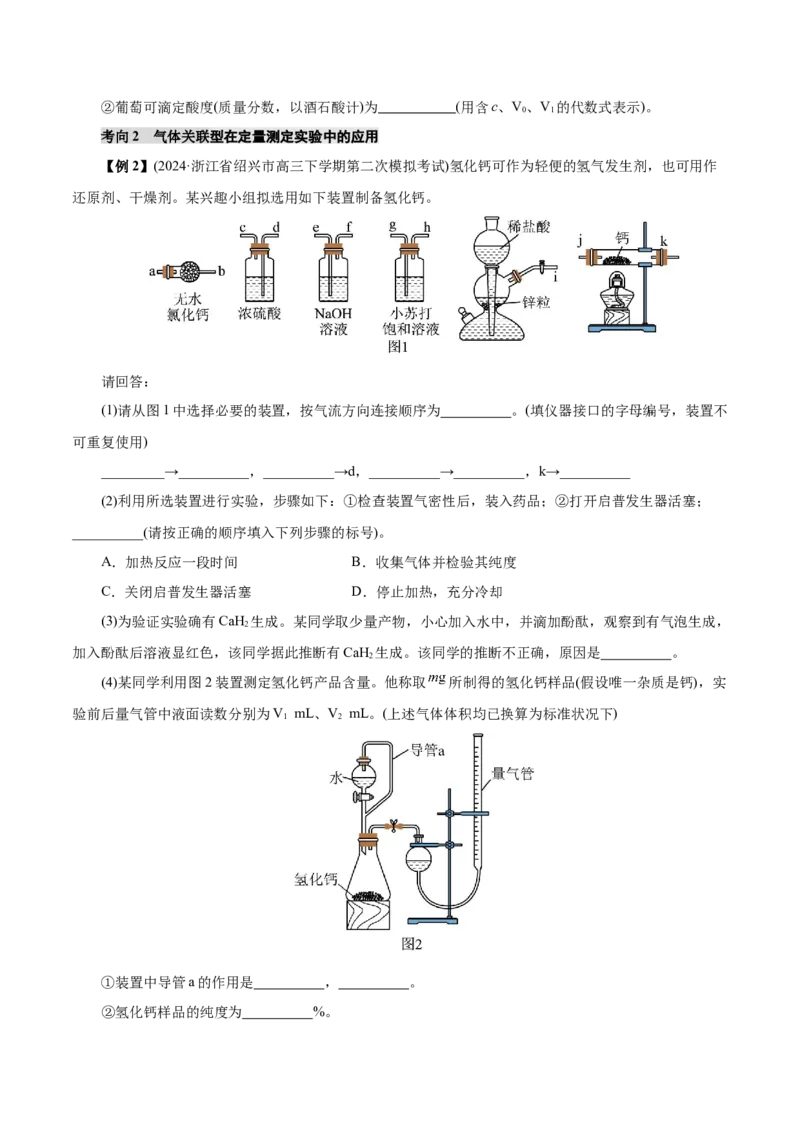
还原剂、干燥剂。某兴趣小组拟选用如下装置制备氢化钙。
请回答:
(1)请从图1中选择必要的装置,按气流方向连接顺序为 。(填仪器接口的字母编号,装置不
可重复使用)
_________→__________,__________→d,__________→__________,k→__________
(2)利用所选装置进行实验,步骤如下:①检查装置气密性后,装入药品;②打开启普发生器活塞;
__________(请按正确的顺序填入下列步骤的标号)。
A.加热反应一段时间 B.收集气体并检验其纯度
C.关闭启普发生器活塞 D.停止加热,充分冷却
(3)为验证实验确有CaH 生成。某同学取少量产物,小心加入水中,并滴加酚酞,观察到有气泡生成,
2
加入酚酞后溶液显红色,该同学据此推断有CaH 生成。该同学的推断不正确,原因是 。
2
(4)某同学利用图2装置测定氢化钙产品含量。他称取 所制得的氢化钙样品(假设唯一杂质是钙),实
验前后量气管中液面读数分别为V mL、V mL。(上述气体体积均已换算为标准状况下)
1 2
①装置中导管a的作用是 , 。
②氢化钙样品的纯度为 %。【名师点睛】
定量实验试题中,如何减小误差的措施是必考点,常见的措施:
①定量仪器的使用(特别是读数,如量气装置读数时要保证液面相平);
②减少固体产物的损失或除去杂质,如洗涤沉淀以及选用合适的洗涤剂(沉淀完全及如何洗涤沉淀);
③保证气体产物全部被吸收,如向装置中通入足量惰性气体将气体产物赶出等;
④沉淀剂的选用,如选用氢氧化钡效果比选用氢氧化钙效果好(因为碳酸钡的相对分子质量比碳酸钙大,
称量误差对结果造成影响小);
⑤防止其他气体物质的干扰,如防止固体产物吸收空气中的二氧化碳和水等;
⑥恒压漏斗的使用;
⑦许多实验中的数据处理,都是对多次测定结果求取平均值,但对于“离群”数据(指与其他测定数据
有很大差异的数据)要舍弃,因为数据离群的原因可能是在操作中出现了较大的失误。
【变式训练】(2024·浙江省金华市十校高三下学期模拟考试)半水煤气(含有 、N、H、HO,以及
2 2 2
少量的HS、CO 和O)经提纯后可获得工业合成氨所需的N 和H 混合气。过程如下:
2 2 2 2 2
已知:①C(s)+HO(g)=CO(g)+H(g) ΔH>0。
2 2
②HS与NaCO 反应的方程式为:NaCO+H S= NaHS+ NaHCO 。
2 2 3 2 3 2 3
③CO(g)+HO(g) CO(g)+H(g) ΔH<0。请回答:
2 2 2
(1)半水煤气通过 溶液(填化学式)可证明有HS气体。
2
(2)在“催化转化炉”的后半段补充通入120℃ HO(g)作“冷激气”,原因是 。
2
(3)已知:高压下CO 极易溶于水;用醋酸亚铜氨溶液(易被氧化)溶液可吸收 ,碱性焦没食子酸溶
2
液(易受酸性气体影响)可吸收O。“精制过程”需除去混合气体中的CO、CO、O 和HO,请排序
2 2 2 2
: ___________ ___________ ___________ ___________。
(a) (b) (c) (d)
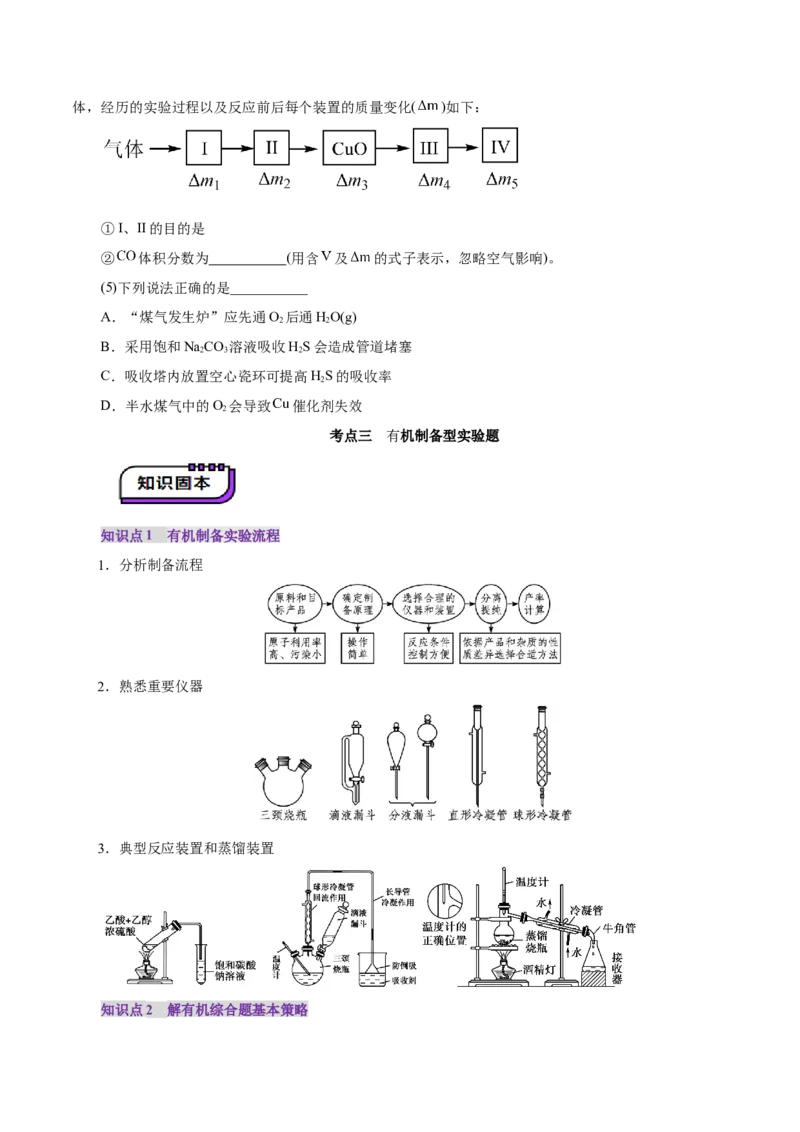
(4)通过测定“催化转化炉”进出口气体中 体积分数以确定 转化率。取标况下 进口或出口气体,经历的实验过程以及反应前后每个装置的质量变化( )如下:
①I、II的目的是
② 体积分数为 (用含 及 的式子表示,忽略空气影响)。
(5)下列说法正确的是___________
A.“煤气发生炉”应先通O 后通HO(g)
2 2
B.采用饱和NaCO 溶液吸收HS会造成管道堵塞
2 3 2
C.吸收塔内放置空心瓷环可提高HS的吸收率
2
D.半水煤气中的O 会导致 催化剂失效
2
考点三 有机制备型实验题
知识点1 有机制备实验流程
1.分析制备流程
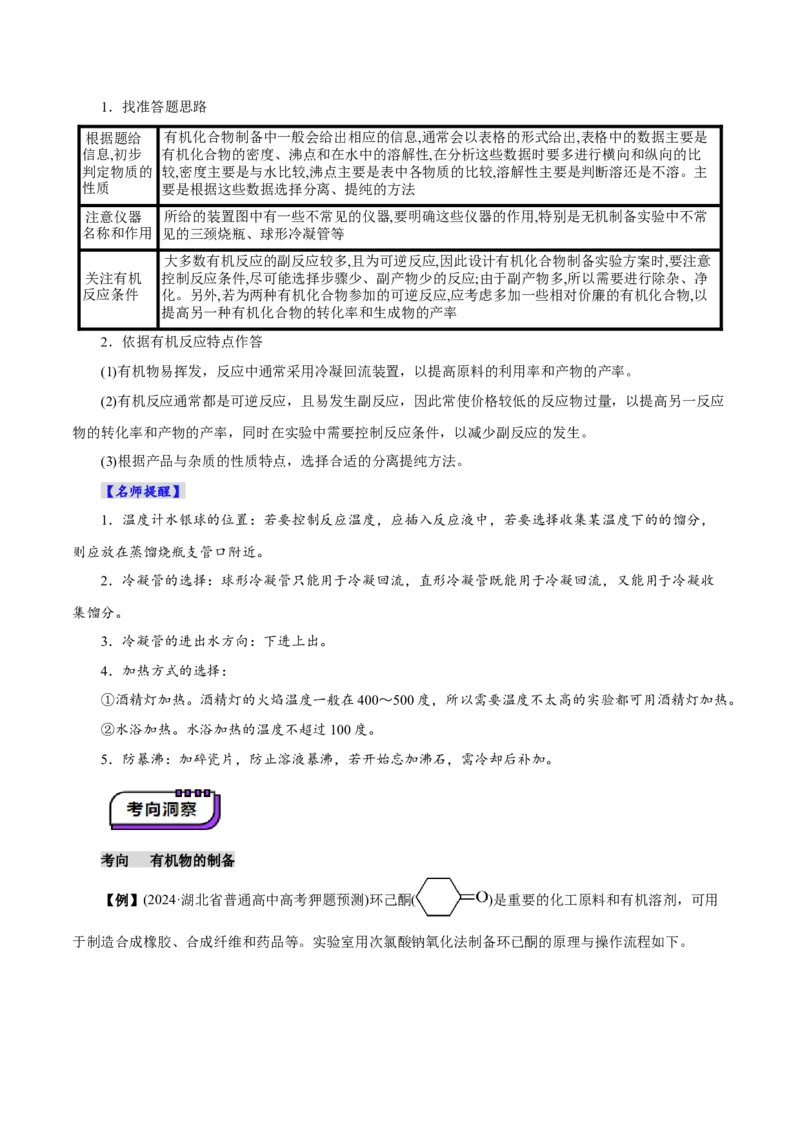
2.熟悉重要仪器
3.典型反应装置和蒸馏装置
知识点2 解有机综合题基本策略1.找准答题思路
根据题给 有机化合物制备中一般会给出相应的信息,通常会以表格的形式给出,表格中的数据主要是
信息,初步 有机化合物的密度、沸点和在水中的溶解性,在分析这些数据时要多进行横向和纵向的比
判定物质的 较,密度主要是与水比较,沸点主要是表中各物质的比较,溶解性主要是判断溶还是不溶。主
性质 要是根据这些数据选择分离、提纯的方法
注意仪器 所给的装置图中有一些不常见的仪器,要明确这些仪器的作用,特别是无机制备实验中不常
名称和作用 见的三颈烧瓶、球形冷凝管等
大多数有机反应的副反应较多,且为可逆反应,因此设计有机化合物制备实验方案时,要注意
关注有机 控制反应条件,尽可能选择步骤少、副产物少的反应;由于副产物多,所以需要进行除杂、净
反应条件 化。另外,若为两种有机化合物参加的可逆反应,应考虑多加一些相对价廉的有机化合物,以
提高另一种有机化合物的转化率和生成物的产率
2.依据有机反应特点作答
(1)有机物易挥发,反应中通常采用冷凝回流装置,以提高原料的利用率和产物的产率。
(2)有机反应通常都是可逆反应,且易发生副反应,因此常使价格较低的反应物过量,以提高另一反应
物的转化率和产物的产率,同时在实验中需要控制反应条件,以减少副反应的发生。
(3)根据产品与杂质的性质特点,选择合适的分离提纯方法。
【名师提醒】
1.温度计水银球的位置:若要控制反应温度,应插入反应液中,若要选择收集某温度下的的馏分,
则应放在蒸馏烧瓶支管口附近。
2.冷凝管的选择:球形冷凝管只能用于冷凝回流,直形冷凝管既能用于冷凝回流,又能用于冷凝收
集馏分。
3.冷凝管的进出水方向:下进上出。
4.加热方式的选择:
①酒精灯加热。酒精灯的火焰温度一般在400~500度,所以需要温度不太高的实验都可用酒精灯加热。
②水浴加热。水浴加热的温度不超过100度。
5.防暴沸:加碎瓷片,防止溶液暴沸,若开始忘加沸石,需冷却后补加。
考向 有机物的制备
【例】(2024·湖北省普通高中高考狎题预测)环己酮( )是重要的化工原料和有机溶剂,可用
于制造合成橡胶、合成纤维和药品等。实验室用次氯酸钠氧化法制备环已酮的原理与操作流程如下。已知:
①环己酮的密度比水的密度小,能与水形成恒沸混合物,沸点为95℃。
②31℃时,环己酮在水中的溶解度为2.4 g。
回答下列问题:
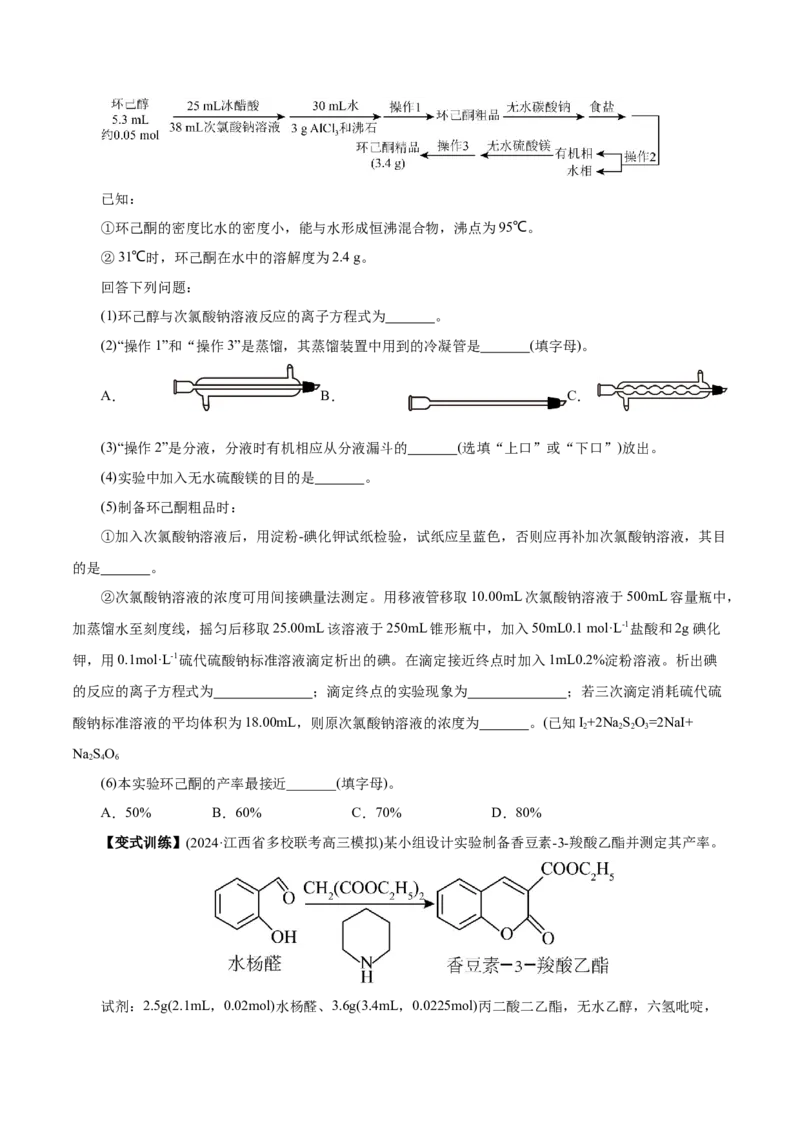
(1)环己醇与次氯酸钠溶液反应的离子方程式为 。
(2)“操作1”和“操作3”是蒸馏,其蒸馏装置中用到的冷凝管是 (填字母)。
A. B. C.
(3)“操作2”是分液,分液时有机相应从分液漏斗的 (选填“上口”或“下口”)放出。
(4)实验中加入无水硫酸镁的目的是 。
(5)制备环己酮粗品时:
①加入次氯酸钠溶液后,用淀粉-碘化钾试纸检验,试纸应呈蓝色,否则应再补加次氯酸钠溶液,其目
的是 。
②次氯酸钠溶液的浓度可用间接碘量法测定。用移液管移取10.00mL次氯酸钠溶液于500mL容量瓶中,
加蒸馏水至刻度线,摇匀后移取25.00mL该溶液于250mL锥形瓶中,加入50mL0.1 mol·L-1盐酸和2g碘化
钾,用0.1mol·L-1硫代硫酸钠标准溶液滴定析出的碘。在滴定接近终点时加入1mL0.2%淀粉溶液。析出碘
的反应的离子方程式为 ;滴定终点的实验现象为 ;若三次滴定消耗硫代硫
酸钠标准溶液的平均体积为18.00mL,则原次氯酸钠溶液的浓度为 。(已知I+2Na SO=2NaI+
2 2 2 3
NaSO
2 4 6
(6)本实验环己酮的产率最接近_______(填字母)。
A.50% B.60% C.70% D.80%
【变式训练】(2024·江西省多校联考高三模拟)某小组设计实验制备香豆素-3-羧酸乙酯并测定其产率。
试剂:2.5g(2.1mL,0.02mol)水杨醛、3.6g(3.4mL,0.0225mol)丙二酸二乙酯,无水乙醇,六氢吡啶,冰醋酸和无水氯化钙。
实验步骤:
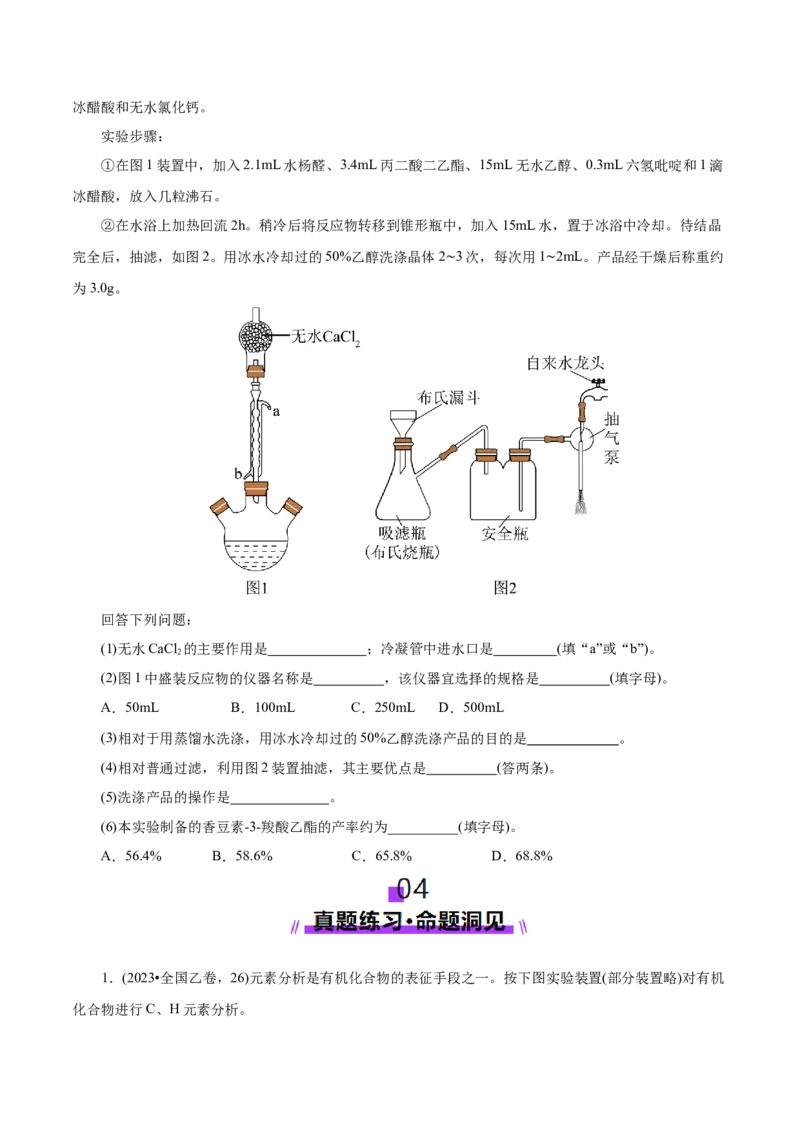
①在图1装置中,加入2.1mL水杨醛、3.4mL丙二酸二乙酯、15mL无水乙醇、0.3mL六氢吡啶和1滴
冰醋酸,放入几粒沸石。
②在水浴上加热回流2h。稍冷后将反应物转移到锥形瓶中,加入15mL水,置于冰浴中冷却。待结晶
完全后,抽滤,如图2。用冰水冷却过的50%乙醇洗涤晶体2 3次,每次用1 2mL。产品经干燥后称重约
为3.0g。 ∼ ∼
回答下列问题:
(1)无水CaCl 的主要作用是 ;冷凝管中进水口是 (填“a”或“b”)。
2
(2)图1中盛装反应物的仪器名称是 ,该仪器宜选择的规格是 (填字母)。
A.50mL B.100mL C.250mL D.500mL
(3)相对于用蒸馏水洗涤,用冰水冷却过的50%乙醇洗涤产品的目的是 。
(4)相对普通过滤,利用图2装置抽滤,其主要优点是 (答两条)。
(5)洗涤产品的操作是 。
(6)本实验制备的香豆素-3-羧酸乙酯的产率约为__________(填字母)。
A.56.4% B.58.6% C.65.8% D.68.8%
1.(2023•全国乙卷,26)元素分析是有机化合物的表征手段之一。按下图实验装置(部分装置略)对有机
化合物进行C、H元素分析。回答下列问题:
(1)将装有样品的Pt坩埚和CuO放入石英管中,先_______,而后将已称重的U型管c、d与石英管连
接,检查_______。依次点燃煤气灯_______,进行实验。
(2)O 的作用有_______。CuO的作用是_______(举1例,用化学方程式表示)。
2
(3)c和d中的试剂分别是_______、_______(填标号)。c和d中的试剂不可调换,理由是_______。
A.CaCl B.NaCl C.碱石灰(CaO+NaOH) D.NaSO
2 2 3
(4)Pt坩埚中样品CxHyOz反应完全后,应进行操作:_______。取下c和d管称重。
(5)若样品CxHyOz为0.0236g,实验结束后,c管增重0.0108g,d管增重0.0352g。质谱测得该有机物
的相对分子量为118,其分子式为_______。
2.(2023•山东卷,18)三氯甲硅烷(SiHCl )是制取高纯硅的重要原料,常温下为无色液体,沸点为
3
31.8℃,熔点为-126.5℃,易水解。实验室根据反应Si+3HCl SiHCl +H ,利用如下装置制备SiHCl 粗品
3 2 3
(加热及夹持装置略)。回答下列问题:
(1)制备SiHCl 时进行操作:(ⅰ)……;(ⅱ)将盛有砫粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间
3
后接通冷凝装置,加热开始反应。操作(ⅰ)为_____;判断制备反应结束的实验现象是_____。图示装置存
在的两处缺陷是_____。
(2)已知电负性Cl>H>Si,SiHCl 在浓 溶液中发生反应的化学方程式为_____。
3(3)采用如下方法测定溶有少量 的SiHCl 纯度。
3
mg样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①_____,②_____(填操作
1
名称),③称量等操作,测得所得固体氧化物质量为mg,从下列仪器中选出①、②中需使用的仪器,依次
2
为_____(填标号)。测得样品纯度为_____(用含m、m 的代数式表示)。
1 2
3.(2023•辽宁省选择性考试,17)2—噻吩乙醇(Mr=128)是抗血栓药物氯吡格雷的重要中间体,其制备
方法如下:
Ⅰ.制钠砂。向烧瓶中加入300mL液体A和4.60g金属钠,加热至钠熔化后,盖紧塞子,振荡至大量
微小钠珠出现。
Ⅱ.制噻吩钠。降温至10℃,加入25mL噻吩,反应至钠砂消失。
Ⅲ.制噻吩乙醇钠。降温至-10℃,加入稍过量的环氧乙烷的四氢呋喃溶液,反应30min。
Ⅳ.水解。恢复室温,加入70mL水,搅拌 ;加盐酸调pH至4~6,继续反应2 h,分液;用水
洗涤有机相,二次分液。
Ⅴ.分离。向有机相中加入无水MgSO ,静置,过滤,对滤液进行蒸馏,蒸出四氢呋喃、噻吩和液体
4
A后,得到产品17.92g。
回答下列问题:
(1)步骤Ⅰ中液体A可以选择_______。
a.乙醇 b.水 c.甲苯 d.液氨
(2)噻吩沸点低于吡咯( )的原因是_______。
(3)步骤Ⅱ的化学方程式为_______。
(4)步骤Ⅲ中反应放热,为防止温度过高引发副反应,加入环氧乙烷溶液的方法是_______。(5)步骤Ⅳ中用盐酸调节pH的目的是_______。
(6)下列仪器在步骤Ⅴ中无需使用的是_______(填名称):无水MgSO 的作用为_______。
4
(7)产品的产率为_______(用 计算,精确至0.1%)。
4.(2023•北京卷,19)资料显示,I 可以将Cu氧化为Cu2+。某小组同学设计实验探究Cu被I 氧化的产
2 2
物及铜元素的价态。
已知:I 易溶于KI溶液,发生反应I+I- I- (红棕色);I 和I-氧化性几乎相同。
2 2 3 2 3
I.将等体积的KI溶液加入到mmol铜粉和nmolI (n>m)的固体混合物中,振荡。
2
实验记录如下:
c(KI) 实验现象
极少量I 溶解,溶液为淡红色;充分反应后,红色的铜粉转
实验Ⅰ 0.01 mol·L-1 2
化为白色沉淀,溶液仍为淡红色
部分I 溶解,溶液为红棕色;充分反应后,红色的铜粉转化
实验Ⅱ 0.1 mol·L-1 2
为白色沉淀,溶液仍为红棕色
I 完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完
实验Ⅲ 4 mol·L-1 2
全溶解,溶液为深红棕色
(1)初始阶段, 被氧化的反应速率:实验Ⅰ (填“>”“<”或“=”)实验Ⅱ。
(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有[Cu(HO) ]2+ (蓝色)或[CuI]- (无色),进行以
2 4 2
下实验探究:
步骤a.取实验Ⅲ的深红棕色溶液,加入CCl,多次萃取、分液。
4
步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
ⅰ.步骤a的目的是 。
ⅱ.查阅资料,2Cu2++4I-=2CuI↓+I ,[Cu(NH )]+ (无色)容易被空气氧化。用离子方程式解释步骤 的溶
2 3 4
液中发生的变化: 。
(3)结合实验Ⅲ,推测实验Ⅰ和Ⅱ中的白色沉淀可能是CuI,实验Ⅰ中铜被氧化的化学方程式是
。分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入浓 溶液, (填实验现象),
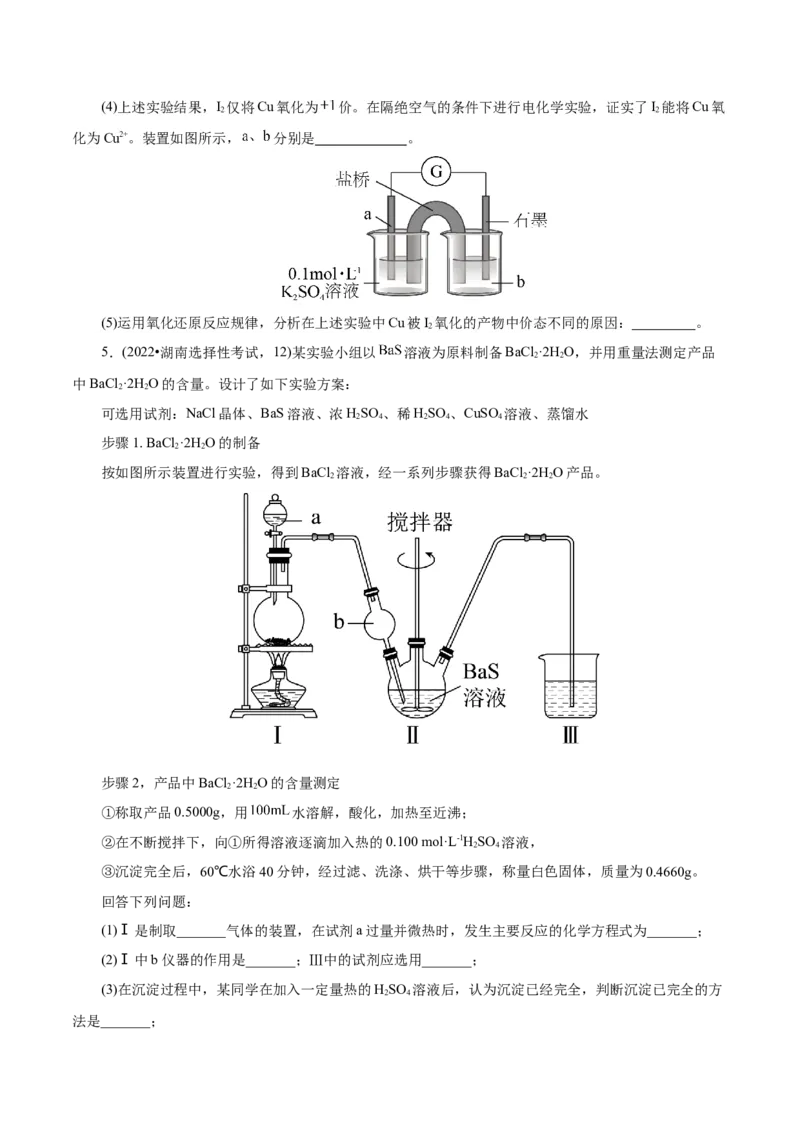
观察到少量红色的铜。分析铜未完全反应的原因是 。(4)上述实验结果,I 仅将Cu氧化为 价。在隔绝空气的条件下进行电化学实验,证实了I 能将Cu氧
2 2
化为Cu2+。装置如图所示, 分别是 。
(5)运用氧化还原反应规律,分析在上述实验中Cu被I 氧化的产物中价态不同的原因: 。
2
5.(2022•湖南选择性考试,12)某实验小组以 溶液为原料制备BaCl ·2H O,并用重量法测定产品
2 2
中BaCl ·2H O的含量。设计了如下实验方案:
2 2
可选用试剂:NaCl晶体、BaS溶液、浓HSO 、稀HSO 、CuSO 溶液、蒸馏水
2 4 2 4 4
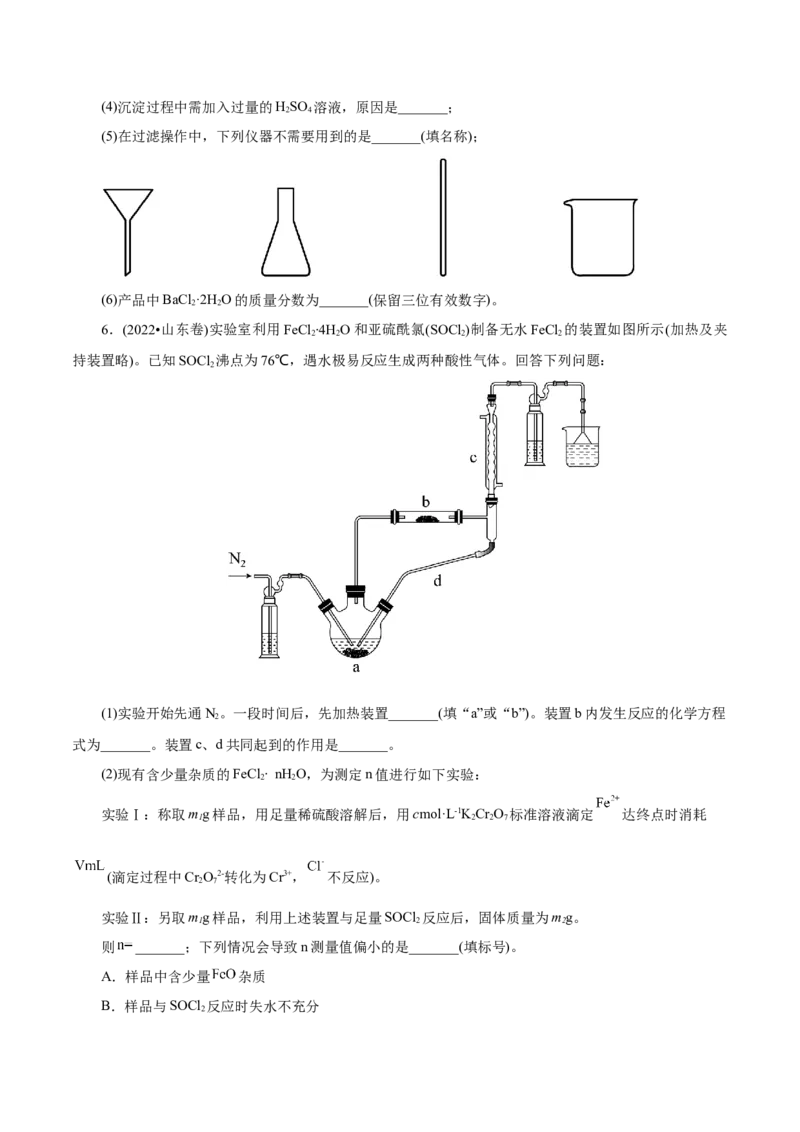
步骤1. BaCl ·2H O的制备
2 2
按如图所示装置进行实验,得到BaCl 溶液,经一系列步骤获得BaCl ·2H O产品。
2 2 2
步骤2,产品中BaCl ·2H O的含量测定
2 2
①称取产品0.5000g,用 水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的0.100 mol·L-1HSO 溶液,
2 4
③沉淀完全后,60℃水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为0.4660g。
回答下列问题:
(1)Ⅰ是制取_______气体的装置,在试剂a过量并微热时,发生主要反应的化学方程式为_______;
(2)Ⅰ中b仪器的作用是_______;Ⅲ中的试剂应选用_______;
(3)在沉淀过程中,某同学在加入一定量热的HSO 溶液后,认为沉淀已经完全,判断沉淀已完全的方
2 4
法是_______;(4)沉淀过程中需加入过量的HSO 溶液,原因是_______;
2 4
(5)在过滤操作中,下列仪器不需要用到的是_______(填名称);
(6)产品中BaCl ·2H O的质量分数为_______(保留三位有效数字)。
2 2
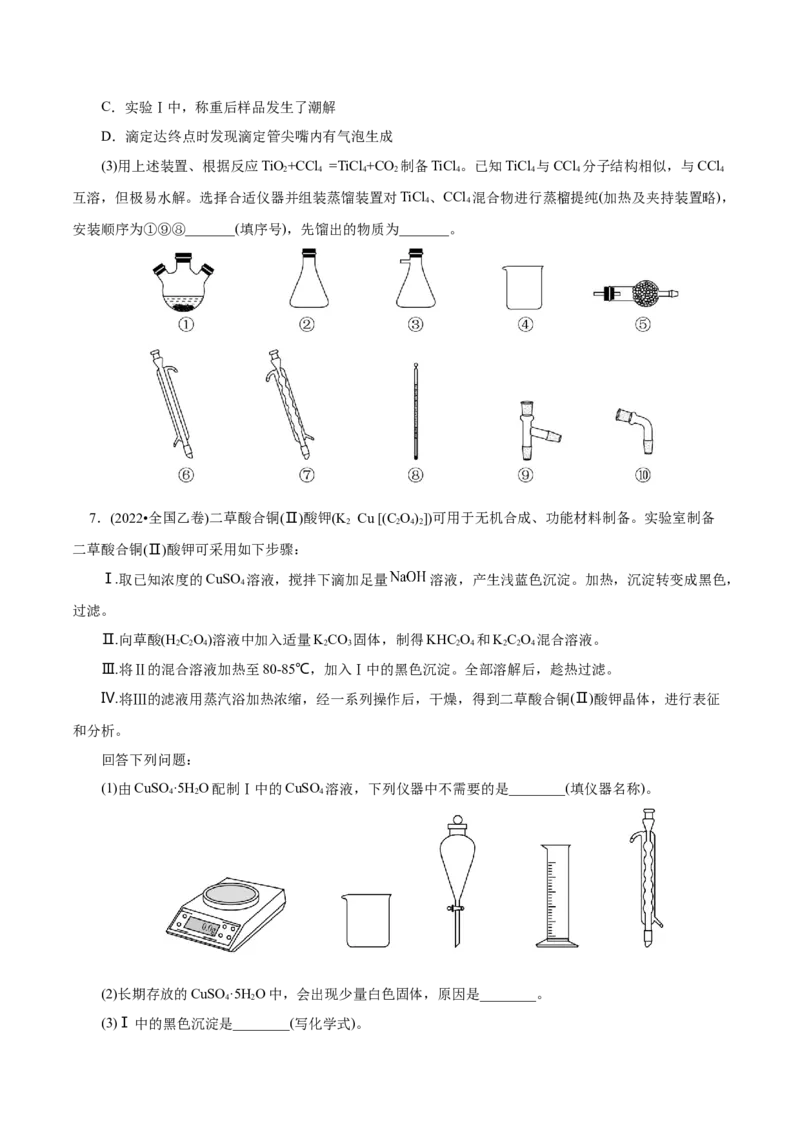
6.(2022•山东卷)实验室利用FeCl ∙4HO和亚硫酰氯(SOCl )制备无水FeCl 的装置如图所示(加热及夹
2 2 2 2
持装置略)。已知SOCl 沸点为76℃,遇水极易反应生成两种酸性气体。回答下列问题:
2
(1)实验开始先通N。一段时间后,先加热装置_______(填“a”或“b”)。装置b内发生反应的化学方程
2
式为_______。装置c、d共同起到的作用是_______。
(2)现有含少量杂质的FeCl ∙ nHO,为测定n值进行如下实验:
2 2
实验Ⅰ:称取mg样品,用足量稀硫酸溶解后,用cmol·L-1KCr O 标准溶液滴定 达终点时消耗
1 2 2 7
(滴定过程中Cr O2-转化为Cr3+, 不反应)。
2 7
实验Ⅱ:另取mg样品,利用上述装置与足量SOCl 反应后,固体质量为mg。
1 2 2
则 _______;下列情况会导致n测量值偏小的是_______(填标号)。
A.样品中含少量 杂质
B.样品与SOCl 反应时失水不充分
2C.实验Ⅰ中,称重后样品发生了潮解
D.滴定达终点时发现滴定管尖嘴内有气泡生成
(3)用上述装置、根据反应TiO+CCl =TiCl +CO 制备TiCl 。已知TiCl 与CCl 分子结构相似,与CCl
2 4 4 2 4 4 4 4
互溶,但极易水解。选择合适仪器并组装蒸馏装置对TiCl 、CCl 混合物进行蒸榴提纯(加热及夹持装置略),
4 4
安装顺序为①⑨⑧_______(填序号),先馏出的物质为_______。
7.(2022•全国乙卷)二草酸合铜(Ⅱ)酸钾(K Cu [(C O)])可用于无机合成、功能材料制备。实验室制备
2 2 4 2
二草酸合铜(Ⅱ)酸钾可采用如下步骤:
Ⅰ.取已知浓度的CuSO 溶液,搅拌下滴加足量 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,
4
过滤。
Ⅱ.向草酸(H C O)溶液中加入适量KCO 固体,制得KHC O 和KC O 混合溶液。
2 2 4 2 3 2 4 2 2 4
Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征
和分析。
回答下列问题:
(1)由CuSO ·5H O配制Ⅰ中的CuSO 溶液,下列仪器中不需要的是________(填仪器名称)。
4 2 4
(2)长期存放的CuSO ·5H O中,会出现少量白色固体,原因是________。
4 2
(3)Ⅰ中的黑色沉淀是________(写化学式)。(4)Ⅱ中原料配比为n(H C O):n(K CO)=1.5:1,写出反应的化学方程式________。
2 2 4 2 3
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入KCO 应采取________的方法。
2 3
(6)Ⅲ中应采用________进行加热。
(7)Ⅳ中“一系列操作”包括________。
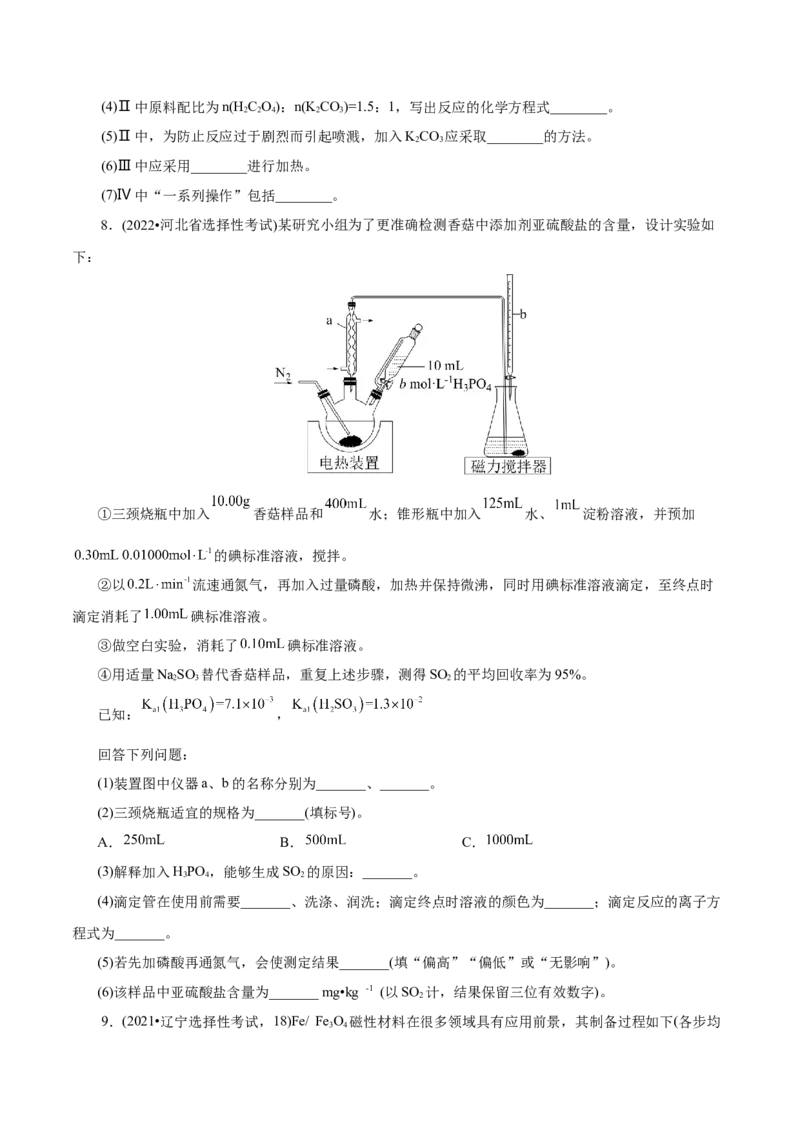
8.(2022•河北省选择性考试)某研究小组为了更准确检测香菇中添加剂亚硫酸盐的含量,设计实验如
下:
①三颈烧瓶中加入 香菇样品和 水;锥形瓶中加入 水、 淀粉溶液,并预加
的碘标准溶液,搅拌。
②以 流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时
滴定消耗了 碘标准溶液。
③做空白实验,消耗了 碘标准溶液。
④用适量NaSO 替代香菇样品,重复上述步骤,测得SO 的平均回收率为95%。
2 3 2
已知: ,
回答下列问题:
(1)装置图中仪器a、b的名称分别为_______、_______。
(2)三颈烧瓶适宜的规格为_______(填标号)。
A. B. C.
(3)解释加入HPO ,能够生成SO 的原因:_______。
3 4 2
(4)滴定管在使用前需要_______、洗涤、润洗;滴定终点时溶液的颜色为_______;滴定反应的离子方
程式为_______。
(5)若先加磷酸再通氮气,会使测定结果_______(填“偏高”“偏低”或“无影响”)。
(6)该样品中亚硫酸盐含量为_______ mg•kg -1 (以SO 计,结果保留三位有效数字)。
2
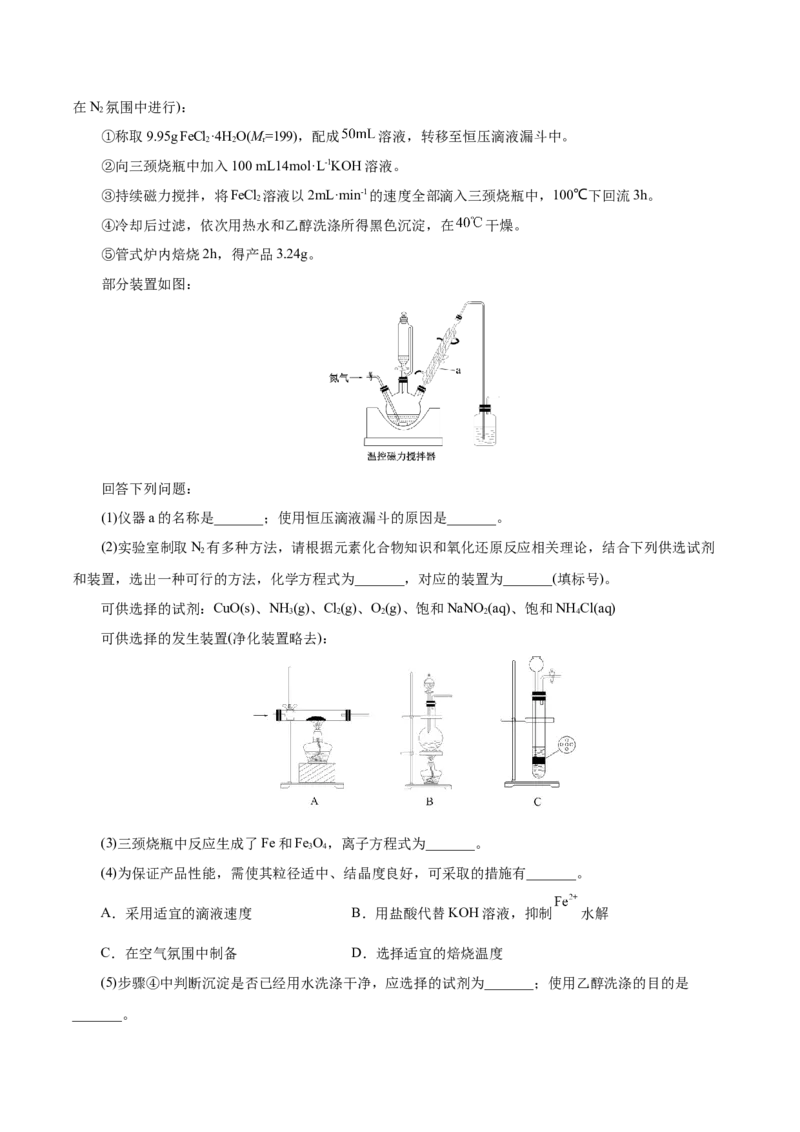
9.(2021•辽宁选择性考试,18)Fe/ Fe O 磁性材料在很多领域具有应用前景,其制备过程如下(各步均
3 4在N 氛围中进行):
2
①称取9.95g FeCl·4H O(M=199),配成 溶液,转移至恒压滴液漏斗中。
2 2 r
②向三颈烧瓶中加入100 mL14mol·L-1KOH溶液。
③持续磁力搅拌,将FeCl 溶液以2mL·min-1的速度全部滴入三颈烧瓶中,100℃下回流3h。
2
④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在 干燥。
⑤管式炉内焙烧2h,得产品3.24g。
部分装置如图:
回答下列问题:
(1)仪器a的名称是_______;使用恒压滴液漏斗的原因是_______。
(2)实验室制取N 有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂
2
和装置,选出一种可行的方法,化学方程式为_______,对应的装置为_______(填标号)。
可供选择的试剂:CuO(s)、NH (g)、Cl(g)、O(g)、饱和NaNO (aq)、饱和NH Cl(aq)
3 2 2 2 4
可供选择的发生装置(净化装置略去):
(3)三颈烧瓶中反应生成了Fe和Fe O,离子方程式为_______。
3 4
(4)为保证产品性能,需使其粒径适中、结晶度良好,可采取的措施有_______。
A.采用适宜的滴液速度 B.用盐酸代替KOH溶液,抑制 水解
C.在空气氛围中制备 D.选择适宜的焙烧温度
(5)步骤④中判断沉淀是否已经用水洗涤干净,应选择的试剂为_______;使用乙醇洗涤的目的是
_______。(6)该实验所得磁性材料的产率为_______(保留3位有效数字)。
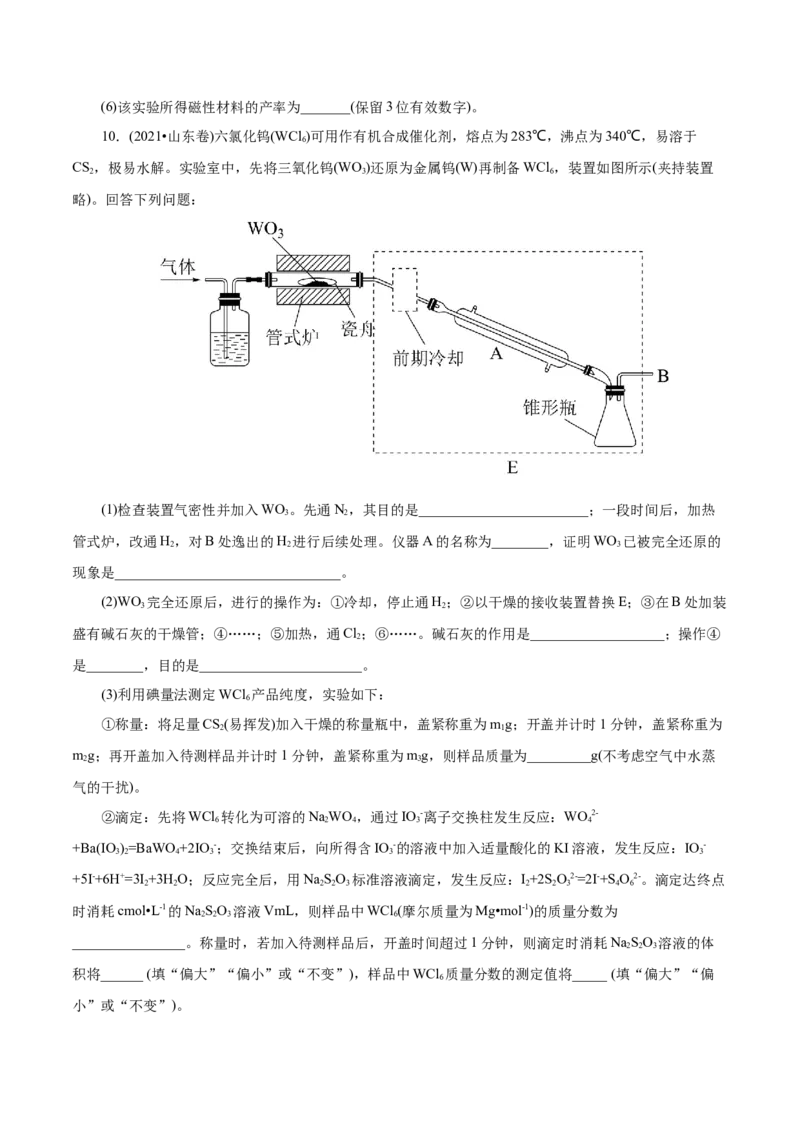
10.(2021•山东卷)六氯化钨(WCl )可用作有机合成催化剂,熔点为283℃,沸点为340℃,易溶于
6
CS,极易水解。实验室中,先将三氧化钨(WO)还原为金属钨(W)再制备WCl,装置如图所示(夹持装置
2 3 6
略)。回答下列问题:
(1)检查装置气密性并加入WO。先通N,其目的是________________________;一段时间后,加热
3 2
管式炉,改通H,对B处逸出的H 进行后续处理。仪器A的名称为________,证明WO 已被完全还原的
2 2 3
现象是________________________________。
(2)WO 完全还原后,进行的操作为:①冷却,停止通H;②以干燥的接收装置替换E;③在B处加装
3 2
盛有碱石灰的干燥管;④……;⑤加热,通Cl;⑥……。碱石灰的作用是___________________;操作④
2
是________,目的是_______________________。
(3)利用碘量法测定WCl 产品纯度,实验如下:
6
①称量:将足量CS(易挥发)加入干燥的称量瓶中,盖紧称重为mg;开盖并计时1分钟,盖紧称重为
2 1
mg;再开盖加入待测样品并计时1分钟,盖紧称重为mg,则样品质量为_________g(不考虑空气中水蒸
2 3
气的干扰)。
②滴定:先将WCl 转化为可溶的NaWO,通过IO -离子交换柱发生反应:WO2-
6 2 4 3 4
+Ba(IO )=BaWO +2IO -;交换结束后,向所得含IO -的溶液中加入适量酸化的KI溶液,发生反应:IO -
3 2 4 3 3 3
+5I-+6H+=3I +3H O;反应完全后,用NaSO 标准溶液滴定,发生反应:I+2S O2-=2I-+S O2-。滴定达终点
2 2 2 2 3 2 2 3 4 6
时消耗cmol•L-1的NaSO 溶液VmL,则样品中WCl(摩尔质量为Mg•mol-1)的质量分数为
2 2 3 6
________________。称量时,若加入待测样品后,开盖时间超过1分钟,则滴定时消耗NaSO 溶液的体
2 2 3
积将______ (填“偏大”“偏小”或“不变”),样品中WCl 质量分数的测定值将_____ (填“偏大”“偏
6
小”或“不变”)。