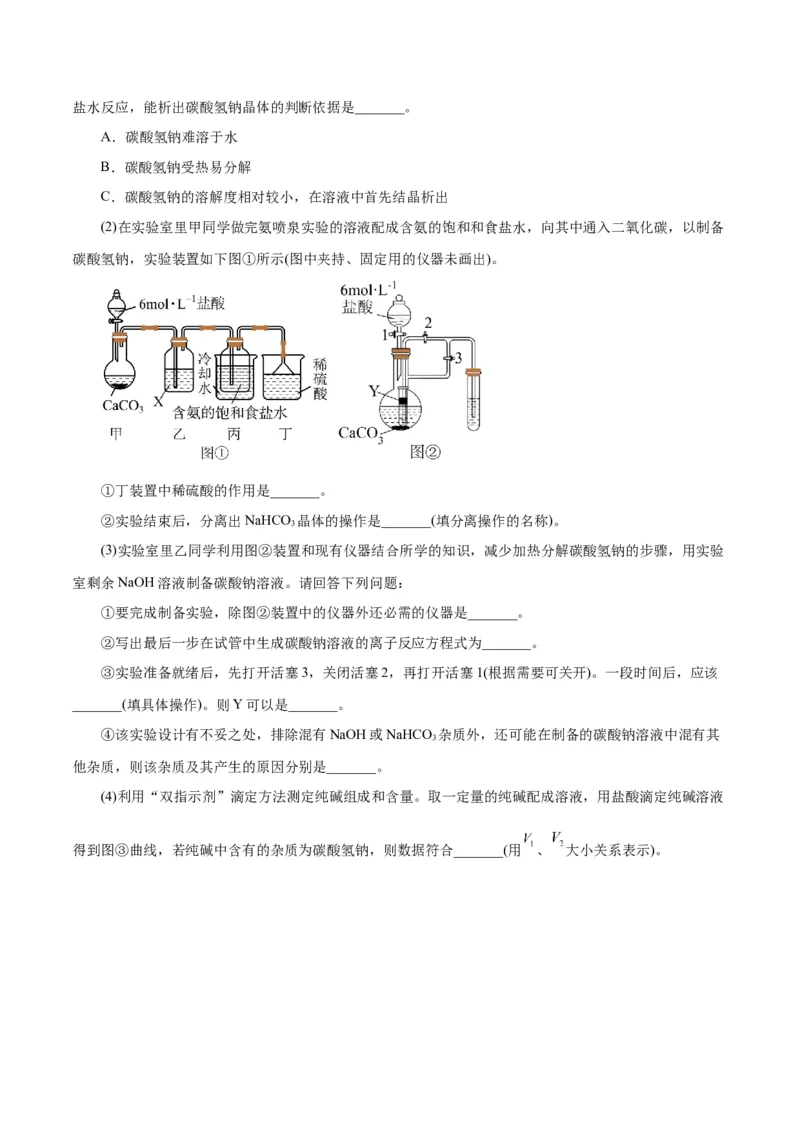
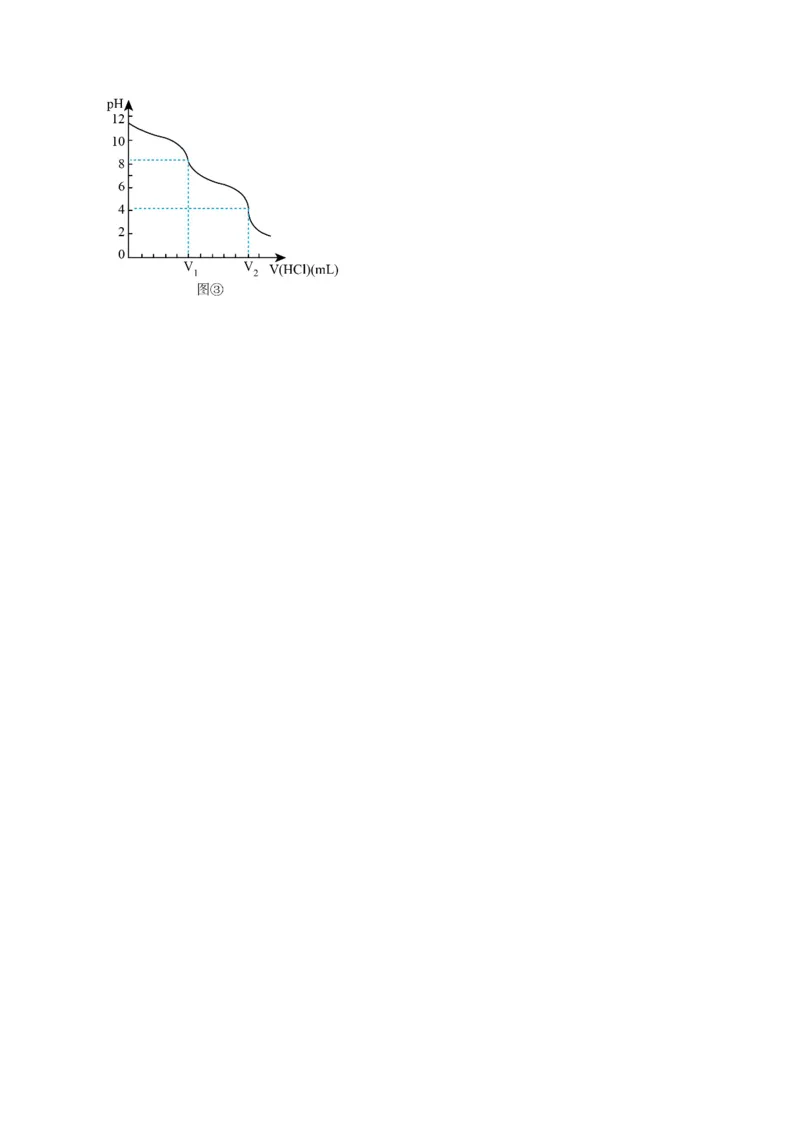
文档内容
第 06 讲 钠及其化合物
【化学学科素养】
1.宏观辨识与微观探析:认识钠及其化合物的性质和应用。能从钠的原子结构及其重要化合物的微观
结构理解其性质,领悟结构决定性质。
2.科学探究与创新意识:了解钠及其化合物的性质探究方案,并积极参与实验探究过程,得出相关结
论。
【必备知识解读】
一、钠的性质及应用
1.钠的物理性质
金属的通性 个性
颜色 导电性、导热性 熔点 硬度 密度
银白色 良好 低 小 比水的小,比煤油的大
2.从钠原子的原子结构认识钠的化学性质——还原性
Na ―――――――――→Na+
(1)与非金属单质(如O、Cl)的反应
2 2
O
2
Cl:2Na+Cl=====2NaCl
2 2
(2)与水反应
①离子方程式:2Na+2HO===2Na++2OH-+H↑。
2 2
②钠与水(含酚酞)反应的实验现象及解释
如果在容器中加一些水,滴入几滴酚酞溶液,然后把一小块钠放入水中,有什么现象?
实验现象:
a.“浮”:将钠投入水中,钠浮在水面上。说明钠的密度比水小。
b.“熔”:钠熔化成小球。说明钠的熔点低。且该反应是放热反应。
c.“游”:小球在水面上四处游动,并伴有嘶嘶声。说明有气体生成。
d.“响”:反应剧烈
e.“红”:反应后的溶液能使酚酞变红。说明反应生成了碱。
离子方程式为:2Na+2HO=2Na++2OH-+H↑。其中,Na做还原剂,HO做氧化剂。
2 2 2
【特别提醒】金属钠与水的反应,其实质是钠与水电离出的H+反应。做实验时,金属钠不慎失火的处
理:用干燥的沙土来灭火,不能用水灭火。钠与水剧烈反应且生成氢气,会放出大量的热,甚至能引起氢气燃烧爆炸。
(3)与盐酸反应
离子方程式:2Na+2H+===2Na++H↑。
2
(4)与羟基化合物的反应
2Na+2C HOH―→2C HONa+H↑
2 5 2 5 2
(5)钠在空气中的变化过程
过程 现象 反应原理
① 变暗 4Na+O===2Na O
2 2
② 成液 NaO+HO===2NaOH
2 2
③ 结块 2NaOH+CO+9HO===Na CO·10H O
2 2 2 3 2
④ 变成粉末 NaCO·10H O===Na CO+10HO
2 3 2 2 3 2
因此,钠久置在空气中,最终变成NaCO 粉末。
2 3
3.钠的制取及保存
(1)制取:化学方程式为2NaCl(熔融)=====2Na+Cl↑。
2
(2)保存:密封保存,通常保存在石蜡油或煤油中。
4.钠的用途
(1)钠钾合金(液态)可用于原子反应堆的导热剂。
(2)用作电光源,制作高压钠灯。
(3)冶炼某些金属
金属钠具有强还原性,熔融状态下可以用于制取金属,如4Na+TiCl =====4NaCl+Ti。
4
二、钠的氧化物与氢氧化物
1.氧化钠与过氧化钠的比较
物质 氧化钠(Na O) 过氧化钠(Na O)
2 2 2
色态 白色固体 淡黄色固体
类别 碱性氧化物 过氧化物
氧的价态 -2 -1
电子式
生成条件 常温 加热或点燃
不稳定(2Na O+
热稳定性 2 稳定
O 2NaO)
2===== 2 2
化学 与水反应 NaO+HO===2NaOH 2NaO+2HO===4NaOH+O↑
2 2 2 2 2 2
性质
与CO 反应 NaO+CO===Na CO 2NaO+2CO===2Na CO+O
2 2 2 2 3 2 2 2 2 3 2
与酸反应(盐酸) NaO+2HCl===2NaCl+ 2NaO+4HCl===4NaCl+2HO
2 2 2 2HO +O↑
2 2
强氧化剂、漂白剂、供氧剂、消
主要性质与用途 具有碱性氧化物通性
毒剂,具有强氧化性
2.氢氧化钠
(1)物理性质:NaOH的俗名为烧碱、火碱或苛性钠;它是一种白色固体,易溶于水并放出大量的热,
有吸水性;吸收空气中的水分而潮解;有很强的腐蚀性。
(2)化学性质
①具有碱的通性
②其他反应
与金属铝反应:2Al+2OH-+6HO===2Na[Al(OH) ]+3H↑
2 4 2
与非金属单质反应:Cl+2OH-===Cl-+ClO-+HO
2 2
(3)NaOH的制取
①土法制碱:NaCO+Ca(OH) ===CaCO ↓+2NaOH
2 3 2 3
②现代工业制碱:2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
三、碳酸钠与碳酸氢钠
1.NaCO 和NaHCO 的比较
2 3 3
名称 碳酸钠(Na CO) 碳酸氢钠(NaHCO )
2 3 3
俗名 纯碱或苏打 小苏打
易溶于水,溶液呈碱 易溶于水(但比NaCO 溶解度小),
水溶性 2 3
性 溶液呈碱性
稳定,但结晶碳酸钠 受热易分解,其分解反应的方程式
稳定性
(Na CO·10H O)易风化 为2NaHCO NaCO+CO↑+HO
2 3 2 3===== 2 3 2 2
CO+2H+===HO+
2 HCO+H+===HO+CO↑
与H+反应 CO 2 ↑ 2 2
主
产生CO 气体的速率NaCO