文档内容
第 07 讲 铁及其化合物
1.我国清代《本草纲目拾遗》中叙述了“铁线粉”:“粤中洋行有舶上铁丝,……日久起销,用刀刮其
销,……,所刮下之销末,名铁线粉”。这里的“铁线粉”是指( )
A.Fe B.FeCl
3
C.FeO D.FeO
2 3
2.下列有关铁及其化合物的说法中不正确的是( )
A.工业上在高温下用CO还原含FeO 的铁矿石炼铁
2 3
B.铁在纯氧中燃烧或高温下和水蒸气反应均能得到FeO
3 4
C.工业上可用铁制容器储存、运输浓硝酸和浓硫酸
D.氯化铁溶液有较强氧化性,故可用作净水剂
3.下列铁及其化合物性质与用途具有对应关系的是
A.Fe粉具有还原性,可用作抗氧化剂 B.Fe O 粉末呈红棕色,可用于制取铁盐
2 3
C.Fe (SO ) 易溶于水,可用作净水剂 D.FeCl 溶液呈酸性,用于蚀刻铜电路板
2 4 3 3
4.要证明某溶液中不含Fe3+,而可能含有Fe2+,进行如下实验操作的最佳顺序为( )
①加入足量氯水 ②加入足量KMnO(H+)溶液 ③加入少量KSCN溶液
4
A.①③ B.③②
C.③① D.①②③
5.坦克、导弹的制造材料主要是金属合金,钢铁便是其中十分重要的一种。下列关于铁的说法中正确的是
( )
A.铁元素属于过渡元素,其原子序数为26
B.单质铁与浓硫酸在常温下不反应
C.铁单质只具有还原性,其阳离子只具有氧化性
D.与相同浓度的盐酸反应生成氢气的速率,纯铁比生铁的快
6.下列各组物质中,X是主体物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其中所加试剂正确
的一组是( )
A B C D
X FeCl 溶液 FeCl 溶液 Fe FeSO 溶液
2 3 4
Y FeCl CuCl Al Fe(SO)
3 2 2 4 3
Z Cl Fe NaOH溶液 Cu
2
7.有一块铁的“氧化物”样品,用140 mL 5.0 mol·L-1盐酸恰好将之完全溶解,所得溶液还能吸收0.025mol Cl,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
2
A.FeO B.FeO
2 3 3 4
C.FeO D.FeO
4 5 5 7
8.A、B、C三种物质中均含有同一种元素M,它们之间有如图所示的转化关系。A为一种金属单质,其产
量直接关系国民经济命脉。反应①②③均为化合反应,反应④为置换反应。下列有关说法不正确的是( )
A.①中所加试剂可能是氯气
B.③中需要加具有氧化性的试剂
C.A与稀硝酸反应一定能实现元素M在①中发生的价态变化
D.元素M在②中发生的价态变化也能通过加碘化钾溶液实现
9.下列指定反应的离子方程式正确的是
A.NaO 与H18O反应:2NaO+2H 18O=4Na++4OH- +18O↑
2 2 2 2 2 2 2
B.向次氯酸钠溶液中通入少量的CO:ClO—+CO +H O=HClO+HCO
2 2 2
C.FeCl 溶液中加过量NaS溶液:S2- + 2Fe3+ =S↓+2Fe2+
3 2
D.向Fe(OH) 胶体中加入HI溶液:Fe(OH) +3H+ =Fe3+ +3H O
3 3 2
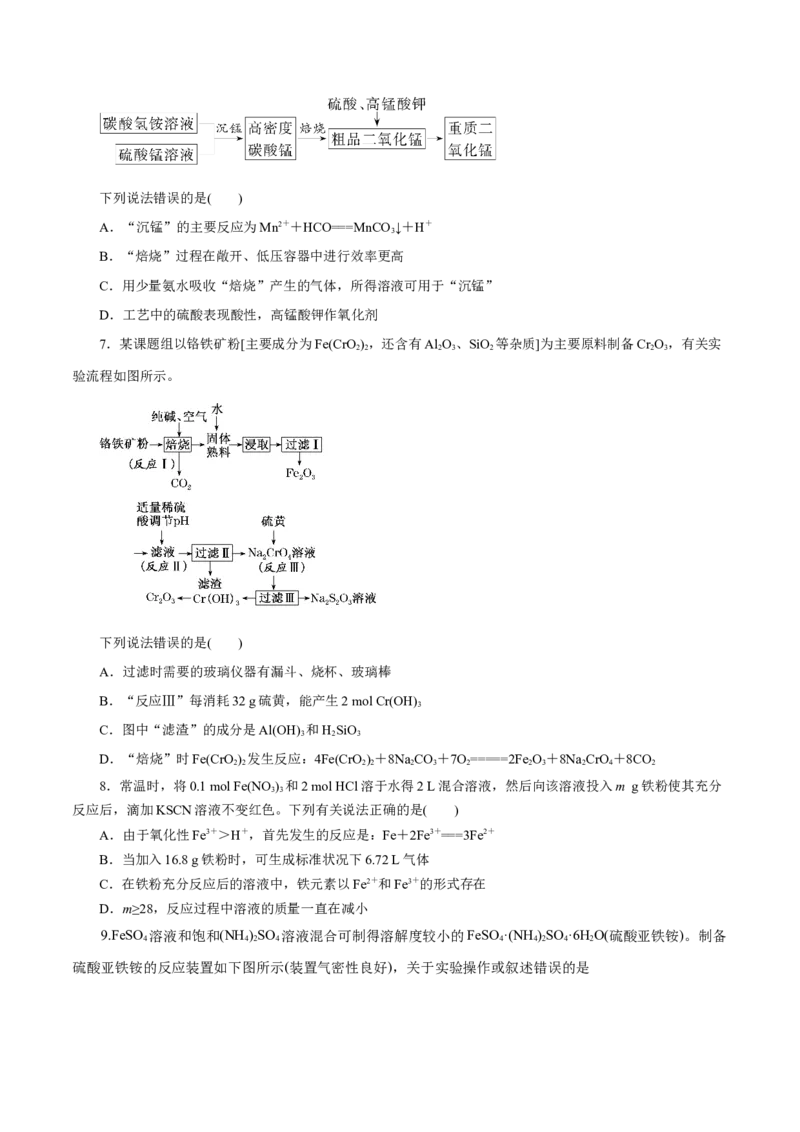
10.如图所示,此装置可用来制取和观察Fe(OH) 在空气中被氧化的颜色变化。实验时必须使用铁屑和6
2
mol·L-1的硫酸,其他试剂任选。
填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的药品是________。A中反应的离子方程式是
____________________________________________________________。
(2)实验开始时先将止水夹a________(填“打开”或“关闭”)。
(3)简述生成Fe(OH) 的操作过程_______________________________________。
2
(4)实验完毕,打开b处止水夹,放入一部分空气,此时B瓶中发生的反应为
________________________________。1.将1.12 g铁粉加入25 mL 2 mol·L-1的氯化铁溶液中,充分反应后,其结果是( )
A.铁粉有剩余,溶液呈浅绿色,Cl-基本保持不变
B.往溶液中滴入无色KSCN溶液,显红色
C.Fe2+和Fe3+的物质的量之比为5∶1
D.氧化产物和还原产物的物质的量之比为2∶5
2.下列除杂的操作不正确的是( )
A.MgCl 溶液中混有少量FeCl:加入足量MgO充分反应后过滤
2 3
B.FeCl 溶液中混有少量FeCl:加入过量铁粉充分反应后过滤
2 3
C.CuCl 溶液中混有少量FeCl:加入NaOH溶液充分反应后过滤
2 3
D.CuCl 溶液中混有少量FeCl:先加入HO 将Fe2+氧化成Fe3+,再加入CuO充分反应后过滤
2 2 2 2
3.下列离子方程式正确的是
A.金属铜与稀硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4HO
2
B.氯化铁和铜反应:Fe3++Cu=Fe2++Cu2+
C.硫酸亚铁溶液与稀硫酸、双氧水混合:2Fe2++2HO+4H+=2Fe3++4HO
2 2 2
D.过量SO 通入NaClO溶液中:SO +HO+ClO-=HClO+HSO
2 2 2
4.Fe2+、Fe3+、Zn2+较完全地形成氢氧化物沉淀的pH分别为6.7、3.7、4.6。某硫酸锌酸性溶液中含有少
量Fe2+、Fe3+杂质离子,为除去这些离子制得纯净的ZnSO,应加入的试剂是( )
4
A.NaOH溶液 B.氨水
C.KMnO、ZnCO D.HO、ZnO
4 3 2 2
5.由硫铁矿烧渣(主要成分:Fe O、Fe O 和FeO)得到绿矾(FeSO ·7H O),再通过绿矾制备铁黄
3 4 2 3 4 2
[FeO(OH)]的流程如下:
烧渣 溶液 绿矾 铁黄
已知:FeS 和铁黄均难溶于水,下列说法不正确的是
2
A.步骤①,最好用硫酸来溶解烧渣
B.步骤②,涉及的离子反应为FeS+14Fe3++8HO=15Fe2++2SO 2-+16H+
2 2 4
C.步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D.步骤④,反应条件控制不当会使铁黄中混有Fe(OH)
3
6.重质二氧化锰具有优良的电化学性能,广泛应用于各类化学电源中。以硫酸锰为原料制备重质二氧化锰
的工艺流程如下:下列说法错误的是( )
A.“沉锰”的主要反应为Mn2++HCO===MnCO↓+H+
3
B.“焙烧”过程在敞开、低压容器中进行效率更高
C.用少量氨水吸收“焙烧”产生的气体,所得溶液可用于“沉锰”
D.工艺中的硫酸表现酸性,高锰酸钾作氧化剂
7.某课题组以铬铁矿粉[主要成分为Fe(CrO),还含有AlO、SiO 等杂质]为主要原料制备CrO,有关实
2 2 2 3 2 2 3
验流程如图所示。
下列说法错误的是( )
A.过滤时需要的玻璃仪器有漏斗、烧杯、玻璃棒
B.“反应Ⅲ”每消耗32 g硫黄,能产生2 mol Cr(OH)
3
C.图中“滤渣”的成分是Al(OH) 和HSiO
3 2 3
D.“焙烧”时Fe(CrO) 发生反应:4Fe(CrO)+8NaCO+7O=====2FeO+8NaCrO+8CO
2 2 2 2 2 3 2 2 3 2 4 2
8.常温时,将0.1 mol Fe(NO) 和2 mol HCl溶于水得2 L混合溶液,然后向该溶液投入m g铁粉使其充分
3 3
反应后,滴加KSCN溶液不变红色。下列有关说法正确的是( )
A.由于氧化性Fe3+>H+,首先发生的反应是:Fe+2Fe3+===3Fe2+
B.当加入16.8 g铁粉时,可生成标准状况下6.72 L气体
C.在铁粉充分反应后的溶液中,铁元素以Fe2+和Fe3+的形式存在
D.m≥28,反应过程中溶液的质量一直在减小
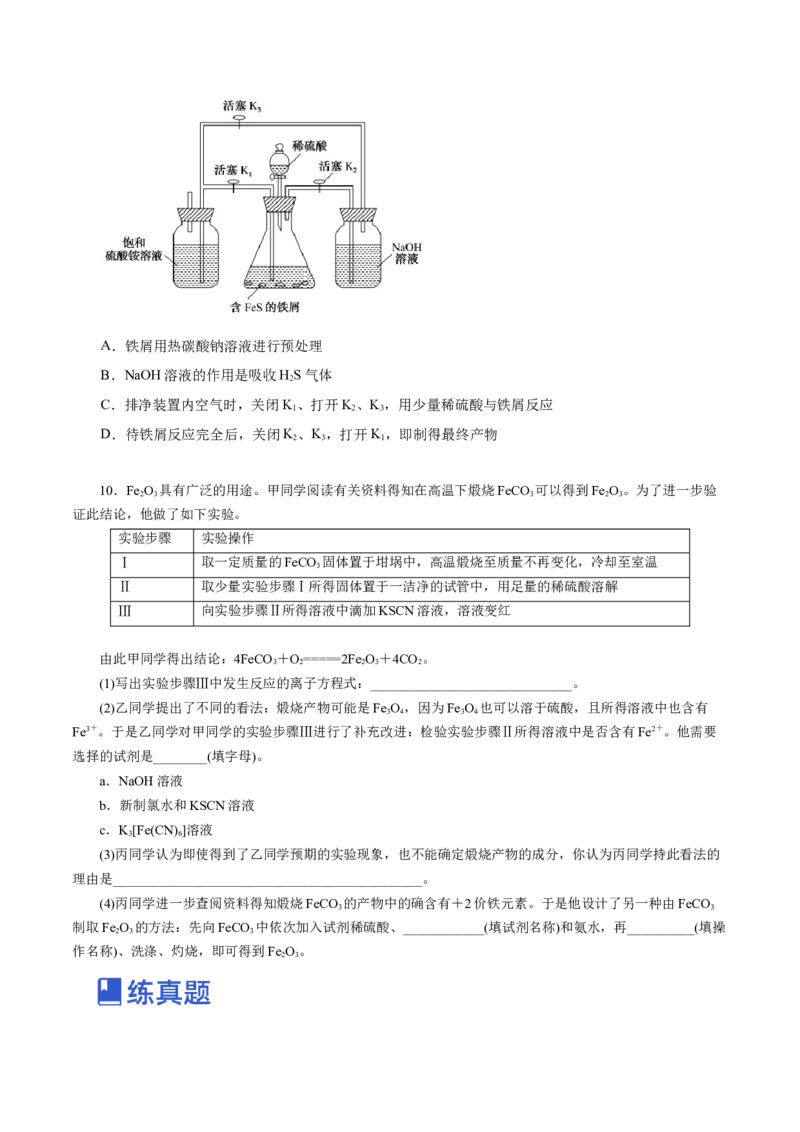
9.FeSO 溶液和饱和(NH )SO 溶液混合可制得溶解度较小的FeSO ·(NH )SO ·6H O(硫酸亚铁铵)。制备
4 4 2 4 4 4 2 4 2
硫酸亚铁铵的反应装置如下图所示(装置气密性良好),关于实验操作或叙述错误的是A.铁屑用热碳酸钠溶液进行预处理
B.NaOH溶液的作用是吸收HS气体
2
C.排净装置内空气时,关闭K、打开K、K,用少量稀硫酸与铁屑反应
1 2 3
D.待铁屑反应完全后,关闭K、K,打开K,即制得最终产物
2 3 1
10.FeO 具有广泛的用途。甲同学阅读有关资料得知在高温下煅烧FeCO 可以得到FeO。为了进一步验
2 3 3 2 3
证此结论,他做了如下实验。
实验步骤 实验操作
Ⅰ 取一定质量的FeCO 固体置于坩埚中,高温煅烧至质量不再变化,冷却至室温
3
Ⅱ 取少量实验步骤Ⅰ所得固体置于一洁净的试管中,用足量的稀硫酸溶解
Ⅲ 向实验步骤Ⅱ所得溶液中滴加KSCN溶液,溶液变红
由此甲同学得出结论:4FeCO+O=====2FeO+4CO。
3 2 2 3 2
(1)写出实验步骤Ⅲ中发生反应的离子方程式:______________________________。
(2)乙同学提出了不同的看法:煅烧产物可能是FeO,因为FeO 也可以溶于硫酸,且所得溶液中也含有
3 4 3 4
Fe3+。于是乙同学对甲同学的实验步骤Ⅲ进行了补充改进:检验实验步骤Ⅱ所得溶液中是否含有Fe2+。他需要
选择的试剂是________(填字母)。
a.NaOH溶液
b.新制氯水和KSCN溶液
c.K[Fe(CN)]溶液
3 6
(3)丙同学认为即使得到了乙同学预期的实验现象,也不能确定煅烧产物的成分,你认为丙同学持此看法的
理由是______________________________________________。
(4)丙同学进一步查阅资料得知煅烧FeCO 的产物中的确含有+2价铁元素。于是他设计了另一种由FeCO
3 3
制取FeO 的方法:先向FeCO 中依次加入试剂稀硫酸、____________(填试剂名称)和氨水,再__________(填操
2 3 3
作名称)、洗涤、灼烧,即可得到FeO。
2 31.(2021·广东卷)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a可与e反应生成b
B.b既可被氧化,也可被还原
C.可将e加入浓碱液中制得d的胶体
D.可存在b→c→d→e→b的循环转化关系
2.下列有关物质性质的叙述错误的是( )
A.(2021·湖南高考)FeO粉末在空气中受热,迅速被氧化成FeO
3 4
B.(2019·天津高考)将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl
2 2
C.(2020·江苏高考)室温下,Fe与浓HSO 不能生成FeSO
2 4 4
D.(2021·浙江高考)铁粉与氧化铝发生的铝热反应可用于焊接铁轨
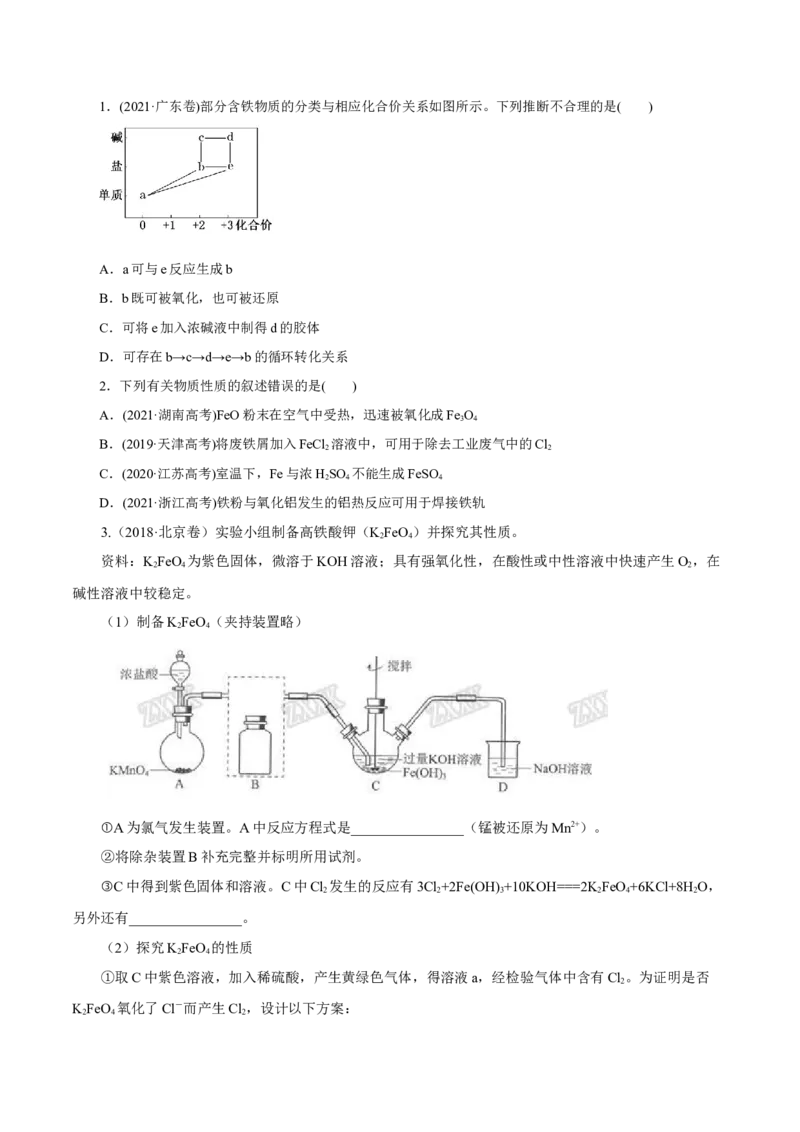
3.(2018·北京卷)实验小组制备高铁酸钾(KFeO)并探究其性质。
2 4
资料:KFeO 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O,在
2 4 2
碱性溶液中较稳定。
(1)制备KFeO(夹持装置略)
2 4
①A为氯气发生装置。A中反应方程式是________________(锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂。
③C中得到紫色固体和溶液。C中Cl 发生的反应有3Cl+2Fe(OH) +10KOH===2KFeO+6KCl+8H O,
2 2 3 2 4 2
另外还有________________。
(2)探究KFeO 的性质
2 4
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl。为证明是否
2
KFeO 氧化了Cl-而产生Cl,设计以下方案:
2 4 2方案Ⅰ 取少量a,滴加KSCN溶液至过量,溶液呈红色。
用KOH溶液充分洗涤C中所得固体,再用KOH溶液将KFeO 溶出,得到紫色溶液
方案Ⅱ 2 4
b。取少量b,滴加盐酸,有Cl 产生。
2
Ⅰ.由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是KFeO 将Cl-氧
2 4
化,还可能由________________产生(用方程式表示)。
Ⅱ.方案Ⅱ可证明KFeO 氧化了Cl-。用KOH溶液洗涤的目的是________________。
2 4
②根据KFeO 的制备实验得出:氧化性Cl________ (填“>”或“<”),而方案Ⅱ实验表
2 4 2 FeO2−
4
明,Cl 和 的氧化性强弱关系相反,原因是________________。
2 FeO2−
4
③资料表明,酸性溶液中的氧化性 > ,验证实验如下:将溶液b滴入MnSO 和足量HSO
FeO2− MnO− 4 2 4
4 4
的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 > 。若能,请说明理由;若不
FeO2− MnO−
4 4
能,进一步设计实验方案。理由或方案:________________。
4.(2021·河北卷·节选)绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液
相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,
实现了CrFeAlMg的深度利用和Na+内循环。工艺流程如下:
回答下列问题:
(1)高温连续氧化工序中被氧化的元素是________(填元素符号)。
(2)工序①的名称为________。
(3)滤渣Ⅰ的主要成分是______________(填化学式)。
(4)工序③中发生反应的离子方程式为__________________________________________________。
(5)物质Ⅴ可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为__________________________________________________________________________________,
可代替NaOH的化学试剂还有________(填化学式)。
(6)热解工序产生的混合气体最适宜返回工序________(填“①”“②”“③”或“④”)参与内循环。