文档内容
第 11 讲 碳、硅及无机非金属材料
目录
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查碳及及其化合物性质和应用
高频考点2 考查硅及其化合物的性质和应用
高频考点3 考查无机非金属材料的分类和应用
高频考点4 考查CO 通入碱溶液中反应产物的判断及计算
2
正文
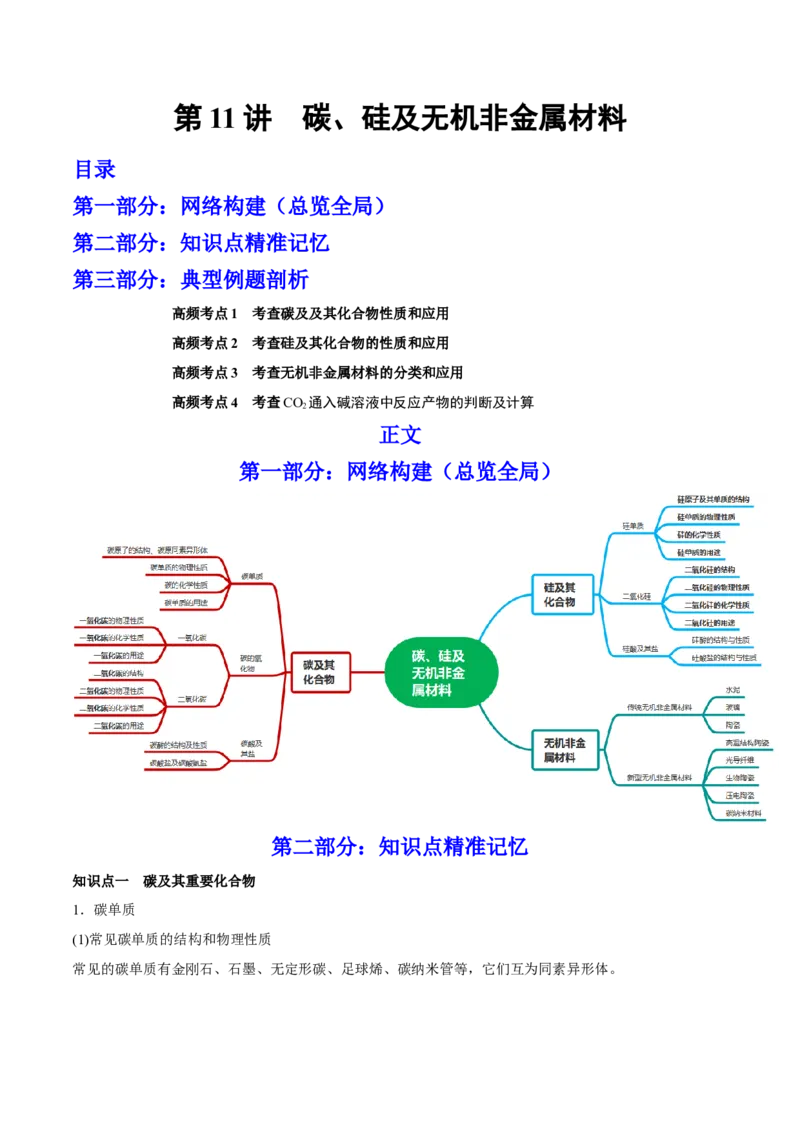
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 碳及其重要化合物
1.碳单质
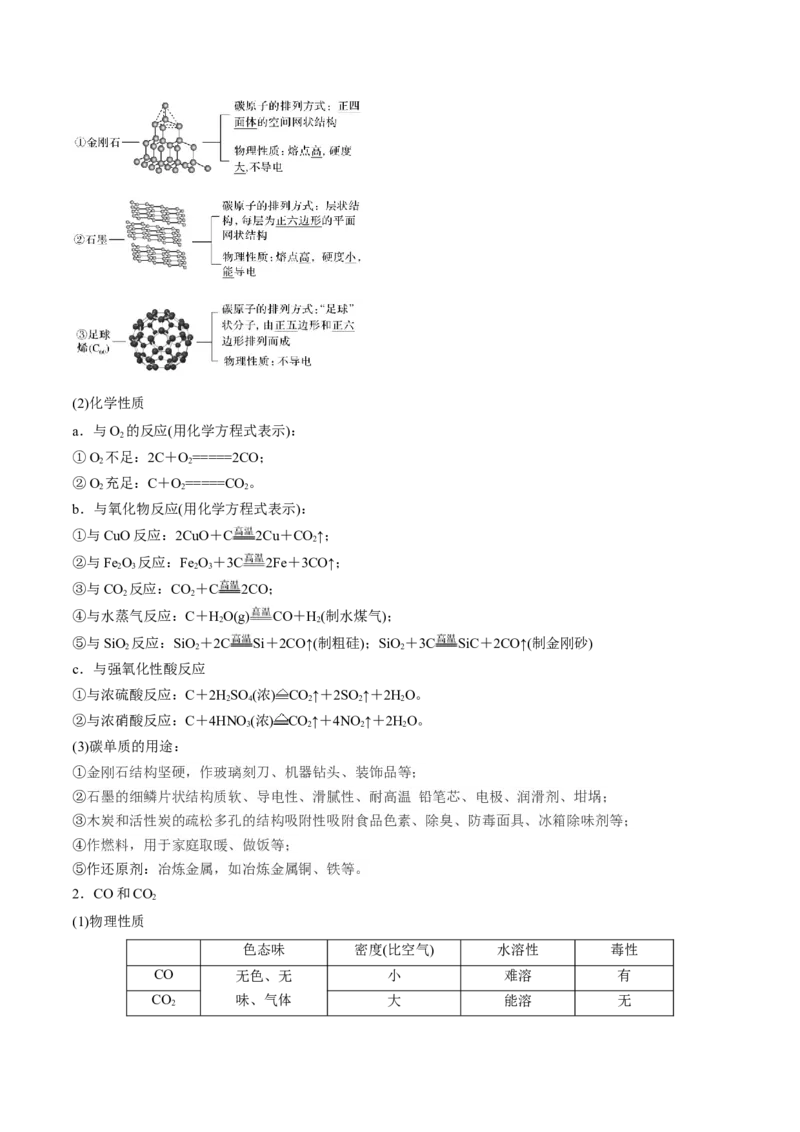
(1)常见碳单质的结构和物理性质
常见的碳单质有金刚石、石墨、无定形碳、足球烯、碳纳米管等,它们互为同素异形体。(2)化学性质
a.与O 的反应(用化学方程式表示):
2
①O 不足:2C+O=====2CO;
2 2
②O 充足:C+O=====CO。
2 2 2
b.与氧化物反应(用化学方程式表示):
①与CuO反应:2CuO+C 2Cu+CO↑;
2
②与Fe O 反应:Fe O+3C 2Fe+3CO↑;
2 3 2 3
③与CO 反应:CO+C 2CO;
2 2
④与水蒸气反应:C+HO(g) CO+H(制水煤气);
2 2
⑤与SiO 反应:SiO+2C Si+2CO↑(制粗硅);SiO+3C SiC+2CO↑(制金刚砂)
2 2 2
c.与强氧化性酸反应
①与浓硫酸反应:C+2HSO (浓) CO↑+2SO ↑+2HO。
2 4 2 2 2
②与浓硝酸反应:C+4HNO(浓) CO↑+4NO ↑+2HO。
3 2 2 2
(3)碳单质的用途:
①金刚石结构坚硬,作玻璃刻刀、机器钻头、装饰品等;
②石墨的细鳞片状结构质软、导电性、滑腻性、耐高温 铅笔芯、电极、润滑剂、坩埚;
③木炭和活性炭的疏松多孔的结构吸附性吸附食品色素、除臭、防毒面具、冰箱除味剂等;
④作燃料,用于家庭取暖、做饭等;
⑤作还原剂:冶炼金属,如冶炼金属铜、铁等。
2.CO和CO
2
(1)物理性质
色态味 密度(比空气) 水溶性 毒性
CO 无色、无 小 难溶 有
CO 味、气体 大 能溶 无
2(2)化学性质
①CO具有较强的还原性,可以与O、金属氧化物等发生反应。
2
如与Fe O 反应:Fe O+3CO=====2Fe+3CO。
2 3 2 3 2
②CO 是典型的酸性氧化物,也具有氧化性。
2
a.酸性氧化物
①与水反应:CO +H O H CO
2 2 2 3
②与碱反应:CO 少量:CO +2NaOH===Na CO +H O;CO 足量:CO +NaOH===NaHCO
2 2 2 3 2 2 2 3
③与碱性氧化物反应:CO +CaO=CaCO
2 3
④与Ca(ClO) 盐溶液反应:Ca(ClO) +CO +H O===CaCO ↓+2HClO(CO 少量);
2 2 2 2 3 2
Ca(ClO) +2CO +2H O===Ca(HCO ) +2HClO(CO 过量);
2 2 2 3 2 2
b.氧化性
①与C反应:CO+C 2CO;
2
②与Mg反应:2Mg+CO 2MgO+C
2
【特别提醒】溶液中通入CO 气体产生沉淀的问题:向BaCl 或CaCl 溶液中通入CO 气体,由于盐酸的酸
2 2 2 2
性比碳酸的强,不会产生BaCO 或CaCO 沉淀。
3 3
3.碳酸和碳酸盐
(1)碳酸
二元弱酸、不稳定,常用CO+HO代替HCO,但酸性比苯酚、次氯酸强。
2 2 2 3
(2)碳酸的正盐和酸式盐的比较
正盐(CO) 酸式盐(HCO)
溶解性 只有钾、钠、铵盐可溶 一般都可溶
热稳定性 正盐>酸式盐
溶液pH 同浓度:正盐>酸式盐
相互转化
CO HCO
4、碳元素在自然界中的循环
①CO 的主要来源:大量含碳燃料的燃烧。
2
②自然界消耗CO 的主要反应:
2
a.溶于江水、海水中:CO+HO HCO;
2 2 2 3
b.光合作用将CO 转化为O;
2 2
c.岩石的风化:CaCO +HO+CO===Ca(HCO)。
3 2 2 3 2知识点二 硅及其化合物
1.硅
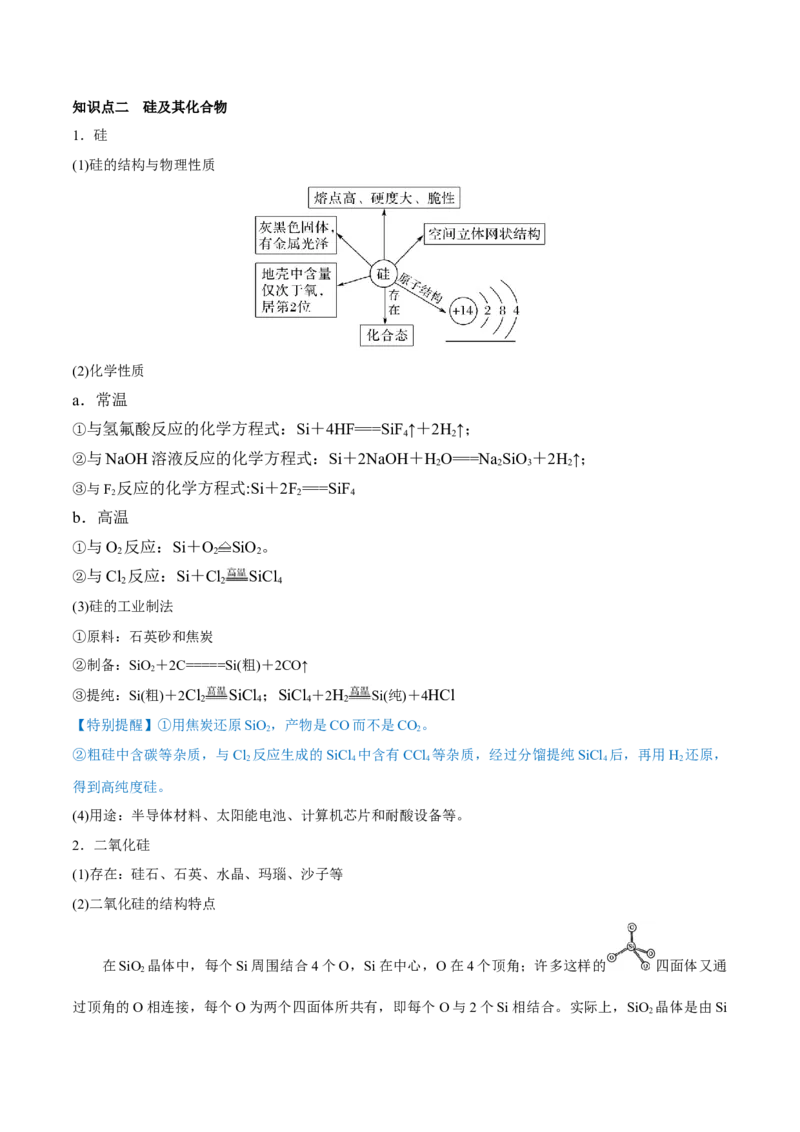
(1)硅的结构与物理性质
(2)化学性质
a.常温
①与氢氟酸反应的化学方程式:Si+4HF===SiF ↑+2H ↑;
4 2
②与NaOH溶液反应的化学方程式:Si+2NaOH+H O===Na SiO +2H ↑;
2 2 3 2
③与F 反应的化学方程式:Si+2F ===SiF
2 2 4
b.高温
①与O 反应:Si+O SiO 。
2 2 2
②与Cl 反应:Si+Cl SiCl
2 2 4
(3)硅的工业制法
①原料:石英砂和焦炭
②制备:SiO+2C=====Si(粗)+2CO↑
2
③提纯:Si(粗)+2Cl SiCl ;SiCl +2H Si(纯)+4HCl
2 4 4 2
【特别提醒】①用焦炭还原SiO,产物是CO而不是CO。
2 2
②粗硅中含碳等杂质,与Cl 反应生成的SiCl 中含有CCl 等杂质,经过分馏提纯SiCl 后,再用H 还原,
2 4 4 4 2
得到高纯度硅。
(4)用途:半导体材料、太阳能电池、计算机芯片和耐酸设备等。
2.二氧化硅
(1)存在:硅石、石英、水晶、玛瑙、沙子等
(2)二氧化硅的结构特点
在SiO 晶体中,每个Si周围结合4个O,Si在中心,O在4个顶角;许多这样的 四面体又通
2
过顶角的O相连接,每个O为两个四面体所共有,即每个O与2个Si相结合。实际上,SiO 晶体是由Si
2和O按1∶2的比例所组成的立体网状结构的晶体。由结构可知,二氧化硅的化学性质很稳定。
(3)物理性质:熔点高,硬度大,不溶于水
(4)化学性质:
a.酸性氧化物
①与碱反应:SiO +2NaOH===Na SiO +H O;
2 2 3 2
②与CaO碱性氧化物反应:SiO +CaO CaSiO
2 3
③与盐反应:SiO +Na CO Na SiO +CO ↑;SiO +CaCO CaSiO +CO ↑(工业制玻璃)
2 2 3 2 3 2 2 3 3 2
b.氧化性:
高温
①与碳反应:SiO
2
+2C Si+2CO↑(制粗硅);SiO
2
+3C SiC+2CO↑(制金刚砂);
②与Mg反应:4Mg+SiO 2MgSi+2MgO;MgSi+2H O=SiH ↑+2Mg(OH) (制硅化氢);
2 2 2 2 4 2
c.特性:
与氢氟酸反应:SiO+4HF===SiF ↑+2H O
2 4 2
(5)用途
①水晶可用于电子工业的部件、光学仪器、工艺品
②SiO 是制光导纤维的重要原料
2
③较纯的石英用于制造石英玻璃
④石英砂用于制玻璃的原料及建筑材料
【特别提醒】(1)由于玻璃的成分中含有SiO,故实验室盛放碱液的试剂瓶用橡皮塞而不用玻璃塞。
2
(2)未进行磨砂处理的玻璃,在常温下是不易被强碱腐蚀的。
(3)因为氢氟酸腐蚀玻璃,与玻璃中的SiO 反应,所以氢氟酸不能用玻璃瓶保存,而应保存在塑料瓶或
2
铅皿中。
(4)SiO 是HSiO 的酸酐,但SiO 不与水反应,不能用SiO 直接与水作用制备HSiO。
2 2 3 2 2 2 3
3.硅酸
(1)物理性质:硅酸是一种白色胶状物质,不溶于水,能形成胶体。新制备的硅酸为透明、胶冻状,硅
酸经干燥脱水形成硅酸干凝胶——“硅胶”。
(2)化学性质:
a.弱酸性:硅酸的酸性很弱,比碳酸的酸性还弱,在与碱反应时只能与强碱反应。如 :
HSiO+2NaOH==Na SiO+2H O。
2 3 2 3 2
b.不稳定性:硅酸的热稳定性很差,受热分解为SiO 和HO:HSiO=====SiO+HO。
2 2 2 3 2 2
(3)制备:由于SiO 不溶于水,所以硅酸是通过可溶性硅酸盐与其他酸反应制得的。
2
NaSiO+2HCl==H SiO↓+2NaCl,
2 3 2 3
NaSiO+CO +H O==H SiO↓+Na CO(证明酸性:HCO>HSiO)。
2 3 2 2 2 3 2 3 2 3 2 3
(4)用途:硅胶可作催化剂的载体和袋装食品、瓶装药品的干燥剂。
4.硅酸盐
(1)硅酸钠
①物理性质:白色、可溶于水的粉末状固体,其水溶液俗称水玻璃,有黏性,水溶液显碱性。
②化学性质——与酸性较硅酸强的酸反应:
a.与盐酸反应的化学方程式:
NaSiO+2HCl===2NaCl+HSiO↓。
2 3 2 3
b.与CO 水溶液反应的化学方程式:
2
NaSiO+HO+CO===Na CO+HSiO↓。
2 3 2 2 2 3 2 3
③用途:黏合剂(矿物胶)、防腐剂和耐火阻燃材料。
【特别提醒】①NaSiO 的水溶液是一种黏合剂,是制备硅胶和木材防火剂等的原料;NaSiO 易与空气中
2 3 2 3
的CO、HO反应,要密封保存。
2 2
②可溶性碳酸盐、硅酸盐的水溶液呈碱性,保存该溶液的试剂瓶不能用玻璃塞,应用橡胶塞。
(2)硅酸盐的氧化物表示法:
氧化物的书写顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,不同氧化物间以“·”隔开。
如硅酸钠(Na SiO)可表示为NaO·SiO ,
2 3 2 2
长石(KAlSi O)可表示为KO·Al O·6SiO。
3 8 2 2 3 2
【特别提醒】(1)氧化物之间以“· ”隔开;(2)计量数配置出现分数应化为整数。硅酸盐改写为氧化物
形式时,各元素的化合价保持不变,且满足化合价代数和为零,各元素原子个数比符合原来的组成。当系
数配置出现分数时一般应化为整数。如上例中KAlSi O,将KO·Al O·3SiO,要写成KO·Al O·6SiO。
3 8 2 2 3 2 2 2 3 2
知识点三 无机非金属材料
1.传统无机非金属材料,如水泥、玻璃、陶瓷等硅酸盐材料。
水泥 玻璃 陶瓷
主要原料 黏土、石灰石、石膏 石灰石、石英砂、纯碱 黏土
主要设备 水泥回转窑 玻璃窑 陶瓷窑
复杂的物理、化学变 主要反应:NaCO+SiO=====NaSiO+ 复杂的物理、化
2 3 2 2 3
变化
化过程 CO↑、CaCO +SiO=====CaSiO +CO↑ 学变化过程
2 3 2 3 2
硅酸三钙(3CaO·SiO )
组成 2 硅酸钠、硅酸钙和二氧化硅 硅酸盐
硅酸二钙(2CaO·SiO )
2铝酸三钙
3CaO·Al O)
2 3
在工农业、科
用途 重要的建筑材料 制化学实验用的玻璃仪器、窗玻璃等 技、生活、实验
室中使用广泛
(1)陶瓷:陶瓷以黏土(主要成分为含水的铝硅酸盐)为主要原料,经高温烧结而成的。
(2)玻璃:普通玻璃的主要成分为NaSiO 、CaSiO 和SiO ,它是以纯碱、石灰石和石英砂为主要原料,
2 3 3 2
经混合、粉碎,在玻璃窑中熔融,发生复杂的物理变化和化学变化而制得的,玻璃可用于生产建筑材料、
光学仪器和各种器皿,还可制造玻璃纤维,用于高强度复合材料等。
(3)水泥:普通硅酸盐水泥的主要原料是黏土和石灰石,二者与其他辅料经混合、研磨后在水泥回转窑
中煅烧,发生复杂的物理变化和化学变化,加入适量石膏调节水泥硬化速率,再研成细粉得到普通水泥。
混凝土是水泥、沙子和碎石等与水混合得到的。
2.新型无机非金属材料
(1)新型陶瓷
新型陶瓷在组成上不再限于传统的硅酸盐体系,在光学、热学、电学、磁学等方面具有很多新的特性和功
能。
(2)新型陶瓷的种类与用途
材料类型 主要特性 示例 用途
火箭发动机的尾管及燃烧
碳化硅、氮化硅与某些金属氧
高温结构陶瓷 耐高温、抗氧化、耐磨蚀 室、汽车发动机、高温电
化物等烧结而成
极材料等
滤波器、扬声器、声纳探
压电陶瓷 实现机械能与电能的相互转化 钛酸盐、锆酸盐
伤器、点火器等
优异的光学性能,耐高温,绝 氧化铝、氧化钇、氮化铝、氟 高压钠灯、激光器、高温
透明陶瓷
缘性好 化钙 探测窗等
可用于电力、交通、医疗
超导陶瓷 在某一临界温度下电阻为零
等领域
(3)碳纳米材料
碳纳米材料是一类新型的无机非金属材料
(1)类型:富勒烯、碳纳米管、石墨烯等。
(2)用途:在能源、信息、医药等领域有广阔的应用前景。
材料类型 性能 用途
比表面积大,高强度,优良的电学性
碳纳米管 生产复合材料、电池和传感器等
能
电阻率低,热导率高,具有很高的强 用于光电器件、超级电容器、电池
石墨烯
度 和复合材料等知识点四 碳、硅及其化合物性质“反常”小结
(1)一般情况下,非金属元素单质熔、沸点低,硬度小,但晶体硅、金刚石熔、沸点高,硬度大,其中金刚
石为自然界中硬度最大的物质。
(2)一般情况下,非金属单质为绝缘体,但硅为半导体,石墨为电的良导体。
(3)Si的还原性强于C,但C在高温下能还原出Si:SiO+2C=====Si+2CO↑。
2
(4)非金属单质与碱反应一般既作氧化剂又作还原剂,且无氢气放出,但硅与强碱溶液反应只作还原剂,且
放出氢气:Si+2NaOH+HO===Na SiO+2H↑。
2 2 3 2
(5)非金属单质一般不与非氧化性酸反应,但硅能跟氢氟酸反应:Si+4HF===SiF ↑+2H↑。
4 2
(6)一般情况下,碱性氧化物+酸―→盐+水,二氧化硅是酸性氧化物,却能与氢氟酸反应:SiO +
2
4HF===SiF ↑+2HO(SiF 不属于盐,故SiO 不是两性氧化物)。
4 2 4 2
(7)一般情况下,无机酸能溶于水,但硅酸却难溶于水。
(8)一般情况下,较强酸+较弱酸的盐―→较弱酸+较强酸的盐(溶液中的反应)。
因碳酸的酸性强于硅酸,所以水玻璃在空气中易变质:NaSiO+HO+CO===Na CO+HSiO(胶体)。
2 3 2 2 2 3 2 3
但在高温下,可发生反应NaCO+SiO=====NaSiO+CO↑(CO 离开反应体系促进反应的正向进行)。
2 3 2 2 3 2 2
(9)一般情况下,金属(Na、K)能置换出水中的氢,但 C 在高温下也能置换出 HO 中的氢:C+
2
HO(g)=====H+CO。
2 2
(10)一般情况下,酸性氧化物与水反应生成相应的含氧酸,但二氧化硅不溶于水,也不与水反应。
知识点五 CO 与碱、盐溶液的反应规律
2
1、与碱溶液的反应
(1)反应原理
NaOH――→NaCO――→NaHCO
2 3 3
(2)反应后溶质成分的判断
x= 溶质成分
x≤1∶1 NaHCO
3
1∶12∶1 NaOH、NaCO
2 3
也可用数轴来表示:
①CO+NaCO+HO===2NaHCO
2 2 3 2 3
②CO+NaSiO+2HO===H SiO↓+NaCO
2 2 3 2 4 4 2 3
或CO+NaSiO+HO===H SiO↓+NaCO
2 2 3 2 2 3 2 3
当CO 过量时,发生反应如下:
2
2CO+NaSiO+2HO===H SiO↓+2NaHCO
2 2 3 2 2 3 3③CO+Ca(ClO) +HO===CaCO ↓+2HClO
2 2 2 3
2、与盐溶液的反应
(1)CO 与盐溶液的常见反应
2
碳酸是一种弱酸,其酸性比盐酸、醋酸要弱,因此,盐酸、醋酸能与碳酸盐反应;其酸性又比硅酸、次氯
酸、苯酚、偏铝酸等强,因此,将CO 气体通入NaSiO 、NaClO、 、NaAlO 等盐溶液中,均能发生
2 2 3 2
反应而生成相应的弱酸和碳酸(氢)盐,这就是“强酸制弱酸”原理的应用。如:
①CO+NaCO+HO===2NaHCO
2 2 3 2 3
②CO+NaSiO+2HO===H SiO↓+NaCO
2 2 3 2 4 4 2 3
或CO+NaSiO+HO===H SiO↓+NaCO
2 2 3 2 2 3 2 3
当CO 过量时,发生反应如下:
2
2CO+NaSiO+2HO===H SiO↓+2NaHCO
2 2 3 2 2 3 3
③CO+Ca(ClO) +HO===CaCO ↓+2HClO
2 2 2 3
当CO 过量时,发生反应如下:
2
2CO+Ca(ClO) +2HO===Ca(HCO )+2HClO
2 2 2 3 2
④CO+ +HO―→ +NaHCO
2 2 3
⑤CO+NaAlO +2HO===Al(OH) ↓+NaHCO (CO 过量时)
2 2 2 3 3 2
CO+2NaAlO +3HO===2Al(OH) ↓+NaCO(CO 少量时)
2 2 2 3 2 3 2
(2)注意事项
①“强酸制弱酸”是一个重要的化学反应规律,但不可认为弱酸就不能“制取”强酸。在某些条件下,当
弱酸的酸根阴离子被沉淀或被氧化后,H+就被“释放”出来,从而生成了强酸。如将HS通入CuSO 溶液
2 4
中或向氢硫酸中滴加氯水,均由氢硫酸这种弱酸生成了强酸:HS+CuSO ===CuS↓+HSO (S2-与Cu2+结
2 4 2 4
合成难溶的CuS),HS+Cl===S↓+2HCl(S2-被氧化)。
2 2
②CO 与 溶液反应的产物与CO 的用量无关,都生成NaHCO ,因为酸性HCO> >HCO。
2 2 3 2 3
③CO 与NaClO溶液反应的产物与CO 的量无关,也只能生成NaHCO ,不能生成NaCO ,因为酸性
2 2 3 2 3
HCO>HClO>HCO。
2 3
④CO、SO 通入CaCl 或BaCl 溶液均不反应,无沉淀产生。
2 2 2 2
第三部分:典型例题剖析
高频考点1 考查碳及及其化合物性质和应用
例1、(2021·全国·高三专题练习)下列有关碳及其化合物的说法正确的是( )
A.CO 是导致酸雨的主要气体
2
B.CO和CO 组成元素相同,所以他们的化学性质相同
2
C.金刚石、石墨是碳的单质,而C 是碳的化合物
60
D.在高温条件下,碳能使CO 转变成CO
2
【解析】A.正常雨水的pH=5.6,就是溶有CO 的缘故,故CO 不是导致酸雨的主要气体,SO 和氮的氧
2 2 2化物才是导致酸雨的主要气体,A错误;B.CO和CO 组成元素相同,但它们分子组成不同,故他们的化
2
学性质不相同,例如CO具有可燃性,CO 却不支持燃烧等,B错误;C.单质是指只含有一种元素的纯净
2
物,故金刚石、石墨是碳的单质,C 也是碳的单质,C错误;D.在高温条件下,碳能使CO 转变成
60 2
CO,CO+C 2CO,D正确;故答案为:D。
2
【答案】D
【变式训练1】(碳循环)(2022·河北·模拟预测)海洋碳循环是全球碳循环的重要组成部分,是影响全球
气候变化的关键控制环节。下图为海洋中碳循环的简单原理图。下列说法错误的是
A.海洋碳循环过程中能将太阳能转化为化学能
B.钙化释放CO 的离子方程式:2HCO +Ca2+=CaCO ↓+CO ↑+H O
2 3 2 2
C.影响海洋碳循环的因素主要有海水的酸碱性、水温、藻类生物的分布等
D.光合作用,每生成0.1mol(CHO) 转移电子数为4N (N 表示阿伏伽德罗常数)
2 x A A
【解析】如图CO 在弱碱性条件下转化成NaCO、NaHCO ,遇氯化钙发生2HCO
2 2 3 3
+Ca2+=CaCO ↓+CO ↑+H O,生成CaCO 沉淀钙化同时释放CO,再经光合作用,形成有机物参与海洋碳循
3 2 2 3 2
环。A. CO 经光合作用形成有机物参与海洋碳循环,过程中能将太阳能转化为化学能,故A正确;B.
2
钙化生成CaCO 沉淀同时,释放CO 的离子方程式:2HCO +Ca2+=CaCO ↓+CO ↑+H O,故B正确;C.
3 2 3 2 2
温度高或酸性条件下,二氧化碳在水中溶解度小,影响海洋碳循环的因素主要有海水的酸碱性、水温、藻
类生物的分布等,故C正确;
D. 光合作用,碳由+4价降为0价,每生成0.1mol(CHO) 转移电子数为0.4xN (N 表示阿伏伽德罗常数),
2 x A A
故D错误;故选D。
【答案】D
【变式训练2】(碳的氧化物的性质及应用)(2022·广东汕头·模拟预测)我国努力争取在2060年前实现碳中
和。下列说法不正确的是A.广泛使用的太阳能电池其光电转换材料是SiO
2
B.可利用CaO或氨水捕集废气中的CO
2
C.一定条件下,将CO 转化为淀粉,实现CO 的资源化利用
2 2
D.研发新型催化剂将CO 分解成碳和O,同时吸收热量
2 2
【解析】A.太阳能电池其光电转换材料是单质Si,不是SiO,A错误;B.CaO或氨水具有碱性,能与酸
2
性气体CO 反应,可减少二氧化碳的量,有利于实现碳中和,B正确;
2
C.将CO 转化为淀粉,实现CO 的资源化利用,可减少二氧化碳的量,有利于实现碳中和,C正确;D.
2 2
将CO 分解成碳和O,需要吸收能量,为吸热反应,可减少二氧化碳的量,有利于实现碳中和,D正确;
2 2
答案选A。
【答案】A
高频考点2 考查硅及其化合物的性质和应用
例2.(2021·全国·高三专题练习)下列表述正确的是
①人造刚玉熔点很高,可用作高级耐火材料,主要成分是二氧化硅
②化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐
③提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料
④夏天到了,游客佩戴由添加氧化亚铜的二氧化硅玻璃制作的变色眼镜来保护眼睛
⑤太阳能电池可采用硅材料制作,其应用有利于环保、节能
A.①②③ B.②④ C.③④⑤ D.③⑤
【解析】人造刚玉主要成分为Al O,①错;玛瑙的主要成分是SiO,②正确;③水泥主要成分是硅酸盐,
2 3 2
正确;④变色眼镜镜片应是在普通硼酸盐玻璃中加入光敏物质AgBr等,并加入极少光敏化剂如CuO等制
成,故④错。⑤硅可用于太阳能电池板,⑤正确;
综上所述,本题答案选D。
【答案】D
【拓展延伸】变色眼镜的玻璃片中含有少量溴化银和微量的氧化铜(作催化剂),当玻璃受到阳光照射时,
发生2AgBr 2Ag+Br 反应,而使玻璃由无色变成灰黑色,把玻璃放到暗处,又因发生2Ag+Br 2AgBr
2 2
反应,而使玻璃由灰黑色变成无色。在制造普通玻璃时常加入少量Cu O可使玻璃显红色。
2
【变式训练1】(二氧化硅的性质和用途)(2021·全国·高三专题练习)二氧化硅广泛存在于自然界中,在
日常生活、生产、科研及新型材料等方面有着重要的用途。a~e是对①~⑤反应中SiO 所表现的化学性质
2
或作用进行判断,其中正确的是
①SiO+2NaOH=NaSiO+H O
2 2 3 2②SiO+2C Si+2CO↑
2
③SiO+4HF=SiF↑+2H O
2 4 2
④NaCO+SiO NaSiO+CO ↑
2 3 2 2 3 2
⑤SiO+3C SiC+2CO↑
2
a.反应①中SiO 作为玻璃的成分被消耗,用于刻蚀玻璃
2
b.反应②中SiO 表现出氧化性
2
c.反应③中SiO 表现了酸性氧化物的通性
2
d.反应④符合用难挥发性的酸酐制取易挥发性的酸酐的道理
e.反应⑤中SiO 未参加氧化还原反应
2
A.ace B.bde C.cde D.ab
【解析】通常用氢氟酸来刻蚀玻璃,与之对应的反应是③,a、c判断错误;反应②是一个置换反应,SiO
2
表现出氧化性,b正确;反应④是一个复分解反应,符合用难挥发的二氧化硅制取易挥发的二氧化碳,d正
确;反应⑤中硅的化合价和氧的化合价都没有改变,e正确。答案选B。
【答案】B
【变式训练2】(硅酸盐的性质和表示方法)青石棉是一种致癌物质,是《鹿特丹公约》中受限制的46种化
学品之一,其化学式为NaFe Si O (OH) 。青石棉用稀硝酸处理时,还原产物只有NO,下列说法不正确的
2 5 8 22 2
是
A.青石棉是一种硅酸盐产品
B.青石棉中含有一定量的石英晶体
C.青石棉的化学组成可表示为NaO·3FeO·Fe O·8SiO·H O
2 2 3 2 2
D.1 mol青石棉能还原1 mol HNO
3
【解析】硅酸盐指的是Si、O与其他化学元素结合而成的化合物的总称,根据青石棉的化学式可知,青石
棉是一种硅酸盐产品,故A说法正确;硅酸盐中不含有SiO ,因此青石棉中不含石英晶体,故B说法错误;
2
按照硅酸盐写成氧化物形式,青石棉的化学式组成用氧化物的形式可表示为NaO·3FeO·Fe O·8SiO·H O,
2 2 3 2 2
故C说法正确;根据C选项分析,青石棉中含有+2价的铁,与硝酸发生氧化还原反应,根据得失电子数
目守恒可知,1 mol青石棉能还原1 mol HNO,故D说法正确。
3
【答案】B高频考点3 考查无机非金属材料的分类和应用
例3.(2021·全国·高三专题练习)下列关于无机非金属材料的说法中不正确的是
A.传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料
B.新型无机非金属材料克服了传统无机非金属材料的许多缺点
C.高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点
D.传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐
【解析】A. 硅酸盐材料是传统的无机非金属材料,主要包括:玻璃、水泥、陶瓷,故A正确;B. 新型无
机非金属材料不但克服了传统的无机非金属材料的缺点,而且同时还具有了如能承受高温、强度较高,故
B正确;C. 高温结构材料属于新型的无机非金属材料,具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度
小等优点,故C正确;D. 新型无机非金属材料如高温结构陶瓷(Si N 陶瓷、SiC陶瓷)的主要成分不是硅酸
3 4
盐,只有传统无机非金属材料才是硅酸盐,故D错误;故答案选:D。
【答案】D
【变式训练1】(传统无机非金属材料)(2021·天津河北·一模)下列关于“嫦娥五号”所用的材料中不属
于新型无机非金属材料的是
A.挖土铲——氮化碳特种钻 B.国旗——复合纤维织物
C.降落伞——氮化硼纤维 D.望远镜——碳化硅特种陶瓷
【解析】A.氮化碳特种钻属于新型无机非金属材料,故A不符合题意;B.复合纤维织物属于新型有机
材料,故B符合题意;C.氮化硼纤维属于新型无机非金属材料,故C不符合题意;D.碳化硅特种陶瓷
属于新型无机非金属材料,故D不符合题意;答案为B。
【答案】B
【变式训练2】(新型无机非金属材料)(2022·上海·三模)由于石墨烯独特的结构,在石墨烯薄膜上施加
较低的电压(1-10V)即可产生较高的热量,平昌冬奥会“北京8分钟”主创团队用石墨烯制作了20℃能发热
4h的智能服饰,向世界展现了新时代的中国形象,下列说法中错误的是
A.石墨烯是能导热的金属材料 B.石墨烯属于单质
C.石墨烯能导电 D.在石墨烯薄膜上施加电压,使电能转化为热能
【解析】A.石墨烯属于碳单质,是能够导热的非金属材料,A错误;B.石墨烯是碳的单质,B正确;
C.石墨烯属于碳单质,碳单质具有良好的导电性,可以导电,C正确;D.根据题干信息可知,在石墨烯薄膜上施加较低的电压(1-10V)即可产生较高的热量,使电能转化为热能,D正确;答案选A。
【答案】A
高频考点4 考查CO 通入碱溶液中反应产物的判断及计算
2
例4.(2021·全国·高三专题练习)往含0.2 mol NaOH和0.1 mol Ba(OH) 的混合溶液中持续稳定地通入CO
2 2
气体6.72 L(标准状况下),则在这一过程中,下列有关溶液中离子总物质的量(n)随通入CO 气体体积(V)的
2
变化曲线中正确的是(离子水解忽略不计)( )
【解析】根据电离方程式:NaOH===Na++OH-,Ba(OH) ===Ba2++2OH-可知,在含0.2 mol NaOH和0.1
2
mol Ba(OH) 的混合溶液中离子的总物质的量为0.2 mol×2+0.1 mol×3=0.7 mol。标准状况下6.72 L CO 的
2 2
物质的量n(CO)==0.3 mol,把CO 气体通入混合溶液中,首先发生反应:Ba2++2OH-+CO===BaCO ↓
2 2 2 3
+HO,当0.1 mol Ba(OH) 恰好反应完全时消耗0.1 mol CO (体积为2.24 L),此时离子的物质的量减少0.3
2 2 2
mol,溶液中离子的物质的量为0.4 mol,排除D选项;然后发生反应:CO +2OH-===CO+HO,当0.2
2 2
mol NaOH完全反应时又消耗0.1 mol CO (体积为2.24 L),消耗总体积为4.48 L,离子的物质的量又减少
2
0.1 mol,此时溶液中离子的物质的量为0.7 mol-0.3 mol-0.1 mol=0.3 mol,排除A选项;继续通入0.1
mol CO 气体,发生反应:CO+HO+CO===2HCO,根据方程式可知:0.1 mol CO 反应,溶液中离子的
2 2 2 2
物质的量增加0.1 mol,此时溶液中离子的物质的量为0.3 mol+0.1 mol=0.4 mol,排除C选项,只有选项
B符合反应实际,故合理选项是B。
【答案】B
【变式训练】(2022·全国·高三专题练习)已知:①KCO+CO +H O→2KHCO;CaCO +CO +H O→Ca
2 3 2 2 3 3 2 2
(HCO ) ②KHCO 、Ca(HCO ) 都易溶于水 ③通入悬浊液中的气体,与溶液反应后才与沉淀反应,
3 2 3 3 2
将足量CO 通入KOH和Ca(OH) 的混合稀溶液中,则生成沉淀的质量和通入的CO 质量的关系中,正
2 2 2
确的是
A. B. C. D.
【解析】根据二氧化碳与氢氧化钙反应生成碳酸钙,所以沉淀质量增加,二氧化碳过量后沉淀又被溶解,
即减少,同时考虑的题给的信息“③通入悬浊液中的气体,与溶液反应后才与沉淀反应”即可完成该题的
解答。一开始二氧化碳与氢氧化钙反应生成碳酸钙,此时沉淀质量增加,当二氧化碳和氢氧化钙反应完毕后,根据题中信息可以知道,此时溶液处出于悬浊液状态,所以此时发生的是二氧化碳和碳酸钾溶液或是
没有反应完全的氢氧化钾的反应,不管怎么样都不会再有沉淀产生,但是同时沉淀的质量也不会减少,当
把碳酸钾及氢氧化钾完全反应后,二氧化碳与碳酸钙反应生成了能够溶于水的碳酸氢钙,此时沉淀逐渐减
少最后为零,则选项B符合题意,故答案选B。
【答案】B