文档内容
第 19 讲 电解池 金属的电化学腐蚀与防护
目录
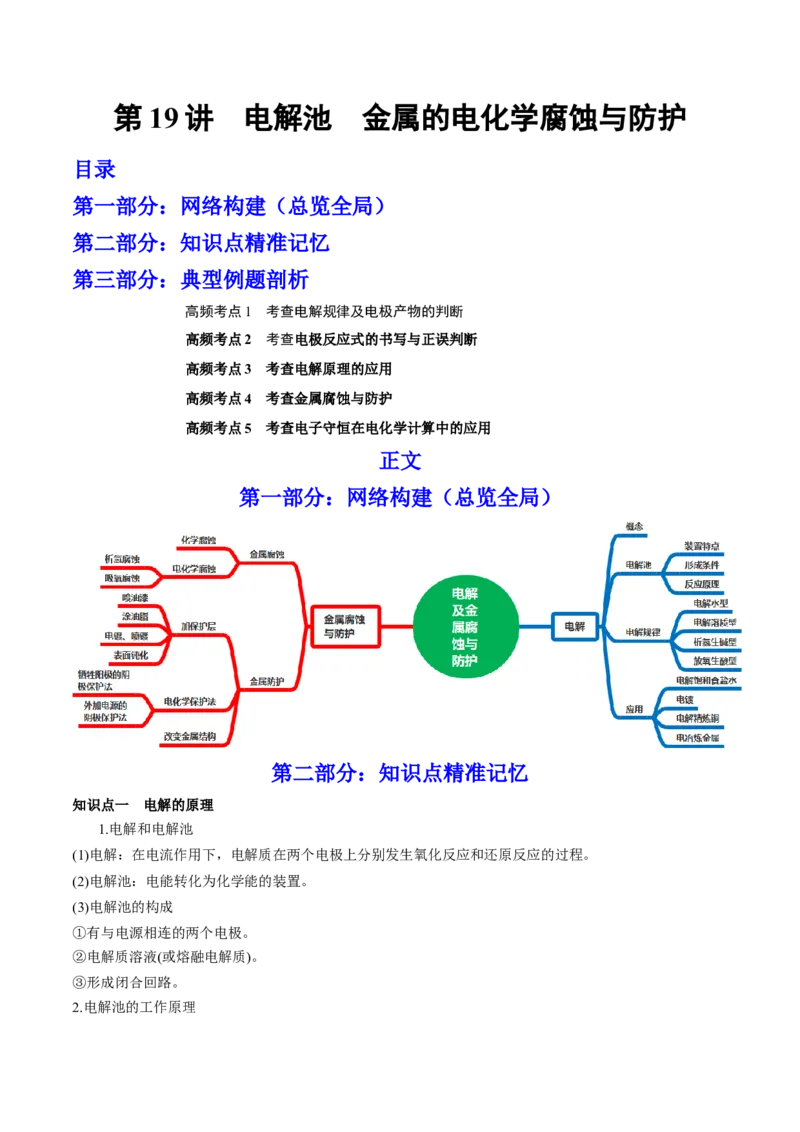
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查电解规律及电极产物的判断
高频考点2 考查电极反应式的书写与正误判断
高频考点3 考查电解原理的应用
高频考点4 考查金属腐蚀与防护
高频考点5 考查电子守恒在电化学计算中的应用
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 电解的原理
1.电解和电解池
(1)电解:在电流作用下,电解质在两个电极上分别发生氧化反应和还原反应的过程。
(2)电解池:电能转化为化学能的装置。
(3)电解池的构成
①有与电源相连的两个电极。
②电解质溶液(或熔融电解质)。
③形成闭合回路。
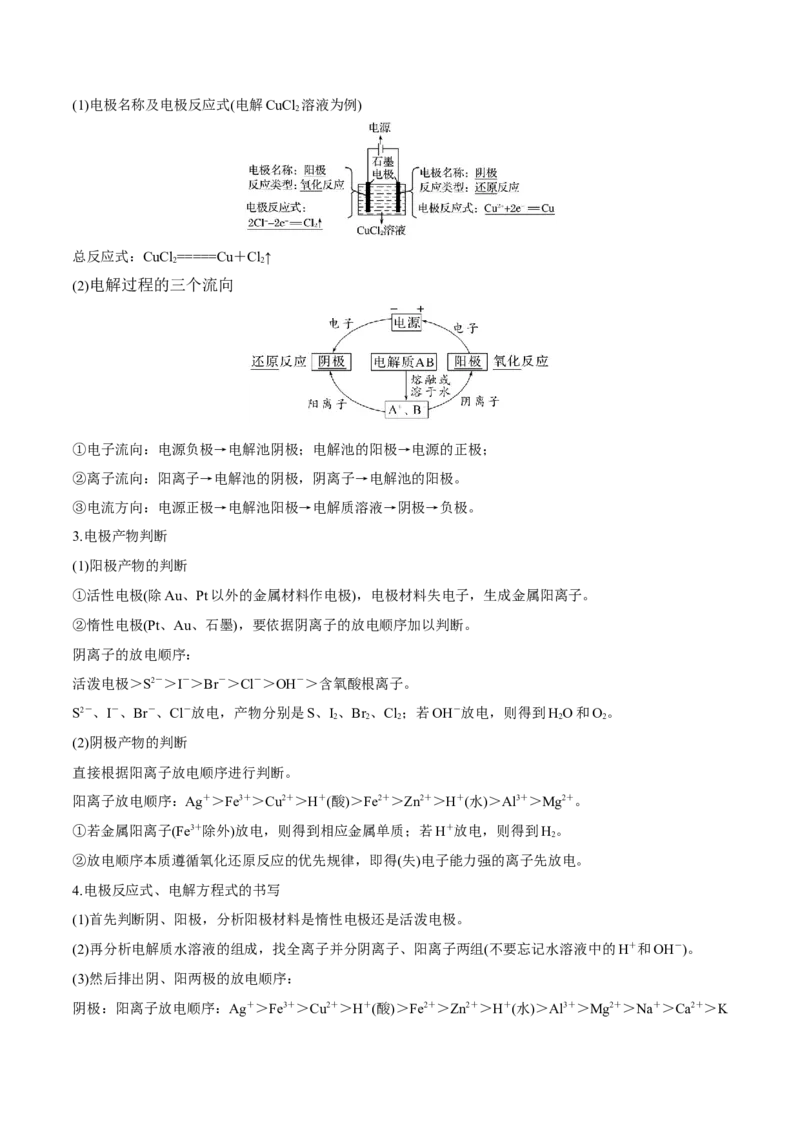
2.电解池的工作原理(1)电极名称及电极反应式(电解CuCl 溶液为例)
2
总反应式:CuCl =====Cu+Cl↑
2 2
(2)电解过程的三个流向
①电子流向:电源负极→电解池阴极;电解池的阳极→电源的正极;
②离子流向:阳离子→电解池的阴极,阴离子→电解池的阳极。
③电流方向:电源正极→电解池阳极→电解质溶液→阴极→负极。
3.电极产物判断
(1)阳极产物的判断
①活性电极(除Au、Pt以外的金属材料作电极),电极材料失电子,生成金属阳离子。
②惰性电极(Pt、Au、石墨),要依据阴离子的放电顺序加以判断。
阴离子的放电顺序:
活泼电极>S2->I->Br->Cl->OH->含氧酸根离子。
S2-、I-、Br-、Cl-放电,产物分别是S、I、Br 、Cl;若OH-放电,则得到HO和O。
2 2 2 2 2
(2)阴极产物的判断
直接根据阳离子放电顺序进行判断。
阳离子放电顺序:Ag+>Fe3+>Cu2+>H+(酸)>Fe2+>Zn2+>H+(水)>Al3+>Mg2+。
①若金属阳离子(Fe3+除外)放电,则得到相应金属单质;若H+放电,则得到H。
2
②放电顺序本质遵循氧化还原反应的优先规律,即得(失)电子能力强的离子先放电。
4.电极反应式、电解方程式的书写
(1)首先判断阴、阳极,分析阳极材料是惰性电极还是活泼电极。
(2)再分析电解质水溶液的组成,找全离子并分阴离子、阳离子两组(不要忘记水溶液中的H+和OH-)。
(3)然后排出阴、阳两极的放电顺序:
阴极:阳离子放电顺序:Ag+>Fe3+>Cu2+>H+(酸)>Fe2+>Zn2+>H+(水)>Al3+>Mg2+>Na+>Ca2+>K+。
阳极:活泼电极>S2->I->Br->Cl->OH->含氧酸根离子。
(4)分析电极反应,判断电极产物,写出电极反应式,要注意遵循原子守恒和电荷守恒。
(5)最后写出电解反应的总化学方程式或离子方程式,并注明“电解”条件。
【特别提醒】①阴极不管是什么材料,电极本身都不反应,一定是溶液(或熔融电解质)中的阳离子放电,
注意离子导体(电解质)是水溶液还是非水状态。②阳极材料不同,电极产物、电极反应式可能不同,最常
用、最重要的放电顺序为阳极:Cl->OH-;阴极:Ag+>Cu2+>H+。③电解水溶液时,K+~Al3+不可能在
阴极放电,即不可能用电解水溶液的方法得到K、Ca、Na、Mg、Al等金属。④书写电解池中的电极反应
式时,要以实际放电的离子表示,但书写总电解反应方程式时,弱电解质要写成分子式。⑤电解质溶液中
未参与放电的离子是否与放电后生成的离子发生反应(离子共存)。⑥要确保两极电子转移数目相同,且注
明条件“电解”。
5.阴、阳极的判断方法
(1)根据外接电源:正极接阳极,负极接阴极。
(2)根据电流方向:从阴极流出,从阳极流入。
(3)根据电子流向:从阳极流出,从阴极流入。
(4)根据离子移向:阴离子移向阳极,阳离子移向阴极。
(5)根据电极产物:阳极——电极溶解、逸出O(或阳极区酸性增强)或Cl;阴极——析出金属、逸出H(或阴
2 2 2
极区碱性增强)。
(6)根据反应类型:阳极发生氧化反应,阴极发生还原反应。
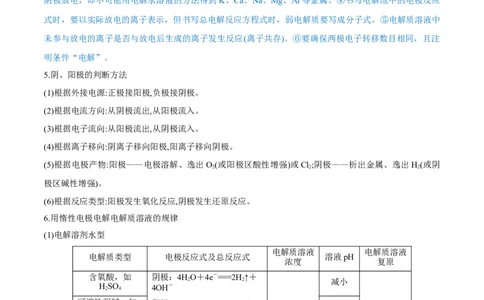
6.用惰性电极电解电解质溶液的规律
(1)电解溶剂水型
电解质溶液 电解质溶液
电解质类型 电极反应式及总反应式 溶液pH
浓度 复原
含氧酸,如 阴极:4HO+4e-===2H ↑+
2 2 减小
H
2
SO
4
4OH-
可溶性强碱,如 阳极:2HO-4e-===O ↑+
2 2 增大 增大 加水
NaOH 4H+
活泼金属含氧酸 总反应式:2HO=====2H↑
2 2 不变
盐,如KNO 3 +O 2 ↑
(2)电解溶质型
电解质 电解质
电解质 电极反应式 溶液
溶液 溶液
类型 及总反应式 pH
浓度 复原
无氧酸,如 阴极:2H++2e-===H 2 ↑ 减小 增大 通入阳极:2Cl--2e-===Cl↑ HCl
2
HCl
总反应式:2HCl=====H↑+Cl↑ 气体
2 2
阴极:Cu2++2e-===Cu 加入
不活泼金属
无氧酸盐, 阳极:2Cl--2e-===Cl↑ CuCl
2 2
如CuCl
2 总反应式:CuCl =====Cu+Cl↑ 固体
2 2
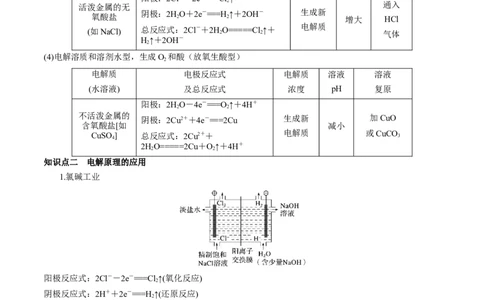
(3)电解溶质和溶剂水型,生成H 和碱(析氢生碱型):
2
电解质 电解质 溶液 溶液
电极反应式及总反应式
(水溶液) 浓度 pH 复原
阳极:2Cl--2e-===Cl↑
活泼金属的无 2 通入
氧酸盐
阴极:2H
2
O+2e-===H
2
↑+2OH- 生成新
增大 HCl
(如NaCl) 总反应式:2Cl-+2H
2
O=====Cl
2
↑+ 电解质
气体
H↑+2OH-
2
(4)电解溶质和溶剂水型,生成O 和酸(放氧生酸型)
2
电解质 电极反应式 电解质 溶液 溶液
(水溶液) 及总反应式 浓度 pH 复原
阳极:2HO-4e-===O ↑+4H+
2 2
不活泼金属的 阴极:2Cu2++4e-===2Cu 生成新 加CuO
含氧酸盐[如 减小
CuSO 4 ] 总反应式:2Cu2++ 电解质 或CuCO 3
2HO=====2Cu+O↑+4H+
2 2
知识点二 电解原理的应用
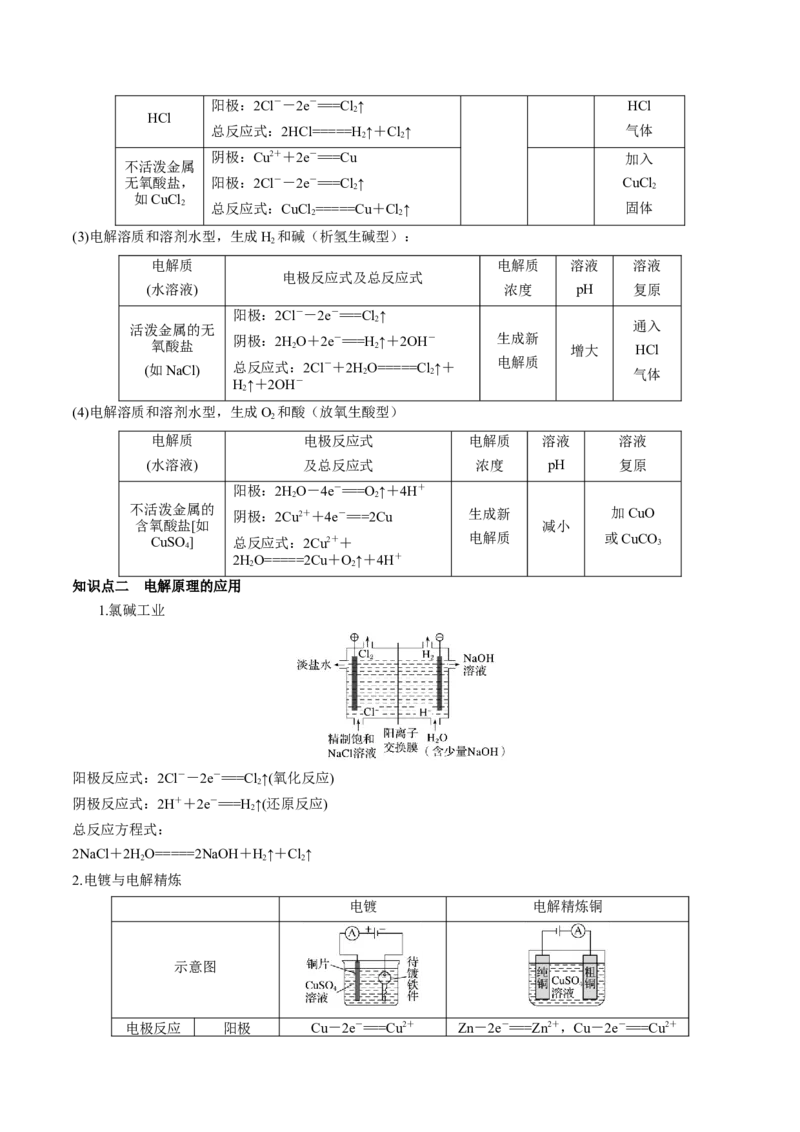
1.氯碱工业
阳极反应式:2Cl--2e-===Cl↑(氧化反应)
2
阴极反应式:2H++2e-===H ↑(还原反应)
2
总反应方程式:
2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
2.电镀与电解精炼
电镀 电解精炼铜
示意图
电极反应 阳极 Cu-2e-===Cu2+ Zn-2e-===Zn2+,Cu-2e-===Cu2+阴极 Cu2++2e-===Cu Cu2++2e-===Cu
电解质溶液的浓度变化 CuSO 溶液的浓度不变 CuSO 溶液的浓度变小
4 4
注意:电解精炼铜时,阳极质量减小,阴极质量增加,溶液中的Cu2+浓度减小。粗铜中不活泼的杂质(金
属活动性顺序中位于铜之后的银、金等),在阳极难以失去电子,当阳极上的铜失去电子变成离子之后,它
们以金属单质的形式沉积于电解槽的底部,成为阳极泥。
3.电冶金
电解冶
冶炼钠 冶炼镁 冶炼铝
炼
电极反 阳极:2Cl--2e-===Cl↑ 阳极:2Cl-2e-===Cl↑ 阳极:6O2--12e-===3O ↑
2 2 2
应 阴极:2Na++2e-===2Na 阴极:Mg2++2e-===Mg 阴极:4Al3++12e-===4Al
MgCl 熔融=====Mg+
2
总反应 2NaCl(熔融)=====2Na+Cl↑ 2Al O(熔融)=====4Al+3O↑
2 2 3 2
Cl↑
2
【特别提醒】(1)氯碱工业所用的饱和食盐水需要精制,除去NaCl中混有的Ca2+、Mg2+、SO。
(2)电镀铜时,电解质溶液中c(Cu2+)不变;电解精炼铜时,电解质溶液中c(Cu2+)减小。
(3)电解熔融MgCl 冶炼镁,而不能电解MgO冶炼镁,是因为MgO的熔点很高;电解熔融Al O 冶炼铝,
2 2 3
而不能电解AlCl 冶炼铝,是因为AlCl 是共价化合物,其熔融态不导电。
3 3
知识点三 金属的腐蚀与防护
1.金属腐蚀的本质
金属原子失去电子变为金属阳离子,金属发生氧化反应。
2.金属腐蚀的类型
(1)化学腐蚀与电化学腐蚀
类型 化学腐蚀 电化学腐蚀
条件 金属跟非金属单质直接接触 不纯金属或合金跟电解质溶液接触
现象 无电流产生 有微弱电流产生
本质 金属被氧化 较活泼金属被氧化
联系 两者往往同时发生,电化学腐蚀更普遍
(2)析氢腐蚀与吸氧腐蚀(以钢铁的腐蚀为例):
类型 析氢腐蚀 吸氧腐蚀
条件 水膜酸性较强(pH≤4.3) 水膜酸性很弱或呈中性
负极 Fe-2e-===Fe2+
电极反应
正极 2H++2e-===H ↑ O+2HO+4e-===4OH-
2 2 2
总反应式 Fe+2H+===Fe2++H↑ 2Fe+O+2HO===2Fe(OH)
2 2 2 2
联系 吸氧腐蚀更普遍
【特别提醒】①电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防腐措施的腐蚀。
②钢铁暴露在潮湿空气中主要发生的是吸氧腐蚀,铁锈的形成过程中主要发生的反应为 4Fe(OH) +O +
2 2
2HO===4Fe(OH) ,2Fe(OH) ===Fe O·xHO(铁锈)+(3-x)H O。
2 3 3 2 3 2 23.金属的防护
(1)电化学防护
①牺牲阳极的阴极保护法——原电池原理
a.负极:比被保护金属活泼的金属;
b.正极:被保护的金属设备。
②外加电流的阴极保护法——电解原理
a.阴极:被保护的金属设备;
b.阳极:惰性金属或石墨。
(2)改变金属的内部结构,如制成合金、不锈钢等。
(3)加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。
【特别提醒】(1)钢铁发生电化学腐蚀时,负极铁去电子生成Fe2+,而不是生成Fe3+。
(2)金属腐蚀时,电化学腐蚀与化学腐蚀往往同时存在,但前者更普遍,危害也更严重。
(3)铜暴露在潮湿的空气中发生的是化学腐蚀,而不是电化学腐蚀,生成铜绿的化学成分是Cu (OH) CO。
2 2 3
(4)两种保护方法的比较:外加电流的阴极保护法比牺牲阳极的阴极保护法保护效果好。
(5)金属越活泼,就越容易失去电子而被腐蚀,金属活动顺序表中位于氢前面和氢后面的金属都能发生吸氧
腐蚀,但只有在金属活动顺序表中氢前面的金属才可能发生析氢腐蚀。
知识点四 电化学有关计算
1.计算依据——三个相等
(1)同一原电池的正、负极的电极反应得、失电子数相等。
(2)同一电解池的阴极、阳极电极反应中得、失电子数相等。
(3)串联电路中的各个电极反应得、失电子数相等。
上述三种情况下,在写电极反应式时,得、失电子数要相等,在计算电解产物的量时,应按得、失电子数
相等计算。
2.计算方法——三种常用方法
(1)根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
(2)根据电子守恒计算
①用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电子数
相等。
②用于混合溶液中分阶段电解的计算。
(3)根据关系式计算
根据得失电子守恒定律建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
如以通过4mole-为桥梁可构建如下关系式:4
⏟2Cl (Br 、I )~O ~2H ~2Cu~4Ag~ M
4e-~ 2 2 2 2 ⏟2 n
阳极产物
阴极产物
(式中M为金属,n为其离子的化合价数值)
该关系式具有总揽电化学计算的作用和价值,熟记电极反应,灵活运用关系式便能快速解答常见的电化学计
算问题。
提示:在电化学计算中,还常利用Q=I·t和Q=n(e-)×N ×1.60×10-19C来计算电路中通过的电量。
A
第三部分:典型例题剖析
高频考点1 考查电解规律及电极产物的判断
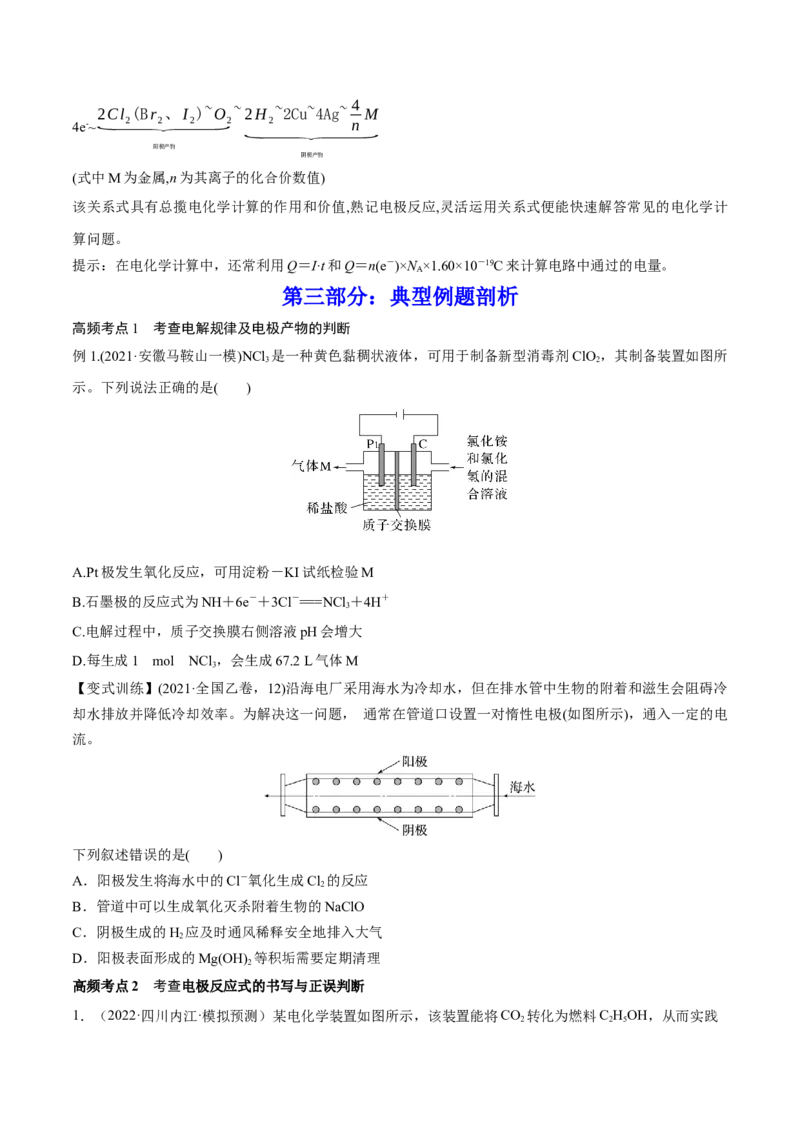
例1.(2021·安徽马鞍山一模)NCl 是一种黄色黏稠状液体,可用于制备新型消毒剂ClO ,其制备装置如图所
3 2
示。下列说法正确的是( )
A.Pt极发生氧化反应,可用淀粉-KI试纸检验M
B.石墨极的反应式为NH+6e-+3Cl-===NCl +4H+
3
C.电解过程中,质子交换膜右侧溶液pH会增大
D.每生成1 mol NCl ,会生成67.2 L气体M
3
【变式训练】(2021·全国乙卷,12)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷
却水排放并降低冷却效率。为解决这一问题, 通常在管道口设置一对惰性电极(如图所示),通入一定的电
流。
下列叙述错误的是( )
A.阳极发生将海水中的Cl-氧化生成Cl 的反应
2
B.管道中可以生成氧化灭杀附着生物的NaClO
C.阴极生成的H 应及时通风稀释安全地排入大气
2
D.阳极表面形成的Mg(OH) 等积垢需要定期清理
2
高频考点2 考查电极反应式的书写与正误判断
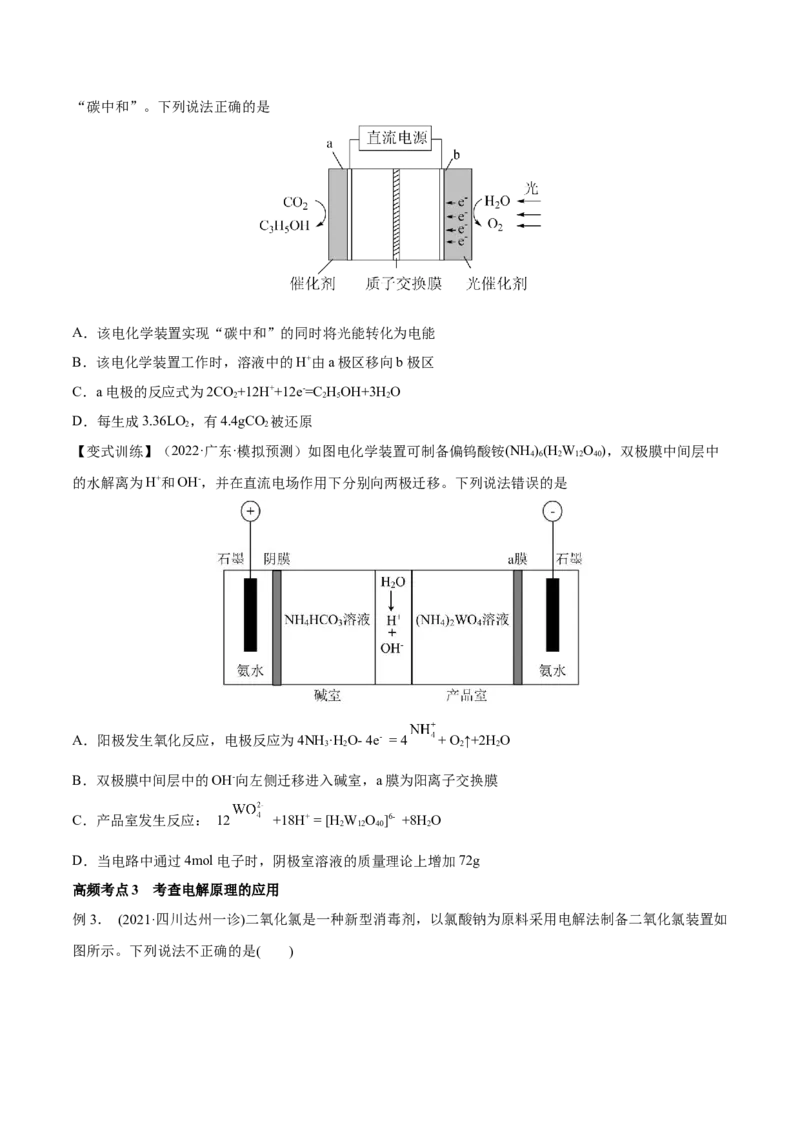
1.(2022·四川内江·模拟预测)某电化学装置如图所示,该装置能将CO 转化为燃料C HOH,从而实践
2 2 5“碳中和”。下列说法正确的是
A.该电化学装置实现“碳中和”的同时将光能转化为电能
B.该电化学装置工作时,溶液中的H+由a极区移向b极区
C.a电极的反应式为2CO+12H++12e-=C HOH+3H O
2 2 5 2
D.每生成3.36LO ,有4.4gCO 被还原
2 2
【变式训练】(2022·广东·模拟预测)如图电化学装置可制备偏钨酸铵(NH )(H W O ),双极膜中间层中
4 6 2 12 40
的水解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法错误的是
A.阳极发生氧化反应,电极反应为4NH ·H O- 4e- = 4 + O ↑+2H O
3 2 2 2
B.双极膜中间层中的OH-向左侧迁移进入碱室,a膜为阳离子交换膜
C.产品室发生反应: 12 +18H+ = [H W O ]6- +8H O
2 12 40 2
D.当电路中通过4mol电子时,阴极室溶液的质量理论上增加72g
高频考点3 考查电解原理的应用
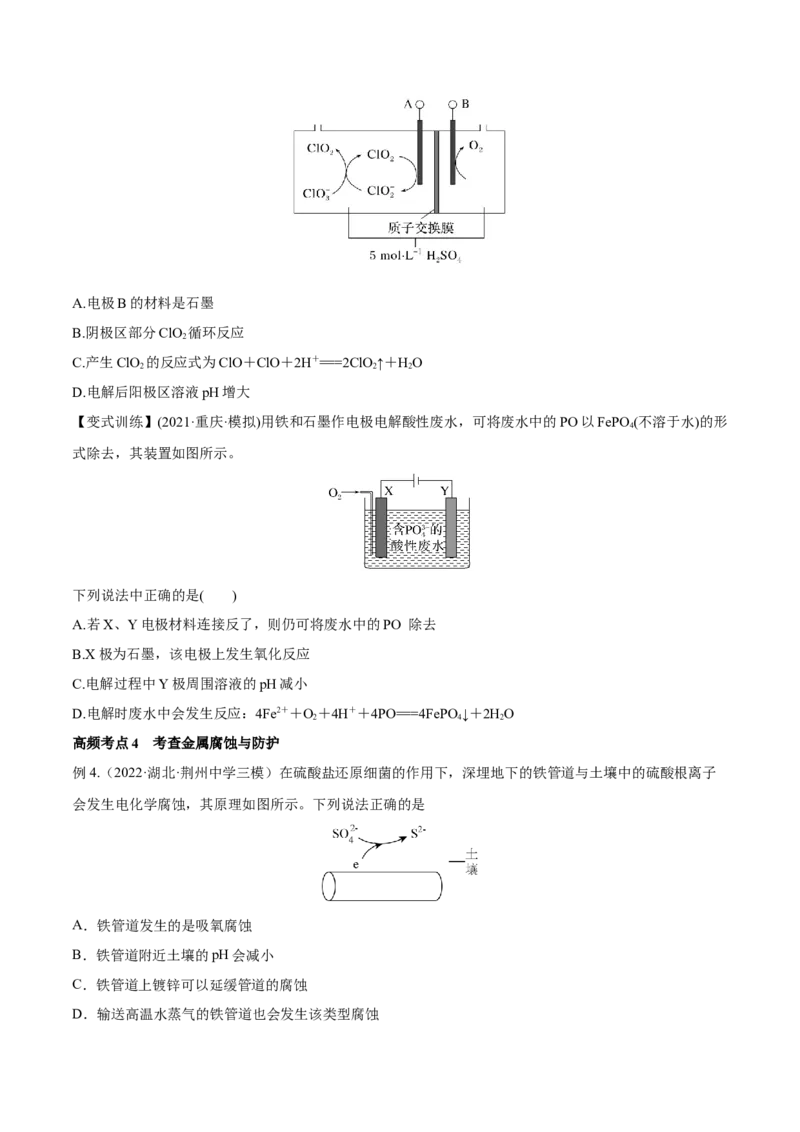
例3. (2021·四川达州一诊)二氧化氯是一种新型消毒剂,以氯酸钠为原料采用电解法制备二氧化氯装置如
图所示。下列说法不正确的是( )A.电极B的材料是石墨
B.阴极区部分ClO 循环反应
2
C.产生ClO 的反应式为ClO+ClO+2H+===2ClO ↑+HO
2 2 2
D.电解后阳极区溶液pH增大
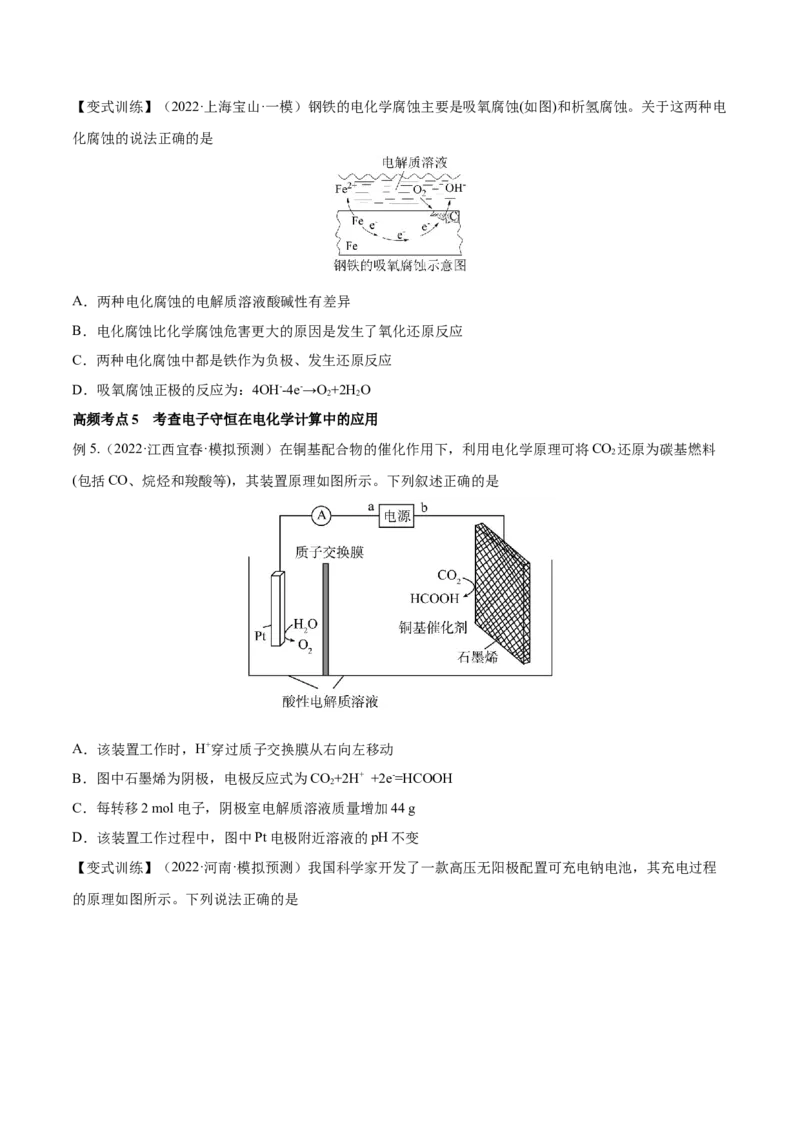
【变式训练】(2021·重庆·模拟)用铁和石墨作电极电解酸性废水,可将废水中的PO以FePO (不溶于水)的形
4
式除去,其装置如图所示。
下列说法中正确的是( )
A.若X、Y电极材料连接反了,则仍可将废水中的PO 除去
B.X极为石墨,该电极上发生氧化反应
C.电解过程中Y极周围溶液的pH减小
D.电解时废水中会发生反应:4Fe2++O+4H++4PO===4FePO↓+2HO
2 4 2
高频考点4 考查金属腐蚀与防护
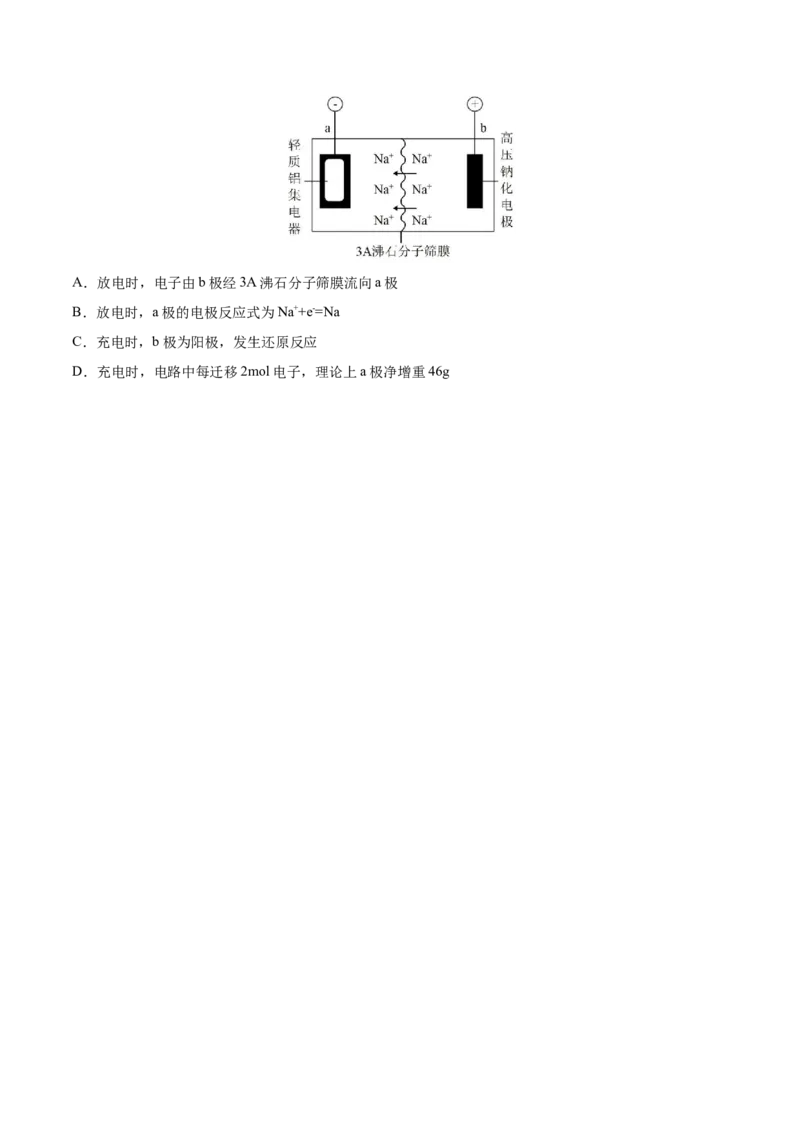
例4.(2022·湖北·荆州中学三模)在硫酸盐还原细菌的作用下,深埋地下的铁管道与土壤中的硫酸根离子
会发生电化学腐蚀,其原理如图所示。下列说法正确的是
A.铁管道发生的是吸氧腐蚀
B.铁管道附近土壤的pH会减小
C.铁管道上镀锌可以延缓管道的腐蚀
D.输送高温水蒸气的铁管道也会发生该类型腐蚀【变式训练】(2022·上海宝山·一模)钢铁的电化学腐蚀主要是吸氧腐蚀(如图)和析氢腐蚀。关于这两种电
化腐蚀的说法正确的是
A.两种电化腐蚀的电解质溶液酸碱性有差异
B.电化腐蚀比化学腐蚀危害更大的原因是发生了氧化还原反应
C.两种电化腐蚀中都是铁作为负极、发生还原反应
D.吸氧腐蚀正极的反应为:4OH--4e-→O+2H O
2 2
高频考点5 考查电子守恒在电化学计算中的应用
例5.(2022·江西宜春·模拟预测)在铜基配合物的催化作用下,利用电化学原理可将CO 还原为碳基燃料
2
(包括CO、烷烃和羧酸等),其装置原理如图所示。下列叙述正确的是
A.该装置工作时,H+穿过质子交换膜从右向左移动
B.图中石墨烯为阴极,电极反应式为CO+2H+ +2e-=HCOOH
2
C.每转移2 mol电子,阴极室电解质溶液质量增加44 g
D.该装置工作过程中,图中Pt电极附近溶液的pH不变
【变式训练】(2022·河南·模拟预测)我国科学家开发了一款高压无阳极配置可充电钠电池,其充电过程
的原理如图所示。下列说法正确的是A.放电时,电子由b极经3A沸石分子筛膜流向a极
B.放电时,a极的电极反应式为Na++e-=Na
C.充电时,b极为阳极,发生还原反应
D.充电时,电路中每迁移2mol电子,理论上a极净增重46g