文档内容
[复习目标] 1.掌握化工流程中条件的控制。2.掌握化工流程中物质的分离和提纯。3.掌握化
工流程中方程式的书写。4.掌握化工流程中的有关计算。
1.(2022·全国乙卷,26)废旧铅蓄电池的铅膏中主要含有PbSO 、PbO 、PbO和Pb,还有少
4 2
量Ba、Fe、Al的盐或氧化物等,为了保护环境、充分利用铅资源,通过下图流程实现铅的
回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质 PbSO PbCO BaSO BaCO
4 3 4 3
K 2.5×10-8 7.4×10-14 1.1×10-10 2.6×10-9
sp
一定条件下,一些金属氢氧化物沉淀时的pH如下表:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH) Pb(OH)
3 2 3 2
开始沉淀的pH 2.3 6.8 3.5 7.2
完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:
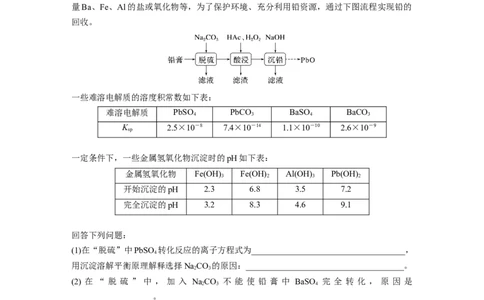
(1)在“脱硫”中PbSO 转化反应的离子方程式为____________________________________,
4
用沉淀溶解平衡原理解释选择NaCO 的原因:_____________________________________。
2 3
(2) 在 “ 脱 硫 ” 中 , 加 入 NaCO 不 能 使 铅 膏 中 BaSO 完 全 转 化 , 原 因 是
2 3 4
___________________。
(3)在“酸浸”中,除加入醋酸(HAc),还要加入HO。
2 2
(ⅰ)能被HO 氧化的离子是_______________________________________________________;
2 2
(ⅱ)H O 促进了金属Pb在醋酸中转化为Pb(Ac) ,其化学方程式为______________________;
2 2 2
(ⅲ)H O 也能使PbO 转化为Pb(Ac) ,HO 的作用是_________________________________。
2 2 2 2 2 2
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是________________。
(5)“沉铅”的滤液中,金属离子有__________。
2.(2022·湖南,17)钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为
TiO,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
2已知“降温收尘”后,粗TiCl 中含有的几种物质的沸点:
4
物质 TiCl VOCl SiCl AlCl
4 3 4 3
沸点/℃ 136 127 57 180
回答下列问题:
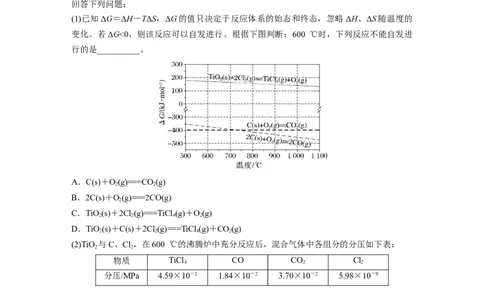
(1)已知ΔG=ΔH-TΔS,ΔG的值只决定于反应体系的始态和终态,忽略ΔH、ΔS随温度的
变化。若ΔG<0,则该反应可以自发进行。根据下图判断:600 ℃时,下列反应不能自发进
行的是__________。
A.C(s)+O(g)===CO(g)
2 2
B.2C(s)+O(g)===2CO(g)
2
C.TiO(s)+2Cl(g)===TiCl (g)+O(g)
2 2 4 2
D.TiO(s)+C(s)+2Cl(g)===TiCl (g)+CO(g)
2 2 4 2
(2)TiO 与C、Cl,在600 ℃的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
2 2
物质 TiCl CO CO Cl
4 2 2
分压/MPa 4.59×10-2 1.84×10-2 3.70×10-2 5.98×10-9
①该温度下,TiO 与C、Cl 反应的总化学方程式为________________________________。
2 2
②随着温度升高,尾气中CO的含量升高,原因是____________________________________。
(3)“除钒”过程中的化学方程式为________________________________________________;
“除硅、铝”过程中,分离TiCl 中含Si、Al杂质的方法是___________________________。
4
(4)“除钒”和“除硅、铝”的顺序______(填“能”或“不能”)交换,理由是
______________
_______________________________________________________________________________
。
(5)下列金属冶炼方法与本工艺流程中加入Mg冶炼Ti的方法相似的是______。A.高炉炼铁
B.电解熔融氯化钠制钠
C.铝热反应制锰
D.氧化汞分解制汞
化工流程题主要考查考生运用化学反应原理及相关知识来解决化工生产中实际问题的能
力,具有考查知识面广、综合性强、思维容量大的特点。工艺流程题设问的地方有:反应速
率与平衡理论的运用,氧化还原反应的判断、化学方程式的书写,利用控制pH分离除杂,
利用溶解度分离,常用的分离方法、实验操作,流程中的物质转化和循环,绿色化学评价,
电化学,计算产量、产率、产品纯度等。这类题型不但综合考查考生在中学阶段所学的元素
及其化合物知识以及物质结构、元素周期律、氧化还原反应、化学用语、电解质溶液、化学
平衡、电化学、实验操作等知识,而且更重要的是能突出考查考生的综合分析判断能力、逻
辑推理能力,且这类试题陌生度高,文字量大,包含信息多,思维能力要求高,近年来已成
为高考化学主观题中的必考题型。
考点一 化工流程中反应条件的控制
1.三氧化二镍(NiO)是重要的电子元件材料和蓄电池材料,工业上利用含镍废料(主要成分
2 3
为镍、铝、氧化铁、碳等)提取Ni O,工业流程如图:
2 3
“预处理”操作可以选择用________(填字母)来除去废旧镍电池表面的矿物油污。
A.纯碱溶液浸泡
B.NaOH溶液浸泡
C.酒精清洗
2.一种从铜阳极泥(主要含有铜、银、金、少量的镍)中分离提取多种金属元素的工艺流程如
下:
“分铜”时,如果反应温度过高,会有明显的放出气体现象,原因是________________________________________________________________________________________________。
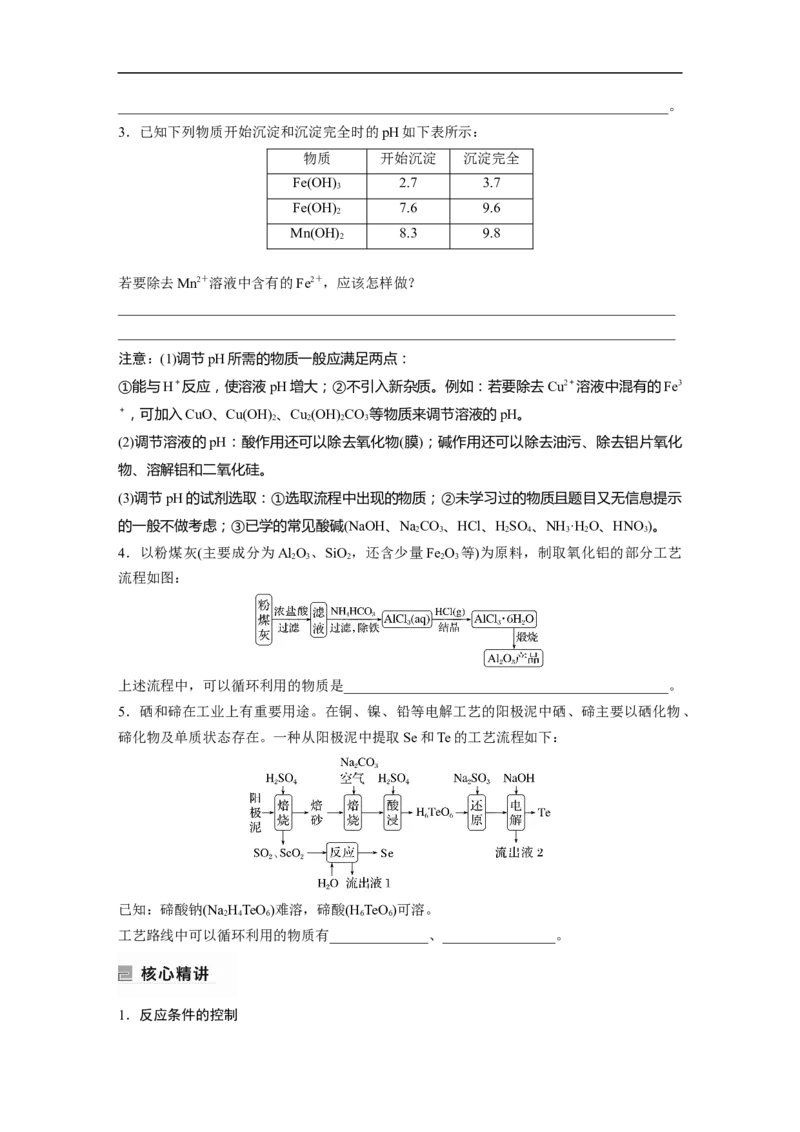
3.已知下列物质开始沉淀和沉淀完全时的pH如下表所示:
物质 开始沉淀 沉淀完全
Fe(OH) 2.7 3.7
3
Fe(OH) 7.6 9.6
2
Mn(OH) 8.3 9.8
2
若要除去Mn2+溶液中含有的Fe2+,应该怎样做?
_______________________________________________________________________________
_______________________________________________________________________________
注意:(1)调节pH所需的物质一般应满足两点:
①能与H+反应,使溶液pH增大;②不引入新杂质。例如:若要除去Cu2+溶液中混有的Fe3
+,可加入CuO、Cu(OH) 、Cu (OH) CO 等物质来调节溶液的pH。
2 2 2 3
(2)调节溶液的pH:酸作用还可以除去氧化物(膜);碱作用还可以除去油污、除去铝片氧化
物、溶解铝和二氧化硅。
(3)调节pH的试剂选取:①选取流程中出现的物质;②未学习过的物质且题目又无信息提示
的一般不做考虑;③已学的常见酸碱(NaOH、NaCO、HCl、HSO 、NH ·H O、HNO)。
2 3 2 4 3 2 3
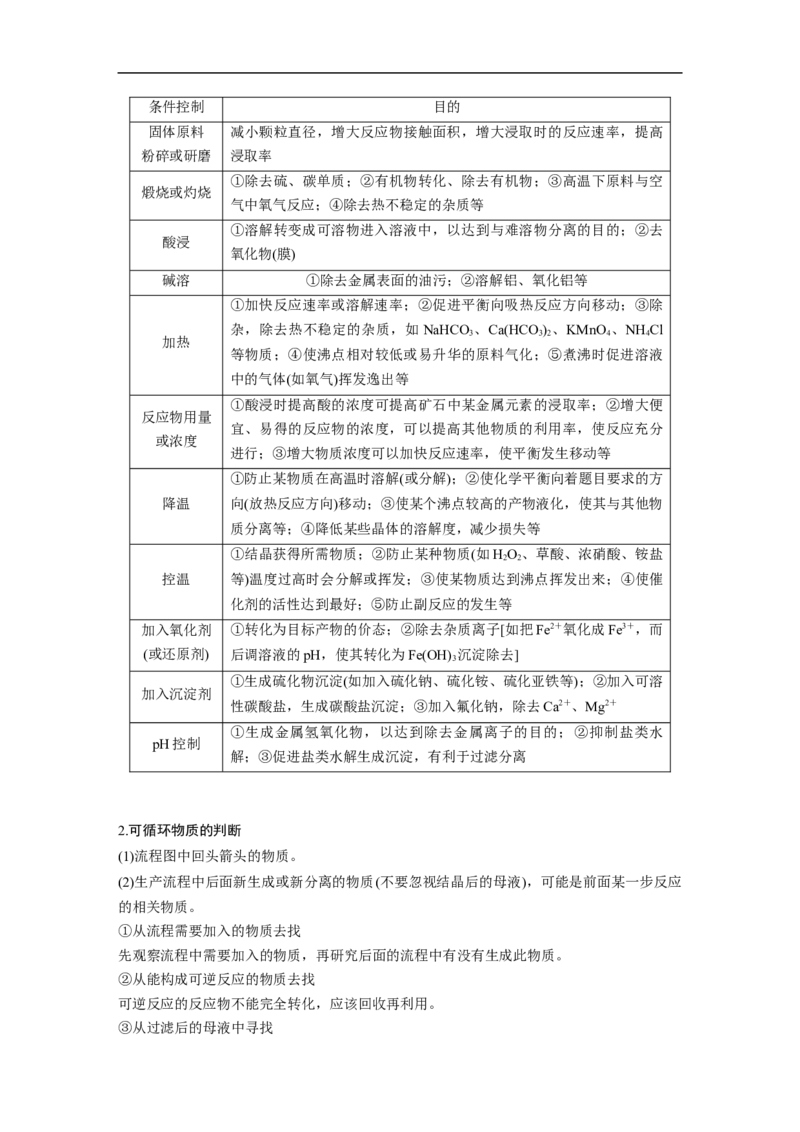
4.以粉煤灰(主要成分为Al O 、SiO ,还含少量Fe O 等)为原料,制取氧化铝的部分工艺
2 3 2 2 3
流程如图:
上述流程中,可以循环利用的物质是______________________________________________。
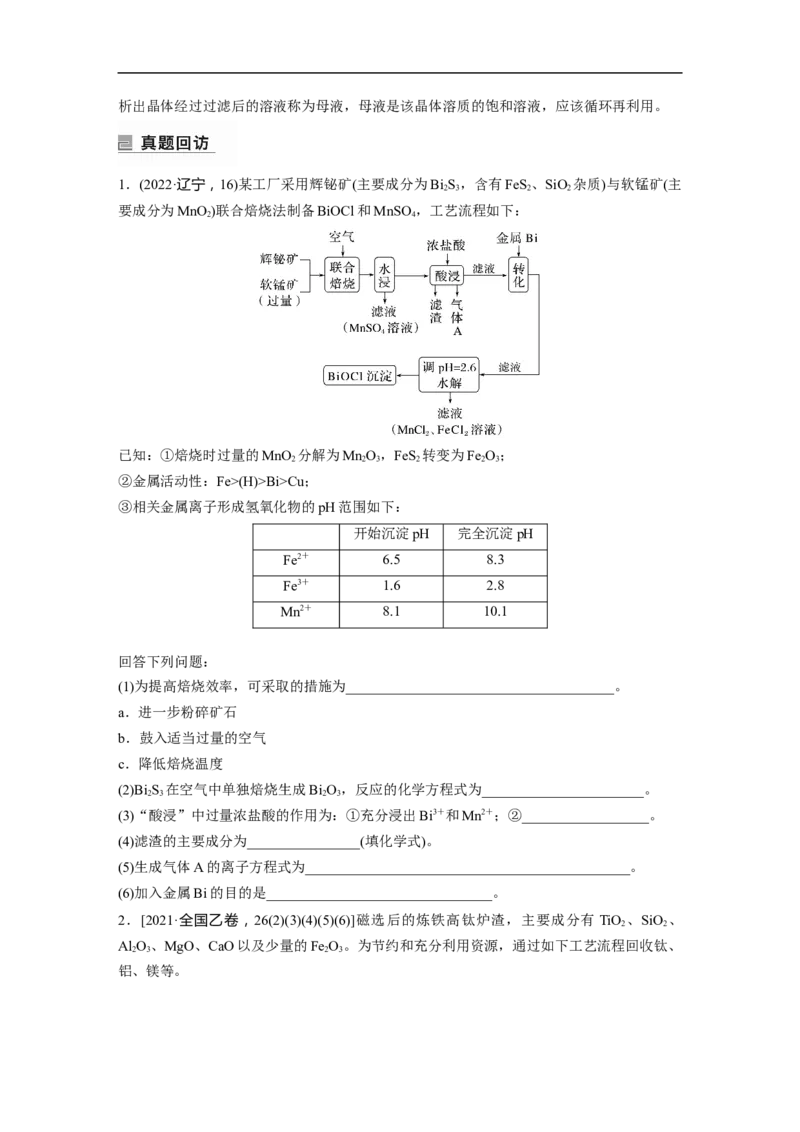
5.硒和碲在工业上有重要用途。在铜、镍、铅等电解工艺的阳极泥中硒、碲主要以硒化物、
碲化物及单质状态存在。一种从阳极泥中提取Se和Te的工艺流程如下:
已知:碲酸钠(Na HTeO )难溶,碲酸(H TeO )可溶。
2 4 6 6 6
工艺路线中可以循环利用的物质有______________、________________。
1.反应条件的控制条件控制 目的
固体原料 减小颗粒直径,增大反应物接触面积,增大浸取时的反应速率,提高
粉碎或研磨 浸取率
①除去硫、碳单质;②有机物转化、除去有机物;③高温下原料与空
煅烧或灼烧
气中氧气反应;④除去热不稳定的杂质等
①溶解转变成可溶物进入溶液中,以达到与难溶物分离的目的;②去
酸浸
氧化物(膜)
碱溶 ①除去金属表面的油污;②溶解铝、氧化铝等
①加快反应速率或溶解速率;②促进平衡向吸热反应方向移动;③除
杂,除去热不稳定的杂质,如NaHCO 、Ca(HCO ) 、KMnO 、NH Cl
3 3 2 4 4
加热
等物质;④使沸点相对较低或易升华的原料气化;⑤煮沸时促进溶液
中的气体(如氧气)挥发逸出等
①酸浸时提高酸的浓度可提高矿石中某金属元素的浸取率;②增大便
反应物用量
宜、易得的反应物的浓度,可以提高其他物质的利用率,使反应充分
或浓度
进行;③增大物质浓度可以加快反应速率,使平衡发生移动等
①防止某物质在高温时溶解(或分解);②使化学平衡向着题目要求的方
降温 向(放热反应方向)移动;③使某个沸点较高的产物液化,使其与其他物
质分离等;④降低某些晶体的溶解度,减少损失等
①结晶获得所需物质;②防止某种物质(如HO 、草酸、浓硝酸、铵盐
2 2
控温 等)温度过高时会分解或挥发;③使某物质达到沸点挥发出来;④使催
化剂的活性达到最好;⑤防止副反应的发生等
加入氧化剂 ①转化为目标产物的价态;②除去杂质离子[如把Fe2+氧化成Fe3+,而
(或还原剂) 后调溶液的pH,使其转化为Fe(OH) 沉淀除去]
3
①生成硫化物沉淀(如加入硫化钠、硫化铵、硫化亚铁等);②加入可溶
加入沉淀剂
性碳酸盐,生成碳酸盐沉淀;③加入氟化钠,除去Ca2+、Mg2+
①生成金属氢氧化物,以达到除去金属离子的目的;②抑制盐类水
pH控制
解;③促进盐类水解生成沉淀,有利于过滤分离
2.可循环物质的判断
(1)流程图中回头箭头的物质。
(2)生产流程中后面新生成或新分离的物质(不要忽视结晶后的母液),可能是前面某一步反应
的相关物质。
①从流程需要加入的物质去找
先观察流程中需要加入的物质,再研究后面的流程中有没有生成此物质。
②从能构成可逆反应的物质去找
可逆反应的反应物不能完全转化,应该回收再利用。
③从过滤后的母液中寻找析出晶体经过过滤后的溶液称为母液,母液是该晶体溶质的饱和溶液,应该循环再利用。
1.(2022·辽宁,16)某工厂采用辉铋矿(主要成分为BiS ,含有FeS 、SiO 杂质)与软锰矿(主
2 3 2 2
要成分为MnO )联合焙烧法制备BiOCl和MnSO ,工艺流程如下:
2 4
已知:①焙烧时过量的MnO 分解为MnO,FeS 转变为Fe O;
2 2 3 2 2 3
②金属活动性:Fe>(H)>Bi>Cu;
③相关金属离子形成氢氧化物的pH范围如下:
开始沉淀pH 完全沉淀pH
Fe2+ 6.5 8.3
Fe3+ 1.6 2.8
Mn2+ 8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为______________________________________。
a.进一步粉碎矿石
b.鼓入适当过量的空气
c.降低焙烧温度
(2)Bi S 在空气中单独焙烧生成BiO,反应的化学方程式为_______________________。
2 3 2 3
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出Bi3+和Mn2+;②__________________。
(4)滤渣的主要成分为________________(填化学式)。
(5)生成气体A的离子方程式为______________________________________________。
(6)加入金属Bi的目的是________________________________。
2.[2021·全国乙卷,26(2)(3)(4)(5)(6)]磁选后的炼铁高钛炉渣,主要成分有 TiO 、SiO 、
2 2
Al O 、MgO、CaO以及少量的Fe O 。为节约和充分利用资源,通过如下工艺流程回收钛、
2 3 2 3
铝、镁等。该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8
回答下列问题:
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,依次
析出的金属离子是__________________________。
(3)“母液①”中Mg2+浓度为______ mol·L-1。
(4)“水浸渣”在 160 ℃“酸溶”,最适合的酸是____________,“酸溶渣”的成分是
________________________________________________________________________。
(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO·xHO沉淀,该反应的离子方
2 2
程式是________________________________________________________________________。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得____________,循环利用。
1.研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回
收工艺的流程如下:
回答下列问题:
(1)反应釜中,溶液的pH、温度(T)与生成沉淀的关系如图,图中区域分别表示铁的化合物稳
定存在的区域。则制备FeOOH适宜的pH和温度分别为________(填字母)。a.2,80 ℃ b.4,90 ℃
c.5,160 ℃ d.6,25 ℃
(2)制备磁性纳米铁棒时,加入NaBH 前先通入N 的作用是________________________。
4 2
(3)常温下,若在含Cd2+、Te4+滤液中加入NaOH溶液调节pH为7,溶液中c(Cd2+)的最大值
为________________________________________________________________________(已知:
K [Cd(OH) ]=5.3×10-15)。
sp 2
(4)从TeO溶液得到“吸附Te”,利用了纳米铁棒的性质有________、________。
2.(1)随着钴酸锂电池的普及使用,从废旧的钴酸锂电池中提取锂、钴等金属材料意义重大。
下图是废旧钴酸锂电池材料(主要成分为LiCoO ,含少量铁、铝、铜等元素的化合物)回收工
2
艺流程:
①“拆解”前需进行“放电”处理的目的是______________________________________。
用食盐水浸泡是放电的常用方法,浸泡放电过程中产生的气体主要有________。
②滤液1中加入NaSO 的主要目的是__________________________________;加入NaClO
2 3 3
的主要目的是_____________________________________。
③“沉钴”过程中,(NH )C O 的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系
4 2 2 4
如图所示:
根据图分析:沉钴时应控制n(C O)∶n(Co2+)为______,温度控制在______℃左右。
2(2)碱式硫酸铝[(1-x)Al(SO )·xAl(OH) ]溶液可用于烟气脱硫。实验室用粉煤灰(主要含
2 4 3 3
Al O、SiO 等)制备碱式硫酸铝溶液,实验流程如下:
2 3 2
已知“调pH”的反应为(2-x)Al(SO ) +3xCaCO +3xHO===2[(1-x)Al(SO )·xAl(OH) ]+
2 4 3 3 2 2 4 3 3
3xCaSO+3xCO↑。
4 2
①“酸浸”时适当增大HSO 溶液浓度的目的是______________________,能达到相同目的
2 4
的方法还有________________________________________(任写一种)。
②“酸浸”时应控制 HSO 溶液的用量,HSO 溶液用量不能过量太多的原因是
2 4 2 4
___________
_______________________________________________________________________________
。
(3)亚氯酸钠(NaClO)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等。以氯酸钠等
2
为原料制备亚氯酸钠的工艺流程如下:
①提高“反应1”反应速率的措施有____________________________________________(答
出一条即可)。母液中溶质的主要成分是_________________________(填化学式)。
②采取“减压蒸发”而不用“常压蒸发”,原因是_______________________________。
③“反应2”中使用HO 而不用其他物质的原因是_________________________________。
2 2
考点二 化工流程中物质的分离与提纯
1.过滤(分离固、液混合物)
从工厂采集废液(含FeSO 和少量ZnSO 、MgSO ),进行四氧化三铁的制备实验。制备流程
4 4 4
如图所示:操作a、b的名称分别为________________________________。
2.萃取法分离
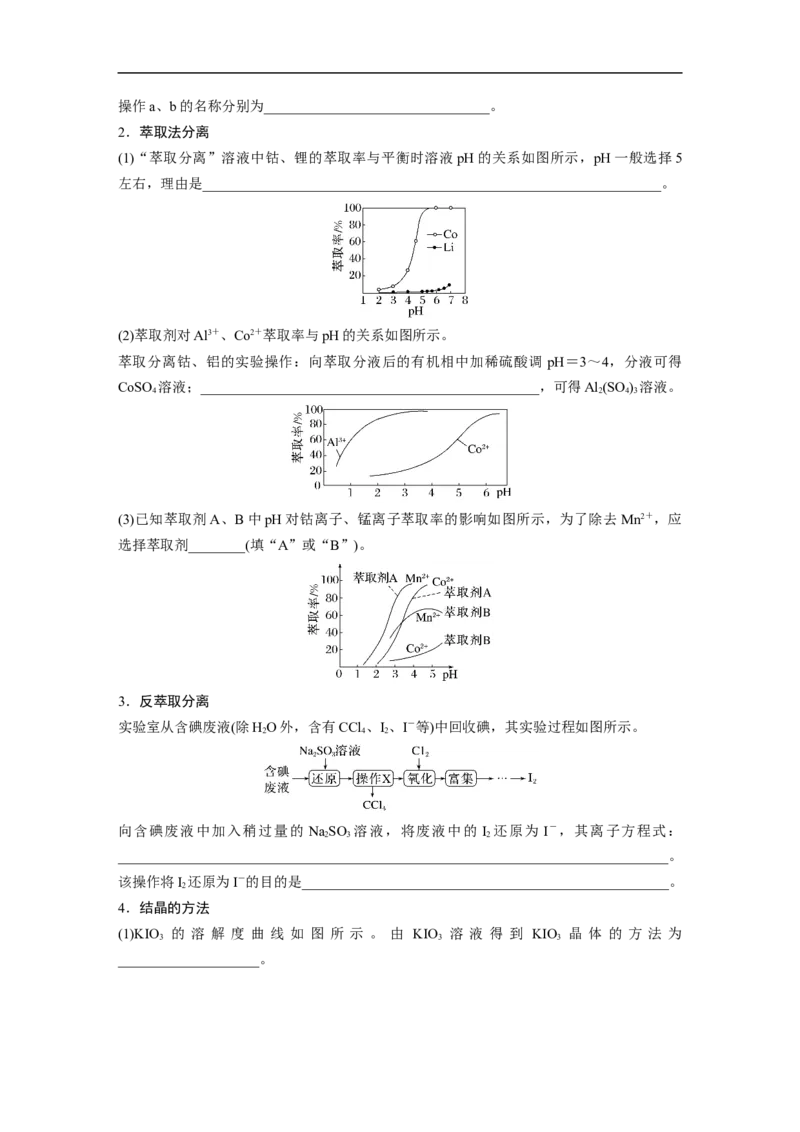
(1)“萃取分离”溶液中钴、锂的萃取率与平衡时溶液pH的关系如图所示,pH一般选择5
左右,理由是_________________________________________________________________。
(2)萃取剂对Al3+、Co2+萃取率与pH的关系如图所示。
萃取分离钴、铝的实验操作:向萃取分液后的有机相中加稀硫酸调 pH=3~4,分液可得
CoSO 溶液;________________________________________________,可得Al (SO ) 溶液。
4 2 4 3
(3)已知萃取剂A、B中pH对钴离子、锰离子萃取率的影响如图所示,为了除去 Mn2+,应
选择萃取剂________(填“A”或“B”)。
3.反萃取分离
实验室从含碘废液(除HO外,含有CCl 、I、I-等)中回收碘,其实验过程如图所示。
2 4 2
向含碘废液中加入稍过量的 NaSO 溶液,将废液中的 I 还原为 I-,其离子方程式:
2 3 2
______________________________________________________________________________。
该操作将I 还原为I-的目的是____________________________________________________。
2
4.结晶的方法
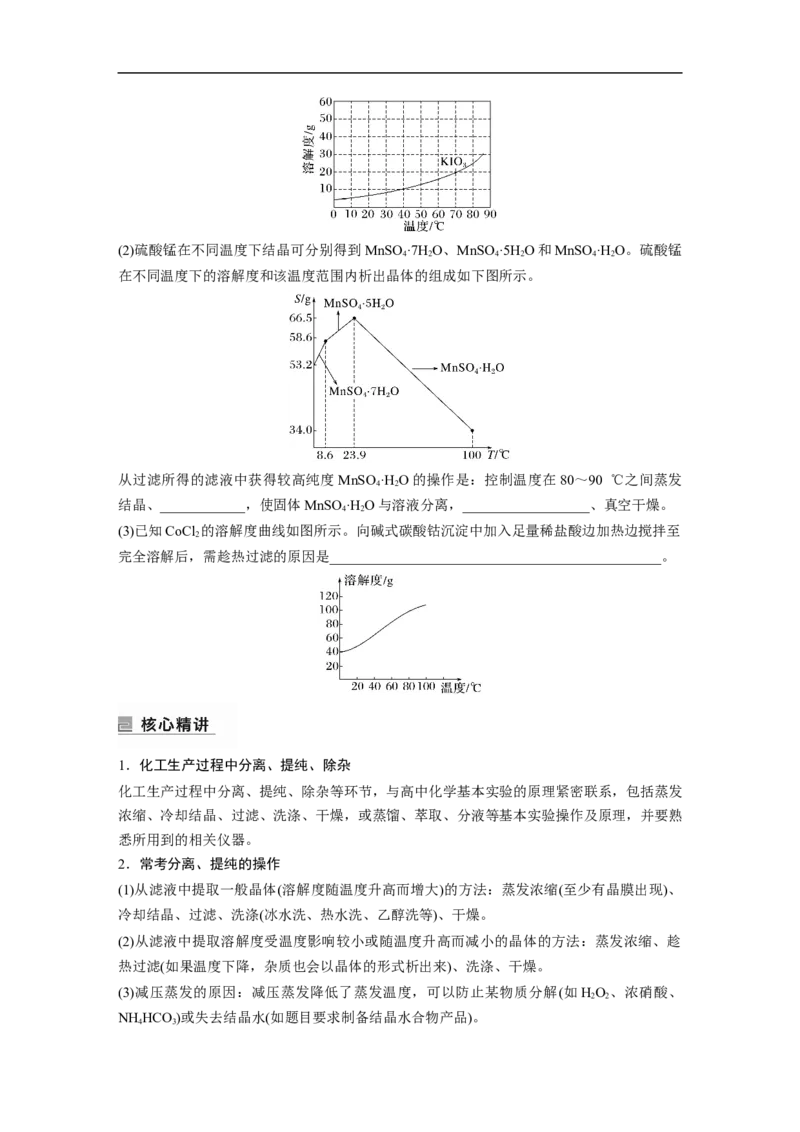
(1)KIO 的 溶 解 度 曲 线 如 图 所 示 。 由 KIO 溶 液 得 到 KIO 晶 体 的 方 法 为
3 3 3
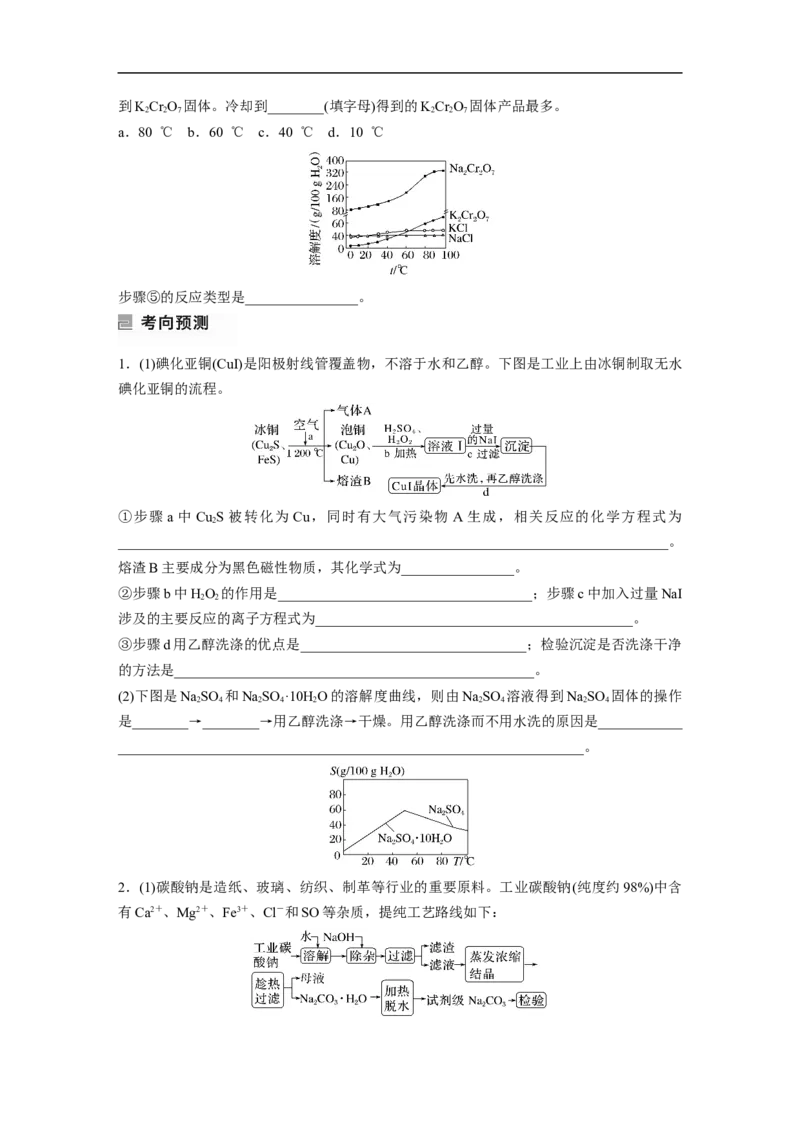
____________________。(2)硫酸锰在不同温度下结晶可分别得到MnSO ·7H O、MnSO ·5H O和MnSO ·H O。硫酸锰
4 2 4 2 4 2
在不同温度下的溶解度和该温度范围内析出晶体的组成如下图所示。
从过滤所得的滤液中获得较高纯度MnSO ·H O的操作是:控制温度在80~90 ℃之间蒸发
4 2
结晶、____________,使固体MnSO ·H O与溶液分离,__________________、真空干燥。
4 2
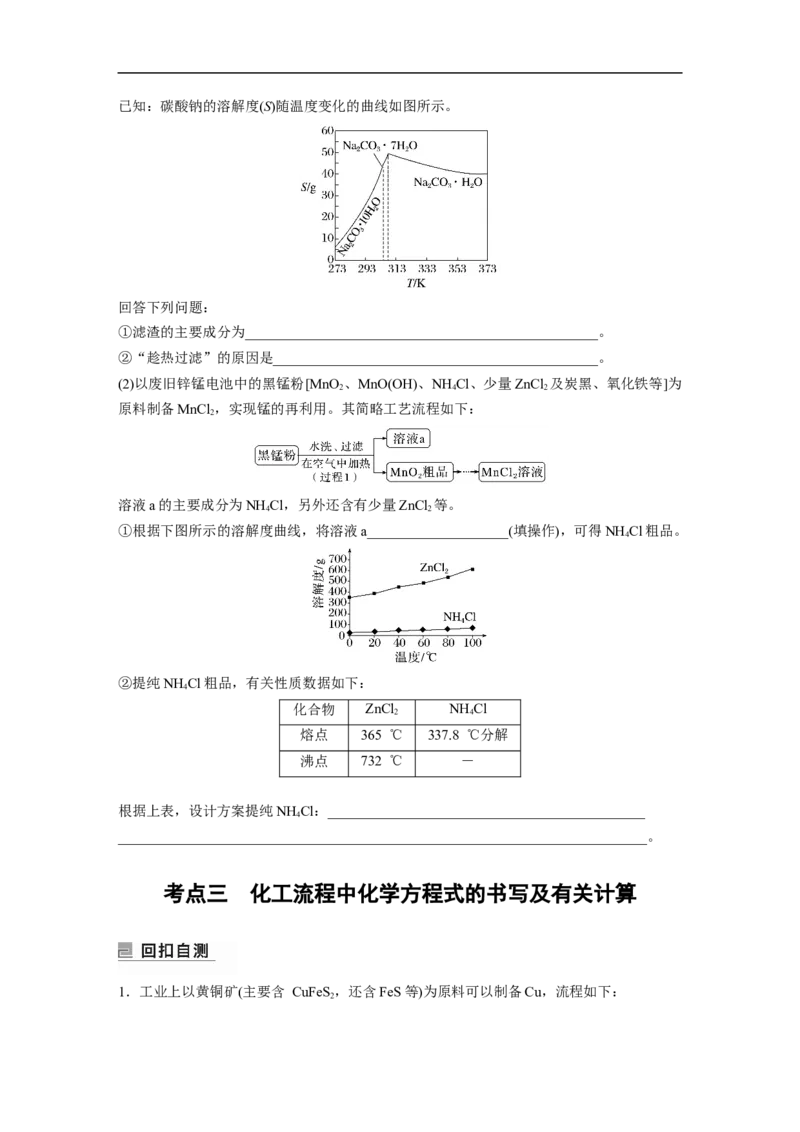
(3)已知CoCl 的溶解度曲线如图所示。向碱式碳酸钴沉淀中加入足量稀盐酸边加热边搅拌至
2
完全溶解后,需趁热过滤的原因是_______________________________________________。
1.化工生产过程中分离、提纯、除杂
化工生产过程中分离、提纯、除杂等环节,与高中化学基本实验的原理紧密联系,包括蒸发
浓缩、冷却结晶、过滤、洗涤、干燥,或蒸馏、萃取、分液等基本实验操作及原理,并要熟
悉所用到的相关仪器。
2.常考分离、提纯的操作
(1)从滤液中提取一般晶体(溶解度随温度升高而增大)的方法:蒸发浓缩(至少有晶膜出现)、
冷却结晶、过滤、洗涤(冰水洗、热水洗、乙醇洗等)、干燥。
(2)从滤液中提取溶解度受温度影响较小或随温度升高而减小的晶体的方法:蒸发浓缩、趁
热过滤(如果温度下降,杂质也会以晶体的形式析出来)、洗涤、干燥。
(3)减压蒸发的原因:减压蒸发降低了蒸发温度,可以防止某物质分解(如HO 、浓硝酸、
2 2
NH HCO )或失去结晶水(如题目要求制备结晶水合物产品)。
4 3(4)洗涤
洗涤试剂 适用范围 目的
除去固体表面吸附着的××杂质,可适当
冷水 产物不溶于水
降低固体因为溶解而造成的损失
蒸馏水
有特殊的物质其溶解度 除去固体表面吸附着的××杂质,可适当
热水
随着温度升高而下降 降低固体因为温度变化溶解而造成的损失
有机溶剂(酒精、 固体易溶于水、难溶于 减少固体溶解;利用有机溶剂的挥发性除
丙酮等) 有机溶剂 去固体表面的水分,产品易干燥
饱和溶液 对纯度要求不高的产品 减少固体溶解
除去固体表面吸附着的可溶于酸、碱的杂
酸、碱溶液 产物不溶于酸、碱
质;减少固体溶解
洗涤沉淀的方法:向过滤器中加入蒸馏水至浸没沉淀,待水自然流下后,重复以上操作
2~3次
检验沉淀是否洗涤干净的方法:取少量最后一次的洗涤液于试管中,向其中滴入某试
剂,若未出现特征反应现象,则沉淀洗涤干净
(5)萃取与反萃取
①萃取:利用物质在两种互不相溶的溶剂中的溶解度不同,将物质从一种溶剂转移到另一种
溶剂的过程。如用CCl 萃取溴水中的Br 。
4 2
②反萃取:用反萃取剂使被萃取物从负载有机相返回水相的过程,为萃取的逆过程。
(6)其他
①蒸发时的气体氛围抑制水解:如从溶液中析出 FeCl 、AlCl 、MgCl 等溶质时,应在HCl
3 3 2
的气流中加热,以防其水解。
②减压蒸馏的原因:减小压强,使液体沸点降低,防止受热分解、氧化等。
3.根据溶解度曲线判断结晶的方法
(1)溶解度受温度影响较小的(如NaCl)采取蒸发结晶的方法。
(2)溶解度受温度影响较大的采取蒸发浓缩、冷却结晶的方法。
(3)带有结晶水的盐,一般采取蒸发浓缩、冷却结晶的方法。
[2017·全国卷Ⅲ,27(4)]重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主
要成分为FeO·Cr O,还含有硅、铝等杂质。制备流程如图所示:
2 3
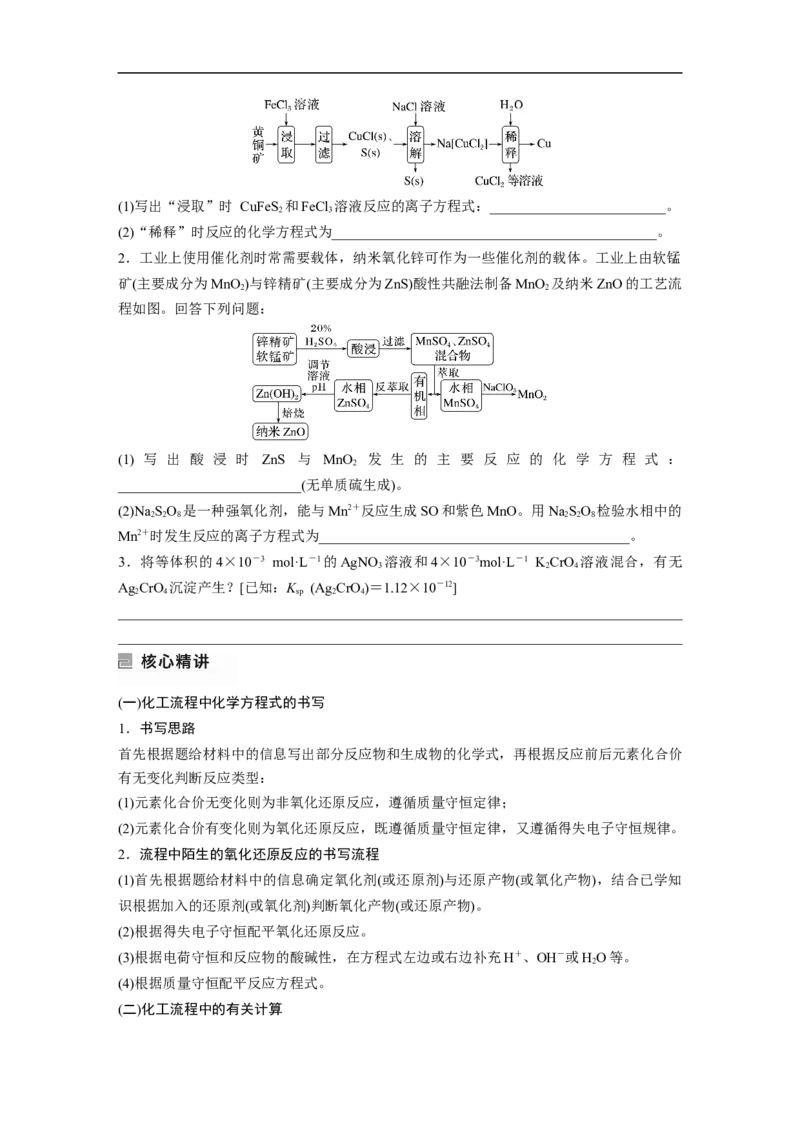
有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到KCr O 固体。冷却到________(填字母)得到的KCr O 固体产品最多。
2 2 7 2 2 7
a.80 ℃ b.60 ℃ c.40 ℃ d.10 ℃
步骤⑤的反应类型是________________。
1.(1)碘化亚铜(CuI)是阳极射线管覆盖物,不溶于水和乙醇。下图是工业上由冰铜制取无水
碘化亚铜的流程。
①步骤 a 中 Cu S 被转化为 Cu,同时有大气污染物 A 生成,相关反应的化学方程式为
2
______________________________________________________________________________。
熔渣B主要成分为黑色磁性物质,其化学式为________________。
②步骤b中HO 的作用是____________________________________;步骤c中加入过量NaI
2 2
涉及的主要反应的离子方程式为_____________________________________________。
③步骤d用乙醇洗涤的优点是________________________________;检验沉淀是否洗涤干净
的方法是___________________________________________________。
(2)下图是NaSO 和NaSO ·10H O的溶解度曲线,则由NaSO 溶液得到NaSO 固体的操作
2 4 2 4 2 2 4 2 4
是________→________→用乙醇洗涤→干燥。用乙醇洗涤而不用水洗的原因是____________
__________________________________________________________________。
2.(1)碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含
有Ca2+、Mg2+、Fe3+、Cl-和SO等杂质,提纯工艺路线如下:已知:碳酸钠的溶解度(S)随温度变化的曲线如图所示。
回答下列问题:
①滤渣的主要成分为__________________________________________________。
②“趁热过滤”的原因是______________________________________________。
(2)以废旧锌锰电池中的黑锰粉[MnO 、MnO(OH)、NH Cl、少量ZnCl 及炭黑、氧化铁等]为
2 4 2
原料制备MnCl ,实现锰的再利用。其简略工艺流程如下:
2
溶液a的主要成分为NH Cl,另外还含有少量ZnCl 等。
4 2
①根据下图所示的溶解度曲线,将溶液a____________________(填操作),可得NH Cl粗品。
4
②提纯NH Cl粗品,有关性质数据如下:
4
化合物 ZnCl NH Cl
2 4
熔点 365 ℃ 337.8 ℃分解
沸点 732 ℃ -
根据上表,设计方案提纯NH Cl:_____________________________________________
4
___________________________________________________________________________。
考点三 化工流程中化学方程式的书写及有关计算
1.工业上以黄铜矿(主要含 CuFeS,还含FeS等)为原料可以制备Cu,流程如下:
2(1)写出“浸取”时 CuFeS 和FeCl 溶液反应的离子方程式:_________________________。
2 3
(2)“稀释”时反应的化学方程式为______________________________________________。
2.工业上使用催化剂时常需要载体,纳米氧化锌可作为一些催化剂的载体。工业上由软锰
矿(主要成分为MnO )与锌精矿(主要成分为ZnS)酸性共融法制备MnO 及纳米ZnO的工艺流
2 2
程如图。回答下列问题:
(1) 写 出 酸 浸 时 ZnS 与 MnO 发 生 的 主 要 反 应 的 化 学 方 程 式 :
2
__________________________(无单质硫生成)。
(2)Na SO 是一种强氧化剂,能与Mn2+反应生成SO和紫色MnO。用NaSO 检验水相中的
2 2 8 2 2 8
Mn2+时发生反应的离子方程式为____________________________________________。
3.将等体积的4×10-3 mol·L-1的AgNO 溶液和4×10-3mol·L-1 KCrO 溶液混合,有无
3 2 4
Ag CrO 沉淀产生?[已知:K (Ag CrO)=1.12×10-12]
2 4 sp 2 4
________________________________________________________________________________
________________________________________________________________________________
(一)化工流程中化学方程式的书写
1.书写思路
首先根据题给材料中的信息写出部分反应物和生成物的化学式,再根据反应前后元素化合价
有无变化判断反应类型:
(1)元素化合价无变化则为非氧化还原反应,遵循质量守恒定律;
(2)元素化合价有变化则为氧化还原反应,既遵循质量守恒定律,又遵循得失电子守恒规律。
2.流程中陌生的氧化还原反应的书写流程
(1)首先根据题给材料中的信息确定氧化剂(或还原剂)与还原产物(或氧化产物),结合已学知
识根据加入的还原剂(或氧化剂)判断氧化产物(或还原产物)。
(2)根据得失电子守恒配平氧化还原反应。
(3)根据电荷守恒和反应物的酸碱性,在方程式左边或右边补充H+、OH-或HO等。
2
(4)根据质量守恒配平反应方程式。
(二)化工流程中的有关计算1.K 计算
sp
(1)判断能否沉淀。
(2)判断能否沉淀完全。
(3)计算某一离子的浓度。
(4)沉淀生成和沉淀完全时pH的计算。
2.产率、纯度的计算
(1)计算公式
纯度=×100%
产物的产率=×100%
(2)计算的关键在于运用守恒或关系式法结合实验原理找到计算的关系,确定数量关系。
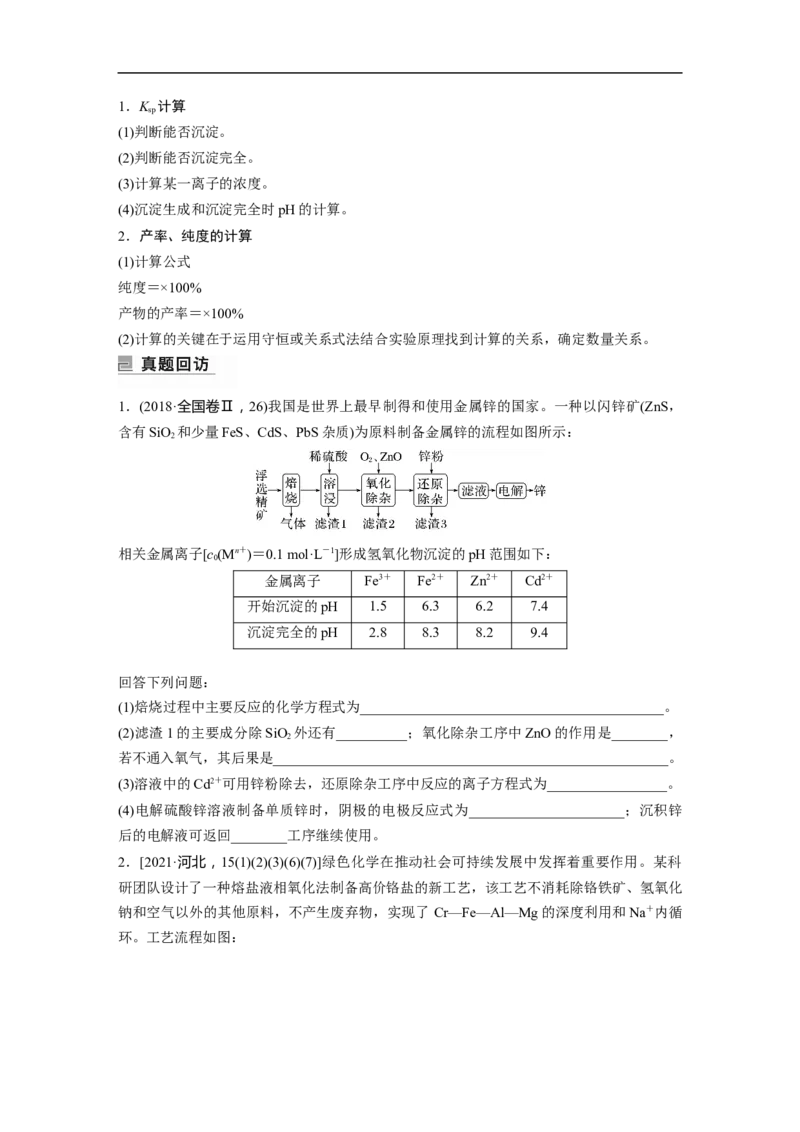
1.(2018·全国卷Ⅱ,26)我国是世界上最早制得和使用金属锌的国家。一种以闪锌矿(ZnS,
含有SiO 和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
2
相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Fe3+ Fe2+ Zn2+ Cd2+
开始沉淀的pH 1.5 6.3 6.2 7.4
沉淀完全的pH 2.8 8.3 8.2 9.4
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为___________________________________________。
(2)滤渣1的主要成分除SiO 外还有__________;氧化除杂工序中ZnO的作用是________,
2
若不通入氧气,其后果是________________________________________________________。
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为_________________。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为______________________;沉积锌
后的电解液可返回________工序继续使用。
2.[2021·河北,15(1)(2)(3)(6)(7)]绿色化学在推动社会可持续发展中发挥着重要作用。某科
研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化
钠和空气以外的其他原料,不产生废弃物,实现了 Cr—Fe—Al—Mg的深度利用和Na+内循
环。工艺流程如图:回答下列问题:
(1)高温连续氧化工序中被氧化的元素是________(填元素符号)。
(2)工序①的名称为____________。
(3)滤渣Ⅰ的主要成分是__________________(填化学式)。
(6)热解工序产生的混合气体最适宜返回工序____________(填“①”“②”“③”或“④”)
参与内循环。
(7)工序④溶液中的铝元素恰好完全转化为沉淀的pH为__________(通常认为溶液中离子浓
度小于10-5 mol·L-1为沉淀完全;Al(OH) +OH-Al(OH) K=100.63;K =10-14,
3 w
K [Al(OH) ]=10-33)。
sp 3
考向一 化工流程中化学方程式的书写
1.(1)利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制
革工业污泥中Cr(Ⅲ)的处理工艺流程如下:
已知:硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
①HO 的作用是将滤液Ⅰ中的Cr3+转化为Cr O,写出此反应的离子方程式:___________
2 2 2
_______________________________________________________________________________
。
②写出上述流程中用SO 进行还原时发生反应的离子方程式:__________________________。
2
(2)ZrO 常用作陶瓷材料,可由锆英砂(主要成分为ZrSiO ,也可表示为ZrO·SiO,还含少量
2 4 2 2
FeCO、Fe O、Al O、SiO 等杂质)通过如下方法制取:
3 2 3 2 3 2已知:ZrSiO 能与烧碱反应生成可溶于水的NaZrO,NaZrO 与酸反应生成ZrO2+。
4 2 3 2 3
①“熔融”过程中,ZrSiO 发生反应的化学方程式为________________________________。
4
②滤渣Ⅲ的成分是Zr(CO)·nZr(OH) 。“调pH=8.0”时,所发生反应的离子方程式为
3 2 4
_______________________________________________________________________________
。
滤渣Ⅲ制备ZrO 的方法是________________________________________________________。
2
考向二 化工流程中的有关计算
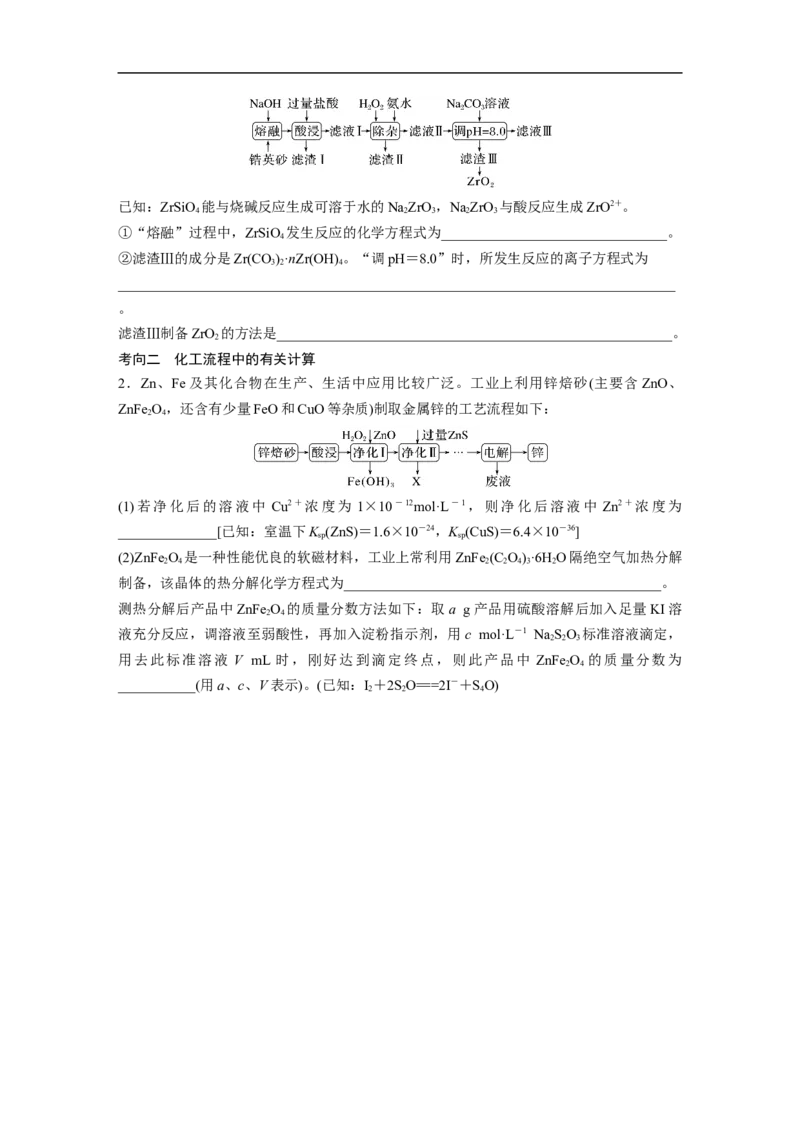
2.Zn、Fe及其化合物在生产、生活中应用比较广泛。工业上利用锌焙砂(主要含ZnO、
ZnFe O,还含有少量FeO和CuO等杂质)制取金属锌的工艺流程如下:
2 4
(1)若净化后的溶液中 Cu2+浓度为 1×10-12mol·L-1,则净化后溶液中 Zn2+浓度为
______________[已知:室温下K (ZnS)=1.6×10-24,K (CuS)=6.4×10-36]
sp sp
(2)ZnFe O 是一种性能优良的软磁材料,工业上常利用ZnFe (C O)·6H O隔绝空气加热分解
2 4 2 2 4 3 2
制备,该晶体的热分解化学方程式为_____________________________________________。
测热分解后产品中ZnFe O 的质量分数方法如下:取a g产品用硫酸溶解后加入足量KI溶
2 4
液充分反应,调溶液至弱酸性,再加入淀粉指示剂,用c mol·L-1 Na SO 标准溶液滴定,
2 2 3
用去此标准溶液 V mL 时,刚好达到滴定终点,则此产品中 ZnFe O 的质量分数为
2 4
___________(用a、c、V表示)。(已知:I+2SO===2I-+SO)
2 2 4