文档内容
第 21 讲 电离平衡
1.下列关于电解质的叙述正确的是( )
A.电解质溶液的浓度越大,其导电性能一定越强
B.强酸和强碱一定是强电解质,不管其水溶液浓度的大小,都能完全电离
C.强极性共价化合物不一定都是强电解质
D.多元酸、多元碱的导电性一定比一元酸、一元碱的导电性强
2.下列事实能证明HCOOH为弱酸的是( )
A.可与NaCO 反应生成CO
2 3 2
B.常温时HCOONa溶液的pH大于7
C.导电能力低于同浓度的硫酸
D.0.1 mol·L-1 HCOOH溶液可以使甲基橙变红
3.将0.1 mol·L-1的氨水加水稀释至0.01 mol·L-1,稀释过程中温度不变,下列叙述正确的是( )
A.稀释后溶液中c(H+)和c(OH-)均减小
B.稀释后溶液中c(OH-)变为稀释前的
C.稀释过程中氨水的电离平衡向左移动
D.稀释过程中溶液中增大
4.HS水溶液中存在电离平衡H S H++HS-和HS- H++S2-。下列说法正确的是( )
2 2
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO 气体,平衡向左移动,溶液pH增大
2
C.滴加新制氯水,平衡向左移动,溶液pH减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
5.稀氨水中存在着电离平衡:NH·HO NH+OH-,若要使平衡向左移动,同时使 c(OH-) 增大,应
3 2
加入的适量物质或采取的措施是( )
①NHCl固体 ②硫酸 ③NaOH固体 ④水 ⑤加热
4
⑥加入少量MgSO 固体
4
A.①②③⑤ B.③⑥
C.③ D.③⑤
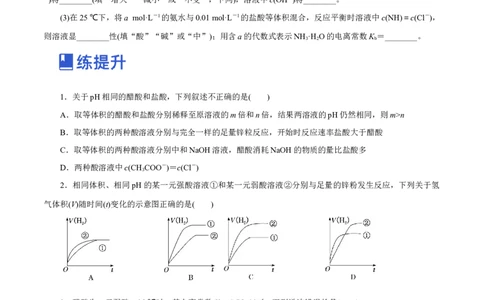
6.常温下,0.2 mol·L-1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示。下列说法正确的是( )
A.HA为强酸
B.该混合溶液pH=7.0
C.该混合溶液中:c(A-)+c(Y)=c(Na+)
D.图中X表示HA,Y表示OH-,Z表示H+
7.已知数据:7.2×10-4、4.6×10-4、4.9×10-10分别是三种酸的电离平衡常数,若已知这些酸可发生如下反
应:
①NaCN+HNO===HCN+NaNO
2 2
②NaCN+HF===HCN+NaF
③NaNO+HF===HNO+NaF
2 2
由此可判断下列叙述中不正确的是( )
A.HF的电离平衡常数为7.2×10-4
B.HNO 的电离平衡常数为4.9×10-10
2
C.根据①③两个反应即可知三种酸的相对强弱
D.HNO 的电离平衡常数比HCN大,比HF小
2
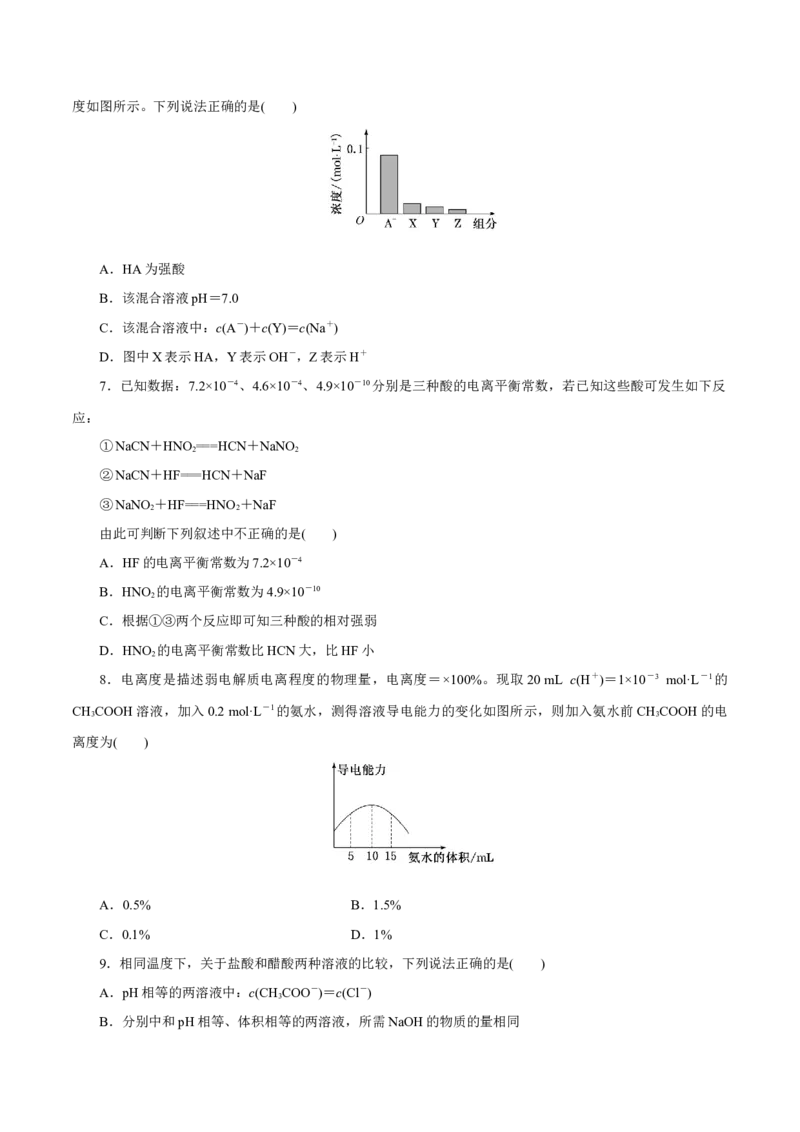
8.电离度是描述弱电解质电离程度的物理量,电离度=×100%。现取20 mL c(H+)=1×10-3 mol·L-1的
CHCOOH溶液,加入0.2 mol·L-1的氨水,测得溶液导电能力的变化如图所示,则加入氨水前CHCOOH的电
3 3
离度为( )
A.0.5% B.1.5%
C.0.1% D.1%
9.相同温度下,关于盐酸和醋酸两种溶液的比较,下列说法正确的是( )
A.pH相等的两溶液中:c(CHCOO-)=c(Cl-)
3
B.分别中和pH相等、体积相等的两溶液,所需NaOH的物质的量相同C.相同浓度的两溶液,分别与金属镁反应,反应速率相同
D.相同浓度的两溶液,分别与NaOH固体反应后呈中性的溶液中(忽略溶液体积变化):c(CHCOO-)=c(Cl
3
-)
10.某一元弱酸(用HA表示)在水中的电离方程式是HA H++A-,回答下列问题:
(1)向溶液中加入适量 NaA固体,以上平衡将向________(填“正”或“逆”)反应方向移动,理由是
_____________________________________________________________。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向________(填“正”或“逆”)反应方向移动,溶液中c(A
-)将________(填“增大”“减小”或“不变”,下同),溶液中c(OH-)将________。
(3)在25 ℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH)=c(Cl-),
则溶液显________性(填“酸”“碱”或“中”);用含a的代数式表示NH·HO的电离常数K=________。
3 2 b
1.关于pH相同的醋酸和盐酸,下列叙述不正确的是( )
A.取等体积的醋酸和盐酸分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m>n
B.取等体积的两种酸溶液分别与完全一样的足量锌粒反应,开始时反应速率盐酸大于醋酸
C.取等体积的两种酸溶液分别中和NaOH溶液,醋酸消耗NaOH的物质的量比盐酸多
D.两种酸溶液中c(CHCOO-)=c(Cl-)
3
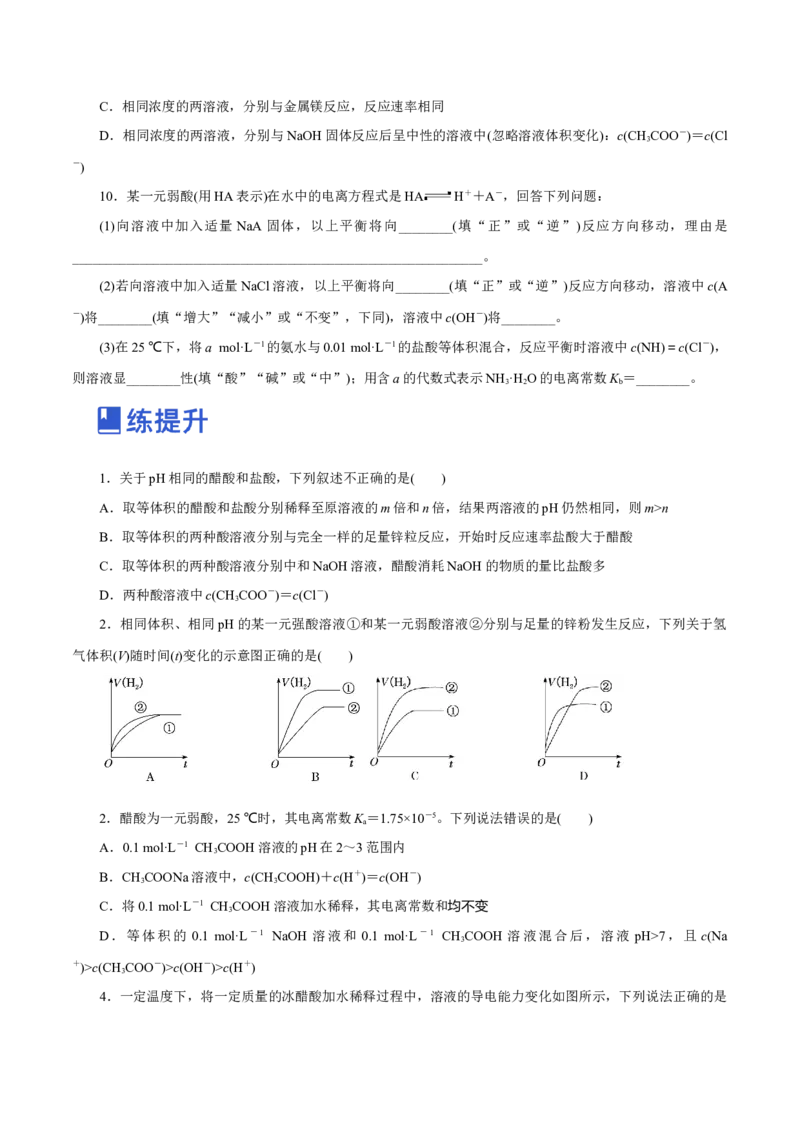
2.相同体积、相同pH的某一元强酸溶液①和某一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢
气体积(V)随时间(t)变化的示意图正确的是( )
2.醋酸为一元弱酸,25 ℃时,其电离常数K=1.75×10-5。下列说法错误的是( )
a
A.0.1 mol·L-1 CHCOOH溶液的pH在2~3范围内
3
B.CHCOONa溶液中,c(CHCOOH)+c(H+)=c(OH-)
3 3
C.将0.1 mol·L-1 CHCOOH溶液加水稀释,其电离常数和均不变
3
D.等体积的 0.1 mol·L-1 NaOH 溶液和 0.1 mol·L-1 CHCOOH 溶液混合后,溶液 pH>7,且 c(Na
3
+)>c(CHCOO-)>c(OH-)>c(H+)
3
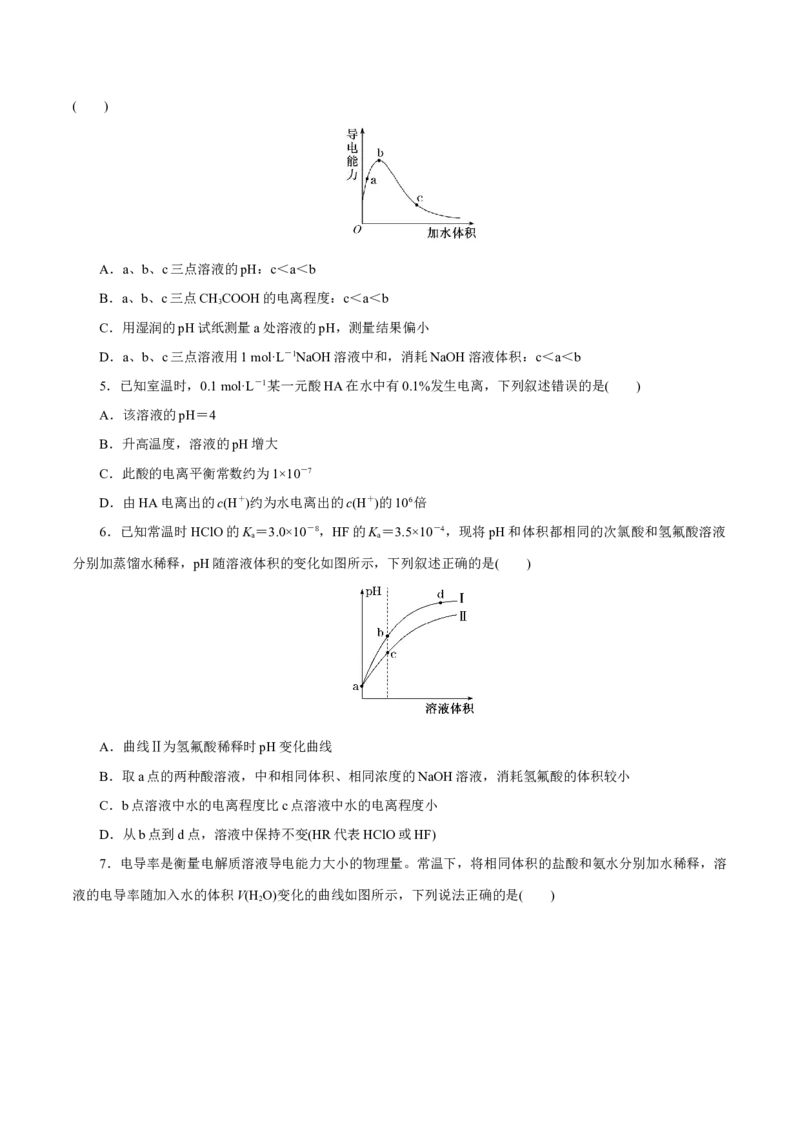
4.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )
A.a、b、c三点溶液的pH:c<a<b
B.a、b、c三点CHCOOH的电离程度:c<a<b
3
C.用湿润的pH试纸测量a处溶液的pH,测量结果偏小
D.a、b、c三点溶液用1 mol·L-1NaOH溶液中和,消耗NaOH溶液体积:c<a<b
5.已知室温时,0.1 mol·L-1某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
A.该溶液的pH=4
B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
6.已知常温时HClO的K=3.0×10-8,HF的K=3.5×10-4,现将pH和体积都相同的次氯酸和氢氟酸溶液
a a
分别加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是( )
A.曲线Ⅱ为氢氟酸稀释时pH变化曲线
B.取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗氢氟酸的体积较小
C.b点溶液中水的电离程度比c点溶液中水的电离程度小
D.从b点到d点,溶液中保持不变(HR代表HClO或HF)
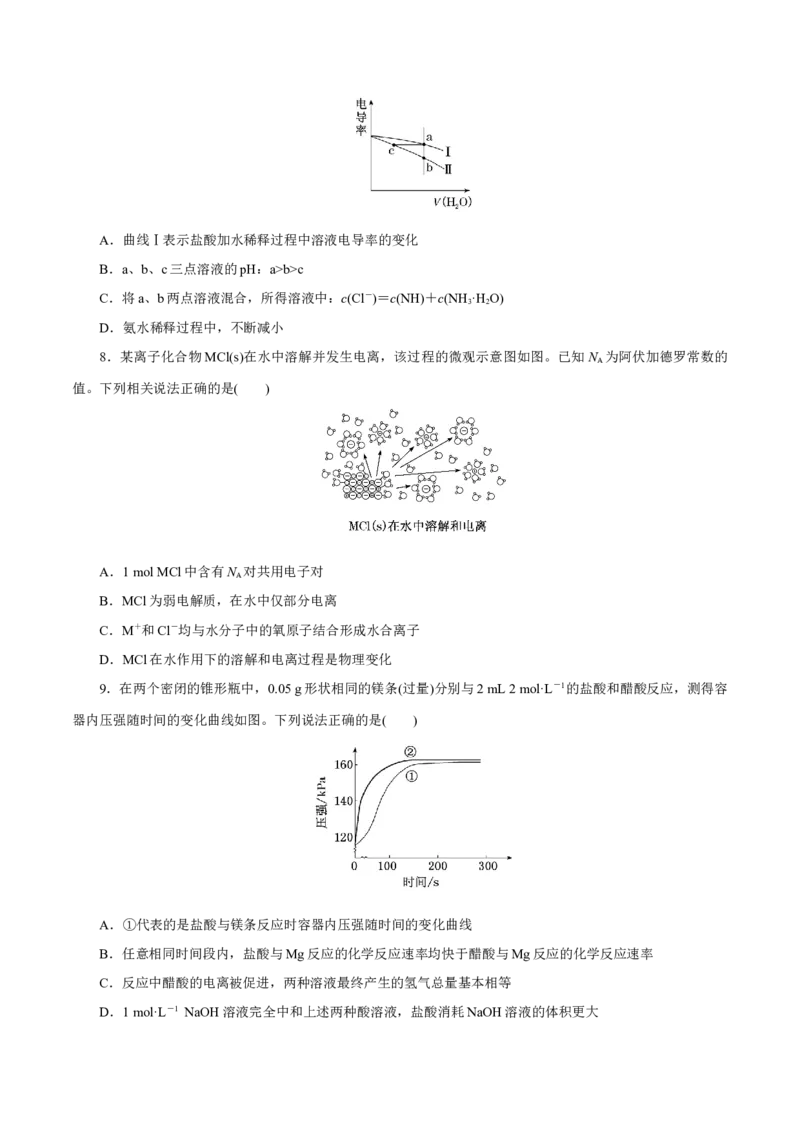
7.电导率是衡量电解质溶液导电能力大小的物理量。常温下,将相同体积的盐酸和氨水分别加水稀释,溶
液的电导率随加入水的体积V(HO)变化的曲线如图所示,下列说法正确的是( )
2A.曲线Ⅰ表示盐酸加水稀释过程中溶液电导率的变化
B.a、b、c三点溶液的pH:a>b>c
C.将a、b两点溶液混合,所得溶液中:c(Cl-)=c(NH)+c(NH·HO)
3 2
D.氨水稀释过程中,不断减小
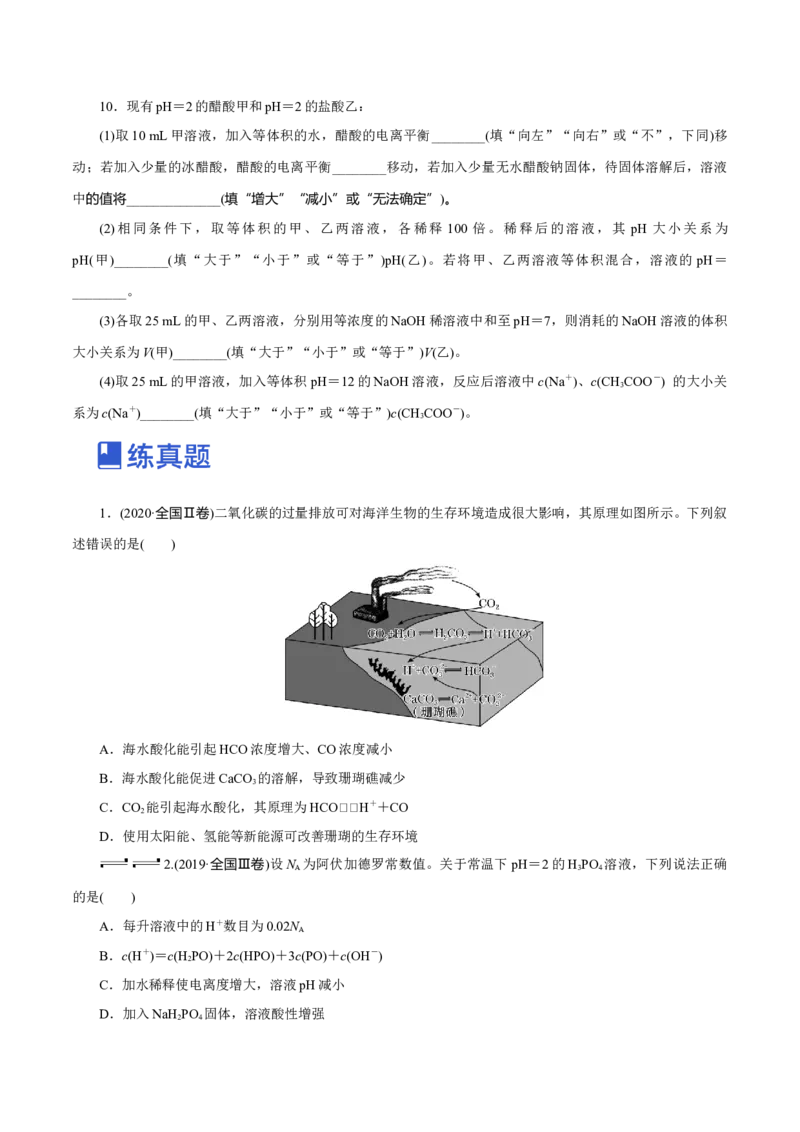
8.某离子化合物MCl(s)在水中溶解并发生电离,该过程的微观示意图如图。已知 N 为阿伏加德罗常数的
A
值。下列相关说法正确的是( )
A.1 mol MCl中含有N 对共用电子对
A
B.MCl为弱电解质,在水中仅部分电离
C.M+和Cl-均与水分子中的氧原子结合形成水合离子
D.MCl在水作用下的溶解和电离过程是物理变化
9.在两个密闭的锥形瓶中,0.05 g形状相同的镁条(过量)分别与2 mL 2 mol·L-1的盐酸和醋酸反应,测得容
器内压强随时间的变化曲线如图。下列说法正确的是( )
A.①代表的是盐酸与镁条反应时容器内压强随时间的变化曲线
B.任意相同时间段内,盐酸与Mg反应的化学反应速率均快于醋酸与Mg反应的化学反应速率
C.反应中醋酸的电离被促进,两种溶液最终产生的氢气总量基本相等
D.1 mol·L-1 NaOH溶液完全中和上述两种酸溶液,盐酸消耗NaOH溶液的体积更大10.现有pH=2的醋酸甲和pH=2的盐酸乙:
(1)取10 mL甲溶液,加入等体积的水,醋酸的电离平衡________(填“向左”“向右”或“不”,下同)移
动;若加入少量的冰醋酸,醋酸的电离平衡________移动,若加入少量无水醋酸钠固体,待固体溶解后,溶液
中的值将______________(填“增大”“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲、乙两溶液,各稀释 100 倍。稀释后的溶液,其 pH 大小关系为
pH(甲)________(填“大于”“小于”或“等于”)pH(乙)。若将甲、乙两溶液等体积混合,溶液的 pH=
________。
(3)各取25 mL的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和至pH=7,则消耗的NaOH溶液的体积
大小关系为V(甲)________(填“大于”“小于”或“等于”)V(乙)。
(4)取25 mL的甲溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CHCOO-) 的大小关
3
系为c(Na+)________(填“大于”“小于”或“等于”)c(CHCOO-)。
3
1.(2020·全国Ⅱ卷)二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如图所示。下列叙
述错误的是( )
A.海水酸化能引起HCO浓度增大、CO浓度减小
B.海水酸化能促进CaCO 的溶解,导致珊瑚礁减少
3
C.CO 能引起海水酸化,其原理为HCOH++CO
2
D.使用太阳能、氢能等新能源可改善珊瑚的生存环境
2.(2019·全国Ⅲ卷)设N 为阿伏加德罗常数值。关于常温下pH=2的HPO 溶液,下列说法正确
A 3 4
的是( )
A.每升溶液中的H+数目为0.02N
A
B.c(H+)=c(HPO)+2c(HPO)+3c(PO)+c(OH-)
2
C.加水稀释使电离度增大,溶液pH减小
D.加入NaHPO 固体,溶液酸性增强
2 43.(2019·天津卷)某温度下,HNO 和CHCOOH的电离常数分别为5.0×10-4和1.7×10-5。将pH和体积均相同
2 3
的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是( )
A.曲线Ⅰ代表HNO 溶液
2
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中保持不变(其中HA、A-分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
4.(2019·江苏卷)室温下,反应 +H O HCO+OH−的平衡常数K=2.2×10−8。将NH HCO 溶
2 2 3 4 3
液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指
定溶液中微粒物质的量浓度关系正确的是
A.0.2 mol·L−1氨水:c (NH ·H O)>c( )> c (OH−)> c (H+)
3 2
B.0.2 mol·L−1NH HCO 溶液(pH>7):c ( )> c ( )> c (H CO)> c (NH ·H O)
4 3 2 3 3 2
C.0.2 mol·L−1氨水和0.2 mol·L−1NH HCO 溶液等体积混合:c( )+c(NH ·H O)=c(H CO)+c (
4 3 3 2 2 3
)+c( )
D.0.6 mol·L−1氨水和0.2 mol·L−1 NH HCO 溶液等体积混合:c (NH ·H O)+ c( )+ c(OH−)=
4 3 3 2
0.3 mol·L−1+ c (H CO)+ c (H+)
2 3