文档内容
第 24 讲 化学反应速率
(模拟精练+真题演练)
完卷时间:50分钟
可能用到的相对原子质量:H 1 C 12 O 16 S 32 Cl 35.5 Cu 64 Ba 137
一、选择题(每小题只有一个正确选项,共12×5分)
1 . ( 2023 春 · 四 川 内 江 · 高 三 四 川 省 资 中 县 第 二 中 学 校 考 开 学 考 试 ) 对 于 可 逆 反 应
,在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
A. B.
C. D.
2.(2023春·山东滨州·高三统考开学考试)某反应 的速率方程为 ,
其半衰期(当剩余的反应物恰好是起始的一半时所需的时间)为 。在650K时,反应物浓度不同时的反
应速率如表所示。
0.025 0.050 0.025
0.040 0.040 0.120
下列说法错误的是
A.该反应可能为基元反应
B.该反应的速率常数
C.当 , ,650K时的反应速率为
D.在过量的B存在时,反应掉93.75%的A所需的时间是1200min
3.(2023·广东茂名·茂名市第一中学校考模拟预测)恒温恒容条件下,向密闭容器中加入一定量X,发生
反应:①X(g) Y(g);②Y(g) Z(g)。已知v=kc (反应物),k为速率常数,如图表明三种物质浓度随时
间的变化以及k受温度的影响。下列说法不正确的是A.反应过程体系的压强始终不变
B.c(Y)随时间先增大后减小
C.随c(X)的减小,反应①、②的速率均逐渐降低
D.温度对反应②的k影响更大
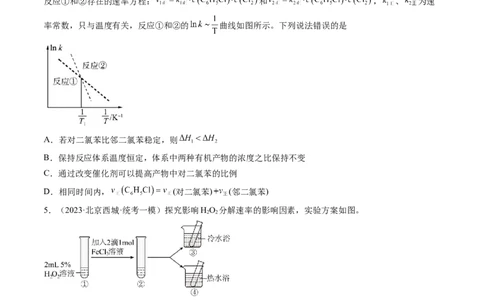
4.(2023·湖南·校联考模拟预测)在一定温度下,以 为催化剂,氯苯和 在 溶液中发生反应
反应①: (邻二氯苯)
反应②: (对二氯苯)
反应①和②存在的速率方程: 和 , 、 为速
率常数,只与温度有关,反应①和②的 曲线如图所示。下列说法错误的是
A.若对二氯苯比邻二氯苯稳定,则
B.保持反应体系温度恒定,体系中两种有机产物的浓度之比保持不变
C.通过改变催化剂可以提高产物中对二氯苯的比例
D.相同时间内, (对二氯苯) (邻二氯苯)
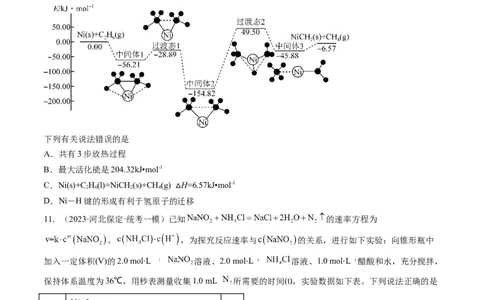
5.(2023·北京西城·统考一模)探究影响HO 分解速率的影响因素,实验方案如图。
2 2
下列说法不正确的是
A.对比①②,可探究FeCl 溶液对HO 分解速率的影响
3 2 2
B.对比②③④,可探究温度对HO 分解速率的影响
2 2
C.HO 是直线形的非极性分子
2 2
D.HO 易溶于水,主要是由于HO 与HO分子之间能形成氢键
2 2 2 2 2
6.(2023·辽宁丹东·统考一模)恒温恒容条件下,向密闭容器中加入一定量X,反应X=2Z经历两步:
①X→Y;②Y→2Z。图为该体系中X、Y、Z浓度随时间变化的曲线。下列说法正确的是A.a为 随t的变化曲线
B. 时,Y的消耗速率大于生成速率
C.随着 的减小,反应①、②速率均降低
D.体系中
7.(2023·福建莆田·统考模拟预测)工业上在 催化作用下生产 的反应为
,该反应可看作两步:① (快);
② (慢)。下列说法正确的是
A.该反应活化能为
B.减小 的浓度能降低 的生成速率
C. 的存在使有效碰撞次数增加,降低了该反应的焓变
D.①的活化能一定大于②的活化能
8.(2023·辽宁丹东·统考二模)反应 的速率方程为 (k为速
率常数,其中 ,A、R为常数, 为活化能,T为开氏温度),其半衰期(反应物消耗
一半所需的时间)为 。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是
0.25 0.5 l 0.5 l
0.05 0.05 0.1 0.1 0.2
1.6 3.2 3.2
A.
B.
C.在过量的B存在时,A剩余25%所需的时间是
D.升温、加入催化剂,缩小容积(加压),均能使k增大,导致反应的瞬时速率加快
9.(2023·浙江宁波·镇海中学校考模拟预测)一定温度下,利用测压法在刚性反应器中研究固体催化剂作
用下的A的分解反应: 。体系的总压强p随时间t的变化如表所示:t/min 0 100 150 250 420 500 580
p/kPa 12.1 13.3 13.9 15.1 17.14 x 19.06
下列说法不正确的是
A.100~150min,消耗A的平均速率为
B.其他条件不变,420min时向刚性容器中再充入少量A,反应速率比原420min时大
C.推测x为18.1
D.升高体系温度,不一定能加快反应速率
10.(2022·广东·统考模拟预测)Ni可活化C H 放出CH,其反应历程如图所示:
2 6 4
下列有关说法错误的是
A.共有3步放热过程
B.最大活化能是204.32kJ•mol-1
C.Ni(s)+C H(l)=NiCH (s)+CH(g) H=6.57kJ•mol-1
2 6 2 4
D.Ni-H键的形成有利于氢原子的迁移
△
11.(2023·河北保定·统考一模)已知 的速率方程为
。 ,为探究反应速率与 的关系,进行如下实验:向锥形瓶中
加入一定体积(V)的2.0 molL 溶液、2.0 molL 溶液、1.0 molL 醋酸和水,充分搅拌,
保持体系温度为36℃,用秒⋅表测量收集1.0 mL 所需⋅要的时间(t),实验数据如⋅下表。下列说法正确的是
V/mL
实验 t/s
溶 醋
溶液 水
液 酸
1 4.0 4.0 8.0 332
2 6.0 4.0 4.0 6.0 148
3 4.0 4.0 4.0 834 12.0 4.0 4.0 37
A. ;
B.实验3用 表示的反应平均速率 mol·s
C.醋酸不参与反应,其浓度的大小对该反应速率无影响
D.速率方程中
12.(2023·山东淄博·校联考二模)某温度下,在金表面发生反应: ,其速率方
程式为 (k为速率常数)。反应过程中, 与S(催化剂)及时间关系如图所示。已知 (半
衰期)为反应物消耗一半所用的时间,下列叙述错误的是
A. ,Ⅰ条件下
B.其他条件相同,S(催化剂)越大,k越大
C.其他条件相同, 增大,反应速率不变
D.该温度下,当S(催化剂) , 时, 为
二、主观题(共3小题,共40分)
13.(14分)(2023·新疆乌鲁木齐·乌鲁木齐市高级中学校考一模)实验小组探究 溶液与 溶
液的反应及其速率,实验过程和现象如表。已知:
i、 具有强氧化性,能完全电离, 易被还原为 ;
ii、淀粉检测 的灵敏度很高,遇低浓度的 即可快速变蓝:
iii、可与 发生反应: 。
编号 1-1 1-2实验操
作
现象 无明显现象 溶液立即变蓝
(1)实验1-1的目的是 。
(2) 与 反应的离子方程式为 。
为了研究 与 反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,
如表。
编 蒸馏水 的淀
变色时间/s
号 溶液 溶液 粉溶液/滴 溶液
2-1 2 0 2.8 2 0.2 立即
2-2 2 0.8 0.2 2 0 30
(3)实验2-1不能用于测定 与KI反应的速率,原因除变色时间过短外还有 。
(4)加入 溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
猜想1: 先与 反应,使 降低;
猜想2: 先与 反应,___________。
①甲同学提出猜想1的依据:由信息iii推测, 的还原性 (填“强于”或“弱于”) 的。
②乙同学根据现有数据证明猜想1不成立,理由是 。
③补全猜想2: 。
(5)查阅文献表明猜想2成立。根据实验2-2的数据,计算 内的平均反应速率
(写出计算式)。
14.(12分)(2023·浙江·模拟预测)科学家在实验室研究利用催化技术将飞机尾气中的NO和CO转变
成CO 和N,其反应为2NO(g)+2CO(g) N(g)+2CO (g)。
2 2 2 2
(1)若将3molNO和2molCO通入10L的恒容密闭容器中,在一定条件下发生上述反应,各组分的物质的量
浓度随时间的变化情况如图1所示。①图中曲线A表示 (填“NO”“CO”“N ”或“CO”,下同)的浓度变化,曲线C表示的是的 浓度变化。
2 2
②在0~4min内NO的平均反应速率v(NO)= ,4min末N 的浓度为 。
2
③4min末,采用下列措施一定能加快上述反应速率的是 (填标号)。
A.升高体系的温度 B.充入一定量的O
2
C.将容器体积变为5L D.充入一定量氦气
(2)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了验证催化剂比表面
积对化学反应速率的影响规律,在温度为T 时,某同学设计了以下三组实验:
0
实验编
T(K) NO的初始浓度(mol•L-1) CO的初始浓度(mol•L-1) 催化剂的比表面积(m2•g-1)
号
Ⅰ T 1.20×10-3 3.80×10-3 75
0
Ⅱ T 1.20×10-3 3.80×10-3 50
0
Ⅲ T 1.20×10-3 3.80×10-3 100
0
在图2中分别画出表中实验Ⅱ、Ⅲ条件下混合气体中NO的浓度随时间变化的曲线,并标明各条曲线的实
验编号 。
15.(14分)在一定条件下,二氧化硫和氧气发生反应:
2SO (g)+O(g)2SO (g)。
2 2 3
(1)降低温度,化学反应速率________(填“增大”“减小”或“不变”)。
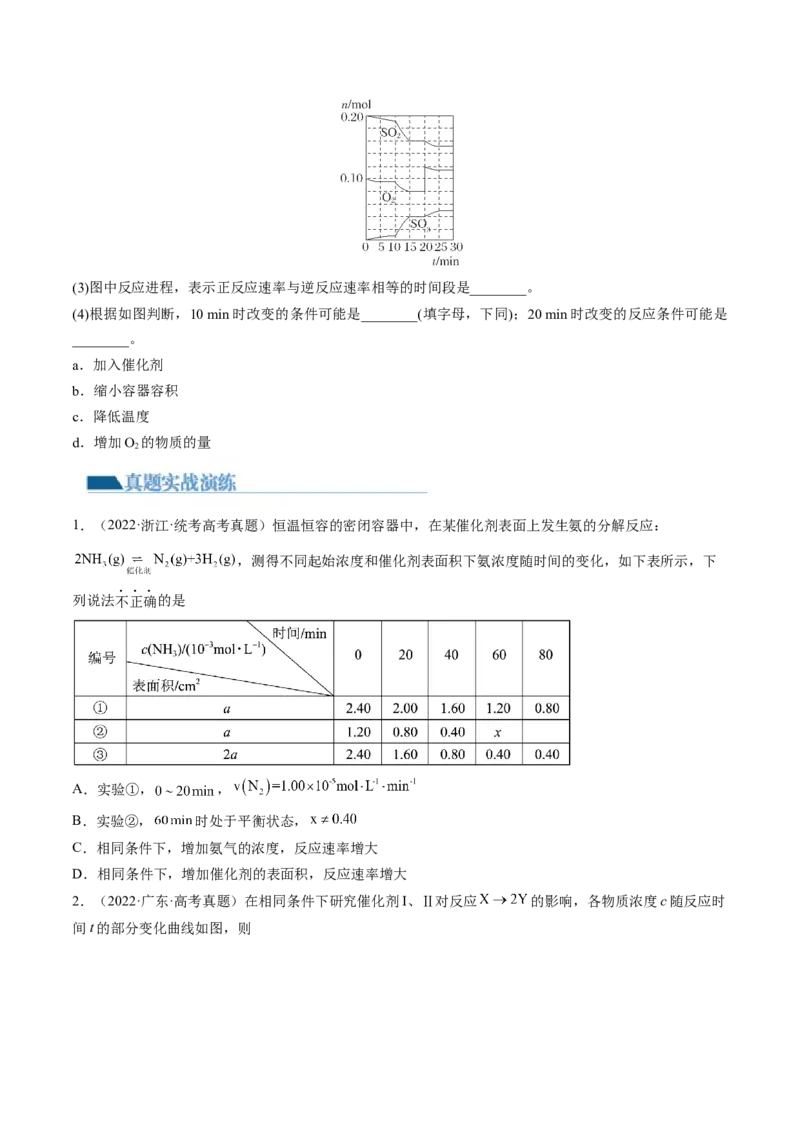
(2)600 ℃时,在一容积为2 L的密闭容器中,将二氧化硫和氧气混合,在反应进行至 10 min和20 min时,
分别改变了影响反应的一个条件,反应过程中 SO 、O 、SO 物质的量变化如图所示,前10 min正反应速
2 2 3
率逐渐________(填“增大”“减小”或“不变”);前15 min内用SO 表示的平均反应速率为________。
3(3)图中反应进程,表示正反应速率与逆反应速率相等的时间段是________。
(4)根据如图判断,10 min时改变的条件可能是________(填字母,下同);20 min时改变的反应条件可能是
________。
a.加入催化剂
b.缩小容器容积
c.降低温度
d.增加O 的物质的量
2
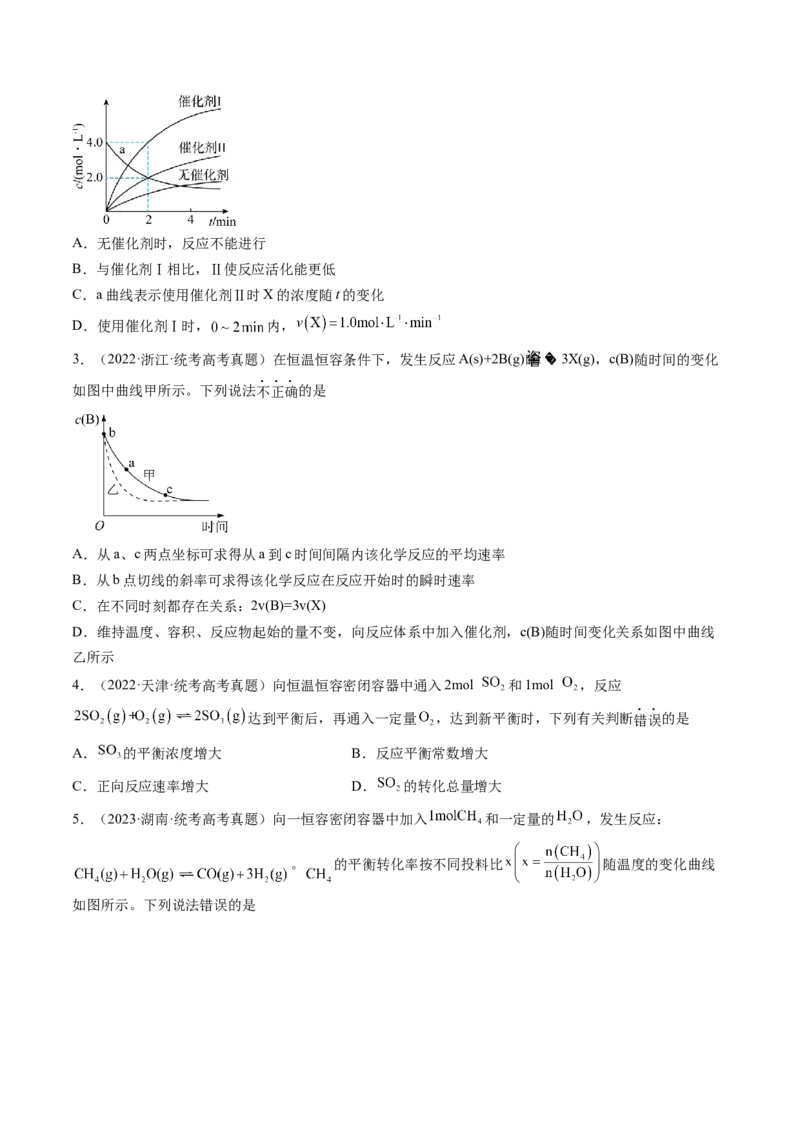
1.(2022·浙江·统考高考真题)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是
A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
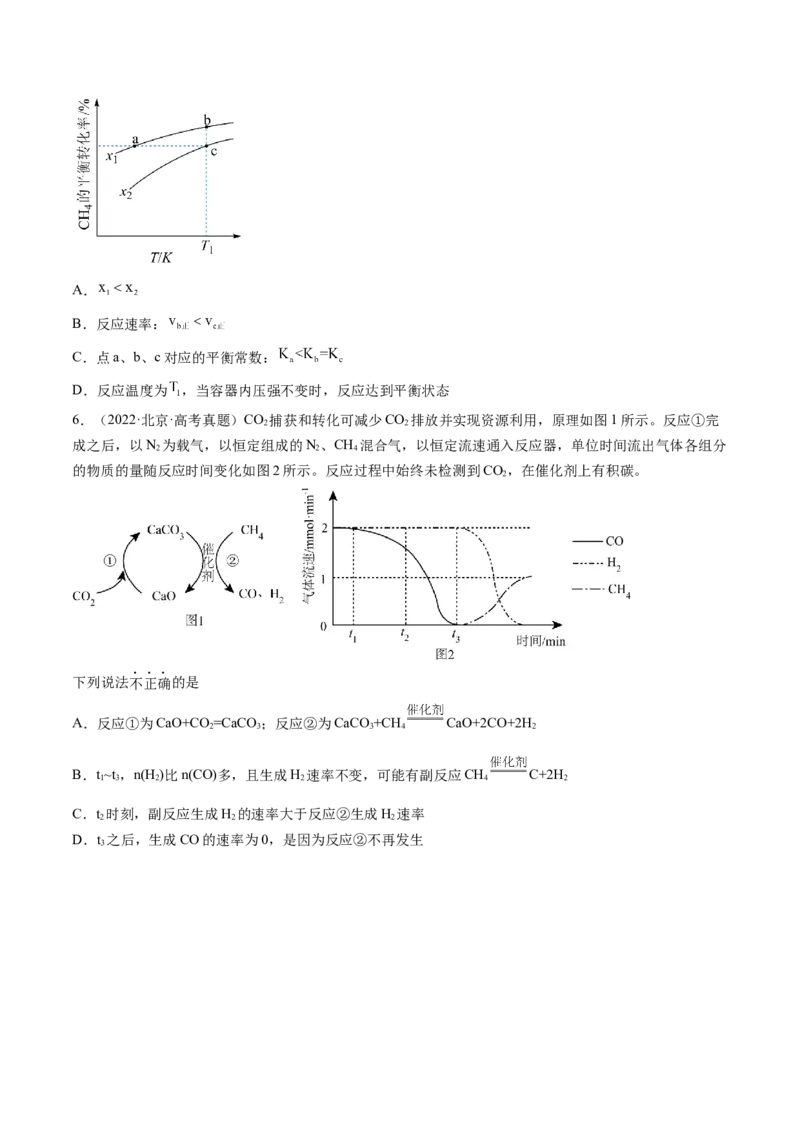
2.(2022·广东·高考真题)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时
间t的部分变化曲线如图,则A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时, 内,
3.(2022·浙江·统考高考真题)在恒温恒容条件下,发生反应A(s)+2B(g) 3X(g),c(B)随时间的变化
如图中曲线甲所示。下列说法不正确的是
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线
乙所示
4.(2022·天津·统考高考真题)向恒温恒容密闭容器中通入2mol 和1mol ,反应
达到平衡后,再通入一定量 ,达到新平衡时,下列有关判断错误的是
A. 的平衡浓度增大 B.反应平衡常数增大
C.正向反应速率增大 D. 的转化总量增大
5.(2023·湖南·统考高考真题)向一恒容密闭容器中加入 和一定量的 ,发生反应:
。 的平衡转化率按不同投料比 随温度的变化曲线
如图所示。下列说法错误的是A.
B.反应速率:
C.点a、b、c对应的平衡常数:
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态
6.(2022·北京·高考真题)CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。反应①完
2 2
成之后,以N 为载气,以恒定组成的N、CH 混合气,以恒定流速通入反应器,单位时间流出气体各组分
2 2 4
的物质的量随反应时间变化如图2所示。反应过程中始终未检测到CO,在催化剂上有积碳。
2
下列说法不正确的是
A.反应①为CaO+CO =CaCO ;反应②为CaCO +CH CaO+2CO+2H
2 3 3 4 2
B.t~t,n(H )比n(CO)多,且生成H 速率不变,可能有副反应CH C+2H
1 3 2 2 4 2
C.t 时刻,副反应生成H 的速率大于反应②生成H 速率
2 2 2
D.t 之后,生成CO的速率为0,是因为反应②不再发生
3