文档内容
第 29 讲 化学综合实验
第一部分:高考真题感悟
1.(2022·全国甲卷)硫化钠可广泛用于染料、医药行业。工业生产的硫化钠粗品中常含有一定量的煤灰
及重金属硫化物等杂质。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。实验室中常用95%乙醇重结晶
纯化硫化钠粗品。回答下列问题:
(1)工业上常用芒硝( )和煤粉在高温下生产硫化钠,同时生成CO,该反应的化学方程式为
_______。
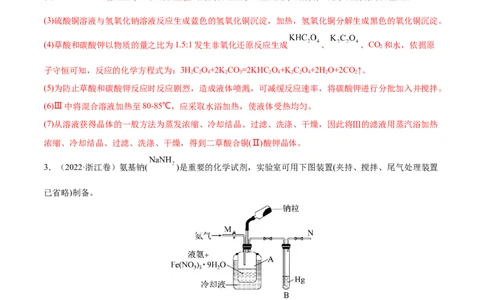
(2)溶解回流装置如图所示,回流前无需加入沸石,其原因是_______。回流时,烧瓶内气雾上升高度不宜
超过冷凝管高度的1/3.若气雾上升过高,可采取的措施是_______。
(3)回流时间不宜过长,原因是_______。回流结束后,需进行的操作有①停止加热 ②关闭冷凝水 ③移去
水浴,正确的顺序为_______(填标号)。
A.①②③ B.③①② C.②①③ D.①③②
(4)该实验热过滤操作时,用锥形瓶而不能用烧杯接收滤液,其原因是_______。过滤除去的杂质为_______。
若滤纸上析出大量晶体,则可能的原因是_______。
(5)滤液冷却、结晶、过滤,晶体用少量_______洗涤,干燥,得到 。
【答案】(1)Na SO ·10H O+4C NaS+4CO↑+10H O
2 4 2 2 2
(2)硫化钠粗品中常含有一定量的煤灰及重金属硫化物等杂质,这些杂质可以直接作沸石 降低温度
(3)硫化钠易溶于热乙醇,若回流时间过长,NaS会直接析出在冷凝管上,使提纯率较低,同时易造成冷凝
2
管下端堵塞,圆底烧瓶内气压过大,发生爆炸 D
(4)防止滤液冷却 重金属硫化物 温度逐渐恢复至室温
(5)冷水
【解析】本实验的实验目的为制备硫化钠并用95%乙醇重结晶纯化硫化钠粗品,工业上常用芒硝(
)和煤粉在高温下生产硫化钠,反应原理为:NaSO ·10H O+4C NaS+4CO↑+10H O,
2 4 2 2 2
结合硫化钠的性质解答问题。
(1)工业上常用芒硝( )和煤粉在高温下生产硫化钠,同时生产CO,根据得失电子守恒,反应
的化学方程式为:NaSO ·10H O+4C NaS+4CO↑+10H O;
2 4 2 2 2
(2)由题干信息,生产的硫化钠粗品中常含有一定量的煤灰及重金属硫化物等杂质,这些杂质可以直接作沸
石,因此回流前无需加入沸石,若气流上升过高,可直接降低降低温度,使气压降低;
(3)硫化钠易溶于热乙醇,若回流时间过长,NaS会直接析出在冷凝管上,使提纯率较低,同时易造成冷凝
2
管下端堵塞,圆底烧瓶内气压过大,发生爆炸;回流结束后,先停止加热,再移去水浴后再关闭冷凝水,
故正确的顺序为①③②,答案选D。
(4)硫化钠易溶于热乙醇,使用锥形瓶可有效防止滤液冷却,重金属硫化物难溶于乙醇,故过滤除去的杂质
为重金属硫化物,由于硫化钠易溶于热乙醇,过滤后温度逐渐恢复至室温,滤纸上便会析出大量晶体;
(5)乙醇与水互溶,硫化钠易溶于热乙醇,因此将滤液冷却、结晶、过滤后,晶体可用少量冷水洗涤,再干
燥,即可得到 。
2.(2022·全国乙卷)二草酸合铜(Ⅱ)酸钾( )可用于无机合成、功能材料制备。实验室制备
二草酸合铜(Ⅱ)酸钾可采用如下步骤:
Ⅰ.取已知浓度的 溶液,搅拌下滴加足量 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过
滤。Ⅱ.向草酸( )溶液中加入适量 固体,制得 和 混合溶液。
Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分
析。
回答下列问题:
(1)由 配制Ⅰ中的 溶液,下列仪器中不需要的是________(填仪器名称)。
(2)长期存放的 中,会出现少量白色固体,原因是________。
(3)Ⅰ中的黑色沉淀是________(写化学式)。
(4)Ⅱ中原料配比为 ,写出反应的化学方程式________。
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入 应采取________的方法。
(6)Ⅲ中应采用________进行加热。
(7)Ⅳ中“一系列操作”包括________。
【答案】(1)分液漏斗和球形冷凝管
(2) 风化失去结晶水生成无水硫酸铜
(3)CuO
(4)3H C O+2K CO=2KHC O+K C O+2H O+2CO↑
2 2 4 2 3 2 4 2 2 4 2 2
(5)分批加入并搅拌
(6)水浴
(7)冷却结晶、过滤、洗涤
【解析】取已知浓度的 溶液,搅拌下滴加足量 溶液,产生浅蓝色沉淀氢氧化铜,加热,氢氧
化铜分解生成黑色的氧化铜沉淀,过滤,向草酸( )溶液中加入适量 固体,制得 和混合溶液,将 和 混合溶液加热至80-85℃,加入氧化铜固体,全部溶解后,趁热
过滤,将滤液用蒸汽浴加热浓缩、冷却结晶、过滤、洗涤、干燥,得到二草酸合铜(Ⅱ)酸钾晶体。
(1)由 固体配制硫酸铜溶液,需用天平称量一定质量的 固体,将称量好的固体放
入烧杯中,用量筒量取一定体积的水溶解 ,因此用不到的仪器有分液漏斗和球形冷凝管。
(2) 含结晶水,长期放置会风化失去结晶水,生成无水硫酸铜,无水硫酸铜为白色固体。
(3)硫酸铜溶液与氢氧化钠溶液反应生成蓝色的氢氧化铜沉淀,加热,氢氧化铜分解生成黑色的氧化铜沉淀。
(4)草酸和碳酸钾以物质的量之比为1.5:1发生非氧化还原反应生成 、 、CO 和水,依据原
2
子守恒可知,反应的化学方程式为:3HC O+2K CO=2KHC O+K C O+2H O+2CO↑。
2 2 4 2 3 2 4 2 2 4 2 2
(5)为防止草酸和碳酸钾反应时反应剧烈,造成液体喷溅,可减缓反应速率,将碳酸钾进行分批加入并搅拌。
(6)Ⅲ中将混合溶液加热至80-85℃,应采取水浴加热,使液体受热均匀。
(7)从溶液获得晶体的一般方法为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,因此将Ⅲ的滤液用蒸汽浴加热
浓缩、冷却结晶、过滤、洗涤、干燥,得到二草酸合铜(Ⅱ)酸钾晶体。
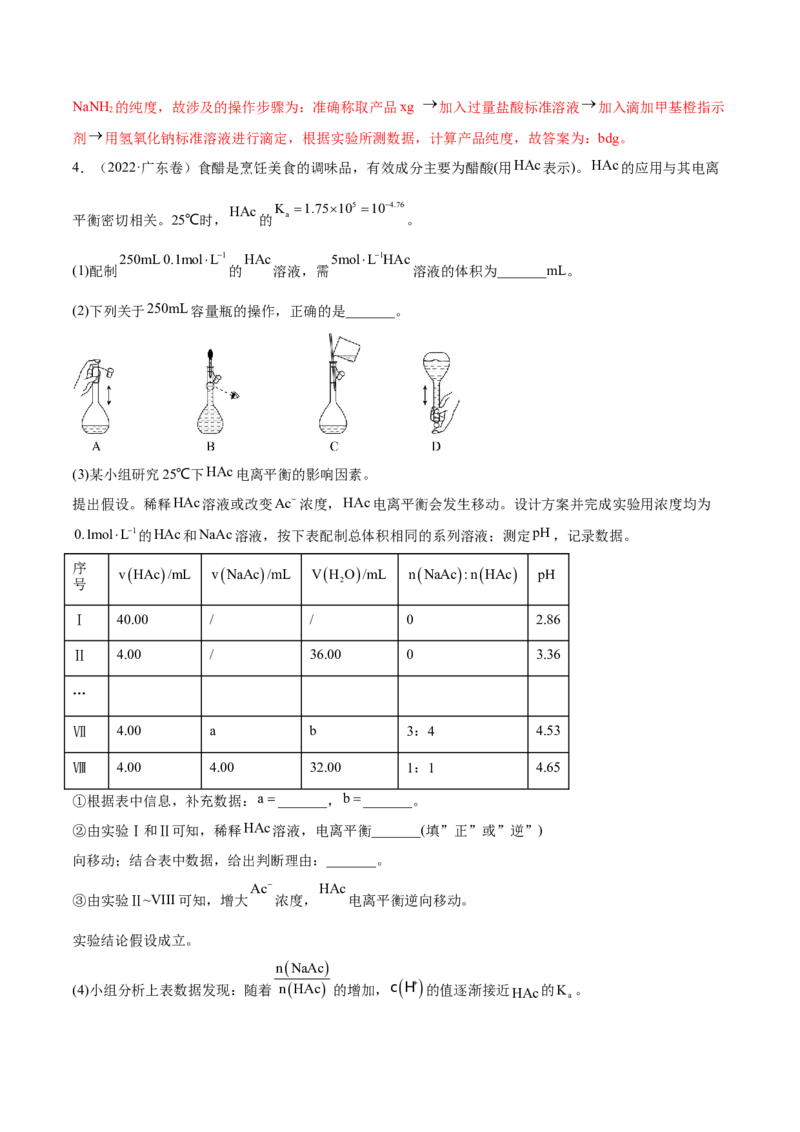
3.(2022·浙江卷)氨基钠( )是重要的化学试剂,实验室可用下图装置(夹持、搅拌、尾气处理装置
已省略)制备。
简要步骤如下:
Ⅰ.在瓶A中加入 液氨和 ,通入氨气排尽密闭体系中空气,搅拌。
Ⅱ.加入5g钠粒,反应,得 粒状沉积物。
Ⅲ.除去液氨,得产品 。已知: 几乎不溶于液氨,易与水、氧气等反应。
请回答:
(1) 的作用是_______;装置B的作用是_______。
(2)步骤Ⅰ,为判断密闭体系中空气是否排尽,请设计方案_______。
(3)步骤Ⅱ,反应速率应保持在液氨微沸为宜。为防止速率偏大,可采取的措施有_______。
(4)下列说法不正确的是_______。
A.步骤Ⅰ中,搅拌的目的是使 均匀地分散在液氨中
B.步骤Ⅱ中,为判断反应是否已完成,可在N处点火,如无火焰,则反应己完成
C.步骤Ⅲ中,为避免污染,应在通风橱内抽滤除去液氨,得到产品
D.产品 应密封保存于充满干燥氮气的瓶中
(5)产品分析:假设 是产品 的唯一杂质,可采用如下方法测定产品 纯度。从下列选项
中选择最佳操作并排序_______。
准确称取产品 计算
a.准确加入过量的水
b.准确加入过量的 标准溶液
c.准确加入过量的 标准溶液
d.滴加甲基红指示剂(变色的 范围4.4~6.2)
e.滴加石蕊指示剂(变色的 范围4.5~8.3)
f.滴加酚酞指示剂(变色的 范围8.2~10.0)g.用 标准溶液滴定
h.用 标准溶液滴定
i.用 标准溶液滴定
【答案】(1) 催化 防止氧气、水进入密闭体系
(2)试管中加满水倒扣于水槽中,M处通入氨气,将N处排出的气体导入试管内。如试管底部出现气泡,则
空气尚未排尽,如未出现气泡,则说明空气已排尽
(3)分批少量加入钠粒;降低冷却液温度;适当增加液氨量(任写一种即可)
(4)BC
(5)bdg
【解析】在硝酸铁催化下钠与液氨的反应来生成NaNH 和氢气,该反应是放热反应,为保证液氨处于微沸
2
状态,需要用冷却液控制一定的温度。NaNH 易与水和氧气发生反应,所以装置B中Hg可防止氧气、水
2
进入密闭体系,导气口N与尾气处理连接装置再处理氨气等,据此结合实验原理分析解答。
(1)结合实验原理,根据实验操作中加入Fe(NO ) 9HO的用料很少,可推知,Fe(NO ) 9HO在反应中作
3 3 2 3 3 2
催化剂,加快反应速率;结合已知信息可知,制备得到的NaNH 易与水和氧气发生反应,所以装置B中
2
Hg可防止氧气、水进入密闭体系,干扰NaNH 的制备,
2
故答案为:催化;防止氧气、水进入密闭体系;
(2)结合氨气极易溶于水,空气中的氮气难溶于水,氧气不易溶于水的物理性质,所以为判断密封体系中空
气是否排尽,可设计方案如下:试管中加满水倒扣于水槽中,M处通入氨气,将N处排出的气体导入试管
内。如试管底部出现气泡,则空气尚未排尽,如未出现气泡,则说明空气已排尽;
(3)上述化学反应中,反应物的浓度、温度均可影响化学反应速率,所以为防止反应速率偏大,可实施的措
施有:分批少量加入钠粒;降低冷却液温度;适当增加液氨量(任写一种即可);
(4)A.步骤I中,搅拌可使液体混合均匀,所以搅拌可使少量的催化剂Fe(NO ) 9HO均匀分散在液氨中,A
3 3 2
正确;B.步骤II中,由于液氨处于微沸状态,故生成的氢气中混有一定量的氨气;氢气虽然是可燃性气体,
由于氨气在空气中不能被点燃,当氨气中只有少量氢气时,则也不能被点然、不会产生火焰,且对易气体
点火有安全隐患,B错误;C.步骤II中得到的粒状沉积物,颗粒较小,颗粒太小的沉淀易在滤纸上形成一
层密实的沉淀,溶液不易透过,所以不适宜选用抽滤装置进行过滤,C错误;D.因为制备的产品NaNH 易
2
与水和氧气发生反应,所以可密封保存于充满干燥氮气的瓶中,D正确;故选BC;
(5)题干信息中提到假设产品NaNH 的唯一杂质为NaOH,因为产品溶于水生成氢氧化钠和氨气,所以可设
2
计利用盐酸标准溶液进行滴定,因滴定终点时,溶液中含氯化钠和氯化铵,所以需选用酸性条件下的酸碱
指示剂判断滴定终点,过量的盐酸再利用氢氧化钠标准液反滴定,最终利用所测数据计算得出产品中NaNH 的纯度,故涉及的操作步骤为:准确称取产品xg 加入过量盐酸标准溶液 加入滴加甲基橙指示
2
剂 用氢氧化钠标准溶液进行滴定,根据实验所测数据,计算产品纯度,故答案为:bdg。
4.(2022·广东卷)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的应用与其电离
HAc K 1.75105 104.76
平衡密切相关。25℃时, 的 a 。
250mL 0.1molL1 HAc 5molL1HAc
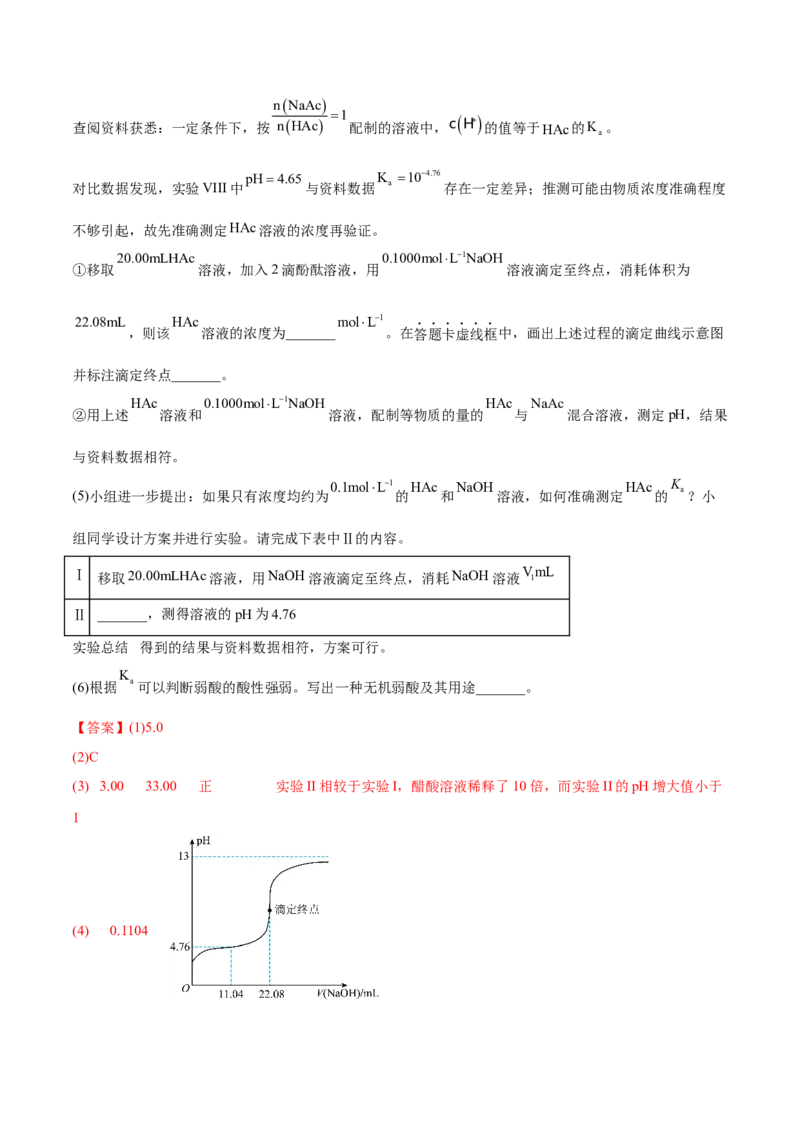
(1)配制 的 溶液,需 溶液的体积为_______mL。
(2)下列关于250mL容量瓶的操作,正确的是_______。
(3)某小组研究25℃下HAc电离平衡的影响因素。
提出假设。稀释HAc溶液或改变Ac浓度,HAc电离平衡会发生移动。设计方案并完成实验用浓度均为
0.1molL1的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
序 vHAc/mL vNaAc/mL VH O/mL nNaAc:nHAc pH
号 2
Ⅰ 40.00 / / 0 2.86
Ⅱ 4.00 / 36.00 0 3.36
…
Ⅶ 4.00 a b 3:4 4.53
Ⅷ 4.00 4.00 32.00 1:1 4.65
①根据表中信息,补充数据:a_______,b_______。
②由实验Ⅰ和Ⅱ可知,稀释HAc溶液,电离平衡_______(填”正”或”逆”)
向移动;结合表中数据,给出判断理由:_______。
Ac HAc
③由实验Ⅱ~VIII可知,增大 浓度, 电离平衡逆向移动。
实验结论假设成立。
nNaAc
(4)小组分析上表数据发现:随着 nHAc 的增加,c H+ 的值逐渐接近HAc的K 。
anNaAc
1
查阅资料获悉:一定条件下,按 nHAc 配制的溶液中,c
H+
的值等于HAc的K 。
a
pH4.65 K 104.76
对比数据发现,实验VIII中 与资料数据 a 存在一定差异;推测可能由物质浓度准确程度
不够引起,故先准确测定HAc溶液的浓度再验证。
20.00mLHAc 0.1000molL1NaOH
①移取 溶液,加入2滴酚酞溶液,用 溶液滴定至终点,消耗体积为
22.08mL HAc molL1
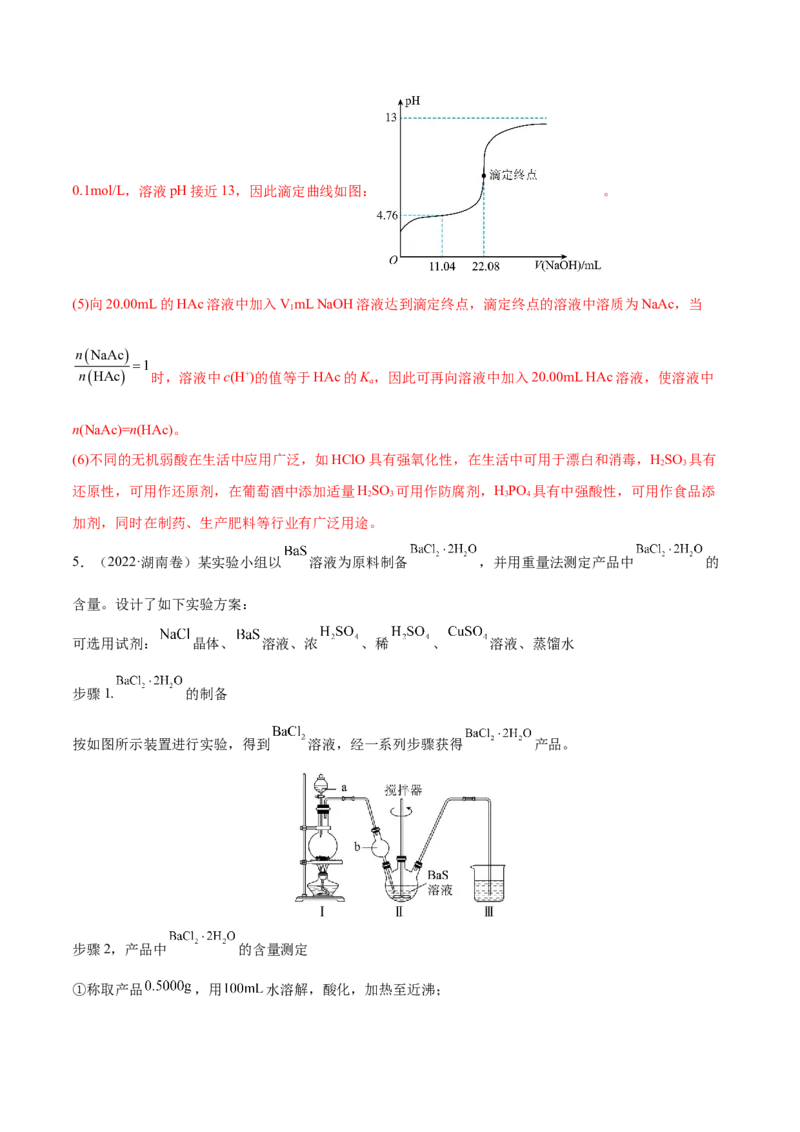
,则该 溶液的浓度为_______ 。在答题卡虚线框中,画出上述过程的滴定曲线示意图
并标注滴定终点_______。
HAc 0.1000molL1NaOH HAc NaAc
②用上述 溶液和 溶液,配制等物质的量的 与 混合溶液,测定pH,结果
与资料数据相符。
0.1molL1 HAc NaOH HAc K
(5)小组进一步提出:如果只有浓度均约为 的 和 溶液,如何准确测定 的 a?小
组同学设计方案并进行实验。请完成下表中Ⅱ的内容。
Ⅰ 移取20.00mLHAc溶液,用NaOH溶液滴定至终点,消耗NaOH溶液 V
1
mL
Ⅱ _______,测得溶液的pH为4.76
实验总结 得到的结果与资料数据相符,方案可行。
K
(6)根据 a可以判断弱酸的酸性强弱。写出一种无机弱酸及其用途_______。
【答案】(1)5.0
(2)C
(3) 3.00 33.00 正 实验II相较于实验I,醋酸溶液稀释了10倍,而实验II的pH增大值小于
1
(4) 0.1104(5)向滴定后的混合液中加入20mL HAc溶液
(6)HClO:漂白剂和消毒液(或HSO :还原剂、防腐剂或HPO :食品添加剂、制药、生产肥料)
2 3 3 4
【解析】(1)溶液稀释过程中,溶质的物质的量不变,因此250mL×0.1mol/L=V×5mol/L,解得V=5.0mL。
(2)A.容量瓶使用过程中,不能用手等触碰瓶口,以免污染试剂,故A错误;
B.定容时,视线应与溶液凹液面和刻度线“三线相切”,不能仰视或俯视,故B错误;
C.向容量瓶中转移液体,需用玻璃棒引流,玻璃棒下端位于刻度线以下,同时玻璃棒不能接触容量瓶口,
故C正确;
D.定容完成后,盖上瓶塞,将容量瓶来回颠倒,将溶液摇匀,颠倒过程中,左手食指抵住瓶塞,防止瓶
塞脱落,右手扶住容量瓶底部,防止容量瓶从左手掉落,故D错误;
综上所述,正确的是C项。
(3)①实验VII的溶液中n(NaAc):n(HAc)=3:4,V(HAc)=4.00mL,因此V(NaAc)=3.00mL,即a=3.00,,由
实验I可知,溶液最终的体积为40.00mL,因此V(H O)=40.00mL-4.00mL-3.00mL=33.00mL,即b=33.00。
2
1
②实验I所得溶液的pH=2.86,实验II的溶液中c(HAc)为实验I的 ,稀释过程中,若不考虑电离平衡移
10
动,则实验II所得溶液的pH=2.86+1=3.86,但实际溶液的pH=3.36<3.86,说明稀释过程中,溶液中n(H+)
增大,即电离平衡正向移动,故答案为:正;实验II相较于实验I,醋酸溶液稀释了10倍,而实验II的
pH增大值小于1。
(4)(i)滴定过程中发生反应:HAc+NaOH=NaAc+H O,由反应方程式可知,滴定至终点时,
2
n(HAc)=n(NaOH),因此22.08mL×0.1mol/L=20.00mL×c(HAc),解得c(HAc)=0.1104mol/L。
(ii)滴定过程中,当V(NaOH)=0时,c(H+)= K a cHAc ≈ 10-4.760.1mol/L=10-2.88mol/L,溶液的pH=2.88,
当V(NaOH)=11.04mL时,n(NaAc)=n(HAc),溶液的pH=4.76,当V(NaOH)=22.08mL时,达到滴定终点,
溶液中溶质为NaAc溶液,Ac-发生水解,溶液呈弱碱性,当NaOH溶液过量较多时,c(NaOH)无限接近0.1mol/L,溶液pH接近13,因此滴定曲线如图: 。
(5)向20.00mL的HAc溶液中加入VmL NaOH溶液达到滴定终点,滴定终点的溶液中溶质为NaAc,当
1
nNaAc
1
nHAc 时,溶液中c(H+)的值等于HAc的K ,因此可再向溶液中加入20.00mL HAc溶液,使溶液中
a
n(NaAc)=n(HAc)。
(6)不同的无机弱酸在生活中应用广泛,如HClO具有强氧化性,在生活中可用于漂白和消毒,HSO 具有
2 3
还原性,可用作还原剂,在葡萄酒中添加适量HSO 可用作防腐剂,HPO 具有中强酸性,可用作食品添
2 3 3 4
加剂,同时在制药、生产肥料等行业有广泛用途。
5.(2022·湖南卷)某实验小组以 溶液为原料制备 ,并用重量法测定产品中 的
含量。设计了如下实验方案:
可选用试剂: 晶体、 溶液、浓 、稀 、 溶液、蒸馏水
步骤1. 的制备
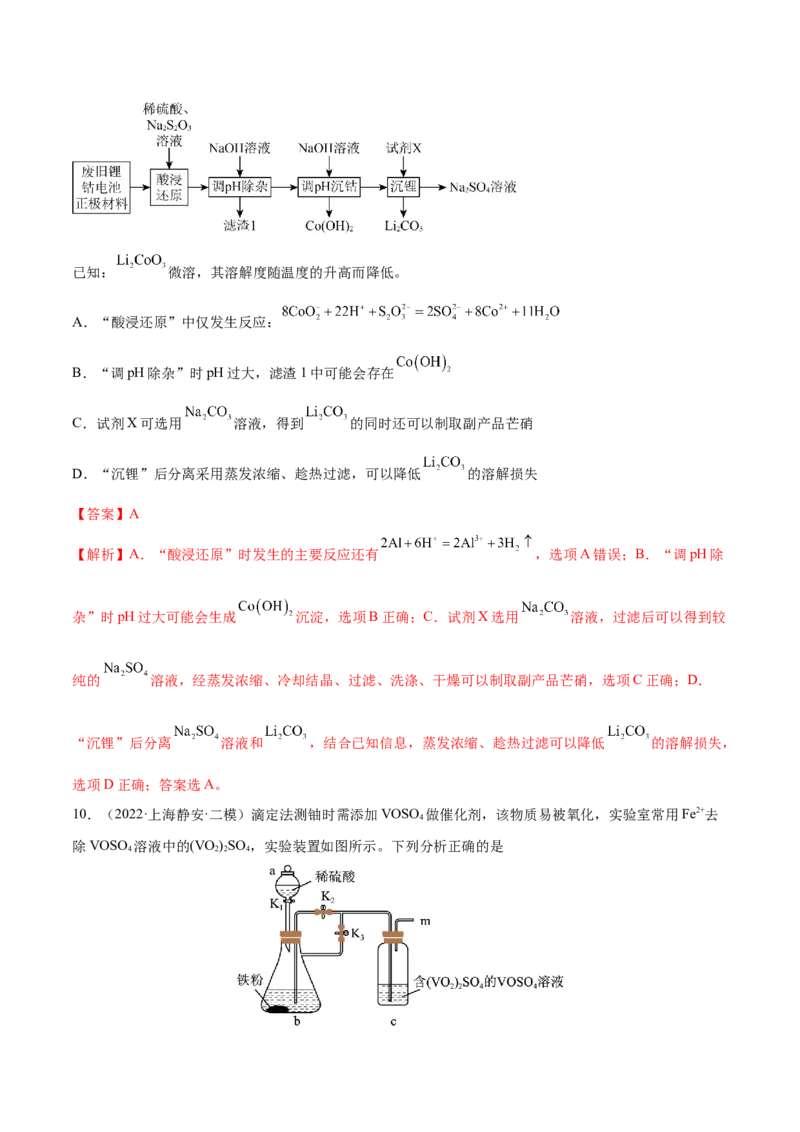
按如图所示装置进行实验,得到 溶液,经一系列步骤获得 产品。
步骤2,产品中 的含量测定
①称取产品 ,用 水溶解,酸化,加热至近沸;②在不断搅拌下,向①所得溶液逐滴加入热的 溶液,
③沉淀完全后, 水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为 。
回答下列问题:
(1)Ⅰ是制取_______气体的装置,在试剂a过量并微热时,发生主要反应的化学方程式为_______;
(2)Ⅰ中b仪器的作用是_______;Ⅲ中的试剂应选用_______;
(3)在沉淀过程中,某同学在加入一定量热的 溶液后,认为沉淀已经完全,判断沉淀已完全的方法是
_______;
(4)沉淀过程中需加入过量的 溶液,原因是_______;
(5)在过滤操作中,下列仪器不需要用到的是_______(填名称);
(6)产品中 的质量分数为_______(保留三位有效数字)。
【答案】(1) HCl HSO (浓)+NaCl NaHSO+HCl↑
2 4 4
(2)防止倒吸 CuSO 溶液
4
(3)静置,取上层清液于一洁净试管中,继续滴加硫酸溶液,无白色沉淀生成,则已沉淀完全
(4)使钡离子沉淀完全
(5)锥形瓶
(6)97.6%
【解析】装置I中浓硫酸和氯化钠共热制备HCl,装置II中氯化氢与BaS溶液反应制备BaCl ·2H O,装置
2 2
III中硫酸铜溶液用于吸收生成的HS,防止污染空气。
2
(1)由分析可知,装置I为浓硫酸和氯化钠共热制取HCl气体的装置,在浓硫酸过量并微热时,浓硫酸与氯
化钠反应生成硫酸氢钠和氯化氢,发生主要反应的化学方程式为:HSO (浓)+NaCl NaHSO+HCl↑。
2 4 4
(2)氯化氢极易溶于水,装置II中b仪器的作用是:防止倒吸;装置II中氯化氢与BaS溶液反应生成HS,
2
HS有毒,对环境有污染,装置III中盛放CuSO 溶液,用于吸收HS。
2 4 2
(3)硫酸与氯化钡反应生成硫酸钡沉淀,因此判断沉淀已完全的方法是静置,取上层清液于一洁净试管中,
继续滴加硫酸溶液,无白色沉淀生成,则已沉淀完全。(4)为了使钡离子沉淀完全,沉淀过程中需加入过量的硫酸溶液。
(5)过滤用到的仪器有:铁架台、烧杯、漏斗、玻璃棒,用不到锥形瓶。
(6)由题意可知,硫酸钡的物质的量为: =0.002mol,依据钡原子守恒,产品中BaCl ·2H O的物质
2 2
的量为0.002mol,质量为0.002mol 244g/mol=0.488g,质量分数为: 100%=97.6%。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·河南开封·二模)实验室利用如图所示装置(已略去夹持、加热及搅拌装置)制取五氯化锑,反应
如下:SbCl +Cl SbCl (相关物质性质如下表)。下列说法错误的是
3 2 5
物质 熔点 沸点 性质
SbCl 73.4℃ 220.3℃ 极易水解
3
79℃/2.9kPa(140℃
SbCl 3.5℃ 极易水解
5 分解)
A.试剂X可以使用无水CaCl
2
B.冷凝管的作用是冷凝回流,从a口进水,b口出水
C.此实验中采用水浴加热的方式比较合适
D.可采用减压蒸馏的方法将SbCl ,从反应液中分离
5
【答案】A
【解析】A.根据题中信息SbCl 和SbCl 极易水解,Cl 有毒故试剂X的作用为防止空气中的水蒸气进入三
3 5 2
颈烧瓶,同时收集氯气,防止污染空气,故不能用CaCl 只能吸收水分,不能吸收氯气,可以用碱石灰,A
2错误;B.冷凝管的作用是冷凝回流,下进上出冷凝效果好,B正确;C.根据题中SbCl 和SbCl 的熔沸点
3 5
和SbCl 2.9kPa(140℃分解),可知采用水浴加热合适,C正确;D.根据SbCl 在2.9kPa(140℃分解),可采
5 5
用减压蒸馏的方法将SbCl 从反应液中分离,D正确;故选A。
5
2.(2022·河南许昌·二模)实验室可用下图装置制备乙酸乙酯,实验开始时先加热至110~120℃,再滴入
乙醇和冰醋酸并使滴入速率与蒸出液体的速率几乎相等,滴加完毕后升温到130℃至不再有液体蒸出。下
列说法错误的是
A.冷凝管的进水口为b
B.可用油浴加热
C.滴加速率不宜过快,是为了防止副反应增多
D.蒸出的液体用饱和碳酸钠溶液洗涤、分液可得到粗乙酸乙酯
【答案】C
【解析】A.为增强冷凝效果,冷凝管中的水下进上出,即进水口为b,A正确;B.所需温度高于水的沸
点,所以可以采用沸点更高的油进行油浴加热,B正确;C.滴加速率不宜过快,是为了减少反应物的蒸
发损失,提高利用率,C错误;D.饱和碳酸钠可以吸收未反应的乙醇和乙酸,同时乙酸乙酯难溶于饱和
碳酸钠溶液,所以洗涤、分液可得到粗乙酸乙酯,D正确;综上所述答案为C。
3.(2022·四川内江·模拟预测)用下图所示装置及药品制备相应的气体,其中不能实现的是( )A.制取NH B.制取乙烯 C.制取Cl D.制取SO
3 2 2
【答案】D
【解析】A.氧化钙溶于水放热,且溶液中氢氧根离子浓度增大,使浓氨水分解产生氨气,A正确;B.乙
醇在浓硫酸作催化剂和加热的条件下能发生消去反应生成乙烯,B正确;C.实验室用二氧化锰与浓盐酸
在加热的条件下发生反应生成氯化锰、氯气和水,C正确;D.铜与浓硫酸反应制取二氧化硫需在加热的
条件下,D装置不能加热,D错误;故答案为D。
4.(2022·广东广州·模拟预测)室温下,某同学用下图中装置在通风棚中进行如下实验:
实验 现象
试管Ⅰ中开始无明显现象,后逐渐有微小气泡生成,反应越来越剧烈,试
管口上方出现红棕色气体,溶液呈蓝色。
试管Ⅱ中剧烈反应,迅速生成大量红棕色气体,溶液呈绿色:之后向溶液
中持续通入 ,溶液又变为蓝色。
下列说法不正确的是A.试管Ⅰ中浅红棕色气体为 ,由铜还原硝酸生成
B.等质量的Cu完全溶解时,Ⅰ中消耗的 更少
C.试管Ⅱ中反应后溶液颜色与试管Ⅰ中的不同,可能是由于溶有
D.蓝色的 呈平面四边形结构,中心离子不可能为 杂化
【答案】A
【解析】A.试管 Ⅰ 中Cu与稀硝酸反应生成NO,然后NO与氧气反应生成浅红棕色气体NO A错误;
2,
B.3mol Cu消耗8mol稀硝酸,1molCu消耗4mol浓硝酸,则等质量的Cu完全溶解时,I中消耗的HNO
3
更少,B正确;C.二氧化氮为红棕色气体,则II中反应后溶液颜色与试管I中的不同,是由于溶有NO ,
2
C正确;D.蓝色的 呈平面四边形结构,中心离子应是sp2杂化,D正确;故选A。
5.(2022·广东广州·模拟预测)下列实验操作能达到实验目的的是
选项 实验操作 实验目的
加热氯化铵和氢氧化钙的混合物,并将产生的气体通过碱石灰进
A 制备干燥的氨气
行干燥验证 的金属活动大于
B 向 溶液中加入一小块金属钠
C 先将浓硫酸加入烧杯中,后缓缓倒入蒸馏水,并不断搅拌 稀释浓硫酸
D 分别测量饱和 与饱和 溶液的 证明 强于
【答案】A
【解析】A.加热氯化铵和氢氧化钙的混合物,产生氨气,将氨气通过碱石灰,除去氨气中的水蒸气,得
到干燥的氨气,A正确;B.钠的金属性强,放入硫酸铜溶液中先与水反应,不能置换出硫酸铜中的铜,
因此无法验证钠的金属性大于铜,B错误;C.浓硫酸溶于水放出大量的热,因此稀释浓硫酸时,应将浓
硫酸沿着烧杯壁缓慢的倒入水中,并用玻璃棒不断搅拌,防止溶液飞溅,C错误;D.饱和 与饱和
溶液的浓度不同,因此不能根据两种物质饱和溶液的pH大小判断其酸性强弱,D错误;答案选A。
6.(2022·上海·复旦附中二模)在下列实验操作中,会导致测量结果偏小的是
A.胆矾品体中结晶水含量测定实验中,坩埚中有受热不分解的物质
B.灼烧法测定 NaCO、NaHCO 混合物中NaCO 的质量分数实验中,未进行恒重操作
2 3 3 2 3
C.HCl标准液滴定未知浓度的NaOH溶液实验中,锥形瓶内溶液溅出
D.气体摩尔体积的测定中,反应结束后未冷却至室温便读数
【答案】C
【解析】A. 胆矾品体中结晶水含量测定实验中,坩埚中有受热不分解的物质,而加热前后固体的质量差
不变,测量结果不变,故A不选;B. 灼烧法测定 NaCO、NaHCO 混合物中NaCO 的质量分数实验中,
2 3 3 2 3
未进行恒重操作,减小的质量小,碳酸氢钠的含量小,碳酸钠的含量增大,故B不选;C. HCl标准液滴
定未知浓度的NaOH溶液实验中,锥形瓶内溶液溅出,引起消耗HCl标准液的体积偏小,导致测量NaOH
溶液浓度偏小,故C选;D. 气体摩尔体积的测定中,反应结束后未冷却至室温便读数,温度高,测得的
气体体积偏大,故D不选;故选C。
7.(2022·辽宁辽阳·二模)下列结论正确且与实验操作及现象相对应的是
实验操作及现象 结论
A 某气体能使湿润的蓝色石蕊试纸变红 该气体的水溶液呈碱性
向某钠盐的溶液中加入稀盐酸,产生能使澄
B 该钠盐可能是碳酸钠
清石灰水变浑浊的气体
C HA的酸性比HB的强
向等体积 的HA溶液和HB溶液中分别加入足量的锌,HA溶液放出的氢气更多
向等浓度的NaCl、NaBr的混合溶液中加入少
D
量 溶液,先有浅黄色沉淀产生
【答案】B
【解析】A.某气体能使湿润的蓝色石蕊试纸变红,说明室温下该气体溶于水后溶液的pH小于5,该气体
的水溶液呈酸性,A错误;B.向某钠盐的溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的气体为二氧
化碳、或二氧化硫,该钠盐可能是碳酸钠、碳酸氢钠、亚硫酸钠或亚硫酸氢钠,B正确;C.向等体积
的HA溶液和HB溶液中分别加入足量的锌,HA溶液放出的氢气更多,则HA的物质的量浓度更大,
HA的酸性比HB的弱,C错误;D.向等浓度的NaCl、NaBr的混合溶液中加入少量 溶液,先有浅
黄色沉淀产生,则AgCl的溶解度大于AgBr, ,D错误;答案选B。
8.(2022·北京·杨镇第一中学模拟预测)最适用于鉴别丁香酚和肉桂酸的试剂是
A.银氨溶液 B.溴的四氯化碳溶液
C.氯化铁溶液 D.氢氧化钠溶液
【答案】C
【解析】A.两种物质均不含醛基,与银氨溶液不反应,不能鉴别,A错误;B.两种物质均含双键,都能
使溴的四氯化碳溶液褪色,不能鉴别,B错误;C.丁香酚中含酚羟基,能与氯化铁溶液发生显色反应;
肉桂酸中不含酚羟基,与氯化铁溶液不反应,C正确;D.丁香酚中的酚羟基和肉桂酸中的羧基与氢氧化
钠溶液均能反应,不能鉴别,D错误;故选C。
9.(2022·江西·模拟预测)以废旧锂钴电池正极材料( 颗粒粉末附着在铝箔表面)为原料,提纯回收
钴元素与锂元素的工艺流程如下。下列叙述错误的是已知: 微溶,其溶解度随温度的升高而降低。
A.“酸浸还原”中仅发生反应:
B.“调pH除杂”时pH过大,滤渣1中可能会存在
C.试剂X可选用 溶液,得到 的同时还可以制取副产品芒硝
D.“沉锂”后分离采用蒸发浓缩、趁热过滤,可以降低 的溶解损失
【答案】A
【解析】A.“酸浸还原”时发生的主要反应还有 ,选项A错误;B.“调pH除
杂”时pH过大可能会生成 沉淀,选项B正确;C.试剂X选用 溶液,过滤后可以得到较
纯的 溶液,经蒸发浓缩、冷却结晶、过滤、洗涤、干燥可以制取副产品芒硝,选项C正确;D.
“沉锂”后分离 溶液和 ,结合已知信息,蒸发浓缩、趁热过滤可以降低 的溶解损失,
选项D正确;答案选A。
10.(2022·上海静安·二模)滴定法测铀时需添加VOSO 做催化剂,该物质易被氧化,实验室常用Fe2+去
4
除VOSO 溶液中的(VO )SO ,实验装置如图所示。下列分析正确的是
4 2 2 4A.VOSO 和(VO )SO 中V元素的化合价相同
4 2 2 4
B.b中反应所生成气体的作用之一是将装置中的空气排尽
C.用小试管在m处收集气体并验纯后,应先关闭K,再打开K
2 3
D.实验完毕,可用氯水和KSCN溶液检验c中溶液是否含有Fe2+
【答案】B
【解析】本实验用Fe2+去除VOSO 溶液中的(VO )SO ,b中稀硫酸和铁粉反应生成H,反应前需要用H
4 2 2 4 2 2
将装置中的空气排尽,防止空气中氧气氧化VOSO,关闭K,打开K,H 将硫酸亚铁溶液压入c中,发
4 3 2 2
生反应。A.VOSO 中V的化合价为+4价,(VO )SO 中V的化合价为+5价,A错误;B.VOSO 易被氧
4 2 2 4 4
化,所以b中反应产生的H 的作用之一就是排尽装置中的空气,防止VOSO 被氧化,B正确;C.用小试
2 4
管在m处收集气体并验纯,应先打开K,再关闭K,C错误;D.实验完毕后,c中含有较多VOSO,
3 2 4
VOSO 易被氧化可与氯水反应,故不能用氯水和KSCN溶液检验c中是否含有Fe2+,D错误;故答案选
4
B。
11.(2022·湖北·黄冈中学模拟预测)下列有关实验现象和实验结论都正确的选项是
实验过程 实验现象 实验结论
向 溶液中滴加3滴
A 溶液,出现白色沉淀后,再 有红褐色沉淀产生
滴加3滴 溶液
两支试管各盛0.1mol/L4mL酸性高锰酸钾溶 加入0.2mol/L草酸
反应物浓度越大,反应速率越
B 液,分别加入0.1mol/L2mL草酸溶液和 溶液试管中,高锰酸
快
0.2mol/L2mL草酸溶液 钾溶液褪色更快
C 室温下,向苯酚钠溶液中通足量 溶液变浑浊 碳酸的酸性比苯酚的强
室温下,用pH试纸分别测定等物质的量浓度
溶液对应的
D 酸性:
的 溶液和 溶液的pH pH试纸蓝色更深
【答案】C
【解析】A. 氢氧化钠过量,滴入氯化铁会产生氢氧化铁红褐色沉淀,没有发生沉淀转化,不能得出所说
结论,A错误;B.根据方程式可知, ,高
锰酸钾过量,溶液颜色不会褪去,B错误;C.碳酸酸性强于苯酚,在苯酚钠溶液中通入二氧化碳会生成
苯酚,苯酚常温下在水中的溶解度小,故溶液变浑浊,C正确;D.次氯酸钠溶液显碱性,且具有漂白性,
能使pH试纸先变蓝后褪色,D错误;故选C。12.(2022·山东日照·三模)实验室用下图所示装置,探究室温下 与 的反应,所用镁条质量和表面
积相同,且均已用砂纸打磨,实验2的镁条放在尖嘴玻璃导管内并浸于蒸馏水中,实验3产生的浑浊物主
要为碱式碳酸镁 。下列说法错误的是
实验1 实验2 实验3
镁条表面有微小气泡,且溶液 镁条表面有较多气泡且产生气泡速率 镁条表面有大量气泡,溶液逐
较长时间无明显变化 逐渐加快,溶液中无明显现象 渐变浑浊
A.实验1现象不明显,可能与 表面生成了难溶的 有关
B.实验2比实验1现象更明显,可能是由于玻璃导管内空间狭小,热量不易散失
C.由实验1和实验3可得出“碱性增强有利于加快镁与水反应速率”的结论
D.实验3中破坏了 在镁条表面的沉积,增大了镁与水的接触面积
【答案】C
【解析】A.镁条已用砂纸打磨,实验1中镁条表面有微小气泡,且溶液较长时间无明显变化,说明镁条
与蒸馏水反应,可能发生的反应为Mg+2HO=Mg(OH)+H ↑,现象不明显的原因可能是Mg表面生成了难
2 2 2
溶的Mg(OH) ,A项正确;B.实验2的镁条放在尖嘴玻璃导管内并浸于蒸馏水中,实验2比实验1现象更
2
明显,可能是由于玻璃导管内空间狭小,热量不易散失,体系温度升高,从而使反应速率加快、Mg(OH)
2
溶解度增大,B项正确;C.实验3产生的浑浊物主要为碱式碳酸镁[mMg(OH) ∙nMgCO],实验1和实验3
2 3
中反应不相同,实验1和实验3中的变量不唯一,故由实验1和实验3不能得出“碱性增强有利于加快镁
与水反应速率”的结论,C项错误;D.实验3产生的浑浊物主要为碱式碳酸镁[mMg(OH) ∙nMgCO],说
2 3
明实验3中 可破坏Mg(OH) 在镁条表面的沉积,增大了镁与水的接触面积,从而镁条表面有大量气
2
泡产生,D项正确;答案选C。
二、主观题(共3小题,共40分)
13.(2022·广西·模拟预测)(14分)亚硝酰硫酸(NOSOH)在重氮化反应中可以代替亚硝酸钠。实验室用
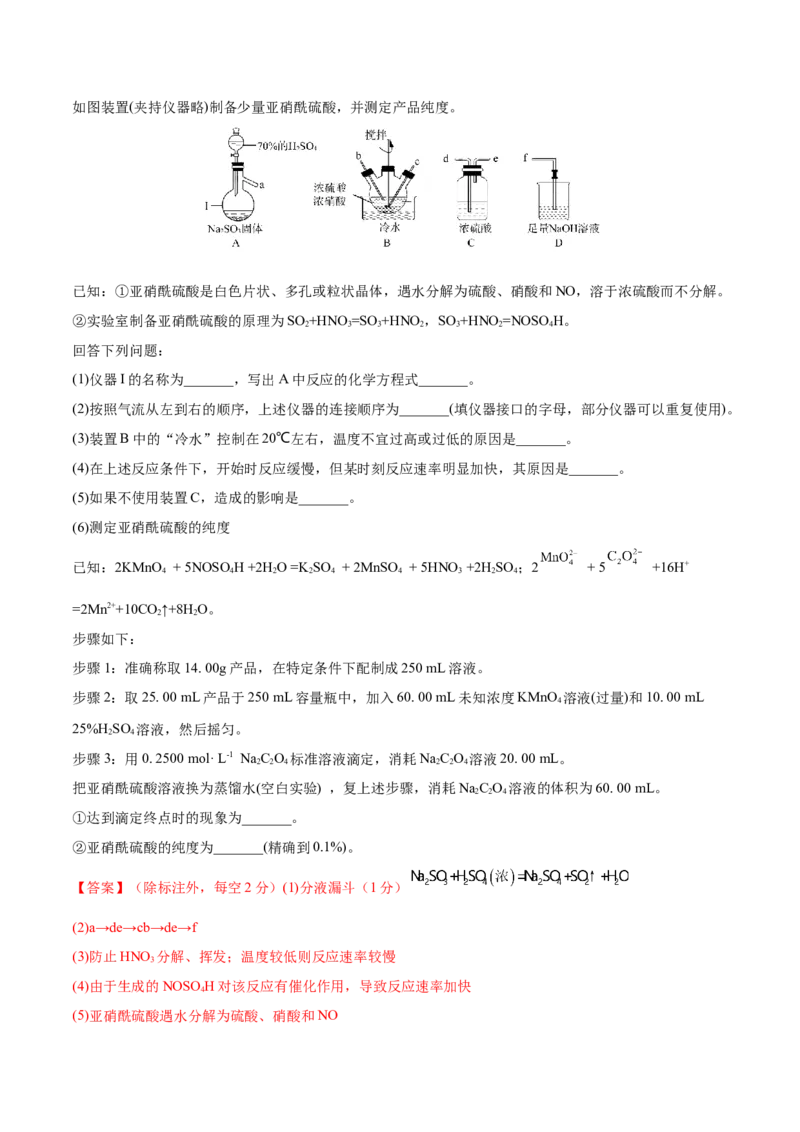
4如图装置(夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
已知:①亚硝酰硫酸是白色片状、多孔或粒状晶体,遇水分解为硫酸、硝酸和NO,溶于浓硫酸而不分解。
②实验室制备亚硝酰硫酸的原理为SO +HNO =SO+HNO ,SO +HNO =NOSO H。
2 3 3 2 3 2 4
回答下列问题:
(1)仪器I的名称为_______,写出A中反应的化学方程式_______。
(2)按照气流从左到右的顺序,上述仪器的连接顺序为_______(填仪器接口的字母,部分仪器可以重复使用)。
(3)装置B中的“冷水”控制在20℃左右,温度不宜过高或过低的原因是_______。
(4)在上述反应条件下,开始时反应缓慢,但某时刻反应速率明显加快,其原因是_______。
(5)如果不使用装置C,造成的影响是_______。
(6)测定亚硝酰硫酸的纯度
已知:2KMnO + 5NOSOH +2H O =K SO + 2MnSO + 5HNO +2H SO ;2 + 5 +16H+
4 4 2 2 4 4 3 2 4
=2Mn2++10CO ↑+8H O。
2 2
步骤如下:
步骤1:准确称取14. 00g产品,在特定条件下配制成250 mL溶液。
步骤2:取25. 00 mL产品于250 mL容量瓶中,加入60. 00 mL未知浓度KMnO 溶液(过量)和10. 00 mL
4
25%H SO 溶液,然后摇匀。
2 4
步骤3:用0. 2500 mol· L-1 NaC O 标准溶液滴定,消耗NaC O 溶液20. 00 mL。
2 2 4 2 2 4
把亚硝酰硫酸溶液换为蒸馏水(空白实验) ,复上述步骤,消耗NaC O 溶液的体积为60. 00 mL。
2 2 4
①达到滴定终点时的现象为_______。
②亚硝酰硫酸的纯度为_______(精确到0.1%)。
【答案】(除标注外,每空2分)(1)分液漏斗(1分)
(2)a→de→cb→de→f
(3)防止HNO 分解、挥发;温度较低则反应速率较慢
3
(4)由于生成的NOSOH对该反应有催化作用,导致反应速率加快
4
(5)亚硝酰硫酸遇水分解为硫酸、硝酸和NO(6)①溶液由浅紫色变为无色,且半分钟内颜色不再恢复(1分) ②90.7%
【解析】在装置A中用NaSO 与浓HSO 发生复分解反应制取SO ,由于亚硝酰硫酸是白色片状、多孔或
2 3 2 4 2
粒状晶体,遇水分解,因此制取的SO 气体需经装置C中浓硫酸的干燥作用,将气体通入B中,与浓硝酸
2
在浓硫酸催化下反应产生NOSOH,再经C的干燥作用,由于SO 是大气污染物,同时硝酸有挥发性,挥
4 2
发的硝酸蒸气及未反应的SO 气体可以使用D中NaOH溶液进行吸收,防止大气污染。
2
(1)根据仪器的构造可知,仪器I的名称为分液漏斗;在装置A中NaSO 与浓HSO 发生复分解反应制
2 3 2 4
取SO ,制备SO 反应的化学方程式为: ;
2 2
(2)在装置A中制取SO 气体,在装置C中干燥SO ,导气管连接应该是长进短出,然后使SO 气体由c
2 2 2
通入B装置中,在装置B中发生反应制取NOSOH,为防止NOSOH水解变质,再连接C装置,挥发的硝
4 4
酸蒸气及未反应的SO 气体用D装置的NaOH溶液进行吸收,故按气流从左到右的顺序,上述仪器接口的
2
连接顺序为:a→de→cb→de→f;
(3)在装置B要使用冷水浴,是由于浓硝酸不稳定,受热或光照易分解,冷水浴就可以防止HNO 分解、
3
挥发;温度较低则反应速率较慢;
(4)在上述反应条件下,开始时反应缓慢,但某时刻反应速率明显加快是由于生成的NOSOH对该反应
4
有催化作用,导致反应速率加快;
(5)如果不使用装置C,造成的影响是亚硝酰硫酸遇水分解为硫酸、硝酸和NO;
(6)随着NaC O 溶液的滴入,溶液中KMnO 溶液浓度逐渐减小,当达到滴定终点时,溶液中KMnO 恰
2 2 4 4 4
好反应完全,此时溶液由浅紫色变为无色,半分钟内溶液不再恢复紫色,故其现象为:滴入最后一滴
NaC O 溶液,溶液由浅紫色变为无色,且半分钟内颜色不再恢复;根据方程式可得关系式:
2 2 4
,现在25.00mLNOSO H溶液中含有NOSOH的物质的量
4 4
,则在14.00g样品中含有NOSOH的物质的量
4
,其质量为: ,所以亚硝酰硫
酸的纯度为 。
14.(2022·广东惠州·二模)(13分)某学习小组在实验室模拟工业制备硫氰化钾(KSCN),装置如图:已知:①CS 不溶于水,比水重;NH 不溶于CS;②E内盛放有CS、水和固体催化剂。
2 3 2 2
实验步骤如下:
(1)制备NH SCN溶液:CS+3NH NH SCN + NH HS (该反应比较缓慢)
4 2 3 4 4
①实验前,先要进行的操作是______。
②实验开始时打开K,加热装置A、D,使A中产生的气体缓缓通入E中,至CS 消失。
1 2
则:装置A中反应的化学方程式是_______;装置C的作用是_________
(2)制备KSCN溶液:熄灭A处的酒精灯,关闭K,将装置D加热至95-100℃除去杂质,一段时间后,打
1
开K,缓缓加入适量的KOH溶液,继续保持加热,制得KSCN溶液。
2
①E的仪器名称是_____。
②写出制备KSCN溶液的化学反应方程式______。
(3)制备硫氰化钾晶体:先滤去E中的固体催化剂,再减压蒸发浓缩,冷却结晶,_______,_______,干燥,
得到硫氰化钾晶体。
(4)测定晶体中KSCN的含量:称取1.0g样品配成100mL溶液,量取20.00mL于锥形瓶中,加入几滴
Fe(NO ) 溶液做指示剂,用0.1000mol/LAgNO 标准溶液滴定,达到滴定终点时消耗AgNO 标准溶液
3 3 3 3
20.00mL。
①滴定时发生的反应:SCN- + Ag+= AgSCN↓(白色)。则滴定终点的现象是_____。
②晶体中KSCN的质量分数为______。
【答案】(除标注外,每空2分)(1)检查装置气密性(1分) 2NH Cl+ Ca(OH) CaCl + 2NH ↑+
4 2 2 3
2HO 观察气泡流速,以便控制加热温度
2
(2)三颈烧瓶 NH SCN + KOH KSCN + NH↑+H O
4 3 2
(3)过滤(1分) 洗涤(1分)
(4)当滴入最后一滴AgNO 溶液时,红色恰好褪去,且半分钟内颜色不恢复 97%
3【解析】在装置A中加热氢氧化钙和氯化铵固体制取氨气,装置B中干燥氨气,氨气易溶于水、不溶于二
硫化碳,通过观察装置C中气泡流速,可控制装置A的加热温度,在装置D的三颈烧瓶的下层CS 液体必
2
须浸没导气管口,从而使反应物充分接触,防止发生倒吸。在装置D中发生反应获得NH SCN,由装置D
4
分液漏斗加入KOH溶液与NH SCN反应生成KSCN。滴定时发生的离子反应为SCN-+Ag+=AgSCN↓,以
4
Fe(NO ) 为指示剂,SCN-与Fe3+反应使溶液呈红色,当滴定结束时溶液红色消失,据此判断滴定终点现象。
3 3
由反应消耗AgNO 的物质的量确定样品中KSCN的物质的量,进而可得其质量分数。
3
(1)实验前,应进行的操作是检查装置的气密性;装置A是制取氨气的装置,药品为NH Cl与Ca(OH) ,
4 2
发生反应的化学方程式是2NH Cl+Ca(OH) CaCl +2NH↑+2H O,因为氨气不溶于CS,所以与CS 反应缓
4 2 2 3 2 2 2
慢,应缓慢通气,从而得出装置C的作用可能是通过观察气泡的快慢来调节氨气的流速,以便控制加热温
度,答案为:2NH Cl+Ca(OH) CaCl +2NH↑+2H O;观察气泡流速,以便控制加热温度;
4 2 2 3 2
(2)①E的仪器名称为三颈烧瓶;
②根据上述分析可知,KOH溶液与NH SCN反应生成KSCN,其化学反应方程式为:NH SCN + KOH
4 4
KSCN + NH↑+H O;
3 2
(3)制备KSCN晶体:减压蒸发浓缩,冷却结晶,过滤、洗涤、干燥,以获得硫氰化钾晶体,故答案为:
过滤;洗涤;
(4)①滴定时发生的离子反应为SCN-+Ag+=AgSCN↓,则刚好沉淀完时的锥形瓶中颜色变化是:红色褪
为无色(或“浅黄色”、“黄色”),即滴定终点现象为:当滴入最后一滴AgNO 溶液时,红色恰好褪去,
3
且半分钟内颜色不恢复;
②由反应SCN-+Ag+= AgSCN↓,可得出n(KSCN)=n(AgNO)=0.1000mol/L×0.02L
3
=0.002mol,KSCN的质量分数为: =97%,答案为:97%。
15.(2021·四川广安·模拟预测)(13分)碘酸钙[Ca(IO)]是广泛使用的既能补钙又能补碘的新型食品添
3 2
加剂,不溶于乙醇,在水中的溶解度随温度降低而减小。实验室制取Ca(IO) 的流程如图所示:
3 2已知:碘酸(HIO )是易溶于水的强酸,不溶于有机溶剂。
3
(1)实验流程中“转化”步骤是为了制得碘酸,该过程在下图所示的装置中进行(部分仪器省略)。
①盛装浓盐酸的仪器的名称为___________。
②橡皮管a的作用是___________。
③装置A中反应需要加热,其反应的离子方程式___________。
(2)三颈烧瓶中发生“转化”的化学方程式___________。
(3)流程中采用冰水浴的目的是__。
(4)有关该实验说法正确的是__。
A.分离出CCl 的操作为分液。
4
B.“调pH=10”后的溶液中只含有KIO
3
C.制得的碘酸钙可选用酒精溶液洗涤
(5)准确称取产品0.25g,加酸溶解后,再加入足量KI发生反应 +5I-+6H+=3I +3H O,滴入2~3滴淀粉溶
2 2
液,用0.2000 mol·L-1NaSO 溶液滴定(I+2 =2I-+ )至终点,消耗NaSO 溶液30.00mL。达滴定终
2 2 3 2 2 2 3
点时的现象是___________, 产品中Ca(IO) 的质量分数___________ [已知Ca(IO) 的摩尔质量:
3 2 3 2
390g·mol-1]
【答案】(除标注外,每空2分)(1)分液漏斗(1分) 平衡压强,使液体顺利流下(1分)
(2)(3)降低碘酸钙的溶解度,便于析出碘酸钙
(4)AC
(5)溶液由蓝色变为无色,且半分钟内不恢复蓝色(1分) 78%
【解析】碘的四氯化碳溶液中通入氯气和水,反应生成碘酸和盐酸,用分液法分离出四氯化碳,在水溶液
中加氢氧化钾调节pH=10,生成氯化钾和碘酸钾,在冰水浴条件下加氯化钙生成碘酸钙沉淀,过滤得产品
碘酸钙。
(1)①根据图示,盛装浓盐酸的仪器的名称为分液漏斗。
②橡皮管a连接分液漏斗上口和烧瓶,使烧瓶和分液漏斗内压强相同,作用是平衡压强,使液体顺利流下。
③装置A中二氧化锰和浓盐酸在加热条件下反应生成氯化锰、氯气、水,反应的离子方程式是
;
(2)三颈烧瓶中氯气、碘、水发生“转化”生成盐酸和碘酸,反应的化学方程式为
;
(3)碘酸钙在水中的溶解度随温度降低而减小,流程中采用冰水浴的目的是降低碘酸钙的溶解度,便于
析出碘酸钙。
(4)A.CCl 是难溶于水的液体,用分液法分离出CCl ,故A正确;B.“调pH=10”后的溶液中含有
4 4
KIO 、KCl,故B错误;C.碘酸钙不溶于乙醇,制得的碘酸钙用酒精溶液洗涤,可减少损失,故C正确;
3
选AC;
(5)达到滴定终点,碘被消耗完全,所以达滴定终点时的现象是溶液由蓝色变为无色,且半分钟内不恢
复蓝色; 根据 +5I-+6H+=3I +3H O、I+2 =2I-+ 得关系式 ~~3I ~~6 ,样品中Ca(IO) 的
2 2 2 2 3 2
物质的量为 ,质量分数为 。