文档内容
第 29 讲 化学综合实验
第一部分:高考真题感悟
1.(2022·全国甲卷)硫化钠可广泛用于染料、医药行业。工业生产的硫化钠粗品中常含有一定量的煤灰
及重金属硫化物等杂质。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。实验室中常用95%乙醇重结晶
纯化硫化钠粗品。回答下列问题:
(1)工业上常用芒硝( )和煤粉在高温下生产硫化钠,同时生成CO,该反应的化学方程式为
_______。
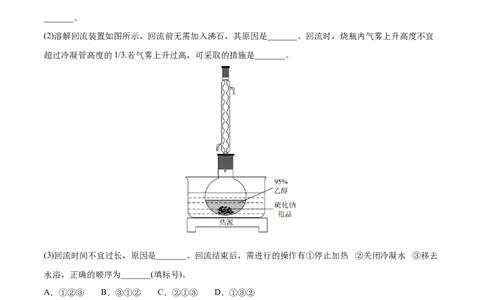
(2)溶解回流装置如图所示,回流前无需加入沸石,其原因是_______。回流时,烧瓶内气雾上升高度不宜
超过冷凝管高度的1/3.若气雾上升过高,可采取的措施是_______。
(3)回流时间不宜过长,原因是_______。回流结束后,需进行的操作有①停止加热 ②关闭冷凝水 ③移去
水浴,正确的顺序为_______(填标号)。
A.①②③ B.③①② C.②①③ D.①③②
(4)该实验热过滤操作时,用锥形瓶而不能用烧杯接收滤液,其原因是_______。过滤除去的杂质为_______。
若滤纸上析出大量晶体,则可能的原因是_______。
(5)滤液冷却、结晶、过滤,晶体用少量_______洗涤,干燥,得到 。
2.(2022·全国乙卷)二草酸合铜(Ⅱ)酸钾( )可用于无机合成、功能材料制备。实验室制备
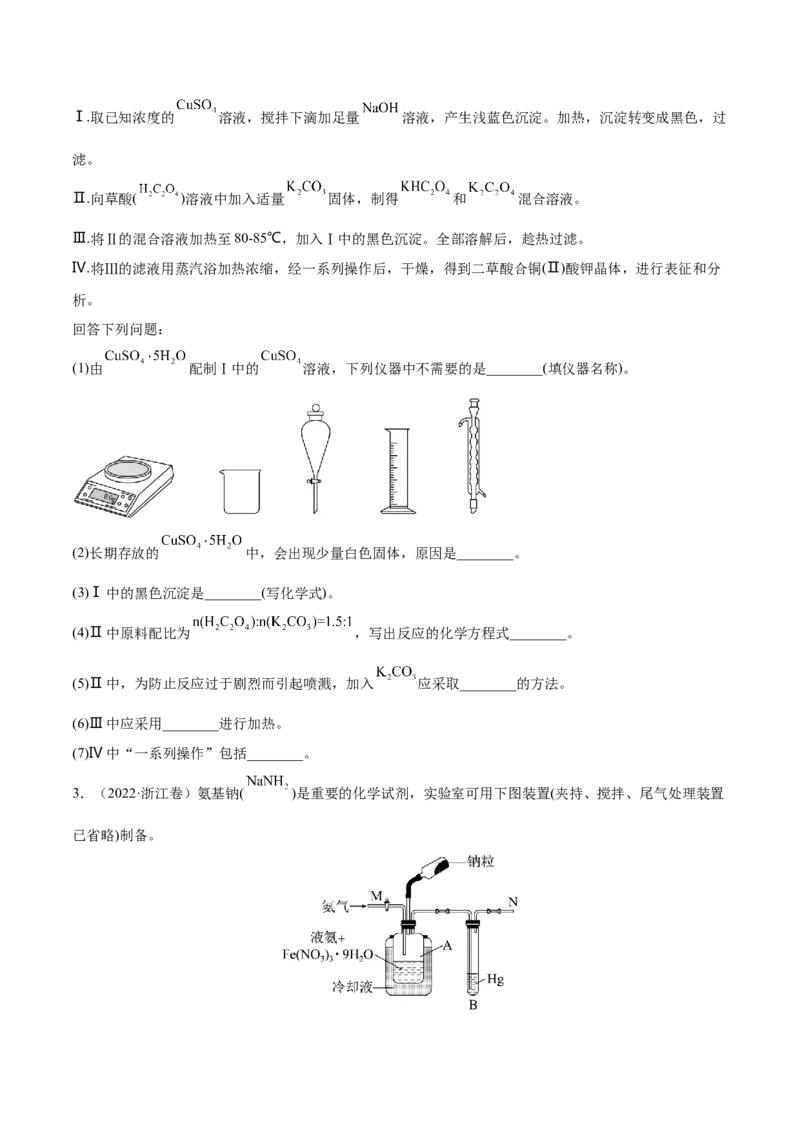
二草酸合铜(Ⅱ)酸钾可采用如下步骤:Ⅰ.取已知浓度的 溶液,搅拌下滴加足量 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过
滤。
Ⅱ.向草酸( )溶液中加入适量 固体,制得 和 混合溶液。
Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分
析。
回答下列问题:
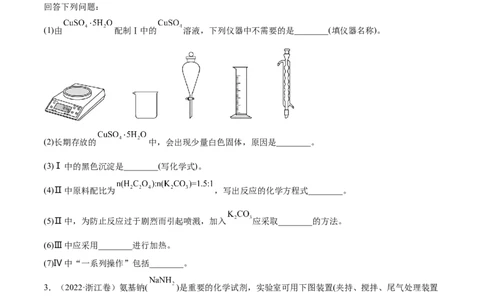
(1)由 配制Ⅰ中的 溶液,下列仪器中不需要的是________(填仪器名称)。
(2)长期存放的 中,会出现少量白色固体,原因是________。
(3)Ⅰ中的黑色沉淀是________(写化学式)。
(4)Ⅱ中原料配比为 ,写出反应的化学方程式________。
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入 应采取________的方法。
(6)Ⅲ中应采用________进行加热。
(7)Ⅳ中“一系列操作”包括________。
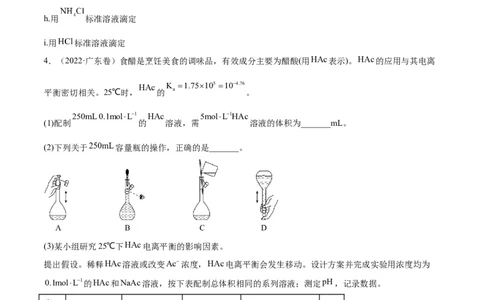
3.(2022·浙江卷)氨基钠( )是重要的化学试剂,实验室可用下图装置(夹持、搅拌、尾气处理装置
已省略)制备。简要步骤如下:
Ⅰ.在瓶A中加入 液氨和 ,通入氨气排尽密闭体系中空气,搅拌。
Ⅱ.加入5g钠粒,反应,得 粒状沉积物。
Ⅲ.除去液氨,得产品 。
已知: 几乎不溶于液氨,易与水、氧气等反应。
请回答:
(1) 的作用是_______;装置B的作用是_______。
(2)步骤Ⅰ,为判断密闭体系中空气是否排尽,请设计方案_______。
(3)步骤Ⅱ,反应速率应保持在液氨微沸为宜。为防止速率偏大,可采取的措施有_______。
(4)下列说法不正确的是_______。
A.步骤Ⅰ中,搅拌的目的是使 均匀地分散在液氨中
B.步骤Ⅱ中,为判断反应是否已完成,可在N处点火,如无火焰,则反应己完成
C.步骤Ⅲ中,为避免污染,应在通风橱内抽滤除去液氨,得到产品
D.产品 应密封保存于充满干燥氮气的瓶中
(5)产品分析:假设 是产品 的唯一杂质,可采用如下方法测定产品 纯度。从下列选项
中选择最佳操作并排序_______。
准确称取产品 计算
a.准确加入过量的水
b.准确加入过量的 标准溶液c.准确加入过量的 标准溶液
d.滴加甲基红指示剂(变色的 范围4.4~6.2)
e.滴加石蕊指示剂(变色的 范围4.5~8.3)
f.滴加酚酞指示剂(变色的 范围8.2~10.0)
g.用 标准溶液滴定
h.用 标准溶液滴定
i.用 标准溶液滴定
4.(2022·广东卷)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的应用与其电离
HAc K 1.75105 104.76
平衡密切相关。25℃时, 的 a 。
250mL 0.1molL1 HAc 5molL1HAc
(1)配制 的 溶液,需 溶液的体积为_______mL。
(2)下列关于250mL容量瓶的操作,正确的是_______。
(3)某小组研究25℃下HAc电离平衡的影响因素。
提出假设。稀释HAc溶液或改变Ac浓度,HAc电离平衡会发生移动。设计方案并完成实验用浓度均为
0.1molL1的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
序 vHAc/mL vNaAc/mL VH O/mL nNaAc:nHAc pH
号 2
Ⅰ 40.00 / / 0 2.86
Ⅱ 4.00 / 36.00 0 3.36
…
Ⅶ 4.00 a b 3:4 4.53
Ⅷ 4.00 4.00 32.00 1:1 4.65①根据表中信息,补充数据:a_______,b_______。
②由实验Ⅰ和Ⅱ可知,稀释HAc溶液,电离平衡_______(填”正”或”逆”)
向移动;结合表中数据,给出判断理由:_______。
Ac HAc
③由实验Ⅱ~VIII可知,增大 浓度, 电离平衡逆向移动。
实验结论假设成立。
nNaAc
(4)小组分析上表数据发现:随着 nHAc 的增加,c H+ 的值逐渐接近HAc的K 。
a
nNaAc
1
查阅资料获悉:一定条件下,按 nHAc 配制的溶液中,c
H+
的值等于HAc的K 。
a
pH4.65 K 104.76
对比数据发现,实验VIII中 与资料数据 a 存在一定差异;推测可能由物质浓度准确程度
不够引起,故先准确测定HAc溶液的浓度再验证。
20.00mLHAc 0.1000molL1NaOH
①移取 溶液,加入2滴酚酞溶液,用 溶液滴定至终点,消耗体积为
22.08mL HAc molL1
,则该 溶液的浓度为_______ 。在答题卡虚线框中,画出上述过程的滴定曲线示意图
并标注滴定终点_______。
HAc 0.1000molL1NaOH HAc NaAc
②用上述 溶液和 溶液,配制等物质的量的 与 混合溶液,测定pH,结果
与资料数据相符。
0.1molL1 HAc NaOH HAc K
(5)小组进一步提出:如果只有浓度均约为 的 和 溶液,如何准确测定 的 a?小
组同学设计方案并进行实验。请完成下表中Ⅱ的内容。
Ⅰ 移取20.00mLHAc溶液,用NaOH溶液滴定至终点,消耗NaOH溶液 V
1
mL
Ⅱ _______,测得溶液的pH为4.76
实验总结 得到的结果与资料数据相符,方案可行。
K
(6)根据 a可以判断弱酸的酸性强弱。写出一种无机弱酸及其用途_______。
5.(2022·湖南卷)某实验小组以 溶液为原料制备 ,并用重量法测定产品中 的含量。设计了如下实验方案:
可选用试剂: 晶体、 溶液、浓 、稀 、 溶液、蒸馏水
步骤1. 的制备
按如图所示装置进行实验,得到 溶液,经一系列步骤获得 产品。
步骤2,产品中 的含量测定
①称取产品 ,用 水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的 溶液,
③沉淀完全后, 水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为 。
回答下列问题:
(1)Ⅰ是制取_______气体的装置,在试剂a过量并微热时,发生主要反应的化学方程式为_______;
(2)Ⅰ中b仪器的作用是_______;Ⅲ中的试剂应选用_______;
(3)在沉淀过程中,某同学在加入一定量热的 溶液后,认为沉淀已经完全,判断沉淀已完全的方法是
_______;
(4)沉淀过程中需加入过量的 溶液,原因是_______;
(5)在过滤操作中,下列仪器不需要用到的是_______(填名称);
(6)产品中 的质量分数为_______(保留三位有效数字)。
第二部分:最新模拟精练完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·河南开封·二模)实验室利用如图所示装置(已略去夹持、加热及搅拌装置)制取五氯化锑,反应
如下:SbCl +Cl SbCl (相关物质性质如下表)。下列说法错误的是
3 2 5
物质 熔点 沸点 性质
SbCl 73.4℃ 220.3℃ 极易水解
3
79℃/2.9kPa(140℃
SbCl 3.5℃ 极易水解
5 分解)
A.试剂X可以使用无水CaCl
2
B.冷凝管的作用是冷凝回流,从a口进水,b口出水
C.此实验中采用水浴加热的方式比较合适
D.可采用减压蒸馏的方法将SbCl ,从反应液中分离
5
2.(2022·河南许昌·二模)实验室可用下图装置制备乙酸乙酯,实验开始时先加热至110~120℃,再滴入
乙醇和冰醋酸并使滴入速率与蒸出液体的速率几乎相等,滴加完毕后升温到130℃至不再有液体蒸出。下
列说法错误的是A.冷凝管的进水口为b
B.可用油浴加热
C.滴加速率不宜过快,是为了防止副反应增多
D.蒸出的液体用饱和碳酸钠溶液洗涤、分液可得到粗乙酸乙酯
3.(2022·四川内江·模拟预测)用下图所示装置及药品制备相应的气体,其中不能实现的是( )
A.制取NH B.制取乙烯 C.制取Cl D.制取SO
3 2 2
4.(2022·广东广州·模拟预测)室温下,某同学用下图中装置在通风棚中进行如下实验:
实验 现象
试管Ⅰ中开始无明显现象,后逐渐有微小气泡生成,反应越来越剧烈,试
管口上方出现红棕色气体,溶液呈蓝色。
试管Ⅱ中剧烈反应,迅速生成大量红棕色气体,溶液呈绿色:之后向溶液
中持续通入 ,溶液又变为蓝色。
下列说法不正确的是A.试管Ⅰ中浅红棕色气体为 ,由铜还原硝酸生成
B.等质量的Cu完全溶解时,Ⅰ中消耗的 更少
C.试管Ⅱ中反应后溶液颜色与试管Ⅰ中的不同,可能是由于溶有
D.蓝色的 呈平面四边形结构,中心离子不可能为 杂化
5.(2022·广东广州·模拟预测)下列实验操作能达到实验目的的是
选项 实验操作 实验目的
加热氯化铵和氢氧化钙的混合物,并将产生的气体通过碱石灰进
A 制备干燥的氨气
行干燥验证 的金属活动大于
B 向 溶液中加入一小块金属钠
C 先将浓硫酸加入烧杯中,后缓缓倒入蒸馏水,并不断搅拌 稀释浓硫酸
D 分别测量饱和 与饱和 溶液的 证明 强于
6.(2022·上海·复旦附中二模)在下列实验操作中,会导致测量结果偏小的是
A.胆矾品体中结晶水含量测定实验中,坩埚中有受热不分解的物质
B.灼烧法测定 NaCO、NaHCO 混合物中NaCO 的质量分数实验中,未进行恒重操作
2 3 3 2 3
C.HCl标准液滴定未知浓度的NaOH溶液实验中,锥形瓶内溶液溅出
D.气体摩尔体积的测定中,反应结束后未冷却至室温便读数
7.(2022·辽宁辽阳·二模)下列结论正确且与实验操作及现象相对应的是
实验操作及现象 结论
A 某气体能使湿润的蓝色石蕊试纸变红 该气体的水溶液呈碱性
向某钠盐的溶液中加入稀盐酸,产生能使澄
B 该钠盐可能是碳酸钠
清石灰水变浑浊的气体
向等体积 的HA溶液和HB溶液中分别
C HA的酸性比HB的强
加入足量的锌,HA溶液放出的氢气更多
向等浓度的NaCl、NaBr的混合溶液中加入少
D
量 溶液,先有浅黄色沉淀产生
8.(2022·北京·杨镇第一中学模拟预测)最适用于鉴别丁香酚和肉桂酸的试剂是
A.银氨溶液 B.溴的四氯化碳溶液
C.氯化铁溶液 D.氢氧化钠溶液
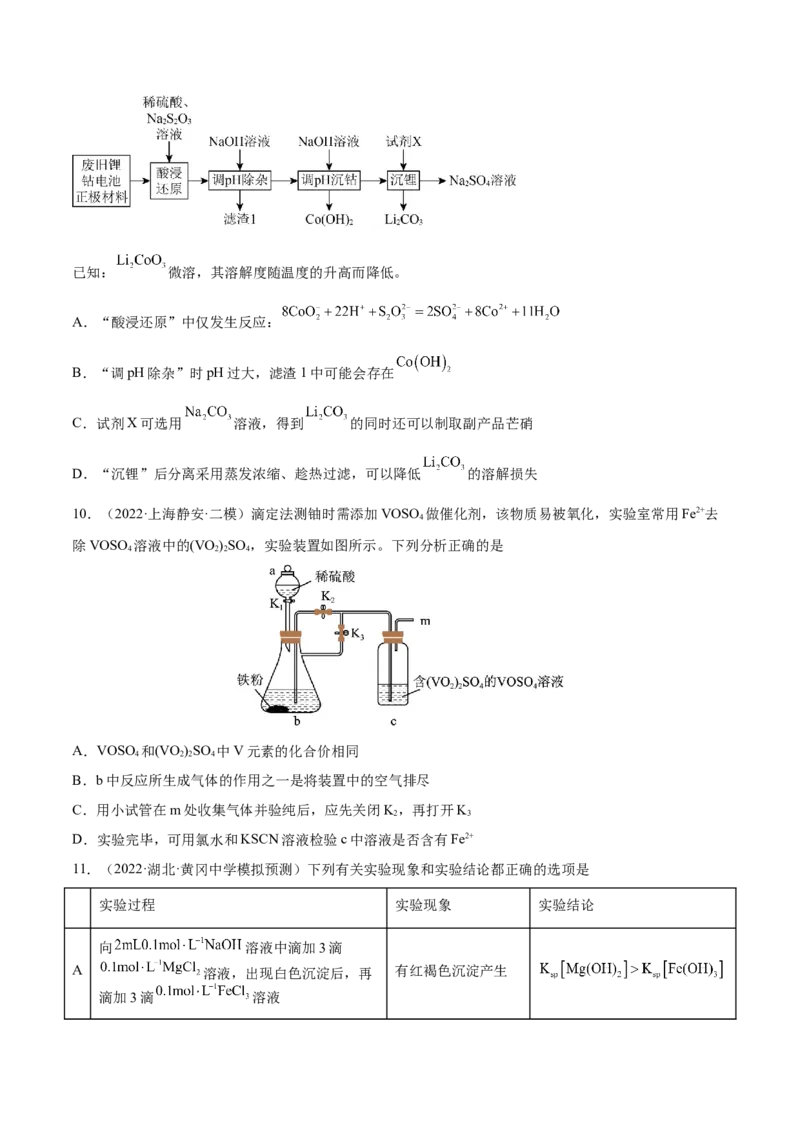
9.(2022·江西·模拟预测)以废旧锂钴电池正极材料( 颗粒粉末附着在铝箔表面)为原料,提纯回收
钴元素与锂元素的工艺流程如下。下列叙述错误的是已知: 微溶,其溶解度随温度的升高而降低。
A.“酸浸还原”中仅发生反应:
B.“调pH除杂”时pH过大,滤渣1中可能会存在
C.试剂X可选用 溶液,得到 的同时还可以制取副产品芒硝
D.“沉锂”后分离采用蒸发浓缩、趁热过滤,可以降低 的溶解损失
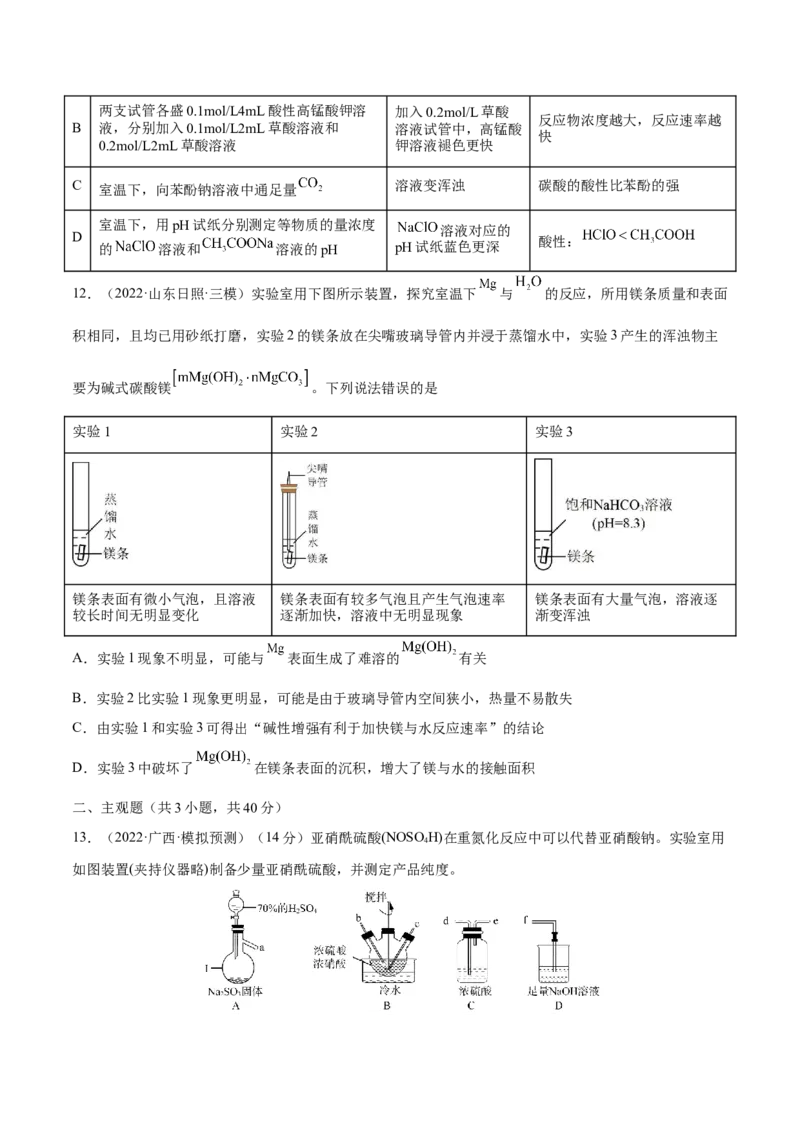
10.(2022·上海静安·二模)滴定法测铀时需添加VOSO 做催化剂,该物质易被氧化,实验室常用Fe2+去
4
除VOSO 溶液中的(VO )SO ,实验装置如图所示。下列分析正确的是
4 2 2 4
A.VOSO 和(VO )SO 中V元素的化合价相同
4 2 2 4
B.b中反应所生成气体的作用之一是将装置中的空气排尽
C.用小试管在m处收集气体并验纯后,应先关闭K,再打开K
2 3
D.实验完毕,可用氯水和KSCN溶液检验c中溶液是否含有Fe2+
11.(2022·湖北·黄冈中学模拟预测)下列有关实验现象和实验结论都正确的选项是
实验过程 实验现象 实验结论
向 溶液中滴加3滴
A 溶液,出现白色沉淀后,再 有红褐色沉淀产生
滴加3滴 溶液两支试管各盛0.1mol/L4mL酸性高锰酸钾溶 加入0.2mol/L草酸
反应物浓度越大,反应速率越
B 液,分别加入0.1mol/L2mL草酸溶液和 溶液试管中,高锰酸
快
0.2mol/L2mL草酸溶液 钾溶液褪色更快
C 室温下,向苯酚钠溶液中通足量 溶液变浑浊 碳酸的酸性比苯酚的强
室温下,用pH试纸分别测定等物质的量浓度
溶液对应的
D 酸性:
的 溶液和 溶液的pH pH试纸蓝色更深
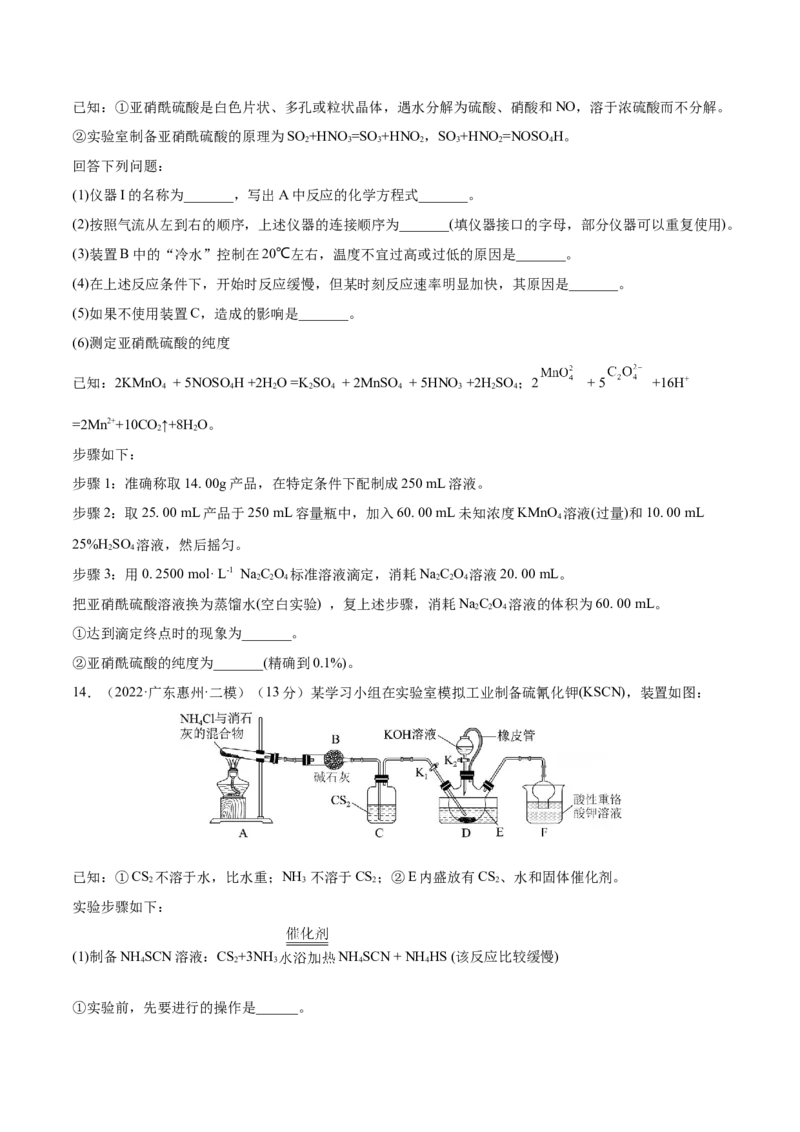
12.(2022·山东日照·三模)实验室用下图所示装置,探究室温下 与 的反应,所用镁条质量和表面
积相同,且均已用砂纸打磨,实验2的镁条放在尖嘴玻璃导管内并浸于蒸馏水中,实验3产生的浑浊物主
要为碱式碳酸镁 。下列说法错误的是
实验1 实验2 实验3
镁条表面有微小气泡,且溶液 镁条表面有较多气泡且产生气泡速率 镁条表面有大量气泡,溶液逐
较长时间无明显变化 逐渐加快,溶液中无明显现象 渐变浑浊
A.实验1现象不明显,可能与 表面生成了难溶的 有关
B.实验2比实验1现象更明显,可能是由于玻璃导管内空间狭小,热量不易散失
C.由实验1和实验3可得出“碱性增强有利于加快镁与水反应速率”的结论
D.实验3中破坏了 在镁条表面的沉积,增大了镁与水的接触面积
二、主观题(共3小题,共40分)
13.(2022·广西·模拟预测)(14分)亚硝酰硫酸(NOSOH)在重氮化反应中可以代替亚硝酸钠。实验室用
4
如图装置(夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。已知:①亚硝酰硫酸是白色片状、多孔或粒状晶体,遇水分解为硫酸、硝酸和NO,溶于浓硫酸而不分解。
②实验室制备亚硝酰硫酸的原理为SO +HNO =SO+HNO ,SO +HNO =NOSO H。
2 3 3 2 3 2 4
回答下列问题:
(1)仪器I的名称为_______,写出A中反应的化学方程式_______。
(2)按照气流从左到右的顺序,上述仪器的连接顺序为_______(填仪器接口的字母,部分仪器可以重复使用)。
(3)装置B中的“冷水”控制在20℃左右,温度不宜过高或过低的原因是_______。
(4)在上述反应条件下,开始时反应缓慢,但某时刻反应速率明显加快,其原因是_______。
(5)如果不使用装置C,造成的影响是_______。
(6)测定亚硝酰硫酸的纯度
已知:2KMnO + 5NOSOH +2H O =K SO + 2MnSO + 5HNO +2H SO ;2 + 5 +16H+
4 4 2 2 4 4 3 2 4
=2Mn2++10CO ↑+8H O。
2 2
步骤如下:
步骤1:准确称取14. 00g产品,在特定条件下配制成250 mL溶液。
步骤2:取25. 00 mL产品于250 mL容量瓶中,加入60. 00 mL未知浓度KMnO 溶液(过量)和10. 00 mL
4
25%H SO 溶液,然后摇匀。
2 4
步骤3:用0. 2500 mol· L-1 NaC O 标准溶液滴定,消耗NaC O 溶液20. 00 mL。
2 2 4 2 2 4
把亚硝酰硫酸溶液换为蒸馏水(空白实验) ,复上述步骤,消耗NaC O 溶液的体积为60. 00 mL。
2 2 4
①达到滴定终点时的现象为_______。
②亚硝酰硫酸的纯度为_______(精确到0.1%)。
14.(2022·广东惠州·二模)(13分)某学习小组在实验室模拟工业制备硫氰化钾(KSCN),装置如图:
已知:①CS 不溶于水,比水重;NH 不溶于CS;②E内盛放有CS、水和固体催化剂。
2 3 2 2
实验步骤如下:
(1)制备NH SCN溶液:CS+3NH NH SCN + NH HS (该反应比较缓慢)
4 2 3 4 4
①实验前,先要进行的操作是______。②实验开始时打开K,加热装置A、D,使A中产生的气体缓缓通入E中,至CS 消失。
1 2
则:装置A中反应的化学方程式是_______;装置C的作用是_________
(2)制备KSCN溶液:熄灭A处的酒精灯,关闭K,将装置D加热至95-100℃除去杂质,一段时间后,打
1
开K,缓缓加入适量的KOH溶液,继续保持加热,制得KSCN溶液。
2
①E的仪器名称是_____。
②写出制备KSCN溶液的化学反应方程式______。
(3)制备硫氰化钾晶体:先滤去E中的固体催化剂,再减压蒸发浓缩,冷却结晶,_______,_______,干燥,
得到硫氰化钾晶体。
(4)测定晶体中KSCN的含量:称取1.0g样品配成100mL溶液,量取20.00mL于锥形瓶中,加入几滴
Fe(NO ) 溶液做指示剂,用0.1000mol/LAgNO 标准溶液滴定,达到滴定终点时消耗AgNO 标准溶液
3 3 3 3
20.00mL。
①滴定时发生的反应:SCN- + Ag+= AgSCN↓(白色)。则滴定终点的现象是_____。
②晶体中KSCN的质量分数为______。
15.(2021·四川广安·模拟预测)(13分)碘酸钙[Ca(IO)]是广泛使用的既能补钙又能补碘的新型食品添
3 2
加剂,不溶于乙醇,在水中的溶解度随温度降低而减小。实验室制取Ca(IO) 的流程如图所示:
3 2
已知:碘酸(HIO )是易溶于水的强酸,不溶于有机溶剂。
3
(1)实验流程中“转化”步骤是为了制得碘酸,该过程在下图所示的装置中进行(部分仪器省略)。
①盛装浓盐酸的仪器的名称为___________。
②橡皮管a的作用是___________。
③装置A中反应需要加热,其反应的离子方程式___________。
(2)三颈烧瓶中发生“转化”的化学方程式___________。
(3)流程中采用冰水浴的目的是__。(4)有关该实验说法正确的是__。
A.分离出CCl 的操作为分液。
4
B.“调pH=10”后的溶液中只含有KIO
3
C.制得的碘酸钙可选用酒精溶液洗涤
(5)准确称取产品0.25g,加酸溶解后,再加入足量KI发生反应 +5I-+6H+=3I +3H O,滴入2~3滴淀粉溶
2 2
液,用0.2000 mol·L-1NaSO 溶液滴定(I+2 =2I-+ )至终点,消耗NaSO 溶液30.00mL。达滴定终
2 2 3 2 2 2 3
点时的现象是___________, 产品中Ca(IO) 的质量分数___________ [已知Ca(IO) 的摩尔质量:
3 2 3 2
390g·mol-1]