文档内容
第 29 讲 水的电离和溶液的酸碱性
(模拟精练+真题演练)
完卷时间:50分钟
可能用到的相对原子质量:H 1 N 14 O 16 S 32 Cu 64
一、选择题(每小题只有一个正确选项,共12×5分)
1.(2023·湖南郴州·校联考模拟预测)实验小组进行实验检测菠菜中草酸和草酸盐的含量(均以草酸计),
主要操作包括:
①菠菜样品研磨成汁,稀硫酸浸泡后取澄清溶液;②转移定容①中的澄清溶液,得待测液;③移取
20.00mL待测液,用 的酸性 溶液滴定。
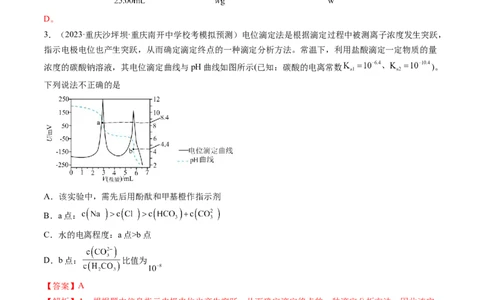
上述操作中,未用到的仪器为
A. B. C. D.
【答案】B
【解析】实验过程中,①所需仪器为研钵、烧杯、玻璃棒、漏斗;②所需仪器为玻璃棒、容量瓶、胶头滴
管;③所需仪器为酸式滴定管、锥形瓶。选项中A为研钵,B为分液漏斗,C为烧杯,D为酸式滴定管。
上述操作中,未用到的仪器为分液漏斗,故选B项。
2.(2023·湖南娄底·统考模拟预测)某小组设计实验测定胆矾( )纯度(杂质不参与反应):称
取 胆矾样品溶于蒸馏水,加入足量KI溶液,充分反应后,过滤。把滤液配制成250mL溶液,准确量
取配制溶液25.00mL于锥形瓶中,滴加2滴溶液X,用 溶液滴定至终点,消耗滴定液
Vml。涉及有关反应如下: , 。下列叙述正确的是
A.X为甲基橙溶液
B.滴加 溶液时选择滴定管如图所示C.滴定管装液之前最后一步操作是水洗
D.胆矾纯度为
【答案】D
【解析】A.滴定反应为碘单质与硫代硫酸钠反应,因为碘单质遇淀粉变蓝,则指示剂X为淀粉溶液,A
项错误;B. 水解而使其溶液显碱性,因此滴加该溶液要选择碱式滴定管,B项错误;C.滴定管
装液之前最后一步操作是润洗,即用待装液润洗滴定管,C项错误;D.根据关系式:
可知,胆矾纯度为 ,D项正确;答案选
D。
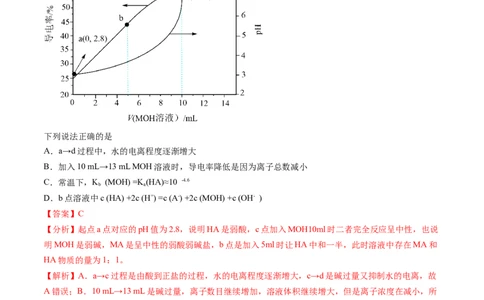
3.(2023·重庆沙坪坝·重庆南开中学校考模拟预测)电位滴定法是根据滴定过程中被测离子浓度发生突跃,
指示电极电位也产生突跃,从而确定滴定终点的一种滴定分析方法。常温下,利用盐酸滴定一定物质的量
浓度的碳酸钠溶液,其电位滴定曲线与pH曲线如图所示(已知:碳酸的电离常数 )。
下列说法不正确的是
A.该实验中,需先后用酚酞和甲基橙作指示剂
B.a点:
C.水的电离程度:a点>b点
D.b点: 比值为
【答案】A
【解析】A.根据题中信息指示电极电位也产生突跃,从而确定滴定终点的一种滴定分析方法,因此该实
验中不需要用指示剂,故A错误;B.a点溶质是碳酸氢钠和氯化钠且两者浓度相等,碳酸氢根既要电离又
要水解,因此 ,故B正确;C.a点溶质是碳酸氢钠和氯化钠,促进
水的电离,而b点溶质是氯化钠和碳酸,抑制水的电离,因此水的电离程度:a点>b点,故C正确;D.
b点: ,故D正确。
综上所述,答案为A。
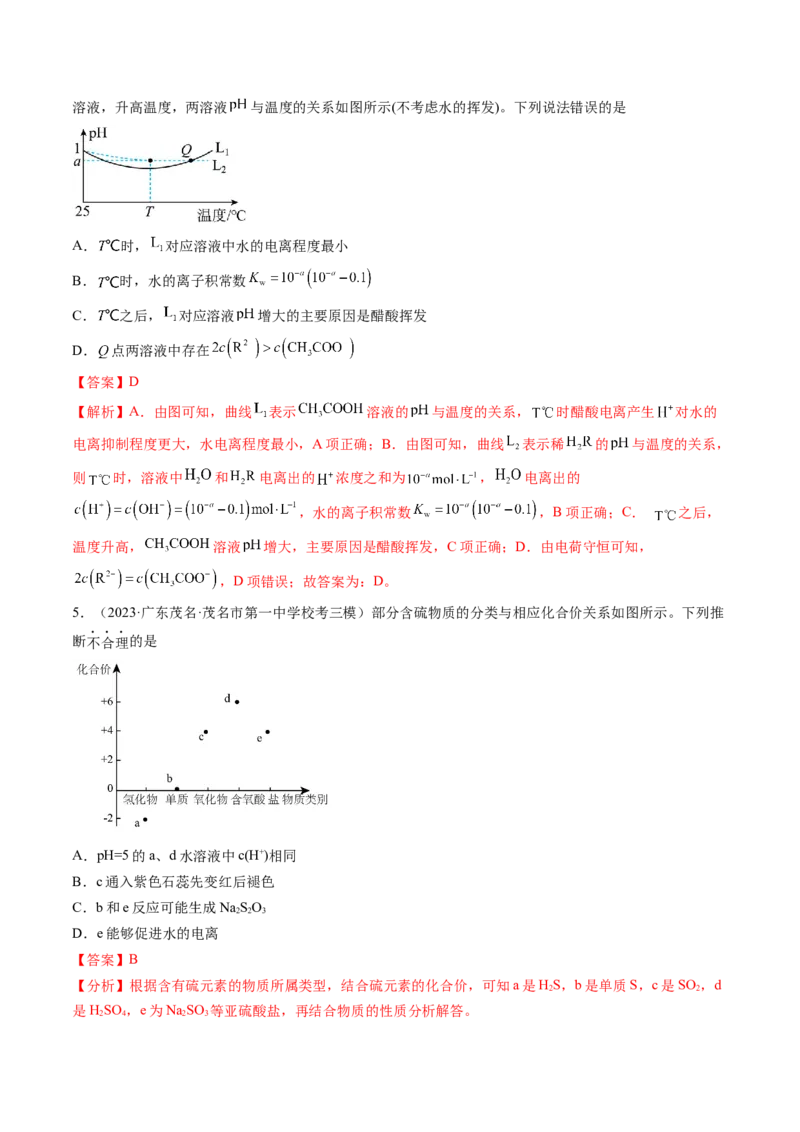
4.(2023·辽宁·校联考模拟预测)已知 下, 均为1的 (难挥发的二元强酸)溶液和溶液,升高温度,两溶液 与温度的关系如图所示(不考虑水的挥发)。下列说法错误的是
A. 时, 对应溶液中水的电离程度最小
B. 时,水的离子积常数
C. 之后, 对应溶液 增大的主要原因是醋酸挥发
D. 点两溶液中存在
【答案】D
【解析】A.由图可知,曲线 表示 溶液的 与温度的关系, 时醋酸电离产生 对水的
电离抑制程度更大,水电离程度最小,A项正确;B.由图可知,曲线 表示稀 的 与温度的关系,
则 时,溶液中 和 电离出的 浓度之和为 , 电离出的
,水的离子积常数 ,B项正确;C. 之后,
温度升高, 溶液 增大,主要原因是醋酸挥发,C项正确;D.由电荷守恒可知,
,D项错误;故答案为:D。
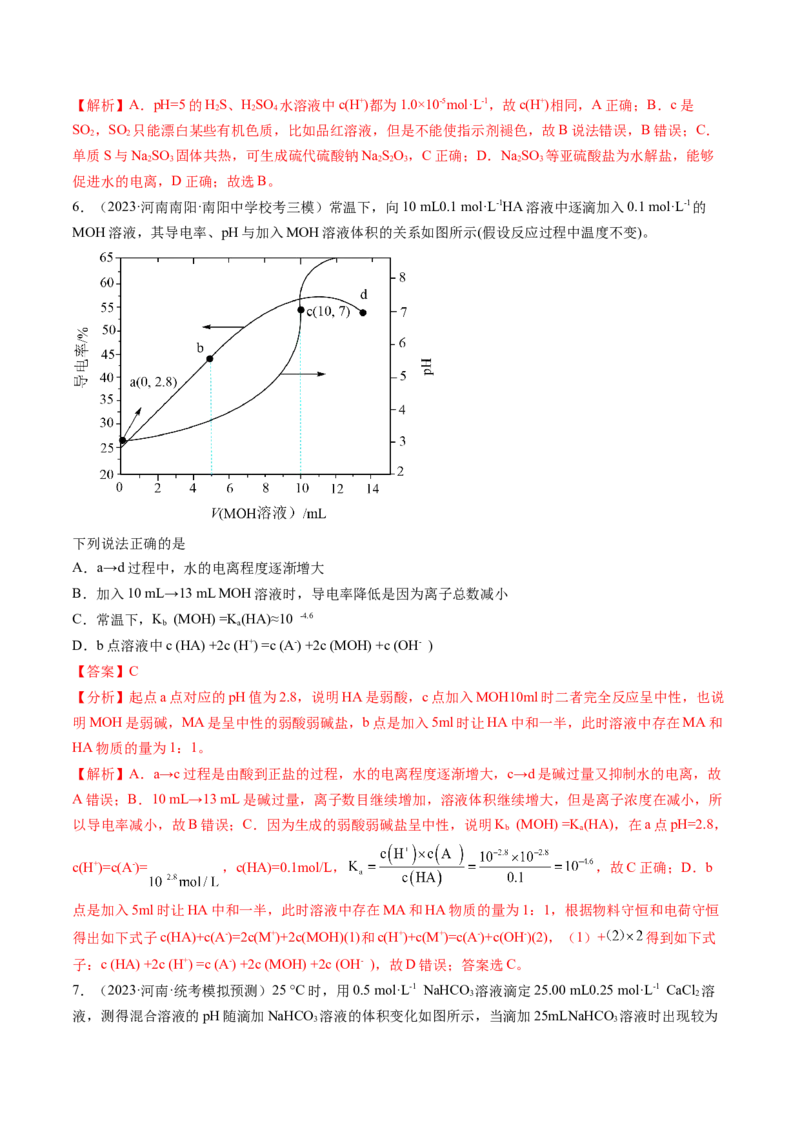
5.(2023·广东茂名·茂名市第一中学校考三模)部分含硫物质的分类与相应化合价关系如图所示。下列推
断不合理的是
A.pH=5的a、d水溶液中c(H+)相同
B.c通入紫色石蕊先变红后褪色
C.b和e反应可能生成NaSO
2 2 3
D.e能够促进水的电离
【答案】B
【分析】根据含有硫元素的物质所属类型,结合硫元素的化合价,可知a是HS,b是单质S,c是SO ,d
2 2
是HSO ,e为NaSO 等亚硫酸盐,再结合物质的性质分析解答。
2 4 2 3【解析】A.pH=5的HS、HSO 水溶液中c(H+)都为1.0×10-5mol·L-1,故c(H+)相同,A正确;B.c是
2 2 4
SO ,SO 只能漂白某些有机色质,比如品红溶液,但是不能使指示剂褪色,故B说法错误,B错误;C.
2 2
单质S与NaSO 固体共热,可生成硫代硫酸钠NaSO,C正确;D.NaSO 等亚硫酸盐为水解盐,能够
2 3 2 2 3 2 3
促进水的电离,D正确;故选B。
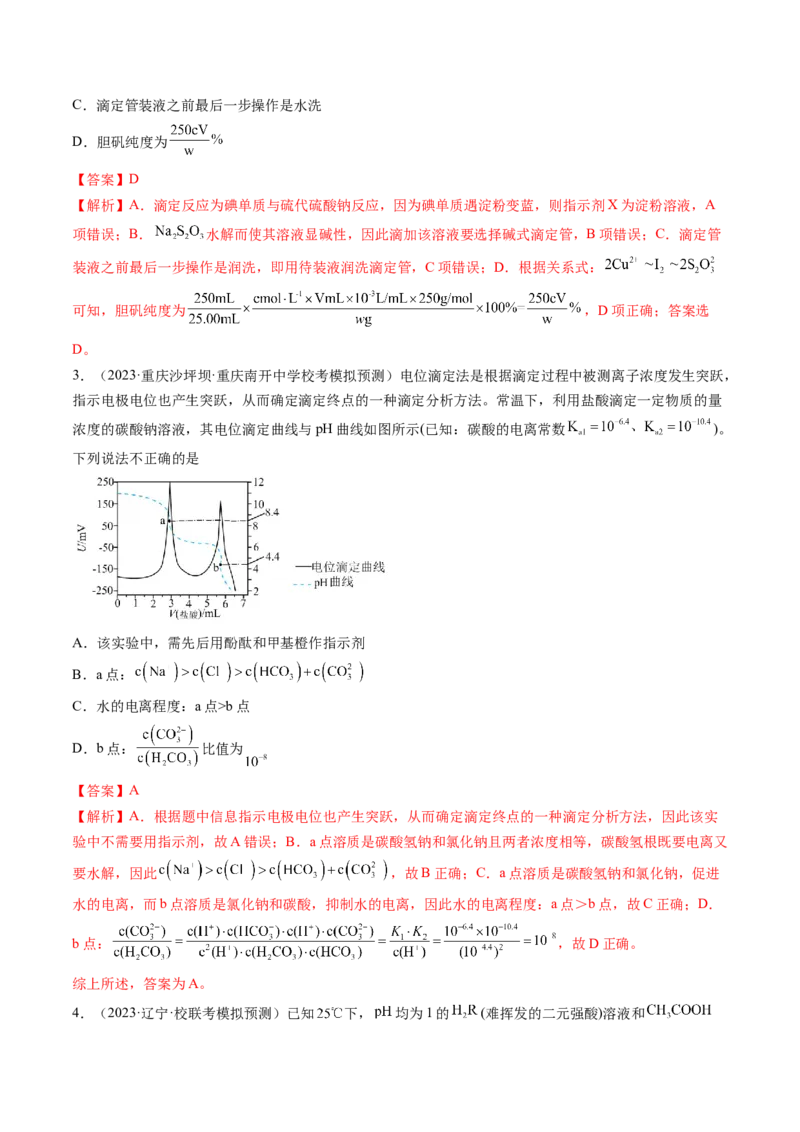
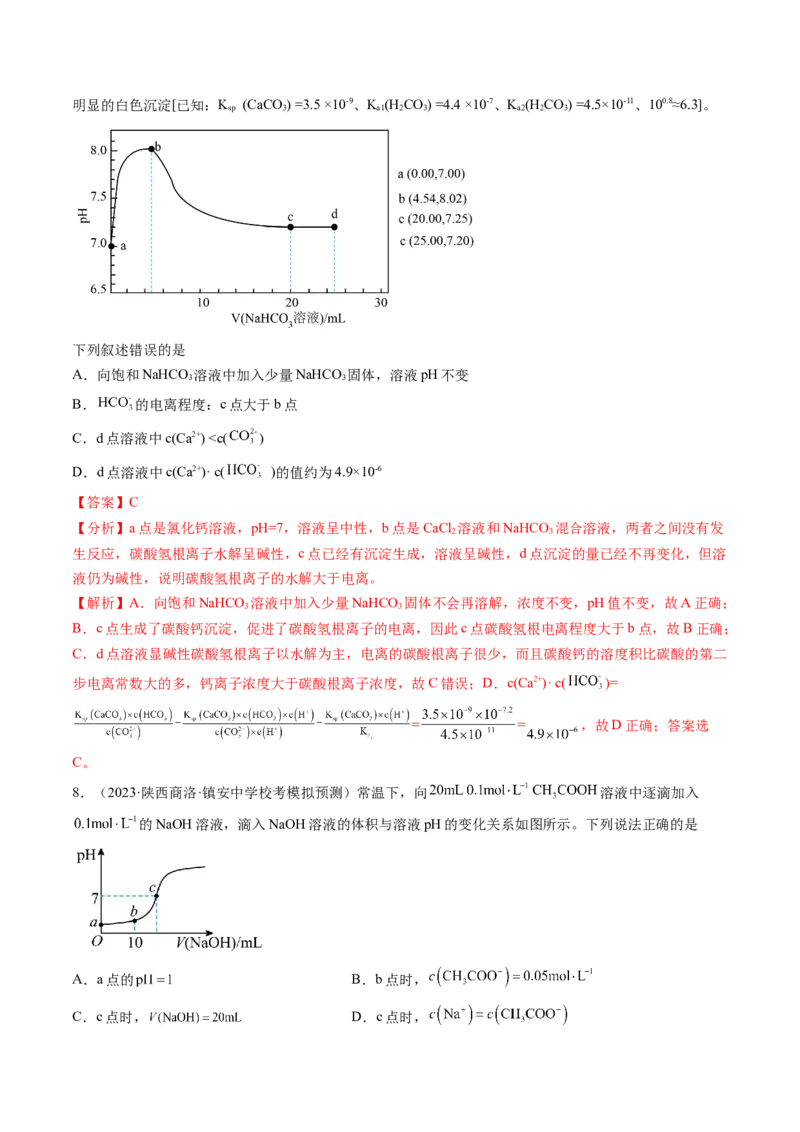
6.(2023·河南南阳·南阳中学校考三模)常温下,向10 mL0.1 mol·L-1HA溶液中逐滴加入0.1 mol·L-1的
MOH溶液,其导电率、pH与加入MOH溶液体积的关系如图所示(假设反应过程中温度不变)。
下列说法正确的是
A.a→d过程中,水的电离程度逐渐增大
B.加入10 mL→13 mL MOH溶液时,导电率降低是因为离子总数减小
C.常温下,K (MOH) =K(HA)≈10 -4.6
b a
D.b点溶液中c (HA) +2c (H+) =c (A-) +2c (MOH) +c (OH- )
【答案】C
【分析】起点a点对应的pH值为2.8,说明HA是弱酸,c点加入MOH10ml时二者完全反应呈中性,也说
明MOH是弱碱,MA是呈中性的弱酸弱碱盐,b点是加入5ml时让HA中和一半,此时溶液中存在MA和
HA物质的量为1:1。
【解析】A.a→c过程是由酸到正盐的过程,水的电离程度逐渐增大,c→d是碱过量又抑制水的电离,故
A错误;B.10 mL→13 mL是碱过量,离子数目继续增加,溶液体积继续增大,但是离子浓度在减小,所
以导电率减小,故B错误;C.因为生成的弱酸弱碱盐呈中性,说明K (MOH) =K(HA),在a点pH=2.8,
b a
c(H+)=c(A-)= ,c(HA)=0.1mol/L, ,故C正确;D.b
点是加入5ml时让HA中和一半,此时溶液中存在MA和HA物质的量为1:1,根据物料守恒和电荷守恒
得出如下式子c(HA)+c(A-)=2c(M+)+2c(MOH)(1)和c(H+)+c(M+)=c(A-)+c(OH-)(2),(1)+ 得到如下式
子:c (HA) +2c (H+) =c (A-) +2c (MOH) +2c (OH- ),故D错误;答案选C。
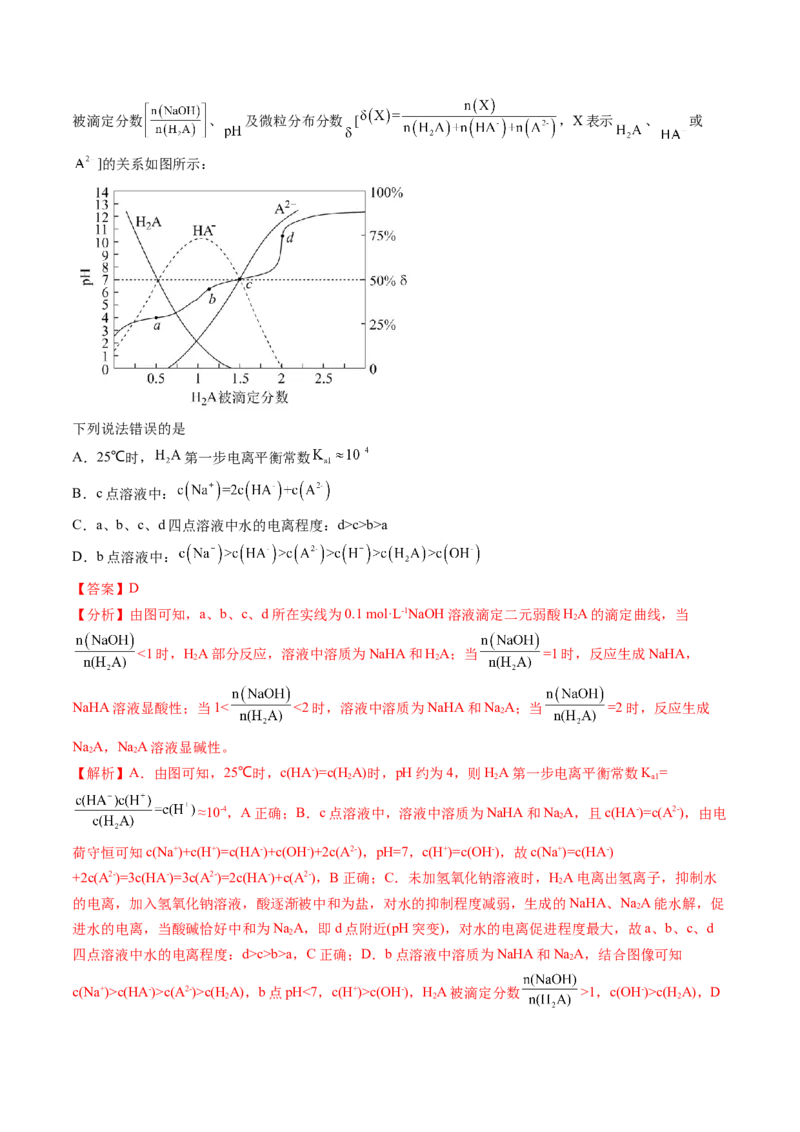
7.(2023·河南·统考模拟预测)25 °C时,用0.5 mol·L-1 NaHCO 溶液滴定25.00 mL0.25 mol·L-1 CaCl 溶
3 2
液,测得混合溶液的pH随滴加NaHCO 溶液的体积变化如图所示,当滴加25mLNaHCO 溶液时出现较为
3 3明显的白色沉淀[已知:K (CaCO) =3.5 ×10-9、K (H CO) =4.4 ×10-7、K (H CO) =4.5×10-11、100.8≈6.3]。
sp 3 a1 2 3 a2 2 3
下列叙述错误的是
A.向饱和NaHCO 溶液中加入少量NaHCO 固体,溶液pH不变
3 3
B. 的电离程度:c点大于b点
C.d点溶液中c(Ca2+) c>b>a
D.b点溶液中:
【答案】D
【分析】由图可知,a、b、c、d所在实线为0.1 mol·L-1NaOH溶液滴定二元弱酸HA的滴定曲线,当
2
<1时,HA部分反应,溶液中溶质为NaHA和HA;当 =1时,反应生成NaHA,
2 2
NaHA溶液显酸性;当1< <2时,溶液中溶质为NaHA和NaA;当 =2时,反应生成
2
NaA,NaA溶液显碱性。
2 2
【解析】A.由图可知,25℃时,c(HA-)=c(H A)时,pH约为4,则HA第一步电离平衡常数K =
2 2 a1
≈10-4,A正确;B.c点溶液中,溶液中溶质为NaHA和NaA,且c(HA-)=c(A2-),由电
2
荷守恒可知c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-),pH=7,c(H+)=c(OH-),故c(Na+)=c(HA-)
+2c(A2-)=3c(HA-)=3c(A2-)=2c(HA-)+c(A2-),B正确;C.未加氢氧化钠溶液时,HA电离出氢离子,抑制水
2
的电离,加入氢氧化钠溶液,酸逐渐被中和为盐,对水的抑制程度减弱,生成的NaHA、NaA能水解,促
2
进水的电离,当酸碱恰好中和为NaA,即d点附近(pH突变),对水的电离促进程度最大,故a、b、c、d
2
四点溶液中水的电离程度:d>c>b>a,C正确;D.b点溶液中溶质为NaHA和NaA,结合图像可知
2
c(Na+)>c(HA-)>c(A2-)>c(H A),b点pH<7,c(H+)>c(OH-),HA被滴定分数 >1,c(OH-)>c(H A),D
2 2 2错误;故选D。
11.(2023·北京东城·北京五十五中校考模拟预测)测定溶液中乙二醛(含少量硝酸)含量的方法如下。
i.取V mL待测溶液于锥形瓶中,加入2滴酚酞溶液,用浓度为0.20 mol·L-1 NaOH溶液滴定至溶液恰好由
无色变为粉红色,中和硝酸。
ii.向i所得溶液加入过量0.50 mol·L-1 NaOH溶液V mL,充全反应,使乙二醛反应生成CHOHCOONa。
1 2
iii.用0.50mol·L-1硫酸滴定ii中溶液至终点,消耗硫酸体积为V mL。
2
下列说法不正确的是
A.根据结构分析,pKa:CHOHCOOH < CH COOH
2 3
B.乙二醛反应生成CHOHCOONa属于氧化还原反应
2
C.待测溶液中乙二醛浓度为(0.5V -V )/ V mol·L-1
1 2
D.若不进行步骤i,测得溶液中乙二醛浓度偏低
【答案】D
【解析】A.pKa越小,酸性越强。氧元素电负性很大,CHOHCOOH中醇羟基的氧原子的作用可使羧基
2
的O-H键极性增强,电离出 变易。CHCOOH中甲基是推电子基团,可使羧基的O-H键极性减弱,电
3
离出 变难,因此pKa: CHOHCOOH< CH COOH,A正确;B.醛基转化为羟基属于还原反应,醛基
2 3
转化为羧基属于氧化反应,B正确;C.根据步骤iii,与硫酸反应的NaOH物质的量为: ,则
与乙二醛反应的NaOH物质的量为: ,根据步骤ii,乙二醛物质的也为
,则待测液中乙二醛的浓度为 ,C正确;D.如
果不进行步骤i,在步骤ii时,除乙二醛消耗NaOH外,HNO 也消耗NaOH,会造成计算得出的与乙二醛
3
反应的NaOH偏多,最后测得溶液中乙二醛浓度偏高,D错误;故选D。
12.(2023·上海·统考模拟预测)0.1 mol·L NaOH溶液分别滴入20 mL 0.1 mol·L HX溶液与20 mL 0.1
mol·L HCl溶液中,其pH随滴入NaOH溶液体积变化的图像如图所示。下列说法正确的是
A.b点: B.c点:
C.a、d点溶液混合后为酸性 D.水的电离程度:d>c>b>a【答案】D
【分析】NaOH是一元强碱,HCl是一元强酸,当滴加20mLNaOH溶液时溶液为中性,则N曲线为HCl溶
液的滴定曲线,M曲线为HX溶液的滴定曲线且可以判断该酸为弱酸。
【解析】A.b点的pH=6则 ,则 ,
故A错误;
B.c点是NaX与HX1:1的混合溶液,根据质子守恒可得: ,故B错误;
C.a、d点溶液混合即30mLNaOH溶液与20 mL 0.1 mol·L HX溶液与20 mL 0.1 mol·L HCl溶液混合,
溶质为NaCl 和1:1的NaX与HX,酸碱性等价于c点,由图可知呈碱性,故C错误;D.d点溶质只有
NaX对水的电离起促进作用,c点NaX与HX1:1的混合溶液,溶液显碱性说明水解程度大于电离程度,
HCl是一元强酸而HX为弱酸,强酸对水的电离的抑制程度更大,所以水的电离程度:d>c>b>a,故D正确;
故选D。
二、主观题(共3小题,共40分)
13.(14分)(2023·四川成都·成都七中校考模拟预测)I.研究水溶液中的粒子行为在研究中具有重要价
值。根据下表所列三种溶液在25℃时的相关数据,按要求填空:
溶液 物质的量浓度 pH
(I)HAc 0.1 mol/L 2.86
(II) 0.1 mol/L 6.14
(III) 0.1 mol/L 1
(1)根据表中数据,写出HAc的电离方程式
(2)比较溶液(II)、(III)中 的大小关系是(II) (III)(填“>”、“<”或“=”)。
(3)溶液(I)和(II)中由水电离出的 之比是 。
II.某小组研究25℃下HAc电离平衡的影响因素。
提出假设 稀释HAc溶液或改变 浓度,HAc电离平衡会发生移动。
设计方案并完成实验 用浓度均为0.1 mol·L 的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;
测定pH,记录数据。
序
V(HAc)/mL V(NaAc)/mL /mL pH
号
I 40.00 / / 0 2.86
II 4.00 / 36.00 0 3.36
VII 4.00 a b 3∶4 4.53VIII 4.00 4.00 32.00 1∶1 4.65
(4)根据表中信息,补充数据:a= ,b= 。
(5)由实验I和II可知,稀释HAc溶液,电离平衡 (填“正”或“逆”)向移动;结合表中数据,给
出判断理由: 。由实验II~VIII可知,增大 浓度,HAc电离平衡逆向移动。
实验结论 假设成立。
【答案】(每空2分)(1)HAc Ac-+H+
(2)<
⇌
(3)1:105
(4)3.00 33.00
(5)正 实验Ⅱ相较于实验Ⅰ,醋酸溶液稀释了10倍,而实验Ⅱ的pH增大值小于1
【解析】(1)0.1mol/L醋酸溶液的pH等于2.86,说明是弱电解质,则其电离方程式为HAc Ac-+H+;
(2)铵根水解显酸性,硫酸氢铵能电离出氢离子抑制铵根的水解,则溶液(Ⅱ)、(Ⅲ)中c( ⇌)的大小关系
是(Ⅱ)<(Ⅲ);(3)醋酸电离出氢离子抑制水的电离,溶液中由水电离出的c(H+)与溶液中的c(OH-)相同,
1.0×10-11.14mol•L-1,氯化铵溶液中铵根水解促进水的电离,溶液中H+是由
水电离出的,c(H+)=1.0×10-6.14mol•L-1,则溶液(I)和(Ⅱ)中由水电离出的c(H+)之比是(1.0×10-11.14mol•L-1):
(1.0×10-6.14mol•L-1)=1:105;(4)由表格中数据可知,保证醋酸钠和醋酸物质的量之比为3:4,二者浓度相等,
则体积比为3:4,则a=3.00mL,总体积是40ml,则b=(40-3.00-4.00)mL=33.00mL;(5)加水稀释,体积增
大,平衡向微粒数增多的方向移动,即向电离的正向移动,强酸溶液不存在电离平衡,稀释10倍pH增大
1,而比较实验I、II,醋酸稀释10倍,pH增大值小于1。
14.(12分)(2023·江西宜春·江西省宜丰中学校考模拟预测)已知25℃时电离常数:
酸 HCO CHCOOH HCN
2 3 3
K K =4.5×10-7K =5.6×10-11 1.75×10-5 6.2×10-10
a a1 a2
(1)H CO、CHCOOH、HCN三种酸中酸性最弱的是 。常温下,pH均为10的NaCO、
2 3 3 2 3
CHCOONa、NaCN、NaHCO 四种溶液中,物质的量浓度最大的是 。
3 3
(2)常温下,向20mL0.01mol·L-1CHCOOH溶液中逐滴加入0.01mol·L-1KOH溶液,其pH变化曲线如图所示
3
(忽略温度变化)。请回答下列有关问题:
①若想观察滴定终点,滴定过程中宜选用 作指示剂(填“酚酞”、“石蕊”或“甲基橙”)。
②b点时,溶液中离子浓度由大到小的顺序是 。(3)常温下,向NaCN溶液中通入少量CO 发生反应的化学方程式为: 。
2
(4)在一定条件下,NaCO 溶液中存在CO +H O HCO +OH-平衡,下列说法不正确的是_______。
2 3 2
A.稀释溶液, 增大 B.通入CO,溶液pH减小
2
C.升高温度,水解平衡常数增大 D.加入NaO固体, 减小
2
【答案】(每空2分)(1)HCN CH COONa
3
(2)酚酞 c(CHCOO-)>c(K+)>c(H+)>c(OH-)
3
(3)NaCN+CO +H O=NaHCO +HCN
2 2 3
(4)A
【解析】(1)电离平衡常数越大,说明电离程度越强,根据表中数据可知,酸性强弱顺序是
CHCOOH>H CO>HCN,因此三种酸中酸性最弱的是HCN;酸的酸性越强,对应酸根离子水解程度越弱,
3 2 3
pH为10的四种盐溶液中,物质的量浓度最大的是CHCOONa;
3
(2)①中和滴定实验中,不用石蕊作指示剂,CHCOOH与KOH恰好完全反应生成CHCOOK,
3 3
CHCOOK为强碱弱酸盐,溶液显碱性,选择指示剂原则之一是指示剂的变色范围与溶液的酸碱性一致,
3
因此用KOH滴定CHCOOH溶液,指示剂为酚酞;②根据图像可知,b点时,混合溶液显酸性;b点加入
3
KOH溶液10mL,此时溶液中溶质为CHCOOK、CHCOOH,且两者物质的量相等,b点溶液显酸性,说
3 3
明醋酸的电离程度大于醋酸根离子的水解程度,因此离子浓度大小顺序是
c(CHCOO-)>c(K+)>c(H+)>c(OH-);
3
(3)根据表中数据,电离平衡常数大小顺序是CHCOOH>H CO>HCN>HCO ,因此NaCN溶液中通入少
3 2 3
量CO,发生NaCN+CO+H O=HCN+NaHCO;
2 2 2
(4)A. ,加水稀释,促使平衡
向右进行,n(CO )减小,n(Na+)、K 不变,因此该比值应减小,故A错误;B.通入CO,CO 与OH-反
h 2 2
应生成HCO ,c(OH-)降低,pH降低,故B正确;C.盐类水解为吸热反应,升高温度,促进水解,水解
常数增大,故C正确;D.加入NaO,氧化钠与水反应生成NaOH,c(OH-)增大,平衡左移,c(HCO )减
2
小,c(CO )增大,该比值减小,故D正确;答案选A。
15.(14分)(2023·湖南长沙·湖南师大附中校考二模)(NH )Cr O 用于有机合成催化剂,媒染剂,显影
4 2 2 7
液等。某化学兴趣小组对(NH )Cr O 的部分性质及组成进行探究。已知:Cr O2-(橙色)+H O 2CrO2-
4 2 2 7 2 7 2 4
(黄色)+2H+。回答下列问题:
(1)在试管中加入少量(NH )Cr O 固体,滴加足量浓KOH溶液,振荡、微热,观察到的主要现象是固体
4 2 2 7
溶解、 、 。
(2)为探究(NH )Cr O (摩尔质量252g/mol)的分解产物,按下图连接好装置,在A中加入5.040g样品进
4 2 2 7
行实验。①仪器B的名称是 。
②加热A至恒重,观察到D中溶液不变色,同时测得A、B中质量变化分别为2.00g、1.44g,写出重铬酸
铵加热分解反应的化学方程式 。
③C的作用是 。
(3)实验室常用甲醛法测定含(NH )Cr O 的样品中氮的质量分数,其反应原理为:2Ba2++Cr O2-
4 2 2 7 2 7
+H O=2BaCrO ↓+2H+、 4NH ++6HCHO =3H++6H O+(CH)NH+[滴定时,1mol(CH )NH+与1molH+相当],
2 4 4 2 2 6 4 2 6 4
然后用NaOH标准溶液滴定反应生成的酸。
实验步骤:称取样品2.800g,配成250mL溶液,移取25.00mL样品溶液于250mL锥形瓶中,用氯化钡溶
液使Cr O2-完全沉淀后,加入10mL20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,
2 7
用0.200 mol·L-1 NaOH标准溶液滴定至终点。重复上述操作3次。
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则滴定时用去NaOH标准溶液的体积
(填“偏大”、“偏小”或“无影响”);滴定时边滴边摇动锥形瓶,眼睛应观察 。
②滴定结果如下表所示
该样品中氮的质量分数为 。
【答案】(除标注外,每空2分)(1)有刺激性气味气体放出 溶液变为黄色(1分)
(2)①U形管(1分) ②(NH )Cr O Cr O+N ↑+4H O ③防止水蒸气进入到B中
4 2 2 7 2 3 2 2
(3)①偏大 锥形瓶内溶液颜色的变化 ②10.00%
【分析】(1)根据NH +与碱反应生成氨气,以及Cr O2-(橙色)+H O 2CrO2-(黄色)+2H+平衡移动解答。
4 2 7 2 4
(2)根据重铬酸铵的元素组成和元素化合价的变化,判断可能的产物。再根据实验现象及玻璃管A和U形管
B的质量变化确定分解产物及产物的物质的量,进而确定参加反应的各物质的计量关系,据此写出重铬酸
钾分解反应的化学方程式。
(3)由甲醛法测定样品中氮的质量分数的反应原理可知,1mol(NH)Cr O 能产生4molH+,其中2molH+是由
4 2 2 72molNH +生成的,NH +产生的H+消耗的NaOH的量占消耗NaOH的总量 ,所以每摩尔氮原子产生的
4 4
H+消耗1molNaOH,据此分析计算。
【解析】(1)(NH )Cr O 固体溶解于水,溶液呈橙色,当滴加足量浓KOH溶液时,NH ++OH-=NH↑+H O,
4 2 2 7 4 3 2
H++OH-=H O,溶液中H+浓度减小,使平衡Cr O2-(橙色)+H O 2CrO2-(黄色)+2H+向正反应方向移动,
2 2 7 2 4
所以观察到的主要现象除固体溶解外,还有刺激性气味气体放出,溶液变为黄色。
(2)①仪器B的名称是U形管。②因碱石灰不能吸收NH ,而D中酚酞溶液不变色,说明重铬酸铵分解无氨
3
气产生。B中碱石灰质量增加,说明有水蒸气生成(质量为1.44g)。但B中增加的质量(1.44g)小于A
中减小的质量(2.00g),说明重铬酸铵分解产生的气体中除水蒸气外还有另外气体,该气体不能被碱石灰
吸收,结合-3价氮的还原性和+6价铬的氧化性推测该气体是氮气,n(N )= =0.02mol,生成
2
0.02molN 时-3价氮元素失去的电子物质的量=0.02mol×6e-=0.12mole-,又因A中样品n[(NH )Cr O]=
2 4 2 2 7
=0.02mol,根据氧化还原反应中电子得失守恒,每个+6价铬原子得到的电子数= =3,
即铬元素化合价由+6价降到+3价,由此推知A中生成固体是Cr O,其物质的量n(CrO)=0.02mol。生成
2 3 2 3
水蒸气的物质的量n(H O)= =0.08mol。则参加反应的各物质的物质的量之比为:n[(NH )Cr O]:
2 4 2 2 7
n(CrO):n(N ):n(H O)=0.02:0.02:0.02:0.08=1:1:1:4。所以重铬酸钾受热分解的化学方程式为:(NH )Cr O
2 3 2 2 4 2 2 7
Cr O+N ↑+4H O。③为了使B中碱石灰只吸收重铬酸钾分解产生的水蒸气,C的作用就是防止D中水
2 3 2 2
蒸气进入到B中。
(3)由甲醛法测定样品中氮的质量分数的反应原理可知,1mol(NH)Cr O 能产生4molH+,其中2molH+是由
4 2 2 7
2molNH +生成的,NH +产生的H+消耗的NaOH的量占消耗NaOH的总量 (每摩尔氮原子生成的H+消耗
4 4
1molNaOH)。①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液,NaOH溶液将被滴定管内壁的
水膜稀释,用该NaOH溶液滴定时用去的NaOH溶液的体积将偏大;中和滴定的关键是准确确定酸与碱恰
好中和的时间点,所以眼睛应观察锥形瓶内溶液颜色的变化。②由表格数据可知,四次平行实验用去的
NaOH标准溶液体积分别为:21.06-1.07=19.99mL、20.89-0.88=20.01mL、21.20-0.20=21.00、20.66-
0.66=20.00mL。显然第三次实验数据异常,舍去。所以滴定用去NaOH标准溶液体积的平均值=
=20.00mL。2.800g样品用去NaOH的总物质的量=0.02000L×0.200mol/L×
=0.04mol,则样品中氮原子物质的量= ×0.04mol=0.02mol,所以样品中含氮质量分数=
×100%=10.00%。
1.(2023·浙江·统考高考真题)草酸( )是二元弱酸。某小组做如下两组实验:实验I:往 溶液中滴加 溶液。
实验Ⅱ:往 溶液中滴加 溶液。
[已知: 的电离常数 ,溶液混合后体积变化忽略不
计],下列说法正确的是
A.实验I可选用甲基橙作指示剂,指示反应终点
B.实验I中 时,存在
C.实验Ⅱ中发生反应
D.实验Ⅱ中 时,溶液中
【答案】D
【解析】A. 溶液被氢氧化钠溶液滴定到终点时生成显碱性的草酸钠溶液,为了减小实验误差要
选用变色范围在碱性范围的指示剂,因此,实验I可选用酚酞作指示剂,指示反应终点,故A错误;B.
实验I中 时,溶质是 、 且两者物质的量浓度相等,
,,则草酸氢根的电离程度大于草酸根的水解程度,因此存在
,故B错误;C.实验Ⅱ中,由于开始滴加的氯化钙量较少而 过量,因此该
反应在初始阶段发生的是 ,该反应的平衡常数为
,因为平衡常数很大,说明反应能够完全进行,当
完全消耗后, 再和 发生反应,故C错误;D.实验Ⅱ中 时,溶液
中的钙离子浓度为 ,溶液中
,故D正确。
综上所述,答案为D。
2.(2023·湖南·统考高考真题)常温下,用浓度为 的 标准溶液滴定浓度均为
的 和 的混合溶液,滴定过程中溶液的 随 ( )的变化曲线
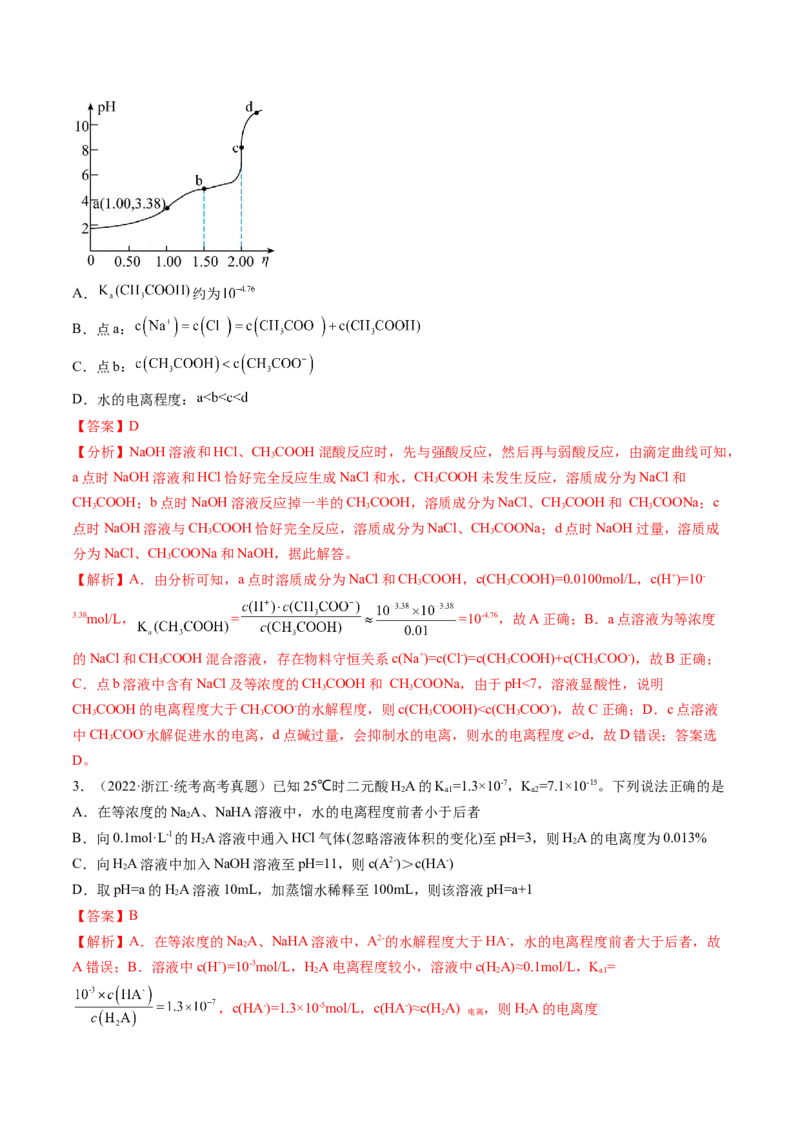
如图所示。下列说法错误的是A. 约为
B.点a:
C.点b:
D.水的电离程度:
【答案】D
【分析】NaOH溶液和HCl、CHCOOH混酸反应时,先与强酸反应,然后再与弱酸反应,由滴定曲线可知,
3
a点时NaOH溶液和HCl恰好完全反应生成NaCl和水,CHCOOH未发生反应,溶质成分为NaCl和
3
CHCOOH;b点时NaOH溶液反应掉一半的CHCOOH,溶质成分为NaCl、CHCOOH和 CHCOONa;c
3 3 3 3
点时NaOH溶液与CHCOOH恰好完全反应,溶质成分为NaCl、CHCOONa;d点时NaOH过量,溶质成
3 3
分为NaCl、CHCOONa和NaOH,据此解答。
3
【解析】A.由分析可知,a点时溶质成分为NaCl和CHCOOH,c(CHCOOH)=0.0100mol/L,c(H+)=10-
3 3
3.38mol/L, = =10-4.76,故A正确;B.a点溶液为等浓度
的NaCl和CHCOOH混合溶液,存在物料守恒关系c(Na+)=c(Cl-)=c(CH COOH)+c(CH COO-),故B正确;
3 3 3
C.点b溶液中含有NaCl及等浓度的CHCOOH和 CHCOONa,由于pH<7,溶液显酸性,说明
3 3
CHCOOH的电离程度大于CHCOO-的水解程度,则c(CHCOOH)d,故D错误;答案选
3
D。
3.(2022·浙江·统考高考真题)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是
2 a1 a2
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为0.013%
2 2
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
【答案】B
【解析】A.在等浓度的NaA、NaHA溶液中,A2-的水解程度大于HA-,水的电离程度前者大于后者,故
2
A错误;B.溶液中c(H+)=10-3mol/L,HA电离程度较小,溶液中c(HA)≈0.1mol/L,K =
2 2 a1
,c(HA-)=1.3×10-5mol/L,c(HA-)≈c(HA) ,则HA的电离度
2 电离 20.013%,故B正确;C.向HA溶液中加入NaOH溶液至pH=11,
2
,则c(A2-)