文档内容
第 2 讲 元素周期表 元素周期律
课 程 标 准 知 识 建 构
1.能说出元素电离能、电负性的含义,能描述主族元
素第一电离能、电负性变化的一般规律,能从电子排
布的角度对这一规律进行解释。能说明电负性大小
与原子在化合物中吸引电子能力的关系,能利用电
负性判断元素的金属性与非金属性的强弱,推断化
学键的极性。
2.能从原子价层电子数目和价层电子排布的角度解
释元素周期表的分区、周期和族的划分。能列举元素
周期律(表)的应用。
3.能说明建构思维模型在人类认识原子结构过程中
的重要作用,能论证证据与模型建立及其发展之间
的关系。简要说明原子核外电子运动规律的理论探
究对研究元素性质及其变化规律的意义。
一、元素周期表
1.原子序数
按照元素在周期表中的顺序给元素编号,称之为原子序数,原子序数=核电
荷数=质子数=核外电子数。
2.元素周期表编排原则
3.元素周期表
(1)结构元素周期表
4.原子结构与周期表的关系
(1)原子结构与周期的关系
原子的最大能层数=周期序数
(2)原子结构与族的关系
①主族元素的价层电子排布特点
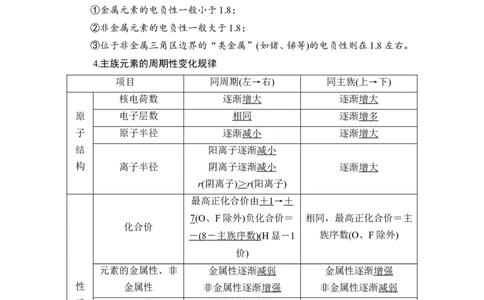
主族 ⅠA ⅡA ⅢA ⅣA
排布特点 n s 1 n s 2 n s 2 n p 1 n s 2 n p 2
主族 ⅤA ⅥA ⅦA
排布特点 n s 2 n p 3 n s 2 n p 4 n s 2 n p 5
②0族:He:1s2;其他ns2np6。
③过渡元素(副族和第Ⅷ族):(n-1)d1~10ns1~2。
(3)元素周期表的分区与价层电子排布的关系
①周期表的分区
②各区价层电子排布特点
分区 价层电子排布
s区 ns1~2
p区 ns2np1~6(除He外)
d区 (n-1)d1~9ns1~2(除钯外)
ds区 (n-1)d10ns1~2
f区 (n-2)f0~14(n-1)d0~2ns2
5.元素周期表的三大应用
(1)科学预测:为新元素的发现及预测它们的原子结构和性质提供了线索。
(2)寻找新材料(3)用于工农业生产。
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)元素周期表中位于金属与非金属分界线附近的元素属于过渡元素( )
(2)第ⅠA族全部是金属元素( )
(3)两短周期元素原子序数相差8,则周期数一定相差1( )
(4)s区全部是金属元素( )
(5)第四周期元素中,锰原子价层电子中未成对电子数最多( )
(6)价层电子排布为5s25p1的元素位于第五周期ⅠA族,是s区元素( )
(7)最外层有2个未成对电子的可能是ns2np2或ns2np4。短周期元素中分别为
C、Si和O、S( )
答案 (1)× (2)× (3)√ (4)× (5)× (6)× (7)√
二、元素周期律
1.原子半径
(1)影响因素
(2)变化规律
①同周期主族元素从左到右,原子半径逐渐减小;
②同主族元素从上到下,原子半径逐渐增大。
2.电离能
(1)第一电离能:气态电中性基态原子失去一个电子转化为气态基态正离子所
需要的最低能量,符号:I ,单位:kJ·mol-1。
1
(2)规律
①同周期从左至右第一电离能总体呈现增大的趋势。
②同族元素:从上至下第一电离能逐渐减小。
③同种原子:逐级电离能越来越大。
【特别提醒】
第二、三、四周期中,第ⅡA族、第ⅤA族元素的第一电离能比相邻元素都大。
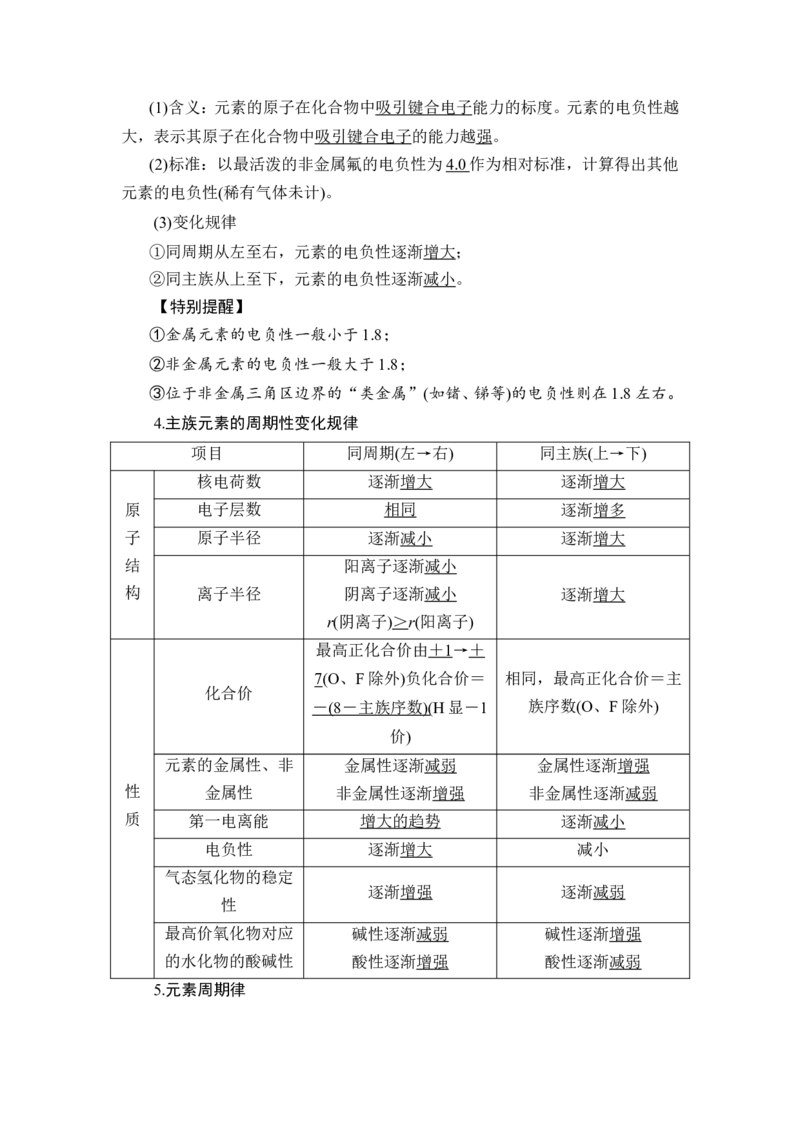
3.电负性(1)含义:元素的原子在化合物中吸引键合电子能力的标度。元素的电负性越
大,表示其原子在化合物中吸引键合电子的能力越强。
(2)标准:以最活泼的非金属氟的电负性为4.0 作为相对标准,计算得出其他
元素的电负性(稀有气体未计)。
(3)变化规律
①同周期从左至右,元素的电负性逐渐增大;
②同主族从上至下,元素的电负性逐渐减小。
【特别提醒】
①金属元素的电负性一般小于1.8;
②非金属元素的电负性一般大于1.8;
③位于非金属三角区边界的“类金属”(如锗、锑等)的电负性则在1.8左右。
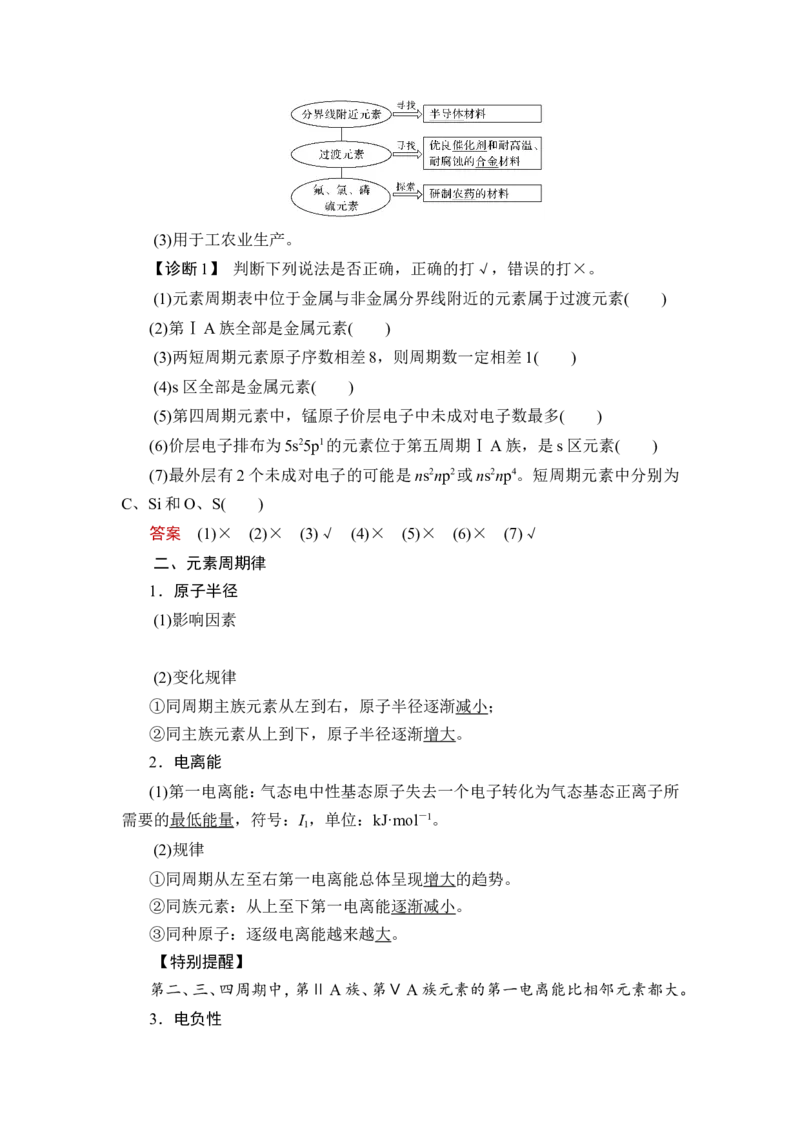
4.主族元素的周期性变化规律
项目 同周期(左→右) 同主族(上→下)
核电荷数 逐渐增大 逐渐增大
原 电子层数 相同 逐渐增多
子 原子半径 逐渐减小 逐渐增大
结 阳离子逐渐减小
构 离子半径 阴离子逐渐减小 逐渐增大
r(阴离子)>r(阳离子)
最高正化合价由 + 1→+
7(O、F除外)负化合价= 相同,最高正化合价=主
化合价
- ( 8 -主族序数 )(H显-1 族序数(O、F除外)
价)
元素的金属性、非 金属性逐渐减弱 金属性逐渐增强
性 金属性 非金属性逐渐增强 非金属性逐渐减弱
质 第一电离能 增大的趋势 逐渐减小
电负性 逐渐增大 减小
气态氢化物的稳定
逐渐增强 逐渐减弱
性
最高价氧化物对应 碱性逐渐减弱 碱性逐渐增强
的水化物的酸碱性 酸性逐渐增强 酸性逐渐减弱
5.元素周期律6.对角线规则
在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,
如 。
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能( )
(2)C、N、O、F四种元素第一电离能从大到小的顺序是N>O>F>C( )
(3)正三价阳离子的电子排布式为1s22s22p63s23p63d5的元素在周期表中位于
Ⅷ族( )
(4)价层电子排布式为4s24p3的元素位于第四周期ⅤA族,是p区元素( )
(5)元素的电负性越大,非金属性越强,第一电离能也越大( )
(6)最外层有2个未成对电子的可能是ns2np2或ns2np4,短周期元素中分别为
C、Si和O、S( )
(7)价层电子排布式为5s25p1的元素位于第五周期ⅠA族,是s区元素( )
答案 (1)× (2)× (3)√ (4)√ (5)× (6)√ (7)×
考点一 元素周期表的结构及应用
【典例1】 (2020·福建南平市高三质检)某同学设计了如图所示元素周期表,
已知Z元素的最外层电子数是次外层的3倍。空格中均有对应的元素填充。下列
说法正确的是( )
A.白格中都是主族元素,灰格中都是副族元素
B.X、Y分别与Z形成的化合物都只有两种
C.X、Y元素最高价氧化物对应的水化物酸性:X>Y
D.X、Y、Z的气态氢化物中最稳定的是X的氢化物
答案 C
解析 按照图示,白格填充的为主族元素和稀有气体元素,灰格填充的为副族元素,A错误; X和Z可以形成NO、NO 、N O 等氮氧化物,不止2种,B错误;
2 2 5
X的最高价氧化物对应的水化物为 HNO ,Y的最高价氧化物对应的水化物为
3
H PO ,则酸性HNO >H PO ,C正确;非金属性越强,气态氢化物的稳定性越强,
3 4 3 3 4
同主族元素,从上到下非金属性减弱,同周期元素,从左到右,非金属性增强,则
非金属性强弱顺序为O>N>P,氢化物最强的是Z的氢化物,H O,D错误。
2
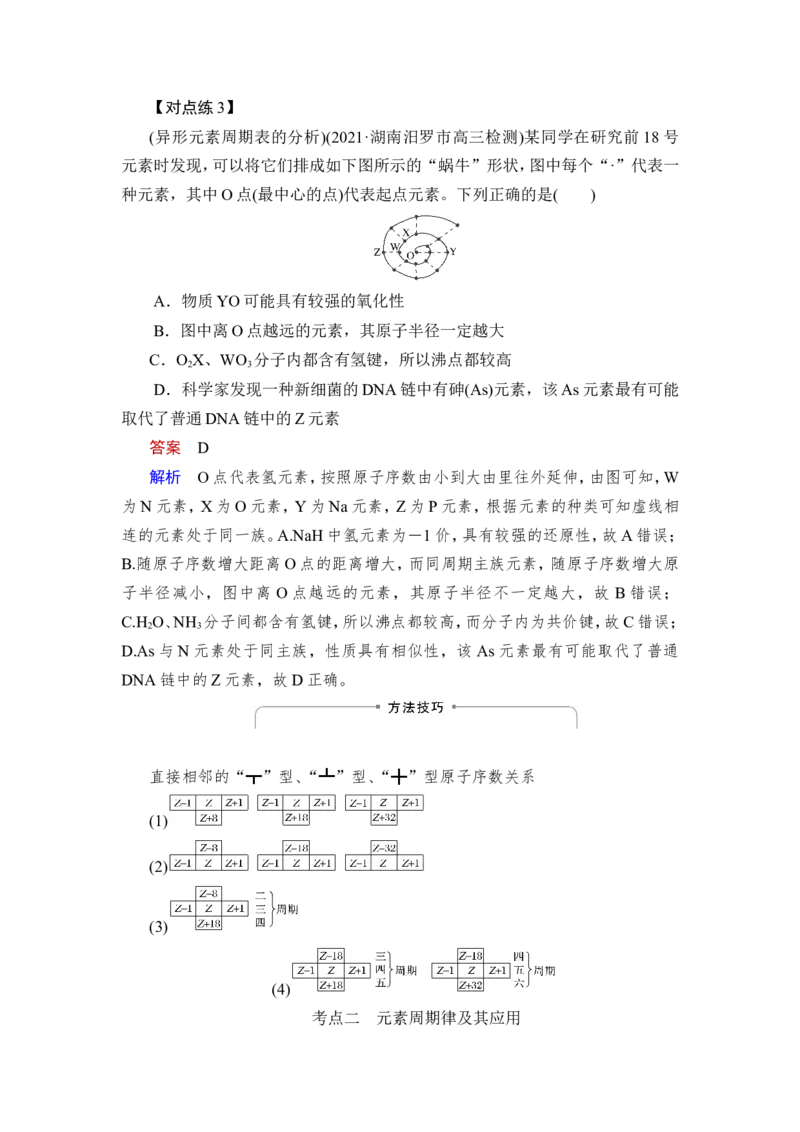
【对点练1】 (依据元素周期表结构推断原子序数)如图为元素周期表中前四
周期的一部分,若B元素的核电荷数为x,则这五种元素的核电荷数之和为 (
)
A.5x+10 B.5x
C.5x+14 D.5x+16
答案 A
解析
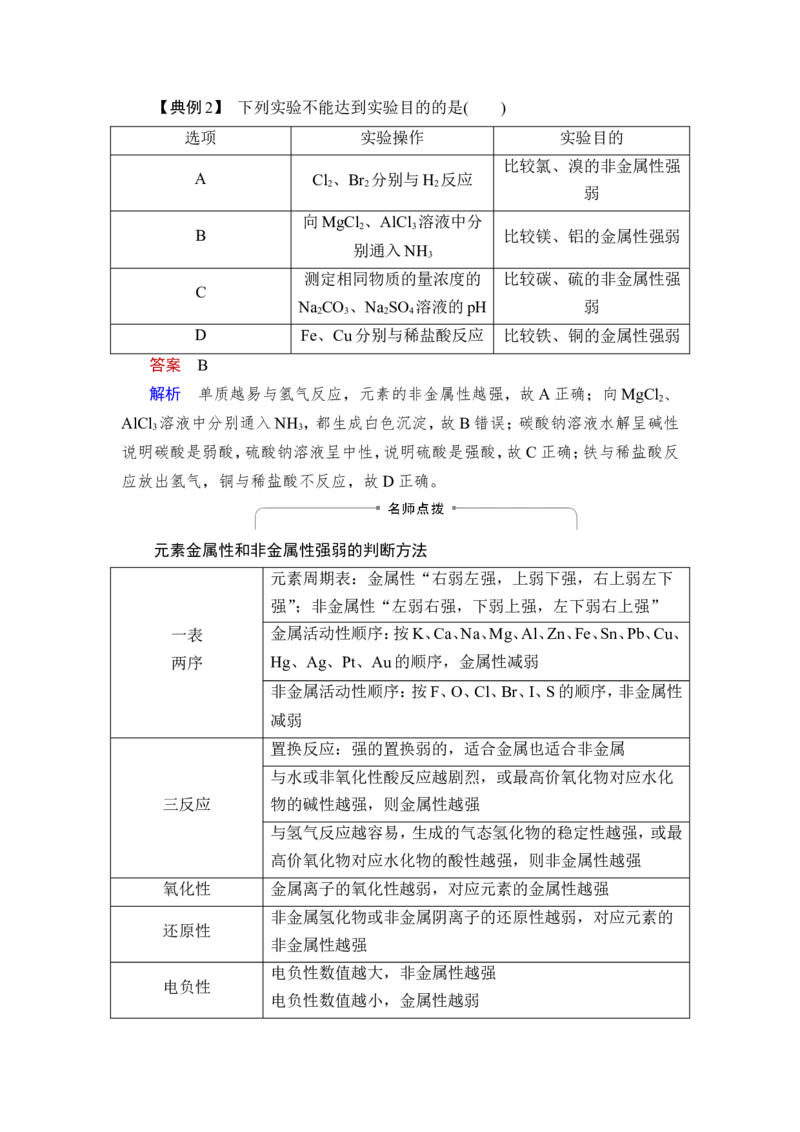
【对点练2】 (周期表的片段在元素推断题中的应用)元素周期表短周期的一
部分如表所示。下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
A.D在过量的B中燃烧的主要产物为DB
3
B.C的氢化物的水溶液酸性比E的强
C.A与B形成的阴离子可能有AB、A B
2
D.E单质中由于形成了氢键,所以很容易液化
答案 C
解析 根据五种元素在元素周期表中的相对位置,可以确定A为碳、B为氧、
C为氟、D为硫、E为氯。A项,硫在氧气中燃烧生成SO ,错误;B项,氢氟酸为弱
2
酸,其酸性比盐酸的弱,错误;C项,碳与氧形成的阴离子较多,AB为碳酸根离子,
A B为草酸根离子,正确;D项,氯气单质分子中没有氢原子,也就不存在氢键,
2
错误。【对点练3】
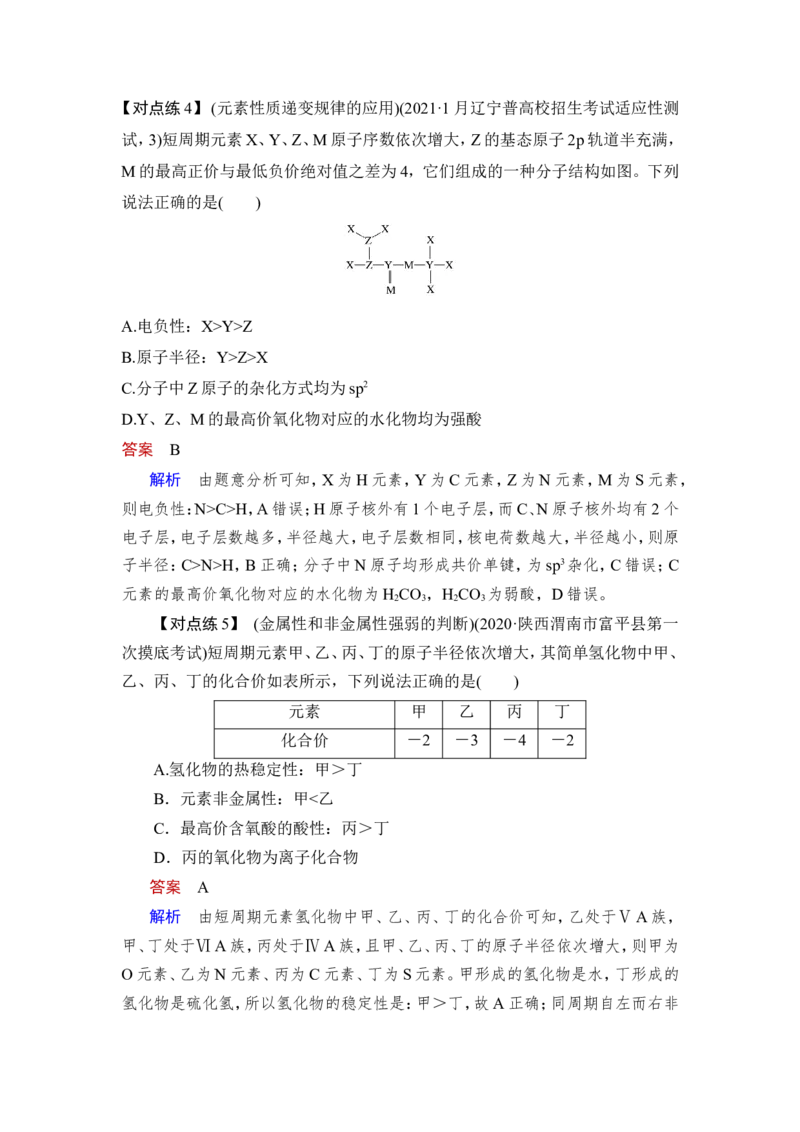
(异形元素周期表的分析)(2021·湖南汨罗市高三检测)某同学在研究前18号
元素时发现,可以将它们排成如下图所示的“蜗牛”形状,图中每个“·”代表一
种元素,其中O点(最中心的点)代表起点元素。下列正确的是( )
A.物质YO可能具有较强的氧化性
B.图中离O点越远的元素,其原子半径一定越大
C.O X、WO 分子内都含有氢键,所以沸点都较高
2 3
D.科学家发现一种新细菌的DNA链中有砷(As)元素,该As元素最有可能
取代了普通DNA链中的Z元素
答案 D
解析 O点代表氢元素,按照原子序数由小到大由里往外延伸,由图可知,W
为N元素,X为O元素,Y为Na元素,Z为P元素,根据元素的种类可知虚线相
连的元素处于同一族。A.NaH中氢元素为-1价,具有较强的还原性,故A错误;
B.随原子序数增大距离O点的距离增大,而同周期主族元素,随原子序数增大原
子半径减小,图中离 O点越远的元素,其原子半径不一定越大,故 B错误;
C.H O、NH 分子间都含有氢键,所以沸点都较高,而分子内为共价键,故C错误;
2 3
D.As与N元素处于同主族,性质具有相似性,该 As元素最有可能取代了普通
DNA链中的Z元素,故D正确。
直接相邻的“┳”型、“┻”型、“╋”型原子序数关系
(1)
(2)
(3)
(4)
考点二 元素周期律及其应用【典例2】 下列实验不能达到实验目的的是( )
选项 实验操作 实验目的
比较氯、溴的非金属性强
A Cl 、Br 分别与H 反应
2 2 2
弱
向MgCl 、AlCl 溶液中分
2 3
B 比较镁、铝的金属性强弱
别通入NH
3
测定相同物质的量浓度的 比较碳、硫的非金属性强
C
Na CO 、Na SO 溶液的pH 弱
2 3 2 4
D Fe、Cu分别与稀盐酸反应 比较铁、铜的金属性强弱
答案 B
解析 单质越易与氢气反应,元素的非金属性越强,故A正确;向MgCl 、
2
AlCl 溶液中分别通入NH ,都生成白色沉淀,故B错误;碳酸钠溶液水解呈碱性
3 3
说明碳酸是弱酸,硫酸钠溶液呈中性,说明硫酸是强酸,故C正确;铁与稀盐酸反
应放出氢气,铜与稀盐酸不反应,故D正确。
元素金属性和非金属性强弱的判断方法
元素周期表:金属性“右弱左强,上弱下强,右上弱左下
强”;非金属性“左弱右强,下弱上强,左下弱右上强”
一表 金属活动性顺序:按K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、Cu、
两序 Hg、Ag、Pt、Au的顺序,金属性减弱
非金属活动性顺序:按F、O、Cl、Br、I、S的顺序,非金属性
减弱
置换反应:强的置换弱的,适合金属也适合非金属
与水或非氧化性酸反应越剧烈,或最高价氧化物对应水化
三反应 物的碱性越强,则金属性越强
与氢气反应越容易,生成的气态氢化物的稳定性越强,或最
高价氧化物对应水化物的酸性越强,则非金属性越强
氧化性 金属离子的氧化性越弱,对应元素的金属性越强
非金属氢化物或非金属阴离子的还原性越弱,对应元素的
还原性
非金属性越强
电负性数值越大,非金属性越强
电负性
电负性数值越小,金属性越弱【对点练4】 (元素性质递变规律的应用)(2021·1月辽宁普高校招生考试适应性测
试,3)短周期元素X、Y、Z、M原子序数依次增大,Z的基态原子2p轨道半充满,
M的最高正价与最低负价绝对值之差为4,它们组成的一种分子结构如图。下列
说法正确的是( )
A.电负性:X>Y>Z
B.原子半径:Y>Z>X
C.分子中Z原子的杂化方式均为sp2
D.Y、Z、M的最高价氧化物对应的水化物均为强酸
答案 B
解析 由题意分析可知,X为H元素,Y为C元素,Z为N元素,M为S元素,
则电负性:N>C>H,A错误;H原子核外有1个电子层,而C、N原子核外均有2个
电子层,电子层数越多,半径越大,电子层数相同,核电荷数越大,半径越小,则原
子半径:C>N>H,B正确;分子中N原子均形成共价单键,为sp3杂化,C错误;C
元素的最高价氧化物对应的水化物为H CO ,H CO 为弱酸,D错误。
2 3 2 3
【对点练5】 (金属性和非金属性强弱的判断)(2020·陕西渭南市富平县第一
次摸底考试)短周期元素甲、乙、丙、丁的原子半径依次增大,其简单氢化物中甲、
乙、丙、丁的化合价如表所示,下列说法正确的是( )
元素 甲 乙 丙 丁
化合价 -2 -3 -4 -2
A.氢化物的热稳定性:甲>丁
B.元素非金属性:甲<乙
C.最高价含氧酸的酸性:丙>丁
D.丙的氧化物为离子化合物
答案 A
解析 由短周期元素氢化物中甲、乙、丙、丁的化合价可知,乙处于ⅤA族,
甲、丁处于ⅥA族,丙处于ⅣA族,且甲、乙、丙、丁的原子半径依次增大,则甲为
O元素、乙为N元素、丙为C元素、丁为S元素。甲形成的氢化物是水,丁形成的
氢化物是硫化氢,所以氢化物的稳定性是:甲>丁,故A正确;同周期自左而右非金属性逐渐增强,故非金属性:甲(O)>乙(N),故B错误;最高价含氧酸的酸性:
碳元素形成碳酸,硫元素形成硫酸,故酸性丙<丁,故C错误;丙的氧化物是CO、
CO ,均属于共价化合物,故D错误。
2
【对点练 6】 (微粒半径大小的比较)比较下列微粒半径大小(用“>”或
“<”填空):
(1)Na________Mg________Cl
(2)Li________Na________K
(3)Na+________Mg2+________Al3+
(4)F-________Cl-________Br-
(5)Cl-________O2-________Na+________Mg2+
(6)Fe2+________Fe3+
答案 (1)> > (2)< < (3)> > (4)< < (5)> > > (6)
>
“三看”法快速判断简单微粒半径的大小
一看电子层数:最外层电子数相同时,电子层数越多,半径越大。
二看核电荷数:当电子层结构相同时,核电荷数越大,半径越小。
三看核外电子数:当电子层数和核电荷数均相同时,核外电子数越大,半径
越大。
【对点练7】 (电离能与电负性的应用)现有四种元素的基态原子的电子排布
式如下:①1s22s22p4②1s22s22p63s23p3③1s22s22p3④1s22s22p5
则下列有关比较中正确的是( )
A.最高正化合价:④>①>③=②
B.电负性:④>①>③>②
C.原子半径:④>③>②>①
D.第一电离能:④>①>③>②
答案 B
解析 根据①、②、③、④核外电子排布式知,这几种元素分别是O、P、N、F
元素;A.在主族元素中,元素的最高化合价与其族序数相等(O、F没有正化合价),
N、P同主族,最高正化合价均为+5价,即③=②,故A错误;B.元素的非金属性
越强,其电负性越大,同一周期中,元素的电负性随着原子序数的增大而增大,四
种元素的非金属性F>O>N>P,这几种元素电负性大小顺序是④>①>③>②故B正确;C.原子的电子层数越多,其原子半径越大,同一周期元素中,原子半径
随着原子序数增大而减小,所以原子半径大小顺序是②>③>①>④,故C错误;
D.元素的非金属性越强,其第一电离能越大,同一周期中,元素的第一电离能随
着原子序数的增大而呈增大趋势,但第ⅡA、第ⅤA族元素第一电离能大于相邻
元素,所以这几种元素第一电离能大小顺序是:④>③>①>②,故D错误。
1.(2020·山东学业水平等级考试,3)短周期主族元素X、Y、Z、W的原子序数
依次增大,基态X原子的电子总数是其最高能级电子数的2倍,Z可与X形成淡
黄色化合物Z X ,Y、W最外层电子数相同。下列说法正确的是( )
2 2
A.第一电离能:W>X>Y>Z
B.简单离子的还原性:Y>X>W
C.简单离子的半径:W>X>Y>Z
D.氢化物水溶液的酸性:Y>W
答案 C
解析 根据Z与X可形成淡黄色化合物Z X ,即该化合物为Na O ,结合原
2 2 2 2
子序数关系可知,X为O元素,Z为Na元素;基态O原子核外有8个电子,是最
高能级2p上排布的电子数的2倍;由原子序数关系可知Y为F元素,则与其同主
族的 W 为 Cl 元素。根据第一电离能递变规律,可知其相对大小顺序为:
F>O>Cl>Na,A项错误;根据非金属性:F>O>Cl,可知简单离子的还原性:Cl->O2
->F-,B项错误;根据离子半径的变化规律,可知简单离子半径:Cl->O2->F->Na
+,C项正确;氢化物水溶液的酸性:HFNa+,B项错误;磷的3p轨道为半满稳定状态,其第一电离能大于硫,C
项错误;NH 分子间存在氢键,导致其沸点高于PH ,D项错误。
3 3
3.(高考组合题)电离能大小的比较及原因。
(1)(2020·全国Ⅰ)Li 及其周期表中相邻元素的第一电离能(I )如表所示。
1
I (Li)>I (Na),原因是_________________________。
1 1
I (Be)>I (B)>I (Li),原因是_____________________________。
1 1 1
I /(kJ·mol-1)
1
Li 520 Be 900 B 801
Na 496 Mg 738 Al 578
(2)(2018·全国卷Ⅲ)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。
第 一 电 离 能 I (Zn)________I (Cu)( 填 “ 大 于 ” 或 “ 小 于 ” ) 。 原 因 是
1 1
___________________________。
(3)(2017·全国卷Ⅲ)元素Mn与O中,第一电离能较大的是________。
答案 (1)Na与Li同主族,Na的电子层数更多,原子半径更大,故第一电离
能更小 Li、Be和B为同周期元素,同周期元素从左至右,第一电离能呈现增大
的趋势;但由于基态Be原子的s能级轨道处于全充满状态,能量更低更稳定,故
其第一电离能大于B的 (2)大于 Zn核外电子排布为全满稳定结构,较难失电
子 (3)O
4.(高考组合题)电负性大小的比较判断。
(1)(2019·全国卷Ⅲ)NH H PO 中,电负性最高的元素是________。
4 2 4
(2)(2016·全国Ⅰ)光催化还原CO 制备CH 反应中,带状纳米Zn GeO 是该反
2 4 2 4
应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是_____________。
(3)(2015·全国卷Ⅱ)O、Na、P、Cl四种元素中电负性最大的是________(填元素
符号)。
答案 (1)O (2)O>Ge>Zn (3)O
5.(高考组合题)原子半径或离子半径大小的判断及原因。
(1)(2019·全国卷Ⅱ)比较离子半径:F-________O2-(填“大于”“等于”或“小于”)。
(2)(2018·全国卷Ⅰ)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是
_________________________________。
(3)(2020·全国卷Ⅲ)氨硼烷(NH BH )含氢量高、热稳定性好,是一种具有潜力
3 3
的固体储氢材料。H、B、N中,原子半径最大的是________。
答案 (1)小于 (2)Li+核电荷数较大 (3)B
6.(高考组合题)对角线规则的应用。
(1)(2020·全国Ⅲ)根据对角线规则,B的一些化学性质与元素________的相似
(2)(2019·全国卷Ⅲ)在周期表中,与 Li 的化学性质最相似的邻族元素是
________,该元素基态原子核外M层电子的自旋状态________(填“相同”或
“相反”)。
答案 (1)Si (2)Mg 相反
一、选择题(每小题只有一个选项符合题意)
1.价电子排布为5s25p1的元素在周期表中的位置是( )
A.第四周期第ⅤA族 B.第五周期第ⅢA族
C.第五周期第ⅠA族 D.第四周期第ⅢA族
答案 B
2.长式周期表共有18个纵行,碱金属为第1列,稀有气体元素为第18列。按
这种规定下列说法正确的是( )
A.第四周期第9列元素是铁元素
B.只有第二列的元素原子最外层电子排布为ns2
C.第9列中元素中没有非金属元素
D.第10、11列为ds区
答案 C
解析 第四周期第9列元素是钴元素,铁元素处于第四周期第8列,A项错
误;氦原子及一些过渡元素原子最外层电子排布也为ns2,B项错误;第9列属于
Ⅷ族,都是金属元素,没有非金属元素,C项正确;第10列属于Ⅷ族,为d区;第
11列属于ⅠB族,为ds区,D项错误。
3.(2020·烟台一模)下列关于原子结构与元素周期表的说法正确的是( )
A.电负性最大的元素位于周期表的左下角
B.基态原子最外层电子排布为ns2的元素都位于周期表ⅡAC.某基态原子的电子排布式为[Ar]3d104s24p1,该元素位于周期表第四周期
ⅢA族
D.基态原子p能级电子半充满的原子第一电离能一定大于p能级有一对成
对电子的
答案 C
解析 A.电负性最大的元素为F元素,位于周期表的右上角,故A错误;B.
基态原子最外层电子排布为ns2的元素,位于周期表ⅡA、0族、过渡元素,如第Ⅱ
A元素原子为ns2,氦最外层1s2,过渡元素中3d14s2,故B错误;C.某基态原子的
电子排布式为[Ar]3d104s24p1,核电荷数31,为Ga元素,位于周期表中的第四周期
第ⅢA族,故C正确;D.基态原子p能级电子半充满的原子第一电离能,不一定
大于p能级有一对成对电子的,p能级有一对成对电子的为四个电子,如P的第
一电离能小于C的第一电离能,故D错误。
4.(2020·山东模考)下列关于原子结构及元素周期表的说法错误的是( )
A.ⅡA族基态原子最外层电子排布均为ns2
B.第三、第四周期同主族元素的原子序数均相差8
C.第四周期ⅡA族与ⅢA族元素的原子序数相差11
D.基态原子3d轨道上有5个电子的元素位于ⅥB族或ⅦB族
答案 B
解析 选项A,ⅡA族元素基态原子最外层电子排布均为ns2,正确;选项B,
第三、第四周期同主族元素的原子序数ⅠA族、ⅡA族均相差8,ⅢA~ⅦA族
均相差18,错误;选项C,第四周期ⅡA族与ⅢA族元素的原子序数相差11,正
确;选项D,基态原子3d轨道上有5个电子的元素是Cr和Mn两种元素,它们分
别位于ⅥB族和ⅦB族,正确。
5.下列事实不能说明元素的金属性或非金属性相对强弱的是( )
选项 事实 结论
A 与冷水反应,Na比Mg强烈 金属性:Na>Mg
B Ca(OH) 的碱性强于Mg(OH) 金属性:Ca>Mg
2 2
C SO 与NaHCO 溶液反应生成CO 非金属性:S>C
2 3 2
t ℃时,Br +H 2HBr K=5.6×107
2 2
D 非金属性:Br>I
I +H 2HI K=43
2 2
答案 C
解析 C项,根据事实可知,H SO 比H CO 酸性强,但H SO 不是最高价含
2 3 2 3 2 3氧酸,故不能说明非金属性:S>C。
6.(2020·青岛三模)下列关于原子结构及元素周期表的说法错误的是( )
A.位于同一轨道内电子的运动状态也不相同
B.位于d区和ds区的元素都是金属元素
C.前四周期未成对电子数最多的元素位于ⅥB族
D.基态原子最外层电子排布为ns1的元素均在ⅠA族或ⅠB族
答案 D
解析 A.同一轨道内电子自旋方向相反,位于同一轨道内电子的运动状态
也不相同,故A正确;B.d区和ds区的元素包括副族和第Ⅷ族元素,副族和第Ⅷ
族元素全部是金属元素,故B正确;C.1~36号元素,未成对电子数最多的元素外
围电子排布为3d54s1,共有6个未成对电子,该元素是铬,处于周期表中第四周期
第ⅥB族,故C正确;D.基态原子最外层电子排布为ns1的元素如铬、铑等,则基
态原子最外层电子排布为ns1的元素并不全在ⅠA族或ⅠB族,故D错误。
7.下列关于Na、Mg、Cl、Br元素及其化合物的说法正确的是( )
A.NaOH的碱性比Mg(OH) 的强
2
B.Cl 得到电子的能力比Br 的弱
2 2
C.原子半径r:r(Br)>r(Cl)>r(Mg)>r(Na)
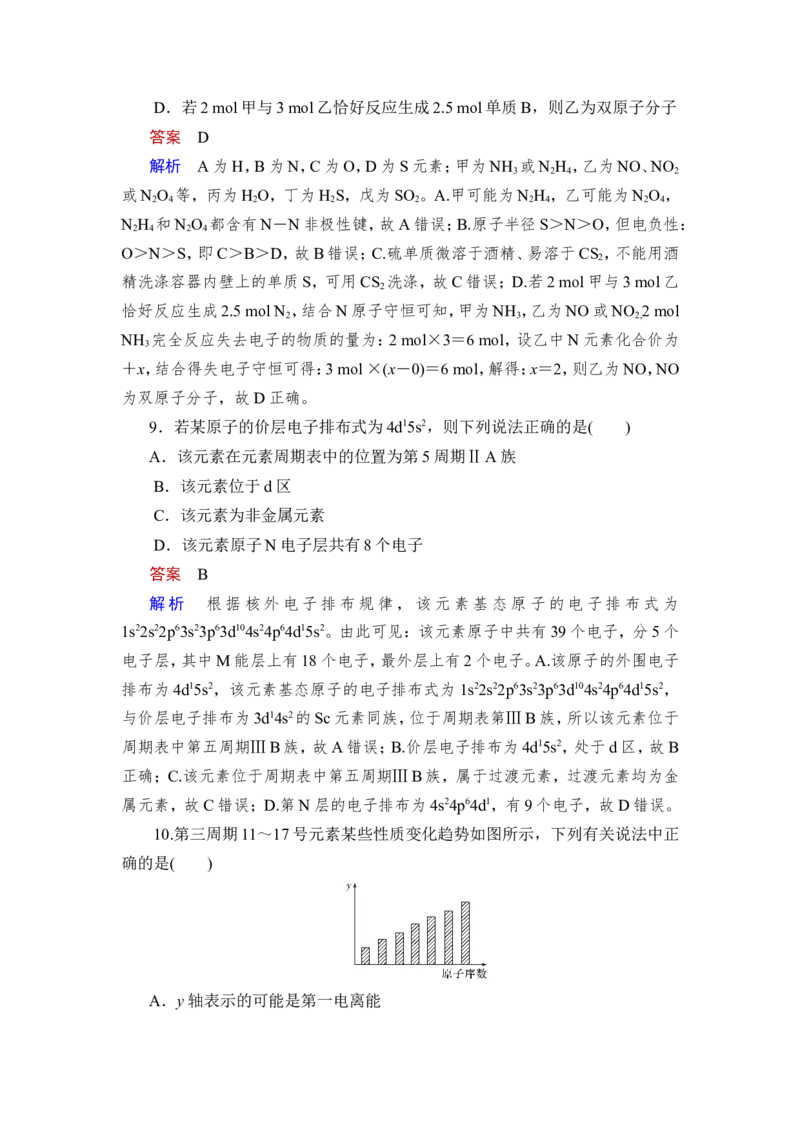
D.原子的最外层电子数n:n(Na)Z>YB.简单氢化物的沸点:W>Z
C.Z与X、Y、R、W均可形成多种化合物
D.Z、R、W三种元素形成的化合物的水溶液呈中性
答案 C
解析 R的原子半径是同周期主族元素中最大的,则R为第ⅠA族元素,根
据题意可知R元素之前至少还有3种短周期元素,所以R为Na元素;Y和X可
以形成阳离子[YX ]+,可推测X为H元素,Y为N元素,[XWZ ]-为酸式盐的阴
4 4
离子,Z、W为同族元素,不难推出Z为O元素,W为S元素;综上所述X为H、Y
为N、Z为O、R为Na、W为S。电子层数越多原子半径越大,电子层数相同核电
荷数越小半径越大,所以原子半径:S>N>O,即W>Y>Z,故A错误;W和Z的简
单氢化物分别为H S、H O,水分子间存在氢键,所以沸点:H SSe>As Br>As>Se
(5)Cu失去一个电子变成电子结构为[Ar]3d10的Cu+,能量较低,结构稳定,所
以Cu的第二电离能相对较大(或Zn失去一个电子变成电子结构为[Ar]3d104s1的
Zn+,易再失去一个电子,所以Zn的第二电离能相对较小。或Cu原子失去一个电
子后,核外电子排布式为[Ar]3d10,而锌原子失去1个电子后的核外电子排
解析 (1)Mn的原子序数为25,电子排布式为1s22s22p63s23p63d54s2,位于第
四周期第ⅦB族,属于d区元素。(2)基态铬原子核外有24个电子,电子排布式为
1s22s22p63s23p63d54s1或[Ar]3d54s1,第四周期最外层电子数为1的原子还有K、
Cu。(3)基态Fe原子核外有4个电子层,电子占据的最高能层为第四层,符号为
N。该能层有s、p、d、f四个能级,原子轨道数为1+3+5+7=16。其价层电子排布
式为3d64s2,故N层的电子数为2。(4)同周期元素从左到右电负性逐渐增大,故
电负性:Br>Se>As。同周期元素从左到右第一电离能呈增大趋势,但由于As的4p
能级半充满,为稳定结构,其第一电离能大于Se,故第一电离能:Br>As>Se。(5)
根据Cu、Zn失去一个电子后的结构,分析再失去一个电子的难易,从而比较Cu、
Zn的第二电离能。
14.下表列出前20号元素中的某些元素性质的一些数据:
元素 原子半径(10-10m) 最高价态(价) 最低价态(价)
① 1.02 +6 -2
② 2.27 +1 -
③ 0.74 - -2
④ 1.43 +3 -
⑤ 0.77 +4 -4
⑥ 1.10 +5 -3
⑦ 0.99 +7 -1
⑧ 1.86 +1 -
⑨ 0.75 +5 -3
⑩ 1.17 +4 -4
请回答下列问题:
(1)以上10种元素中,第一电离能最小的是________(填序号)。
(2)上述⑤⑥⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足
8电子稳定结构的物质可能是________(写分子式)。元素⑨和⑩形成的化合物的化学式为________,元素①的原子价层电子排布式是________。
(3)①⑥⑦⑩ 四种元素的气态氢化物的稳定性,由强到弱的顺序是
____________________________________________________________________
(填化学式)。
(4)③和⑨两元素比较,非金属性较弱的是________(填名称),可以验证你的
结论的是下列中的________。
A.气态氢化物的挥发性和稳定性
B.单质中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表③和⑨两元素)
F.两单质在自然界的存在形式
答案 (1)② (2)PCl 、CCl Si N 3s23p4
3 4 3 4
(3)HCl>H S>PH >SiH (4)氮元素 CE
2 3 4
解析 由题意可知,10种元素是前20号元素,根据表中数据,我们不难推出
①S,②K,③O,④Al,⑤C,⑥P,⑦Cl,⑧Na,⑨N,⑩Si。(1)在同一周期中,从
第ⅠA族到第ⅦA族,元素的第一电离能呈增大趋势;同一主族中,从上向下,元
素的第一电离能逐渐减小,故在10种元素中,第一电离能最小的是②K。(2)C、
P、Cl中的某两种元素形成的化合物中,PCl 或CCl 分子中的每一个原子都满足
3 4
8电子稳定结构;根据化合价知氮和硅形成氮化硅Si N ;硫元素的原子价层电子
3 4
排布式是3s23p4。(3)元素的非金属性越强,形成气态氢化物越稳定,非金属性强弱
为Cl>S>P>Si,故其氢化物稳定性为HCl>H S>PH >SiH 。(4)氧元素和氮元素相
2 3 4
比,非金属性较弱的是氮元素,可通过C、E验证。
15.表1是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
试回答下列问题:
表1
(1)元素p为26号元素,请写出其基态原子电子排布式:
________________________。
(2)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_______________________________。
(3)o、p两元素的部分电离能数据如表2:
元素
o p
电离能/kJ·mol-1
I 717 759
1
I 1 509 1 561
2
I 3 248 2 957
3
表2
比较两元素的I 、I 可知,气态o2+再失去一个电子比气态p2+再失去一个电子
2 3
难。对此,你的解释是___________________________________。
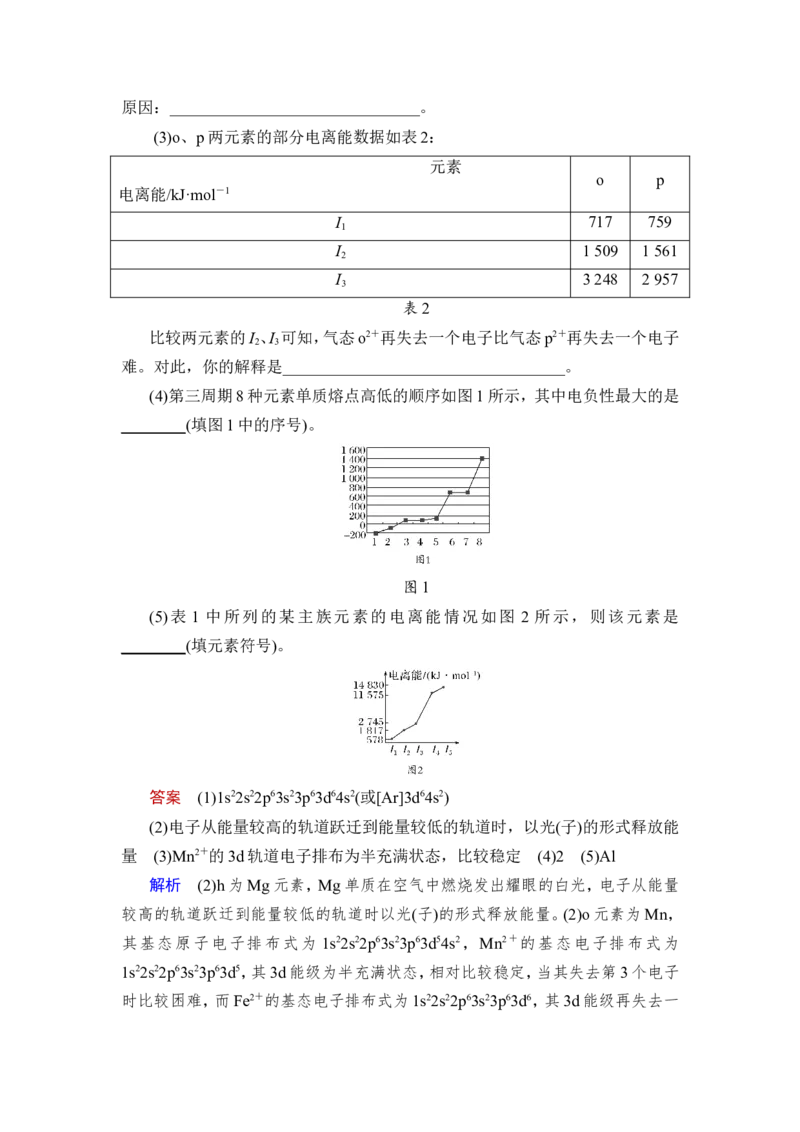
(4)第三周期8种元素单质熔点高低的顺序如图1所示,其中电负性最大的是
________(填图1中的序号)。
图1
(5)表 1 中所列的某主族元素的电离能情况如图 2 所示,则该元素是
________(填元素符号)。
答案 (1)1s22s22p63s23p63d64s2(或[Ar]3d64s2)
(2)电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能
量 (3)Mn2+的3d轨道电子排布为半充满状态,比较稳定 (4)2 (5)Al
解析 (2)h为Mg元素,Mg单质在空气中燃烧发出耀眼的白光,电子从能量
较高的轨道跃迁到能量较低的轨道时以光(子)的形式释放能量。(2)o元素为Mn,
其基态原子电子排布式为 1s22s22p63s23p63d54s2,Mn2+的基态电子排布式为
1s22s22p63s23p63d5,其3d能级为半充满状态,相对比较稳定,当其失去第3个电子
时比较困难,而Fe2+的基态电子排布式为1s22s22p63s23p63d6,其3d能级再失去一个电子即为半充满状态,故其失去第3个电子比较容易。(4)第三周期8种元素分
别为钠、镁、铝、硅、磷、硫、氯、氩,其单质中钠、镁、铝形成金属晶体,熔点依次升
高;硅形成原子晶体;磷、硫、氯、氩形成分子晶体,且常温下磷、硫为固体,氯气、
氩为气体,8种元素熔点最低的为氩,其次为氯,其中电负性最大的为氯。(5)由图
可知,该元素的电离能I 远大于I ,故为第ⅢA族元素,应为Al。
4 3
微专题18 “位—构—性”综合推断题的解题方法
一、依据原子结构或物质结构推断元素
1.根据核外电子的排布三大规律推断元素
(1)最外层电子规律
最外层电子数(N) 3≤N<8 N=1或2 N>次外层电子数
第ⅠA族、第ⅡA
元素在周期表中的 ⅢA族~ⅦA 第二周期(Li、Be)除
族、第Ⅷ族、副族、0
位置 族 外
族元素氦
(2)“阴三、阳四”规律
某元素阴离子最外层电子数与次外层电子数相等,该元素位于第三周期;若
为阳离子,则位于第四周期。如S2-、K+最外层电子数与次外层电子数相等,则S
位于第三周期,K位于第四周期。
(3)“阴上、阳下”规律
电子层结构相同的离子,若电性相同,则位于同周期,若电性不同,则阳离子
位于阴离子的下一周期。如O2-、F-、Na+、Mg2+、Al3+电子层结构相同,则Na、
Mg、Al位于O、F的下一周期。
2.依据物质结构推断元素
突破口是元素的价态。
(1)常见非金属元素。H、Cl、F:一价,形成一个共价键;O、S:二价,形成两个
共价键;N、P:三价,形成三个共价键;C、Si:四价,形成四个共价键。
(2)常见金属元素。K、Na、Li:形成+1价阳离子;Ca、Mg:形成+2价阳离子。
【典例1】 (2020·课标全国Ⅱ,13)一种由短周期主族元素组成的化合物(如图
所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和
为24。下列有关叙述错误的是( )
A.该化合物中,W、X、Y之间均为共价键B.Z的单质既能与水反应,也可与甲醇反应
C.Y的最高化合价氧化物的水化物为强酸
D.X的氟化物XF 中原子均为8电子稳定结构
3
答案 D
解析 由题意,4种短周期元素中,Z的原子序数最大,且能形成Z+,则Z为
Na元素,W的原子序数最小,且形成一个化学键,则W为H元素,再由4种元素
的原子序数之和为24,可知X与Y的原子序数之和为12,结合题给化合物中X
与Y的成键数,可知X为B元素,Y为N元素。从该化合物的成键情况可确定H、
B、N之间均为共价键,A项正确;Na为活泼金属,既能与水反应,又能与CH OH
3
发生置换反应生成H ,B项正确;氮元素的最高价氧化物对应的水化物为HNO ,
2 3
是典型的强酸,C项正确;BF 中B原子不满足8电子稳定结构,D项错误。
3
二、依据元素周期表结构片段推断元素
族序数等于周期数的元素 H、Be、Al
族序数等于周期数2倍的元素 C、S
族序数等于周期数3倍的元素 O
周期数是族序数2倍的元素 Li、Ca
周期数是族序数3倍的元素 Na、Ba
最高正价与最低负价代数和为零的短周期元素 H、C、Si
最高正价是最低负价绝对值3倍的短周期元素 S
除H外,原子半径最小的元素 F
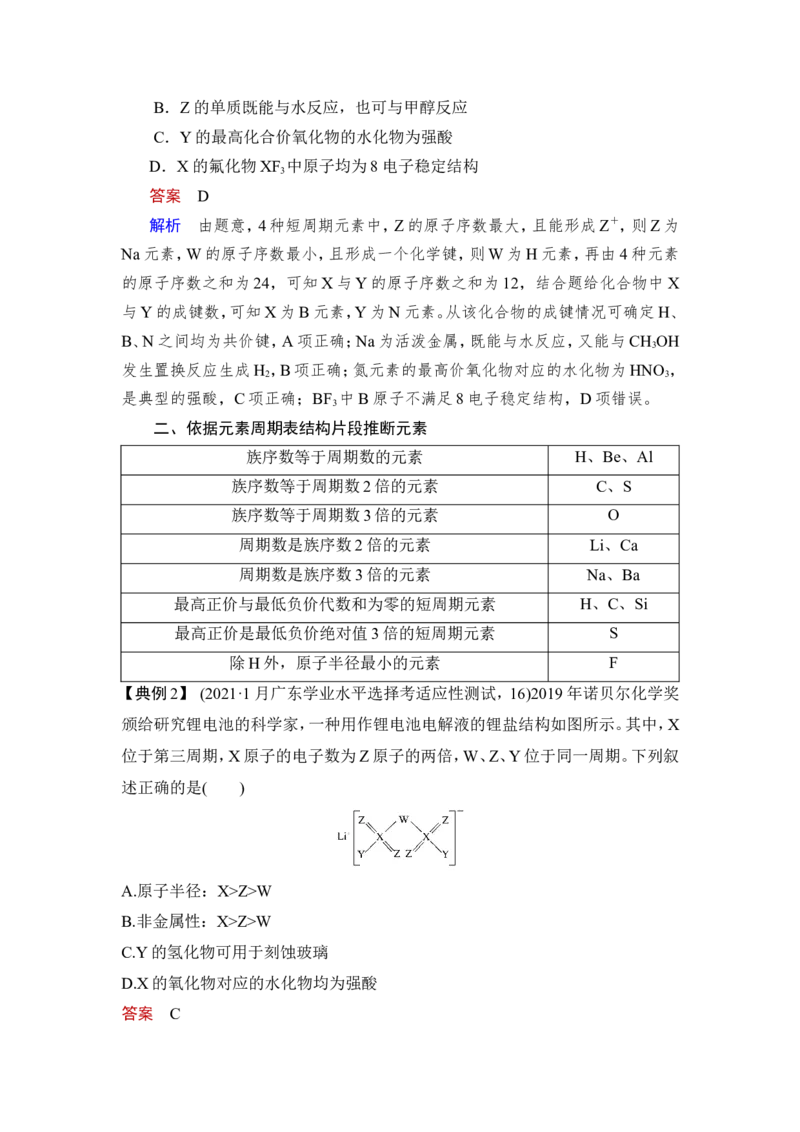
【典例2】 (2021·1月广东学业水平选择考适应性测试,16)2019年诺贝尔化学奖
颁给研究锂电池的科学家,一种用作锂电池电解液的锂盐结构如图所示。其中,X
位于第三周期,X原子的电子数为Z原子的两倍,W、Z、Y位于同一周期。下列叙
述正确的是( )
A.原子半径:X>Z>W
B.非金属性:X>Z>W
C.Y的氢化物可用于刻蚀玻璃
D.X的氧化物对应的水化物均为强酸
答案 C解析 据图可知X可以形成6个共价键,X原子的电子数为Z原子的两倍,
则原子序数为偶数,且位于第三周期,所以为S元素,则Z为O元素;W、Z、Y位
于同一周期,Y可以形成一个共价键,则Y为F元素,整个离子带一个单位负电
荷,则W为N元素。A.电子层数越多,原子半径越大,电子层数相同,核电荷数越
小原子半径越大,所以原子半径S>N>O,即X>W>Z,故A错误;B.同主族自上而
下非金属性减弱,所以非金属性O>S,即Z>X,故B错误;C.Y为F元素,其氢化
物为HF,可以与SiO 反应从而刻蚀玻璃,故C正确;D.X为S元素,其+4价氧化
2
物对应的水化物H SO 为弱酸,故D错误。
2 3
三、依据元素及其化合物性质和转化关系推断元素
物质特性 推断元素
形成化合物种类最多的元素或单质是自然界中硬度最大的物质的
C
元素或气态氢化物中氢的质量分数最大的元素
空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素 N
地壳中含量最多的元素或氢化物的沸点最高的元素或氢化物在通
O
常情况下呈液态的元素
最活泼的金属元素或最高价氧化物对应水化物碱性最强的元素或
Cs
阳离子的氧化性最弱的元素
单质最易着火的非金属元素 P
焰色试验呈黄色的元素 Na
焰色试验呈紫色(透过蓝色钴玻璃)的元素 K
单质密度最小的元素 H
单质密度最小的金属元素 Li
常温下单质呈液态的非金属元素 Br
常温下单质呈液态的金属元素 Hg
最高价氧化物及其水化物既能与强酸反应,又能与强碱反应的元素 Al
元素的气态氢化物和它的最高价氧化物对应水化物发生氧化还原
S
反应的元素
常见的一种元素存在几种单质的元素 C、P、O、S
【典例3】 (2020·威海二模)X、Y、Z、W为原子序数依次增大的短周期主族元
素,只有W为金属元素。甲、乙、丙分别为X、Z、W三种元素所对应的单质。A、
B、C、D均为由X、Y、Z三种元素组成的化合物,化合物B的稀溶液常用于保存
动物标本。它们的转化关系如图所示。下列说法错误的是( )A.X与Z可组成非极性分子
B.原子半径大小关系是:r(X)<r(Z)<r(Y)<r(W)
C.四种化合物中B的沸点最低
D.四种化合物中Y原子的杂化方式有2种
答案 A
解析 化合物B的稀溶液常用于保存动物标本,B为HCHO,则X、Y、Z分别
为H、C、O;甲、乙、丙分别为X、Z、W三种元素所对应的单质,可确定甲、乙分别
为H 、O ;由转化关系可知,A为CH OH,C为HCOOH,D为HCOOCH ;A与丙
2 2 3 3
反应可生成甲,则丙为Na,W为Na。A.X与Z分别为H和O,二者可组成H O、
2
H O ,它们都是极性分子,故A错误;B.H的核外只有1个电子层,半径最小,C、
2 2
O同周期,C在O的左边,原子半径C比O大,Na的电子层数最多,半径最大,所
以原子半径大小关系是:r(H)<r(O)<r(C)<r(Na),故B正确;C.四种化合物中,B
为HCHO,常温下呈气态,而另三种物质都呈液态,所以B的沸点最低,故C正确;
D.四种化合物中Y原子的杂化方式有:含-CH 的物质,碳原子发生sp3杂化,含
3
碳氧双键的物质,碳氧双键中碳原子发生sp2杂化,故D正确。
1.(2021·1月重庆市学业水平选择考适应性测试,6)短周期主族元素W、X、Y、Z
的原子序数依次增大,W的核外电子数等于其主族序数,X的单质在空气中含量
最多,Y的最高价氧化物的水化物是两性化合物,Z的最高正价与最低负价代数
和为4。下列说法错误的是( )
A.W与X形成的最简单化合物极易溶于水
B.Y和Z可形成化合物Y Z
2 3
C.最外层电子数Z>X>Y>W
D.Y和Z的简单离子的电子层结构相同
答案 D
解析 W为氢元素,X为氮元素,Y为铝元素,Z为硫元素。A项,NH 极易溶
3
于水,正确;B项,铝与硫可形成Al S ,正确;C项,最外层电子数S>N>Al>H,正
2 3
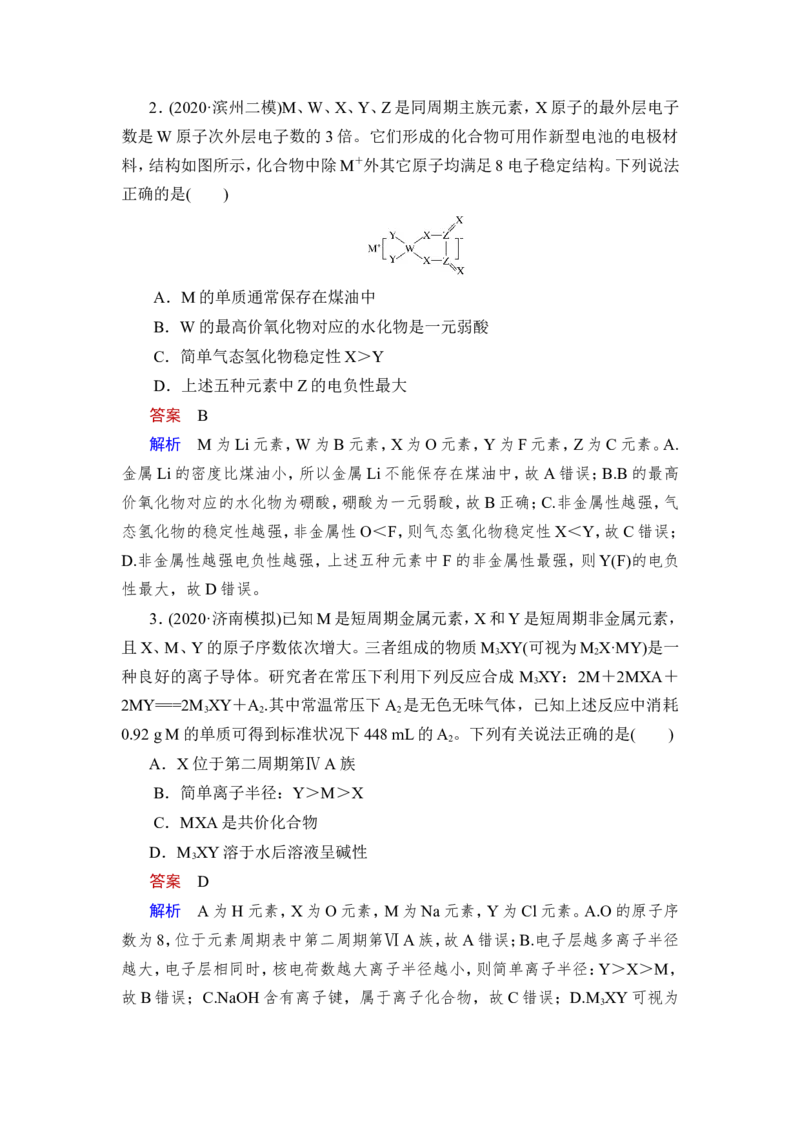
确;D项,Al3+为10电子离子,S2-为18电子离子,电子层结构不同,错误。2.(2020·滨州二模)M、W、X、Y、Z是同周期主族元素,X原子的最外层电子
数是W原子次外层电子数的3倍。它们形成的化合物可用作新型电池的电极材
料,结构如图所示,化合物中除M+外其它原子均满足8电子稳定结构。下列说法
正确的是( )
A.M的单质通常保存在煤油中
B.W的最高价氧化物对应的水化物是一元弱酸
C.简单气态氢化物稳定性X>Y
D.上述五种元素中Z的电负性最大
答案 B
解析 M为Li元素,W为B元素,X为O元素,Y为F元素,Z为C元素。A.
金属Li的密度比煤油小,所以金属Li不能保存在煤油中,故A错误;B.B的最高
价氧化物对应的水化物为硼酸,硼酸为一元弱酸,故B正确;C.非金属性越强,气
态氢化物的稳定性越强,非金属性O<F,则气态氢化物稳定性X<Y,故C错误;
D.非金属性越强电负性越强,上述五种元素中F的非金属性最强,则Y(F)的电负
性最大,故D错误。
3.(2020·济南模拟)已知M是短周期金属元素,X和Y是短周期非金属元素,
且X、M、Y的原子序数依次增大。三者组成的物质M XY(可视为M X·MY)是一
3 2
种良好的离子导体。研究者在常压下利用下列反应合成 M XY:2M+2MXA+
3
2MY===2M XY+A .其中常温常压下A 是无色无味气体,已知上述反应中消耗
3 2 2
0.92 g M的单质可得到标准状况下448 mL的A 。下列有关说法正确的是( )
2
A.X位于第二周期第ⅣA族
B.简单离子半径:Y>M>X
C.MXA是共价化合物
D.M XY溶于水后溶液呈碱性
3
答案 D
解析 A为H元素,X为O元素,M为Na元素,Y为Cl元素。A.O的原子序
数为8,位于元素周期表中第二周期第ⅥA族,故A错误;B.电子层越多离子半径
越大,电子层相同时,核电荷数越大离子半径越小,则简单离子半径:Y>X>M,
故B错误;C.NaOH含有离子键,属于离子化合物,故C错误;D.M XY可视为
3Na O·NaCl,溶于水生成氢氧化钠,其水溶液呈碱性,故D正确。
2
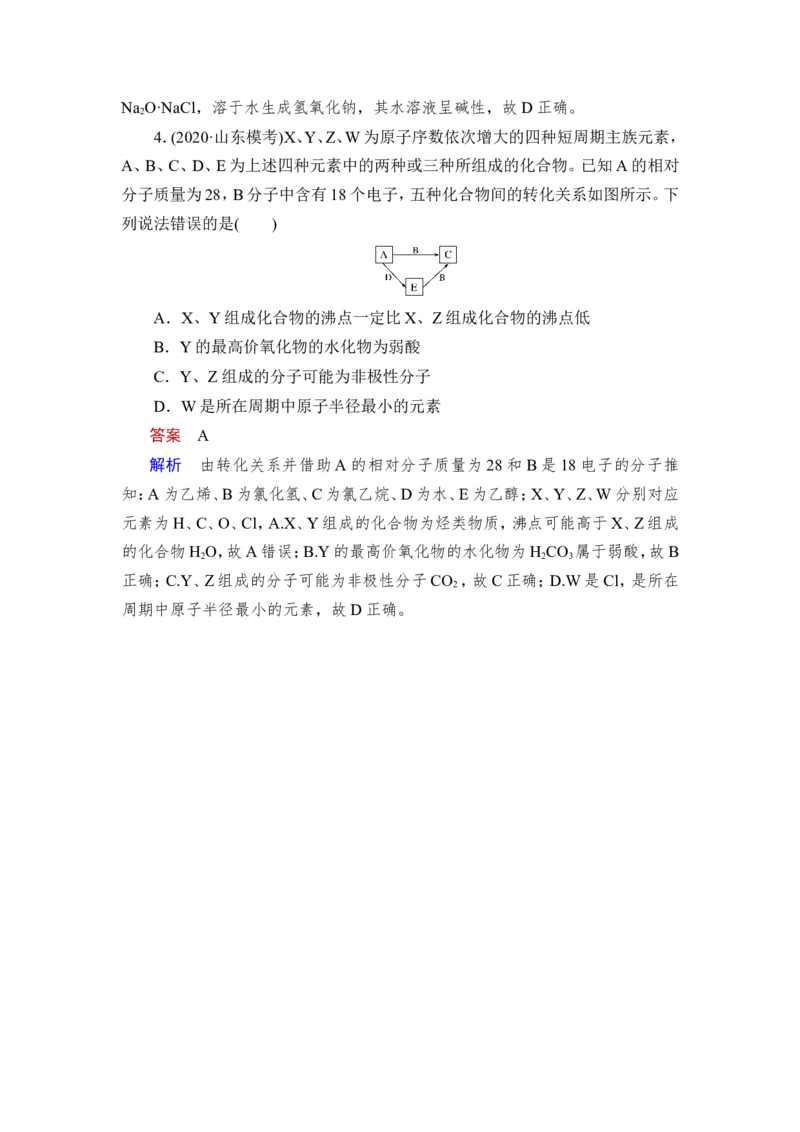
4.(2020·山东模考)X、Y、Z、W为原子序数依次增大的四种短周期主族元素,
A、B、C、D、E为上述四种元素中的两种或三种所组成的化合物。已知A的相对
分子质量为28,B分子中含有18个电子,五种化合物间的转化关系如图所示。下
列说法错误的是( )
A.X、Y组成化合物的沸点一定比X、Z组成化合物的沸点低
B.Y的最高价氧化物的水化物为弱酸
C.Y、Z组成的分子可能为非极性分子
D.W是所在周期中原子半径最小的元素
答案 A
解析 由转化关系并借助A的相对分子质量为28和B是18电子的分子推
知:A为乙烯、B为氯化氢、C为氯乙烷、D为水、E为乙醇;X、Y、Z、W分别对应
元素为H、C、O、Cl,A.X、Y组成的化合物为烃类物质,沸点可能高于X、Z组成
的化合物H O,故A错误;B.Y的最高价氧化物的水化物为H CO 属于弱酸,故B
2 2 3
正确;C.Y、Z组成的分子可能为非极性分子CO ,故C正确;D.W是Cl,是所在
2
周期中原子半径最小的元素,故D正确。