文档内容
第 53 讲 酸碱中和滴定及拓展应用
[复习目标] 1.了解酸碱中和滴定的原理和滴定终点的判断方法,知道指示剂选择的方法。
2.掌握酸碱中和滴定的操作和数据处理误差分析的方法。3.掌握滴定法在定量测定中的应用。
考点一 酸碱中和滴定的原理与操作
1.原理
利用酸碱中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法。以标准
HCl 溶液滴定待测的 NaOH 溶液,待测的 NaOH 溶液的物质的量浓度为 c(NaOH)=
________________。
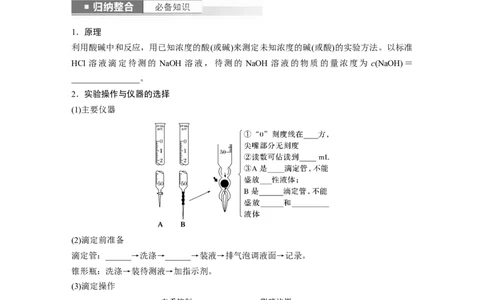
2.实验操作与仪器的选择
(1)主要仪器
(2)滴定前准备
滴定管:______→洗涤→______→装液→排气泡调液面→记录。
锥形瓶:洗涤→装待测液→加指示剂。
(3)滴定操作
(4)滴定终点
滴入最后半滴标准液,指示剂变色,且在半分钟内不恢复原来的颜色,停止滴定,并记录标
准溶液的体积。
(5)数据处理
按上述操作重复________次,根据每次所用标准液的体积计算待测液的物质的量浓度,最后
求出待测液的物质的量浓度的________。3.关键
(1)准确测定参加反应的酸、碱溶液的______。
(2)选取适当的指示剂,准确判断______________________________________________。
熟记:常见酸碱指示剂的变色范围
指示剂 变色范围和pH
石蕊
甲基橙
酚酞
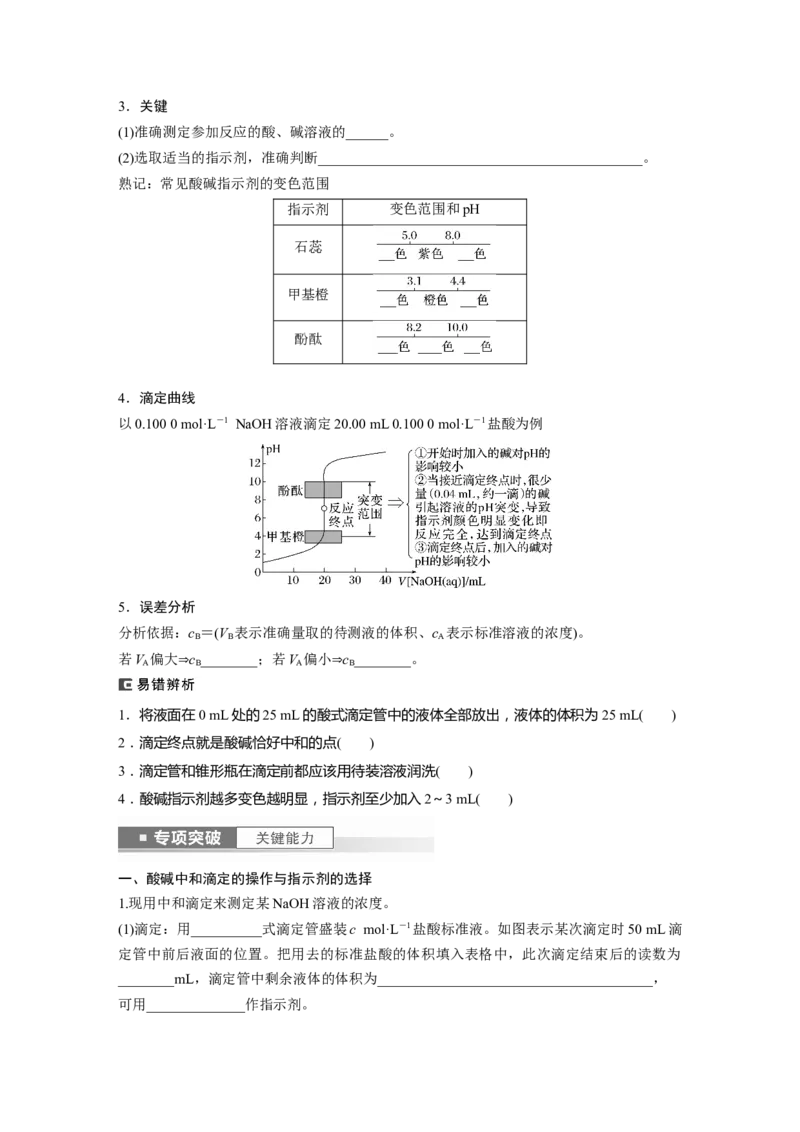
4.滴定曲线
以0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1盐酸为例
5.误差分析
分析依据:c =(V 表示准确量取的待测液的体积、c 表示标准溶液的浓度)。
B B A
若V 偏大⇒c ________;若V 偏小⇒c ________。
A B A B
1.将液面在0 mL处的25 mL的酸式滴定管中的液体全部放出,液体的体积为25 mL( )
2.滴定终点就是酸碱恰好中和的点( )
3.滴定管和锥形瓶在滴定前都应该用待装溶液润洗( )
4.酸碱指示剂越多变色越明显,指示剂至少加入2~3 mL( )
一、酸碱中和滴定的操作与指示剂的选择
1.现用中和滴定来测定某NaOH溶液的浓度。
(1)滴定:用__________式滴定管盛装c mol·L-1盐酸标准液。如图表示某次滴定时50 mL滴
定管中前后液面的位置。把用去的标准盐酸的体积填入表格中,此次滴定结束后的读数为
________mL,滴定管中剩余液体的体积为_______________________________________,
可用______________作指示剂。(2)排出碱式滴定管中气泡的方法应采用下图______(填“甲”“乙”或“丙”)的操作,然后
挤压玻璃球使尖嘴部分充满碱液。
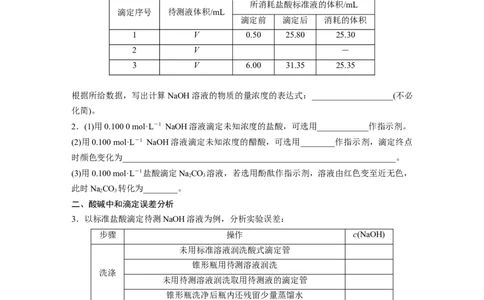
(3)有关数据记录如下:
所消耗盐酸标准液的体积/mL
滴定序号 待测液体积/mL
滴定前 滴定后 消耗的体积
1 V 0.50 25.80 25.30
2 V -
3 V 6.00 31.35 25.35
根据所给数据,写出计算NaOH溶液的物质的量浓度的表达式:___________________(不必
化简)。
2.(1)用0.100 0 mol·L-1 NaOH溶液滴定未知浓度的盐酸,可选用____________作指示剂。
(2)用0.100 mol·L-1 NaOH溶液滴定未知浓度的醋酸,可选用________作指示剂,滴定终点
时颜色变化为________________________________________________________________。
(3)用0.100 mol·L-1盐酸滴定NaCO 溶液,若选用酚酞作指示剂,溶液由红色变至近无色,
2 3
此时NaCO 转化为________。
2 3
二、酸碱中和滴定误差分析
3.以标准盐酸滴定待测NaOH溶液为例,分析实验误差:
步骤 操作 c(NaOH)
未用标准溶液润洗酸式滴定管
锥形瓶用待测溶液润洗
洗涤
未用待测溶液润洗取用待测液的滴定管
锥形瓶洗净后瓶内还残留少量蒸馏水
取液 取碱液的滴定管尖嘴部分有气泡且取液结束前气泡消失
滴定完毕后立即读数,半分钟后颜色又变红
滴定前滴定管尖嘴部分有气泡,滴定后消失
滴定
滴定过程中振荡时有液滴溅出
滴定过程中,向锥形瓶内加少量蒸馏水
滴定前仰视读数或滴定后俯视读数
读数
滴定前俯视读数或滴定后仰视读数三、滴定曲线的分析
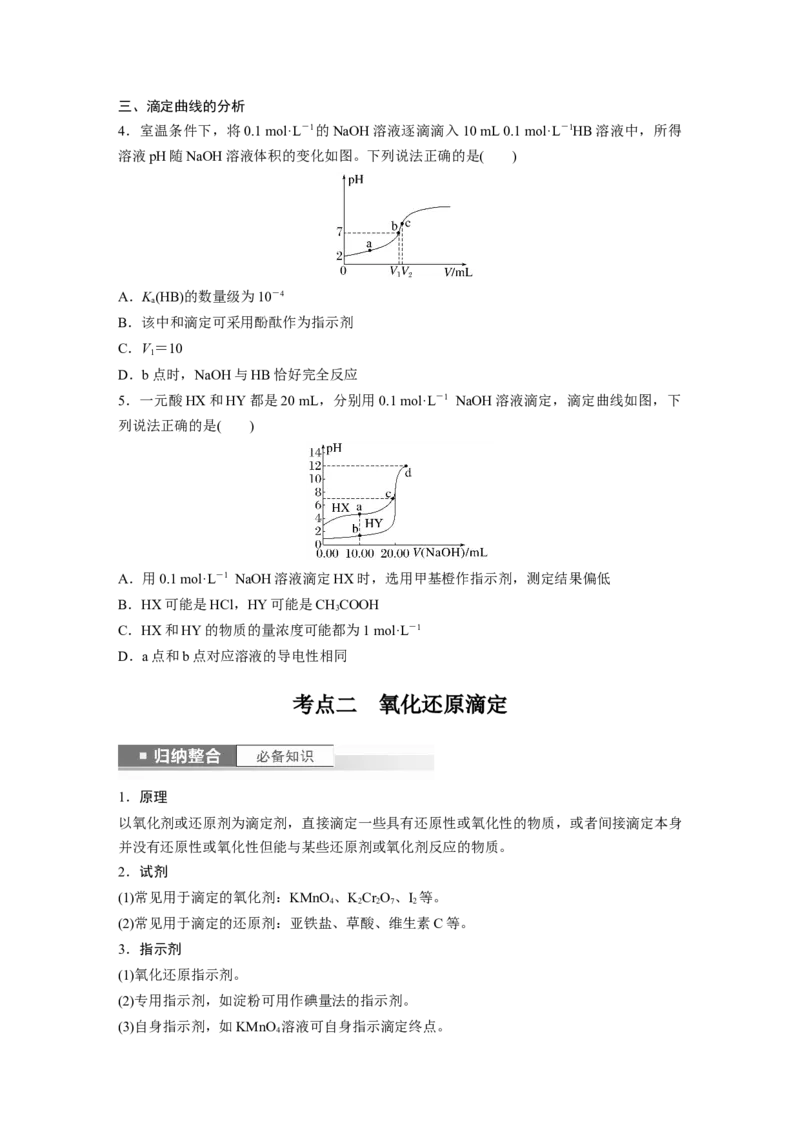
4.室温条件下,将0.1 mol·L-1的NaOH溶液逐滴滴入10 mL 0.1 mol·L-1HB溶液中,所得
溶液pH随NaOH溶液体积的变化如图。下列说法正确的是( )
A.K(HB)的数量级为10-4
a
B.该中和滴定可采用酚酞作为指示剂
C.V=10
1
D.b点时,NaOH与HB恰好完全反应
5.一元酸HX和HY都是20 mL,分别用0.1 mol·L-1 NaOH溶液滴定,滴定曲线如图,下
列说法正确的是( )
A.用0.1 mol·L-1 NaOH溶液滴定HX时,选用甲基橙作指示剂,测定结果偏低
B.HX可能是HCl,HY可能是CHCOOH
3
C.HX和HY的物质的量浓度可能都为1 mol·L-1
D.a点和b点对应溶液的导电性相同
考点二 氧化还原滴定
1.原理
以氧化剂或还原剂为滴定剂,直接滴定一些具有还原性或氧化性的物质,或者间接滴定本身
并没有还原性或氧化性但能与某些还原剂或氧化剂反应的物质。
2.试剂
(1)常见用于滴定的氧化剂:KMnO 、KCr O、I 等。
4 2 2 7 2
(2)常见用于滴定的还原剂:亚铁盐、草酸、维生素C等。
3.指示剂
(1)氧化还原指示剂。
(2)专用指示剂,如淀粉可用作碘量法的指示剂。
(3)自身指示剂,如KMnO 溶液可自身指示滴定终点。
4一、直接滴定型
1.为了测定某样品中NaNO 的含量,某同学进行如下实验:①称取样品a g,加水溶解,
2
配制成100 mL溶液。②取25.00 mL溶液于锥形瓶中,用0.020 0 mol·L-1 KMnO 标准溶液
4
(酸性)进行滴定,滴定结束后消耗KMnO 溶液 V mL。
4
(1)滴定过程中发生反应的离子方程式是____________________________________________;
测得该样品中NaNO 的质量分数为____________。
2
(2)若滴定过程中刚出现颜色变化就停止滴定,则测定结果________(填“偏大”“偏小”或
“无影响”)。
二、连续反应型
2.(2022·上海金山区二模)称取0.500 g CuCl成品置于过量FeCl (aq)中,待固体完全溶解后,
3
用0.200 0 mol·L-1的Ce(SO) 标准液滴定至终点,消耗Ce(SO) 标准液24.60 mL。相关
4 2 4 2
反应如下:Fe3++CuCl===Fe2++Cu2++Cl-;Ce4++Fe2+===Fe3++Ce3+。则CuCl的质量分
数是________(保留四位有效数字),若滴定操作耗时过长可能会使测定的 CuCl质量分数
______(填“偏大”或“偏小”)。
三、试剂过量型
3.烟道气中的NO 是主要的大气污染物之一,为了监测其含量,选用如下采样和检测方法。
x
将V L气样通入适量酸化的HO 溶液中,使NO 完全被氧化为NO,加水稀释至100.00
2 2 x
mL。量取20.00 mL该溶液,加入V mL c mol·L-1 FeSO 标准溶液(过量),充分反应后,用
1 1 4
c mol·L-1 KCr O 标准溶液滴定剩余的Fe2+,终点时消耗V mL。
2 2 2 7 2
回答下列问题:
(1)滴定过程中发生下列反应:
3Fe2++NO+4H+===NO↑+3Fe3++2HO
2
Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
则气样中NO 折合成NO 的含量为__________ mg·m-3。
x 2
(2)若FeSO 标准溶液部分变质,会使测定结果________(填“偏高”“偏低”或“无影响”)。
4
答题规范(6) 滴定终点判断
当滴入最后半滴×××标准溶液后,溶液变成×××色,且半分钟内不恢复原来的颜色。
解答此类题目注意三个关键点:
(1)最后半滴:必须说明是滴入“最后半滴”溶液。
(2)颜色变化:必须说明滴入“最后半滴”溶液后溶液“颜色的变化”。(3)半分钟:必须说明溶液颜色变化后“半分钟内不再恢复原来的颜色”。
(1)用a mol·L-1的盐酸滴定未知浓度的NaOH溶液,用酚酞作指示剂,达到滴定终点的现象
是________________________________________________________________________
__________________________________________________________________________;
若用甲基橙作指示剂,滴定终点现象是________________________________________
__________________________________________________________________________。
(2)用标准碘溶液滴定溶有SO 的水溶液,以测定水中SO 的含量,应选用__________作指示
2 2
剂,达到滴定终点的现象是__________________________________________________
__________________________________________________________________________。
(3)用标准酸性KMnO 溶液滴定溶有SO 的水溶液,以测定水中SO 的含量,是否需要选用
4 2 2
指示剂________(填“是”或“否”),达到滴定终点的现象是___________________
________________________________________________________________________。
(4)用氧化还原滴定法测定TiO 的质量分数:一定条件下,将TiO 溶解并还原为Ti3+,再用
2 2
KSCN溶液作指示剂,用NH Fe(SO ) 标准溶液滴定Ti3+至全部生成Ti4+,滴定Ti3+时发生
4 4 2
反应的离子方程式为______________________________________________________,
达到滴定终点的现象是____________________________________________________
________________________________________________________________________。
(5)用标准KI溶液滴定含有Fe3+的溶液,应选用__________作指示剂,滴定终点现象是
________________________________________________________________________
________________________________________________________________________。
1.(2021·广东,7)测定浓硫酸试剂中HSO 含量的主要操作包括:①量取一定量的浓硫酸,
2 4
稀释;②转移定容得待测液;③移取20.00 mL待测液,用0.100 0 mol·L-1的NaOH溶液滴
定。上述操作中,不需要用到的仪器为( )
2.正误判断,正确的打“√”,错误的打“×”。(1)可用“图1”测定醋酸浓度(2021·河北,3A)( )
(2)可用“图2”量取一定体积的KMnO 溶液(2021·天津,6B)( )
4
(3)碱式滴定管排气泡的操作如“图3”(2022·湖南,4A)( )
(4)用标准液润洗滴定管后,应将润洗液从滴定管上口倒出(2022·浙江6月选考,11A)( )
3.(2022·浙江6月选考,23)25 ℃时,向20 mL浓度均为0.1 mol·L-1的盐酸和醋酸的混合
溶液中逐滴加入0.1 mol·L-1的NaOH溶液(醋酸的K=1.8×10-5;用0.1 mol·L-1的NaOH溶
a
液滴定20 mL等浓度的盐酸,滴定终点的pH突跃范围4.3~9.7)。下列说法不正确的是(
)
A.恰好中和时,溶液呈碱性
B.滴加NaOH溶液至pH=4.3的过程中,发生反应的离子方程式为H++OH-===HO
2
C.滴定过程中,c(Cl-)=c(CHCOO-)+c(CHCOOH)
3 3
D.pH=7时,c(Na+)>c(Cl-)>c(CHCOO-)>c(CHCOOH)
3 3
4.[2022·江苏,16(4)]实验中需要测定溶液中Ce3+的含量。已知水溶液中Ce4+可用准确浓度
的(NH )Fe(SO ) 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为
4 2 4 2
亮黄色,滴定反应为Fe2++Ce4+===Fe3++Ce3+。请补充完整实验方案:①准确量取25.00
mL Ce3+溶液[c(Ce3+)约为0.2 mol·L-1],加氧化剂将Ce3+完全氧化并去除多余氧化剂后,用
稀硫酸酸化,将溶液完全转移到 250 mL容量瓶中后定容;②按规定操作分别将0.020 00
mol·L-1
(NH )Fe(SO ) 和待测Ce4+溶液装入如图所示的滴定管中:③__________________
4 2 4 2
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
5.[2022·辽宁,17(7)]测定氢醌法制取HO 样品含量的方法如下:
2 2取2.50 g产品,加蒸馏水定容至100 mL摇匀,取20.00 mL于锥形瓶中,用0.050 0 mol·L-1
酸性KMnO 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为 19.98 mL、20.90
4
mL、20.02 mL。假设其他杂质不干扰结果,产品中HO 质量分数为__________。
2 2