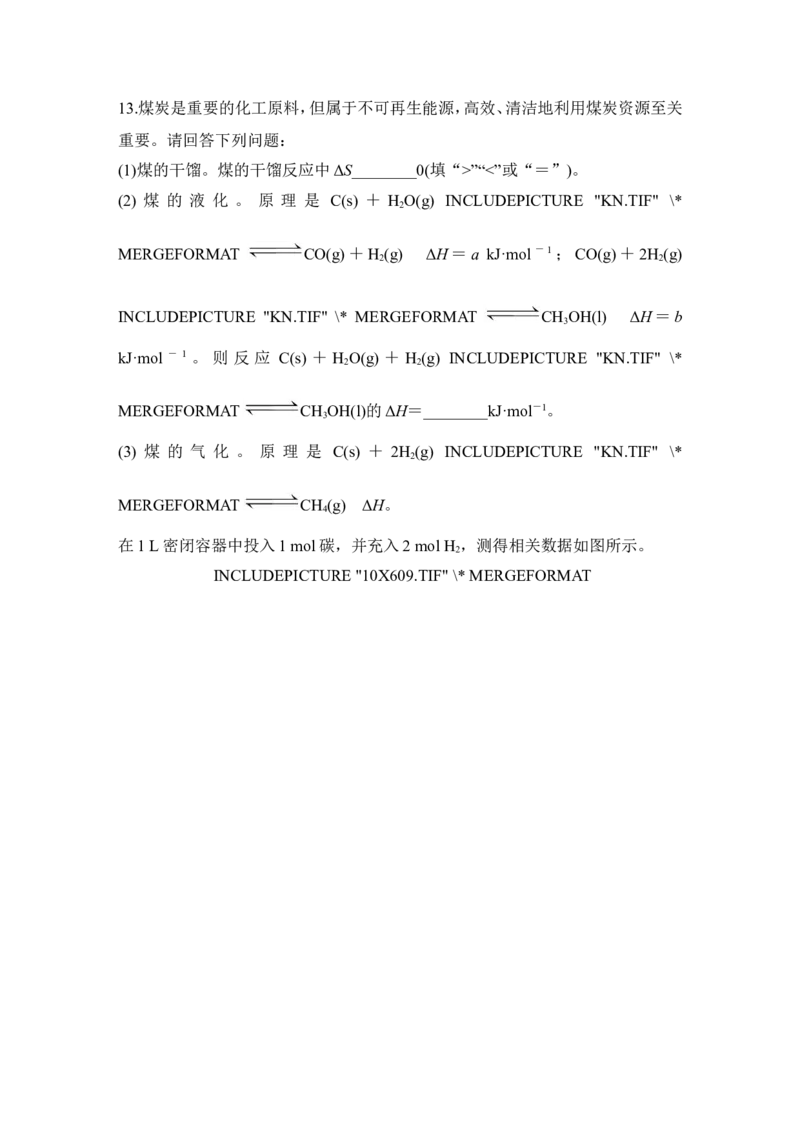文档内容
第3讲 化学平衡常数 化学反应进行的方向
【2020·备考】
最新考纲:1.了解化学平衡常数的含义,能利用化学平衡常数进行相关计算。2.能
正确计算化学反应的转化率。
核心素养:1.变化观念与平衡思想:能从化学平衡常数的角度分析化学反应,运用
化学平衡常数解决问题。能多角度、动态地分析化学反应的转化率,运用化学反应
原理解决实际问题。2.证据推理与模型认知:知道可以通过分析、推理等方法认识
研究对象的本质特征、构成要素及其相互关系,建立模型。能运用模型(Q 与K的
c
关系)解释化学平衡的移动,揭示现象的本质和规律。
考点一 化学平衡常数 转化率
(频数:★★★ 难度:★★☆)
INCLUDEPICTURE "名师课堂.tif" \* MERGEFORMAT INCLUDEPICTURE
" 名 师 课 堂 .tif" \* MERGEFORMAT
INCLUDEPICTURE " 书名号 .TIF " \* MERGEFORMAT INCLUDEPICTURE
" 书名号 .TIF" \* MERGEFORMAT 名师课堂导语 化学平衡常数和转化率是高
考必考点,主要考查化学平衡常数表达式;化学平衡常数和转化率的计算;特别是
通过平衡压强来表示平衡常数和计算转化率是近几年高考重点,复习时应加以关
注。
1.化学平衡常数
(1)概念:
在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓
度幂之积的比值是一个常数,用符号K 表示。
(2)表达式:
对 于 反 应 mA(g) + nB(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMATpC(g)+qD(g),
K=。
(3)实例
化学方程式 平衡常数 关系式
N (g)+3H (g)
2 2
INCLUDEPICTURE
"KN.TIF" \* K =
1
MERGEFORMAT
2NH (g)
3
N (g)+ (g)
2 2
INCLUDEPICTURE
"KN.TIF" \* K = K 2 =(或K 1 ) K 3 =
2
MERGEFORMAT
NH (g)
3
2NH (g) N (g)
3 2 K =
+3H (g) 3
2
INCLUDEPICTURE " 名 师 课 堂 实 录 .tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
(1)纯液体、纯固体物质或稀溶液中水的浓度均不写,但是水蒸气的浓度要写。在非
水溶液中进行的反应,若有水参加或生成,则水的浓度不可视为常数,应写进平衡
常数表达式中。
(2)平衡常数表达式中各物质的浓度为平衡时的浓度,其书写形式与化学方程式的
书写有关。
(4)意义及影响因素
①K值越大,反应物的转化率越大,正反应进行的程度越大通常K>105可认为反应
彻底,K<10-5认为反应不能发生。
②K只受温度影响,与反应物或生成物的浓度变化无关。
③化学平衡常数是指某一具体反应的平衡常数。(5)应用
①判断可逆反应进行的程度。
②利用化学平衡常数,判断反应是否达到平衡或向何方向进行。
对于化学反应 aA(g)+bB(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
cC(g)+dD(g)的任意状态,浓度商:Q =。
c
Q <K,反应向正反应方向进行;
c
Q =K,反应处于平衡状态;
c
Q >K,反应向逆反应方向进行。
c
③利用K可判断反应的热效应:若升高温度,K值增大,则正反应为吸热反应;若
升高温度,K值减小,则正反应为放热反应。
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
(1)计算化学平衡常数利用的是物质的平衡浓度,而不是任意时刻浓度,也不能用
物质的量。
(2)催化剂能加快化学反应速率,但对化学平衡无影响,也不会改变平衡常数的大
小。
2.平衡转化率
对于上例反应中A(g)的平衡转化率可表示为:
α(A)= × 100% {c (A)代表A的初始浓度,c (A)代表A的平衡浓度}。
0 平
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
1.对于 A(g)+B(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
C(g)类反应,达到平衡后,保持温度、容积不变,又加入一定量的A,则平衡向正反
应方向移动,α(B)增大而α(A)减小。
2.对于 aA(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT bB(g)类
反应,达到平衡后,保持温度、容积不变,又加入一定量的A,相当于增大压强。[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)平衡常数表达式中,可以是物质的任一浓度(×)
(2)催化剂能改变化学反应速率,也能改变平衡常数(×)
(3)平衡常数发生变化,化学平衡不一定发生移动(×)
(4)化学平衡发生移动,平衡常数不一定发生变化(√)
(5)平衡常数和转化率都能体现可逆反应进行的程度(√)
2.(教材改编题)(RJ 选修 4·P 2 改编)已知反应 A(g)+3B(g) INCLUDEPICTURE
32
"KN.TIF" \* MERGEFORMAT 3C(g)在一定温度下达到平衡,该反应的平
衡常数表达式为________________。若各物质的平衡浓度分别为c(A)=2.0 mol·L
-1、c(B)=2.0 mol·L-1、c(C)=1.0 mol·L-1,则K=________。
答案 K= 0.062 5
3.(思维探究题)已知下列反应在某温度下的平衡常数:
H (g)+S(s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT H S(g)
2 2
K
1
S(s)+O (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT SO (g)
2 2
K
2
则 在 该 温 度 下 反 应 H (g) + SO (g) INCLUDEPICTURE "KN.TIF" \*
2 2
MERGEFORMAT O (g)+H S(g)的平衡常数为________。
2 2
答案 K /K 。
1 2
INCLUDEPICTURE "题组诊断.tif" \* MERGEFORMAT INCLUDEPICTURE
" 题 组 诊 断 .tif" \* MERGEFORMAT
[A组 基础知识巩固]
1.(2018·潍坊质检)某温度下,在一个2 L的密闭容器中,加入4 mol X和2 mol Y
进行如下反应:3X(g)+2Y(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT4Z(s)+2W(g),反应一段时间后达到平衡,测得生成1.6 mol Z,则下列说
法正确的是( )
A.该反应的化学平衡常数表达式是K=
B.此时,Y的平衡转化率是40%
C.增大该体系的压强,化学平衡常数增大
D.增加Y,Y的平衡转化率增大
解析 化学平衡常数的表达式中不能出现固体或纯液体物质,而物质Z是固体,A
错误;根据化学方程式可知,平衡时减少的Y的物质的量是1.6 mol×=0.8 mol,
所以Y的转化率为×100%=40%,B正确;平衡常数只与温度有关,增大压强时平
衡常数不变,C错误;增加Y后平衡右移,X的转化率增大,而Y的转化率减小,D
错误。
答案 B
2. 某 温 度 下 , 反 应 H (g) + CO (g) INCLUDEPICTURE "KN.TIF" \*
2 2
MERGEFORMAT H O(g)+CO(g)的平衡常数K=。该温度下,在甲、乙、丙
2
三个恒容密闭容器中,投入H (g)和CO (g),其起始浓度如表所示:
2 2
起始浓度 甲 乙 丙
c(H )/(mol·L-1) 0.010 0.020 0.020
2
c(CO )/(mol·L-1) 0.010 0.010 0.020
2
下列判断不正确的是( )
A.平衡时,乙中CO 的转化率大于60%
2
B.平衡时,甲中和丙中H 的转化率均是60%
2
C.平衡时,丙中c(CO )是甲中的2倍,是0.008 mol·L-1
2
D.反应开始时,乙中的反应速率最快,甲中的反应速率最慢
解析 设甲容器中,平衡时氢气的变化浓度为 x,则:K==,解得x=0.006 0
mol·L-1,平衡时c(H )=c(CO )=0.010-x=0.004 0 mol·L-1,c(H O)=c(CO)=
2 2 2
0.006 0 mol·L-1,α(H )=×100%=60%。因乙中H 的起始浓度大于甲,故乙平衡
2 2
相当于是甲平衡正向移动的结果,乙中CO 的转化率大于60%,A项正确;丙平衡
2
可看作是 2 个甲平衡合并而成的,又因 H (g)+CO (g) INCLUDEPICTURE
2 2"KN.TIF" \* MERGEFORMAT H O(g)+CO(g)是平衡不受压强影响的反
2
应,故丙平衡中物质的转化率不变,仅各物质的浓度是甲平衡中各物质浓度的 2
倍,所以B、C项正确;由于三组反应中丙中各物质的浓度最大,甲中各物质的浓
度最小,所以丙反应速率最快,甲反应速率最慢,D项错误。
答案 D
3.(2018·湖南师大附中摸底)N O 是一种新型硝化剂,一定温度下发生反应
2 5
2N O (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT 4NO (g)+
2 5 2
O (g) ΔH>0,T 温度下的部分实验数据为:
2 1
t/s 0 500 1 000 1 500
c(N O )/(mol·L-1) 5.00 3.52 2.50 2.50
2 5
下列说法不正确的是( )
A.500 s内,N O 的分解速率为2.96×10-3 mol·L-1·s-1
2 5
B.T 温度下的平衡常数为K =125,1 000 s时N O 的转化率为50%
1 1 2 5
C.其他条件不变时,T 温度下反应到1 000 s时测得N O (g)浓度为2.98 mol·L-1,
2 2 5
则有T T ,则有K >K
1 1 2 2 1 2 1 2
解析 500 s 内 c(N O )由 5.00 mol·L-1降低到 3.52 mol·L-1,则有 (N O )==
2 5 v 2 5
2.96×10-3mol·L-1·s-1,A正确。1 000 s时,c(N O )=2.50 mol·L-1,则c(NO )=5
2 5 2
mol·L-1,c(O )=1.25 mol·L-1,此时N O 的转化率为×100%=50%;化学平衡常
2 2 5
数K ===125,B正确。T 温度下反应到1 000 s时测得N O (g)浓度为2.98 mol·L
1 2 2 5
-1>2.50 mol·L-1,说明反应正向进行的程度减小,又反应ΔH>0,故有T >T ,C错
1 2
误。该反应为吸热反应,升高温度,平衡正向移动,平衡常数增大,由于T >T ,则有
1 2
K >K ,D正确。
1 2
答案 C
【规范答题】
化学平衡计算模板
反应:mA(g)+nB(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMATpC(g)+qD(g),令A、B起始物质的量(mol)分别为a、b,达到平衡后,A的消耗量为
mx,容器容积为V L。
对于反应物:n(平)=n(始)-n(变)
对于生成物:n(平)=n(始)+n(变)
则有:(1)平衡常数:K=。
(2)A的平衡浓度:c(A) =mol·L-1。
平
(3)A的转化率:α(A) =×100%。
平
(4)A的体积分数:φ(A)=×100%。
(5)平衡与起始压强之比:=。
(6)混合气体的平均密度:
ρ =g·L-1。
混
(7)平衡时混合气体的平均摩尔质量:
M=g·mol-1。
[B组 考试能力过关]
4.[2017·课标全国Ⅰ,28(3)]近期发现,H S是继NO、CO之后第三个生命体系气体
2
信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列
问题:
H S与CO 在高温下发生反应:H S(g)+CO (g) INCLUDEPICTURE "KN.TIF" \*
2 2 2 2
MERGEFORMAT COS(g) +H O(g)。在610 K时,将0.10 mol CO 与0.40
2 2
mol H S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
2
(1)H S的平衡转化率α =________%,反应平衡常数K=________。
2 1
(2)在 620 K 重复试验,平衡后水的物质的量分数为 0.03,H S 的转化率
2
α ________α ,该反应的ΔH________0。(填“>”“<”或“=”)
2 1
(3)向反应器中再分别充入下列气体,能使H S转化率增大的是________(填标号)。
2
A. H S B. CO
2 2
C.COS D.N
2
解析=0.02,x=0.01。H S的转化率为×100%=2.5%。K==2.8×10-3。
2
(2)水的物质的量分数增大,说明平衡正向移动,H S的转化率增大;温度升高,平
2
衡正向移动,说明正反应是吸热反应。(3)增大H S浓度,平衡正向移动,CO 转化
2 2
率增大,H S转化率降低,A错误;同理,增大CO 浓度,H S转化率增大,CO 转化
2 2 2 2
率降低,B正确;增大COS浓度,平衡向逆反应方向移动,H S转化率降低,C错误;
2
加入不反应的N ,反应物、生成物浓度均不变,平衡不移动,H S转化率不变,D错
2 2
误。
答案 (1)2.5 2.8×10-3 (2)> > (3)B
5.(2018·课标全国Ⅱ,27)CH CO 催化重整不仅可以得到合成气(CO和H ),还对
4 2 2
温室气体的减排具有重要意义。回答下列问题:
(1)CH CO 催化重整反应为:CH (g)+CO (g)===2CO(g)+2H (g)。
4 2 4 2 2
已知:C(s)+2H (g)===CH (g) ΔH=-75 kJ·mol-1
2 4
C(s)+O (g)===CO (g) ΔH=-394 kJ·mol-1
2 2
C(s)+O (g)===CO(g) ΔH=-111 kJ·mol-1
2
该催化重整反应的ΔH=________kJ·mol-1。有利于提高CH 平衡转化率的条件是
4
________(填标号)。
A.高温低压 B.低温高压
C.高温高压 D.低温低压
某温度下,在体积为2 L的容器中加入2 mol CH 、1 mol CO 以及催化剂进行重整
4 2
反应,达到平衡时CO 的转化率是50%,其平衡常数为________ mol2·L-2。
2
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少
相关数据如下表:
积碳反应CH (g)=== C(s) 消碳反应CO (g)
4 2
+2H (g) +C(s) ===2CO(g)
2
ΔH/(kJ·mol-1) 75 172催化
33 91
剂X
活化能(kJ·mol-1)
催化
43 72
剂Y
①由上表判断,催化剂 X________Y(填“优于”或“劣于”),理由是
______________________________________________________________________。
在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温
度的变化关系如图1所示,升高温度时,下列关于积碳反应、消碳反应的平衡常数
(K)和速率( )的叙述正确的是________(填标号)。
v
A.K 、K 均增加
积 消
B. 减小、 增加
v积 v消
C.K 减小、K 增加
积 消
D. 增加的倍数比 增加的倍数大
v消 v积
INCLUDEPICTURE "18GK15.TIF" \* MERGEFORMAT
②在一定温度下,测得某催化剂上沉积碳的生成速率方程为 =k·p(CH )·[p(CO )]
v 4 2
-0.5(k为速率常数)。在p(CH )一定时,不同p(CO )下积碳量随时间的变化趋势如图
4 2
2 所 示 , 则 p (CO ) 、 p (CO ) 、 p (CO ) 从 大 到 小 的 顺 序 为
a 2 b 2 c 2_____________________________________________________________________。
解析 (1)将已知中3个反应依次记为①、②、③,根据盖斯定律③×2-①-②得
该催化重整反应的ΔH=(-111×2+75+394) kJ·mol-1=+247 kJ·mol-1。由于该
反应为吸热且气体体积增大的反应,要提高CH 的平衡转化率,需在高温低压下
4
进行。根据平衡时消耗的CO 为1 mol×50%=0.5 mol,则消耗的CH 为0.5 mol,
2 4
生成的CO和H 均为1 mol,根据三段式法可知平衡时CH 、CO 、CO和H 的平衡
2 4 2 2
浓度分别为0.75 mol·L-1、0.25 mol·L-1、0.5 mol·L-1、0.5 mol·L-1,则平衡常数K=
= mol2·L-2。(2)①从表格中数据可看出相对于催化剂X,用催化剂Y催化时积碳
反应的活化能大,则积碳反应的反应速率小,而消碳反应活化能相对小,则消碳反
应的反应速率大,再根据题干信息“反应中催化剂活性会因积碳反应而降低”可
知催化剂X劣于催化剂Y。结合图示可知500~600 ℃随温度升高积碳量增加,而
600~700 ℃随温度升高积碳量减少,故随温度升高,K 和K 均增加,且消碳反
积 消
应速率增加的倍数比积碳反应的大,故A、D正确。②由该图像可知在反应时间和
p(CH )相同时,图像中速率关系 > > ,结合沉积碳的生成速率方程 =
4 va vb vc v
k·p(CH )·[p(CO )]-0.5,在p(CH )相同时,随着p(CO )增大,反应速率逐渐减慢,即
4 2 4 2
可判断:p (CO )>p (CO )>p (CO )。
c 2 b 2 a 2
答案 (1)247 A
(2)①劣于 相对于催化剂X,催化剂Y积碳反应的活化能大,积碳反应的速率小
而消碳反应活化能相对小,消碳反应速率大 AD ②p (CO )>p (CO )>p (CO )
c 2 b 2 a 2
考点二 化学反应进行的方向
(频数:★☆☆ 难度:★☆☆)
INCLUDEPICTURE "名师课堂.tif" \* MERGEFORMAT INCLUDEPICTURE
" 名 师 课 堂 .tif" \* MERGEFORMAT
INCLUDEPICTURE " 书名号 .TIF " \* MERGEFORMAT INCLUDEPICTURE
" 书名号 .TIF" \* MERGEFORMAT 名师课堂导语 化学反应进行的方向,在高考中很少涉及,复习时没必要拓展强化,只要抓住教材主干知识点进行落实即可。
1.自发过程
(1)含义
在一定条件下,不需要借助外力作用就能自动进行的过程。
(2)特点
①体系趋向于从高能状态转变为低能状态(体系对外部做功或释放热量)。
②在密闭条件下,体系有从有序转变为 无 序 的倾向性(无序体系更加稳定)。
2.化学反应方向
(1)判据
(2)一般规律:
①ΔH<0,ΔS>0的反应任何温度下都能自发进行;
②ΔH>0,ΔS<0的反应任何温度下都不能自发进行;
③ΔH和ΔS的作用相反,且相差不大时,温度对反应的方向起决定性作用。当
ΔH<0,ΔS<0时低温下反应能自发进行;当ΔH>0,ΔS>0时,高温下反应能自发进
行。
INCLUDEPICTURE " 名 师 课 堂 实 录 .tif" \* MERGEFORMATINCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
(1)熵:衡量体系混乱程度的物理量,符号为S,单位为J·mol-1·K-1。
(2)对于一个特定的气相反应,熵变的大小取决于反应前后的气体物质的化学计量
数大小。
(3)复合判据计算时要注意单位换算。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)放热过程均可以自发进行,吸热过程均不能自发进行(×)
(2)CaCO =====CaO+CO ↑是一个熵增的过程(√)
3 2
(3)焓变是影响反应是否具有自发性的唯一因素(×)
(4)ΔH<0、ΔS>0时,反应一定能自发进行(√)
(5)吸热且熵增加的反应,当温度升高时,反应一定能自发进行(×)
(6)-10 ℃的水结成冰,可用熵变的判据来解释反应的自发性(×)
2.(教材改编题)(RJ选修4·P 1改编)下列过程的熵变的判断不正确的是( )
36
A.溶解少量食盐于水中,ΔS>0
B.纯碳和氧气反应生成CO(g),ΔS>0
C.H O(g)变成液态水,ΔS>0
2
D.CaCO (s)加热分解为CaO(s)和CO (g),ΔS>0
3 2
答案 C
3.(思维探究题)能自发进行的反应一定能实际发生吗?
答案 不一定;化学反应方向的判据指出的仅仅是在一定条件下化学反应自发进
行的趋势,并不能说明在该条件下反应一定能实际发生,还要考虑化学反应的快
慢问题。
INCLUDEPICTURE "题组诊断.tif" \* MERGEFORMAT INCLUDEPICTURE
" 题 组 诊 断 .tif" \* MERGEFORMAT
[A组 基础知识巩固]
1.反应2AB(g)===C(g)+3D(g)在高温时能自发进行,反应后体系中物质的总能量
升高,则该反应的ΔH、ΔS应为( )A.ΔH<0,ΔS>0 B.ΔH<0,ΔS<0
C.ΔH>0,ΔS>0 D.ΔH>0,ΔS<0
解析 该反应中气体的物质的量增加,ΔS>0。反应后体系中物质的总能量升高,说
明正反应是吸热反应,ΔH>0。
答案 C
2.(2018·天津河东区调研)下列说法不正确的是( )
A.ΔH<0、ΔS>0的反应在任何温度下都能自发进行
B.NH HCO (s)===NH (g)+H O(g)+CO (g) ΔH=+185.57 kJ·mol-1能自发进行,
4 3 3 2 2
原因是体系有自发地向混乱度增加的方向转变的倾向
C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应
自发性的判据
D.在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的速率
解析 反应的ΔH<0、ΔS>0,则始终存在ΔH-TΔS<0,在任何温度下该反应都能自
发进行,A正确。反应NH HCO (s)===NH (g)+H O(g)+CO (g)的ΔH>0、ΔS>0,则
4 3 3 2 2
高温下存在ΔH-TΔS<0,若该反应能自发进行,说明体系有自发地向混乱度增加
的方向转变的倾向,B正确。ΔH、ΔS都与反应的自发性有关,但要根据ΔH-TΔS
判断反应的自发性,不能将ΔH或ΔS单独作为反应自发性的判据,C错误。在其他
外界条件不变的情况下,使用催化剂可以改变反应的活化能,从而改变反应速率,
D正确。
答案 C
3.(1)汽车燃油不完全燃烧时产生 CO,有人设想按下列反应除去 CO:
2CO(g)===2C(s)+O (g)
2
已 知 该 反 应 的 ΔH>0 , 简 述 该 设 想 能 否 实 现 的 依 据 :
______________________________________________________________________
_____________________________________________________________________
。
(2)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利
用催化技术将尾气中的NO和CO转化成CO 和N ,化学方程式如下:2NO+2CO
2 2
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT 2CO +N 。反应能够
2 2自发进行,则反应的ΔH________0(填“>”“<”或“=”)。
解析 (1)2CO(g)===2C(s)+O (g),该反应是焓增、熵减的反应。根据ΔG=ΔH-
2
TΔS,ΔG>0,不能实现。
(2)该反应为熵减反应,能自发进行说明ΔH<0。
答案 (1)该反应是焓增、熵减的反应,任何温度下均不自发进行 (2)<
【规律总结】
焓变、熵变和温度对化学反应方向的影响
ΔH ΔS ΔH-TΔS 反应情况
- + 永远是负值 在任何温度下过程均自发进行
+ - 永远是正值 在任何温度下过程均非自发进行
+ + 低温为正高温为负 低温时非自发,高温时自发
- - 低温为负高温为正 低温时自发,高温时非自发
[B组 考试能力过关]
4.下列有关说法不正确的是________。
A.(2016·全国甲卷)C H (g)+NH (g)+O (g)===C H N(g)+3H O(g) ΔH=-515
3 6 3 2 3 3 2
kJ·mol-1和C H (g)+O (g)===C H O(g)+H O(g) ΔH=-353 kJ·mol-1两个反应
3 6 2 3 4 2
在热力学上趋势均很大
B.(2015·天津高考)Na与H O的反应是熵增的放热反应,该反应能自发进行
2
C.(2014·天津高考)某吸热反应能自发进行,因此该反应是熵增反应
D.(2014·江苏高考)2NO(g)+2CO(g)===N (g)+2CO (g)在常温下能自发进行,则
2 2
该反应的ΔH>0
E.(2013·江苏高考)反应NH (g)+HCl(g)===NH Cl(s)在室温下可自发进行,则该反
3 4
应的ΔH<0
F.(2012·江苏高考)CaCO (s)===CaO(s)+CO (g)室温下不能自发进行,说明该反应
3 2
的ΔH<0
G.(2011·江苏高考)一定温度下,反应 MgCl (l)===Mg(l)+Cl (g)的ΔH>0、ΔS>0
2 2
答案 DF
INCLUDEPICTURE "分层课时作业.TIF" \* MERGEFORMAT
INCLUDEPICTURE "分层课时作业.TIF" \* MERGEFORMAT[A级 全员必做题]
1.T ℃ 时 可 逆 反 应 mA(g) + nB(s) INCLUDEPICTURE "KN.TIF" \*
MERGEFORMAT pC(g)的平衡常数为K,下列说法中正确的是( )
A.K值越大,表明该反应越有利于C的生成,反应物的转化率越大
B.若缩小反应器的容积,能使平衡正向移动,则K增大
C.K=
D.如果m+n=p,则K=1
解析 对于一个确定的反应来说,K值只与温度有关,K越大,越有利于平衡向右
进行,A正确;温度不变,K值不变,B错误;B是固体,其浓度视为常数,不应出现
在计算式中,C错误;由K的计算表达式知D错误。
答案 A
2.反应CO(g)+2H (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2
CH OH(g) ΔH<0达到平衡后,只改变一个反应条件,下列所画示意图不正确的
3
是( )
INCLUDEPICTURE "10X602.TIF" \* MERGEFORMAT
解析 A项,升温,化学平衡逆向移动,CH OH产率降低,正确;B项,升温,CO的
3
转化率降低,不正确;C项,加压,化学平衡正向移动,H 的转化率升高,正确;D项,
2
增大压强,平衡常数不变,正确。
答案 B
3.为了探究FeCl 溶液和KI溶液的反应是否存在一定的限度,取5 mL 0.5 mol·L-1
3
KI溶液,滴加0.1 mol·L-1 FeCl 溶液5~6滴,充分反应。下列实验操作能验证该
3
反应是否存在限度的是( )A.再滴加AgNO 溶液,观察是否有黄色沉淀产生
3
B.再加入CCl 振荡后,观察下层液体颜色是否变为紫红色
4
C.再加入CCl 振荡后,取上层清液,滴加AgNO 溶液,观察是否有白色沉淀产生
4 3
D.再加入CCl 振荡后,取上层清液,滴加KSCN溶液,观察溶液是否变成血红色
4
解析 FeCl 溶液和KI溶液的反应2Fe3++2I- INCLUDEPICTURE "KN.TIF" \*
3
MERGEFORMAT 2Fe2++I 。A.无论是否存在反应限度滴加AgNO 溶液
2 3
都生成沉淀,错误;B.是否变为紫红色,只能说明是否生成碘,不能确定是否存在
反应限度,错误;C.反应前后溶液中均存在Cl-,错误;D.滴加KSCN可以知道Fe3
+是否反应完,从而确定反应是否有限度,正确。
答案 D
4.(2019·西安市铁一中学质检)O 是一种很好的消毒剂,具有高效、洁净、方便、经
3
济等优点。O 可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀菌消
3
毒能力。常温常压下发生的反应如下:
反应① O INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT O +[O]
3 2
ΔH>0 平衡常数为K ;
1
反应② [O]+O INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT 2O
3 2
ΔH<0 平衡常数为K ;
2
总反应:2O INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT 3O
3 2
ΔH<0 平衡常数为K。
下列叙述正确的是( )
A.降低温度,总反应K减小
B.K=K +K
1 2
C.适当升温,可提高消毒效率
D.压强增大,K 减小
2
解析 降温,总反应平衡向右移动,K增大,A项错误;K =、K =、K==K ·K ,B
1 2 1 2
项错误;升高温度,反应①平衡向右移动,c([O])增大,可提高消毒效率,C项正确;
对于给定的反应,平衡常数只与温度有关,D项错误。答案 C
5.密闭容器中,由H 和CO直接制备二甲醚(CH OCH ),其过程包含以下反应:
2 3 3
i.CO(g) + 2H (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2
CH OH(g) ΔH =-90.1 kJ·mol-1
3 1
ⅱ.2CH OH(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
3
CH OCH (g)+H O(g)
3 3 2
ΔH =-24.5 kJ·mol-1
2
当其他条件相同时,由H 和CO直接制备二甲醚的反应中,CO平衡转化率随条件
2
X的变化曲线如图所示。下列说法中正确的是( )
INCLUDEPICTURE "10X603.TIF" \* MERGEFORMAT
A.由H 和CO直接制备二甲醚的反应为放热反应
2
B.条件X为压强
C.X增大,二甲醚的产率一定增大
D.X增大,该反应的平衡常数一定减小
解析 根据盖斯定律,将ⅰ×2+ⅱ得:2CO(g)+4H (g) INCLUDEPICTURE
2
"KN.TIF" \* MERGEFORMAT CH OCH (g) + H O(g) ΔH = - 204.7
3 3 2
kJ·mol-1,因此由H 和CO直接制备二甲醚的反应为放热反应,A项正确;若X表
2
示压强,根据2CO(g)+4H (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2
CH OCH (g)+H O(g)可知,压强越大,CO的平衡转化率越大,与图像不符,
3 3 2
B项错误;根据图像可知,X可能是温度,温度升高,平衡逆向移动,CO的平衡转
化率减小,二甲醚的产率减小,C项错误;根据图像可知,X可能是CO的浓度,增
大CO的浓度,CO的平衡转化率减小,但平衡常数不变,D项错误。
答案 A6.甲、乙两个密闭容器中均发生反应:C(s)+2H O(g) INCLUDEPICTURE
2
"KN.TIF" \* MERGEFORMAT CO (g)+2H (g) ΔH>0,有关实验数据如
2 2
下表所示:
起始量/mol 平衡量/mol
达到平衡所
容器 容积/L 温度/℃ 平衡常数
需时间/min
C(s) H O(g) H (g)
2 2
甲 2 T 2 4 3.2 3.5 K
1 1
乙 1 T 1 2 1.2 3 K
2 2
下列说法正确的是( )
A.T 2n(H ) ,因为该反应
1 2 2 甲 2 乙 2 甲 2 乙
为吸热反应,升高温度有利于平衡正向移动,说明T >T ,A项错误;乙容器中反应
1 2
达平衡时,c(H O)=0.8 mol·L-1、c(CO )=0.6 mol·L-1、c(H )=1.2 mol·L-1,K ==
2 2 2 2
=1.35,B项正确;容器容积不变,碳为固体,正反应方向气体的质量增大,因此反
应正向进行时混合气体的密度增大,C项错误;乙容器中,3 min内H O减少了1.2
2
mol,而前1.5 min内反应速率大于后1.5 min内反应速率,故前1.5 min内H O的
2
物质的量减小的快,反应进行到1.5 min时,n(H O)<1.4 mol,D项错误。
2
答案 B
7.(2018·山东烟台自主练习,7)已知NO和O 经反应①和反应②转化为NO ,其能
2 2
量变化随反应过程的图示如下。
INCLUDEPICTURE "10X604.TIF" \* MERGEFORMAT
①2NO(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT N O (g)
2 2ΔH ,平衡常数K
1 1
②N O (g) + O (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2 2 2
2NO (g) ΔH ,平衡常数K
2 2 2
下列说法中不正确的是( )
A.ΔH <0,ΔH <0
1 2
B.2NO(g) + O (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2
2NO (g)的平衡常数K=K /K
2 1 2
C. 表 示 2NO(g) + O (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2
2NO (g)的ΔH=ΔH +ΔH
2 1 2
D.反应②的速率大小决定 2NO(g)+O (g) INCLUDEPICTURE "KN.TIF" \*
2
MERGEFORMAT 2NO (g)的反应速率
2
解析 由题图可知反应①和反应②的反应物总能量高于生成物总能量,所以
ΔH <0,ΔH <0,A项正确;反应①+反应②得2NO(g)+O (g) INCLUDEPICTURE
1 2 2
"KN.TIF" \* MERGEFORMAT 2NO (g),所以K=K ×K ,B项错误;反应
2 1 2
①+反应②得 2NO(g)+O (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2
2NO (g),所以ΔH=ΔH +ΔH ,C项正确;反应速率主要取决于慢反应的
2 1 2
反应速率,反应②的活化能大于反应①,所以反应②的反应速率小于反应①,故反
应 ② 的 速 率 大 小 决 定 2NO(g) + O (g) INCLUDEPICTURE "KN.TIF" \*
2
MERGEFORMAT 2NO (g)的反应速率,D项正确。
2
答案 B
8.恒温、恒压下,将1 mol O 和2 mol SO 气体充入一体积可变的容器中(状态Ⅰ),
2 2
发生反应 2SO (g) +O (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2 2
2SO (g),状态Ⅱ时达平衡,则O 的转化率为( )
3 2A.60% B.40%
C.80% D.90%
解析 恒温、恒压下,气体的体积比等于物质的量之比。设O 的转化率为x。
2
有(2-2x)+(1-x)+2x=3×,解得x=0.6。
答案 A
9.(2017·福建宁德质检)在300 mL的密闭容器中,放入镍粉并充入一定量的CO气
体,一定条件下发生反应:Ni(s)+4CO(g) INCLUDEPICTURE "KN.TIF" \*
MERGEFORMAT Ni(CO) (g),已知该反应平衡常数与温度的关系如下表。
4
温度/℃ 25 80 230
平衡常数 5×104 2 1.9×10-5
下列说法正确的是( )
A.上述生成Ni(CO) (g)的反应为吸热反应
4
B.25 ℃时反应 Ni(CO) (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
4
Ni(s)+4CO(g)的平衡常数为0.5
C.在某条件下达到平衡,测得Ni(CO) 、CO浓度均为0.5 mol·L-1,则此时温度高于
4
80 ℃
D.80 ℃达到平衡时,保持体积不变,往体系中充入少量的Ni(CO) ,再次达到平衡
4
后CO的体积分数减小
解析 A项,化学平衡常数只受温度的影响,根据表格中数据,随着温度的升高,
平衡常数减小,因此正反应是放热反应,故错误;B 项,Ni(s)+4CO(g)
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT Ni(CO) (g),化学平衡
4
常 数 的 表 达 式 为 K = , Ni(CO) (g) INCLUDEPICTURE "KN.TIF" \*
1 4
MERGEFORMAT Ni(s)+4CO(g),化学平衡常数的表达式为K =,K ==
2 2=2×10-5,故错误;C项,化学平衡常数为=8>2,因此温度低于80 ℃,故错误;D
项,相当于增大压强,平衡向正反应方向移动,达到平衡后CO的体积分数减小,
故D正确。
答案 D
10.(2018·张家口期末)TiO 和TiCl 均为重要的工业原料。已知:
2 4
Ⅰ.TiCl (g)+O (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
4 2
TiO (s)+2Cl (g)
2 2
ΔH =-175.4 kJ·mol-1
1
Ⅱ.2C(s) + O (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2
2CO(g) ΔH =-220.9 kJ·mol-1
2
请回答下列问题:
(1)TiCl (g) 与 CO(g) 反 应 生 成 TiO (s) 、 C(s) 和 氯 气 的 热 化 学 方 程 式 为
4 2
_____________________________________________________________________。
升 高 温 度 , 对 该 反 应 的 影 响 为
_____________________________________________。
(2)若反应Ⅱ的逆反应活化能表示为 E kJ·mol-1,则E________220.9(填“>”“<”或
“=”)。
(3)t ℃时,向10 L恒容密闭容器中充入1 mol TiCl 和2 mol O ,发生反应Ⅰ。5 min
4 2
达到平衡时测得TiO 的物质的量为0.2 mol。
2
①0~5 min内,用Cl 表示的反应速率 (Cl )=________。
2 v 2
②TiCl 的平衡转化率α=________。
4
③下列措施,既能加快逆反应速率又能增大TiCl 的平衡转化率的是________(填
4
选项字母)。
A.缩小容器容积 B.加入催化剂
C.分离出部分TiO D.增大O 浓度
2 2
④t ℃时,向10 L恒容密闭容器中充入3 mol TiCl 和一定量O 的混合气体,发生
4 2
反应Ⅰ,两种气体的平衡转化率(α)与起始的物质的量之比的关系如图所示:INCLUDEPICTURE "P337.TIF" \* MERGEFORMAT
能表示 TiCl 平衡转化率的曲线为________(填“L ”或“L ”);M 点的坐标为
4 1 2
________。
解 析 (1) 已 知 : Ⅰ .TiCl (g) + O (g) INCLUDEPICTURE "KN.TIF" \*
4 2
MERGEFORMAT TiO (s)+2Cl (g)
2 2
ΔH =-175.4 kJ·mol-1
1
Ⅱ.2C(s) + O (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2
2CO(g) ΔH =-220.9 kJ·mol-1,用Ⅰ-Ⅱ,TiCl (g)+2CO(g)===TiO (s)+2Cl (g)
2 4 2 2
+2C(s) ΔH=-175.4 kJ·mol-1-(-220.9 kJ·mol-1)=+45.5 kJ·mol-1;升高温度
反应速率加快,平衡正向移动,反应物的转化率增大;
(2)若反应Ⅱ的逆反应活化能表示为E,正反应是放热反应,则E>220.9 kJ·mol-1;
(3)①0~5 min内,用Cl 表示的反应速率 (Cl )=2 (TiCl )=2×0.2 mol/(10 L×5
2 v 2 v 4
min)=0.008 mol·L-1·min-1;② TiCl 的平衡转化率 α=0.2 mol/1 mol×100%=
4
20%;③A.缩小容器容积,反应速率加快,平衡不移动,故A错误;B.加入催化剂平
衡不移动,故B错误;C.分离出部分TiO 速率变慢,故C错误;D.增大O 浓度既能
2 2
加快逆反应速率又能增大TiCl 的平衡转化率,故D正确;故选D。④随TiCl 浓度
4 4
的增加,TiCl 转化率越来越小,能表示TiCl 平衡转化率的曲线为L ;M点表示
4 4 2
n(TiCl )/n(O )=方程式的计量数比=1时,TiCl 的转化率与O 的转化率相同,即a
4 2 4 2
=1;由t ℃时,向10 L恒容密闭容器中充入1 mol TiCl 和2 mol O ,发生反应Ⅰ。
4 2
5 min达到平衡时测得TiO 的物质的量为0.2 mol。平衡时四种物质的浓度分别为
2
0.08 mol·L-1 TiCl 、0.18 mol·L-1O ,0.04 mol·L-1 Cl ,平衡常数K==;t ℃时,向
4 2 2
10 L恒容密闭容器中充入3 mol TiCl 和3 mol O 的混合气体时,n(TiCl )/n(O )=
4 2 4 2
方程式的计量数比,M点两物质的转化率相等,设转化率为x,则平衡时四种物质的浓度分别为:0.3(1-x)mol·L-1TiCl 、0.3(1-x)mol·L-1O ,0.6 x mol·L-1Cl ,温度
4 2 2
不变,平衡常数不变,=,解得x=1/7。
答案 (1)TiCl (g)+2CO(g)===TiO (s)+2Cl (g)+2C(s) ΔH=+45.5 kJ·mol-1
4 2 2
反应速率加快,平衡正向移动,反应物的转化率增大 (2)>
(3)①0.008 mol·L-1·min-1 ②20% ③D ④L
2
[B级 拔高选做题]
11.T ℃ 时 , 在 一 容 积 为 2 L 的 密 闭 容 器 中 发 生 反 应 : C(s) + 2NO(g)
1
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT N (g)+CO (g)。向密闭
2 2
容器中加入NO和足量的活性炭,反应进行到不同时间时测得各物质的物质的量
如下:
时间 0 min 10 min 20 min 30 min 40 min 50 min
n(NO)/mol 3.0 1.6 1.0 1.0 a a
n(N )/mol 0 0.7 1.0 1.0 1.2 1.2
2
n(CO )/mol 0 0.7 1.0 1.0 0.3 0.3
2
结合表中数据判断,下列说法正确的是( )
A.30 min时改变的条件一定是充入氮气
B.在10~20 min内, (CO )=0.03 mol·L-1·min-1
v 2
C.若升温至T ℃时,该反应的平衡常数K=0.062 5,则ΔH>0
2
D.容器中混合气体的密度保持不变,标志着该反应达到化学平衡状态
解析 A项,根据题意知,T ℃时平衡常数K==1,可得=1,a=0.6,则30 min时
1
改变条件导致平衡右移,且CO 的量减小,因此30 min时改变的条件是减小二氧
2
化碳的量,错误;B项,在10~20 min内, (CO )=
v 2
0.015 mol·L-1·min-1,错误;C项,T ℃时,K=1,若升温至T ℃时,反应的平衡常
1 2
数K=0.062 5,K减小,则升温使平衡左移,说明逆反应为吸热反应,则ΔH<0,错
误;D项,由题意可知,反应前后容器中气体体积不变,反应前后气体质量发生变
化,因此容器中混合气体的密度保持不变时,可以说明反应已达到化学平衡状态,正确。
答案 D
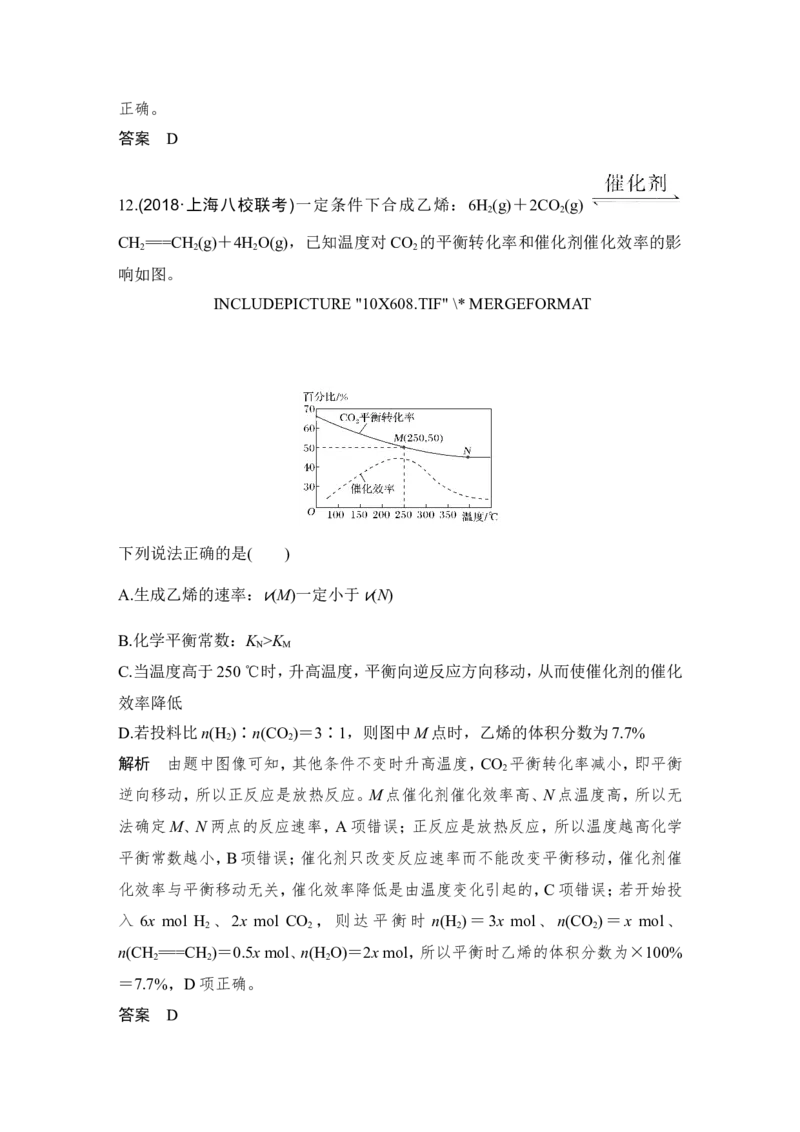
12.(2018·上海八校联考)一定条件下合成乙烯:6H (g)+2CO (g)
2 2
CH ===CH (g)+4H O(g),已知温度对CO 的平衡转化率和催化剂催化效率的影
2 2 2 2
响如图。
INCLUDEPICTURE "10X608.TIF" \* MERGEFORMAT
下列说法正确的是( )
A.生成乙烯的速率: (M)一定小于 (N)
v v
B.化学平衡常数:K >K
N M
C.当温度高于250 ℃时,升高温度,平衡向逆反应方向移动,从而使催化剂的催化
效率降低
D.若投料比n(H )∶n(CO )=3∶1,则图中M点时,乙烯的体积分数为7.7%
2 2
解析 由题中图像可知,其他条件不变时升高温度,CO 平衡转化率减小,即平衡
2
逆向移动,所以正反应是放热反应。M点催化剂催化效率高、N点温度高,所以无
法确定M、N两点的反应速率,A项错误;正反应是放热反应,所以温度越高化学
平衡常数越小,B项错误;催化剂只改变反应速率而不能改变平衡移动,催化剂催
化效率与平衡移动无关,催化效率降低是由温度变化引起的,C项错误;若开始投
入 6x mol H 、2x mol CO ,则达平衡时 n(H )=3x mol、n(CO )=x mol、
2 2 2 2
n(CH ===CH )=0.5x mol、n(H O)=2x mol,所以平衡时乙烯的体积分数为×100%
2 2 2
=7.7%,D项正确。
答案 D13.煤炭是重要的化工原料,但属于不可再生能源,高效、清洁地利用煤炭资源至关
重要。请回答下列问题:
(1)煤的干馏。煤的干馏反应中ΔS________0(填“>”“<”或“=”)。
(2) 煤 的 液 化 。 原 理 是 C(s) + H O(g) INCLUDEPICTURE "KN.TIF" \*
2
MERGEFORMAT CO(g)+H (g) ΔH=a kJ·mol-1;CO(g)+2H (g)
2 2
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT CH OH(l) ΔH=b
3
kJ·mol - 1 。 则 反 应 C(s) + H O(g) + H (g) INCLUDEPICTURE "KN.TIF" \*
2 2
MERGEFORMAT CH OH(l)的ΔH=________kJ·mol-1。
3
(3) 煤 的 气 化 。 原 理 是 C(s) + 2H (g) INCLUDEPICTURE "KN.TIF" \*
2
MERGEFORMAT CH (g) ΔH。
4
在1 L密闭容器中投入1 mol碳,并充入2 mol H ,测得相关数据如图所示。
2
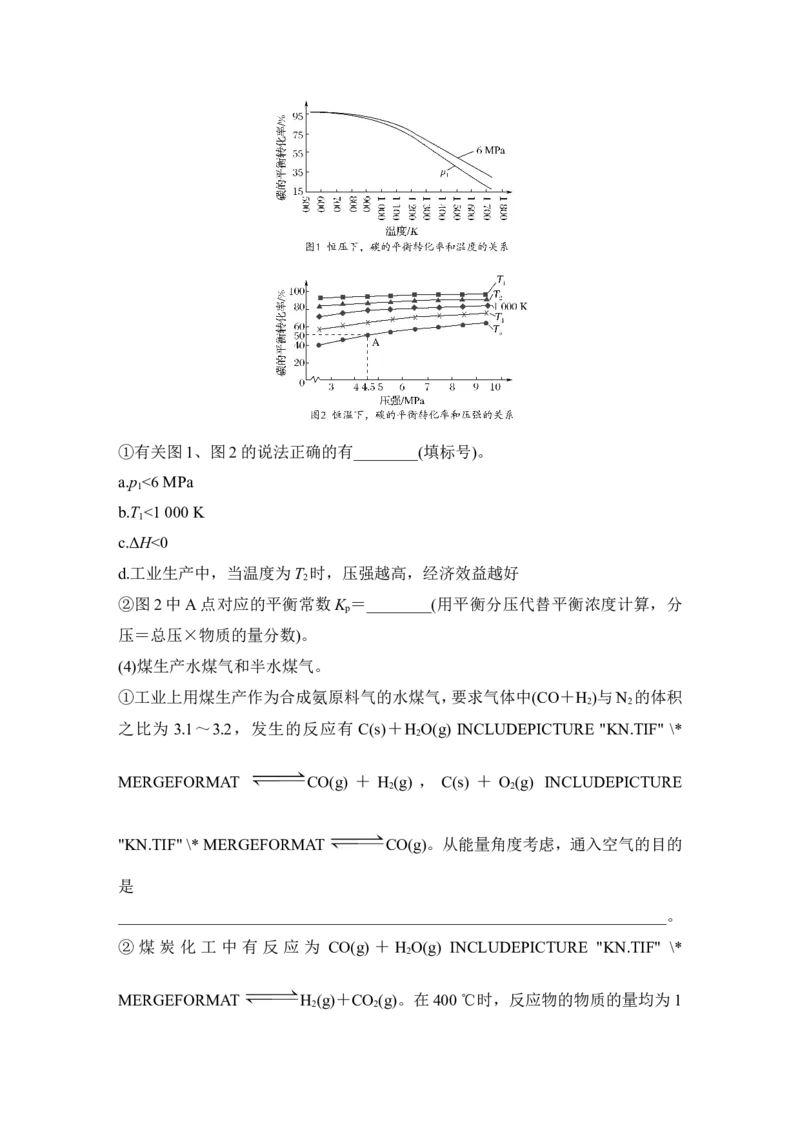
INCLUDEPICTURE "10X609.TIF" \* MERGEFORMAT①有关图1、图2的说法正确的有________(填标号)。
a.p <6 MPa
1
b.T <1 000 K
1
c.ΔH<0
d.工业生产中,当温度为T 时,压强越高,经济效益越好
2
②图2中A点对应的平衡常数K =________(用平衡分压代替平衡浓度计算,分
p
压=总压×物质的量分数)。
(4)煤生产水煤气和半水煤气。
①工业上用煤生产作为合成氨原料气的水煤气,要求气体中(CO+H )与N 的体积
2 2
之比为 3.1~3.2,发生的反应有 C(s)+H O(g) INCLUDEPICTURE "KN.TIF" \*
2
MERGEFORMAT CO(g) + H (g) , C(s) + O (g) INCLUDEPICTURE
2 2
"KN.TIF" \* MERGEFORMAT CO(g)。从能量角度考虑,通入空气的目的
是
____________________________________________________________________。
② 煤 炭 化 工 中 有 反 应 为 CO(g) + H O(g) INCLUDEPICTURE "KN.TIF" \*
2
MERGEFORMAT H (g)+CO (g)。在400 ℃时,反应物的物质的量均为1
2 2mol,在绝热恒容条件下开始反应,下列不能说明反应达到平衡状态的有
________(填标号)。
a.体系的压强不再发生变化
b.混合气体的密度不变
c.混合气体的平均相对分子质量不变
d.各组分的物质的量浓度不再改变
e.体系的温度不再发生变化
f. (CO)= (H O)
v正 v逆 2
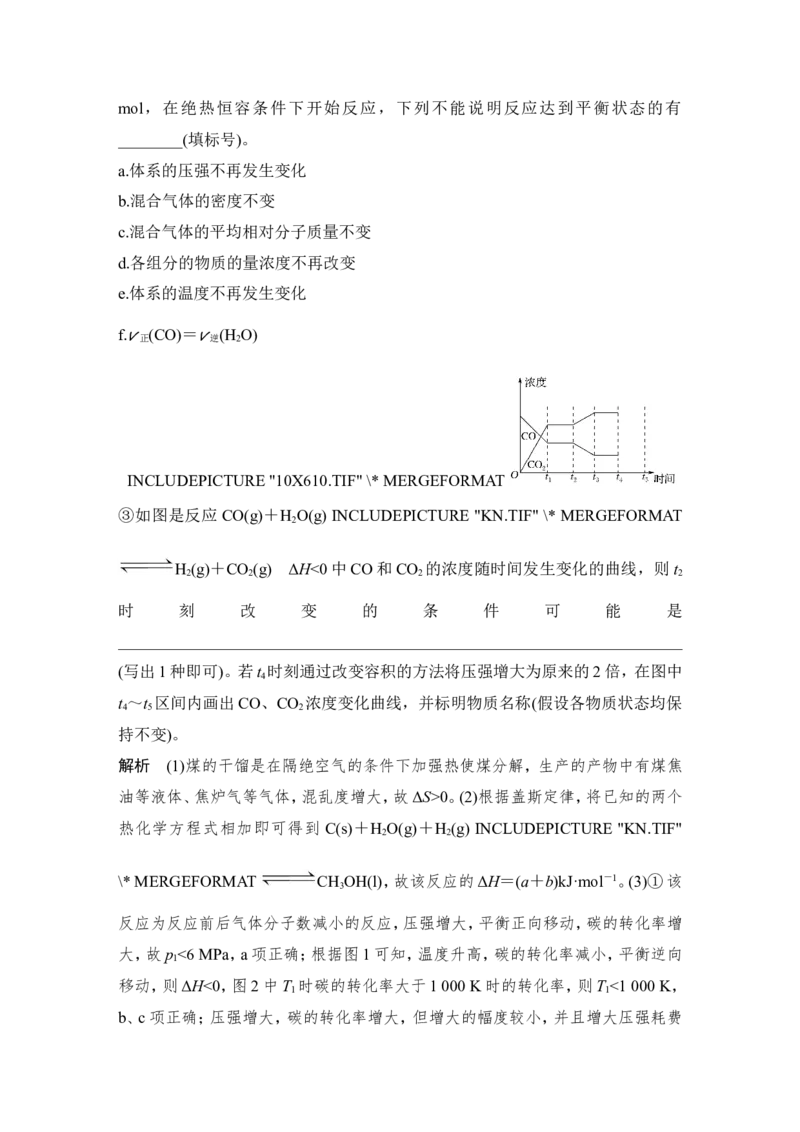
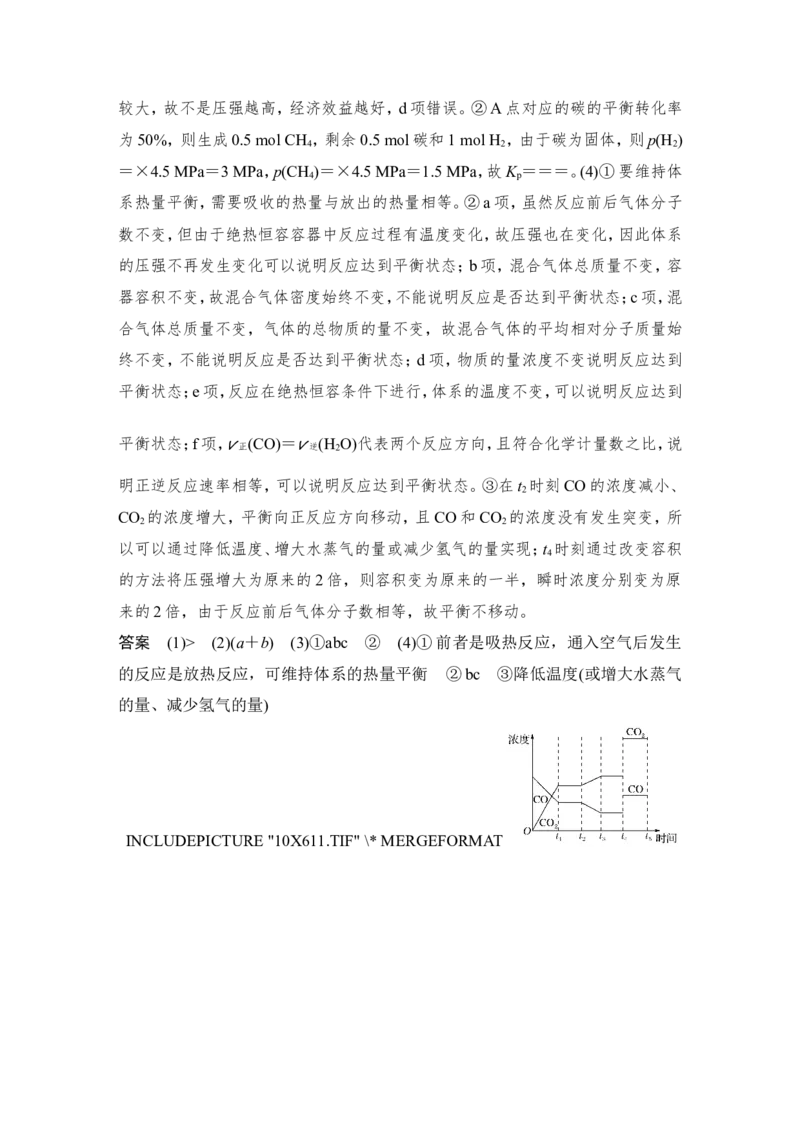
INCLUDEPICTURE "10X610.TIF" \* MERGEFORMAT
③如图是反应 CO(g)+H O(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2
H (g)+CO (g) ΔH<0中CO和CO 的浓度随时间发生变化的曲线,则t
2 2 2 2
时 刻 改 变 的 条 件 可 能 是
______________________________________________________________________
(写出1种即可)。若t 时刻通过改变容积的方法将压强增大为原来的2倍,在图中
4
t ~t 区间内画出CO、CO 浓度变化曲线,并标明物质名称(假设各物质状态均保
4 5 2
持不变)。
解析 (1)煤的干馏是在隔绝空气的条件下加强热使煤分解,生产的产物中有煤焦
油等液体、焦炉气等气体,混乱度增大,故ΔS>0。(2)根据盖斯定律,将已知的两个
热化学方程式相加即可得到 C(s)+H O(g)+H (g) INCLUDEPICTURE "KN.TIF"
2 2
\* MERGEFORMAT CH OH(l),故该反应的ΔH=(a+b)kJ·mol-1。(3)①该
3
反应为反应前后气体分子数减小的反应,压强增大,平衡正向移动,碳的转化率增
大,故p <6 MPa,a项正确;根据图1可知,温度升高,碳的转化率减小,平衡逆向
1
移动,则ΔH<0,图2中T 时碳的转化率大于1 000 K时的转化率,则T <1 000 K,
1 1
b、c项正确;压强增大,碳的转化率增大,但增大的幅度较小,并且增大压强耗费较大,故不是压强越高,经济效益越好,d项错误。②A点对应的碳的平衡转化率
为50%,则生成0.5 mol CH ,剩余0.5 mol碳和1 mol H ,由于碳为固体,则p(H )
4 2 2
=×4.5 MPa=3 MPa,p(CH )=×4.5 MPa=1.5 MPa,故K ===。(4)①要维持体
4 p
系热量平衡,需要吸收的热量与放出的热量相等。②a项,虽然反应前后气体分子
数不变,但由于绝热恒容容器中反应过程有温度变化,故压强也在变化,因此体系
的压强不再发生变化可以说明反应达到平衡状态;b项,混合气体总质量不变,容
器容积不变,故混合气体密度始终不变,不能说明反应是否达到平衡状态;c项,混
合气体总质量不变,气体的总物质的量不变,故混合气体的平均相对分子质量始
终不变,不能说明反应是否达到平衡状态;d项,物质的量浓度不变说明反应达到
平衡状态;e项,反应在绝热恒容条件下进行,体系的温度不变,可以说明反应达到
平衡状态;f项, (CO)= (H O)代表两个反应方向,且符合化学计量数之比,说
v正 v逆 2
明正逆反应速率相等,可以说明反应达到平衡状态。③在t 时刻CO的浓度减小、
2
CO 的浓度增大,平衡向正反应方向移动,且CO和CO 的浓度没有发生突变,所
2 2
以可以通过降低温度、增大水蒸气的量或减少氢气的量实现;t 时刻通过改变容积
4
的方法将压强增大为原来的2倍,则容积变为原来的一半,瞬时浓度分别变为原
来的2倍,由于反应前后气体分子数相等,故平衡不移动。
答案 (1)> (2)(a+b) (3)①abc ② (4)①前者是吸热反应,通入空气后发生
的反应是放热反应,可维持体系的热量平衡 ②bc ③降低温度(或增大水蒸气
的量、减少氢气的量)
INCLUDEPICTURE "10X611.TIF" \* MERGEFORMAT