文档内容
第四章 非金属及其化合物
能力提升检测卷
时间:90分钟 分值:100分
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2022·江苏南通·模拟预测)下列有关物质的性质与用途具有对应关系的是
A.晶体Si熔点高,可用作计算机芯片
B.NH HCO 受热易分解,可用作氮肥
4 3
C.SO 具有还原性,可用于漂白纸浆
2
D.Al(OH) 能与酸反应,可用作抗胃酸药
3
2.(2022·上海静安·二模)关于化工生产,下列说法错误的是
A.工业常用电解饱和食盐水的方法来制取氯气
B.硫酸工业在常压下用SO 与O 反应制取SO
2 2 3
C.联合制碱法、氨碱法所需的CO 都来自石灰石的分解
2
D.通常以海带、紫菜等为原料提取碘
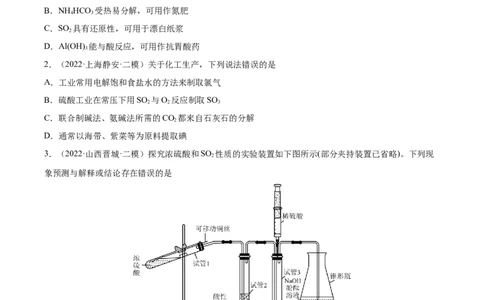
3.(2022·山西晋城·二模)探究浓硫酸和SO 性质的实验装置如下图所示(部分夹持装置已省略)。下列现
2
象预测与解释或结论存在错误的是
选
仪器 现象预测 解释或结论
项
冷却后,把液体倒入水中,溶液为蓝
A 试管1 铜被氧化,转化为Cu2+
色
B 试管2 紫红色溶液由深变浅,直至褪色 SO 具有还原性
2
C 试管3 注入稀硫酸后,出现黄色浑浊 SO 具有氧化性
2D 锥形瓶 溶液红色变浅 NaOH溶液完全转化为NaHSO 溶液
3
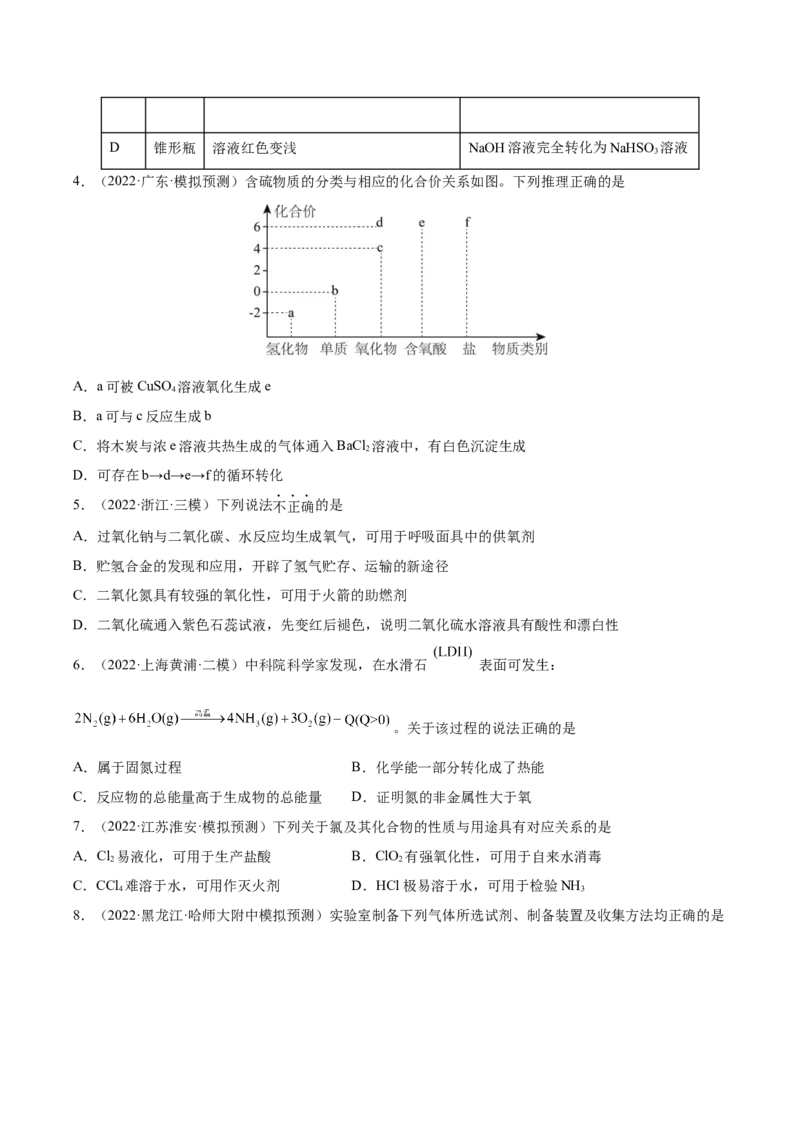
4.(2022·广东·模拟预测)含硫物质的分类与相应的化合价关系如图。下列推理正确的是
A.a可被CuSO 溶液氧化生成e
4
B.a可与c反应生成b
C.将木炭与浓e溶液共热生成的气体通入BaCl 溶液中,有白色沉淀生成
2
D.可存在b→d→e→f的循环转化
5.(2022·浙江·三模)下列说法不正确的是
A.过氧化钠与二氧化碳、水反应均生成氧气,可用于呼吸面具中的供氧剂
B.贮氢合金的发现和应用,开辟了氢气贮存、运输的新途径
C.二氧化氮具有较强的氧化性,可用于火箭的助燃剂
D.二氧化硫通入紫色石蕊试液,先变红后褪色,说明二氧化硫水溶液具有酸性和漂白性
6.(2022·上海黄浦·二模)中科院科学家发现,在水滑石 表面可发生:
。关于该过程的说法正确的是
A.属于固氮过程 B.化学能一部分转化成了热能
C.反应物的总能量高于生成物的总能量 D.证明氮的非金属性大于氧
7.(2022·江苏淮安·模拟预测)下列关于氯及其化合物的性质与用途具有对应关系的是
A.Cl 易液化,可用于生产盐酸 B.ClO 有强氧化性,可用于自来水消毒
2 2
C.CCl 难溶于水,可用作灭火剂 D.HCl极易溶于水,可用于检验NH
4 3
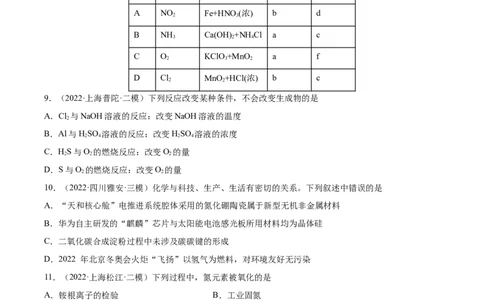
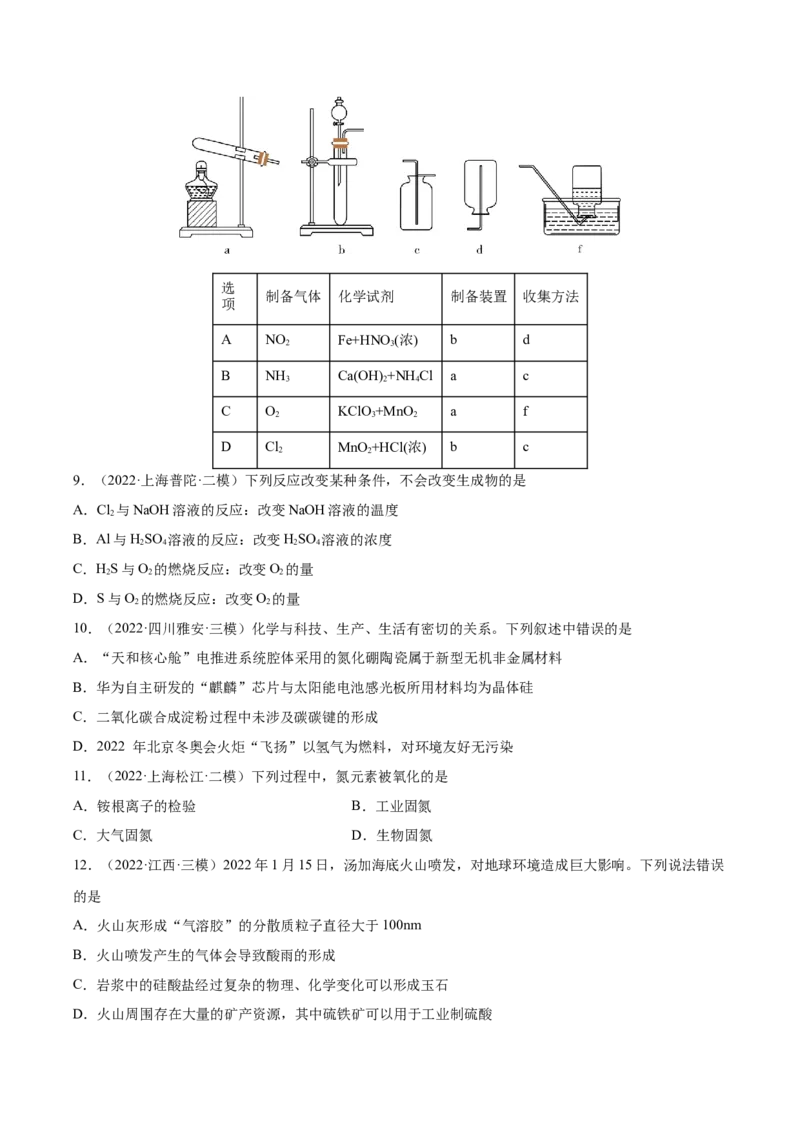
8.(2022·黑龙江·哈师大附中模拟预测)实验室制备下列气体所选试剂、制备装置及收集方法均正确的是选
制备气体 化学试剂 制备装置 收集方法
项
A NO Fe+HNO (浓) b d
2 3
B NH Ca(OH) +NHCl a c
3 2 4
C O KClO+MnO a f
2 3 2
D Cl MnO +HCl(浓) b c
2 2
9.(2022·上海普陀·二模)下列反应改变某种条件,不会改变生成物的是
A.Cl 与NaOH溶液的反应:改变NaOH溶液的温度
2
B.Al与HSO 溶液的反应:改变HSO 溶液的浓度
2 4 2 4
C.HS与O 的燃烧反应:改变O 的量
2 2 2
D.S与O 的燃烧反应:改变O 的量
2 2
10.(2022·四川雅安·三模)化学与科技、生产、生活有密切的关系。下列叙述中错误的是
A.“天和核心舱”电推进系统腔体采用的氮化硼陶瓷属于新型无机非金属材料
B.华为自主研发的“麒麟”芯片与太阳能电池感光板所用材料均为晶体硅
C.二氧化碳合成淀粉过程中未涉及碳碳键的形成
D.2022 年北京冬奥会火炬“飞扬”以氢气为燃料,对环境友好无污染
11.(2022·上海松江·二模)下列过程中,氮元素被氧化的是
A.铵根离子的检验 B.工业固氮
C.大气固氮 D.生物固氮
12.(2022·江西·三模)2022年1月15日,汤加海底火山喷发,对地球环境造成巨大影响。下列说法错误
的是
A.火山灰形成“气溶胶”的分散质粒子直径大于100nm
B.火山喷发产生的气体会导致酸雨的形成
C.岩浆中的硅酸盐经过复杂的物理、化学变化可以形成玉石
D.火山周围存在大量的矿产资源,其中硫铁矿可以用于工业制硫酸13.(2022·上海上海·模拟预测)将碳与浓硫酸反应产生的气体分别通入下列溶液后,所得溶液一定澄清
的是
A.品红溶液 B.石灰水 C.氢硫酸 D.硝酸钡溶液
14.(2022·广东·铁一中学三模)关于化合物ClONO 的性质,下列推测不合理的是
2
A.水解生成盐酸和硝酸 B.与盐酸作用能产生氯气
C.与NaOH溶液反应可生成两种钠盐 D.具有强氧化性
15.(2012·上海·高三零模)有如下转化关系(其他产物及反应所需条件均已略去)。
以下推断错误的是( )
A.当X是盐酸时,则F是稀硝酸
B.当X是氢氧化钠时,则F可能是稀硝酸
C.当X是氢氧化钠时,B跟Cl 反应可能有白烟现象
2
D.当X是氢氧化钠时,B有可能使酸性高锰酸钾溶液褪色
16.(2020·河南信阳·一模)60 mL NO 和 O 的混合气体通入到倒立在水槽中盛满水的玻璃筒(带刻度)中,
2 2
充分反应后,筒内剩余 10 mL 气体,则原混合气体中的 NO 与 O 的体积比可能为
2 2
A.3:1 B.6:1 C.9:1 D.12:1
二、主观题(共5小题,共52分)
17.(2022·上海崇明·二模)(6分)Cl、SO 、NO 都是化工生产中的重要气体,均可用氨水或NaOH溶
2 2 x
液处理,防止污染空气。请回答下列问题:
(1)化工厂可用浓氨水来检验Cl 是否泄漏(已知3Cl+8NH→6NH Cl+N ),当有少量Cl 泄漏时,可以观察到
2 2 3 4 2 2
的现象是_______,若反应中有0.08mol的氨气被氧化,则有_______mo1电子发生转移。
(2)①若用热烧碱溶液吸收Cl 气反应后的混合溶液中,含NaCl、NaClO和NaClO 物质的量比值为n:1:
2 3
1,则n=_______。
②SO 是形成酸雨的主要原因,取某化工区空气样本用蒸馏水处理,检测所得溶液,所含离子及其浓度如
2
下:
离子 Na+ K+ H+ Cl-
NH SO NO
浓度/(mol·L-1) 6×10-6 4×10-6 2×10-5 a 4×10-5 2×10-5 3×10-5
根据表中数据计算,检测的溶液pH=_______。
(3)NO 是燃油汽车尾气中的主要污染物之一。
2
①在催化剂和加热条件下,NO 与NH 可反应生成无害物质,请写出反应的化学方程式:_______。
2 3②实验室可用烧碱溶液吸收NO 和NO,(已知2NO +2NaOH→NaNO+NaNO +H O,
2 2 2 3 2
NO +NO+2NaOH→2NaNO +H O),当消耗100mL0.5mo1L-1的烧碱溶液时,共吸收混合气体_______L(标
2 2 2
准状态)。 ⋅
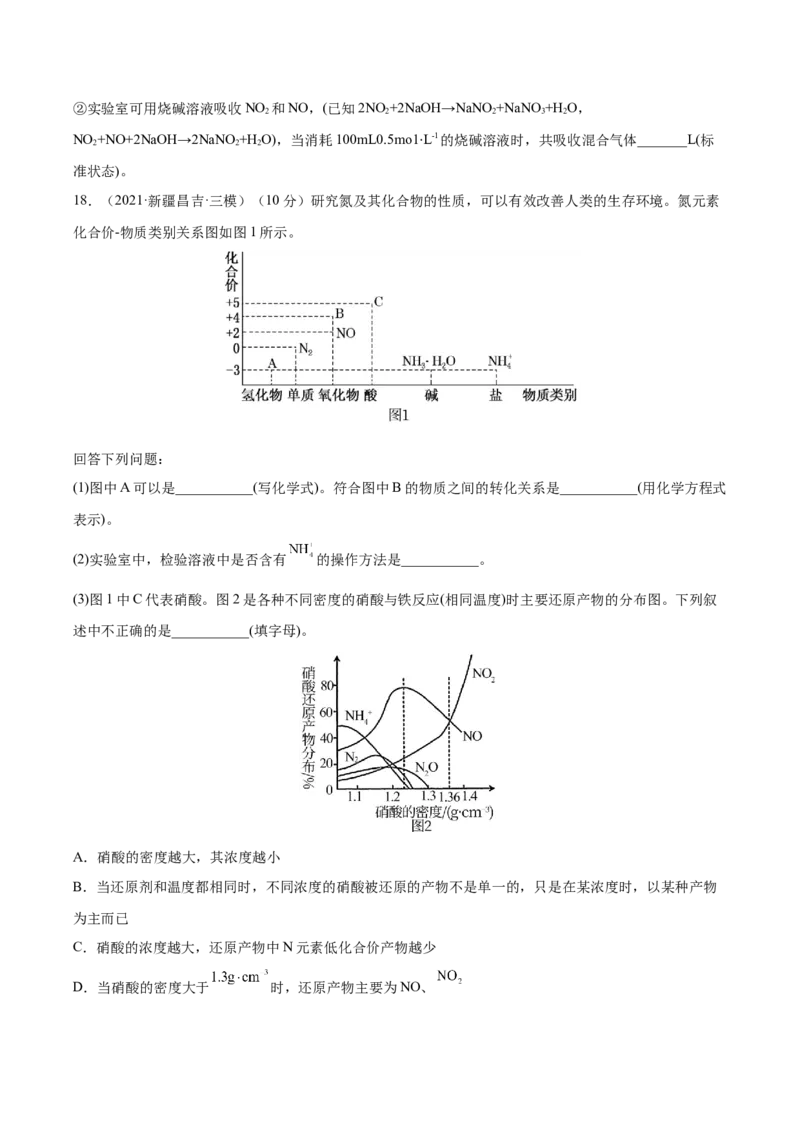
18.(2021·新疆昌吉·三模)(10分)研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素
化合价-物质类别关系图如图1所示。
回答下列问题:
(1)图中A可以是___________(写化学式)。符合图中B的物质之间的转化关系是___________(用化学方程式
表示)。
(2)实验室中,检验溶液中是否含有 的操作方法是___________。
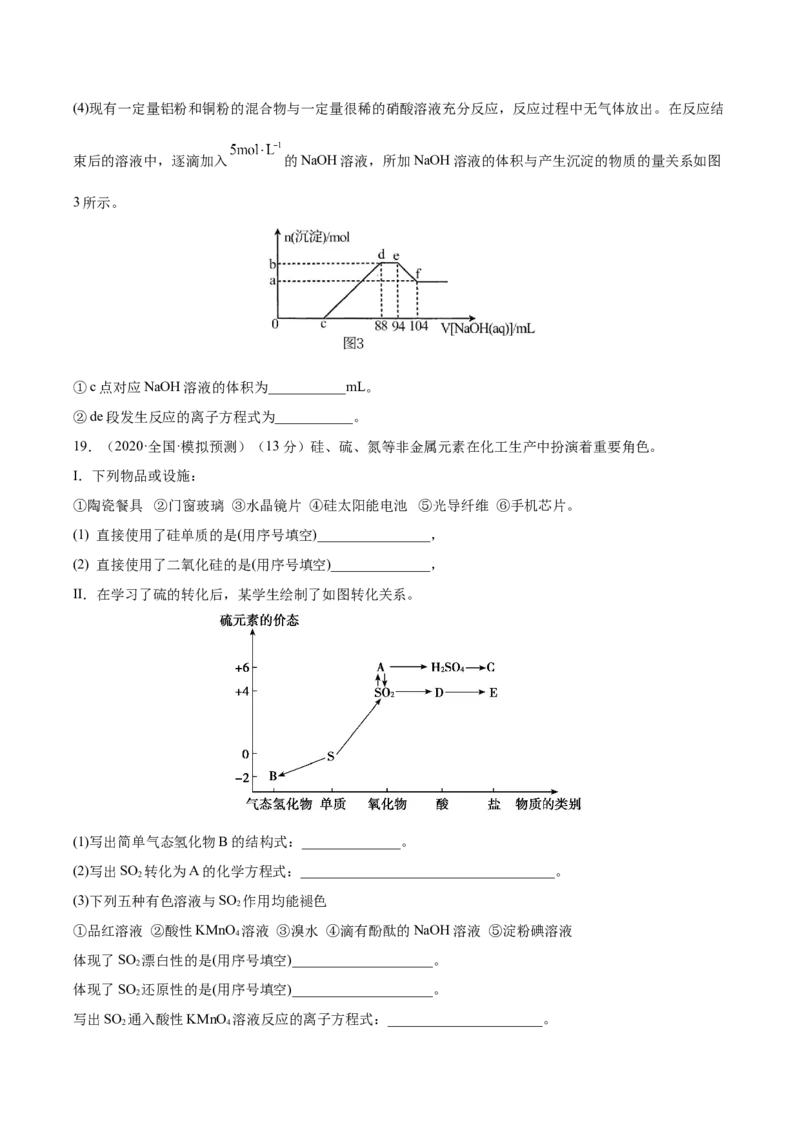
(3)图1中C代表硝酸。图2是各种不同密度的硝酸与铁反应(相同温度)时主要还原产物的分布图。下列叙
述中不正确的是___________(填字母)。
A.硝酸的密度越大,其浓度越小
B.当还原剂和温度都相同时,不同浓度的硝酸被还原的产物不是单一的,只是在某浓度时,以某种产物
为主而已
C.硝酸的浓度越大,还原产物中N元素低化合价产物越少
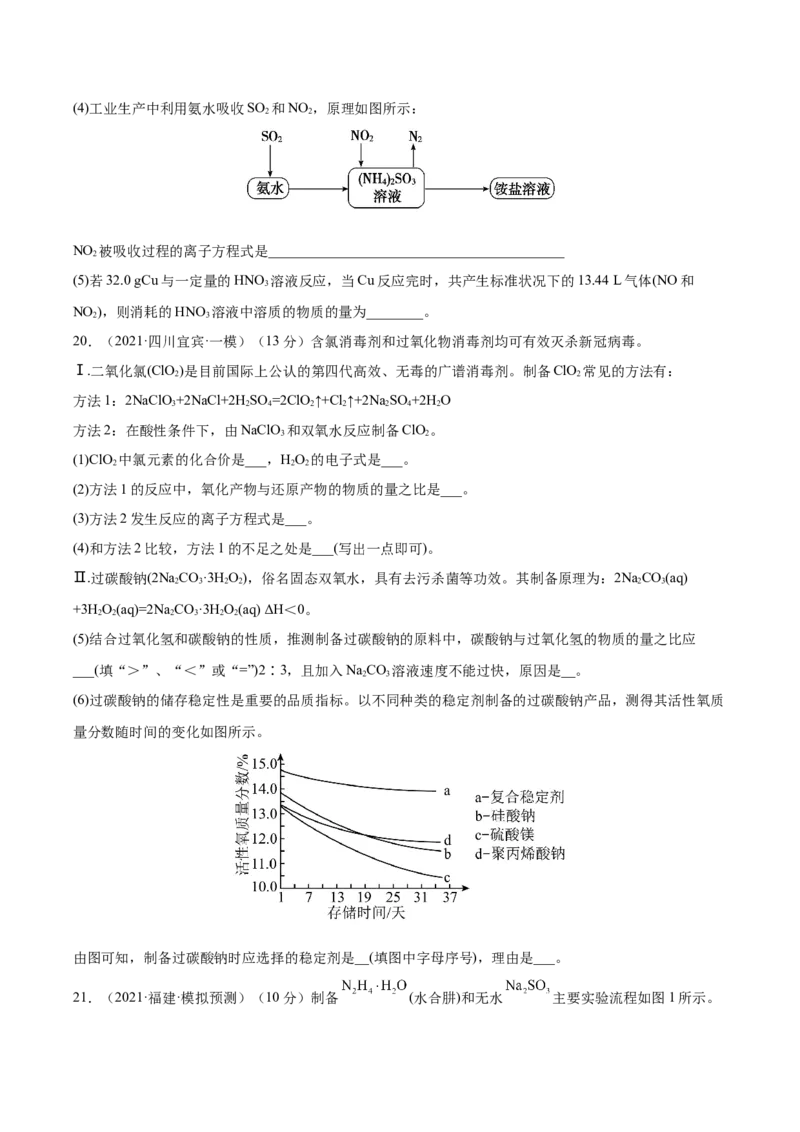
D.当硝酸的密度大于 时,还原产物主要为NO、(4)现有一定量铝粉和铜粉的混合物与一定量很稀的硝酸溶液充分反应,反应过程中无气体放出。在反应结
束后的溶液中,逐滴加入 的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如图
3所示。
①c点对应NaOH溶液的体积为___________mL。
②de段发生反应的离子方程式为___________。
19.(2020·全国·模拟预测)(13分)硅、硫、氮等非金属元素在化工生产中扮演着重要角色。
I.下列物品或设施:
①陶瓷餐具 ②门窗玻璃 ③水晶镜片 ④硅太阳能电池 ⑤光导纤维 ⑥手机芯片。
(1) 直接使用了硅单质的是(用序号填空)________________,
(2) 直接使用了二氧化硅的是(用序号填空)______________,
II.在学习了硫的转化后,某学生绘制了如图转化关系。
(1)写出简单气态氢化物B的结构式:______________。
(2)写出SO 转化为A的化学方程式:____________________________________。
2
(3)下列五种有色溶液与SO 作用均能褪色
2
①品红溶液 ②酸性KMnO 溶液 ③溴水 ④滴有酚酞的NaOH溶液 ⑤淀粉碘溶液
4
体现了SO 漂白性的是(用序号填空)____________________。
2
体现了SO 还原性的是(用序号填空)____________________。
2
写出SO 通入酸性KMnO 溶液反应的离子方程式:______________________。
2 4(4)工业生产中利用氨水吸收SO 和NO ,原理如图所示:
2 2
NO 被吸收过程的离子方程式是__________________________________________
2
(5)若32.0 gCu与一定量的HNO 溶液反应,当Cu反应完时,共产生标准状况下的13.44 L气体(NO和
3
NO ),则消耗的HNO 溶液中溶质的物质的量为________。
2 3
20.(2021·四川宜宾·一模)(13分)含氯消毒剂和过氧化物消毒剂均可有效灭杀新冠病毒。
Ⅰ.二氧化氯(ClO )是目前国际上公认的第四代高效、无毒的广谱消毒剂。制备ClO 常见的方法有:
2 2
方法1:2NaClO+2NaCl+2HSO =2ClO ↑+Cl↑+2Na SO +2H O
3 2 4 2 2 2 4 2
方法2:在酸性条件下,由NaClO 和双氧水反应制备ClO 。
3 2
(1)ClO 中氯元素的化合价是___,HO 的电子式是___。
2 2 2
(2)方法1的反应中,氧化产物与还原产物的物质的量之比是___。
(3)方法2发生反应的离子方程式是___。
(4)和方法2比较,方法1的不足之处是___(写出一点即可)。
Ⅱ.过碳酸钠(2Na CO·3H O),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:2NaCO(aq)
2 3 2 2 2 3
+3H O(aq)=2Na CO·3H O(aq) ΔH<0。
2 2 2 3 2 2
(5)结合过氧化氢和碳酸钠的性质,推测制备过碳酸钠的原料中,碳酸钠与过氧化氢的物质的量之比应
___(填“>”、“<”或“=”)2∶3,且加入NaCO 溶液速度不能过快,原因是__。
2 3
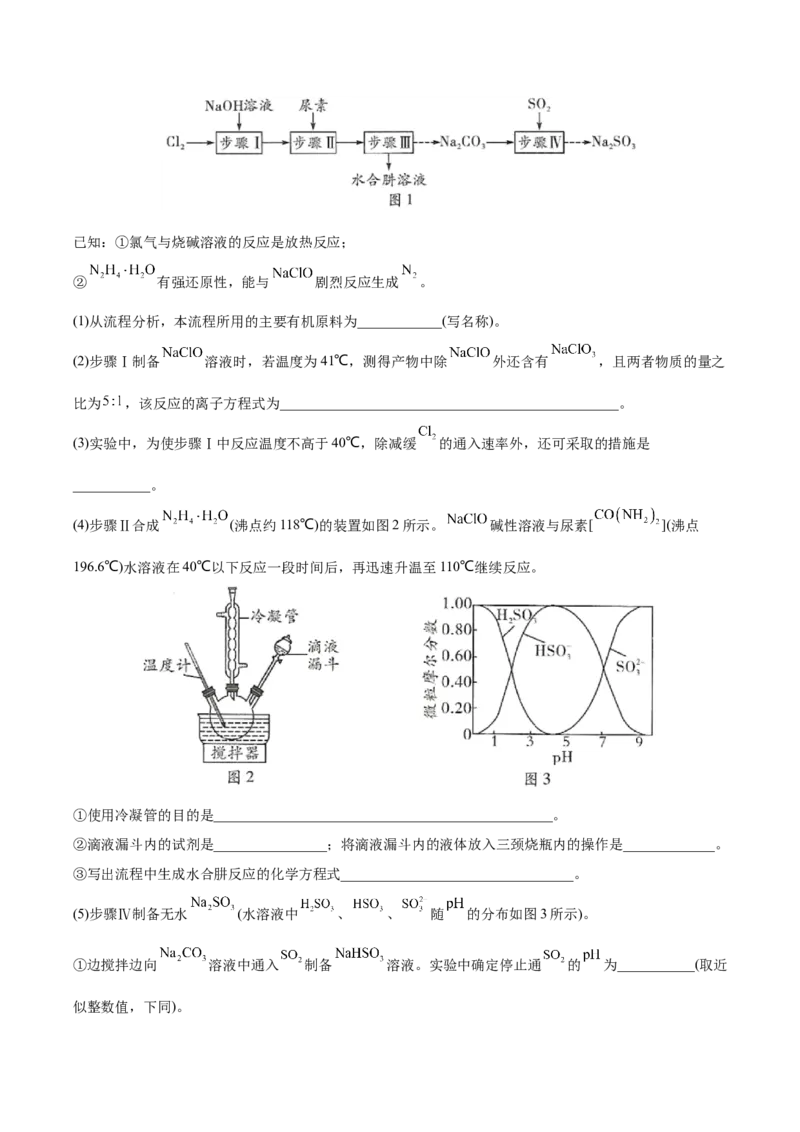
(6)过碳酸钠的储存稳定性是重要的品质指标。以不同种类的稳定剂制备的过碳酸钠产品,测得其活性氧质
量分数随时间的变化如图所示。
由图可知,制备过碳酸钠时应选择的稳定剂是__(填图中字母序号),理由是___。
21.(2021·福建·模拟预测)(10分)制备 (水合肼)和无水 主要实验流程如图1所示。已知:①氯气与烧碱溶液的反应是放热反应;
② 有强还原性,能与 剧烈反应生成 。
(1)从流程分析,本流程所用的主要有机原料为____________(写名称)。
(2)步骤Ⅰ制备 溶液时,若温度为41℃,测得产物中除 外还含有 ,且两者物质的量之
比为 ,该反应的离子方程式为________________________________________________。
(3)实验中,为使步骤Ⅰ中反应温度不高于40℃,除减缓 的通入速率外,还可采取的措施是
___________。
(4)步骤Ⅱ合成 (沸点约118℃)的装置如图2所示。 碱性溶液与尿素[ ](沸点
196.6℃)水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。
①使用冷凝管的目的是________________________________________________。
②滴液漏斗内的试剂是________________;将滴液漏斗内的液体放入三颈烧瓶内的操作是_____________。
③写出流程中生成水合肼反应的化学方程式_________________________________。
(5)步骤Ⅳ制备无水 (水溶液中 、 、 随 的分布如图3所示)。
①边搅拌边向 溶液中通入 制备 溶液。实验中确定停止通 的 为___________(取近
似整数值,下同)。②用制得的 溶液再制 溶液的 应控制在_________________。