文档内容
综合大题标准练(二)
1.(11分)SrCO 可用于金属冶炼和锶盐制备等。以天青石(成分为SrSO 、BaSO 、CaSO 、SiO )为原料制备
3 4 4 4 2
SrCO 的工艺流程如图。
3
已知:常温下,K (SrSO )=3.2×10-7、K (BaSO )=1.0×10-10、K (SrCO )=1.6×10-9。
sp 4 sp 4 sp 3
(1)天青石磨成粉的目的是 ,为达到同样的目的还可以采取的措施为
(填1条即可)。
(2)天青石粉中的SrSO 与氨水、NH HCO 溶液反应的离子方程式为 ;NH HCO 溶
4 4 3 4 3
液中c(NH ·H O)+c(OH-)+c(CO2- ) (填“>”“<”或“=”)c(H CO )+c(H+);将滤液1蒸发浓缩、冷
3 2 3 2 3
却结晶可得副产物 (填化学式)。
(3)滤渣的主要成分为 (填化学式)。
(4)打浆酸溶后的滤液加热至95~100 ℃,加NaOH溶液调pH=14的目的是 。
(5)碱析后获得Sr(OH) 溶液的操作为 。
2
(6)实验室可通过 鉴别NaOH和Sr(OH) 。
2
答案 (1)增大接触面积,加快反应速率 搅拌 (2)SrSO +NH ·H O+HCO- ===SrCO +N H+ +SO2- +H O
4 3 2 3 3 4 4 2
= (N H ) SO (3)BaSO 、SiO (4)促使Ca2+沉淀,便于除杂 (5)过滤 (6)焰色试验
4 2 4 4 2
解析 在天青石(成分为SrSO 、BaSO 、CaSO 、SiO )中加入氨水和碳酸氢铵,得到滤液1主要溶质为硫
4 4 4 2
酸铵,硫酸锶转化为碳酸锶,再向固体中加入盐酸,滤渣中主要成分为二氧化硅和硫酸钡,打浆酸溶后的
滤液加热至95~100 ℃,加NaOH溶液调pH=14将钙离子转化为氢氧化钙,加入氢氧化钠碱析得到氢氧化
锶,加纯水溶解后通入二氧化碳生成碳酸锶,据此回答。(2)天青石粉中的SrSO 与氨水、NH HCO 溶液反
4 4 3
应生成碳酸锶、硫酸铵和水,离子方程式为SrSO +NH ·H O+HCO- ===SrCO +N H+ +SO2- +H O;根据质
4 3 2 3 3 4 4 2
子守恒,则c(NH ·H
O)+c(OH-)+c(CO2-
)=c(H CO )+c(H+)。
3 2 3 2 3
2.(18分)高效、安全的消毒剂优氯净,其有效成分氰尿酸钠( )可溶于水,难溶于冰水,常温下
性质稳定,受热易分解。实验室可通过以下装置和原理(夹持仪器已略去)来制取。已知:
(1)a、b中分别盛放浓盐酸和高浓度NaClO溶液,a和b的仪器可以相同,则仪器名称为 。
(2)连接好仪器, ,再用热毛巾捂住圆底烧瓶,检查装置气密性。
(3)丙中反应温度控制在10 ℃左右,温度不宜过高的原因是 、
。
(4)乙中液体为 ;通入三颈烧瓶中的气体的作用是 。
(5)将所得产品充分析出并分离的操作为 、过滤、冷水洗涤、低温干燥。
(6)产品有效氯含量测定:称取0.100 0 g产品,配成100 mL溶液,取50 mL溶液于锥形瓶中,依次加入适
量醋酸溶液和过量的KI溶液。用0.100 0 mol·L-1标准Na S O 溶液滴定至溶液呈浅黄色时,滴加2滴淀粉
2 2 3
溶液,继续滴定至终点,共消耗Na S O 溶液18.00 mL。(已知:Na S O 转化为Na S O )
2 2 3 2 2 3 2 4 6
①测定过程中,生成I 的离子方程式为 。
2
②产品有效氯含量为 (产品有效氯以转化为HClO中氯元素的质量来计算)。
答案 (1)分液漏斗(或恒压滴液漏斗) (2)关闭a和b中的活塞,将丁中导管末端插入水中 (3)防止温度过
高产品分解 防止Cl 与NaOH发生副反应生成NaClO (4)饱和食盐水 Cl 与NaOH溶液反应生成
2 3 2
NaClO,使NaClO保持较高浓度 (5)冰水冷却结晶 (6)①HClO+2I-+CH COOH===Cl-+CH COO-+I +H O
3 3 2 2
②63.9%
解析 (1)a、b装置中盛放的试剂分别是浓盐酸和次氯酸钠溶液,浓盐酸具有挥发性,反应需要控制反应速
率,则仪器为分液漏斗或恒压滴液漏斗。(2)实验开始前需要检查装置的气密性,所以要关闭分液漏斗(或
恒压滴液漏斗)的活塞,将丁中导管末端插入水中,用热毛巾捂住甲装置的圆底烧瓶,若导管口有气泡产生,
拿掉热毛巾导管口处产生一段水柱,则证明气密性良好。(3)氰尿酸钠受热易分解,而且氯气和氢氧化钠反
应,温度不同,产物不同,低温生成次氯酸钠,而高温生成氯酸钠,所以温度控制在10 ℃左右,不宜过
高,可以防止温度过高产品分解,也可以防止Cl 与NaOH发生副反应生成NaClO 。(4)由题意知制备氰尿
2 3
酸钠的试剂为氰尿酸和高浓度的NaClO溶液,反应过程中NaClO溶液的浓度会逐渐降低,为了保持NaClO溶液的浓度,向三颈烧瓶中通入Cl ,使之与生成的NaOH反应生成NaClO,但浓盐酸有很强的挥
2
发性,挥发出的HCl会与生成的NaOH反应,从而降低NaOH的利用率,则乙装置中的应盛放饱和食盐水,
吸收挥发出的HCl。(6)根据已知②知样品中氯元素的质量等于反应生成的次氯酸中氯元素的质量,根据题
意可知, KI被HClO氧化为I ,反应的离子方程式为2I-+HClO+CH COOH===I +Cl-+CH COO-+2H O,再
2 3 2 3 2
向溶液中加入标准Na S O 溶液与I 反应,反应的方程式为I +2Na S O ===2NaI+Na S O ,则有
2 2 3 2 2 2 2 3 2 4 6
1 1
n(HClO)=n(I )= n(Na S O )= ×0.100 0 mol·L-1×18.00×10-3 L=9×10-4 mol,则样品有效氯含量=
2 2 2 2 3 2
9×10-4mol
×100 mL×35.5 g·mol-1
50 mL ×100%=63.9%。
0.100 0 g
3.(10分)CO 不仅是一种温室气体,也是一种来源广泛且廉价易得的碳资源,可通过热化学、电化学等方
2
法再利用。
(Ⅰ)科学家通过如下反应利用CO 合成甲醇:CO (g)+3H (g) CH OH(g)+H O(g)
2 2 2 3 2
1
已知:H (g)+ O (g)===H O(g) ΔH =-245 kJ·mol-1
2 2 2 2 1
3
CH OH(g)+ O (g)===CO (g)+2H O(g) ΔH =-681 kJ·mol-1
3 2 2 2 2 2
(1)计算上述合成甲醇反应的焓变ΔH= kJ·mol-1。
(2)科学研究中常用产物的时空收率(单位物质的量催化剂表面产物分子的平均生成速率)来衡量催化效果,
在3 MPa,n(CO
2
)∶n(H
2
)=1∶2时,不同Ni、Ga配比的Ni⁃Ga/SiO
2
催化剂下,测定甲醇时空收率随温度的
变化曲线如图所示,甲醇时空收率随温度变化先增大后减小的原因是
。催化剂的最佳配比和反应温度是 。
(3)将等量CO 和H 充入恒温恒容密闭容器中反应合成甲醇,已知该温度下反应的化学平衡常数K=0.01,
2 2
下列事实说明该反应已达平衡的是 (填字母)。
A.气体密度保持不变
B.H O(g)与CO (g)的生成速率相等
2 2
C.某时刻容器中c(CO )=0.8 mol·L-1,c(H )=0.5 mol·L-1,c(CH OH)=c(H O)=0.1 mol·L-1
2 2 3 2
D.混合气体的平均相对分子质量不变
(Ⅱ)甲烷干重整反应可以将两类重要的温室气体和CH 进行重整,涉及主要反应如下:
4
反应Ⅰ:CO (g)+CH (g) 2CO(g)+2H (g) ΔH =+247 kJ·mol-1
2 4 2 1
反应Ⅱ:CO (g)+H (g) CO(g)+H O(g) ΔH =+41 kJ·mol-1
2 2 2 2(4)恒温恒容2 L密闭容器中,按n(CO )=n(CH )=n(Ar)=1 mol投料,初始总压3 MPa,达到平衡状态时测得
2 4
CO 转化率为60%,平衡总压为3.8 MPa。计算该温度下反应Ⅰ的浓度平衡常数K= 。
2 c
n(CO )
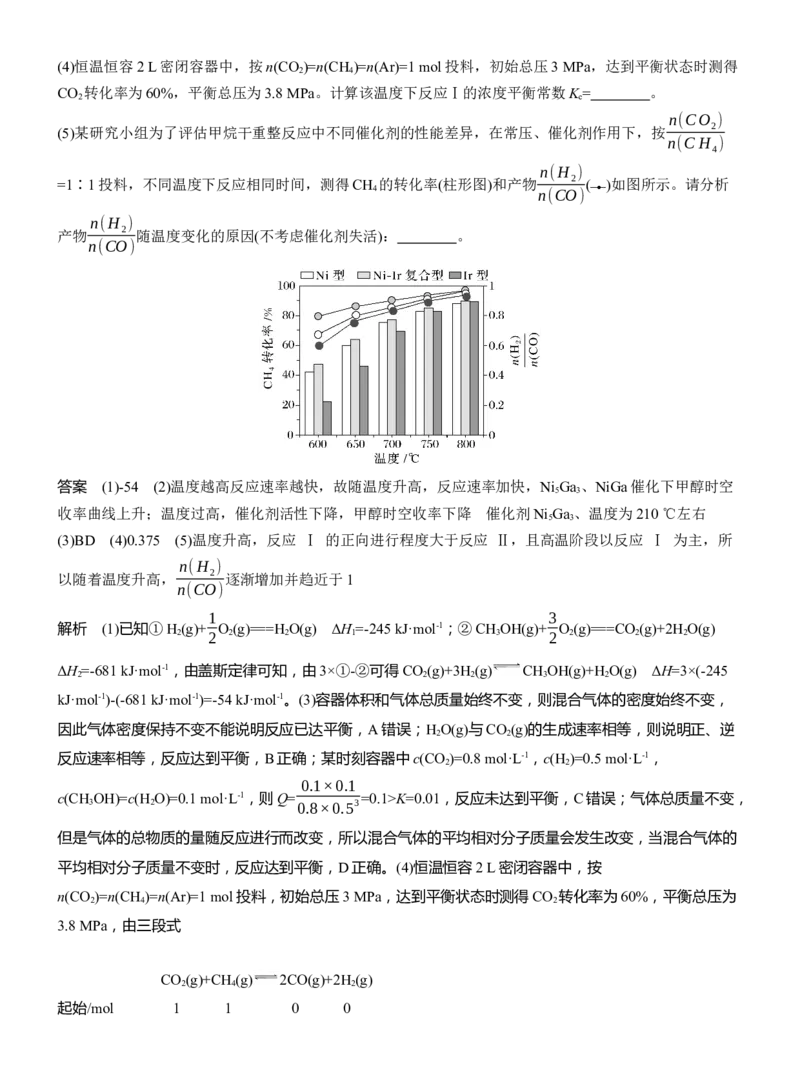
(5)某研究小组为了评估甲烷干重整反应中不同催化剂的性能差异,在常压、催化剂作用下,按 2
n(CH )
4
n(H )
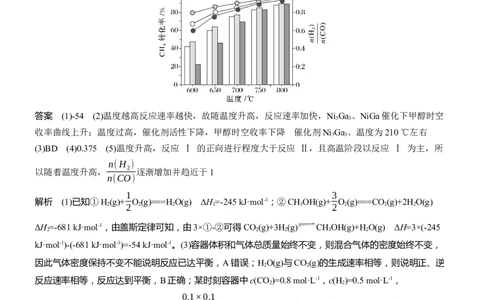
=1∶1投料,不同温度下反应相同时间,测得CH 的转化率(柱形图)和产物 2 ( )如图所示。请分析
4 n(CO)
n(H )
产物 2 随温度变化的原因(不考虑催化剂失活): 。
n(CO)
答案 (1)-54 (2)温度越高反应速率越快,故随温度升高,反应速率加快,Ni Ga 、NiGa催化下甲醇时空
5 3
收率曲线上升;温度过高,催化剂活性下降,甲醇时空收率下降 催化剂Ni Ga 、温度为210 ℃左右
5 3
(3)BD (4)0.375 (5)温度升高,反应 Ⅰ 的正向进行程度大于反应 Ⅱ,且高温阶段以反应 Ⅰ 为主,所
n(H )
以随着温度升高, 2 逐渐增加并趋近于1
n(CO)
1 3
解析 (1)已知①H (g)+ O (g)===H O(g) ΔH =-245 kJ·mol-1;②CH OH(g)+ O (g)===CO (g)+2H O(g)
2 2 2 2 1 3 2 2 2 2
ΔH =-681 kJ·mol-1,由盖斯定律可知,由3×①-②可得CO (g)+3H (g) CH OH(g)+H O(g) ΔH=3×(-245
2 2 2 3 2
kJ·mol-1)-(-681 kJ·mol-1)=-54 kJ·mol-1。(3)容器体积和气体总质量始终不变,则混合气体的密度始终不变,
因此气体密度保持不变不能说明反应已达平衡,A错误;H O(g)与CO (g)的生成速率相等,则说明正、逆
2 2
反应速率相等,反应达到平衡,B正确;某时刻容器中c(CO )=0.8 mol·L-1,c(H )=0.5 mol·L-1,
2 2
0.1×0.1
c(CH OH)=c(H O)=0.1 mol·L-1,则Q= =0.1>K=0.01,反应未达到平衡,C错误;气体总质量不变,
3 2 0.8×0.53
但是气体的总物质的量随反应进行而改变,所以混合气体的平均相对分子质量会发生改变,当混合气体的
平均相对分子质量不变时,反应达到平衡,D正确。(4)恒温恒容2 L密闭容器中,按
n(CO )=n(CH )=n(Ar)=1 mol投料,初始总压3 MPa,达到平衡状态时测得CO 转化率为60%,平衡总压为
2 4 2
3.8 MPa,由三段式
CO (g)+CH (g) 2CO(g)+2H (g)
2 4 2
起始/mol 1 1 0 0变化/mol x x 2x 2x
平衡/mol 1-x 1-x 2x 2x
CO (g)+H (g) CO(g)+H O(g)
2 2 2
起始/mol 1-x 2x 2x 0
变化/mol y y y y
平衡/mol 1-x-y 2x-y 2x+y y
x+ y (1+1-x- y+1-x+2x- y+2x+ y+ y)mol 3.8 MPa
得 ×100%=60%, = ,解得x=0.4,y=0.2,则
1 3mol 3 MPa
0.4mol 0.6mol 1mol 0.6mol
c(CO )= =0.2 mol·L-1、c(CH )= =0.3 mol·L-1、c(CO)= =0.5 mol·L-1、c(H )= =0.3
2 2 L 4 2 L 2 L 2 2 L
0.32×0.52
mol·L-1,反应 Ⅰ 的浓度平衡常数K= =0.375。
c 0.3×0.2
4.(11分)化合物H是一种在外力作用前完全化学惰性但是在施加外力后可以进行化学降解的新型高分子,
其合成路线如下:
已知:
① ;
②RCOOR RCH OH。
2
(1)反应Ⅰ的反应类型是 。
(2)化合物B的酸性比HOOC(CH ) COOH (填“强”或“弱”)。
2 2
(3)化合物C的官能团为碳碳三键、 (写名称)。
(4)化合物D中碳原子的杂化类型为sp杂化、 。
(5)化合物E(C H O )的结构简式为 。
10 12 5(6)反应Ⅱ的第一步反应化学方程式为 。
(7)X是E的同分异构体,写出同时满足下列条件X的结构简式: (任写一种)。
①X的核磁共振氢谱有三组峰,峰面积比为3∶2∶1;
②1 mol X能与2 mol NaHCO 恰好完全反应;
3
③含有两个环。
(8)参考上面流程设计以 和 为原料合成 的路线(无机试剂任
选)。
答案 (1)加成反应 (2)强 (3)羧基 (4)sp2杂化、sp3杂化 (5)
(6) +4KOH +2KBr+4H O
2
(7) 、 、 、 、 、
、 、 、 、 、
、 等
(8)
解析 与Br 发生加成反应生成B,B与KOH/乙醇加热反应后加H SO 酸化生成C,
2 2 4
C与CH OH在浓硫酸存在下发生酯化反应生成D,D与 在一定条件下发生题给已知①的反应生成E,
3
结合E的分子式知,E为 ,E与H 发生加成反应生成F,F为 ,
2
F与LiAlH 发生题给已知②的反应生成G,G经一系列反应得到H。(2)由于—Br是吸电子基团,使得
4
HOOCCHBrCHBrCOOH的羧基中羟基的极性大于HOOCCH CH COOH的羧基中羟基的极性,
2 2
HOOCCHBrCHBrCOOH更易电离出H+,故HOOCCHBrCHBrCOOH的酸性比HOOCCH CH COOH强。
2 2(7)E的分子式为C H O ,不饱和度为5,X是E的同分异构体,1 mol X能与2 mol NaHCO 恰好完全反应,
10 12 5 3
1个X中含2个羧基,X中含两个环、核磁共振氢谱有三组峰且峰面积之比为3∶2∶1,说明含2个甲基且
结构对称性高,符合条件的同分异构体的结构简式见答案。(8)对比 与 和
的结构,可利用题给已知①构建碳骨架,即 与
一定条件下反应生成 , 与H 反应生成 ,
2
发生题给已知②的反应得到 ,合成路线见答案。