文档内容
考点 09 氯及其化合物
(好题冲关)
【基础过关】
1.(2023·江苏省南通市三模)NaClO是家用消毒液的有效成分,这是利用了NaClO的( )
A.碱性 B.强氧化性 C.还原性 D.受热后不稳定性
2.下列关于氯及其化合物的性质与用途具有对应关系的是( )
A.Cl 易液化,可用于生产盐酸 B.ClO 有强氧化性,可用于自来水消毒
2 2
C.CCl 难溶于水,可用作灭火剂 D.HCl极易溶于水,可用于检验NH
4 3
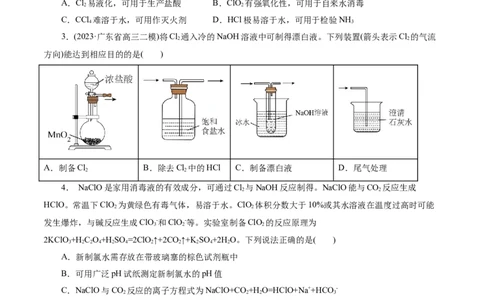
3.(2023·广东省高三二模)将Cl 通入冷的NaOH溶液中可制得漂白液。下列装置(箭头表示Cl 的气流
2 2
方向)能达到相应目的的是( )
A.制备Cl B.除去Cl 中的HCl C.制备漂白液 D.尾气处理
2 2
4. NaClO是家用消毒液的有效成分,可通过Cl 与NaOH反应制得。NaClO能与CO 反应生成
2 2
HClO。常温下ClO 为黄绿色有毒气体,易溶于水。ClO 体积分数大于10%或其水溶液在温度过高时可能
2 2
发生爆炸,与碱反应生成ClO -和ClO -等。实验室制备ClO 的反应原理为
3 2 2
2KClO+H C O+H SO =2ClO ↑+2CO ↑+K SO +2H O。下列说法正确的是( )
3 2 2 4 2 4 2 2 2 4 2
A.新制氯水需存放在带玻璃塞的棕色试剂瓶中
B.可用广泛pH试纸测定新制氯水的pH值
C.NaClO与CO 反应的离子方程式为NaClO+CO +H O=HClO+Na++HCO-
2 2 2 3
D.使用NaClO消毒时,可用盐酸酸化
5.实验室既可用浓盐酸与MnO 在加热时反应制备Cl ,也可用KMnO 与浓盐酸在常温下反应制备
2 2 4
Cl,下列有关说法不正确的是( )
2
A.KMnO 的氧化性比MnO 的强
4 2
B.制备Cl 的整个实验过程中,只需要使用氧化剂与还原剂
2
C.用排气法收集Cl 时,不需要利用其他试剂就能确定集气瓶中已收集满
2
D.用足量MnO 与含有4 mol HCl的浓盐酸在加热条件下反应,得到Cl 的物质的量小于1 mol
2 2
6.75%乙醇和84消毒液等均能有效灭活新冠病毒。84消毒液的主要成分是次氯酸钠。设N 为阿伏加
A
资料收集整理【淘宝店铺:向阳百分百】德罗常数的值,下列说法正确的是( )
A.74.5g次氯酸钠中含有的离子数目为2N
A
B.1mol次氯酸钠与足量盐酸反应转移的电子数为2N
A
C.46g 75%乙醇中含有的氧原子数大于6N
A
D.利用氯气和氢氧化钠溶液反应制取0.1 mol次氯酸钠需要消耗2.24L氯气
7.(2023·广东省广州市三模)某溶液的主要成分为NaClO(含有一定量的NaOH),既能杀菌消毒又能漂
白。下列用来解释事实的离子方程式不正确的是( )
A.该溶液可用NaOH溶液吸收Cl 制备:Cl+2OH-=Cl-+ClO-+H O
2 2 2
B.该溶液与洁厕灵(主要成分为HCl)混合产生Cl:2H++Cl-+ClO-=Cl↑+H O
2 2 2
C.该溶液与过氧化氢溶液混合产生O:2ClO-+H O=2Cl-+O ↑+2OH-
2 2 2 2
D.该溶液加白醋可增强漂白作用:CHCOOH+ClO-=HClO+CH COO-
3 3
8.(2023·北京市海淀区三模)某消毒液的主要成分为NaClO(pH=13),已知饱和NaClO溶液的pH约为
11.下列用来解释事实的方程式中,不合理的是( )
A.该消毒液可用NaOH溶液吸收Cl 制备:Cl+2OH-= ClO-+ Cl-+H O
2 2 2
B.该消毒液与洁厕灵(主要成分为 )混用,产生Cl:ClO-+ Cl-+2H+= Cl ↑+H O
2 2 2
C.该消毒液加白醋,可增强漂白作用:CHCOOH+ClO-=CH COO-+HClO
3 3
D.该消毒液中加少量FeSO 溶液生成红褐色沉淀:2Fe2++ClO-+5H O= Cl-+2Fe(OH) ↓ +4H+
4 2 3
9.部分含氯物质的分类与相应氯元素的化合价关系下图所示。下列说法错误的是( )
A.a 与d,a与e在酸性情况下反应,均可以得到b
B.c 为一种新型自来水消毒剂,代替 b的原因是:c的毒性更小
C.b 的水溶里加入 CaCO ,可以增加d的产量
3
D.消毒液可用于环境消毒,主要是因为含有d,e的固体可用于实验室制O
2
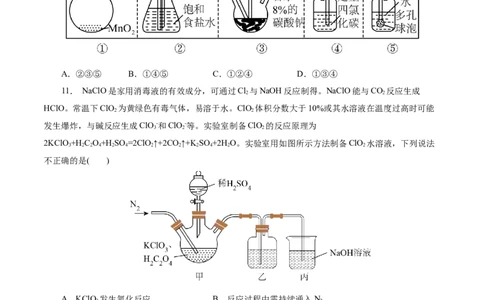
10.已知氯气和空气按体积比1∶3混合通入潮湿的碳酸钠中能生成ClO,且反应放热;不含Cl 的
2 2
资料收集整理【淘宝店铺:向阳百分百】ClO易与水反应生成HClO;ClO在42℃以上会分解生成Cl 和O。设计如图装置(部分夹持装置略)制备
2 2 2 2
HClO,每个虚线框表示一个装置单元,其中存在错误的是( )
A.②③⑤ B.①④⑤ C.①②④ D.①③④
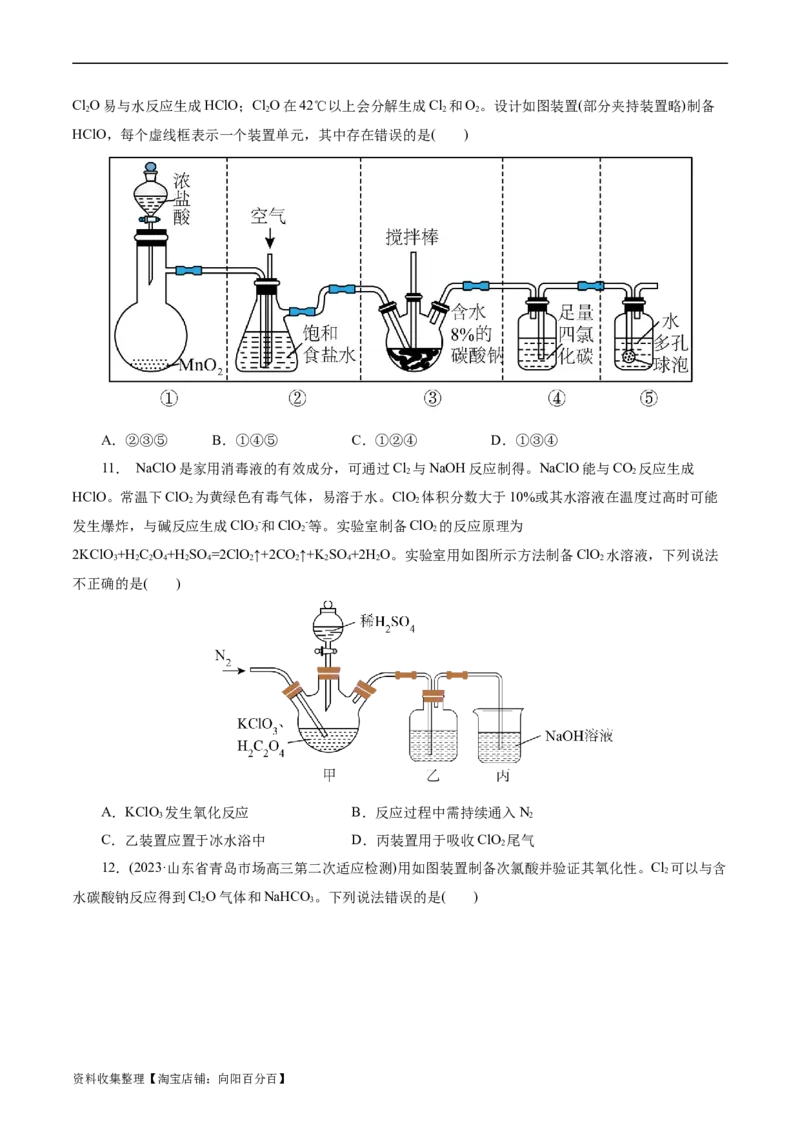
11. NaClO是家用消毒液的有效成分,可通过Cl 与NaOH反应制得。NaClO能与CO 反应生成
2 2
HClO。常温下ClO 为黄绿色有毒气体,易溶于水。ClO 体积分数大于10%或其水溶液在温度过高时可能
2 2
发生爆炸,与碱反应生成ClO -和ClO -等。实验室制备ClO 的反应原理为
3 2 2
2KClO+H C O+H SO =2ClO ↑+2CO ↑+K SO +2H O。实验室用如图所示方法制备ClO 水溶液,下列说法
3 2 2 4 2 4 2 2 2 4 2 2
不正确的是( )
A.KClO 发生氧化反应 B.反应过程中需持续通入N
3 2
C.乙装置应置于冰水浴中 D.丙装置用于吸收ClO 尾气
2
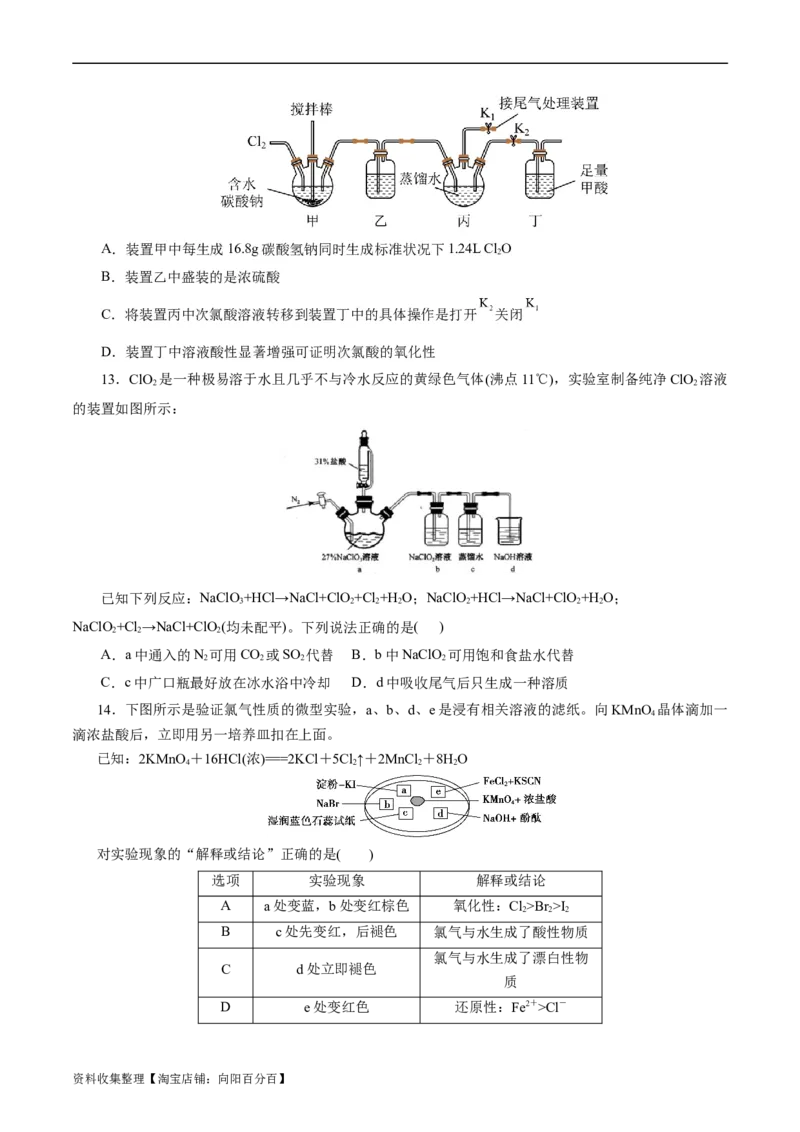
12.(2023·山东省青岛市场高三第二次适应检测)用如图装置制备次氯酸并验证其氧化性。Cl 可以与含
2
水碳酸钠反应得到ClO气体和NaHCO 。下列说法错误的是( )
2 3
资料收集整理【淘宝店铺:向阳百分百】A.装置甲中每生成16.8g碳酸氢钠同时生成标准状况下1.24L Cl O
2
B.装置乙中盛装的是浓硫酸
C.将装置丙中次氯酸溶液转移到装置丁中的具体操作是打开 关闭
D.装置丁中溶液酸性显著增强可证明次氯酸的氧化性
13.ClO 是一种极易溶于水且几乎不与冷水反应的黄绿色气体(沸点11℃),实验室制备纯净ClO 溶液
2 2
的装置如图所示:
已知下列反应:NaClO+HCl→NaCl+ClO +Cl+H O;NaClO+HCl→NaCl+ClO +H O;
3 2 2 2 2 2 2
NaClO+Cl→NaCl+ClO (均未配平)。下列说法正确的是( )
2 2 2
A.a中通入的N 可用CO 或SO 代替 B.b中NaClO 可用饱和食盐水代替
2 2 2 2
C.c中广口瓶最好放在冰水浴中冷却 D.d中吸收尾气后只生成一种溶质
14.下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO 晶体滴加一
4
滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO +16HCl(浓)===2KCl+5Cl↑+2MnCl +8HO
4 2 2 2
对实验现象的“解释或结论”正确的是( )
选项 实验现象 解释或结论
A a处变蓝,b处变红棕色 氧化性:Cl>Br >I
2 2 2
B c处先变红,后褪色 氯气与水生成了酸性物质
氯气与水生成了漂白性物
C d处立即褪色
质
D e处变红色 还原性:Fe2+>Cl-
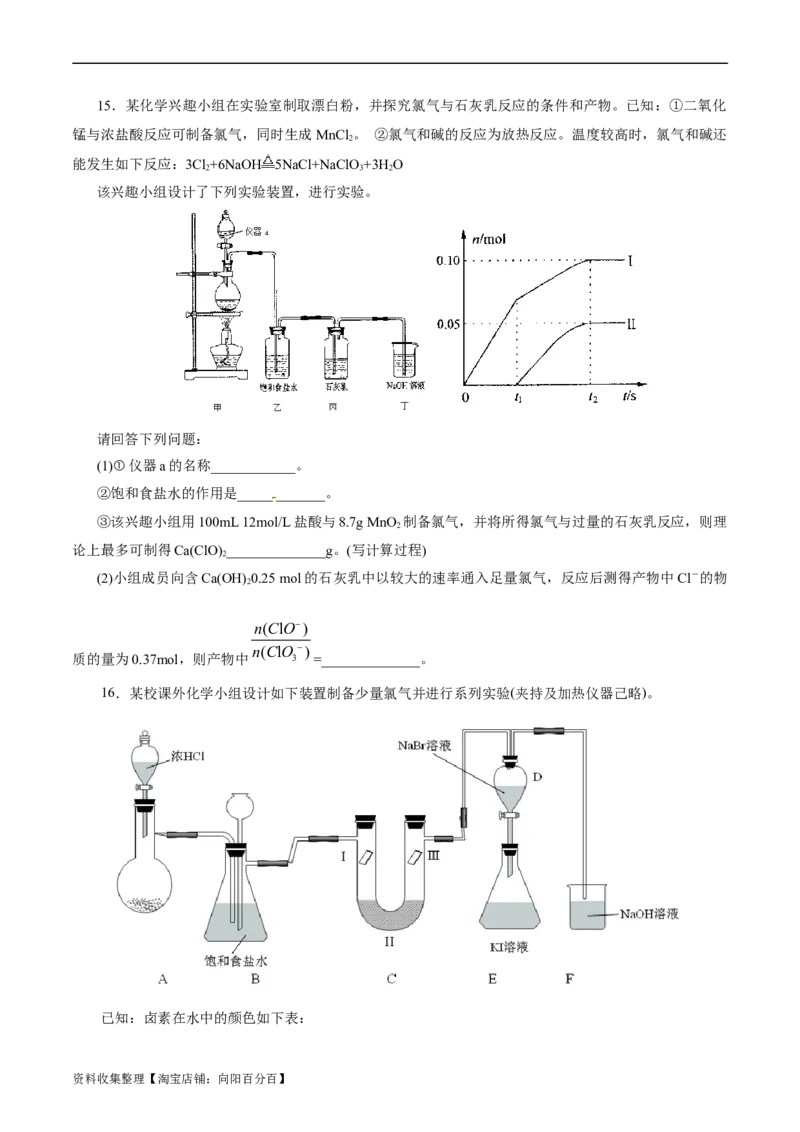
资料收集整理【淘宝店铺:向阳百分百】15.某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。已知:①二氧化
锰与浓盐酸反应可制备氯气,同时生成MnCl 。 ②氯气和碱的反应为放热反应。温度较高时,氯气和碱还
2
能发生如下反应:3Cl+6NaOH 5NaCl+NaClO +3H O
2 3 2
该兴趣小组设计了下列实验装置,进行实验。
请回答下列问题:
(1)①仪器a的名称____________。
②饱和食盐水的作用是____________。
③该兴趣小组用100mL 12mol/L盐酸与8.7g MnO 制备氯气,并将所得氯气与过量的石灰乳反应,则理
2
论上最多可制得Ca(ClO) ______________g。(写计算过程)
2
(2)小组成员向含Ca(OH) 0.25 mol的石灰乳中以较大的速率通入足量氯气,反应后测得产物中Cl-的物
2
n(ClO)
n(ClO )
质的量为0.37mol,则产物中 3 =______________。
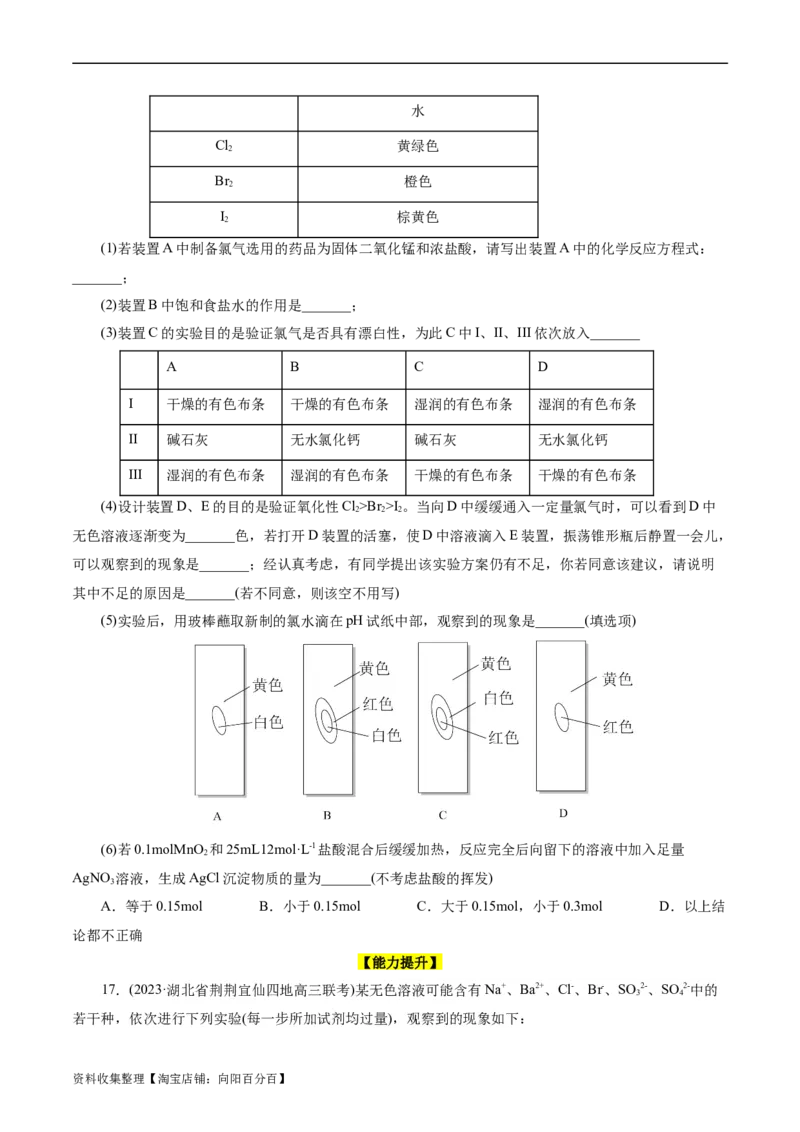
16.某校课外化学小组设计如下装置制备少量氯气并进行系列实验(夹持及加热仪器己略)。
已知:卤素在水中的颜色如下表:
资料收集整理【淘宝店铺:向阳百分百】水
Cl 黄绿色
2
Br 橙色
2
I 棕黄色
2
(1)若装置A中制备氯气选用的药品为固体二氧化锰和浓盐酸,请写出装置A中的化学反应方程式:
_______;
(2)装置B中饱和食盐水的作用是_______;
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入_______
A B C D
I 干燥的有色布条 干燥的有色布条 湿润的有色布条 湿润的有色布条
II 碱石灰 无水氯化钙 碱石灰 无水氯化钙
III 湿润的有色布条 湿润的有色布条 干燥的有色布条 干燥的有色布条
(4)设计装置D、E的目的是验证氧化性Cl>Br >I 。当向D中缓缓通入一定量氯气时,可以看到D中
2 2 2
无色溶液逐渐变为_______色,若打开D装置的活塞,使D中溶液滴入E装置,振荡锥形瓶后静置一会儿,
可以观察到的现象是_______;经认真考虑,有同学提出该实验方案仍有不足,你若同意该建议,请说明
其中不足的原因是_______(若不同意,则该空不用写)
(5)实验后,用玻棒蘸取新制的氯水滴在pH试纸中部,观察到的现象是_______(填选项)
(6)若0.1molMnO 和25mL12mol·L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量
2
AgNO 溶液,生成AgCl沉淀物质的量为_______(不考虑盐酸的挥发)
3
A.等于0.15mol B.小于0.15mol C.大于0.15mol,小于0.3mol D.以上结
论都不正确
【能力提升】
17.(2023·湖北省荆荆宜仙四地高三联考)某无色溶液可能含有Na+、Ba2+、Cl-、Br-、SO 2-、SO 2-中的
3 4
若干种,依次进行下列实验(每一步所加试剂均过量),观察到的现象如下:
资料收集整理【淘宝店铺:向阳百分百】步
操作 现象
骤
(1) 向溶液中滴加氯水,再加入CCl 振荡、静置 下层呈橙红色
4
(2) 分液,向水溶液中加入Ba(NO ) 溶液和稀HNO 有白色沉淀产生
3 2 3
(3) 过滤,向滤液中加入AgNO 方稀溶液和稀HNO 有白色沉淀产生
3 3
下列结论正确的是( )
A.肯定含有的离子是Na+、Br-
B.肯定没有的离子是Ba2+、SO 2-
4
C.如果步骤(2)没有加入稀HNO,白色沉淀可能含有BaSO
3 3
D.如果将步骤(1)中氯水换成HO,对结论没有影响
2 2
18.(2023·辽宁省部分重点吕学协作体高三模拟考试)高铁酸钾可以用于饮用水处理。工业上制备
KFeO 的一种方法是向KOH溶液中通入氯气,然后再加入Fe (NO ) 溶液:
2 4 3 3
①Cl+KOH →KCl+KClO+KClO +H O;
2 3 2
②Fe (NO )+ KClO+KOH→K FeO+KNO + KCl+H O(方程式均未配平)。
3 3 2 4 3 2
下列说法正确的是( )
A.氯气与热的石灰乳反应制得的漂白粉或漂粉精可以用于游泳池等场所的消毒
B.若反应①中n(ClO-):n(ClO -)= 3:1,则该反应还原产物与氧化产物的物质的量之比为
3
C.用上述方法得到2mol KFeO 时最多消耗3mol Cl
2 4 2
D.处理饮用水时,加入高铁酸钾效果相当于加入氯气和铝盐两种物质
19.常温下,向 的NaClO溶液中缓慢通入SO 气体,使其充分吸收,溶液pH与通入
2
SO 物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解)。下列说法错误的是( )
2
A.NaClO溶液中存在c(HClO)=c(OH﹣)-c(H+)
B.常温下,HClO的电离平衡常数为10-3.8
资料收集整理【淘宝店铺:向阳百分百】