文档内容
考点 24 化学反应的方向
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
焓变与熵变 2022浙江1月选考20题,2分;2021浙江6月选考17题,2分;
2022辽宁卷18(1)题,13分;2022湖南卷17(1)题,14分;2021浙
反应自发性判断
江6月选考29(1)题,10分;2021•海南卷16(1)(2) 题,10分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,主要考查:认识自然界中发生的一些自发过程,加强从物质的微观层面理解
反应过程中能量和混乱度变化的能力;了解焓变与熵变的含义,理解焓变、熵变与反应方向的关系;能综
合运用焓变与熵变判断反应进行的方向。
【备考策略】
(1)了解自发过程和化学反应的自发性,知道化学反应是有方向的;
(2)知道化学反应的方向与反应的焓变和熵变有关,能利用能量判椐、熵判椐和复合判据对反应进行方
向的判断。
(3)根据ΔH-TΔS<0判断的只是反应自发进行的可能性,具体的反应能否实际发生,还涉及化学反应
速率的问题
【命题预测】
预计2023年的高考仍然把化学反应进行方向判断融入反应原理综合题中。
考法 1 自发过程与自发反应
1.自发过程
(1)含义:在一定条件下,不用借助外力,就能自发进行的过程。
(2)特点
①能量角度:体系趋向于从高能状态转变为低能状态(体系对外部做功或者放热量)
②混乱度角度:在密闭条件下,体系有从有序自发转变为无序的倾向
③具有方向性:即过程的某个方向在一定条件下自发进行,而该过程逆方向在该条件下肯定不能自发
进行2.自发反应
(1)定义:在给定条件下,可以自发地进行到显著程度的化学反应。如:食品腐败
(2)自发反应的特征
①具有方向性,即反应的某个方向在一定条件下是自发的,则其逆反应在该条件下肯定不自发,如:
食物在常温下会腐败,但是由腐败的食物变为食物是不可能自发进行的。
②体系趋向于从高能量状态转变为低能量状态。如:煤炭在一定条件下会自发燃烧成低能量的二氧化
碳。
③体系趋向于从有序体系转变为无序体系。如:老师离开教室后,学生在无约束的状态下会自发地由
有序的状态进入混乱的状态。
(1)自发反应不是看是否需要条件,而是看是否需要持续施加外力(如加热等);有的需要一定条件引发
反应,一旦反应后即可自发进行。如:碳的燃烧需要点燃。
(2)一般的,如果一个过程是自发的,则其逆过程就是非自发的。非自发过程要想发生,则必须对它做
功,如利用水泵可将水从低处抽向高出,通电可将水分解生成氢气和氧气。
(3)判断某反应是否自发,只是判断反应的方向,与是否会发生、反应的快慢、反应的热效应无关。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)所有自发进行的化学反应都是放热反应( )
(2)自发反应在任何条件下都能发生( )
(3)同一物质的固,液、气三种状态的熵值相同( )
(4)非自发过程在一定条件下可能变成自发过程( )
(5)需要加热才能够进行的过程肯定不是自发过程( )
答案:(1)× (2) × (3)× (4) √ (5)×
例1 下列不属于自发进行的变化是( )
A.红墨水加到清水使整杯水变红 B.冰在室温下融化成水
C.电解饱和食盐水 D.铁器在潮湿的空气中生锈
【答案】C
【解析】A项,扩散现象,是熵增加的自发过程,A不符合题意;B项,冰的熔点为0℃,水常温是液
体,冰在室温下融化成水,是熵增加的自发过程,B不符合题意;C项,电解饱和食盐水,是在外电场的
作用下强制发生的氧化还原反应,不是自发过程,C符合题意;D项,铁在潮湿的空气中生锈是发生了自
发的氧化还原反应,属于电化学腐蚀,是自发进行的化学过程,D不符合题意;故选C。例2 在常温常压下,下列属于自发过程的是( )
A.2C(s) + O (g) = 2CO(g)
2
B.NH Cl(s) = NH (g) + HCl(g)
4 3
C.CHCOOH(l) = CH COOH(s)
3 3
D.2Cr3+(aq) + 3Cl (aq) + 7H O(l) = Cr O (aq) + 6Cl-(aq)+14H+(aq)
2 2 2
【答案】A
【解析】A项,2C(s) + O (g) = 2CO(g)是熵增的放热反应,△H−T S<0,属于自发过程,故A选;B
2
项,NH
4
Cl(s) = NH
3
(g) + HCl(g)是熵增的吸热反应,温度较高时,△H−△T S<0,可以进行,故B不选;C
项,CH
3
COOH(l) = CH
3
COOH(s)是熵减的吸热现象,在常温常压下,不能△自发进行,故C不选;D项,氧
化性Cr O2-> Cl ,根据氧化剂的氧化性大于氧化产物的氧化性规律可知,2Cr3+(aq) + 3Cl (aq) + 7H O(l) =
2 7 2 2 2
Cr O2- (aq) + 6Cl-(aq)+14H+(aq)不能发生,故D不选;故选A。
2 7
对点1 下列说法正确的是( )
A.自发反应是指不需要条件就能发生的反应
B.非自发过程在任何条件下都不可能变为自发过程
C.在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向
D.常温下,反应C(s)+CO(g) 2CO(g)不能自发进行,则该反应的△H>0
2
【答案】D
【解析】A项,自发反应是指在一定温度和压强下,不需要外界帮助即可发生的化学反应,故A错误;
B项,非自发过程在一定条件下可能变为自发过程,如碳酸钙受热分解的反应是熵增的吸热反应,属于在
高温下进行的非自发过程,故B错误;C项,使用催化剂只能降低反应的活化能,加快反应速率,但不能
改变化学反应进行的方向,故C错误;D项,碳与二氧化碳生成一氧化碳的反应是熵增的吸热反应, 0,
故D正确;故选D。
对点2 下列说法中正确的是( )
A.铁在潮湿空气中生锈是自发过程
B.电解池的反应是属于自发反应
C.NH NO 溶于水吸热,说明其溶于水不是自发过程
4 3
D.非自发反应在任何条件下一定都不能发生
【答案】A
【解析】铁在潮湿空气中易生锈,故A正确;电解池的反应需要外界提供电能,电解池的反应不属于
自发反应,故B错误;NH NO 溶于水是自发过程,故C错误;非自发反应改变条件后有可能发生,故D
4 3
项错误。考法 2 熵变
1.熵
(1)概念:衡量体系混乱度的物理量,其符号为S,单位为J·mol-1·K-1。
(2)特点:混乱度越大,体系越无序,体系的熵值就越大。
(3)影响因素:①同一物质:S(高温)>S(低温);S(g)>S(l)>S(s);②相同条件下,不同的物质一般具有不
同的熵值,分子结构越复杂,熵值越大。③S(混合物)>S(纯净物)
2.熵变
(1)概念:反应产物总熵和反应物总熵之差。
(2)计算式:ΔS=∑S(反应产物)- ∑S(反应物)
3.熵判据
(1)对于确定的化学反应,在一定条件下,具有确定的熵变。
(2)熵变(ΔS)只与反应体系的始态和终态有关,与反应进行的途径无关。
(3)熵变(ΔS)是决定反应能否自发进行的一个因素,但不是唯一因素。
(4)熵增加(ΔS>0)有利于反应的自发进行。
1.同一种物质由固态到液态、由液态到气态或自固态直接到气态的过程,是熵增加的过程,其熵变
为正值。
2.气态物质的物质的量增大的反应,是熵增加的反应,熵变通常是正值。
3.气态物质的物质的量减小的反应,是熵减小的反应,熵变通常是负值。
4.熵增加的反应有利于反应自发进行,但有些熵减少的反应也能自发进行。
例1 (2021•浙江6月选考,17)相同温度和压强下,关于物质熵的大小比较,合理的是( )
A.1molCH (g)<1molH (g) B.1molH O(g)<2molH O(g)
4 2 2 2
C.1molH O(s)>1molH O(l) D.1molC(s,金刚石)>1molC(s,石黑)
2 2
【答案】B
【解析】A项,CH(g)和H(g)物质的量相同,且均为气态,CH(g)含有的原子总数多,CH(g)的摩尔
4 2 4 4
质量大,所以熵值1molCH (g)>1molH (g),A错误;B项,相同状态的相同物质,物质的量越大,熵值越
4 2
大,所以熵值1molH O(g)<2molH O(g),B正确;C项,等量的同物质,熵值关系为:S(g)>S(l)>S(s),
2 2
所以熵值1molH O(s)<1molH O(l),C错误;D项,从金刚石和石墨的结构组成上来看,金刚石的微观结
2 2
构更有序,熵值更低,所以熵值1molC(s,金刚石)<1molC(s,石黑),D错误;故选B。
例2 下列说法正确的是( )A.常温常压下,NaCO、CaCO 的溶解焓变相近,NaCO(s) 2Na+(aq)+CO 2-(aq) ΔS;
2 3 3 2 3 3 1
CaCO (s) Ca2+(aq)+CO 2-(aq) ΔS,则ΔS>ΔS
3 3 2 1 2
B.NaCl(s)=NaCl (1) ΔS<0
C.常温常压下,3O(g) 2O (g) ΔS>0
2 3
D.常温常压下,2CO(g) C(s)+O (g) ΔS>0
2
【答案】A
【解析】A项,溶解焓相近,主要由熵变决定反应方向,NaCO(s)更易溶解,所以ΔS>ΔS,A正确;
2 3 1 2
B项,固体变为液体,混乱程度增大,ΔS>,B错误;C项,气体分子数减少,混乱程度减小,ΔS<0,C
错误;D项,反应前后,气体分子数减少,混乱程度减小,ΔS<0,D错误;故选A。
对点1 下列反应△S>0的是( )
A.HCl(g)+NH (g)=NH Cl(s) B.2CO(g)=2C(s)+O (g)
3 4 2
C.N(g)+3H(g)=2NH (g) D.CaCO (s)=CaO(s)+CO (g)
2 2 3 3 2
【答案】D
【解析】A项,该反应为气体系数之和减小的反应,ΔS<0,A不符合题意;B项,该反应为气体系数
之和减小的反应,ΔS<0,B不符合题意;C项,该反应为气体系数之和减小的反应,ΔS<0,C不符合题
意;D项,该反应为气体系数之和增大的反应,ΔS>0,D符合题意;故选D。
对点2 下列对熵变的判断中不正确的是( )
A.少量的食盐溶解于水中:ΔS>0
B.纯碳和氧气反应生成CO(g):ΔS>0
C.气态水变成液态水:ΔS>0
D.CaCO (s)受热分解为CaO(s)和CO(g):ΔS>0
3 2
【答案】C
【解析】食盐溶于水是典型的熵增加过程;2C(s)+O(g)===2CO(g),气体的物质的量增大,为熵增大
2
的反应;气态水变成液态水是体系混乱度减小的过程,为熵减小的过程;CaCO (s)的分解产生了气体,为
3
熵增大的反应。
考法 3 化学反应进行方向的判据
1.焓判据
(1)放热过程中体系能量降低,ΔH <0 ,具有自发的倾向。
(2)实验发现,大多数放热反应是可以自发进行的。
例如:Zn(s) +CuSO (aq) =ZnSO (aq) +Cu(s) ΔH =-216.8kJ/mol
4 4
(3)有些吸热反应也可以自发进行,如Ba(OH) ·8H O晶体与NH Cl晶体的反应是吸热的,但是这个反
2 2 4
应却是可以自发进行的,故不能只根据放热或者吸热来判断化学反应的方向,焓变只是影响反应方向的一种因素。
2.熵判据
(1)熵的定义
描述体系混乱程度的物理量,一般用S表示。熵值越大,体系的混乱度越大 。
(2)熵的大小
同种物质的熵值与其存在状态有关, S(g)>S(l)> S(s)。
(3)熵判据
体系的混乱度(即熵值)增加, ΔS>0,反应有自发的倾向。
有些熵减的过程也能自发进行,如乙烯聚合为聚乙烯的反应,故熵变只是影响反应方向的一种因素。
3.复合判据(自由能ΔG)
在等温、等压条件下的封闭体系中(不考虑体积变化做功以外的其他功),自由能的变化(符号为ΔG,
单位为kJ/mol) 综合反映了体系的焓变和熵变对自发过程的影响:ΔG = ΔH-TΔS。这时,化学反应总是向
着自由能减小的方向进行,直到体系达到平衡。即:
当ΔG <0时,反应能自发进行;
当ΔG =0时,反应处于平衡状态;
当ΔG >0时,反应不能自发进行。
情况 焓变 熵变 自由能变化 反应能否自发进行
① ΔH<0 ΔS>0 ΔG<0 能
② ΔH>0 ΔS<0 ΔG>0 不能
③ ΔH<0 ΔS<0 无法判断 无法判断
④ ΔH>0 ΔS>0 无法判断 无法判断
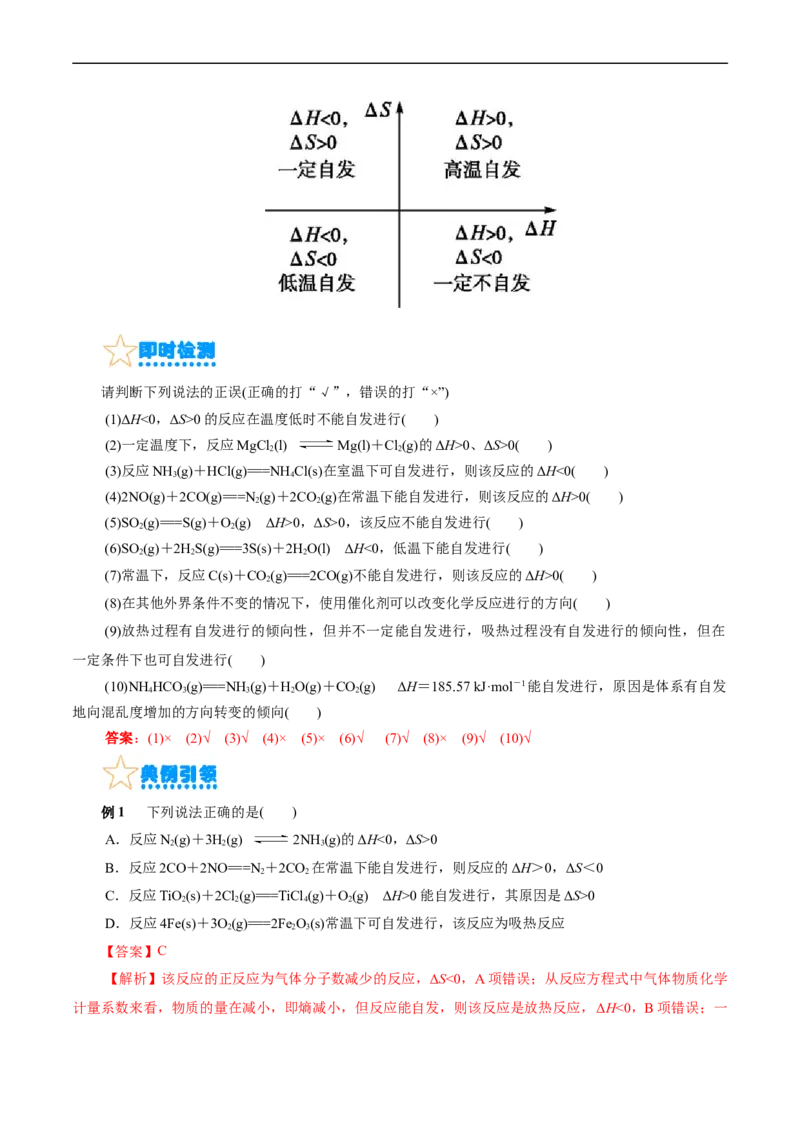
焓变、熵变和温度对化学反应方向的影响
ΔH ΔS ΔH-TΔS 反应情况
- + 永远是负值 在任何温度下均自发进行
+ - 永远是正值 在任何温度下均非自发进行
+ + 低温为正,高温为负 低温时非自发,高温时自发
- - 低温为负,高温为正 低温时自发,高温时非自发请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)ΔH<0,ΔS>0的反应在温度低时不能自发进行( )
(2)一定温度下,反应MgCl (l) Mg(l)+Cl(g)的ΔH>0、ΔS>0( )
2 2
(3)反应NH (g)+HCl(g)===NHCl(s)在室温下可自发进行,则该反应的ΔH<0( )
3 4
(4)2NO(g)+2CO(g)===N (g)+2CO(g)在常温下能自发进行,则该反应的ΔH>0( )
2 2
(5)SO (g)===S(g)+O(g) ΔH>0,ΔS>0,该反应不能自发进行( )
2 2
(6)SO (g)+2HS(g)===3S(s)+2HO(l) ΔH<0,低温下能自发进行( )
2 2 2
(7)常温下,反应C(s)+CO(g)===2CO(g)不能自发进行,则该反应的ΔH>0( )
2
(8)在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向( )
(9)放热过程有自发进行的倾向性,但并不一定能自发进行,吸热过程没有自发进行的倾向性,但在
一定条件下也可自发进行( )
(10)NH HCO (g)===NH(g)+HO(g)+CO(g) ΔH=185.57 kJ·mol-1能自发进行,原因是体系有自发
4 3 3 2 2
地向混乱度增加的方向转变的倾向( )
答案:(1)× (2)√ (3)√ (4)× (5)× (6)√ (7)√ (8)× (9)√ (10)√
例1 下列说法正确的是( )
A.反应N(g)+3H(g) 2NH (g)的ΔH<0,ΔS>0
2 2 3
B.反应2CO+2NO===N +2CO 在常温下能自发进行,则反应的ΔH>0,ΔS<0
2 2
C.反应TiO(s)+2Cl(g)===TiCl (g)+O(g) ΔH>0能自发进行,其原因是ΔS>0
2 2 4 2
D.反应4Fe(s)+3O(g)===2Fe O(s)常温下可自发进行,该反应为吸热反应
2 2 3
【答案】C
【解析】该反应的正反应为气体分子数减少的反应,ΔS<0,A项错误;从反应方程式中气体物质化学
计量系数来看,物质的量在减小,即熵减小,但反应能自发,则该反应是放热反应,ΔH<0,B项错误;一个吸热反应如果能自发进行,则该反应一定是熵增大反应,C项正确;该反应的气体分子数减小,即熵减
小,但反应能自发,说明反应一定为放热反应,D项错误。
例2 下列关于焓判据和熵判据的说法中,不正确的是( )
A.放热的自发过程可能是熵减小的过程,吸热的自发过程一定为熵增加的过程
B.4Fe(OH) (s)+2HO(l)+O(g)=4Fe(OH) (s) ΔH=-444.3kJ·mol-1ΔS=-280.1J·mol-1·K-1在常温常压下能自
2 2 2 3
发进行
C.在室温下碳酸钙的分解反应不能自发进行,但同样是这个吸热反应在较高温度(1200K)下则能自发
进行
D.放热过程(ΔH<0)或熵增加(ΔS>0)的过程一定是自发的
【答案】D
【解析】A项,反应自发进行的判断依据是ΔH-TΔS<0,放热的自发过程中ΔH<0,ΔS可能小于0
也可能大于0,所以放热的自发过程可能是熵减小的过程,吸热的自发过程中ΔH>0、ΔH-TΔS<0,则ΔS
必须>0,所以吸热的自发过程一定为熵增加的过程,A正确;B项,常温下T=298K,则-444.3kJ•mol-1-
298K×(-280.1J•mol-1•K-1)=-366.8302kJ/mol<0,即ΔH-TΔS<0,所以该反应在常温常压能自发进行,B正确;
C项,碳酸钙分解的方程式为CaCO (s) CaO(s)+CO (g),其中ΔH>0,ΔS>0,高温时才能满足反应自发
3 2
进行的条件ΔH-TΔS<0,所以碳酸钙的⇌分解在室温下不能自发进行,但在较高温度(1200K)下能自发进行,
C正确;D项,当ΔG=ΔH-TΔS<0时反应自发,仅ΔH<0或ΔS>0无法确保ΔG<0,即不一定自发,D
错误;故选D。
对点1 下列反应在任何温度下均能自发进行的是( )
A.2N(g)+O(g)===2N O(g) ΔH=163 kJ·mol-1
2 2 2
B.Ag(s)+Cl(g)===AgCl(s) ΔH=-127 kJ·mol-1
2
C.HgO(s)===Hg(l)+O(g) ΔH=91 kJ·mol-1
2
D.HO(l)===O(g)+HO(l) ΔH=-98 kJ·mol-1
2 2 2 2
【答案】D
【解析】对于A项,ΔH>0,ΔS<0,在任何温度下,ΔH-TΔS>0,即任何温度下反应都不能自发进行;
对于B项,ΔH<0,ΔS<0,在较低温度下,ΔH-TΔS<0,即低温下反应能自发进行;对于C项,ΔH>0,
ΔS>0,若使反应自发进行,即ΔH-TΔS<0,必须升高温度,即反应只有在较高温度时能自发进行;对于
D项,ΔH<0,ΔS>0,在任何温度下,ΔH-TΔS<0,即在任何温度下反应均能自发进行。
对点2 下表中内容与结论相对应的是( )
选项 内容 结论
A HO(g)变成HO(l) ΔS>0
2 2
B 硝酸铵溶于水可自发进行 该过程的ΔS>0