文档内容
考点 3 盐类水解
1.3年真题考点分布
考点分布
年份 卷区
盐类的水解 盐类水解的影响因素 离子浓度大小比较 综合应用
重庆 √
北京 √ √
2023
海南 √
湖南 √
海南 √
湖南 √ √
2022 江苏 √
辽宁 √
浙江 √ √
北京 √
海南 √
湖南 √
2021
辽宁 √
山东 √
浙江 √ √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于该专题主要考查:
1.盐类的水解及其影响因素
2.盐类水解的应用
3.离子浓度大小比较
【备考策略】熟练掌握盐类水解有一定限度,是可以调控的。能多角度、动态地分析盐类水解平衡,并运用平
衡移动原理解决实际问题。
【命题预测】预测2024年高考通过考查盐类水解的本质特征和应用。能运用模型解释盐类水解平衡的移动,揭
示现象的本质和规律。
考法 1 盐类水解及其规律
一、盐类水解及其规律
1.定义在溶液中盐电离出来的离子跟水电离产生的H+或OH-结合生成弱电解质的反应。
2.实质
盐电离―→―→
破坏了水的电离平衡―→水的电离程度增大―→溶液呈碱性、酸性或中性
3.特点
→水解反应是可逆反应
|
→水解反应是酸碱中和反应的逆反应
|
→水解反应程度很微弱
4.规律
有弱才水解,越弱越水解;谁强显谁性,同强显中性。
是否 溶液的
盐的类型 实例 水解的离子 溶液的pH
水解 酸碱性
强酸强碱盐 NaCl、KNO 否 中性 pH=7
3
强酸弱碱盐 NH Cl、Cu(NO ) 是 NH、Cu2+ 酸性 pH<7
4 3 2
弱酸强碱盐 CHCOONa、NaCO 是 CHCOO-、CO 碱性 pH>7
3 2 3 3
5.盐类水解离子方程式的书写要求
(1)一般来说,盐类水解的程度不大,应该用可逆号“ 表示。盐类水解一般不会产生沉淀和气体,所以不用
符号“↓”和“↑”表示水解产物。
(2)多元弱酸盐的水解是分步进行的,水解离子方程式要分步表示。
(3)多元弱碱阳离子的水解也是分步进行的,但通常简化为一步表示。
盐的类型 实例 水解的离子方程式
一元弱酸 NH 4 Cl NH+ 4 + H 2 O ⇌ NH 3 ·H 2 O + H+
盐/弱碱盐
CH 3 COONa CH 3 COO- + H 2 O ⇌ CH 3 COOH + OH-
Na 2 CO 3 CO 3 2- + H 2 O ⇌ HCO 3 - + OH- ;HCO 3 - + H 2 O ⇌ H 2 CO 3 + OH-
多元弱酸盐
Na 2 S S2- + H 2 O ⇌ HS- + OH- ;HS- + H 2 O ⇌ H 2 S + OH-
FeCl 3 Fe3+ + 3H 2 O ⇌ Fe(OH) 3 + 3H+
多元弱碱盐
CuCl 2 Cu2+ + 2H 2 O ⇌ Cu(OH) 2 + 2H+
(4)水解分别显酸性和碱性的离子组由于相互促进水解程度较大,书写时要用“===”“↑” “↓”等。
【方法技巧】盐类水解的规律及拓展应用
(1)强酸的酸式盐只电离,不水解,溶液呈酸性。
如NaHSO 溶液中:NaHSO===Na++H++SO。
4 4
(2)弱酸的酸式盐溶液的酸碱性,取决于酸式酸根离子的电离程度和水解程度的相对大小。
①若电离程度小于水解程度,则溶液呈碱性。如NaHCO 溶液中:HCO H++CO(次要),HCO+HO HCO+OH-(主要)。
3 2 2 3
同类离子还有HS-、HPO。
②若电离程度大于水解程度,则溶液呈酸性。
如NaHSO 溶液中:HSO H++SO(主要),HSO+HO HSO +OH-(次要)。
3 2 2 3
同类离子还有HPO。
2
(3)相同条件下的水解程度
①正盐>相应酸式盐。
如相同条件下水解程度:CO>HCO。
②水解相互促进的盐>单独水解的盐>水解相互抑制的盐。
如相同条件下NH的水解程度:(NH )CO>(NH)SO >(NH)Fe(SO )。
4 2 3 4 2 4 4 2 4 2
(4)弱酸弱碱盐中的阴、阳离子都水解,其溶液的酸碱性取决于弱酸阴离子和弱碱阳离子水解程度的相对大小。
当K =K (K为电离常数)时,溶液呈中性,如CHCOONH;当K >K 时,溶液呈酸性,如HCOONH ;当
酸 碱 3 4 酸 碱 4
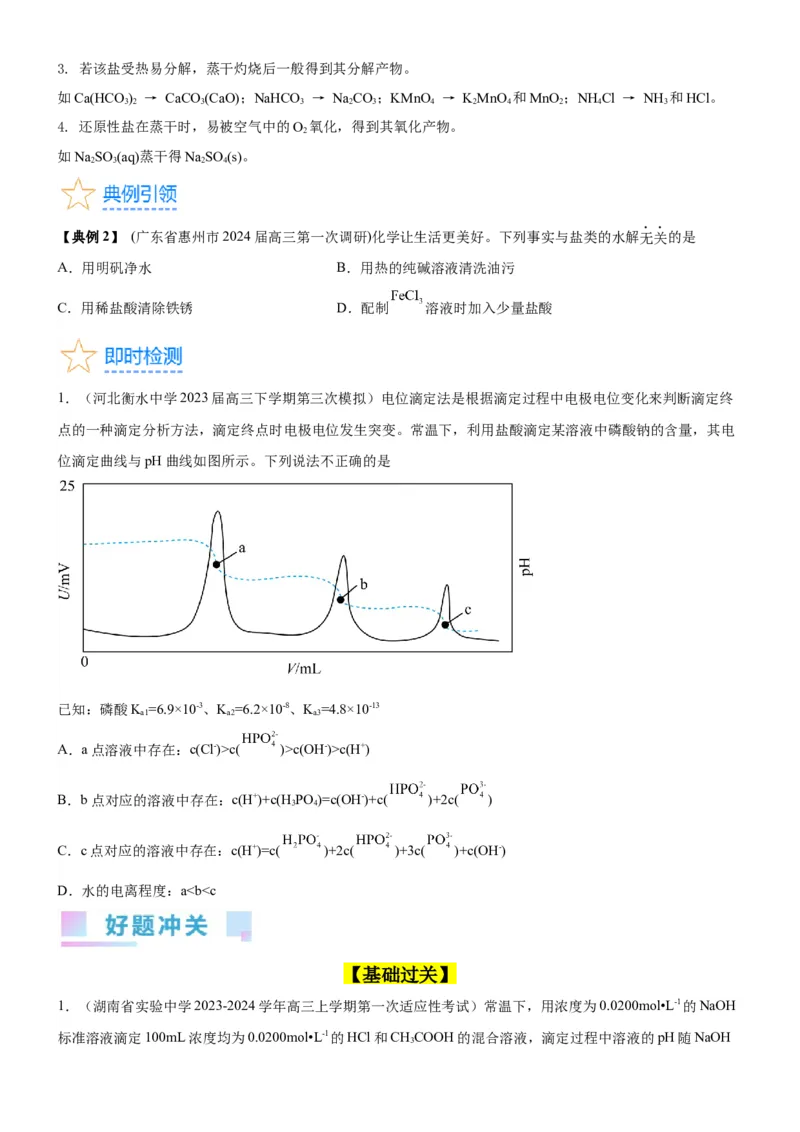
K c( )>c(OH-)>c(H+)
B.b点对应的溶液中存在:c(H+)+c(H PO )=c(OH-)+c( )+2c( )
3 4
C.c点对应的溶液中存在:c(H+)=c( )+2c( )+3c( )+c(OH-)
D.水的电离程度:ab>a>d
6.(河北省保定市定州中学2023届高三下学期模拟)常温下,某实验人员在两个相同的容器中分别加入
20mL0.2mol·L-1NaA溶液和40mL0.1mol·L-1NaHA溶液,再分别用0.2mol·L-1盐酸滴定,利用pH计和压力传感
2
器检测,绘制曲线如图所示。(已知HA溶液达到某浓度后,会放出一定量气体,溶液体积变化可忽略不计)
2下列说法不正确的是
A.图中曲线乙和丙代表向NaHA溶液中滴加盐酸
B.由图可知,K (H A)×K (H A)>K
a1 2 a2 2 w
C.根据pHV(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂
D.a点溶液中存在:c(Na+)+c(H+)>2c(A2-)+c(HA-)+c(OH-)
7.(辽宁省大连市第八中学2023届高三高考适应性测试)常温时,分别向一元酸 溶液和 溶液中滴加
溶液, 与 的关系如图所示[ 表示 或 ]。已知常温时, 。
下列说法正确的是
A.曲线①表示 与 的关系
B.一元酸 的电离平衡常数
C.对于曲线②的溶液,N点水的电离程度大于M点
D.M点时,对于 溶液:
8.(浙江省金丽衢十二校2022-2023学年高三第一次联考)下列物质的水溶液呈碱性的是
A.NaCl B.B(OH) C.NaHCO D.NaHSO
3 3 4
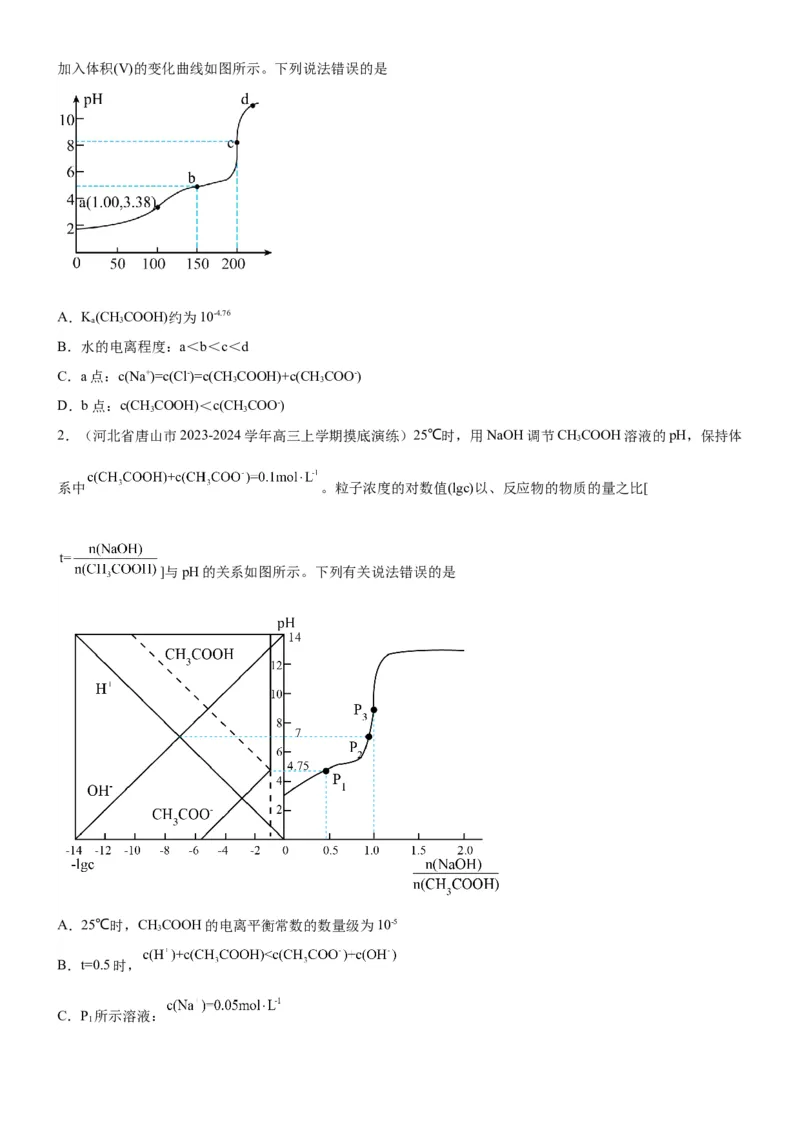
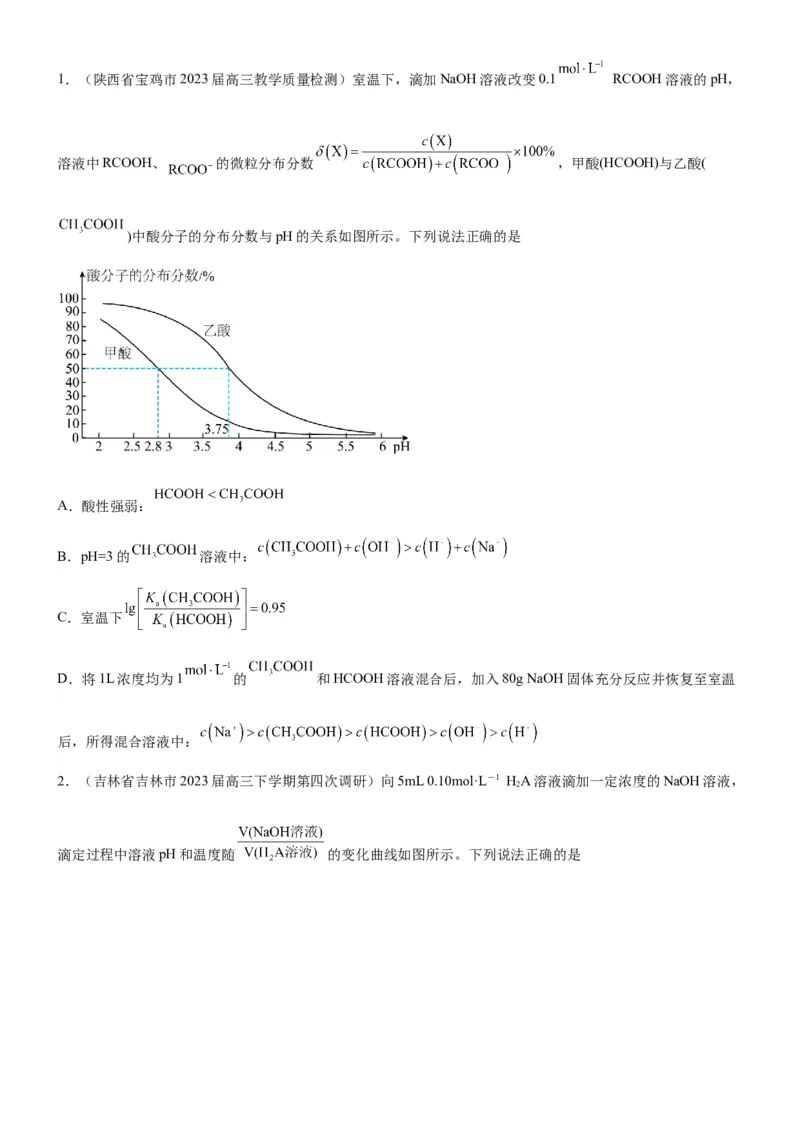
【能力提升】1.(陕西省宝鸡市2023届高三教学质量检测)室温下,滴加NaOH溶液改变0.1 RCOOH溶液的pH,
溶液中RCOOH、 的微粒分布分数 ,甲酸(HCOOH)与乙酸(
)中酸分子的分布分数与pH的关系如图所示。下列说法正确的是
A.酸性强弱:
B.pH=3的 溶液中:
C.室温下
D.将1L浓度均为1 的 和HCOOH溶液混合后,加入80g NaOH固体充分反应并恢复至室温
后,所得混合溶液中:
2.(吉林省吉林市2023届高三下学期第四次调研)向5mL 0.10mol·L-1 HA溶液滴加一定浓度的NaOH溶液,
2
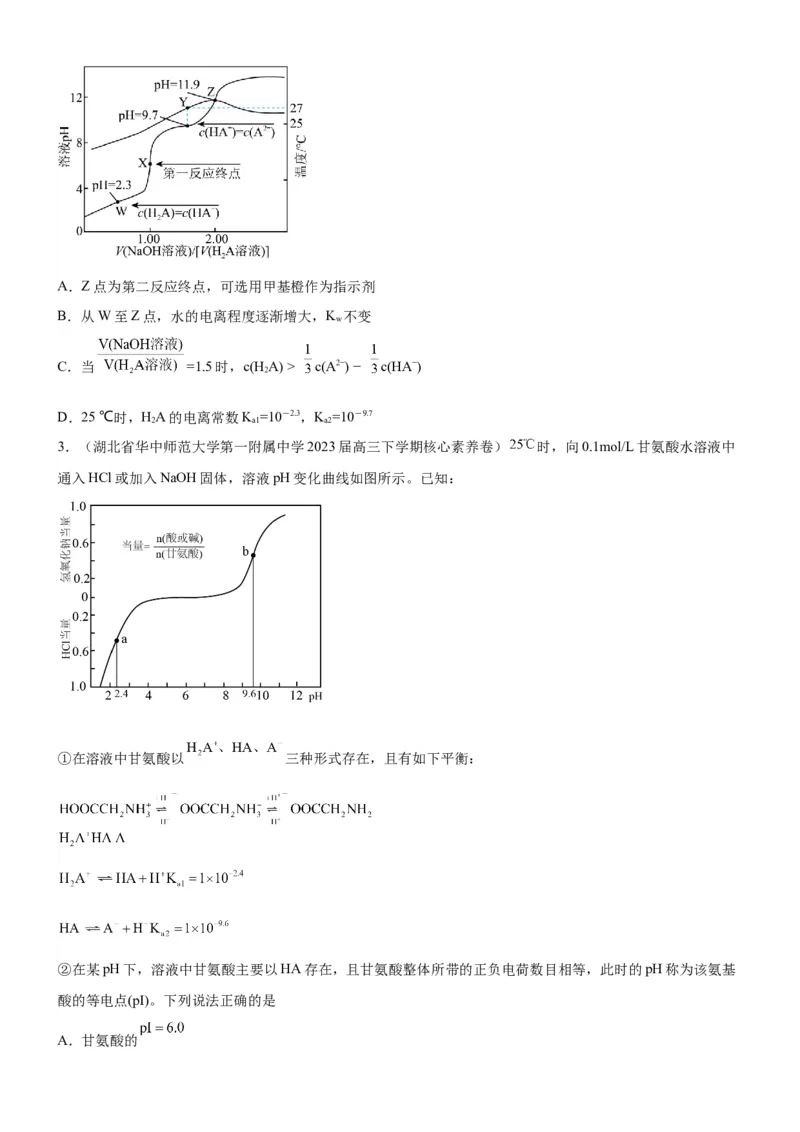
滴定过程中溶液pH和温度随 的变化曲线如图所示。下列说法正确的是A.Z点为第二反应终点,可选用甲基橙作为指示剂
B.从W至Z点,水的电离程度逐渐增大,K 不变
w
C.当 =1.5时,c(HA) > c(A2−) − c(HA−)
2
D.25 ℃时,HA的电离常数K =10-2.3,K =10-9.7
2 a1 a2
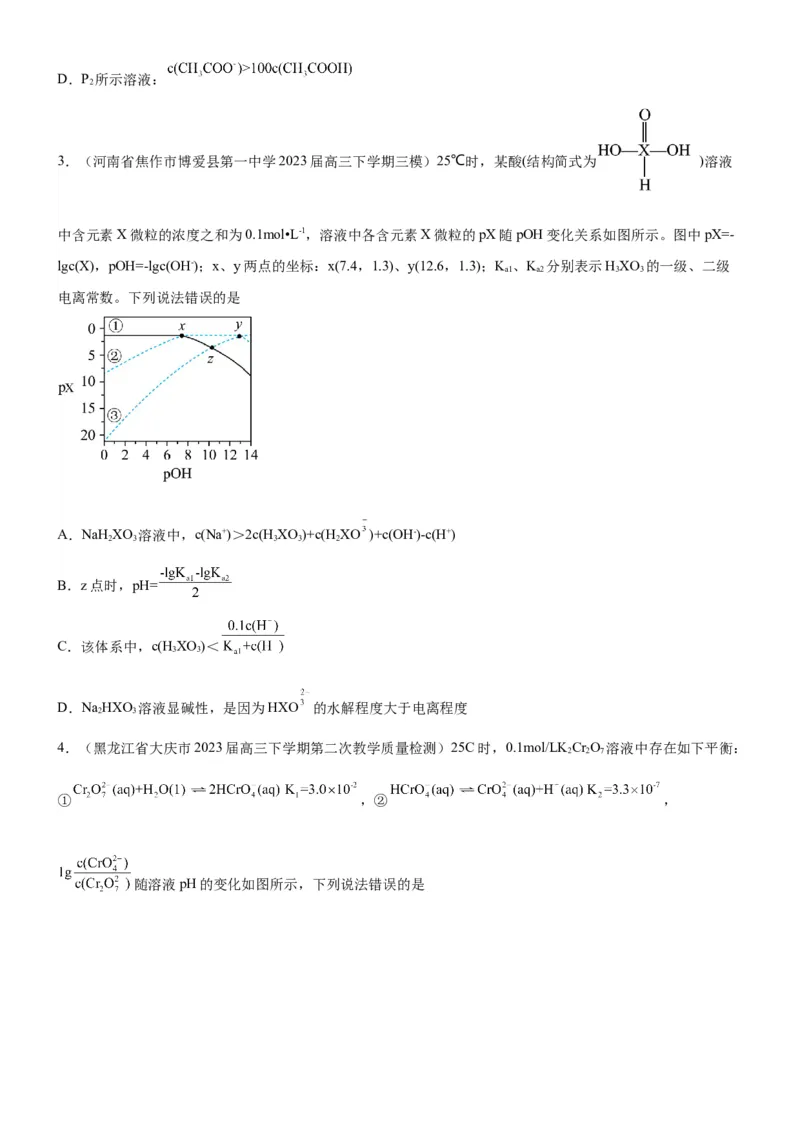
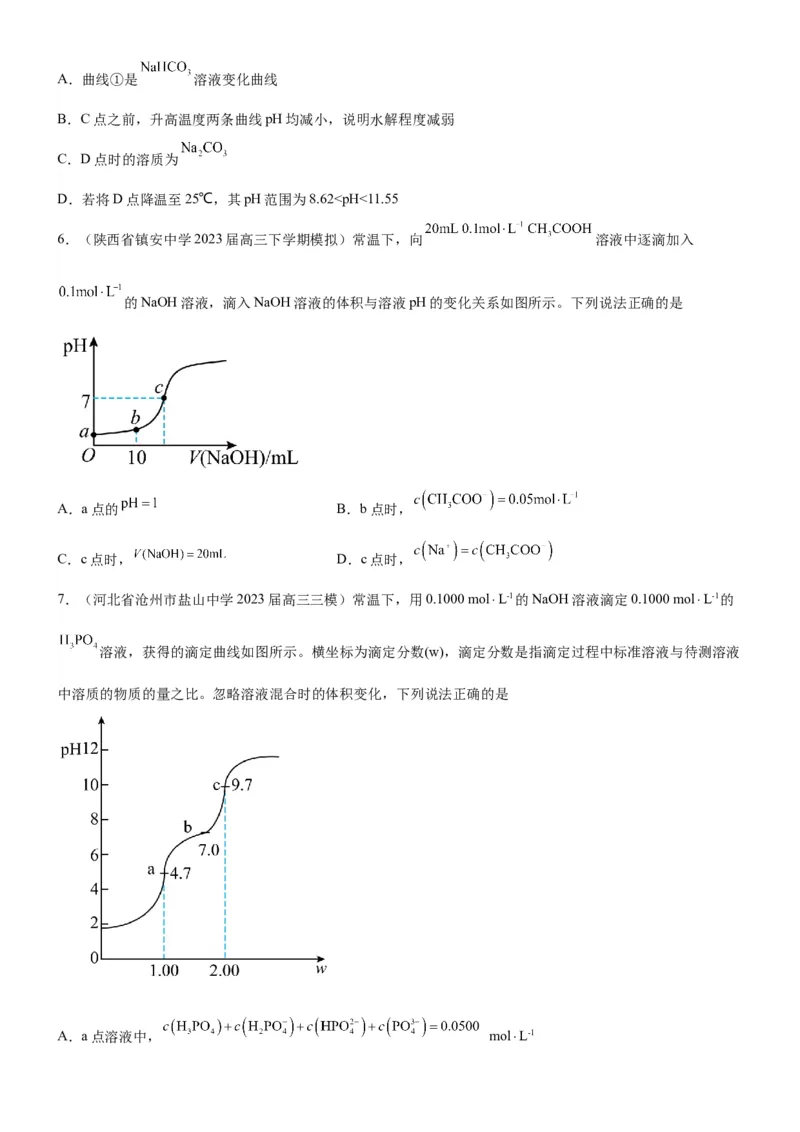
3.(湖北省华中师范大学第一附属中学2023届高三下学期核心素养卷) 时,向0.1mol/L甘氨酸水溶液中
通入HCl或加入NaOH固体,溶液pH变化曲线如图所示。已知:
①在溶液中甘氨酸以 三种形式存在,且有如下平衡:
②在某pH下,溶液中甘氨酸主要以HA存在,且甘氨酸整体所带的正负电荷数目相等,此时的pH称为该氨基
酸的等电点(pI)。下列说法正确的是
A.甘氨酸的B.
C.a点溶液中,
D.b点NaOH当量=0.5
4.(江苏省南通市如皋市2024届高三上学期期初考试押题卷)室温下,通过下列实验探究 的性质。已
知:25℃时, 的 、 的 。
实验1:配制 溶液,测得溶液 约为12;
实验2:取 溶液,向其中加入少量 固体充分搅拌,一段时间后过滤。向滤渣中加
入足量稀盐酸,固体完全溶解;
实验3:取 溶液,向其中缓慢滴入等体积 稀盐酸。
下列说法正确的是
A.实验1所得溶液中,
B.根据实验2,可推测
C.实验3反应后溶液中存在:
D.25℃时,反应 的平衡常数
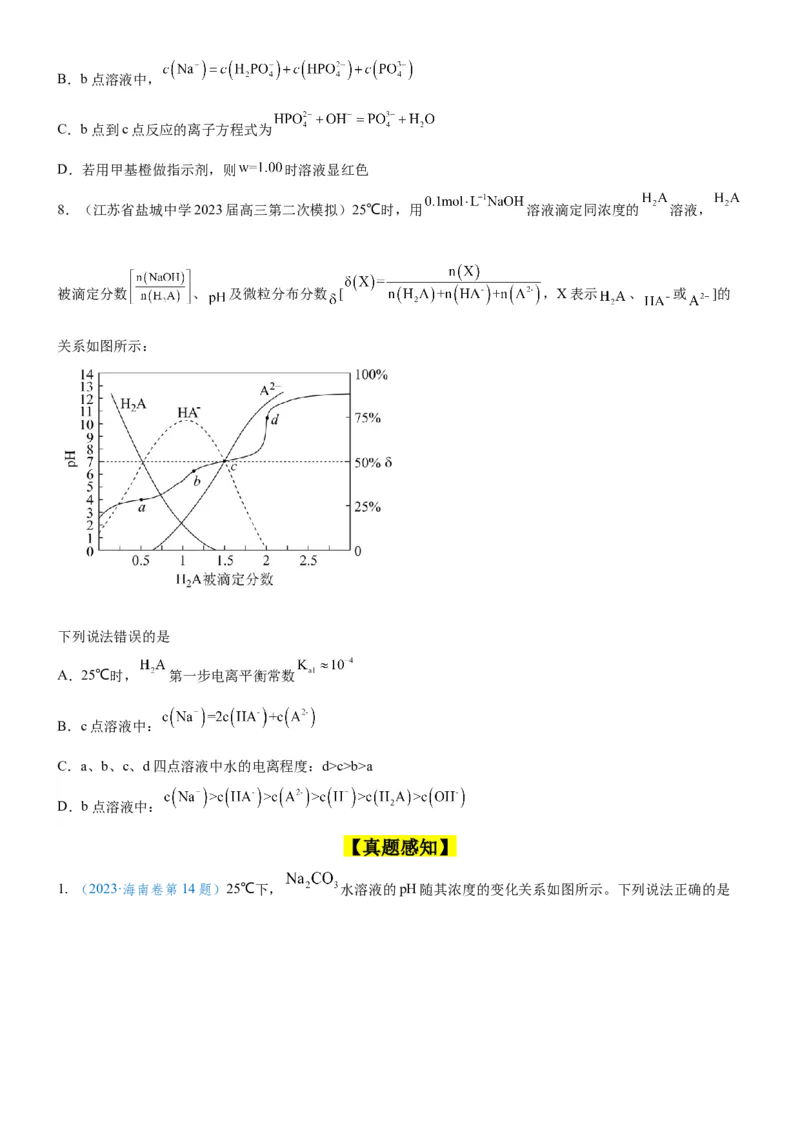
5.(河北省衡水市第二中学2023届高三下学期三模)实验测得等物质的量浓度的 和 溶液的
pH随温度变化如图所示。下列说法正确的是A.曲线①是 溶液变化曲线
B.C点之前,升高温度两条曲线pH均减小,说明水解程度减弱
C.D点时的溶质为
D.若将D点降温至25℃,其pH范围为8.62c>b>a
D.b点溶液中:
【真题感知】
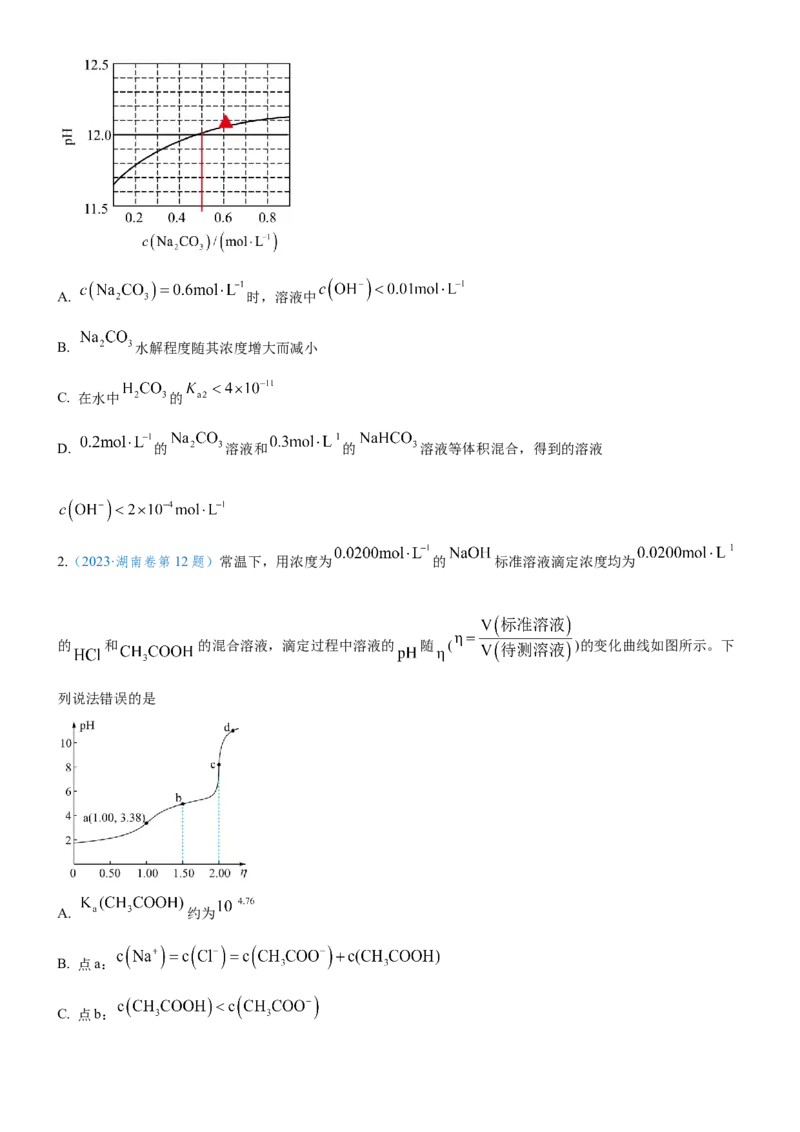
1. (2023·海南卷第14题)25℃下, 水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是A. 时,溶液中
B. 水解程度随其浓度增大而减小
C. 在水中 的
D. 的 溶液和 的 溶液等体积混合,得到的溶液
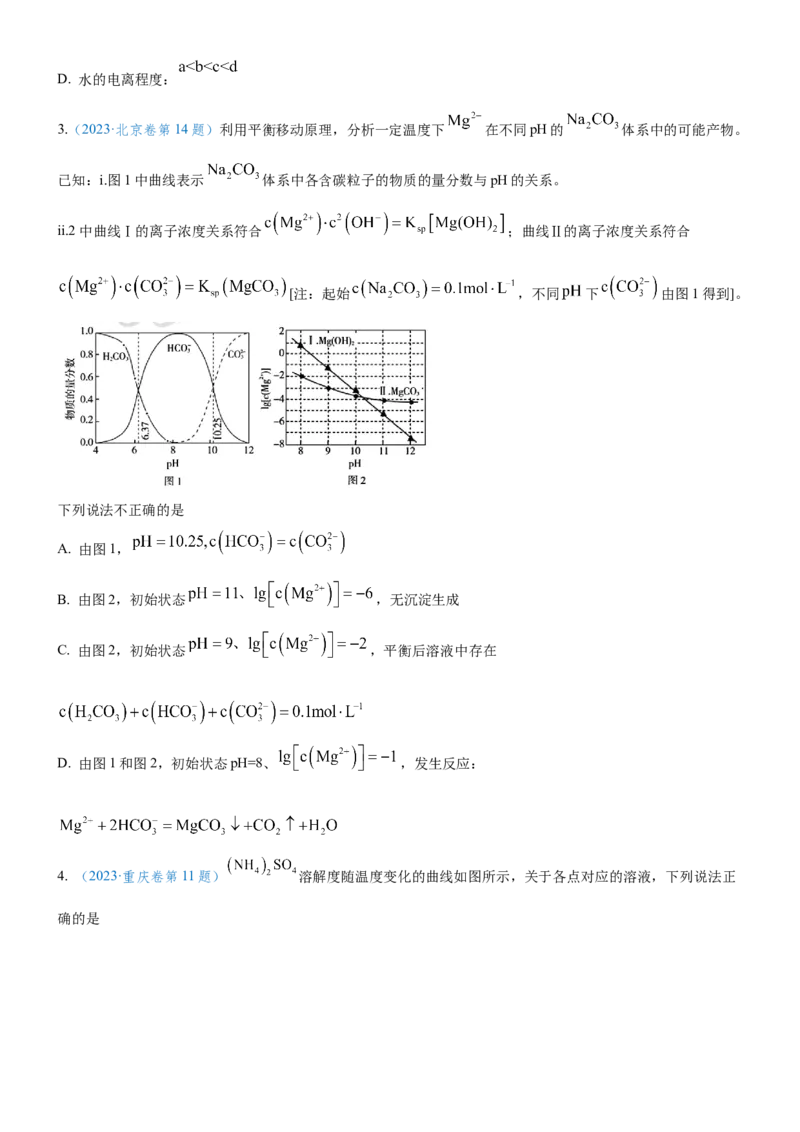
2.(2023·湖南卷第12题)常温下,用浓度为 的 标准溶液滴定浓度均为
的 和 的混合溶液,滴定过程中溶液的 随 ( )的变化曲线如图所示。下
列说法错误的是
A. 约为
B. 点a:
C. 点b:D. 水的电离程度:
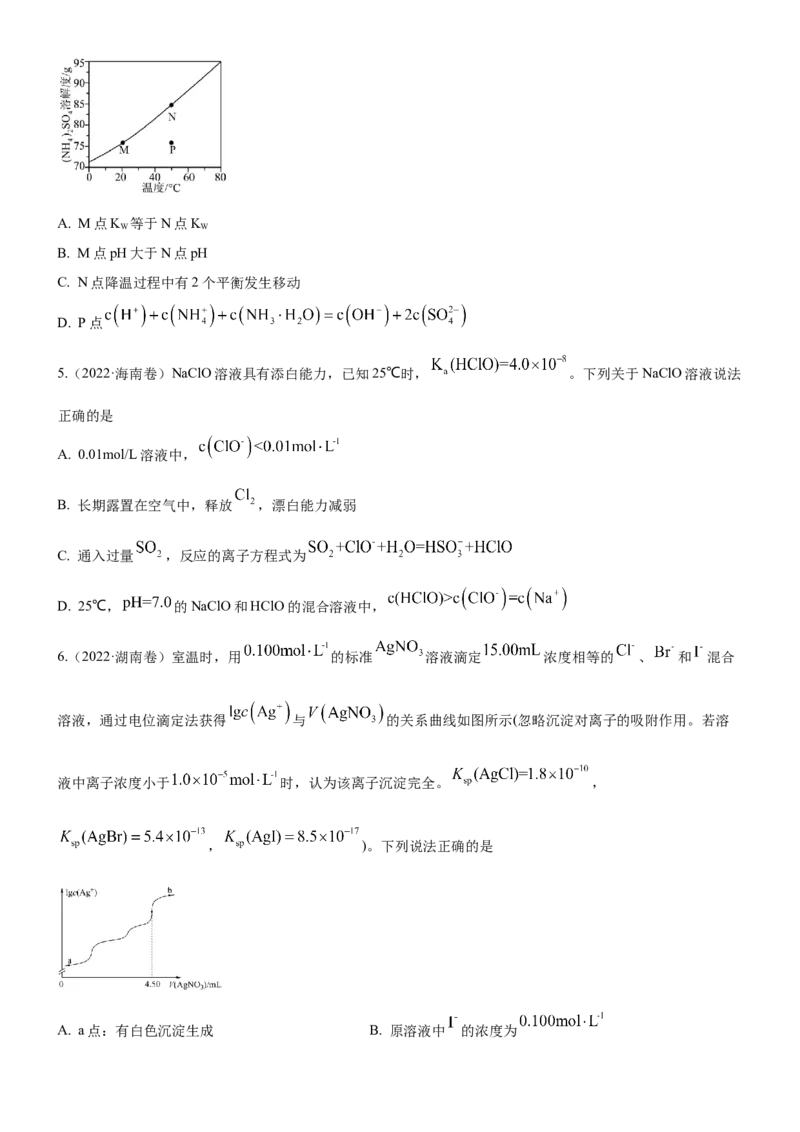
3.(2023·北京卷第14题)利用平衡移动原理,分析一定温度下 在不同pH的 体系中的可能产物。
已知:i.图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系。
ii.2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 ,不同 下 由图1得到]。
下列说法不正确的是
A. 由图1,
B. 由图2,初始状态 ,无沉淀生成
C. 由图2,初始状态 ,平衡后溶液中存在
D. 由图1和图2,初始状态pH=8、 ,发生反应:
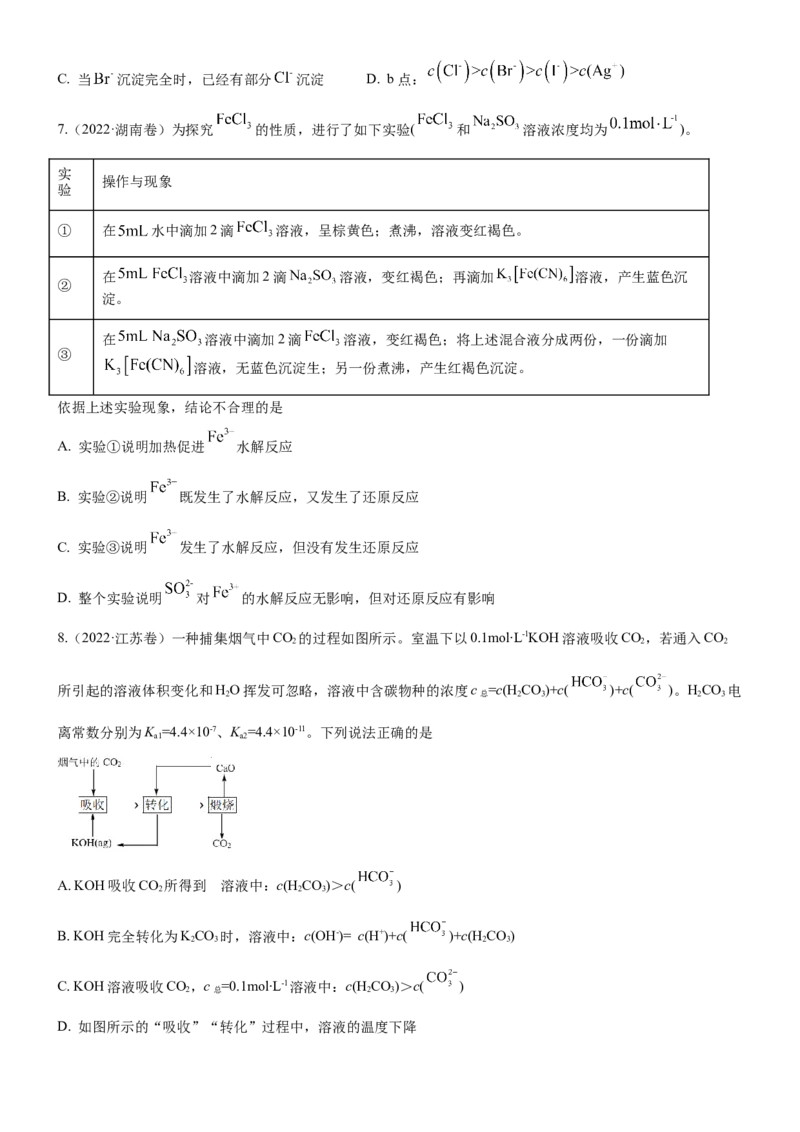
4. (2023·重庆卷第11题) 溶解度随温度变化的曲线如图所示,关于各点对应的溶液,下列说法正
确的是A. M点K 等于N点K
W W
B. M点pH大于N点pH
C. N点降温过程中有2个平衡发生移动
D. P点
5.(2022·海南卷)NaClO溶液具有添白能力,已知25℃时, 。下列关于NaClO溶液说法
正确的是
A. 0.01mol/L溶液中,
B. 长期露置在空气中,释放 ,漂白能力减弱
C. 通入过量 ,反应的离子方程式为
D. 25℃, 的NaClO和HClO的混合溶液中,
6.(2022·湖南卷)室温时,用 的标准 溶液滴定 浓度相等的 、 和 混合
溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸附作用。若溶
液中离子浓度小于 时,认为该离子沉淀完全。 ,
, )。下列说法正确的是
A. a点:有白色沉淀生成 B. 原溶液中 的浓度为C. 当 沉淀完全时,已经有部分 沉淀 D. b点:
7.(2022·湖南卷)为探究 的性质,进行了如下实验( 和 溶液浓度均为 )。
实
操作与现象
验
① 在 水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色。
在 溶液中滴加2滴 溶液,变红褐色;再滴加 溶液,产生蓝色沉
②
淀。
在 溶液中滴加2滴 溶液,变红褐色;将上述混合液分成两份,一份滴加
③
溶液,无蓝色沉淀生;另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是
A. 实验①说明加热促进 水解反应
B. 实验②说明 既发生了水解反应,又发生了还原反应
C. 实验③说明 发生了水解反应,但没有发生还原反应
D. 整个实验说明 对 的水解反应无影响,但对还原反应有影响
8.(2022·江苏卷)一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收CO,若通入CO
2 2 2
所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度c =c(H CO)+c( )+c( )。HCO 电
2 总 2 3 2 3
离常数分别为K =4.4×10-7、K =4.4×10-11。下列说法正确的是
a1 a2
的
A. KOH吸收CO 所得到 溶液中:c(H CO)>c( )
2 2 3
B. KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c( )+c(H CO)
2 3 2 3
C. KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c( )
2 总 2 3
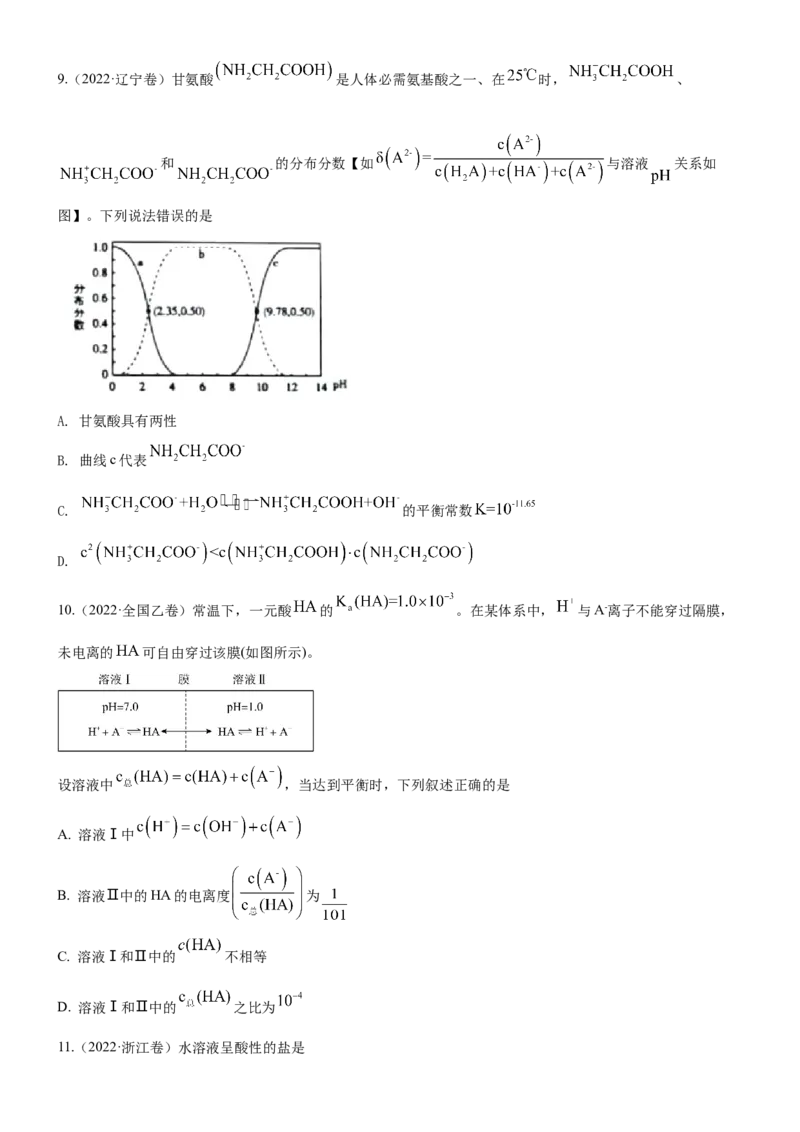
D. 如图所示的“吸收”“转化”过程中,溶液的温度下降9.(2022·辽宁卷)甘氨酸 是人体必需氨基酸之一、在 时, 、
和 的分布分数【如 与溶液 关系如
图】。下列说法错误的是
A. 甘氨酸具有两性
B. 曲线c代表
C. 的平衡常数
D.
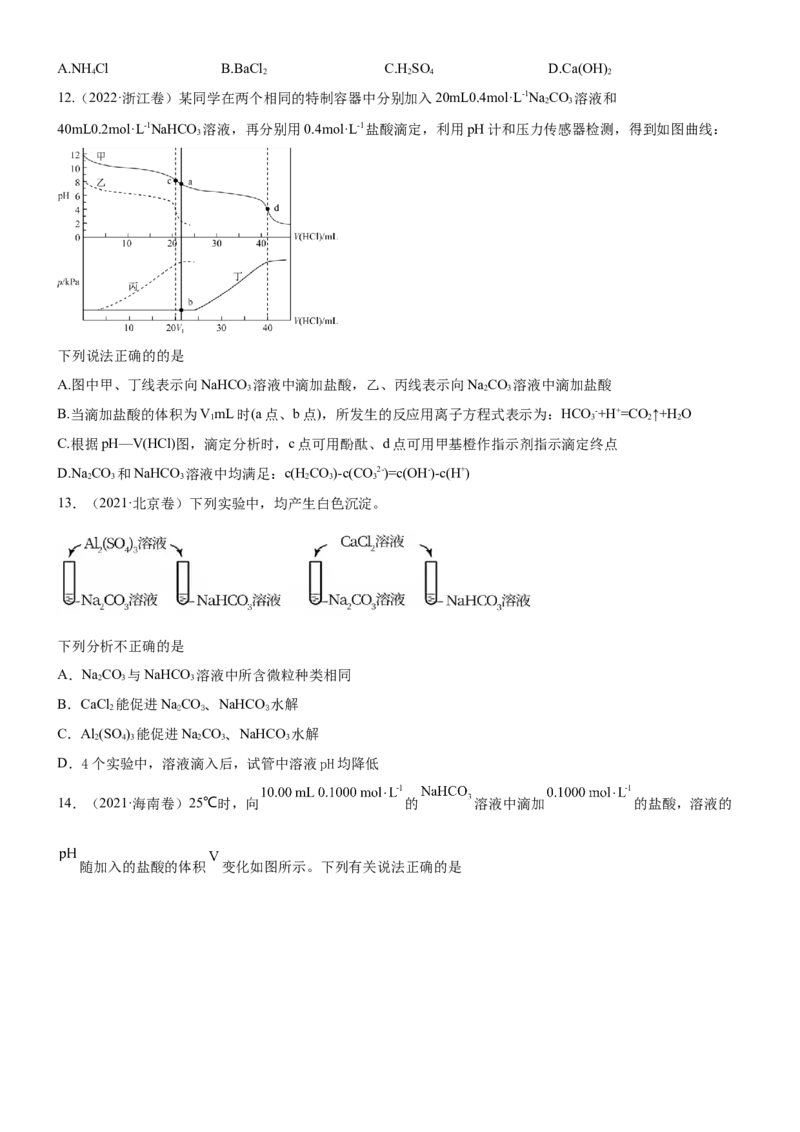
10.(2022·全国乙卷)常温下,一元酸 的 。在某体系中, 与A-离子不能穿过隔膜,
未电离的 可自由穿过该膜(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是
A. 溶液Ⅰ中
B. 溶液Ⅱ中的HA的电离度 为
C. 溶液Ⅰ和Ⅱ中的 不相等
D. 溶液Ⅰ和Ⅱ中的 之比为
11.(2022·浙江卷)水溶液呈酸性的盐是A.NH Cl B.BaCl C.HSO D.Ca(OH)
4 2 2 4 2
12.(2022·浙江卷)某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和
2 3
40mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲线:
3
下列说法正确的的是
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO -+H+=CO ↑+H O
1 3 2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO2-)=c(OH-)-c(H+)
2 3 3 2 3 3
13.(2021·北京卷)下列实验中,均产生白色沉淀。
下列分析不正确的是
A.NaCO 与NaHCO 溶液中所含微粒种类相同
2 3 3
B.CaCl 能促进NaCO、NaHCO 水解
2 2 3 3
C.Al (SO ) 能促进NaCO、NaHCO 水解
2 4 3 2 3 3
D.4个实验中,溶液滴入后,试管中溶液pH均降低
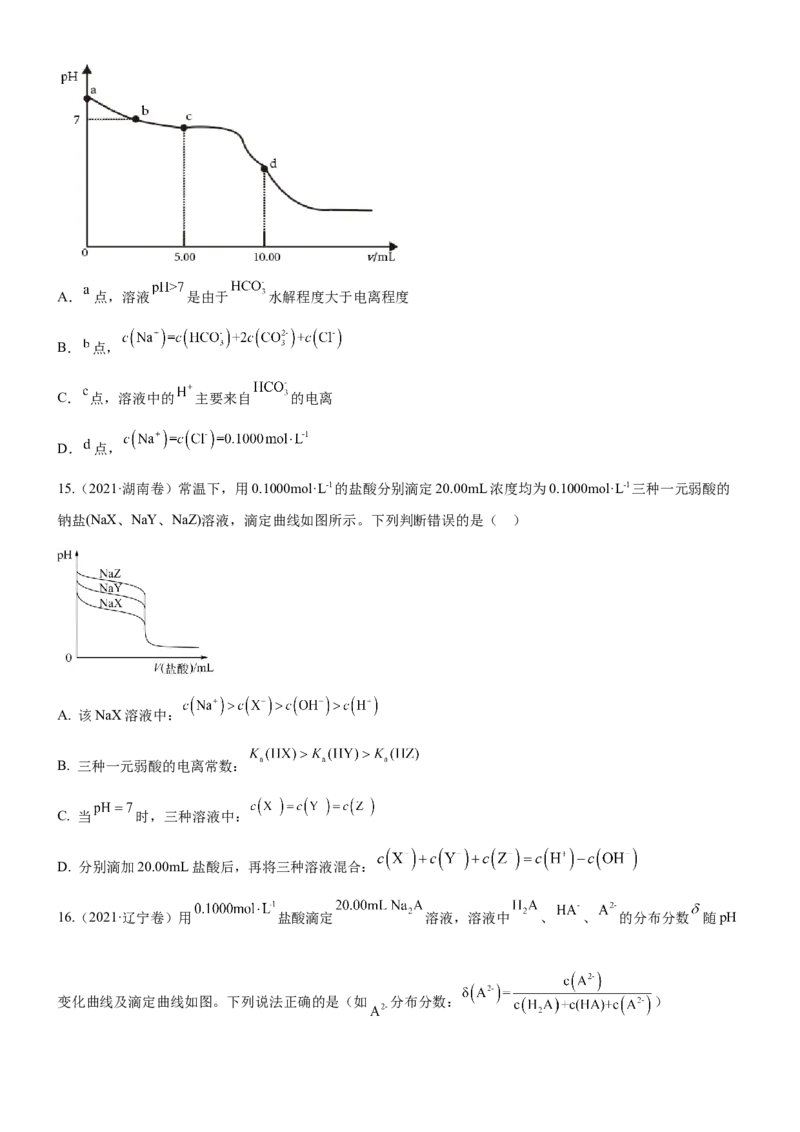
14.(2021·海南卷)25℃时,向 的 溶液中滴加 的盐酸,溶液的
随加入的盐酸的体积 变化如图所示。下列有关说法正确的是A. 点,溶液 是由于 水解程度大于电离程度
B. 点,
C. 点,溶液中的 主要来自 的电离
D. 点,
15.(2021·湖南卷)常温下,用0.1000mol·L-1的盐酸分别滴定20.00mL浓度均为0.1000mol·L-1三种一元弱酸的
钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( )
A. 该NaX溶液中:
B. 三种一元弱酸的电离常数:
C. 当 时,三种溶液中:
D. 分别滴加20.00mL盐酸后,再将三种溶液混合:
16.(2021·辽宁卷)用 盐酸滴定 溶液,溶液中 、 、 的分布分数 随pH
变化曲线及滴定曲线如图。下列说法正确的是(如 分布分数: )A. 的 为 B.c点:
C.第一次突变,可选酚酞作指示剂 D.
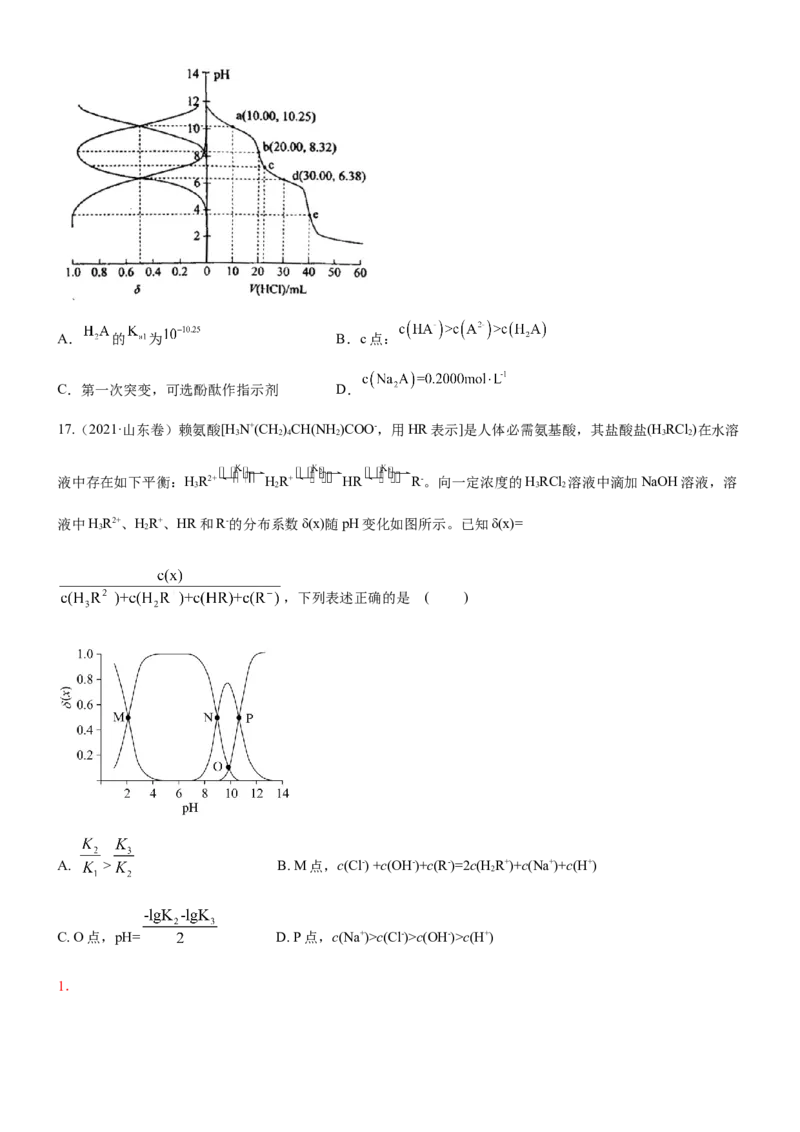
17.(2021·山东卷)赖氨酸[H N+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,其盐酸盐(H RCl )在水溶
3 2 4 2 3 2
液中存在如下平衡:HR2+ HR+ HR R-。向一定浓度的HRCl 溶液中滴加NaOH溶液,溶
3 2 3 2
液中HR2+、HR+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=
3 2
,下列表述正确的是 ( )
A. > B. M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C. O点,pH= D. P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
1.