文档内容
解密 04 氧化还原反应
一、单选题
1.(2022·山东济宁·高三期中)下列文献记载内容涉及氧化还原反应的是
A.《旧唐书•严震传》:“梁汉之间,刀耕火耨”
B.唐代诗人刘禹锡《浪淘沙》:“美人首饰侯王印,尽是沙中浪底来”
C.葛洪《肘后备急方》:“青蒿一握,以水二升渍,绞取汁”
D.《吕氏春秋》:“金柔锡柔,合两柔则刚"
2.(2022·陕西·汉中市龙岗学校高三阶段练习)下列过程所用的物质中,利用了其氧化性
的是
A.用SO 的水溶液吸收Br B.用锌块防止钢铁船体腐蚀
2 2
C.用FeCl 溶液腐蚀铜板 D.用铁粉防止FeSO 溶液氧化
3 4
3.(2022·北京·清华附中高三阶段练习)下列离子检验利用了氧化还原反应的是
选
待检验离子 检验试剂
项
A Fe3+ KSCN溶液
B I- Cl、淀粉溶液
2
C 稀盐酸、氯化钡溶液
SO
D
NH
浓NaOH溶液、湿润的红色石蕊试纸
A.A B.B C.C D.D
4.(2022·北京市第一六一中学高三期中)下列实验中物质的颜色变化与氧化还原反应无
关的是
A.将NaO 粉末露置在空气中,固体由淡黄色变为白色
2 2
B.向 悬浊液中滴加FeCl 溶液,固体由白色变为红褐色
3
C.向KCr O 酸性溶液中加入乙醇,溶液由橙色变为绿色
2 2 7
D.向KI溶液中通入少量氯气,溶液由无色变为棕黄色
5.(2021·内蒙古·巴彦淖尔市临河区第三中学高三阶段练习)下列反应不属于四种基本类
型反应,但属于氧化还原反应的是
A.Cu+2FeCl =2FeCl +CuCl B.HNO+KOH=KNO +H O
3 2 2 3 3 2C.2KMnO KMnO +MnO+O ↑ D.C+CO 2CO
4 2 4 2 2 2
6.(2022·宁夏·青铜峡市宁朔中学高三开学考试)下列化学反应中电子转移的表示方法正
确的是
A.
B.
C.
D.
7.(2022·黑龙江·哈尔滨七十三中高三阶段练习)赤铜矿的主要成分是氧化亚铜(Cu O),
2
辉铜矿的主要成分是硫化亚铜(Cu S),将赤铜矿与辉铜矿混合加热有如下反应:
2
Cu S+2Cu O=6Cu+SO ↑,下列对于该反应的说法正确的是
2 2 2
A.该反应中的氧化剂只有Cu O B.Cu既是氧化产物又是还原产物
2
C.Cu S在反应中只做还原剂 D.氧化产物与还原产物的质量之比为1∶6
2
8.(2022·天津市西青区杨柳青第一中学高三阶段练习)水与下列物质反应时,水表现出
氧化性的是
A. B. C. D.Na
9.(2021·海南省东方市琼西中学高三阶段练习)根据下列反应:(1)2Fe3++2I-=2Fe2++I ;
2
(2)Br +2Fe2+=2Br-+2Fe3+,判断离子的还原性由强到弱的顺序是
2
A.Br->I->Fe2+ B.I->Fe2+>Br-
C.Fe2+>I->Br- D.Br->Fe2+>I-
10.(2022·辽宁·高三阶段练习)为实现下列物质之间的转化,需要加入还原剂才能实现
的是
A. B. C. D.
11.(2022·重庆市永川北山中学校高三期中)碘元素在海水中主要以 的形式存在,几种
含碘粒子之间有如图所示的转化关系,下列说法不正确的是A.可用淀粉-KI试纸和食醋检验加碘盐中是否含有碘
B.途径①的离子方程式为:
C.由图可知氧化性:
D.途径②中若生成1 mol ,反应中转移电子10 mol
12.(2020·山西实验中学高三阶段练习)下列反应的离子方程式书写错误的是
A.Fe O 溶于过量的氢碘酸溶液中:Fe O+6H++2I-=2 Fe2++I +3H O
2 3 2 3 2 2
B.过量SO 与氨水反应:SO +NH•H O=NH +HSO
2 2 3 2
C.向明矾中加入Ba(OH) 溶液使SO 恰好沉淀完全:2Al3++6OH-+3Ba2++3SO
2
=2Al(OH) ↓+3BaSO ↓
3 4
D.酸性KMnO 溶液与HC O 溶液反应:5HC O+2MnO +6H+=2Mn2++10CO ↑+8H O
4 2 2 4 2 2 4 2 2
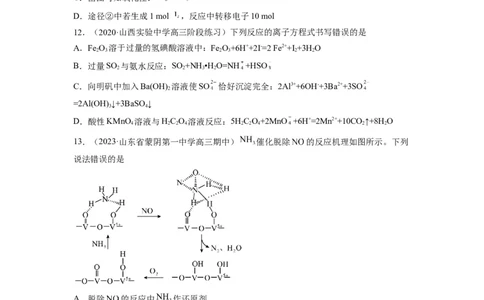
13.(2023·山东省蒙阴第一中学高三期中) 催化脱除 的反应机理如图所示。下列
说法错误的是
A.脱除 的反应中 作还原剂
B.反应过程中V元素的化合价发生变化
C.每脱除 消耗
D. 脱除 的化学方程式为:
14.(2023·江苏·姜堰中学高三阶段练习)常温下,将NO与H 的混合气体通入Ce(SO)
2 4 2
与Ce (SO ) 的混合溶液中,其物质的转化过程如图所示。下列说法不正确的是
2 4 3A.H+为该转化过程的中间产物
B.反应前后溶液中Ce3+和Ce4+的总数保持不变
C.反应I中氧化剂与还原剂的物质的量之比为2:1
D.反应II中每生成22.4LN ,转移的电子数目为4×6.02×1023
2
15.(2020·山西实验中学高三阶段练习)一定量的Fe、FeO、Fe O 、Fe O 的混合物
2 3 3 4
中加入350mL 2mol/L的稀硝酸恰好使混合物完全溶解,放出2.24L NO(标准状况),往所得
溶液中加入KSCN溶液,无红色出现;若用足量的H 在加热条件下还原相同质量的混合
2
物,所得到的铁的物质的量为
A.0.1mol B.0.225mol C.0.3mol D.0.25mol
16.(2022·山东日照·高三期中)N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.标准状况下,22.4LCCl 中含有的分子数为N
4 A
B.一定条件下,2molSO 和1molO 充分反应,转移的电子数小于4N
2 2 A
C.0.01mol•L-1的盐酸中所含有的H+的数为0.01N
A
D.1molH O 在氧化还原反应中完全反应时转移的电子数一定为2N
2 2 A
二、填空题
17.(2022·青海·海南藏族自治州高级中学高三阶段练习)亚硝酸钠( )是一种用途
广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产
生 、 和 ,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这
种废水必须处理后才能排放。处理方法之一如下: _______ _______ _______
_______ _______ _______ _______ _______
(1)请完成该化学方程式并配平。_______
(2) 中N的化合价为_______,由N的化合价推测 具有_______(填“氧化性”、
“还原性”或“氧化性、还原性”)。
(3)用上述反应来处理 并不是最佳方法,其原因是_______。从环保角度来讲,要将
转化为氮气,所用物质的_______(填“氧化性”或“还原性”)应该比 更
_______(填“强”或“弱”)。(4)下列方法不能用来区分固体 和 的是_______(填序号)。
A.分别溶于水并滴加酚酞试液 B.分别溶于水并滴加 酸化的 溶
液
C.分别加强热并收集气体检验 D.用筷子分别蘸取固体品尝味道
(5) 与 反应: ,若有0.5mol氧化剂被还
原,则被氧化的还原剂的物质的量是_______mol。
(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式
_______。
18.(2022·江苏淮安·高三期中)溶液常 用作氧化还原反应滴定的标准液,利用
氧化 制备 的装置如图所示(加热、夹持装置略):
已知: 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
回答下列问题:
(1) 的化学名称为_______。
(2)装置A中所发生反应的化学方程式为_______;其中a的作用是_______。
(3)装置C中盛装的试剂是_______。
(4)分析发现该装置有不足之处,改进的方法是_______。
(5)为测定某 固体的纯度,现用 的酸性 溶液进行滴定。(已知:
)称取 固体溶于水配成500mL溶
液,取 溶液置于锥形瓶中,用 溶液滴定至终点,消耗 溶
液V mL。滴定终点的现象为_______, 固体的纯度为_______。一、单选题
1.(2022·北京·牛栏山一中高三期中)因发生氧化还原反应使溶液pH降低的是
A.向 悬浊液中滴加 溶液,固体由白色变为红褐色
B.向 酸性溶液中加入乙醇,溶液由橙色变为绿色
C.向溴水中通入少量 气体,溴水颜色变浅
D.用明矾 处理污水
2.(2022·重庆·永州市第一中学高三阶段练习)宋代著名法医学家宋慈的《洗冤集录》中
有银针验毒的记载,“银针验毒”的原理为 ,下列说法正确的
是
A.X的化学式为AgS B.反应中X是氧化产物
C.反应中Ag和 均是还原剂 D.银针验毒时,空气中 失去电子
3.(2022·辽宁·鞍山一中高三阶段练习)下列说法正确的是
A.向100mL3mol·L-1的稀硝酸中加入5.6g铁,铁不能完全溶解
B.过氧化钠溶于水生成氢氧化钠,但过氧化钠不是碱性氧化物
C.原电池的两极发生的反应均为氧化还原反应
D.氯气与石灰乳反应:2Cl+2Ca(OH) =CaCl +CaClO +2HO
2 2 2 2 2
4.(2019·福建·三明一中高三阶段练习)如图表示吸热反应、置换反应、氧化还原反应之
间的关系,从下列选项反应中选出属于区域V的是( )
A.NaO+2CO =Na CO+O B.NaOH+HCl=NaCl+H O
2 2 2 2 3 2 2
C.2NaHO =2Na CO+H O+CO↑ D.2Na+2HO=NaOH+H ↑
3 2 3 2 2 2 2
5.(2022·全国·高三专题练习)下列单、双线桥的表示方法正确的是
A.
B.
C.
D.
6.(2022·湖北十堰·高三期中) 、 、 、 、 的氧化性依次减弱,
下列反应在水溶液中不可能发生的是A.
B.
C.
D.
7.(2022·江西·丰城市东煌学校高三期中)为了防止枪支生锈,常采用化学处理使枪支的
钢铁零件表面生成Fe O 的致密保护层-—“发蓝”。化学处理过程中,其中一步反应为。
3 4
3Fe+NaNO +5NaOH=3Na FeO+H O+ NH ↑。下列叙述不正确的是
2 2 2 2 3
A.NH 为还原产物 B.上述反应中铁被氧化
3
C.NO 的氧化性大于FeO D.反应中转移2mole-,生成NH 8.5g
3
8.(2021·湖南·株洲二中高三开学考试)对于白磷引起的中毒,硫酸铜溶液是一种解毒剂,
有关反应如下:11P+15CuSO+24H O=5Cu P+6HPO +15H SO ,关于该反应下列说法正确
4 2 3 3 4 2 4
的是
A.CuSO 既不作氧化剂,也不作还原剂
4
B.11 mol P被氧化时,该反应中有30 mol电子发生转移
C.还原性:CuSO > H PO
4 3 4
D.该反应的氧化剂和还原剂的物质的量之比是10:3
9.(2022·全国·高三专题练习)根据下列化学方程式:① 2MnO +16H++10Cl-=2Mn2+
+5Cl↑+8H O ② 2Fe2++ Cl =2Fe3++2Cl- ③ 2Fe3++Cu=2Fe2+ + Cu2+ ④Fe+Cu2+=Fe2+ + Cu;可判
2 2 2
断MnO 、Cu2+、Fe3+、Cl 的氧化性由强到弱的顺序为:
2
A.Fe3+>MnO >Cl>Cu2+ B.Cu2+> Cl >MnO >Fe3+
2 2
C.Cl>MnO > Fe3+>Cu2+ D.MnO >Cl>Fe3+>Cu2+
2 2
10.(2022·广东深圳·高三期中)我国科学家设计如下图所示“电了转移链”过程,实现
了低温条件下氧化 高效制 。
下列说法正确的是
A.该过程中, 的电子最终传递给
B.理论上, 不能被 直接氧化为C.参加反应的 和 的物质的量之比为1∶2
D.可通过 的水解制取
二、填空题
11.(2021·辽宁·丹东市教师进修学院高三期中)高铁酸钾( )是一种暗紫色固体,
低温碱性条件下比较稳定。高铁酸钾能溶于水,是一种新型、高效、多功能水处理剂。
I.工业上干法制高铁酸钾有两种方法:
方法一:反应原理为: ,将制得的
高铁酸钠进一步转化成高铁酸钾。
(1)根据上述方程式判断还原剂为___,每生成 转移的电子数为______。
方法二: 、 、 混合加热共熔生成高铁酸盐和 等产物。
(2)该反应氧化剂与还原剂的物质的量之比为______。
II.某学习小组设计如图方案制备高铁酸钾:
(3)其中第一步操作是:在 溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁
少量多次地加入上述溶液中,温度保持0℃反应1小时,则采用的合适控温方式是
___________。反应的离子方程式为___________。
(4)高铁酸钾和水发生反应,生成一种胶体能吸附杂质净水,同时还产生一种气体,写出反
应的离子方程式为___________。
(5)在低温下,向 溶液中加入饱和 溶液能析出 ,其原因是_____。
12.(2022·浙江·东阳市横店高级中学高三阶段练习)煤炭中的硫以FeS 的形式存在,在
2
有水和空气及脱硫微生物存在的条件下发生氧化还原反应,有关反应的离子方程式依次为
① ;
②_______Fe2++_______O +_______H+ _______Fe3++_______;
2
③ ;④ 。
已知:FeS 中的硫元素为-1价。
2
回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②的离子方程式配平并补充完整_______。
(2)反应③中的还原剂是_______。
(3)观察上述反应,硫元素最终转化为_______从煤炭中分离出来。
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化培烧的化学反应为
、 。若48 mol FeS 完全反应
2
耗用氧气2934.4 L(标准状况),则反应产物中Fe O 与Fe O 的物质的量之比为_______。
3 4 2 3
13.(2022·全国·高三专题练习)按要求书写离子方程式:
(1)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。在一氧化
还原反应的体系中,共有KCl、 、浓 、 、 、 、 七种
物质。在反应后的溶液中加入 (不溶于冷水),溶液又变为紫红色, 反应后变为
无色的 。写出该实验中涉及反应的离子方程式:_______。
(2)+6价铬的毒性很强,具有一定的致癌作用,需要转化为低毒的 ,再转化为不溶物除
去,废水中含有的 可以用绿矾( )除去。测得反应后的溶液中含 、
、 、 等阳离子。写出该反应的离子方程式:_______。
(3)已知:① (绿色)(强碱性条件);
② (强酸性条件)。
将 溶液滴入NaOH溶液中微热,得到透明的绿色溶液,写出反应的离子方程式:
_______。
14.(2021·江西·高三期中)氧化还原反应在工业生产、环保及科研中有广泛的应用,请
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
I.氢化亚铜(CuH)是一种难溶物质,用CuSO 溶液和“另一物质”在40~50℃时反应可生成
4
它。CuH具有的性质有:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体,
Cu+在酸性条件下发生的反应是2Cu+=Cu2++Cu。
(1)写出CuH在氯气中燃烧的化学反应方程式:___________。
(2)CuH溶解在稀盐酸中生成的气体是 ___________(填化学式)。
(3)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸
中反应的离子方程式:___________。
II.钒性能优良,用途广泛,有金属“维生素”之称。完成下列填空:
(4)将废钒催化剂(主要成分VO)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离
2 5子,该反应的化学方程式是 ______。
(5)向上述所得溶液中加入KClO 溶液,完善并配平反应的离子方程式。____
3
+_____VO2++_____=______Cl-+______VO +_____,___________。
(6)V O 能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与NaSO 溶液反应被吸收,
2 5 2 3
则 、Cl-、VO2+还原性由大到小的顺序是 ___________。
15.(2022·全国·高三专题练习)次氯酸钠溶液和二氯异氰尿酸钠(C NOClNa)都是常用
3 3 3 2
的杀菌消毒剂。 NaClO可用于制备二氯异氰尿酸钠.
(1)NaClO溶液可由低温下将Cl 缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式
2
为__________;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间
过长且见光,将会导致消毒作用减弱,其原因是__________________。
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是
否达到优质品标准。实验检测原理为
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,
加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用 NaSO 标准溶液
2 2 3
滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗NaSO 溶液20.00mL。
2 2 3
①通过计算判断该样品是否为优质品_______。(写出计算过程,
)
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值____________(填“偏高”
或“偏低”)。