文档内容
通关 06 物质结构与性质
目录
【高考预测】预测考向,总结常考点及应对的策略
【技法必备】提供方法技巧,解决问题策略
【误区点拨】点拨常见的易错点
【抢分通关】分析命题热点,把握解题技巧,精选名校模拟题
概率预测 ☆ ☆ ☆ ☆ ☆
题型预测 选择题、解答题☆ ☆ ☆ ☆ ☆
①原子核外电子的排布
②元素的电离能、电负性及微粒半径的大小比较
③“两大理论”与微粒构型
考向预测 ④分子性质与微粒间作用
⑤成键方式、晶体类型的判断
⑥有关晶体的计算
⑦解释原因类简答题
物质结构与性质的相关知识不论在必修模块还是选修模块中均处于相当重要的地位,是分析物质的
结构和性质重要的理论依据,随着新课标新高考的实施,在选择题中涉及物质结构与性质的题目增多,创
新
增大,综合性增强。本专题的考查点主要围绕原子、分子和晶体的结构与性质设置的,根据试题的外观征
以及考查模块的不同,可将物质结构与性质分为四个考查热点:一是原子、分子结构与性质;二是晶胞分
析;三是元素推断与元素周期律;四是主观题中物质结构与性质知识的考查。
技法1 微粒半径的比较(以短周期为例)
1.相同电性微粒半径大小的比较
①原子半径:左下角的钠最大
②阳离子半径:左下角的钠离子最大
③阴离子半径:左下角的磷离子最大
2.不同电性微粒半径大小的比较
①同周期:阴离子半径>阳离子半径,如Na+<Cl-
②同元素:电子数越多,微粒半径越大,如Fe2+>Fe3+③同结构:质子数越多,离子半径越小,如Na+<O2-
技法2 根据价层电子对互斥模型判断分子或离子的空间结构
1.方法I
根据上述方法I计算出σ键电子对数和中心原子上的孤电子对数,在确定了σ键电子对数和中心原子
上的孤电子对数后,可以依据下面的方法确定相应的较稳定的分子或离子的空间结构:
σ键电子对数+孤电子对数=价层电子对数⃗价层电子对相互排斥VSEPR模型⃗略去孤电子对分子的空间结构
以CO、NH +、NF 为例:
2 4 3
①CO :中心C原子的价电子为4,配位原子为氧原子,配位原子数为2,即有2对σ键电子对数,中心C
2
原子上的孤电子对数=[4-2x(8-6)]/2=0,即中心C原子无孤电子对,VSEPR模型就是分子的实际构型,价层
电子对数为2的VSEPR模型为直线形,则CO 的实际构型为直线形。
2
②NH +:中心N原子的价电子为5,配位原子为氢原子,配位原子数为4,NH +带1个正电荷,中心N原
4 4
子上的孤电子对数=[5-1-4x(2-1)]/2=0,即中心N原子无孤电子对,VSEPR模型就是分子的实际构型,价层
电子对数为4的VSEPR模型为正面体形,则NH +的实际构型为正四面体形。
4
③NF :中心N原子的价电子为5,配位原子为氟原子,配位原子数为3,不带电荷,中心N原子上的孤电
3
子对数=[5-3x(8-7)]/2=1,即中心N原子有1孤电子对,VSEPR模型略去1孤电子对才是分子的实际构型,
价层电子对数为4的VSEPR模型为正面体形,则NF 的实际构型为三角锥形。
3
2.方法II
根据上述方法II计算出价层电子对总数和中心原子上的孤电子对数,根据价层电子对总数得出VSEPR模
型,由VSEPR模型略去孤电子对就可以得出分子的实际构型。
价层电子对数⃗价层电子对相互排斥VSEPR模型⃗略去孤电子对分子的空间结构
以CO、NH +、NF 为例:
2 4 3
①CO :中心C原子的价电子为4,配位原子为氧原子,不计算配位原子数,中心C原子的价层电子对数
2
=4/2=2,中心碳原子与两个氧原子结合,故CO 中C原子孤电子对数=2-2=0,即中心C原子无孤电子对,
2
VSEPR模型就是分子的实际构型,价层电子对数为2的VSEPR模型为直线形,则CO 的实际构型为直线
2
形。
②NH +:中心N原子的价电子为5,配位原子为氢原子,配位原子数为4,NH +带1个正电荷,中心N原
4 4
子的价层电子对数=(5+4-1)/2=4,中心N原子与4个氢原子结合,故NH +中N原子孤电子对数=4-4=0,即
4
中心N原子无孤电子对,VSEPR模型就是分子的实际构型,价层电子对数为4的VSEPR模型为正面体
形,则NH +的实际构型为正四面体形。
4
③NF :中心N原子的价电子为5,配位原子为氟原子,配位原子数为3,不带电荷,中心N原子的价层电
3
子对数=(5+3)/2=4,中心N原子与3个氟原子结合,故NF 中N原子孤电子对数=4-3=1,即中心N原子有1
3
孤电子对,VSEPR模型略去1孤电子对才是分子的实际构型,价层电子对数为4的VSEPR模型为正面体
形,则NF 的实际构型为三角锥形。
3
【特别说明】①中心原子不含孤电子对的分子(或离子),VSEPR模型与分子(或离子)的空间结构一致。
②中心原子若有孤电子对,孤电子对也要占据中心原子周围的空间,并与成键电子对互相排斥,则
VSEPR模型与分子的空间结构不一致。推测分子的立体模型必须略去 VSEPR模型中的孤电子对。技法3 杂化轨道类型的判断方法
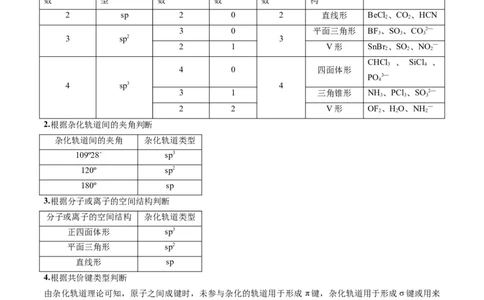
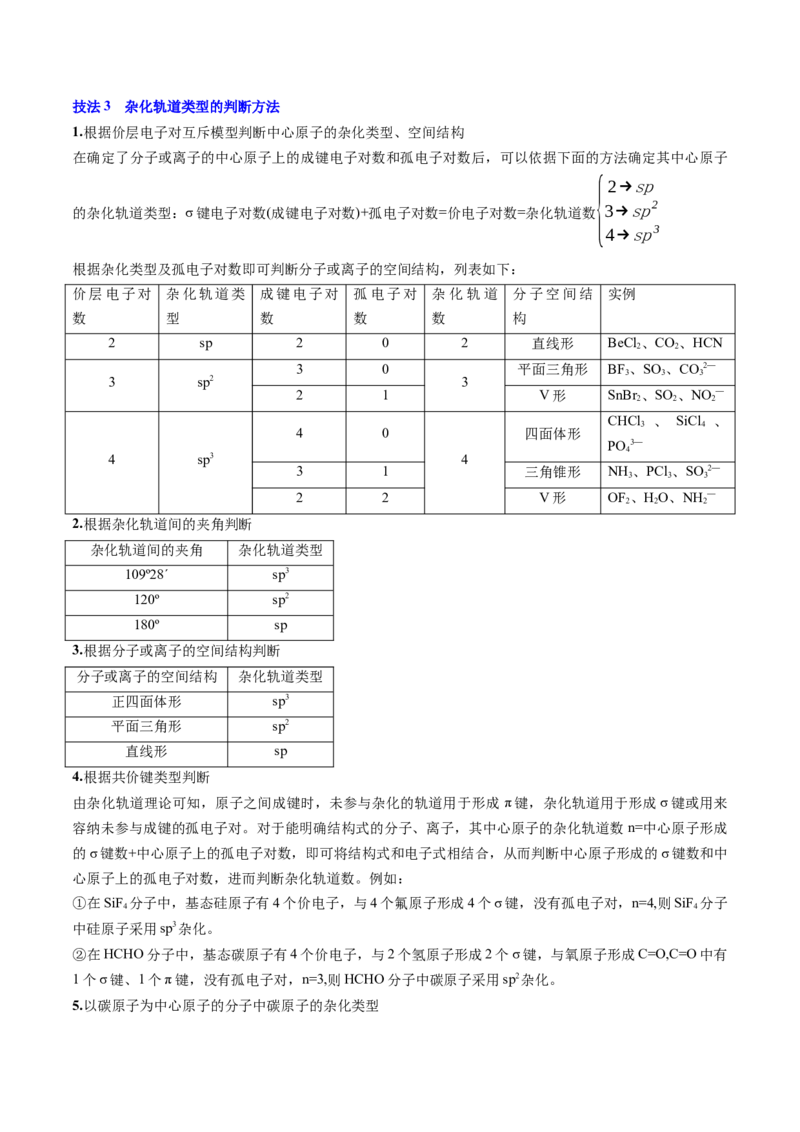
1.根据价层电子对互斥模型判断中心原子的杂化类型、空间结构
在确定了分子或离子的中心原子上的成键电子对数和孤电子对数后,可以依据下面的方法确定其中心原子
{
2→sp
的杂化轨道类型:σ键电子对数(成键电子对数)+孤电子对数=价电子对数=杂化轨道数
3→sp2
4→sp3
根据杂化类型及孤电子对数即可判断分子或离子的空间结构,列表如下:
价层电子对 杂化轨道类 成键电子对 孤电子对 杂化轨道 分子空间结 实例
数 型 数 数 数 构
2 sp 2 0 2 直线形 BeCl 、CO、HCN
2 2
3 0 平面三角形 BF、SO 、CO2—
3 3 3
3 sp2 3
2 1 V形 SnBr 、SO 、NO —
2 2 2
CHCl 、 SiCl 、
3 4
4 0 四面体形
PO 3—
4
4 sp3 4
3 1 三角锥形 NH 、PCl 、SO 2—
3 3 3
2 2 V形 OF 、HO、NH —
2 2 2
2.根据杂化轨道间的夹角判断
杂化轨道间的夹角 杂化轨道类型
109º28´ sp3
120º sp2
180º sp
3.根据分子或离子的空间结构判断
分子或离子的空间结构 杂化轨道类型
正四面体形 sp3
平面三角形 sp2
直线形 sp
4.根据共价键类型判断
由杂化轨道理论可知,原子之间成键时,未参与杂化的轨道用于形成 π键,杂化轨道用于形成σ键或用来
容纳未参与成键的孤电子对。对于能明确结构式的分子、离子,其中心原子的杂化轨道数 n=中心原子形成
的σ键数+中心原子上的孤电子对数,即可将结构式和电子式相结合,从而判断中心原子形成的σ键数和中
心原子上的孤电子对数,进而判断杂化轨道数。例如:
①在SiF 分子中,基态硅原子有4个价电子,与4个氟原子形成4个σ键,没有孤电子对,n=4,则SiF 分子
4 4
中硅原子采用sp3杂化。
②在HCHO分子中,基态碳原子有4个价电子,与2个氢原子形成2个σ键,与氧原子形成C=O,C=O中有
1个σ键、1个π键,没有孤电子对,n=3,则HCHO分子中碳原子采用sp2杂化。
5.以碳原子为中心原子的分子中碳原子的杂化类型①没有形成π键,为sp3杂化:CH、CCl 、
4 4
②形成一个π键,为sp2杂化:CH=CH 、苯(大π键)、 、
2 2
③形成两个π键,为sp杂化:CH≡CH、O=C=O(CO )、S=C=S(CS )
2 2
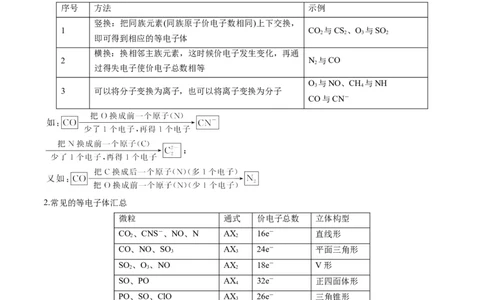
技法4 确定等电子体的方法
1.确定方法:同主族代换或同周期相邻元素替换,交换过程中注意电荷变化。变换过程中注意电荷变化,
并伴有元素种类的改变
序号 方法 示例
竖换:把同族元素(同族原子价电子数相同)上下交换,
1 CO 与CS、O 与SO
2 2 3 2
即可得到相应的等电子体
横换:换相邻主族元素,这时候价电子发生变化,再通
2 N 与CO
2
过得失电子使价电子总数相等
O 与NO、CH 与NH
3 4
3 可以将分子变换为离子,也可以将离子变换为分子
CO与CN-
2.常见的等电子体汇总
微粒 通式 价电子总数 立体构型
CO、CNS-、NO、N AX 16e- 直线形
2 2
CO、NO、SO AX 24e- 平面三角形
3 3
SO 、O、NO AX 18e- V形
2 3 2
SO、PO AX 32e- 正四面体形
4
PO、SO、ClO AX 26e- 三角锥形
3
CO、N AX 10e- 直线形
2
CH、NH AX 8e- 正四面体形
4 4
技法5 晶体类型的判断方法
1.依据构成晶体的微粒和微粒间作用力判断
由阴、阳离子形成离子键构成的晶体为离子晶体;由原子形成的共价键构成的晶体为原子晶体;由分子依
靠分子间作用力形成的晶体为分子晶体;由金属阳离子、自由电子以金属键形成的晶体为金属晶体
2.依据物质的分类判断
①活泼金属氧化物和过氧化物(如KO、NaO 等),强碱(如NaOH、KOH等),绝大多数的盐是离子晶体
2 2 2②部分非金属单质、所有非金属氢化物、部分非金属氧化物、几乎所有的酸、绝大多数有机物的晶体是分
子晶体
③常见的单质类原子晶体有金刚石、晶体硅、晶体硼等,常见的化合物类原子晶体有 SiC、SiO 、AlN、
2
BP、CaAs等
④金属单质、合金是金属晶体
3.依据晶体的熔点判断
不同类型晶体熔点大小的一般规律:原子晶体>离子晶体>分子晶体。金属晶体的熔点差别很大,如钨、铂
等熔点很高,铯等熔点很低
4.依据导电性判断
①离子晶体溶于水及熔融状态时均能导电
②原子晶体一般为非导体
③分子晶体为非导体,但分子晶体中的电解质(主要是酸和强极性非金属氢化物)溶于水时,分子内的化学
键断裂形成自由移动的离子,也能导电
④金属晶体是电的良导体
5.依据硬度和机械性能判断
一般情况下,硬度:原子晶体>离子晶体>分子晶体。金属晶体多数硬度大,但也有较小的,且具有延展性
技法6 晶胞中微粒数目的计算方法——均摊法
1.原则:晶胞中任意位置上的一个原子如果是被n个晶胞所共有,那么,每个晶胞对这个原子分得的份额
就是
2.方法:
①长方体(正方体)晶胞中不同位置的粒子数的计算
a.处于顶点上的粒子,同时为8个晶胞所共有,每个粒子有属于该晶胞
b.处于棱边上的粒子,同时为4个晶胞所共有,每个粒子有属于该晶胞
c.处于晶面上的粒子,同时为2个晶胞所共有,每个粒子有属于该晶胞
d.处于晶胞内部的粒子,则完全属于该晶胞
②非长方体晶胞中粒子视具体情况而定
三棱柱
六棱柱石墨晶胞每一层内碳原子排成六边形,其顶点(1个碳
平面型
原子)被三个六边形共有,每个六边形占
3.熟记几种常见的晶胞结构及晶胞含有的粒子数目
晶体 NaCl CsCl ZnS CaF 金刚石
2
晶体结构
4个Na 4个Ca2
1个Cs+, 4个S2-,
粒子数目 +, +, 8个C
1个Cl- 4个Zn2+
4个Cl- 8个F-
晶体 简单立方 体心立方 面心立方 氮化硼 干冰
晶体结构
粒子数目 1个原子 2个原子 4个原子 4个B,4个N 4个CO
2
技法8 原子分数坐标参数的确定方法
1.原子分数坐标参数
(1)概念:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标
(2)原子分数坐标的确定方法
①依据已知原子的坐标确定坐标系取向
②一般以坐标轴所在正方体的棱长为1个单位
③从原子所在位置分别向x、y、z轴作垂线,所得坐标轴上的截距即为该原子的分数坐标
(3)示例
z 晶胞中原子坐标
E
F
A(0,0,0), B(0,1,0), C(1,1,0), D(1,0,0),
H G
E(0,0,1), F(0,1,1), G(1,1,1), H(1,0,1),
体心:(,,), 上面心:(,,1), 下面心:(,,0),
A
B y 左面心:(,0,),右面心:(,1,), 前面心:(1,,),
D C 后面心:(0,,)
x
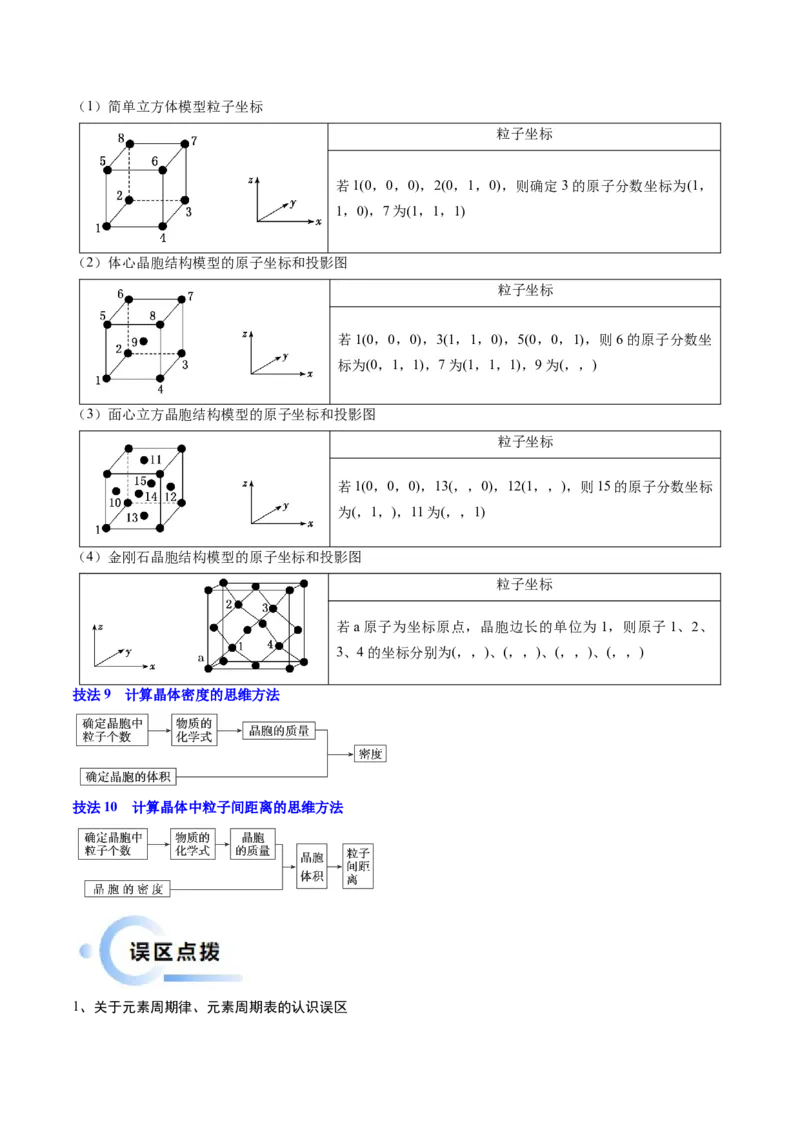
2.典型晶胞结构模型的原子分数坐标(1)简单立方体模型粒子坐标
粒子坐标
若1(0,0,0),2(0,1,0),则确定3的原子分数坐标为(1,
1,0),7为(1,1,1)
(2)体心晶胞结构模型的原子坐标和投影图
粒子坐标
若1(0,0,0),3(1,1,0),5(0,0,1),则6的原子分数坐
标为(0,1,1),7为(1,1,1),9为(,,)
(3)面心立方晶胞结构模型的原子坐标和投影图
粒子坐标
若1(0,0,0),13(,,0),12(1,,),则15的原子分数坐标
为(,1,),11为(,,1)
(4)金刚石晶胞结构模型的原子坐标和投影图
粒子坐标
若a原子为坐标原点,晶胞边长的单位为1,则原子1、2、
3、4的坐标分别为(,,)、(,,)、(,,)、(,,)
技法9 计算晶体密度的思维方法
技法10 计算晶体中粒子间距离的思维方法
1、关于元素周期律、元素周期表的认识误区(1)误认为主族元素的最高正价一定等于族序数。但是,F无正价。
(2)误认为元素的非金属性越强,其氧化物对应水化物的酸性就越强。但是,HClO、HSO 是弱酸,忽略了
2 3
关键词“最高价”。
(3)误认为同周期相邻两主族元素原子序数之差等于1。忽视了相差11(第4、5周期)和25(第6、7周期)。
(4)误认为失电子难的原子得电子的能力一定强。碳原子、稀有气体元素的原子失电子难,得电子也难。
(5)误认为得失电子多的原子,得失电子的能力一定强。
(6)误认为最高正价和最低负价绝对值相等的元素只有第ⅣA族的某些元素。忽视了第ⅠA族的H的最高
正价为+1价,最低负价为-1价。
2、分子结构性质认识的5个易错易混点
(1)误认为分子的稳定性与分子间作用力和氢键有关,其实分子的稳定性与共价键的强弱有关。
(2)误认为组成相似的分子,中心原子的杂化类型相同,其实要看其σ键和孤电子对数是否分别相同。如CO
2
和SO 中心原子的杂化方式不同,CO 分子中C原子是sp杂化,SO 分子中S原子是sp2杂化。
2 2 2
(3)误认为只要含有氢键物质的熔、沸点就高,其实不一定,分子间的氢键会使物质的熔、沸点升高,而分子内
氢键一般会使物质的熔、沸点降低。
(4)误认为只含有极性键的分子都一定是极性分子,其实不ー定。如CO2、BF3等是非极性分子。
(5)误认为杂化轨道构型和分子构型一致,其实不一定。如H2O中氧原子是sp3杂化,杂化轨道构型为四面体,
但由于分子中存在孤对电子,根据价层电子对互斥理论可知,H2O的分子构型是V形。
3、晶胞计算易错提醒
(1)在使用均摊法计算晶胞中微粒个数时,要注意晶胞的形状,不同形状的晶胞,应先分析任意位置上的一
个粒子被几个晶胞所共有。如六棱柱晶胞中,顶点、侧棱、底面上的棱、面心原子依次被6、3、4、2个晶
胞所共有。
(2)在计算晶胞中粒子个数的过程中,不是任何晶胞都可用均摊法。
(3)注意晶胞与团簇分子的区别,前者可用均摊法计算,后者不能用均摊法计算,而是直接数原子个数计算
分子式。
【热点一】原子、分子结构与性质
1.(2024·山东潍坊·一模) 在气态或非极性溶剂中均可通过氯桥键二聚成 ,熔融 和
可形成 。下列说法正确的是
A. 为极性分子 B. 中 原子的杂化方式为
C. 熔点高于 的熔点 D. 中含有 单键
【答案】C
【解析】A. 正负电荷重心重合,为非极性分子,A错误;B. 结构为 ,原子形成4个共价键,杂化方式为 ,B错误;C. 为离子化合物, 为共价化合物,则
熔点高于 的熔点,C正确;D. 结构为 , 中含有
单键,D错误;故选C。
2.(2024·河北石家庄·二模)我国的超级钢研究居于世界领先地位,某种超级钢中除铁外,还含有的元素
为锰、碳、铝、钒。下列说法错误的是
A.该超级钢所含元素中,位于p区和d区的种类数之比为2:3
B.基态Fe2+核外电子占据的最高能层的符号为M,该能层轨道表示式为
C.可用K[Fe(CN) ]溶液检验Fe2+,该物质中σ键与π键的个数比为1:1
3 6
D.由碳元素组成的富勒烯、碳纳米管和石墨烯互为同素异形体
【答案】B
【解析】A.上述五种元素中,C、Al的最外层电子都分布在p轨道,所以它们位于周期表的p区,铁、
锰、钒处于d区,位于p区和d区的种类数之比为2∶3,A正确;
B.铁原子失去2个电子形成亚铁离子,基态Fe2+核外电子占据的最高能层的符号为M,该能层轨道表示
式为 ,B错误;C.单键均为σ键,三键含有1个σ键2个π键;1个铁
离子和CN-形成6个配位键,1个CN-中存在1个1个σ键2个π键;则K[Fe(CN) ]中σ键与π键的个数比
3 6
为12∶12=1∶1,C正确;D.由碳元素组成的富勒烯、碳纳米管和石墨烯均为性质不同的碳单质,互为同素
异形体,D正确;故选B。
3.(2024·北京房山·一模)物质结构决定物质性质,下列性质不能通过元素的电负性进行解释的是
A. 的沸点高于 的沸点
B.乙烯能发生加成反应,而乙烷不能
C. 酸性大于 的酸性
D.气态氟化氢中存在 分子,而气态氯化氢中只存在 分子
【答案】B
【解析】A.O的电负性强于S,O能与H形成分子间氢键而S不能与H形成分子间氢键,故水的沸点高
于硫化氢,A不符合;B.乙烯能发生加成反应是因为含有碳碳双键,乙烷中没有不饱和键,不能发生加
成反应,与电负性无关,B符合;C.F的电负性强于Cl,-CF 的极性强于-CCl ,导致CFCOOH中羧基更
3 3 3
容易电离出氢离子,故而酸性更强,C不符合;D.F的电负性很强,使HF分子间形成氢键,导致气态
HF中存在二聚分子(HF) ,而Cl的电负性不足以使HCl形成分子间氢键,气态HCl中只有HCl分子,D不
2
符合;故答案选B。
4.(2024·北京东城·一模)下列对事实的分析正确的是
选项 事实 分析A 键角: 电负性:CS 原子半径:P>S
C 沸点:CO> CO为极性分子, 为非极性分子
D 热稳定性:HF>HCl HF中存在氮键,HCl中不存在氢键
【答案】C
【解析】A.CH 分子中的中心原子C的价层电子对数为4,无孤电子对,NH 分子中的中心原子N的价层
4 3
电子对数为4,孤电子对数为1、HO分子中的中心原子O的价层电子对数为4,孤电子对数为2,由于孤
2
电子对对成键电子对的斥力大于成键电子对对成键电子对的斥力,所以键角大小为 ,故A
错误;B.P、S位于第二周期,同一周期主族元素,从左往右第一电离能有增大的趋势,但P的3p轨道半
充满,比较稳定,其第一电离能高于同周期相邻的两种元素,故B错误;C.CO和N 结构相似,相对分
2
子质量相等,但CO为极性分子,N 为非极性分子,因此CO的沸点高于N 的沸点,故C正确;D.F、Cl
2 2
位于同一主族,同一主族从上到下,原子半径增大,元素非金属性减弱,对应氢化物的稳定性减弱,所以
热稳定性:HF>HCl,故D错误;故答案为:C。
5.(2024·河北·一模)下列有关物质结构与性质的说法正确的是
A.C=C键的键能比C—C键的大,所以碳碳双键的化学性质比碳碳单键稳定
B.某基态原子的价层电子排布为4d25s2,该原子N层上有3个空轨道
C.雪花是天空中的水汽经凝华而来的一种晶体,其六角形形状与氢键的方向性有关
D.碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
【答案】C
【解析】A. C=C键的键能比C—C键的大,但碳碳双键的键能小于碳碳单键键能的2倍,碳碳双键不稳
定,易断裂,所以碳碳双键的化学性质比碳碳单键更不稳定,A错误;B.该元素第N层的电子排布为
4s24p64d2,d有5个轨道,基态原子第N能层上还有3个空轨道,但4f上有7个轨道均没有电子,故该原
子N层上有10个空轨道,B错误;C.氢键具有方向性和饱和性,导致雪花内分子有序排列,故雪花都是
六角形形状,C正确;D.碘易溶于浓碘化钾溶液,发生的反应为I+I- ,与相似相溶原理无关,甲烷
2
是非极性分子,HO是极性分子,故CH 难溶于水可用“相似相溶”原理解释,D错误;
2 4
故答案为:C。
【热点二】晶胞分析与计算
1.(2024·北京·一模)将铁粉在NH 和H 的混合气氛中加热,可得含Fe和N的磁性材料,其晶体的晶胞
3 2
如下图,晶胞边长均为apm。下列说法不正确的是已知:1cm=1010pm,阿伏加德罗常数的值为N 。
A
A.距离N最近的Fe有6个
B.Fe之间的最近距离为
C.该晶体的密度为 g·cm-3
D.若将N置于晶胞顶点,则Fe位于体心和棱心
【答案】C
【解析】A.N位于体心,处于Fe围成的正八面体的中心,因此有6个,故A正确;B.Fe之间的最近距
离为面对角线的一半,因此为 ,故B正确;C.Fe位于晶胞中的顶点和面心,有
个,N位于体心有1个, ,故C错误;D.若将N
置于晶胞顶点,有 ,Fe位于晶胞中的体心和棱心,有 个,与原有的比值关系相同,故
D正确;故答案选C。
2.(2024·山东聊城·一模)科学工作者发现了一种光解水的催化剂,其晶胞结构如图所示,已知晶胞参数
为a pm,设 为阿伏加德罗常数的值。下列说法中错误的是
A.O位于由Ce构成的四面体空隙中
B.Ce在晶胞中的配位数为8
C.Ce与Ce最近的距离为
D.该晶体的摩尔体积
【答案】D
【分析】据“均摊法”,晶胞中,Ce的个数为 ,O的个数为8,
【解析】A.根据晶胞结构可知O位于Ce构成的正四面体空隙中 ,A正确;B.以底面面心的Ce为
例,上、下层各有4个氧原子,故在晶胞中的配位数为8,B正确;C.Ce与Ce最近的距离为Ce与Ce最
近的距离为面对角线一半,为 ,C正确;D.1个晶胞体积为a3×10-36m3,含有4个Ce和8个O,则该晶体的摩尔体积为 ×a3×10-36m3×N = ,D错误;故选D。
A
3.(2024·重庆·模拟预测)为维护国家安全和利益,2023年7月3日,我国决定对镓、锗相关物项实施出
口管制。氮化镓的晶胞结构如下图所示(晶胞参数为apm)。下列说法不正确的是
A.该物质的化学式为GaN
B.晶体结构中Ga的配位数为4
C.该晶体的密度为
D.第二周期基态原子第一电离能大于N的元素有2种
【答案】C
【解析】A.该晶胞中含4个Ga原子、4个N原子,该物质的化学式为GaN,A正确;B.与N原子最近
且等距离的Ga原子有4个,N的配位数为4,Ga的配位数也为4,B正确;C.GaN晶体的密度为
,C错误;D.与N元素位于同一周期且基态原子第一电能比N大的有F和Ne,D正确;
故选C。
4.(2024·辽宁·一模)现有一种由正离子An+、Bm+和负离子X—组成的无机固体电解质,该物质在高温相
为无序结构,低温相为有序结构,两者的结构如图,下列说法错误的是
A.n=2,m=1
B.高温相中X—的堆积方式和氯化钠中Cl—的堆积方式相同
C.低温相中An+的配位数为4
D.高温相的良好导电性与其结构中存在大量的空位有关
【答案】A
【解析】A.由题意可知,无机固体电解质低温相为有序结构,由晶胞结构可知,晶胞中位于体内的An+的
个数为4、Bm+的个数为2,位于顶点、面上、棱上和体心的X—的个数为8× +10× +4× +1=8,则晶胞的
化学式为ABX,由化合价代数和为0可得:2n+m=4,经讨论可得:m=2、n=1,故A错误;B.氯化钠晶
2 4胞中氯离子的堆积方式为立方最密堆积,由晶胞结构可知,高温相为立方晶系,晶胞中X—的堆积方式也
为立方最密堆积,所以高温相中X—的堆积方式与氯化钠中氯离子的堆积方式相同,故B正确;C.由晶胞
结构可知,低温相晶胞中A+与4个X—的距离最近,则A+的配位数为4,故C正确;D.与低温相相比可
知,高温相晶胞中A+发生迁移使空位数目增多,为阳离子的流动提供了运动通道,所以高温相的良好导电
性与其结构中存在大量的空位有关,故D正确;故选A。
5.(2024·新疆·一模)实验室可用萤石(CaF )与浓硫酸制取HF,氢氟酸可用来刻蚀玻璃,发生反应:
2
,CaF 的立方晶胞如图所示,其晶胞参数为apm。下列说法不正确的是
2
A.氢化物的稳定性:HF>H O>SiH
2 4
B.SiF、HO、SO 、SiO 四者的中心原子的杂化方式相同
4 2 2
C.CaF 的晶体密度为 (N 为阿伏伽德罗常数的值)
2 A
D.CaF 晶体中Ca2+和Ca2+之间的最近距离与F-和F-之间的最近距离之比为
2
【答案】D
【解析】A. 周期表中同主族从下到上,同周期从左到右,元素的非金属性增强,最高价氧化物对应的水
化物的酸性增强,元素的氢化物稳定性增强,元素的非金属性F>O>Si,氢化物的稳定性:HF>H O>SiH,
2 4
故A正确;B. SiF、HO、SO 、SiO 四者的中心原子的杂化方式相同,均为sp3杂化,故B正确;C.
4 2 2
由氟化钙晶胞可知每个晶胞中含有4个Ca2+,8个F-,CaF 的晶体密度为
2
,故C正确;D. CaF 晶体中Ca2+和Ca2+之间的最近距离
2
与F-和F-之间的最近距离之比为 ,故D错误;故选D。
【热点三】元素推断与元素周期律
1.(2024·浙江·二模)已知 是原子序数依次增大的前四周期元素。 的核外电子总数
与其周期数相同, 与 相邻且 的原子序数是 的两倍,基态 的轨道全部充满。下列说法正确的
是
A.简单氢化物的沸点:
B.第一电离能:
C.A、B、C三种元素只形成共价化合物D.B的简单氢化物的水溶液能溶解E的最高价氧化物对应的水化物
【答案】D
【分析】已知 是原子序数依次增大的前四周期元素。 的核外电子总数与其周期数相
同,A为H元素, 与 相邻且 的原子序数是 的两倍,C为O元素,B为N元素,D为S元素,
基态 的轨道全部充满,E为Cu,以此解答。
【解析】A.NH 和HO分子间都存在氢键,但HO分子形成的氢键更多,则简单氢化物的沸点:
3 2 2
NH N>S>H,故B错误;C.H、N、O三种元素可以形成共价化
合物HNO,也可以形成离子化合物NH NO ,故C错误;D.N的简单氢化物为氨气,氨气的水溶液为氨
3 4 3
水,氨水能溶解Cu(OH) ,故D正确;故选D。
2
2.(2024·浙江杭州·二模)A、B、C、D、E、F为六种原子序数依次增大的短周期元素,A、B、D位于
同一主族,且D的原子半径在短周期元素原子中最大,C是周期表中电负性最大的元素,基态E原子的核
外电子有7种空间运动状态,基态F原子有3个未成对电子。下列说法正确的是
A.C的最低价氢化物的沸点低于F的最低价氢化物
B.A元素形成的离子半径小于B元素形成的离子半径
C.A、B、E形成化合物中阴离子中心原子的杂化方式为sp2
D.C、D、E形成的某种化合物能降低冶炼E单质的能耗
【答案】D
【分析】A、B、C、D、E、F为六种原子序数依次增大的短周期元素,A、B、D位于同一主族,且D的
原子半径在短周期元素原子中最大,则A是H元素,B是Li元素,D是Na元素;C是周期表中电负性最
大的元素,则C是F元素;基态E原子的核外电子有7种空间运动状态,则E核外电子排布是
1s22s2p63s23p1,E是Al元素;基态F原子有3个未成对电子,则F核外电子排布是1s22s2p63s23p3,F是P元
素,然后根据元素周期律及物质的性质分析解答。
【解析】根据上述分析可知:A是H,B是Li,C是F,D是Na,E是Al,F是P元素。
A.C 是F元素,F是P元素,它们形成的简单氢化物HF、PH ,HF分子之间除存在分子间作用力外,还
3
存在氢键,增加了分子之间的吸引作用,导致其沸点比只存在分子间作用力的PH 高,A错误;B.A是
3
H,B是Li,若H形成的简单离子是H-,Li形成的简单离子是Li+,电子层数相同时,原子序数越大半径越
小,所以离子半径:H->Li+,B错误;C.A是H,B是Li,E是Al,三种元素形成的化合物LiAlH ,其阴
4
离子 的价层电子对数是4+ =4,因此中心Al原子杂化类型是sp3,C错误;D.根据上述分析
可知:C是F,D是Na,E是Al,三种元素形成的化合物是NaAlF,NaAlF 俗称冰晶石;单质Al冶炼时
3 6 3 6
采用电解熔融Al O 的方法,但由于该物质是离子化合物,熔点是2050℃,熔点很高,为降低其熔点,通
2 3
常要加入冰晶石NaAlF,可以使Al O 在1000℃左右熔化,从而可节约大量能量而降低能耗,D正确;故
3 6 2 3
选D。
3.(2024·广东·一模)2024年是元素周期表诞生的第155周年。已知短周期主族元素X、Y、Z、M、N,
其原子序数与其对应的0.1mol/L最高价氧化物的水化物溶液,在常温下的pH关系如图所示。下列说法中正确的是
A.X和Y元素均在p区 B.元素的电负性:Z>M>N
C.M的含氧酸根离子的中心原子为sp2杂化 D.XN 和ZN 的空间构型均为三角锥形
3 3
【答案】D
【分析】短周期主族元素X、Y、Z、M、N,由其原子序数与其对应的0.1mol⋅L-1最高价氧化物的水化物
溶液在常温下的pH关系图可知,X、N均对应一元强酸,结合原子序数可知X为N元素、N为Cl元素;
Y对应一元强碱,Y为Na元素;由溶液的pH可知,Z对应不是强酸,M对应二元强酸,结合原子序数可
知Z为P元素、M为S元素,以此来解答。
【解析】由上述分析可知,X为N元素、Y为Na元素、Z为P元素、M为S元素、N为Cl元素,A.X即
N元素位于p区,Y即Na元素位于s区,A错误;B.同周期主族元素从左向右电负性增大,则元素的电
负性即P<S<Cl即Z<M<N,B错误;C.M的含氧酸根离子为硫酸根离子或亚硫酸根离子,其中心原
子为sp3杂化,C错误;D.NCl 和PCl 中N、P均为sp3杂化,均含1对孤对电子,可知空间构型均为三角
3 3
锥形,D正确;故答案为:D。
4.(2024·云南大理·二模)科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种
新型超分子,其分子结构如下图所示(Y和Y之间重复单元的W、X未全部标出),W、X、Z分别位于不同
周期,Z是同周期中金属性最强的元素,下列说法正确的是
A.简单气态氢化物的沸点:
B.第一电离能:
C. 只含有离子键
D.原子半径:
【答案】D
【分析】W、X、Y、Z是原子序数依次递增的短周期元素,W、X、Z分别位于不同周期,则W为H元
素,Y、Z分别位于第二、第三周期;Z是同周期中金属性最强的元素,则Z为Na元素;新型超分子中
X、Y形成的共价键数目分别为4、2,则X为C元素、Y为O元素。【解析】A.水分子能形成分子间氢键,甲烷不能形成分子间氢键,所以水分子的分子间作用力大于甲
烷,沸点高于甲烷,故A错误;B.金属元素的第一电离能小于非金属元素,同周期元素,从左到右第一
电离能呈增大趋势,所以三种元素的第一电离能大小顺序为 ,故B错误;C.过氧化
钠是含有离子键和非极性键的离子化合物,故C错误;D.三种原子中氢原子的原子半径最小,同周期元
素,从左到右原子半径依次减小,则原子半径大小顺序为 ,故D正确;故选D。
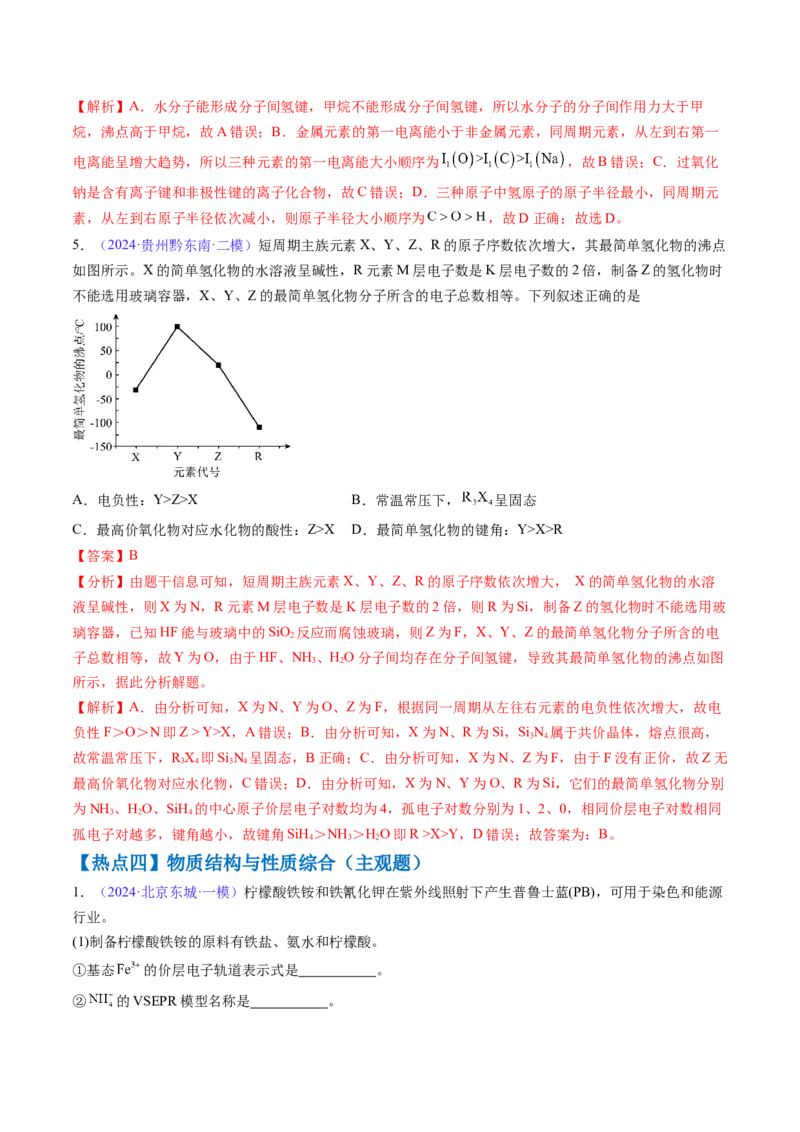
5.(2024·贵州黔东南·二模)短周期主族元素X、Y、Z、R的原子序数依次增大,其最简单氢化物的沸点
如图所示。X的简单氢化物的水溶液呈碱性,R元素M层电子数是K层电子数的2倍,制备Z的氢化物时
不能选用玻璃容器,X、Y、Z的最简单氢化物分子所含的电子总数相等。下列叙述正确的是
A.电负性:Y>Z>X B.常温常压下, 呈固态
C.最高价氧化物对应水化物的酸性:Z>X D.最简单氢化物的键角:Y>X>R
【答案】B
【分析】由题干信息可知,短周期主族元素X、Y、Z、R的原子序数依次增大, X的简单氢化物的水溶
液呈碱性,则X为N,R元素M层电子数是K层电子数的2倍,则R为Si,制备Z的氢化物时不能选用玻
璃容器,已知HF能与玻璃中的SiO 反应而腐蚀玻璃,则Z为F,X、Y、Z的最简单氢化物分子所含的电
2
子总数相等,故Y为O,由于HF、NH 、HO分子间均存在分子间氢键,导致其最简单氢化物的沸点如图
3 2
所示,据此分析解题。
【解析】A.由分析可知,X为N、Y为O、Z为F,根据同一周期从左往右元素的电负性依次增大,故电
负性F>O>N即Z > Y>X,A错误;B.由分析可知,X为N、R为Si,Si N 属于共价晶体,熔点很高,
3 4
故常温常压下,R X 即Si N 呈固态,B正确;C.由分析可知,X为N、Z为F,由于F没有正价,故Z无
3 4 3 4
最高价氧化物对应水化物,C错误;D.由分析可知,X为N、Y为O、R为Si,它们的最简单氢化物分别
为NH 、HO、SiH 的中心原子价层电子对数均为4,孤电子对数分别为1、2、0,相同价层电子对数相同
3 2 4
孤电子对越多,键角越小,故键角SiH>NH >HO即R >X>Y,D错误;故答案为:B。
4 3 2
【热点四】物质结构与性质综合(主观题)
1.(2024·北京东城·一模)柠檬酸铁铵和铁氰化钾在紫外线照射下产生普鲁士蓝(PB),可用于染色和能源
行业。
(1)制备柠檬酸铁铵的原料有铁盐、氨水和柠檬酸。
①基态 的价层电子轨道表示式是 。
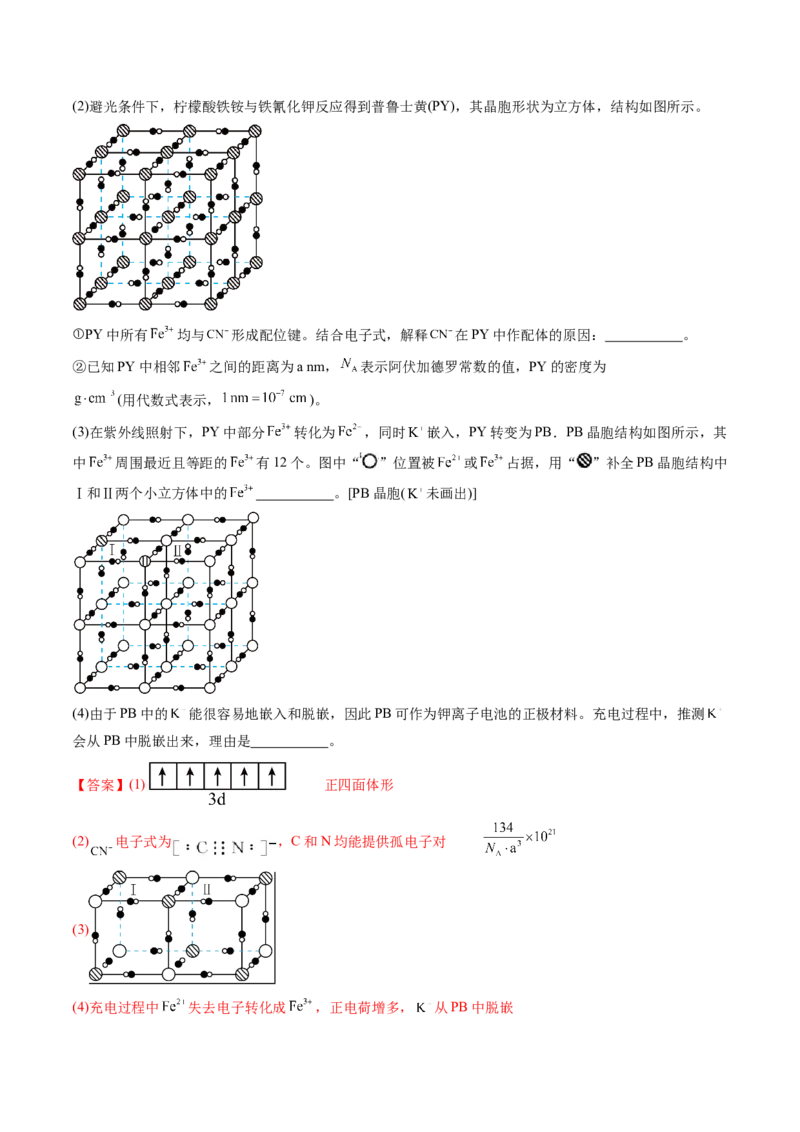
② 的VSEPR模型名称是 。(2)避光条件下,柠檬酸铁铵与铁氰化钾反应得到普鲁士黄(PY),其晶胞形状为立方体,结构如图所示。
①PY中所有 均与 形成配位键。结合电子式,解释 在PY中作配体的原因: 。
②已知PY中相邻 之间的距离为a nm, 表示阿伏加德罗常数的值,PY的密度为
(用代数式表示, )。
(3)在紫外线照射下,PY中部分 转化为 ,同时 嵌入,PY转变为PB.PB晶胞结构如图所示,其
中 周围最近且等距的 有12个。图中“ ”位置被 或 占据,用“ ”补全PB晶胞结构中
Ⅰ和Ⅱ两个小立方体中的 。[PB晶胞( 未画出)]
(4)由于PB中的 能很容易地嵌入和脱嵌,因此PB可作为钾离子电池的正极材料。充电过程中,推测
会从PB中脱嵌出来,理由是 。
【答案】(1) 正四面体形
(2) 电子式为 ,C和N均能提供孤电子对
(3)
(4)充电过程中 失去电子转化成 ,正电荷增多, 从PB中脱嵌【解析】(1)①铁是26号元素,基态Fe3+的价层电子排布式为3d5,价层电子轨道表示式是
;
② 的中心原子为N,价层电子对为4对,VSEPR模型名称正四面体形结构;
(2)①CN-的电子式为 ,其中C和N均有孤对电子存在,能提供孤电子对;
②在PY的晶胞结构中最小的一个立方体中,8个Fe3+位于立方体的顶角,属于一个小立方体的Fe3+有8×
=1,CN-位于小立方体的棱心,属于一个小立方体的CN-有12× =3,一个小立方体的质量为 =
g,一个小立方体的体积为(a×10-7)3=a3×10-21cm3,PY的密度为: g/cm3;
(3)根据PB晶胞结构,其中 周围最近且等距的 有12个,用“ ”补全PB晶胞结构中Ⅰ和Ⅱ
两个小立方体中的 ,结果如下: ;
(4)充电过程中阳极上发生 失去电子转化成 ,正电荷增多, 从PB中脱嵌。
2.(2024·浙江杭州·二模)氮、硫和氯等是构成化合物的常见元素。已知:2SO +H O=
3 2
。
(1)某化合物的晶胞如图所示,其化学式是 , 周围最近的 有 个,晶体类型是
。
(2)下列说法正确的是___________。
A.能量最低的激发态Cl原子的M层电子排布图为
B.电负性:C. 中两个 键的镜面在空间上相互垂直
D.第一电离能:
(3)① 和 发生如下过程: ,硫酸起到 (填
“酸”、“碱”)的作用。
比较键角 , (填“>”、“<”或“=”),理由是 。
(4)将 与 发生化合反应生成 型离子化合物,其中A为 ,写出B的结构式
。
【答案】(1)Cs[ ][ ] 8 离子晶体
2
(2)CD
(3)酸 > 中氮为sp杂化,是直线形结构, 中氮为sp2杂化,为平面三角形结构
(4)
【解析】(1)据“均摊法”,晶胞中含 个 、 个 、 个Cs,则化
学式为Cs[ ][ ];由图可知, 周围最近的 在上下层各有4个,共有8个,该物质中含有离
2
子键,其晶体类型是离子晶体;
(2)A.氯为17号元素,基态Cl原子核外电子排布为1s22s22p63s23p5,能量最低的激发态Cl原子则会有1
个3s电子跃迁到3p轨道,故M层电子排布图为 ,错误;B.同周期从左
到右,金属性减弱,非金属性增强,元素的电负性变大;同主族由上而下,金属性增强,非金属性逐渐减
弱,元素电负性减弱;电负性: ,错误;C. 键为镜面对称,则 中两个 键的镜面在空间上相
互垂直,正确;D.同一主族随原子序数变大,原子半径变大,第一电离能变小;同一周期随着原子序数
变大,第一电离能呈增大趋势,故第一电离能: ,正确;故选CD;
(3)反应中硫酸提供氢离子,起到酸的作用; 中氮为sp杂化,是直线形结构, 中氮为sp2杂
化,为平面三角形结构,故键角 , > ;
(4) 与 发生化合反应生成 型离子化合物,其中A为 ,结合质量守恒可
知,B为含有1个N、2个S、6个O形成的负三价阴离子,结合已知:2SO +H O= ,则
3 2B为 。
3.(2024·北京房山·一模)氮元素能与金属或者非金属元素形成种类繁多、应用广泛的化合物。
(1)基态N原子的价层电子轨道表示式是 。
(2)与碳氢化合物类似,N、H两元素之间也可以形成氮烷、氮烯。
①在最简单的氮烯分子中,N的杂化方式是 。
② 具有很强的还原性,是常用的火箭推进剂,它在常温常压下为无色液体。判断 是否溶于水并
说明理由 。
(3)配合物 可用作广谱杀菌剂,其中Cu属于 区元素,该配合物中的配位原子
是 ,配位数是 。
(4) 的某种晶体结构中,原子间均以单键结合,其硬度比金刚石大,原因是 。
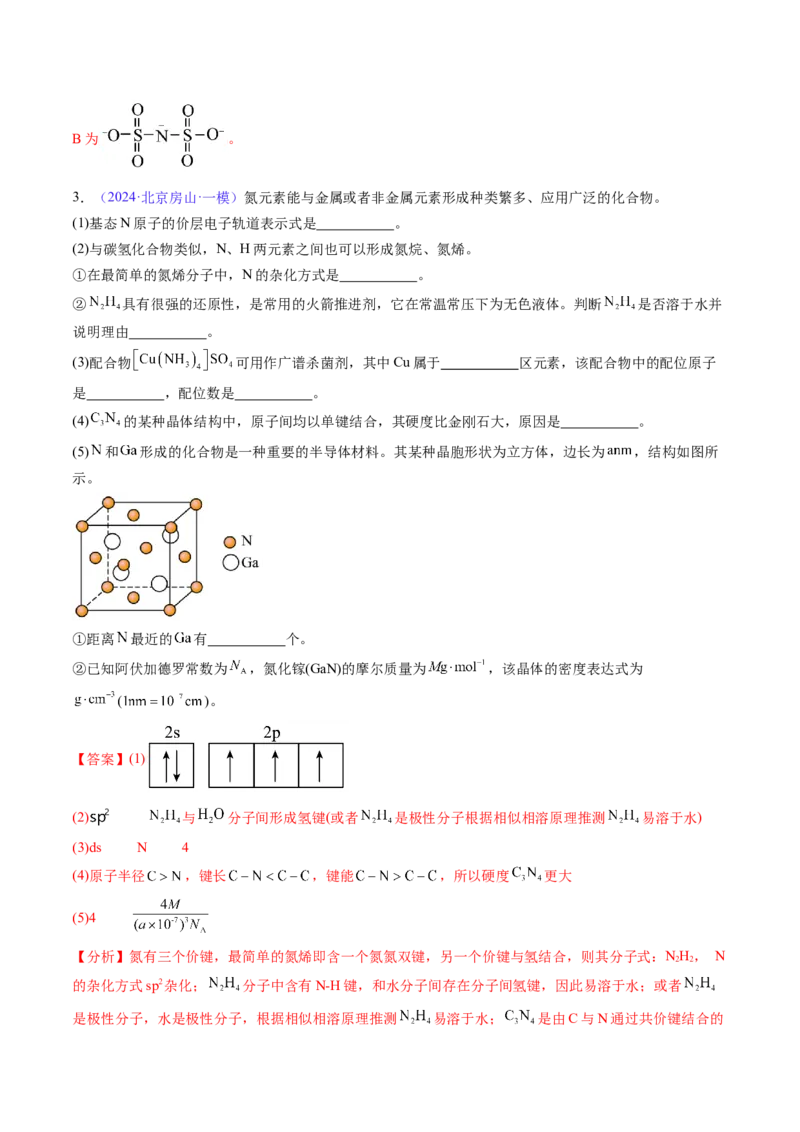
(5) 和 形成的化合物是一种重要的半导体材料。其某种晶胞形状为立方体,边长为 ,结构如图所
示。
①距离 最近的 有 个。
②已知阿伏加德罗常数为 ,氮化镓(GaN)的摩尔质量为 ,该晶体的密度表达式为
( )。
【答案】(1)
(2) 与 分子间形成氢键(或者 是极性分子根据相似相溶原理推测 易溶于水)
(3)ds N 4
(4)原子半径 ,键长 ,键能 ,所以硬度 更大
(5)4
【分析】氮有三个价键,最简单的氮烯即含一个氮氮双键,另一个价键与氢结合,则其分子式:NH, N
2 2
的杂化方式sp2杂化; 分子中含有N-H键,和水分子间存在分子间氢键,因此易溶于水;或者
是极性分子,水是极性分子,根据相似相溶原理推测 易溶于水; 是由C与N通过共价键结合的共价晶体。原子半径 ,键长 ,键能 ,所以硬度 更大;利用均摊法结
合晶胞示意图可知1个晶胞中Ga数目为 ,N原子数目为4,化学式为GaN。
【解析】(1)N的核电荷数为7,核外有7个电子,基态N原子电子排布式为1s22s22p3,则基态N原子的
价层电子排布式是2s22p3,价层电子轨道表示式为: ,故答案 :
;
(2)氮有三个价键,最简单的氮烯即含一个氮氮双键,另一个价键与氢结合,则其分子式:NH, N的
2 2
杂化方式sp2杂化; 分子中含有N-H键,和水分子间存在分子间氢键,因此易溶于水;或者 是
极性分子,水是极性分子,根据相似相溶原理推测 易溶于水,故答案为:sp2; 与 分子间形
成氢键(或者 是极性分子根据相似相溶原理推测 易溶于水);
(3) 中Cu原子核外29个电子,价层电子排布式为: ,属于ds区;
[Cu(NH )]SO 的内界离子是[Cu(NH )]2+,其中心Cu2+结合的配位体是NH , 配位原子为:N;Cu2+配位数
3 4 4 3 4 3
是4,故答案为:ds;N;4;
(4) 是由C与N通过共价键结合的共价晶体。原子半径 ,键长 ,键能
,所以硬度 更大,故答案为:原子半径 ,键长 ,键能
,所以硬度 更大;
(5)①GaN晶体中1个N原子和周围四个Ga原子形成极性共价键,1个Ga原子和周围四个N原子形成
极性共价键,则Ga原子周围等距且最近的氮原子有4个;
②由题干晶胞示意图可知1个晶胞中Ga数目为 ,N原子数目为4,化学式为GaN,则晶胞
密度 ,故答案为: 。
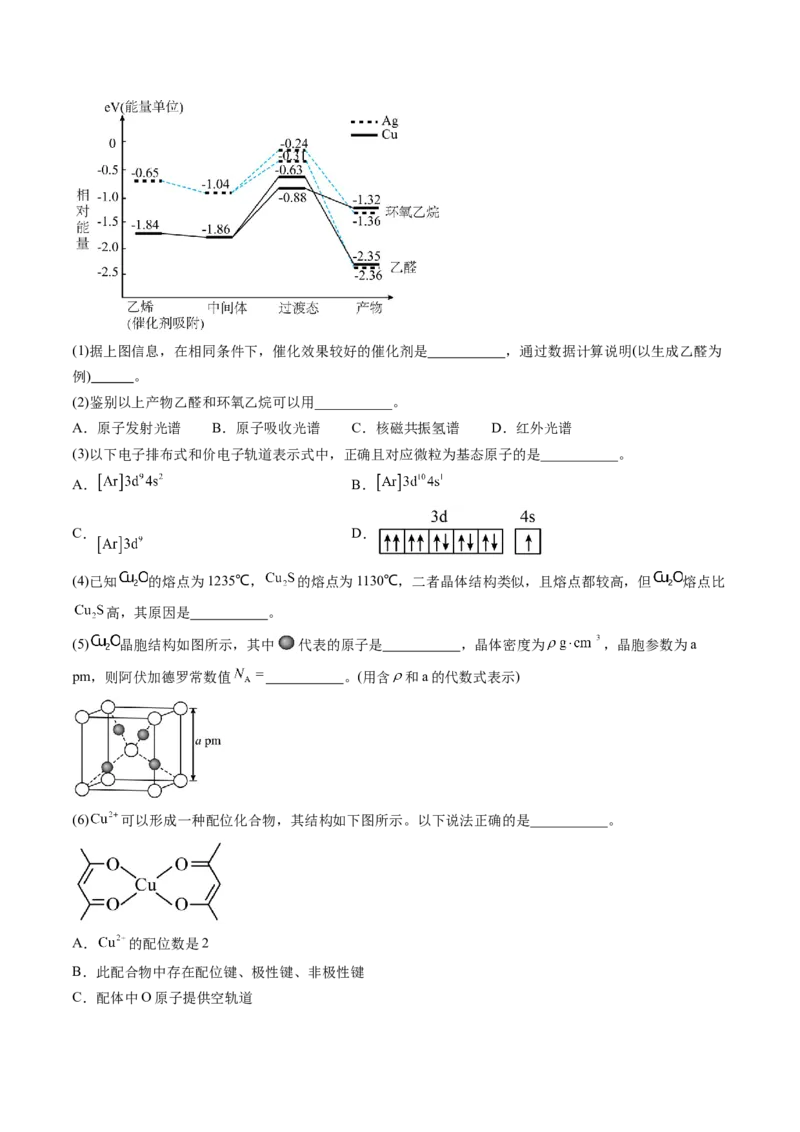
4.(2024·上海嘉定·二模)在铜、银催化下,乙烯与氧气反应生成环氧乙烷( )和乙醛,下图是该反应
的部分历程。(1)据上图信息,在相同条件下,催化效果较好的催化剂是 ,通过数据计算说明(以生成乙醛为
例) 。
(2)鉴别以上产物乙醛和环氧乙烷可以用___________。
A.原子发射光谱 B.原子吸收光谱 C.核磁共振氢谱 D.红外光谱
(3)以下电子排布式和价电子轨道表示式中,正确且对应微粒为基态原子的是___________。
A. B.
C. D.
(4)已知 的熔点为1235℃, 的熔点为1130℃,二者晶体结构类似,且熔点都较高,但 熔点比
高,其原因是 。
(5) 晶胞结构如图所示,其中 代表的原子是 ,晶体密度为 ,晶胞参数为a
pm,则阿伏加德罗常数值 。(用含 和a的代数式表示)
(6) 可以形成一种配位化合物,其结构如下图所示。以下说法正确的是___________。
A. 的配位数是2
B.此配合物中存在配位键、极性键、非极性键
C.配体中O原子提供空轨道D. 提供孤电子对
(7)已知:常温下,① ;
②
则常温下 。
【答案】(1)银 银催化下生成乙醛的活化能 ,小于铜催化下生成乙醛的
活化能
(2)CD
(3)B
(4) 半径比 半径小, 中离子键强于 中离子键
(5)
(6)B
(7)
【解析】(1)以生成乙醛为例,在铜催化下,中间体生成过渡态的活化能为
,在银催化下,中间体生成过渡态的活化能为 ,活化能小,化学反应速率
快,催化剂催化效果好,故催化效果较好的催化剂是银;
故答案为:银;银催化下生成乙醛的活化能 ,小于铜催化下生成乙醛的活化
能 ;
(2)A.原子发射光谱是原子光谱的一种,原子光谱的特征谱线可以鉴定元素,环氧乙烷和乙醛组成元素
相同,都含有C、H、O,原子发射光谱不能鉴别环氧乙烷和乙醛,A错误;
B.原子吸收光谱也是原子光谱的一种,原子光谱的特征谱线可以鉴定元素,环氧乙烷和乙醛组成元素相
同,原子吸收光谱也不能鉴别环氧乙烷和乙醛,B错误;
C.环氧乙烷结构对称,只有1种氢原子,核磁共振氢谱只有1个吸收峰,乙醛结构中有2种氢原子,核磁
共振氢谱有2个吸收峰,核磁共振氢谱能鉴别环氧乙烷和乙醛,C正确;
D.二者结构不同,化学键种类不同,环氧乙烷含有 ,乙醛含有 ,官能团不同,则红
外光谱图不同,红外光谱能鉴别环氧乙烷和乙醛,D正确;
故答案为:CD;
(3)A.该电子排布式表示的微粒有 个电子,核外有29个电子的原子为铜,其基态原子的电
子排布式是 ,A错误;
B.该电子排布式表示的是铜的基态原子,B正确;C. 表示的微粒有 个电子,核外有29个电子的原子为镍,其基态原子的电子排布式是
,C错误;
D.该价电子轨道表示式中3d能级有2个轨道中的电子自旋方向相同,违背泡利原理,D错误;
故答案为:B;
(4)二者都为离子晶体结构,故熔点都较高,组成 晶体的 半径比组成 晶体的 半径小,
中离子键强于 中离子键,故 熔点比 高;
故答案为: 半径比 半径小, 中离子键强于 中离子键;
(5)在晶胞结构图中, 位于体内有4个,白球位于顶角与体心有2个,二者个数比为2:1,故 代表
的原子是 ;
根据晶体密度 ,则 ,故 ;
故答案为: ; ;
(6)A. 的配位数是4,A错误;B.此配合物中 提供空轨道,O原子提供孤电子对形成配位
键、存在 极性键及 非极性键,B正确;C.配体中O原子提供孤电子对,C错误;D. 为
中心离子,提供空轨道,D错误;故答案为:B;
(7)已知常温下, ;
,
则
;
故答案为: 。
5.(2024·内蒙古呼和浩特·一模)钛被称为“未来金属”,广泛应用于国防、航空航天、生物材料等领
域,如氮化钛和钛的卤化物。
(1)基态Ti原子的价电子排布图为 ;前10号元素中,第一电离能比N大的元素有 种。
(2)Ti(IV)的极化能力强,不能从水溶液中获得其含氧酸正盐,只能得到水解产物如TiOSO 和TiO(NO )。
4 3 2
其中阴离子SO 的空间构型为 ,NO 中心原子的杂化方式为 ,TiOSO 组成元素的电负性由
4
大到小顺序是 。
(3)TiF 和TiCl 熔点如表所示,二者熔点相差较大的原因是 。
4 4化合物 TiF TiCl
4 4
熔点/℃ 377 -24.12
(4)在浓TiCl 的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl •6H O的晶体,
3 3 2
该晶体中两种配体的物质的量之比为1:2,则由该配合离子组成的晶体化学式还可以写为 。
(5)氨化钛晶体的晶胞结构如图所示,该晶体结构中与N原子距离最近且相等的Ti原子有 个;若该
晶胞的密度为ρg•cm-3,阿伏加德罗常数的值为N ,则晶胞中Ti原子与N原子的最近距离为 nm(用
A
含ρ,N 的代数式表示)
A
【答案】(1) 3
(2)正四面体(形)sp2 OSTi
(3)TiF 为分子晶体,TiCl 为离子晶体
4 4
(4)[TiCl (H O) ]Cl•2H O
2 2 4 2
(5)6 ×107
【解析】(1)Ti原子序数22,核外电子排布: ,价电子排布图:
;同周期元素从左到右,元素第一电离能逐渐增大,N核外电子排布处于半
充满的稳定状态,第一电离能大于相邻元素,则前10号元素中,第一电离能比N大的元素有He、F、Ne
共3种元素;
(2) 中心原子S原子价层电子对数: ,无孤电子对,空间构型为正四面体形;
中心原子N杂化轨道数: ,属于 杂化;同周期元素从左到右元素电负性逐渐增
强,同族元素从上到下,元素电负性逐渐减弱,则电负性大小:O>S>Ti;
(3)TiF 和TiCl 熔点如表所示,二者熔点相差较大的原因:TiF 为分子晶体,TiCl 为离子晶体;
4 4 4 4
(4)配位数为6、组成为TiCl •6H O的晶体,该晶体中两种配体的物质的量之比为1:2,则由该配合离
3 2
子组成的晶体化学式还可以写:[TiCl (H O) ]Cl•2H O;
2 2 4 2
(5)根据晶体结构,与N原子距离最近且相等的Ti原子有6个;设晶胞参数为anm,晶胞中含N个数:、含Ti个数: ;根据密度计算公式: ,解得
,Ti原子与N原子的最近距离为棱长的一半,即 。