文档内容
重难点 03 离子反应
一、电解质溶液导电情况分析
1.电解质溶液的导电原理
电解质电离出的阴、阳离子在外加电场的作用下,发生定向移动实现导电过程,一般情况下,自由移动离
子的浓度越大,所带的电荷数越多,电解质溶液的导电能力越强。
2.同一温度下,强电解质溶液(a)、弱电解质溶液(b)、金属导体(c)的导电能力相同,若升高温度,它们的导
电能力大小顺序为b>a>c。
二、书写离子方程式时的易错点
1.两种电解质溶液混合,至少电离出两种阴离子和两种阳离子,这四种(或更多种)离子之间都能两两结合成
难电离(或难溶)的物质或后续离子之间的氧化还原反应,这样的离子反应称为多重反应。在写这类反应的
离子方程式时易丢失其中的一组反应。
如:(1)Ba(OH) 溶液与HSO 溶液混合
2 2 4
Ba 2 + + 2OH - + 2H + + SO == =BaSO ↓ + 2H O。
4 2
(2)Ba(OH) 溶液与(NH )SO 溶液混合
2 4 2 4
Ba 2 + + 2OH - + 2NH + SO == =BaSO ↓ + 2NH ·H O。
4 3 2
(3)CuSO 溶液与Ba(OH) 溶液混合
4 2
Cu 2 + + SO + Ba 2 + + 2OH - == =Cu(OH) ↓ + BaSO ↓。
2 4
2.“拆分”陷阱
离子方程式的正误判断中,常常设置物质是否能“拆分”陷阱,氧化物、弱电解质、沉淀、多元弱酸的酸
式酸根(HSO除外)在离子方程式中均不能拆分。在复习时,应熟记常见的弱电解质、溶解度表及常见多元
弱酸的酸式酸根。
3.“守恒”陷阱
离子方程式除符合质量守恒外,还应符合电荷守恒,做题时往往只注意质量守恒,而忽略电荷守恒,这也
是命题者经常设置的“陷阱”。
4.“原理”陷阱
离子反应应符合客观事实,而试题往往设置不符合“反应原理”的陷阱,如 Fe和非氧化性酸反应应生成
Fe2+,金属和氧化性酸反应不生成H,应注意隐含反应,“===”“ ”使用是否正确以及反应条件等。
2
5.“量比”陷阱
在离子方程式正误判断中,做题时往往忽略相对量的影响,试题往往设置“离子方程式正确,但不符合相
对量”的陷阱。突破“陷阱”的方法一是审准“相对量”的多少,二是看离子反应是否符合该量。
如:(1)CO 通入NaOH溶液中:
2
碱过量:CO + 2OH - == =CO + H O;
2 2
碱不足:CO + OH - == =HCO 。
2(2)Na CO 溶液与稀盐酸反应:
2 3
稀盐酸不足: CO + H + == =HCO ;
稀盐酸过量: CO + 2H + == =CO ↑ + H O。
2 2
(3)铝盐溶液与强碱溶液反应:
铝盐过量: Al 3 + + 3OH - == =Al(OH) ↓;
3
强碱过量: Al 3 + + 4OH - == =AlO + 2H O。
2
(4)NaAlO 溶液与强酸溶液反应:
2
NaAlO 过量: AlO + H + + H O == =Al(OH) ↓;
2 2 3
强酸过量: AlO + 4H + == =Al 3 + + 2H O。
2
(5)CO 通入NaAlO 溶液中:
2 2
NaAlO 过量: 2AlO + CO + 3H O == =2Al(OH) ↓ + CO ;
2 2 2 3
NaAlO 不足: AlO + CO + 2H O == =Al(OH) ↓ + HCO 。
2 2 2 3
(6)Fe与稀HNO 溶液反应:
3
Fe过量: 3Fe + 2NO + 8H + == =3Fe 2 + + 2NO↑ + 4H O;
2
稀HNO 过量: Fe + NO + 4H + == =Fe 3 + + NO↑ + 2H O。
3 2
(7)NH HSO 溶液与NaOH溶液的反应:
4 4
NaOH不足: H + + OH - == =H O;
2
NaOH过量: NH + H + + 2OH - == =NH ·H O + H O。
3 2 2
(8)向FeBr 溶液中通Cl:
2 2
Cl 少量:Cl + 2F e 2 + == =2F e 3 + + 2C l - ;
2 2
Cl 过量: 2Fe 2 + + 4Br - + 3Cl == =2Fe 3 + + 2Br + 6C l - 。
2 2 2
(9)Ba(OH) 溶液与NaHSO 溶液反应:
2 4
①n[Ba(OH) ]∶n(NaHSO)=1∶1
2 4
Ba 2 + + OH - + H + + SO == =BaSO ↓ + H O,此时溶液呈碱性;
4 2
②n[Ba(OH) ]∶n(NaHSO)=1∶2
2 4
Ba 2 + + 2OH - + 2H + + SO == =BaSO ↓ + 2H O,此时溶液呈中性,若向该溶液中再加入Ba(OH) 溶液,反应为
4 2 2
SO + Ba 2 + == =BaSO ↓。
4
三、判断离子能否大量共存的“四个要点”
判断多种离子能否大量共存于同一溶液中,归纳起来就是:一色、二性、三特殊、四反应。
(1)一色——溶液颜色
几种常见离子的颜色:
离子 Cu2+ Fe3+ Fe2+ MnO
溶液颜色 蓝色 棕黄色 浅绿色 紫红色
(2)二性——溶液的酸碱性
①在酸性溶液中,OH-及弱酸根阴离子(如CO、SO、S2-、CHCOO-等)不能大量存在。
3
②在碱性溶液中,H+及弱碱阳离子(如NH、Al3+、Fe3+等)不能大量存在。(3)三特殊——三种特殊情况:
①AlO与HCO不能大量共存:AlO+HCO+HO===Al(OH) ↓+CO。
2 3
②“NO+H+”组合具有强氧化性,能与S2-、Fe2+、I-、SO等还原性的离子发生氧化还原反应而不能大
量共存。
③NH与CHCOO-、CO,Mg2+与HCO等组合中,虽然两种离子都能水解且水解相互促进,但总的水解
3
程度仍很小,它们在溶液中仍能大量共存。
(4)四反应——四种反应类型
四反应是指离子间通常能发生的四种类型的反应,能相互反应的离子显然不能大量共存。
①复分解反应:如Ba2+与SO,NH与OH-,H+与CHCOO-等。
3
②氧化还原反应:如Fe3+与I-、S2-,NO(H+)与Fe2+等。
③相互促进的水解反应:如Al3+与CO、HCO或AlO等。
④络合反应:如Fe3+与SCN-等。
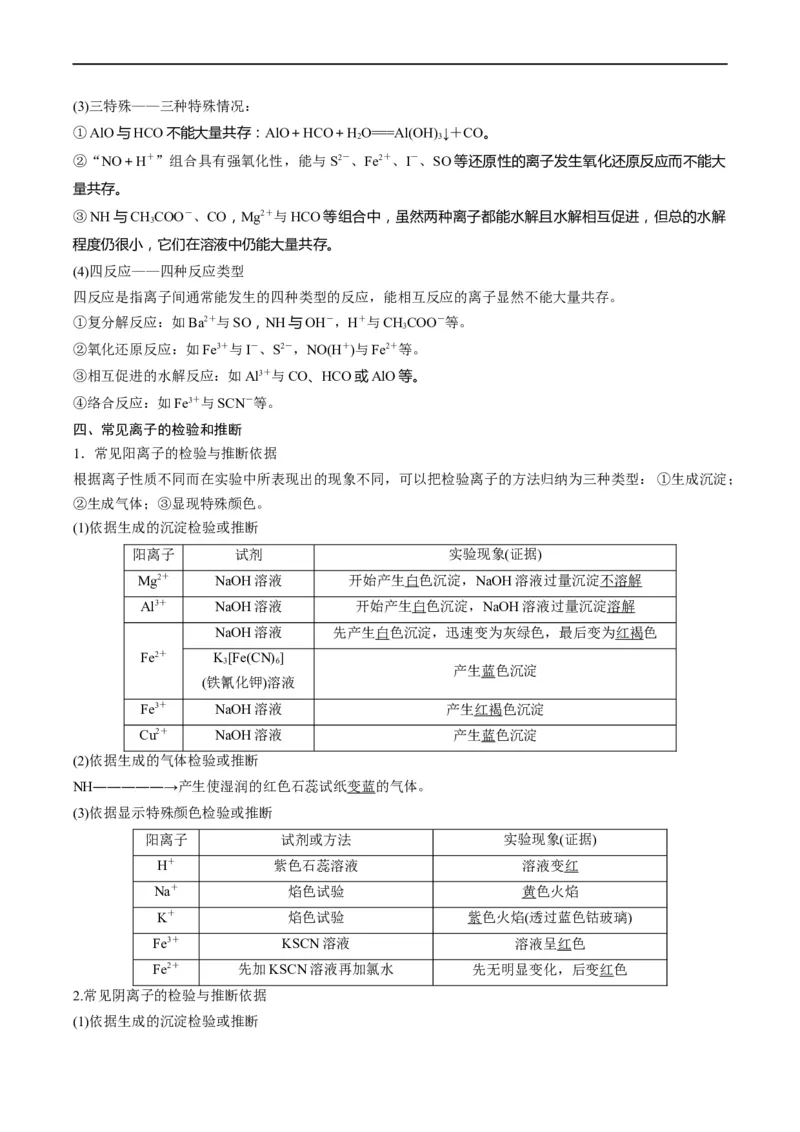
四、常见离子的检验和推断
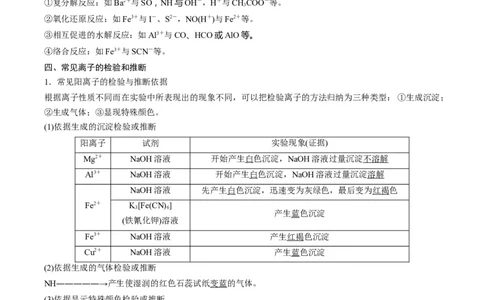
1.常见阳离子的检验与推断依据
根据离子性质不同而在实验中所表现出的现象不同,可以把检验离子的方法归纳为三种类型:①生成沉淀;
②生成气体;③显现特殊颜色。
(1)依据生成的沉淀检验或推断
阳离子 试剂 实验现象(证据)
Mg2+ NaOH溶液 开始产生白色沉淀,NaOH溶液过量沉淀不溶解
Al3+ NaOH溶液 开始产生白色沉淀,NaOH溶液过量沉淀溶解
NaOH溶液 先产生白色沉淀,迅速变为灰绿色,最后变为红褐色
Fe2+ K[Fe(CN) ]
3 6
产生蓝色沉淀
(铁氰化钾)溶液
Fe3+ NaOH溶液 产生红褐色沉淀
Cu2+ NaOH溶液 产生蓝色沉淀
(2)依据生成的气体检验或推断
NH―――――→产生使湿润的红色石蕊试纸变蓝的气体。
(3)依据显示特殊颜色检验或推断
阳离子 试剂或方法 实验现象(证据)
H+ 紫色石蕊溶液 溶液变红
Na+ 焰色试验 黄色火焰
K+ 焰色试验 紫色火焰(透过蓝色钴玻璃)
Fe3+ KSCN溶液 溶液呈红色
Fe2+ 先加KSCN溶液再加氯水 先无明显变化,后变红色
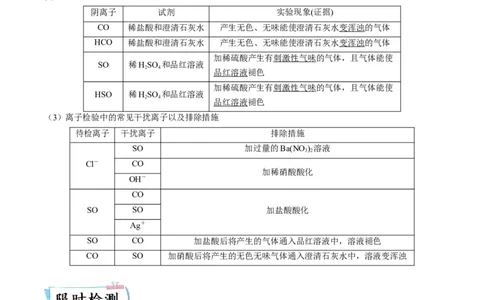
2.常见阴离子的检验与推断依据
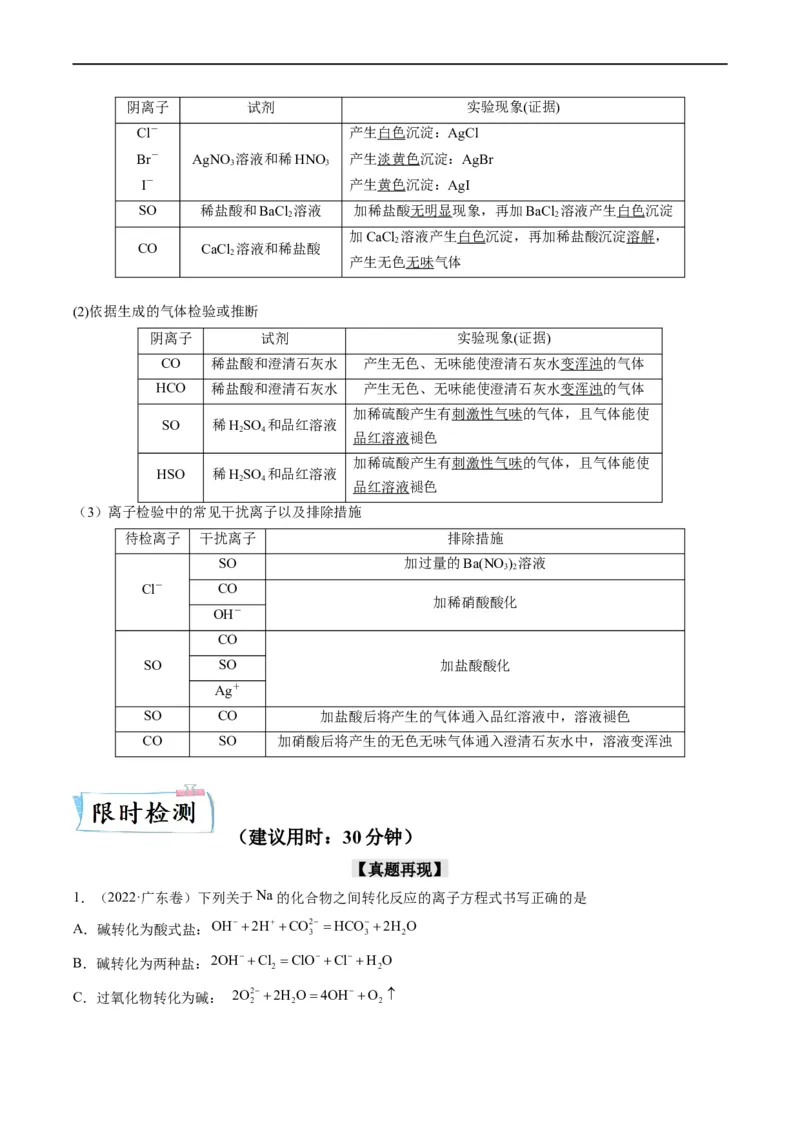
(1)依据生成的沉淀检验或推断阴离子 试剂 实验现象(证据)
Cl- 产生白色沉淀:AgCl
Br- AgNO 溶液和稀HNO 产生淡黄色沉淀:AgBr
3 3
I- 产生黄色沉淀:AgI
SO 稀盐酸和BaCl 溶液 加稀盐酸无明显现象,再加BaCl 溶液产生白色沉淀
2 2
加CaCl 溶液产生白色沉淀,再加稀盐酸沉淀溶解,
2
CO CaCl 溶液和稀盐酸
2
产生无色无味气体
(2)依据生成的气体检验或推断
阴离子 试剂 实验现象(证据)
CO 稀盐酸和澄清石灰水 产生无色、无味能使澄清石灰水变浑浊的气体
HCO 稀盐酸和澄清石灰水 产生无色、无味能使澄清石灰水变浑浊的气体
加稀硫酸产生有刺激性气味的气体,且气体能使
SO 稀HSO 和品红溶液
2 4
品红溶液褪色
加稀硫酸产生有刺激性气味的气体,且气体能使
HSO 稀HSO 和品红溶液
2 4
品红溶液褪色
(3)离子检验中的常见干扰离子以及排除措施
待检离子 干扰离子 排除措施
SO 加过量的Ba(NO ) 溶液
3 2
Cl- CO
加稀硝酸酸化
OH-
CO
SO SO 加盐酸酸化
Ag+
SO CO 加盐酸后将产生的气体通入品红溶液中,溶液褪色
CO SO 加硝酸后将产生的无色无味气体通入澄清石灰水中,溶液变浑浊
(建议用时:30分钟)
【真题再现】
1.(2022·广东卷)下列关于Na的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:OH2HCO2 HCO2H O
3 3 2
B.碱转化为两种盐:2OHCl ClOClH O
2 2
C.过氧化物转化为碱: 2O22H O4OHO
2 2 2D.盐转化为另一种盐: Na SiO 2H H SiO 2Na
2 3 2 3
【答案】B
【解析】A.向氢氧化钠溶液中通入足量的二氧化碳,碱可以转化成酸式盐,离子方程式为:CO+OH-=
2
HCO
,故A错误;
3
B.氯气通入NaOH溶液中可以生成氯化钠和次氯酸钠两种盐,其离子方程式为:Cl+2OH-=Cl-+ClO-
2
+H O,故B正确;
2
C.钠的过氧化物为NaO,可以和水反应生成氢氧化钠,但在离子方程式里NaO 不能拆成离子,故C错
2 2 2 2
误;
D.硅酸钠溶于水,在离子方程式里要写成离子,故D错误;
故选B。
2.(2022·湖南卷)下列离子方程式正确的是
A.Cl 通入冷的NaOH溶液:Cl +2OH-=Cl-+ClO-+H O
2 2 2
B.用醋酸和淀粉-KI溶液检验加碘盐中的IO
3
-:IO
3
-+5I-+6H+=3I
2
+3H
2
O
C.FeSO 溶液中加入H O 产生沉淀:2Fe2++H O +4H O=2Fe(OH) +4H+
4 2 2 2 2 2 3
D.NaHCO 溶液与少量的Ba(OH) 溶液混合:HCO-+Ba2++OH-=BaCO +H O
3 2 3 3 2
【答案】AC
【解析】A.Cl 通入冷的 NaOH溶液中发生反应生成氯化钠和次氯酸钠,该反应的离子方程式为
2
Cl+2OH-=Cl-+ClO-+H O,A正确;
2 2
B.用醋酸和淀粉-KI溶液检验加碘盐中的IO 的原理是IO 在酸性条件下与I-发生归中反应生成I 而遇淀
3 3 2
粉变蓝,由于醋酸是弱酸,在离子方程式中不能用H+表示,因此B不正确;
C.HO 具有较强的氧化性,FeSO 溶液中加入HO 产生的沉淀是氢氧化铁,该反应的离子方程式为2Fe2+
2 2 4 2 2
+ H O+4H O=2Fe(OH) ↓+4H+,C正确;
2 2 2 3
D.NaHCO 溶液与少量的Ba(OH) 溶液混合后发生反应生成碳酸钡沉淀、碳酸钠和水,NaHCO 过量,
3 2 3
Ba(OH) 全部参加反应,因此该反应的离子方程式为2HCO+Ba2++2OH-=BaCO ↓+CO2+2H O,D不正确;
2 3 3 3 2
综上所述,本题选AC。
3.(2022·全国甲卷)能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH+2H O=AlO+4NH
3 2 2 4
C.硅酸钠溶液中通入二氧化碳:SiO 2 +CO +H O=HSiO+HCO
3 2 2 3 3
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO 2
2 4 4 4
=BaSO ↓+2H O
4 2
【答案】D
【解析】A.硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为NO或NO ,反应
2的离子方程式为4H++2NO+S2-=S↓+2NO↑+2H O(浓)或8H++2NO+3S2-=3S↓+2NO↑+4H O(稀),A错误;
3 2 2 3 2
B.明矾在水中可以电离出Al3+,可以与氨水中电离出的OH-发生反应生成Al(OH) ,但由于氨水的碱性较
3
弱,生成的Al(OH) 不能继续与弱碱发生反应,故反应的离子方程式为Al3++3NH·H O=Al(OH) ↓+3NH,
3 3 2 3 4
B错误;
C.硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则根据其通入的量
2 2
的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO +H O+CO=H SiO↓+CO (CO 少量)或SiO
3 2 2 2 3 3 2
2 +2H O+2CO=H SiO↓+2HCO(CO 过量),C错误;
3 2 2 2 3 3 2
D.将等物质的量浓度的Ba(OH) 与NH HSO 溶液以体积比1:2混合,Ba(OH) 电离出的OH-与NH HSO
2 4 4 2 4 4
电离出的H+反应生成水,Ba(OH) 电离出的Ba2+与NH HSO 电离出的SO 2 反应生成BaSO 沉淀,反应的
2 4 4 4 4
离子方程为为Ba2++2OH-+2H++SO 2 =BaSO ↓+2H O,D正确;
4 4 2
故答案选D。
4.(2022·广东卷)实验室进行粗盐提纯时,需除去Ca2+、Mg2+和SO2 ,所用试剂包括BaCl 以及
4 2
A.Na CO、NaOH、HCl B.Na CO、HCl、KOH
2 3 2 3
C.K CO、HNO、NaOH D.Na CO、NaOH、HNO
2 3 3 2 3 3
【答案】A
【解析】除杂过程中不能引入新杂质,同时为保证除杂完全,所加除杂试剂一般过量,然后选择合适的试
剂将所加过量的物质除去。
粗盐中主要成分为NaCl。除去Ca2+选用CO2将其转化为沉淀,为了不引入新杂质,所加物质的阳离子为
3
Na+,即选用NaCO 除去Ca2+,同理可知,除去Mg2+需选用NaOH,除去SO2 需选用BaCl ,因所加除杂
2 3 4 2
试剂均过量,因此向粗盐样品中加入除杂试剂的顺序中,BaCl 先于NaCO 加入,利用NaCO 除去Ca2+和
2 2 3 2 3
多余的BaCl ,因NaCO、NaOH均过量,成为新杂质,需要过滤后向滤液中加入HCl,至溶液中不再有
2 2 3
气泡产生,以此除去NaCO、NaOH,然后将溶液蒸干得到较为纯净的食盐产品,综上所述,答案为A。
2 3
5.(2022·全国乙卷)某白色粉末样品,可能含有Na SO 、Na SO 、Na S O 和Na CO 。取少量样品进
2 4 2 3 2 2 3 2 3
行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
2
该样品中确定存在的是
A.Na SO、Na S O B.Na SO、Na S O
2 4 2 2 3 2 3 2 2 3
C.Na SO、Na CO D.Na SO、Na CO
2 4 2 3 2 3 2 3
【答案】A
【解析】由题意可知,①取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之间能共存,②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体放出,说明固体中存在NaSO,发生反应SO2-
2 2 3 2 3
+2H+=S↓+H O+SO ↑,离心分离,③取②的上层清液,向其中滴加BaCl 溶液,有沉淀生成,则沉淀为
2 2 2
BaSO,说明固体中存在NaSO ,不能确定是否有NaSO 和NaCO,NaSO 与过量盐酸反应生成二氧化
4 2 4 2 3 2 3 2 3
硫,NaCO 与过量盐酸反应生成二氧化碳,而这些现象可以被NaSO 与过量盐酸反应的现象覆盖掉,综
2 3 2 2 3
上分析,该样品中确定存在的是:NaSO 、NaSO,
2 4 2 2 3
答案选A。
6.(2021·广东)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方程式书
写正确的是
A.Na O 放入水中:Na O H O2NaOHO
2 2 2 2 2 2
B.H O(g)通过灼热铁粉: 3H O2FeFe O 3H
2 2 2 3 2
C.铜丝插入热的浓硫酸中:CuH SO CuSO H
2 4 4 2
D.SO 通入酸性 KMnO 溶液中:5SO 2H O2MnO 5SO2 4H 2Mn2
2 4 2 2 4 4
【答案】D
【详解】
A.Na O 放入水中化学方程式应该是:2Na O 2H O4NaOHO ,A选项中氧元素不守恒,
2 2 2 2 2 2
A错误;
H O(g)
B. 通过灼热铁粉应高温条件下生成四氧化三铁和氢气,B错误;
2
C.铜丝插入热的浓硫酸中生成的气体不是氢气,应是二氧化硫,C错误;
D.SO
2
通入酸性KMnO
4
溶液中,SO
2
被MnO-
4
氧化为SO2
4
- ,MnO-
4
被SO
2
还原为Mn2+,再根据得失
电子守恒、电荷守恒和元素守恒可得离子方程式为5SO 2H O2MnO 5SO2 4H 2Mn2 ,D
2 2 4 4
正确;
故选D。
7.(2021·湖南)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
粒子组 判断和分析
不能大量共存,因发生反应:
A Na、Al3、Cl、NH H O
3 2 Al3 4NH H O=AlO 4NH 2H O
3 2 2 4 2
不能大量共存,因发生反应:
B H、K、S
2
O
3
2 、SO2
4
2H S O2=SSO H O
2 3 2 2
C Na、Fe3、SO2 、H O 能大量共存,粒子间不反应
4 2 2
D H、Na、Cl、MnO 能大量共存,粒子间不反应
4【答案】B
【详解】
A.Al3+和NH HO生成Al(OH)
沉淀而不是生成AlO
,故A错误;
3 2 3 2
B.S
O2
和H+反应生成单质硫、二氧化硫和水,离子方程式为:2H++ S
O2
=S↓+SO↑+H O,故B正确;
2 3 2 3 2 2
C.Fe3+可以将HO 氧化得Fe2+和O,不能大量共存,故C错误;
2 2 2
D.在酸性条件下MnO
能将Cl-氧化为Cl,不能大量共存,故D错误;
4 2
答案选B。
【优选特训】
1.滴有酚酞的Ba(OH) 溶液显红色,在上述溶液中分别滴加X溶液后有下列现象。下列说法不正确的是(
2
)
序号 装置 X溶液 现象
Ⅰ 盐酸 溶液红色褪去,无沉淀,灯泡亮度没有明显变化
溶液红色不变,有白色沉淀生成,灯泡亮度没有
Ⅱ NaSO 溶液
2 4
明显变化
Ⅲ HSO 溶液 溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗
2 4
A.实验Ⅰ中溶液红色褪去,说明发生了反应:H++OH-===H O
2
B.实验Ⅱ中溶液红色不变,且灯泡亮度没有明显变化,说明溶液中依然存在大量的Na+与OH-
C.实验Ⅲ中溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗,说明发生了反应:Ba2++2OH-+2H++
SO===BaSO ↓+2HO
4 2
D.将实验Ⅱ中NaSO 溶液换成CuSO 溶液,现象与原实验Ⅱ中的现象相同
2 4 4
【答案】D
【解析】CuSO 与Ba(OH) 发生复分解反应:Ba(OH) +CuSO ===BaSO ↓+Cu(OH) ↓,溶液中离子浓度减
4 2 2 4 4 2
小,灯泡逐渐变暗,氢氧根离子浓度减小,红色褪去,而且有蓝色沉淀生成,与加入NaSO 溶液的实验现
2 4
象不同,故D符合题意。
2.(2022·广东梅州·一模)宏观—微观—符号是化学的三重表征,下列说法对应的离子方程式正确的是
A.氯化铁溶液腐蚀铜箔:Fe3++Cu=Fe2++Cu2+
B.侯氏制碱法中NaHCO 晶体的制备:NH +CO +H O=HCO+NH
3 3 2 2 3 4
C.软锰矿与浓盐酸加热制取Cl:MnO +4Cl-+4H+=MnCl +2H O+Cl ↑
2 2 2 2 2
D.含氢氧化铝的胃舒平治疗胃酸过多:Al(OH) +3H+=Al3++3H O
3 2
【答案】D
【解析】
A.离子方程式应满足电荷守恒,氯化铁溶液腐蚀铜箔:2Fe3++Cu═2Fe2++Cu2+,故A错误;B.侯氏制碱法中NaHCO 的制备原理为:NaCl+NH +CO +H O=NaHCO ↓+NHCl,改为离子方程式为:
3 3 2 2 3 4
Na++NH+CO +H O═NaHCO↓+NH,故B错误;
3 2 2 3 4
C.软锰矿(二氧化锰)与浓盐酸混合加热制取Cl 的离子反应为MnO +4H++2Cl-=Mn2++Cl↑+2H O,故C错
2 2 2 2
误;
D.氢氧化铝和胃酸中的盐酸反应生成氯化铝和水,反应的离子方程式为:Al(OH) +3H+=Al3++3H O,故D
3 2
正确;
故选:D。
3.(2022·北京西城·一模)下列方程式不能准确解释相应实验现象的是
Δ
A.MnO 和浓盐酸共热产生黄绿色气体:MnO +4H++2Cl- Mn2++Cl +2H O
2 2 2 2
B.Na加入滴有酚酞的水中,溶液变红:2Na+2H O=2Na2OH H
2 2
Δ
C.加热Fe和S的混合物生成黑色固体:2Fe+3S Fe S
2 3
D.加热蓝色的CuCl 溶液,溶液变绿: [Cu(H O) ]2+(aq,蓝色) +4Cl-(aq) [CuCl ]2-(aq,黄色)+4H O(l)
2 2 4 4 2
【答案】C
【解析】A.MnO 和浓盐酸共热产生黄绿色气体Cl,其离子反应方程式为
2 2
Δ
MnO +4H++2Cl- Mn2++Cl +2H O,故A项正确;
2 2 2
B.Na加入滴有酚酞的水中,发生反应生成NaOH,溶液呈碱性,酚酞遇碱变红,其离子反应方程式为:
2Na+2H O=2Na2OHH ,故B项正确;
2 2
Δ
C.加热Fe和S的混合物生成黑色固体FeS,其化学反应方程式为Fe+S FeS,故C项错误;
D.加热蓝色的CuCl 溶液,溶液变绿,体系中发生了络合反应生成了黄色的[CuCl ]2-,且正反应方向吸热,
2 4
最终看到的绿色是它们的混合颜色,其离子反应方程式为:[Cu(H O) ]2+(aq,蓝色)+4Cl-(aq) [CuCl ]2-(aq,
2 4 4
黄色)+4H O(l) ΔH>0,故D项正确;
2 ⇌
答案选C。
4.下列反应的离子方程式正确的是( )
A.氢氧化钠溶液中通入少量二氧化硫:SO +OH-=== HSO
2
B.碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO+Ba2++OH-=== BaCO↓+HO
3 2
C.盐酸滴入氨水中:H++OH-=== H O
2
D.碳酸钙溶解于稀硝酸中:CO+2H+ ===CO ↑+HO
2 2
【答案】B
【解析】氢氧化钠和二氧化硫量的大小关系决定了反应产物,氢氧化钠溶液中通入少量二氧化硫:SO +
2
2OH-===SO+HO,故A错误;碳酸氢钠溶液与足量氢氧化钡溶液混合,则氢氧化钡剩余,发生反应:
2
HCO+Ba2++OH-===BaCO ↓+HO,故B正确;NH ·H O是弱碱,在离子方程式中不能拆,盐酸滴入氨
3 2 3 2
水中:H++NH ·H O===H O+NH,故C错误;碳酸钙是难溶物,不能拆成离子形式,反应为CaCO +2H
3 2 2 3+===CO ↑+HO+Ca2+,故D错误。
2 2
5.下列离子方程式书写正确的是
A.向CuSO 溶液中通入H S气体:Cu2++S2-=CuS
4 2
B.将FeO固体放入稀硝酸中:FeO+2H+=Fe2++H O
2
C.NaHSO 溶液与BaOH 溶液反应至溶液是中性;2H++SO2-+Ba2++2OH-=BaSO +2H O
4 2 4 4 2
D.向FeCl 溶液中加入铜粉:Fe3++Cu=Fe2++Cu2+
3
【答案】C
【解析】
A.H S是弱电解质,需体现在方程式中,Cu2++H S=CuS2H ,A错误;
2 2
B.硝酸有强氧化性,能氧化Fe2为Fe3并生成NO与水,3FeO+10H++NO=3Fe3++5H O+NO,B错误;
3 2
C.NaHSO 溶液与BaOH 溶液反应至溶液是中性;2H++SO2-+Ba2++2OH-=BaSO +2H O,C正确;
4 2 4 4 2
D.向FeCl 溶液中加入铜粉:2Fe3++Cu=2Fe2++Cu2+,D错误;
3
答案选C。
6.(2022·北京通州·一模)下列用于解释事实的方程式书写不正确的是
A.新切开的钠的光亮表面在空气中很快变暗:4NaO =2Na O
2 2
B.将 通入苯酚钠溶液中出现浑浊:2 +CO +H O→2 +Na CO
CO 2 2 2 3
2
C.向AlCl 溶液中滴加氨水产生白色沉淀:Al3 3NH H OAl(OH) 3NH
3 3 2 3 4
D.向AgCl悬浊液中滴加KI溶液产生黄色沉淀:AgCl(s)I(aq)AgI(s)Cl(aq)
【答案】B
【解析】A.钠的还原性强,能与空气中的氧气迅速反应生成氧化钠,所以新切开的钠的光亮表面在空气
中很快变暗,反应的方程式为4NaO =2Na O,故A正确;
2 2
B.二氧化碳与苯酚钠溶液反应生成苯酚和碳酸氢钠,反应的方程式为 +CO +H O→
2 2
+NaHCO ,故B错误;
3
C.氯化铝溶液与氨水反应生成氢氧化铝白色沉淀和氯化铵,反应的离子方程式为
Al3 3NH H OAl(OH) 3NH ,故C正确;
3 2 3 4
D.氯化银的溶度积小于碘化银,向氯化银悬浊液中滴加碘化钾溶液产生黄色沉淀的反应为氯化银与碘化
钾溶液反应生成碘化银和氯化钾,反应的离子方程式为AgCl(s)I(aq)AgI(s)Cl(aq),故D正确;
故选B。
7.(2022·湖北武汉·模拟预测)对于下列实验,能正确描述其反应的离子方程式是A.向氢氧化钡溶液中滴加硫酸氢钠溶液:H OH=H O
2
B.向覆铜板上滴加FeCl 溶液:2Fe3 Cu=2Fe2 Cu2
3
C.向纯碱溶液中滴加少量盐酸:CO22H=CO H O
3 2 2
D.向次氯酸钙溶液中通入少量SO 气体:2ClOSO H O=2HClOSO2
2 2 2 3
【答案】B
【解析】
A.氢氧化钡溶液中滴加硫酸氢钠溶液,还会生成硫酸钡沉淀,A错误;
B.铜和氯化铁反应生成氯化铜和氯化亚铁:2Fe3 Cu=2Fe2 Cu2,B正确;
C.纯碱溶液中滴加少量盐酸生成碳酸氢钠和氯化钠,CO2- +H+= HCO- ,C错误;
3 3
D.次氯酸根离子具有氧化性,会和二氧化硫生成硫酸根离子,SO +3 ClO-+ H O =SO2- +Cl-+2HClO,D错
2 2 4
误;
故选B。
8.常温下,下列各组离子能大量共存的是( )
A.Mg2+、Na+、MnO、SO
B.Fe2+、NH、NO、H+
C.OH-、Na+、SO、Cu2+
D.Al3+、K+、CO、Cl-
答案 A
解析 Fe2+和NO、H+三者发生氧化还原反应不共存,B项错误;OH-和Cu2+生成沉淀不共存,C项错误;
Al3+和CO发生相互促进的水解反应不共存,D项错误。
9.(2022·重庆·一模)常温下,下列各组离子在指定环境中一定能大量共存的是
A.澄清透明的中性溶液:Fe3、Ba2、Cl、NO
3
B.能使pH试纸变深红的溶液:K、Na、I、CrO2
4
C.pH13的NaOH溶液:Na、Cl、SO2、AlO
4 2
D.c
OH-
< K
w
的溶液:Ca2、K、NO
2
、CHCOO
【答案】C
【解析】
A.铁离子在溶液中水解使溶液呈酸性,澄清透明的中性溶液不可能存在铁离子,故A错误;
B.能使pH试纸变深红的溶液为酸性溶液,酸性溶液中铬酸根离子会转化为重铬酸根离子,重铬酸根离子
会与碘离子发生氧化还原反应,不能大量共存,故B错误;
C.Na、Cl、SO2、AlO四种离子在pH为13的氢氧化钠溶液中不发生任何反应,能大量共存,故C
4 2
正确;D.c
OH-
< K 的溶液为酸性溶液,酸性溶液中亚硝酸根离子和醋酸根离子能与氢离子反应,不能大量
w
共存,故D错误;
故选C。
10.(2022·湖南长沙·一模)25℃时,下列各组离子或分子在指定溶液中一定能大量共存的是
A.由水电离的c H 11014molL1 的溶液中:NO
3
、I、Na、Al3
B.甲基橙呈红色的溶液:NH、Ba2、AlO、Cl
4 2
C.0.1molL1FeCl
3
溶液:K、H、SO2
4
、MnO
4
Kw
11013molL1
D.
c
H 的溶液中:
NH
、
Ca2
、
Cl
、
NO
4 3
【答案】D
【解析】
A.由水电离的c H 11014molL1 的溶液中存在大量氢离子或氢氧根离子,Al3与氢氧根离子反应,
在溶液中一定不能大量共存;若溶液中存在大量氢离子时,硝酸根离子、氢离子和碘离子发生氧化还原反
应,不能大量共存,故A错误;
B.甲基橙呈红色的溶液中存在大量氢离子,NH、AlO之间发生双水解反应,AlO与氢离子反应,在溶
4 2 2
液中不能大量共存,故B错误;
C.氯化铁溶液含Cl,具有还原性,与H、MnO发生氧化还原反应,在溶液中不能大量共存,故C错误;
4
Kw
c OH =11013molL1
D.
c
H 的溶液中存在大量氢离子,四种离子之间不反应,在溶液中能够大量
共存,故D正确;
故选:D。
11.(2022·湖南·岳阳市教育科学技术研究院二模)下列各组澄清溶液中离子能大量共存,且加入X试剂
后发生反应的离子方程式书写正确的是
选项 离子组 X试剂 离子方程式
A Na+、Fe3+、SO 2 4 、Cl- 过量H 2 S 2Fe3++H 2 S=2Fe2++S↓+2H+
B Fe2+、K+、NO3 、Br- 少量HI 4H++3Fe2++NO3 =3Fe3++NO↑+2HO
2
C NH4 、Fe3+、AlO2 、Na+ 少量铜粉 2Fe3++Cu=2Fe2++Cu2+
D AlO2 、Na+、K+、HCO3 过量HCl 5H++HCO3 +AlO -=Al3++CO ↑+3H O
2 2 2
【答案】A【解析】A.Na+、Fe3+、SO 2 、Cl-之间不反应,能够大量共存,加入过量HS后发生反应:2Fe3+
4 2
+H S═2Fe2++S↓+2H+,故A正确;
2
B.Fe2+、K+、NO、Br-之间能够大量共存,但I-的还原性大于Fe2+,加入少量HI后只有I-被氧化,正确的
3
离子方程式为8H++6I-+2NO═3I +2NO↑+3HO,离子方程式书写错误,故B错误;
3 2 2
C.AlO与Fe3+发生双水解反应,离子反应为:3AlO+Fe3++6H O═Fe(OH) ↓+3Al(OH) ↓,在溶液中不能大
2 2 2 3 3
量共存,故C错误;
D.AlO、HCO之间发生双水解反应,不能大量共存,不满足题干要求,故D错误;
2 3
故选:A。
12.(2022·湖南衡阳·二模)下列各组澄清溶液中的离子能大量共存,且加入试剂后发生反应的离子方程
式书写正确的是
选
离子 试剂 离子方程式
项
A NH4 、Mg2+、Fe3+、SO 2 4 少量铜粉 Fe3++Cu=Fe2++Cu2+
B Fe2+、H+、Cl-、NO3 KNO 3 溶液 3Fe2++ NO3 +4H+=3Fe3++NO↑+2H 2 O
C K+、Na+、ClO-、SO 2 4 少量SO 2 SO 2 +H 2 O+ClO-=SO 2 4 +HClO+Cl-
D K+、Na+、SO3 2 、AlO2 少量NH 4 Cl NH4 +AlO2 +2H 2 O=Al(OH) 3 ↓+NH 3 ·H 2 O
【答案】D
【解析】A.NH、Mg2+、Fe3+、SO 2 之间互不反应,能够共存,Cu和Fe3+反应,电子不守恒、电荷不守
4 4
恒,离子方程式应该为:2Fe3++Cu=2Fe2++Cu2+,A错误;
B.NO与H+、Fe2+会发生氧化还原反应,不能大量共存,离子方程式书写合理,B错误;
3
C.K+、Na+、ClO-、SO 2 之间互不反应,能够大量共存;通入少量SO ,ClO-与SO 发生氧化还原反应。
4 2 2
当SO 少量,ClO-过量时,离子方程式应该为:SO +H O+3ClO-=SO 2 +2HClO+Cl-,C错误;
2 2 2 4
D.K+、Na+、SO 2 、AlO之间互不反应,能够共存;加入少量NH Cl时,NH与AlO-反应生成Al(OH)
4 2 4 4 2 3
沉淀和NH ·H O,反应的离子方程式为:NH+ AlO+2H O= Al(OH) ↓+ NH ·H O, D正确;
3 2 4 2 2 3 3 2
故合理选项是D。
13.(2022·北京西城·一模)向100mL 0.01mol/L BaOH 溶液中滴加0.1mol/L NaHCO 溶液,测得溶液
2 3
电导率的变化如图。下列说法不正确的是A.BaOH 和NaHCO 都是强电解质
2 3
B.A→B电导率下降的主要原因是发生了反应:Ba22OH2HCO=BaCO 2H OCO2
3 3 2 3
C.B→C,溶液中的c
OH
减小
D.A、B、C三点水的电离程度:A<B<C
【答案】B
【解析】A. BaOH 和NaHCO 在溶液中均完全电离,均属于强电解质,故A正确;
2 3
B.A→B加入NaHCO 的物质的量小于BaOH 的物质的量,发生的反应为
3 2
Ba2++OH-+HCO-=BaCO H O,故B错误;
3 3 2
C.B→C时加入的NaHCO 继续消耗氢氧根离子,C点两者恰好完全反应,因此B→C溶液中c
OH
减小,
3
故C正确;
D.酸或碱抑制水的电离,含有弱离子的盐水解促进水的电离,A点溶液中全部是BaOH
,水的电离受到
2
抑制,电离程度最小,B点为反应一半点,氢氧化钡还有剩余,C点BaOH 和NaHCO 恰好完全反应,因
2 3
此水的电离程度:A<B<C,故D正确;
答案选B。
14.对某无色溶液分别进行下列操作,所得现象和结论均正确的是( )
A.加入氨水,产生白色沉淀,证明原溶液中存在Al3+
B.加入AgNO 溶液,产生白色沉淀,证明原溶液中存在Cl-
3
C.加入盐酸酸化的BaCl 溶液,生成白色沉淀,证明原溶液中存在SO
2
D.加入NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,证明原溶液中存在NH
答案 D
解析 A项,加入氨水,产生白色沉淀,该白色沉淀可能为氢氧化镁,原溶液中可能存在 Mg2+,错误;B
项,加入AgNO 溶液,产生白色沉淀,该白色沉淀可能为碳酸银,原溶液中可能含有 CO,错误;C项,
3
加入盐酸酸化的BaCl 溶液,生成白色沉淀,该白色沉淀可能为氯化银,原溶液中可能含有Ag+,错误。
2
15.(2022·湖南岳阳·一模)下列离子组中加(或通)入相应试剂后,判断和分析均正确的是
选项 离子组 加(或通)入试剂 判断和分析AlO- HCO-
A Na+、K+、 AlO- 2、Cl- 足量NaHCO 3 溶液
不能大量共存,因 2和 3之间会发生完全双
水解生成CO 气体和Al(OH) 沉淀
2 3
Na+、Mg2+、 SO2 4 - 、 不能大量共存,会发生下列反应
B 足量NaOH溶液
HCO- Mg2++HCO
3
-+OH-=MgCO
3
+H
2
O
3
NH+
4、Ca2+、Cl-、
C 足量CO 能大量共存,粒子间不反应
2
NO-
3
不能大量共存,会发生下列氧化还原反应
D Na+、K+、ClO-、Cl- 少量SO
2 ClO-+H O+SO =Cl-+SO2-+2H+
2 2 4
【答案】C
【解析】
A.向含有Na+、K+、AlO- 、Cl-离子的溶液中加入足量NaHCO 溶液,AlO- 与HCO-电离产生的H+及溶液
2 3 2 3
中的HO反应产生Al(OH) 沉淀而不能大量共存,反应的离子方程式为:AlO- +HCO-+H O=Al(OH) ↓+
2 3 2 3 2 3
CO2
,A错误;
3
B.Mg(OH) 比MgCO 溶解度更小,向含有Na+、Mg2+、SO2- 、HCO-的溶液中加入足量NaOH溶液,
2 3 4 3
Mg2+、OH-会反应产生Mg(OH) 沉淀,不能大量共存;HCO- 、OH-会反应产生CO2、HO,也不能大量共
2 3 3 2
存,B错误;
C.向含有NH+、Ca2+、Cl-、NO-
的溶液中通入足量CO 气体,微粒之间不能发生任何反应,因此能大量
4 3 2
共存,C正确;
D.H+、ClO-会反应产生弱酸HClO,不能大量共存。向含有Na+、K+、ClO-、Cl-的溶液中通入少量SO 气
2
体,会发生反应:3ClO-+H O+SO =Cl-+SO2-+2HClO,不能大量共存,D错误;
2 2 4
故合理选项是C。
16.某无色溶液中可能含有①Na+、②Ba2+、③Cl-、④Br-、⑤SO、⑥SO、⑦Fe2+中的几种离子,依
次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
步骤 操作 现象
Ⅰ 用pH试纸检验 溶液的pH大于7
Ⅱ 向溶液中滴加氯水,再加入CCl ,振荡,静置 CCl 层呈橙红色
4 4
Ⅲ 取Ⅱ的上层溶液,加入Ba(NO ) 溶液和稀硝酸 有白色沉淀产生
3 2
将 Ⅲ 过滤,向滤液中加入AgNO 溶液和稀硝
3
Ⅳ 有白色沉淀产生
酸下列结论正确的是( )
A.肯定含有的离子是①④⑤
B.肯定没有的离子是②⑤⑦
C.可能含有的离子是①②⑥
D.不能确定的离子是①③⑥
【答案】A
【解析】
根据步骤Ⅰ,该溶液呈碱性,则该溶液是强碱弱酸盐溶液,所以一定存在 SO,则一定不存在Ba2+;在碱
性的无色溶液中,一定不存在Fe2+;溶液呈电中性,所以溶液中的阳离子只能是 Na+;步骤Ⅱ说明该溶液
中一定存在Br-;步骤Ⅲ不能说明有SO存在,因为该溶液中一定存在SO,加入氯水后SO被氧化为SO,
与Ba(NO ) 反应生成BaSO 沉淀;步骤Ⅳ不能确定Cl-的存在,因为加入的氯水中含有Cl-。因此一定存
3 2 4
在的离子是①④⑤,一定不存在的离子是②⑦,不能确定的离子是③⑥,故A正确。
17.一瓶无色澄清的溶液,其中可能含有H+、NH、Na+、Al3+、Fe3+、I-、NO、CO、SO、AlO。取该溶
液进行以下实验:
①用pH试纸检验,溶液呈强酸性 ②取溶液适量,加入少量CCl 和数滴新制氯水,振荡,CCl 层呈紫红
4 4
色 ③该溶液的焰色试验没有黄色;根据以上实验结果,下列推断正确的是( )
A.向该溶液中加入BaCl 不一定能观察到白色沉淀
2
B.可以确定没有Na+、Fe3+、CO、AlO,不能确定是否有NO
C.该溶液可能是NH NO 与HI的混合
4 3
D.一定没有Al3+、CO和NO
【答案】A
【解析】
不能确定是否含SO,则向该溶液中加入BaCl 不一定能观察到白色沉淀,故A正确;一定不含Na+、Fe3
2
+、NO、CO、AlO,故B错误;该溶液中一定不含NO,故C错误;不能确定是否含Al3+,故D错误。
18.根据图示信息书写方程式。
(1)NaN 是一种易溶于水(NaN ===Na++N)的白色固体,可用于有机合成和汽车安全气囊的产气等。钠法
3 3
(液氨法)制备NaN 的工艺流程如下:
3
①反应Ⅰ的化学方程式为________________________________________________________。
②销毁NaN 可用NaClO溶液,该销毁反应的离子方程式为_____________________________________(N
3
被氧化为N)。
2
(2)利用钴渣[含Co(OH) 、Fe(OH) 等]制备钴氧化物的工艺流程如下:
3 3Co(OH) 溶解还原反应的离子方程式为____________________________________________________。
3
【答案】(1)①2NaNH +NO========NaN +NH +NaOH
2 2 3 3
②ClO-+2N+HO===Cl-+2OH-+3N↑
2 2
(2)2Co(OH) +SO+4H+===2Co2++SO+5HO
3 2