文档内容
2024 年高考化学一轮收关卷
化 学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cl 35.5 Si28 Cu64 Te128
第Ⅰ卷(选择题 共42分)
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.2023年10月31日8时11分,神舟十六号载人飞船返回舱在东风着陆场成功着陆,神舟十六号载人飞
行任务取得圆满成功。下列有关说法中错误的是
A.神舟十六号返回舱在着陆前会先抛掉多余的推进剂——水合肼 ,水合肼难溶于水
B.神舟十六号太阳敏感器光学窗口上的石英玻璃主要成分是二氧化硅
C.神舟十六号飞船返回舱侧壁金属壳体用的是铝合金材料,其硬度比纯铝的大
D.神舟十六号飞船返回舱“外衣”中的酚醛树脂属于合成有机高分子化合物
2.三水硫氰化亚铁 可用作有机溶液中过氧化物的指示剂,其中S、C、N三原子没有形成
大 键。下列有关推断不正确的是
A. 电子式为
B. 露置在空气中比 更易氧化
C. 配成溶液,加入过量过氧化氢,溶液最后显红色
D.还原性铁粉与HSCN溶液在隔绝空气条件下可制备硫氰化亚铁
3.下列化学用语表示正确的是
A.溴的简化电子排布式:
B.1-丁醇的键线式:
C. 形成的 键模型:
D.水的VSEPR模型:
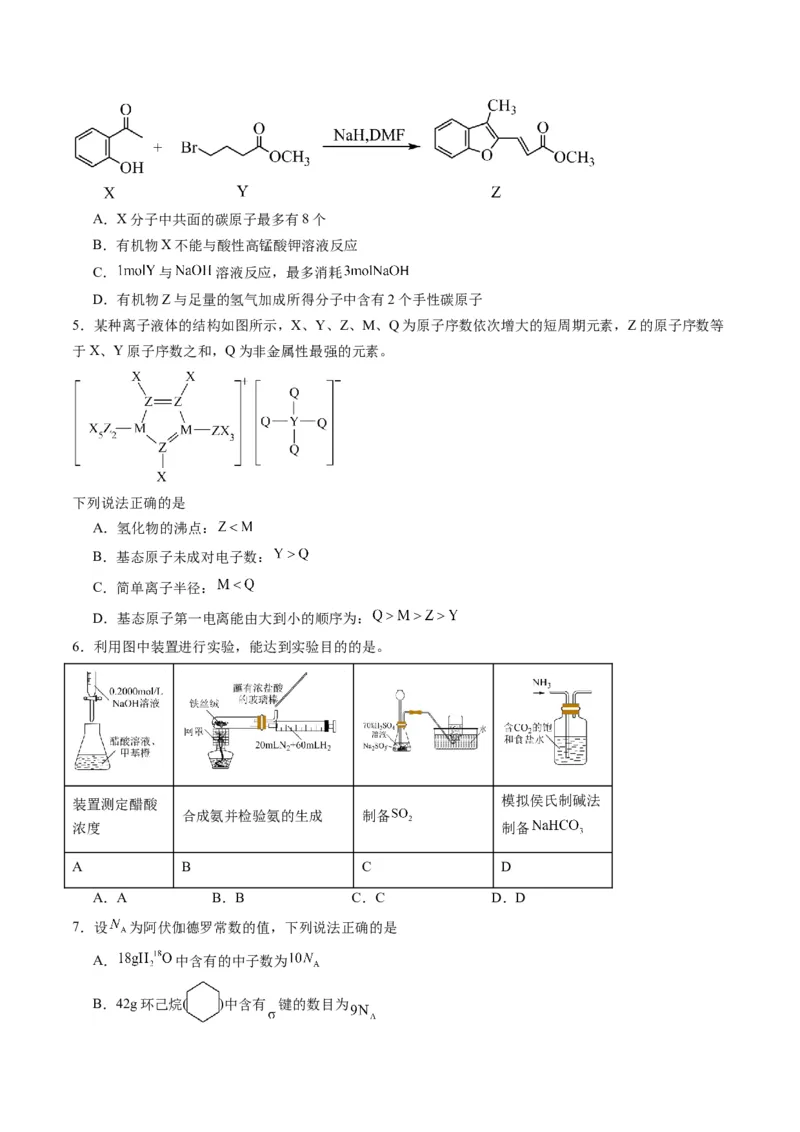
4.药物异搏定合成路线中的某一步反应如图所示(部分产物未给出),下列说法正确的是A.X分子中共面的碳原子最多有8个
B.有机物X不能与酸性高锰酸钾溶液反应
C. 与 溶液反应,最多消耗
D.有机物Z与足量的氢气加成所得分子中含有2个手性碳原子
5.某种离子液体的结构如图所示,X、Y、Z、M、Q为原子序数依次增大的短周期元素,Z的原子序数等
于X、Y原子序数之和,Q为非金属性最强的元素。
下列说法正确的是
A.氢化物的沸点:
B.基态原子未成对电子数:
C.简单离子半径:
D.基态原子第一电离能由大到小的顺序为:
6.利用图中装置进行实验,能达到实验目的的是。
装置测定醋酸 模拟侯氏制碱法
合成氨并检验氨的生成 制备
浓度 制备
A B C D
A.A B.B C.C D.D
7.设 为阿伏伽德罗常数的值,下列说法正确的是
A. 中含有的中子数为
B.42g环己烷( )中含有 键的数目为C.标准状况下, 中含有的分子数为
D. 与足量NaOH溶液反应,所得溶液中 的个数为
8.下列过程中对应的离子方程式正确的是
A.向苯酚钠溶液中通入少量 :
B.酚酞滴入碳酸钠溶液中变红:
C.同浓度同体积明矾 溶液与 溶液混合:
D.用醋酸和淀粉 溶液检验加碘盐中的 :
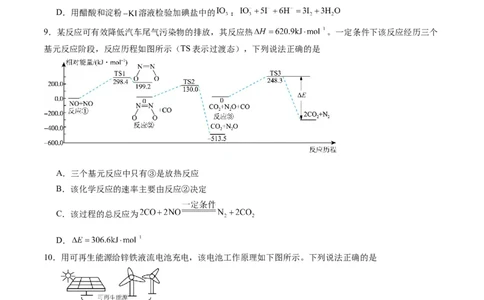
9.某反应可有效降低汽车尾气污染物的排放,其反应热 。一定条件下该反应经历三个
基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法正确的是
A.三个基元反应中只有③是放热反应
B.该化学反应的速率主要由反应②决定
C.该过程的总反应为
D.
10.用可再生能源给锌铁液流电池充电,该电池工作原理如下图所示。下列说法正确的是
A.放电时,M为正极
B.放电时,M极发生的电极反应为:
C.充电时, 穿过交换膜进入N极室D.充电时,总反应为:
11.用绿矾( )制备电池电极材料 的流程如下:
下列说法正确的是
A.反应1中 转化为
B.可用酸性 溶液检验反应1中 是否完全反应
C.可以使用KSCN溶液检验 沉淀是否洗涤干净
D.反应2中氧化剂与还原剂的物质的量之比为2:1
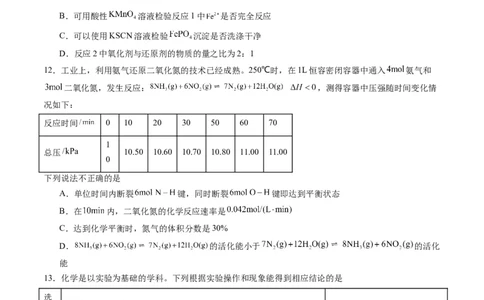
12.工业上,利用氨气还原二氧化氮的技术已经成熟。250℃时,在1L恒容密闭容器中通入 氨气和
二氧化氮,发生反应: ,测得容器中压强随时间变化情
况如下:
反应时间 0 10 20 30 50 60 70
1
总压 10.50 10.60 10.70 10.80 11.00 11.00
0
下列说法不正确的是
A.单位时间内断裂 键,同时断裂 键即达到平衡状态
B.在 内,二氧化氮的化学反应速率是
C.达到化学平衡时,氮气的体积分数是30%
D. 的活化能小于 的活化
能
13.化学是以实验为基础的学科。下列根据实验操作和现象能得到相应结论的是
选
实验操作和现象 结论
项
向麦芽糖溶液中加入少量稀硫酸,加热,滴加NaOH溶液调至呈碱
A 麦芽糖水解产物具有还原性
性,再加入银氨溶液,水浴加热,可观察到产生银镜
常温下,向 溶液中加入 溶液,将带火星的木条放在试管
B 氧化性:
口,木条复燃
C 向2mL 0.01 KI溶液中加入5mL 0.01 溶液,溶 和 的反应存在限度液呈棕黄色,再滴加几滴KSCN溶液,溶液变为红色
向2mL0.1 KCl溶液中先滴加4滴0.1 溶
AgCl转化为AgI,
D
液,再滴加4滴0.1 KI溶液,先产生白色沉淀,再产生黄色
沉淀
A.A B.B C.C D.D
14.含氰废水中氰化物的主要形态是HCN和CN-,CN-具有较强的配位能力,能与Cu+形成一种无限长链离
子,其片段为 ;CN-结合H+能力弱于CO 。氰化物浓度较低时,可在碱性条件
下用HO 或Cl 将其转化为N;浓度较高时,可加入HCN、Fe和KCO 溶液反应生成K[Fe(CN) ]溶液。
2 2 2 2 2 3 4 6
下列说法正确的是
A.基态Fe2+核外电子排布式为[Ar]3d54s1
B.K[Fe(CN) ]中Fe2+的配位数为6
4 6
C.Cu+与CN-形成的离子的化学式为[Cu(CN) ]2-
3
D.某铁晶体(晶胞如图所示)中与每个Fe紧邻的Fe数为6
第 II 卷(非选择题 共 58 分)
二、非选择题:本题共4个小题,共58分。
15.(14分)碳酸亚铁( )是菱铁矿的主要成分,可用作补血剂。实验室制备 的装置如下图所
示。
已知: 为白色难溶于水的固体,在潮湿的空气中易被氧化为 。回答下列问题:
(1)仪器a的名称为 。
(2)实验开始时,打开 、 ,关闭 ,其目的是 ;一段时间后 (填具体操
作),使 溶液进入仪器c中。
(3)仪器d中的试剂为 ,其作用是 。
(4)实验结束,将仪器c中的混合物过滤、洗涤、干燥,得到 粗品。①确认沉淀是否洗涤干净的操作及现象是 。
②若粗品未及时进行干燥处理,在空气中将部分变为红褐色,发生反应的化学方程式是 。
(5)由于碳酸钠溶液碱性较强,制备过程中会产生杂质 (填化学式)。若用 代替
,可制得更纯净的 ,制备过程中产生无色气体,该反应的离子方程式是 。
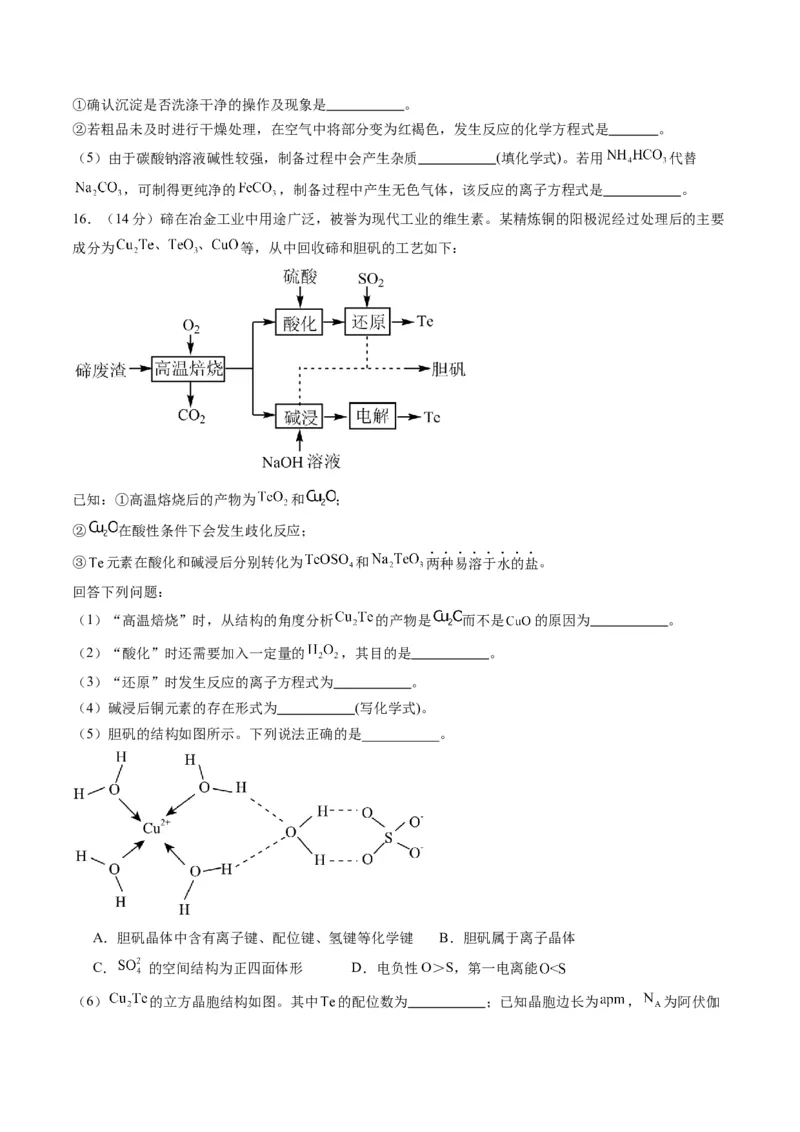
16.(14分)碲在冶金工业中用途广泛,被誉为现代工业的维生素。某精炼铜的阳极泥经过处理后的主要
成分为 等,从中回收碲和胆矾的工艺如下:
已知:①高温熔烧后的产物为 和 ;
② 在酸性条件下会发生歧化反应;
③ 元素在酸化和碱浸后分别转化为 和 两种易溶于水的盐。
回答下列问题:
(1)“高温焙烧”时,从结构的角度分析 的产物是 而不是 的原因为 。
(2)“酸化”时还需要加入一定量的 ,其目的是 。
(3)“还原”时发生反应的离子方程式为 。
(4)碱浸后铜元素的存在形式为 (写化学式)。
(5)胆矾的结构如图所示。下列说法正确的是___________。
A.胆矾晶体中含有离子键、配位键、氢键等化学键 B.胆矾属于离子晶体
C. 的空间结构为正四面体形 D.电负性O>S,第一电离能
(6) 的立方晶胞结构如图。其中 的配位数为 ;已知晶胞边长为 , 为阿伏伽德罗常数的值,则该晶体的密度为 (列出计算式即可)。
17.(15分)“氰化提金”产生的废水中含有一定量的 ,为处理含氰废水科研人员进行了大量研究。
回答下列问题:
(1)25℃,氢氰酸(HCN)、碳酸在水中的电离常数如下表:
酸 HCN
①常温下,将 的HCN溶液加水稀释至1000mL,溶液的pH 6(填“>”“<”或“=”)。
②常温下,pH相等的NaCN和 溶液相比,浓度较大的是 (填化学式)溶液。
③将少量 通入NaCN溶液中,反应的离子方程式是 。
④常温下,在 溶液中加入 溶液。所得混合溶液中离子浓度由
大到小的顺序是 。
(2)HCN的电子式是 。
(3)电解法处理含氰废水也是常用方法之一,其原理如图所示。
①电解时,阴极是 (填“A”或“B”)。
②电解时, 发生反应的电极反应式是 。
③常温下,为了研究pH对除氰效率的影响,控制电流密度为 ,电解时间1h,测得除氰效率(%)随
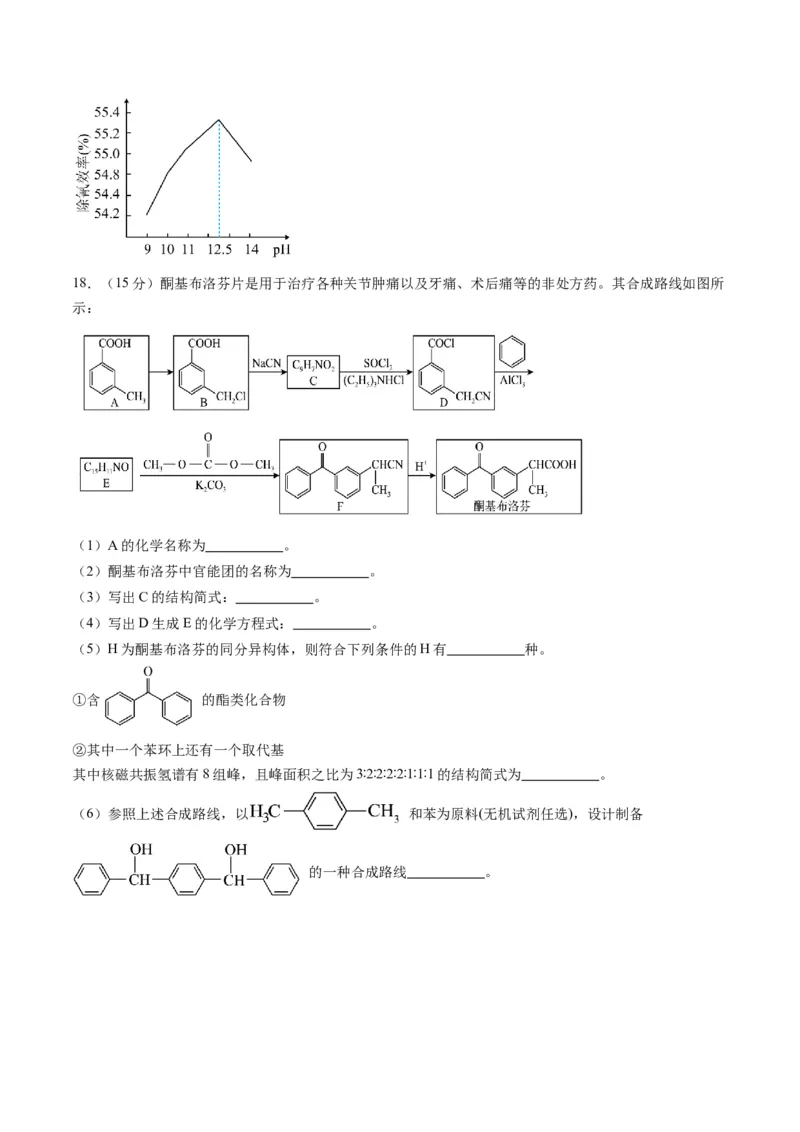
pH变化如图所示。结合图中信息分析,当 ,除氰效率降低,原因是 。18.(15分)酮基布洛芬片是用于治疗各种关节肿痛以及牙痛、术后痛等的非处方药。其合成路线如图所
示:
(1)A的化学名称为 。
(2)酮基布洛芬中官能团的名称为 。
(3)写出C的结构简式: 。
(4)写出D生成E的化学方程式: 。
(5)H为酮基布洛芬的同分异构体,则符合下列条件的H有 种。
①含 的酯类化合物
②其中一个苯环上还有一个取代基
其中核磁共振氢谱有8组峰,且峰面积之比为3∶2∶2∶2∶2∶1∶1∶1的结构简式为 。
(6)参照上述合成路线,以 和苯为原料(无机试剂任选),设计制备
的一种合成路线 。