文档内容
高考解密 02 化学常用计量
A 组 基础练
1.(2022·浙江·模拟预测) 为阿伏伽德罗常数的值,下列说法正确的是
A.24g石墨中含有0.6 个C—C键
B.1mol二氧化硅固体中含有2 个σ键
C.标准状况下 含有2.6 个质子数
D.0.6mol铁单质与水蒸气高温条件下完全反应,该反应转移1.6 个电子
【答案】D
【解析】A.石墨中平均1个碳原子形成1.5个碳碳键,24g石墨(物质的量为2mol)中含有3 个C—C
键,A错误;B.二氧化硅中1个硅原子能形成4个硅氧σ键,1mol二氧化硅固体中含有4 个σ键,B
错误;C.标准状况下乙醇为液体,不能计算其物质的量,C错误;D.铁单质与水蒸气高温条件下完全反
应生成四氧化三铁,电子转移情况为 ,0.6mol铁单质与水蒸气高温条件下完全反应,该反应转移
电子1.6mol,为1.6 个电子,D正确;故选D。
2.(2022·上海·模拟预测)将V L浓度为0.3mol/L的盐酸浓度扩大一倍,采取的措施合理的是
A.将溶液加热浓缩至原来体积的一半
B.通入标准状况下的HCl气体6.72L
C.加入3mol/L的盐酸0.2V L,再稀释至1.5V L
D.加入等体积0.9mol/L的盐酸,混合均匀
【答案】C
【解析】A.将溶液加热浓缩至原来体积的一半时,由于HCl的挥发,不能使其浓度扩大一倍,A不合理;B.标准状况下6.72LHCl的物质的量为0.3mol,但向溶液中通入HCl气体时溶液的体积会发生变化,所以
浓度不能扩大一倍,B不合理;C.V L浓度为0.3mol/L的盐酸中有0.3VmolHCl,3mol/L的盐酸0.2V L含
HCl的物质的量为0.6Vmol,稀释至1.5V L,浓度为 =0.6mol/L,C合理;D.两种盐酸混
合后,溶液的体积不能直接加和,所以混合后溶液的物质的量浓度不是原来的2倍,D不合理;综上所述
答案为C。
3.(2022·上海·模拟预测) 溶液中含有 ,取 该溶液用水稀释至VmL,则稀释
后 物质的量浓度为
A. B. C. D.
【答案】B
【解析】VmLAl (SO ) 溶液中含有Al3+mg,则 的物质的量为 mol,取 mL该溶液稀释至VmL,
2 4 3
则 的物质的量为 mol,则其物质的量浓度为 mol÷(V×10-3)L= ,故答案选B。
4.(2022·广西南宁·模拟预测)设 为阿伏加德罗常数的值。下列说法正确的是
A. 在空气中充分燃烧转移的电子数为0.2
B. 晶体中含有的离子数为2
C. 的 溶液中 数为0.2
D.密闭容器中充入 和 ,充分反应后容器内的分子总数为2
【答案】B
【解析】A.0.1mol Na在空气中充分燃烧生成NaO,转移的电子数为0.1N ,A错误;B.NaHSO 在熔融
2 2 A 4
状态下电离出Na+和 ,由此可知NaHSO 由Na+和 构成,故1mol NaHSO 晶体中含有的离子数
4 4
为2N ,B正确;C.1L pH=1的HSO 溶液中,c(H+)=0.1mol/L,则n(H+)=0.1mol/L1L=0.1mol,H+的数目
A 2 4
为0.1N ,C错误;D.根据反应2NO+O =2NO 可知,2mol NO和1mol O 反应生成2mol NO ,但NO 还
A 2 2 2 2 2会发生反应 ,故充分反应后容器内的分子总数小于2N ,D错误;故选B。
A
5.(2023·广东·深圳市光明区高级中学模拟预测)实验室中利用硫化亚铁和硫化锌混合物进行如图实验
(忽略 在水中的溶解)。下列说法错误的是。
A.“4.5g固体”一定是铁锌混合物 B.“溶液2”中的溶质只有
C.混合物中硫元素的质量分数约为38% D.反应②能生成标准状况下
【答案】C
【解析】A.4.5g固体分两种情况,可能全为Fe,也可能是Fe与Zn的混合物;假设全为Fe,
,根据Fe守恒则,n(Fe)= n(FeS)=0.08mol,
则m(FeS)=n×M=0.08mol×88g/mol=7.04g,而题目中FeS与ZnS混合物质量为6.9g,故第一种假设不正确,
即“4.5g固体”一定是铁锌混合物,A正确;B.4.5g固体中含有Zn,则溶液中午FeCl 和HCl,“溶液2”
2
中溶质只有ZnCl,B正确;C.设混合物FeS与ZnS中,硫元素的质量分数为38%,而FeS中硫的含量为
2
,ZnS中硫的含量为 ,二者混合物中硫的含量应该在33%~36%之间,
不可能为38%,C错误;D.生成 ,H守恒n(HCl)=0.05mol,n(HCl) =0.2mol,
总
Zn+2HCl=ZnCl +H ↑,Zn总量为0.1mol( ),该反应消耗的Zn为0.025mol,D正确;故
2 2
选C。
6.(2022·浙江温州·模拟预测)将40.8gFe、FeO混合物置于纯氧中加热,迅速被氧化生成46.4g Fe O,
3 4
则Fe、FeO的物质的量之比为A.1:3 B.1:2 C.1:1 D.2:1
【答案】A
【解析】46.4g Fe O 中,n(Fe O)= =0.2mol,则n(Fe)=0.6mol;40.8gFe、FeO混合物中,
3 4 3 4
n(Fe)=0.6mol,m(Fe)=0.6mol×56g/mol=33.6g,m(O)=40.8g-33.6g=7.2g,n(FeO)=n(O)= =0.45mol,则
n(Fe)=0.6mol-0.45mol=0.15mol,Fe、FeO的物质的量之比为0.15mol : 0.45mol=1 : 3,故选A。
7.(2022·浙江·模拟预测)某工厂使用的煤中硫的质量分数为1.28%,该工厂每天燃烧这种煤100t,请计
算:
(1)100t该煤含S的物质的量为_______mol。
(2)假设煤中的硫全部转化为SO ,每天产生的SO 气体在标准状况下体积为_______L。
2 2
(3)若把产生的SO 全部用来生产硫酸,每天可得到98%的浓硫酸质量_______吨(请写出计算过程)
2
【答案】(1)4×104(2)8.96×105(3)4
【解析】(1)某工厂使用的煤中硫的质量分数为1.28%,该工厂每天燃烧这种煤100t,100t该煤含S的物
质的量为 mol。
(2)由硫原子个数守恒可知,假设煤中的硫全部转化为SO ,每天产生的SO 物质的量为
2 2
mol、在标准状况下体积为4×104mol×22.4L/mol=8.96×105L。
(3)由硫原子个数守恒可知,若把产生的二氧化硫全部用来生产硫酸,理论上每天产生的硫酸的物质的
量为4×104mol,则每天可得到98%的浓硫酸的质量 ,即4吨。
8.(2021·浙江·模拟预测)25℃时,醋酸电离平衡常数 ,
溶液与 溶液混合均匀(混合后溶液体积不变)。请计算:
(1)求混合液的 _______(保留2位有效数字,下同)。(2)向混合液中加0.10mL(2滴) 盐酸,求此时溶液中 _______ 。(写出计算过程)
【答案】(1)5.0 (2)
【解析】(1)混合后溶液中:
,根据公式 ,
= ,pH ;(2)
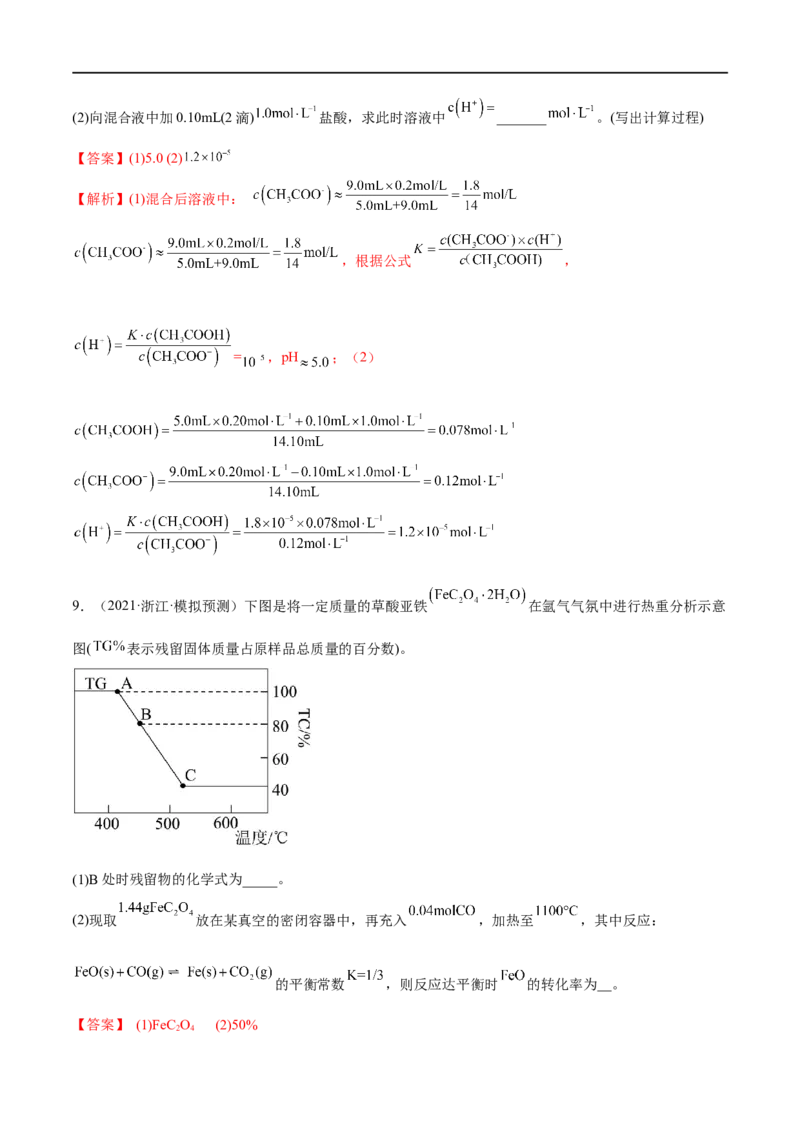
9.(2021·浙江·模拟预测)下图是将一定质量的草酸亚铁 在氩气气氛中进行热重分析示意
图( 表示残留固体质量占原样品总质量的百分数)。
(1)B处时残留物的化学式为_____。
(2)现取 放在某真空的密闭容器中,再充入 ,加热至 ,其中反应:
的平衡常数 ,则反应达平衡时 的转化率为__。
【答案】 (1)FeC O (2)50%
2 4【解析】(1)M(FeC O•2H O)=180g/mol,M(FeC O)=144g/mol;假设原FeC O•2H O有180g,则B处时,
2 4 2 2 4 2 4 2
残留固体的质量为180g80%=144g,即1mol FeC O•2H O分解,失去2mol 水变为FeC O,故B处残留固
2 4 2 2 4
体为FeC O;
2 4
(2)假设原FeC O•2H O有180g,C处时,残留固体的质量为180g40%=72g,结合题中给出的信息可得C
2 4 2
处残留的固体为FeO,则FeC O 的分解反应为 ;在密闭容器中,1.44g FeC O
2 4 2 4
(即0.01mol)分解产生0.01mol FeO、0.01mol CO、0.01mol CO ,再充入0.04mol CO,则容器中最初有
2
0.05mol CO,设容器体积为1L,且反应达到平衡时,FeO转化x mol,则反应三段式为:
则c(CO)=(0.05-x)mol/L,c(CO)=(0.01+x)mol/L,K= = = ,解得x=0.005,即0.01mol
2
FeO的在平衡时转化了0.005mol,故FeO的转化率为 =50%。
10.(2022·全国·高三专题练习)重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成
分为FeO·Cr O,还含有硅、铝等杂质。制备流程如图所示:
2 3
某工厂用m kg 铬铁矿粉(含Cr O 40%)制备KCr O,最终得到产品 m kg,产率为_______。
1 2 3 2 2 7 2
【答案】 ×100%
【解析】m kg 铬铁矿粉,含Cr O 的质量为m 40%kg,则生成KCr O 的理论质量为m 40%
1 2 3 1 2 2 7 1
kg,则所得产品的产率为 100%= ×100%。B 组 提升练
1.(2022·黑龙江·佳木斯一中三模)MOH 为一元弱碱,向 MCl 的稀溶液中不断加入蒸馏水,c(H+)随
c(M+)而变化。实验发现,某温度下,c2 (H+)~c(M+)为线性关系,如下图实线所示。
下列叙述错误的是
A.当 c(M+) = 2 ×10-4 mol·L-1时,c(OH-) = 1×10-7 mol·L-1
B.溶液中存在:c(M+) + c(H+) = c(Cl- ) + c(OH-)
C.该温度下,M+的水解平衡常数 K = 1×10-10
h
D.a 点溶液中:c(Cl-) > c(M+) > c(H+) > c(MOH) > c(OH-)
【答案】D
【解析】A.该温度下纯水溶液中c(H+)=c(OH-),Kw= c(H+) c(OH-)=c2(H+)=2 10-14,当 c(M+) = 2 ×10-4
mol·L-1 时,c2(H+)=4 10-14,K = 2 10-14,故c(OH-) = 1×10-7 mol·L-1,A正确;B.溶液呈电中性,故MCl
w
的稀溶液中始终存在:c(M+) + c(H+) = c(Cl- ) + c(OH-),B正确;C.该温度下,M+ 的水解方程式为M+
+H O MOH+H+,平衡常数 K= ,利用c(M+) = 2 ×10-4 mol·L-1 点进行计算,该点c(H+)=2×10-7
2 h
mol·L-1, c(OH-) = 1×10-7 mol·L-1,c(MOH)= c(H+)- c(OH-)= 1×10-7 mol·L-1,故K=
h
,C正确;D. ,其中c(M+)=1 10-4
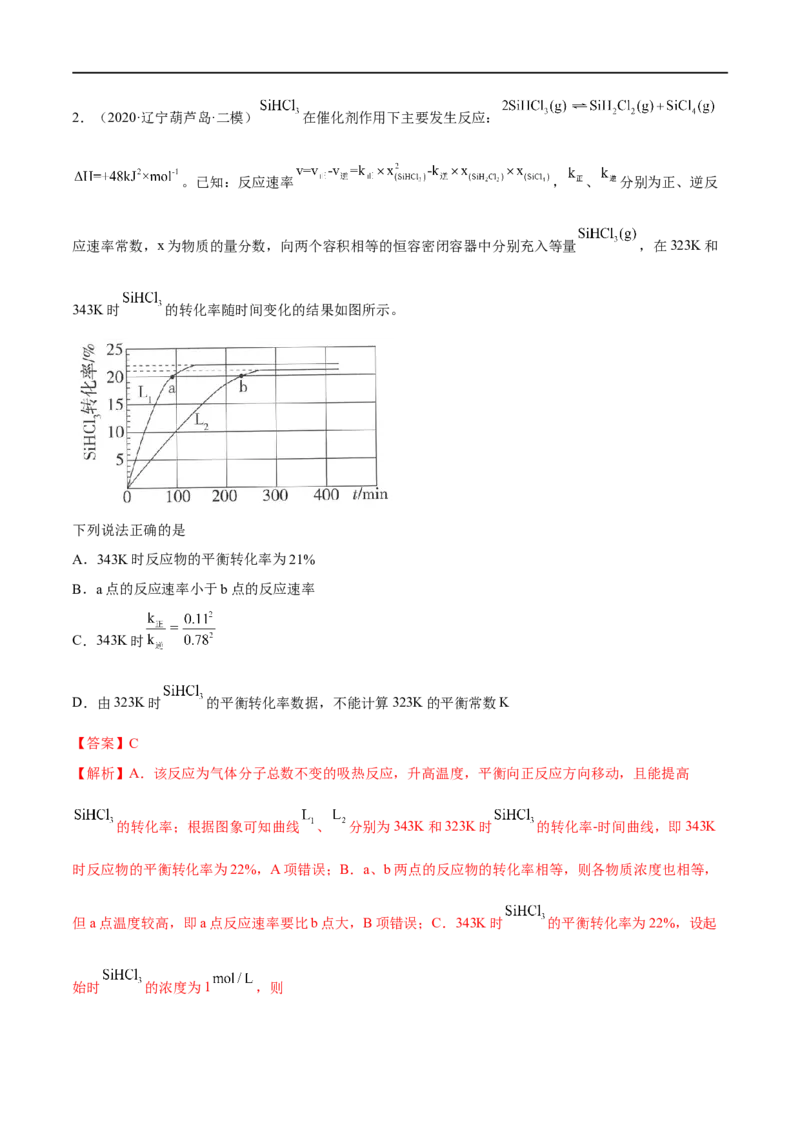
mol·L-1,c(OH-)/c(MOH)=2>1,故c(OH-)>c(MOH),D错误。2.(2020·辽宁葫芦岛·二模) 在催化剂作用下主要发生反应:
。已知:反应速率 , 、 分别为正、逆反
应速率常数,x为物质的量分数,向两个容积相等的恒容密闭容器中分别充入等量 ,在323K和
343K时 的转化率随时间变化的结果如图所示。
下列说法正确的是
A.343K时反应物的平衡转化率为21%
B.a点的反应速率小于b点的反应速率
C.343K时
D.由323K时 的平衡转化率数据,不能计算323K的平衡常数K
【答案】C
【解析】A.该反应为气体分子总数不变的吸热反应,升高温度,平衡向正反应方向移动,且能提高
的转化率;根据图象可知曲线 、 分别为343K和323K时 的转化率-时间曲线,即343K
时反应物的平衡转化率为22%,A项错误;B.a、b两点的反应物的转化率相等,则各物质浓度也相等,
但a点温度较高,即a点反应速率要比b点大,B项错误;C.343K时 的平衡转化率为22%,设起
始时 的浓度为1 ,则平衡时 ,则 ,即 ,C项正确;D.同理,
由323K时 的转化率为21%,设起始时 为1 ,根据三段式法可求出平衡时 、
、 分别为0.79 、0.105 和0.105 ,则平衡常数 ,
D项错误;答案选C。
3.(2022·山东·模拟预测)向分别盛有10mL3mol·L-1的盐酸和NaOH溶液的甲、乙两烧杯中,加入等质量
的铝粉,反应结束后,相同温度和压强测得生成的气体体积分别为V 、V ,下列说法正确的是
(甲) (乙)
A.消耗的HCl和NaOH的物质的量比为V(甲):V(乙)
B.若V(甲):V(乙)=1:2,投入的铝粉质量为0.54g
C.若V(甲):V(乙)=1:3,铝粉在两烧杯中都恰好完全反应
D.若盐酸和NaOH溶液都完全反应,两反应的电子转移数之比为1:1
【答案】B
【解析】A.此实验反应的化学方程式为2Al+6HCl=2AlCl +3H ↑,2Al+2NaOH+2H O=2NaAlO +3H ↑,通
3 2 2 2 2
过化学方程式可以看出,消耗的HCl和NaOH的物质的量比为3V :V ,A错误;B.盐酸和NaOH溶
(甲) (乙)
液中的溶质的物质的量均为0.03mol,测得生成的气体体积比为V :V =1:2,即生成的氢气物质的量
(甲) (乙)
之比是1:2,设铝与酸完全反应时,生成的氢气的物质的量为x, ,得:
x=0.015mol;相同条件下气体的物质的量之比等于体积之比,所以氢氧化钠和铝反应生成的氢气的物质的
量为:0.015mol×2=0.03mol,碱与铝反应时,铝反应完全,设铝的物质的量为y,,得:y=0.02mol,所以铝的质量为:0.02mol×27g/mol=0.54g,
B正确;C.根据方程式,当为V :V =1:3时,消耗等物质的量的HCl和氢氧化钠,铝粉过量,C错
(甲) (乙)
误;D.根据方程式,HCl完全反应,该反应中转移电子的物质的量为0.03mol,NaOH完全反应,该反应
中转移电子的物质的量为0.09mol,两反应的电子转移数之比为1:3,D错误;故答案为:B。
4.(2022·河南·模拟预测)设N 为阿伏加德罗常数的值。下列说法 正确的是
A
A.44.8 L丙烯和44.8 L丙烷中含有的碳原子数均为6N
A
B.将1mol明矾完全溶于水,所得溶液中阴离子总数小于2N
A
C.12.8g铜完全溶于未知浓度的硝酸中,转移的电子数为0.4N
A
D.1 mol苯乙烯( )与足量H 在催化剂和加热条件下反应,形成C- H键的数目最多为2
2
N
A
【答案】C
【解析】A.对于气体物质有 ,但是该条件下Vm未知,无法计算碳原子数,A项错误;B.
, 的数目为2N ,同时水电离产生阴离子,所以总数目大于2N ,B项错误;
A A
C.铜与硝酸反应中关系式为Cu~2e-, ,则电子的数目为0.4N ,C项正确;D.
A
苯乙烯中苯环消耗3molH 产生6molC-H,C=C消耗1molH 形成2molC-H,总共形成8N C-H,D项错误;
2 2 A
故选C。
5.(2022·浙江金华·二模)某兴趣小组设计实验测定“自然晶盐"的含碘量。取5.00g自然晶盐,加蒸馏水
使其完全溶解后加稀硫酸酸化并加入足量的KI溶液,使 与KI反应完全。以淀粉为指示剂,逐滴滴加
的 溶液5.00mL,达到滴定终点(反应为 )。
(1)写出 与KI反应的离子方程式___________。
(2)上述“自然晶盐"中的碘元素含量为___________mg/kg(写出计算过程,精确到小数点后一位)。【答案】(1) (2)21.2
【解析】(1)由题意可知,酸性条件下,碘酸钾与碘化钾反应生成硫酸钾、碘和水,反应的离子方程式为
;
(2)由方程式可得如下关系:KIO ~3I ~6Na SO,滴定消耗5.00mL1.0×10-3mol/L硫代硫酸钠溶液,则5.00g
3 2 2 2 3
自然晶盐中的碘元素含量为 =21.2mg/kg。
C 组 真题练
1.(2022·浙江·高考真题) 为阿伏加德罗常数的值,下列说法正确的是
A. 中含有 个阳离子
B. 乙烷和丙烯的混合气体中所含碳氢键数为
C. 含有中子数为
D. 和 于密闭容器中充分反应后, 分子总数为
【答案】C
【解析】A. 由钠离子和硫酸氢根离子构成,其中的阳离子只有钠离子, 的物质的量为0.1mol,因此,其中只含有
个阳离子,A说法不正确;B.没有指明气体的温度和压强,无法确定 乙烷和丙烯的混合气体的物质的量是多少,因此,无法确定其
中所含碳氢键的数目,B说法不正确;C. 分子中有6个中子, 的物质的量为0.5mol,因此, 含有的中子数为 ,C
说法正确;D. 和 发生反应生成 ,该反应是可逆反应,反应物不能完全转化为生成物,因此, 和 于密闭容器中
充分反应后, 分子总数小于 ,D说法不正确。综上所述,本题选C。2.(2020·浙江·高考真题)一定温度下,在2 L的恒容密闭容器中发生反应:A(g)+2B(g) 3C(g)反应过程中的部分数据如下表所示:
物质的量(n/mol)
时间(t/min)
n(A) n(B) n(C)
0 2.0 2.4 0
5 0.9
10 1.6
15 1.6
下列说法正确的是A.0~5 min用C表示的平均反应速率为0. 09 mol·L-1·min-1
B.该反应在10 min后才达到平衡
C.平衡状态时,c(C)=0.6 mol·L-1
D.物质B的平衡转化率为20%
【答案】AC
【解析】A.0~5 min内C的物质的量增加了0.9 mol,由于容器的容积是2 L,则用C物质浓度变化表示的反应速率v(C)=
,A正确;B.反应进行到10 min时,A物质的物质的量减少0.4 mol,根据物质反应转化关系可知B物质的物质
的量减少0.8 mol,B的物质的量为2.4 mol-0.8 mol=1.6 mol,B的物质的量等于15 min时B的物质的量,说明该反应在10 min时已经达到平衡状态,
而不是在10 min后才达到平衡,B错误;C.根据选项B分析可知:反应在进行到10 min时,A物质的物质的量减少0.4 mol,根据物质反应转化关系
可知B物质的物质的量减少0.8 mol,则此时B的物质的量为2.4 mol-0.8 mol=1.6 mol,B的物质的量等于15 min时B的物质的量,说明该反应在10
min时已经达到平衡状态,此时反应产生C的物质的量是1.2 mol,由于容器的容积是2 L,则 平衡状态时,c(C)= =0.6 mol·L-1,C正确;D.
反应开始时n(B)=2.4 mol,反应达到平衡时△n(B)=0.8 mol,则B物质的平衡转化率为: ,D错误;故合理选项是AC。
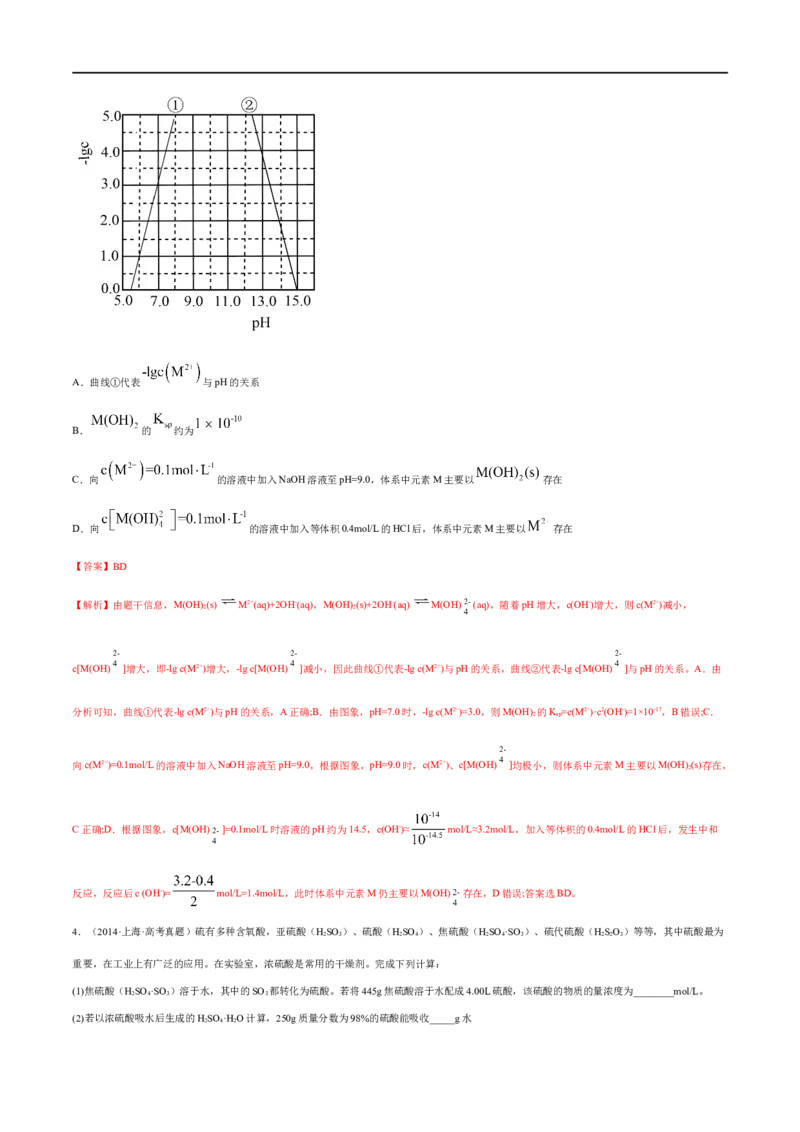
3.(2022·海南·高考真题)某元素M的氢氧化物 在水中的溶解反应为: 、
,25℃,-lgc与pH的关系如图所示,c为 或 浓度的值。下列说法错误的是A.曲线①代表 与pH的关系
B. 的 约为
C.向 的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以 存在
D.向 的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以 存在
【答案】BD
【解析】由题干信息,M(OH)(s) M2+(aq)+2OH-(aq),M(OH)(s)+2OH-(aq) M(OH) (aq),随着pH增大,c(OH-)增大,则c(M2+)减小,
2 2
c[M(OH) ]增大,即-lg c(M2+)增大,-lg c[M(OH) ]减小,因此曲线①代表-lg c(M2+)与pH的关系,曲线②代表-lg c[M(OH) ]与pH的关系。A.由
分析可知,曲线①代表-lg c(M2+)与pH的关系,A正确;B.由图象,pH=7.0时,-lg c(M2+)=3.0,则M(OH) 的K =c(M2+)·c2(OH-)=1×10-17,B错误;C.
2 sp
向c(M2+)=0.1mol/L的溶液中加入NaOH溶液至pH=9.0,根据图象,pH=9.0时,c(M2+)、c[M(OH) ]均极小,则体系中元素M主要以M(OH)(s)存在,
2
C正确;D.根据图象,c[M(OH) ]=0.1mol/L时溶液的pH约为14.5,c(OH-)≈ mol/L≈3.2mol/L,加入等体积的0.4mol/L的HCl后,发生中和
反应,反应后c (OH-)= mol/L=1.4mol/L,此时体系中元素M仍主要以M(OH) 存在,D错误;答案选BD。
4.(2014·上海·高考真题)硫有多种含氧酸,亚硫酸(HSO)、硫酸(HSO)、焦硫酸(HSO·SO)、硫代硫酸(HSO)等等,其中硫酸最为
2 3 2 4 2 4 3 2 2 3
重要,在工业上有广泛的应用。在实验室,浓硫酸是常用的干燥剂。完成下列计算:
(1)焦硫酸(HSO·SO)溶于水,其中的SO都转化为硫酸。若将445g焦硫酸溶于水配成4.00L硫酸,该硫酸的物质的量浓度为________mol/L。
2 4 3 3
(2)若以浓硫酸吸水后生成的HSO·HO计算,250g质量分数为98%的硫酸能吸收_____g水
2 4 2(3)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:
3FeS+8O=FeO+6SO 4FeS+11 O=2FeO+8SO
2 2 3 4 2 2 2 2 3 2
若48mol FeS 完全反应耗用氧气2934.4L(标准状况),计算反应产物中FeO与FeO物质的量之比_______。
2 3 4 2 3
(4)用硫化氢制取硫酸,既能充分利用资源又能保护环境,是一种很有发展前途的制备硫酸的方法。
硫化氢体积分数为0.84的混合气体(HS、HO、N)在空气中完全燃烧,若空气过量77%,计算产物气体中SO体积分数________(水是气体)。
2 2 2 2
(已知空气组成:N体积分数0.79、O体积分数0.21)
2 2
【答案】 (1)1.25 (2)40 (3)2:9 (4)0.075
【解析】(1)445g焦硫酸的物质的量= =2.5mol,其中硫酸和三氧化硫均是2.5mol,2.5mol三氧化硫又产生2.5mol硫酸,则溶液中硫酸
的物质的量是5.0mol,浓度是 =1.25mol/L;(2)250g质量分数为98%的硫酸中硫酸的质量是250g×98%=245g,其中溶剂水是5g,硫酸的物
质的量是 =2.5mol,可以结合水的物质的量是2.5mol,质量是2.5mol×18g/mol=45g,因此还可以吸收水的质量是45g-5g=40g;(3)设
FeO的物质的量是amol,FeO的物质的量是bmol;反应中消耗氧气的物质的量是 =131mol;则根据方程式可知3a+2b=48、
3 4 2 3
8a+5.5b=131,解得a=4、b=18,则n (FeO):n(FeO)=2:9;(4)设混合气为1体积,根据氯化氢完全燃烧的方程式2HS+3O= 2SO+2HO 可知,
3 4 2 3 2 2 2 2
0.84体积硫化氢完全燃烧生成0.84体积二氧化硫和0.84体积水,消耗1.26体积氧气。反应中空气过量77%,因此所需空气为 ×1.77=10.62,
则二氧化硫体积分数 = =0.075。
5.(2011·四川·高考真题)(节选)三草酸合铁酸钾晶体(K
3
[Fe(C
2
O
4
)
3
]·xH
2
O)是一种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含
量和结晶水的含量,某实验小组做了如下实验:
(1)铁含量的测定
步骤一:称量5.00g三草酸合铁酸钾晶体,配制成250mL溶液。
步骤二:取所配溶液25.00mL于锥形瓶中,加稀HSO酸化,滴加KMnO 溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO-被还原成Mn2+。向
2 4 4 4
反应后的溶液中计入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
步骤三:用0.010mol/L KMnO 溶液滴定步骤二所得溶液至终点,消耗KMnO 溶液20.02mL滴定中MnO-被还原成Mn2+ 。重复步骤二、步骤三操作,
4 4 4
滴定消耗0.010mol/L KMnO 溶液19.98mL。
4
请回答下列问题:
④ 实验测得该晶体中铁的质量分数为__________。在步骤二中,若加入的KMnO 的溶液的量不够,则测得的铁含量__________。(选填“偏低”
4
“偏高”“不变”)
【答案】(1) 11.2% 偏高【解析】(1)在步骤三中亚铁离子被高锰酸钾氧化,发生的离子反应为:5Fe2++MnO +8H+=5Fe3++Mn2++4HO,故答案为:5Fe2++MnO +8H+=5Fe3+
2
+Mn2++4HO;④根据步骤三中的离子反应可知:n(Fe)=5n(MnO )=5× ×10-3×0.01 mol•L-1×10=1.0×10-2mol,m(Fe)=56
2
g•mol-1×10-2mol=0.56g。晶体中铁的质量分数= ×100%=11.2%,若在步骤二中滴入酸性高锰酸钾溶液不足,则会有部分草酸根离子未被氧化,
在步骤三中则会造成消耗酸性高锰酸钾溶液的量偏大,从而计算出的铁的量增多,含量偏高,故答案为:11.2%;偏高;