文档内容
高考解密09 电化学基础
A 组 基础练
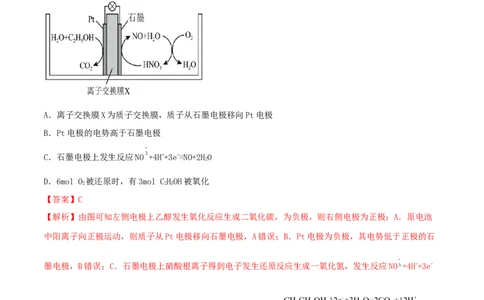
1.(2022·四川成都·统考模拟预测)研究发现,在酸性乙醇燃料电池中加入硝酸,可使电池持续大电
流放电,其工作原理如图所示。下列说法正确的是
A.离子交换膜X为质子交换膜,质子从石墨电极移向Pt电极
B.Pt电极的电势高于石墨电极
C.石墨电极上发生反应NO +4H++3e-=NO+2HO
2
D.6mol O 被还原时,有3mol CHOH被氧化
2 2 5
【答案】C
【解析】由图可知左侧电极上乙醇发生氧化反应生成二氧化碳,为负极,则右侧电极为正极;A.原电池
中阳离子向正极运动,则质子从Pt电极移向石墨电极,A错误;B.Pt电极为负极,其电势低于正极的石
墨电极,B错误;C.石墨电极上硝酸根离子得到电子发生还原反应生成一氧化氮,发生反应NO +4H++3e-
=NO+2HO,C正确;D.乙醇发生氧化反应生成二氧化碳,反应为 ,根
2
据电子守恒可知, ,则6mol O 被还原时,有2mol CHOH被氧化,D错误;
2 2 5
故选C。
2.(2022·辽宁沈阳·辽宁实验中学校考模拟预测)科学家研制出一种高性能水系酸碱双液锌-溴二次
电池,其总反应为: ,中间的双极性膜(BPM)能隔开酸碱双液且能允许 通过,如图所示。下列说法正确的是
A.放电时, 向锌极电极迁移
B.放电时,负极区的pH减小
C.充电时,锌与外接电源正极相连,将电能转化为化学能
D.充电时,石墨电极发生反应:
【答案】B
【解析】由图可知:新型酸碱双液锌溴二次电池放电时,左侧Zn电极发生失去电子的氧化反应生成ZnO,
为负极,电极反应式为:Zn+2OH--2e-=ZnO+HO;电池右侧为正极, 在正极上发生得电子的还原反应生成
2
Br-,电极反应式为: +2e-=3Br-,放电时,阳离子移向正极、阴离子移向负极;充电时,原电池的负极
与外加电源负极相接,为电解池的阴极,正极为电解池的阳极,电极反应与放电时相反。A.原电池中左
侧Zn电极为负极,右侧石墨电极为正极,放电时,阳离子移向正极,即K+向石墨电极迁移,故A错误;
B.放电时,负极电极反应式为:Zn+2OH--2e-=ZnO+HO,所以负极区的pH减小,故B正确;C.据分析可知,
2
充电时,锌与外接电源负极相连,故C错误;D.充电时,原电池正极石墨电极与外加电源正极相接,为电
解池的阳极,发生氧化反应,所以石墨电极发生反应为:3Br--2e-= ,故D错误;故选B。
3.(2022·广东茂名·化州市第一中学校考一模)一种钠离子电池的工作原理如图所示,已知放电时正
极反应为 ,四甘醇二甲醚充当电解液的有机溶剂。下列说法正确的是A.放电时, 从左极室通过阳离子交换膜进入右极室
B.放电时,电流方向为M→用电器→N→电解液→M
C.充电时,N极的电极反应式为
D.充电时,每转移1mol电子,两电极质量变化量相差23g
【答案】B
【解析】A.根据正极反应式结合装置图,可知M为原电池的正极、N为原电池的负极。放电时阳离子在电
解质溶液中向正极移动, 由右室经过阳离子交换膜进入左室,A错误;B.电流方向由正极经过用电器
到达负极,然后通过电解质溶液到达正极形成回路,B正确;C.充电时N电极为阴极得到电子,发生还原
反应, ,C错误;D.充电时每转移1mol电子,M极质量减少23g、N极质量增加
23g,两电极质量变化量相差46g,D错误;答案选B。
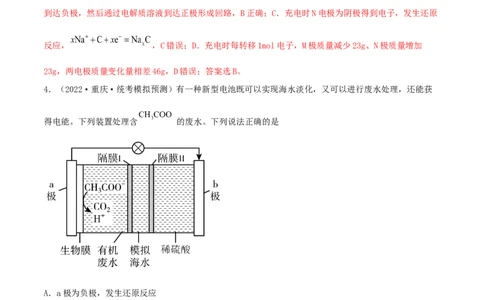
4.(2022·重庆·统考模拟预测)有一种新型电池既可以实现海水淡化,又可以进行废水处理,还能获
得电能。下列装置处理含 的废水。下列说法正确的是
A.a极为负极,发生还原反应
B. 通过隔膜II进入右室
C.负极反应为
D.若处理含有29.5g 的废水,模拟海水理论上可除NaCl 234g
【答案】D
【解析】A.由图中物质变化可知, 在a极发生氧化反应,生成CO,因此a极为负极,A错误;
2B.a极为负极, 应该透过隔膜I进入左室,B错误;C.负极反应为
,C错误;D.每消耗1mol 时,转移电子物质的量为
8mol,消耗8mol NaCl;若处理含有29.5g即0.5mol 的废水时,模拟海水理论上可除4mol
NaCl,即234g,D正确。因此,本题选D。
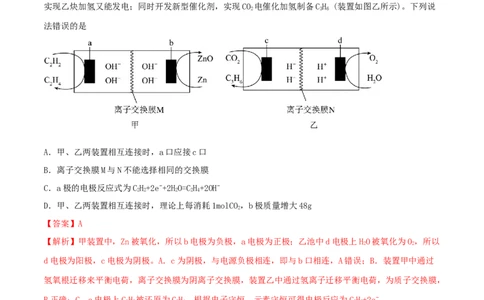
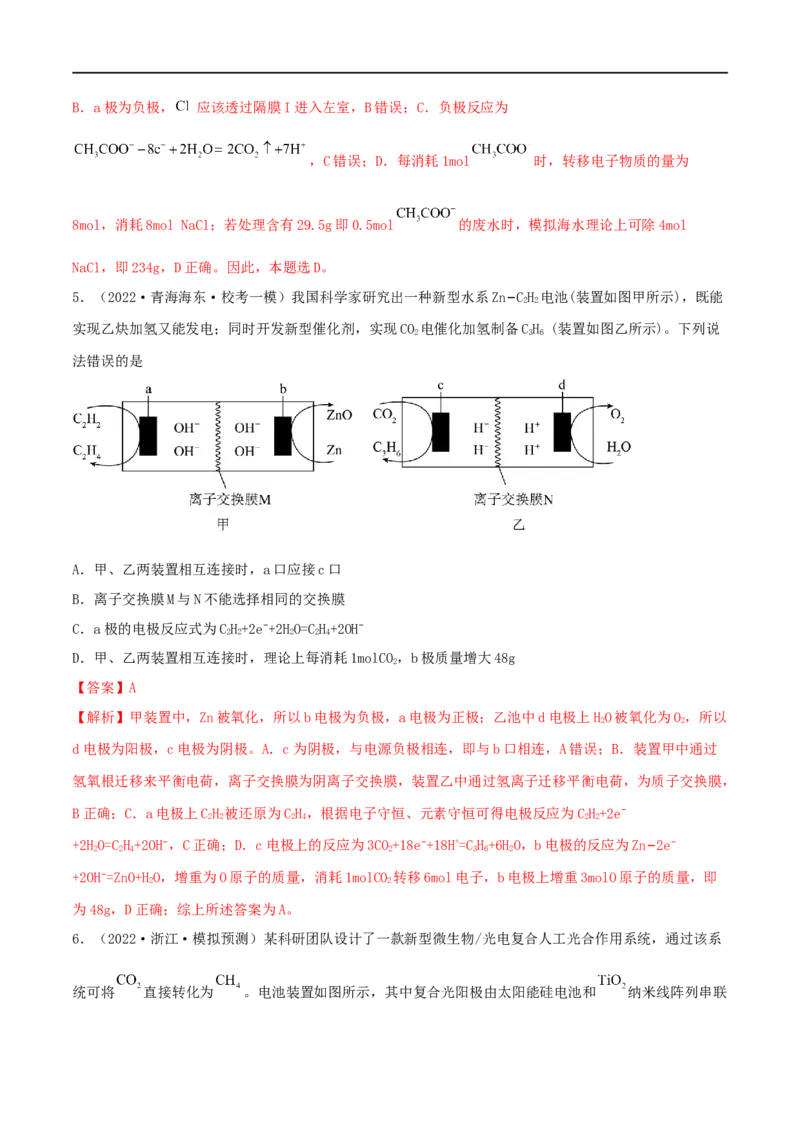
5.(2022·青海海东·校考一模)我国科学家研究出一种新型水系Zn−CH 电池(装置如图甲所示),既能
2 2
实现乙炔加氢又能发电;同时开发新型催化剂,实现CO 电催化加氢制备CH (装置如图乙所示)。下列说
2 3 6
法错误的是
A.甲、乙两装置相互连接时,a口应接c口
B.离子交换膜M与N不能选择相同的交换膜
C.a极的电极反应式为CH+2e−+2HO=CH+2OH−
2 2 2 2 4
D.甲、乙两装置相互连接时,理论上每消耗1molCO,b极质量增大48g
2
【答案】A
【解析】甲装置中,Zn被氧化,所以b电极为负极,a电极为正极;乙池中d电极上HO被氧化为O,所以
2 2
d电极为阳极,c电极为阴极。A.c为阴极,与电源负极相连,即与b口相连,A错误;B.装置甲中通过
氢氧根迁移来平衡电荷,离子交换膜为阴离子交换膜,装置乙中通过氢离子迁移平衡电荷,为质子交换膜,
B正确;C.a电极上CH 被还原为CH,根据电子守恒、元素守恒可得电极反应为CH+2e−
2 2 2 4 2 2
+2HO=CH+2OH−,C正确;D.c电极上的反应为3CO+18e−+18H+=CH+6HO,b电极的反应为Zn−2e−
2 2 4 2 3 6 2
+2OH−=ZnO+HO,增重为O原子的质量,消耗1molCO 转移6mol电子,b电极上增重3molO原子的质量,即
2 2
为48g,D正确;综上所述答案为A。
6.(2022·浙江·模拟预测)某科研团队设计了一款新型微生物/光电复合人工光合作用系统,通过该系
统可将 直接转化为 。电池装置如图所示,其中复合光阳极由太阳能硅电池和 纳米线阵列串联组装而成,双极膜中的 可被解离为 和 ,并在电场作用下向两极移动,下列说法不正确的是
A.人工光合作用系统工作过程中电子由电极A向电极B移动
B.通过该装置可实现光能→电能→化学能的转化
C.电极B上发生的电极反应为
D.该装置工作过程中电极A一侧溶液的pH将减小
【答案】D
【解析】电解池阴阳极的判断:①失电子、化合价升高、被氧化、发生氧化反应的一极是阳极;②得电子、
化合价降低、被还原、发生还原反应的一极是阴极;③电子流向是经外电路从阳极流向电源的正极,从电
源的负极流向阴极;④阴离子流向阳极极,阳离子流向阴极极;⑤一般阳极溶解逐渐溶解,阴极逐渐增重
或有气泡产生;⑥一般有氧气生成的一极是阳极;根据题意,该装置为以复合光阳极由太阳能硅电池转化
,其中电极A有氧气生成,为阳极,电极反应为 ,则电极B为阴极,电极反
应为 ;A.由题意可知,该装置为电解池,电极B上 得电子生成 ,可
知电极B发生还原反应,为阴极,则电极A为阳极,电子由电极A向电极B移动,A正确;B.该装置工作
时,太阳能硅电池将光能直接转化为电能,然后电能转化为化学能,故通过该装置可实现光能 电能→化
学能的转化,B正确:
C.电极B上 得电子生成 ,电极反应式为 ,C正确;D.电极A上发
生的电极反应为 ,反应消耗 ,同时双极膜上会有 移向电极A,则电极A一侧溶液的 的量保持不变,故 不变,D错误;故选D。
7.(2023·北京顺义·一模)锂钒氧化物二次电池的工作原理为: ,下图是用
该电池电解含镍酸性废水制备单质镍的装置示意图,下列说法不正确的是
A.电解过程中Y电极上的电极反应为:
B.电解过程中,b中NaCl溶液的物质的量浓度会增大
C.锂钒氧化物二次电池可以用LiCl水溶液作为电解液
D.锂钒氧化物二次电池充电时A电极的电极反应为:
【答案】C
【解析】电解含镍酸性废水制备单质镍,镀镍铁棒为阴极,发生反应Ni2++2e-=Ni,B是锂钒氧化物二次电
池的负极,A是正极,碳棒是电解池的阳极。A.电解含镍酸性废水制备单质镍,镀镍铁棒为阴极,电解过
程中Y电极上的电极反应为: ,故A正确;B.电解过程中,c中氯离子通过阴离子交换膜
进入b、a中钠离子通过阳离子交换膜进入b,b中NaCl溶液的物质的量浓度会增大,故B正确;C.锂能
与水反应,锂钒氧化物二次电池不能用LiCl水溶液作为电解液,故C错误;D.A是锂钒氧化物二次电池
的正极,充电时,正极发生氧化反应,锂钒氧化物二次电池充电时A电极的电极反应为
, 故D正确;选C。
8.(2022·浙江·模拟预测)双极膜应用于各种装置中,发挥着巨大作用。如图所示装置是将捕捉的二
氧化碳转化为 而矿化封存,减少空气中的碳排放。下列说法正确的是A.向碱室中加入 固体,有利于 的矿化封存
B.两个双极膜中间层的 均向左移动
C. 极为阳极,电极反应式为
D. 在碱室形成
【答案】B
【解析】A.碱室中二氧化碳和碱反应生成碳酸根离子,碳酸根离子通过左侧阴离子交换膜进入中间室内,
与 结合形成碳酸钙,加入 固体不利于 的吸收,故A错误;B.右侧双极膜中氢离子进入
酸室生成盐酸,左侧双极膜中氢离子左移在电极 上发生还原反应生成 ,故B正确;C.左侧双极膜中
氢氧根离子进入碱室,与二氧化碳反应生成碳酸根离子,氢离子左移在电极 上发生还原反应生成 ,所
以 为阴极,电极反应式为 ,故C错误;D. 通过左侧阴离子交换膜进入中间室内与
结合形成碳酸钙, 在中间室形成,故D错误;选B。
9.(2022·浙江·校联考模拟预测)利用 电池可将雾霾中的 、 转化为硫酸铵,其回收利
用装置如图所示。电池工作时的总反应为 ,充放电时, 在正极材料上嵌入或脱嵌,随之在石墨中发生了 的生成与解离。下列有关说法不正确的是
A.转化为硫酸铵时,M与b相接,N与a相接
B.电池工作时,负极电极反应式为:
C.该装置实际工作过程中需要在C处通入适量 或者补充适量
D.理论上当消耗2.24L(标准状况) 时,电池中两池质量差改变2.8g
【答案】C
【解析】根据题中信息,左边装置为化学电源,根据电池工作时总反应,以及原电池工作原理,LiC 电极
x 6
为负极,Li FePO 电极为正极,右边装置为电解池,利用该电池电解雾霾中NO、SO 转化为硫酸铵,硫元
1-x 4 2
素化合价升高,失去电子,根据电解原理,通入SO 的一极为阳极,通入NO的一极为阴极;A.电解池中
2
阳极接电源的正极,阴极接电源的负极,根据上述分析,M接b,N接a,故A说法正确;B.电池工作时,
负极上失去电子,化合价升高,根据电池工作总反应,负极反应式为LiC-xe-=6C+xLi+,故B说法正确;
x 6
C.阳极反应式为SO-2e-+2HO=SO +4H+,阴极反应式为NO+5e-+6H+=NH +HO,电解总反应为5SO+2NO+8HO
2 2 2 2 2
(NH)SO+4HSO,因为制备硫酸铵,因此实际工作中需要在C处通入适量的氨气,故C说法错误;
4 2 4 2 4
D.理论上消耗标准状况下2.24LSO 时,转移电子物质的量为0.2mol,电池工作时,负极反应式为LiC-
2 x 6
xe-=6C+xLi+,正极反应式为Li FePO+xLi++xe-=LiFePO,负极质量减少0.2mol×7g/mol=1.4g,正极质量
1-x 4 4
增大1.4g,电池中两池质量差改变2.8g,故D说法正确;答案为C。
10.(2022·重庆·校联考三模)回答下列问题:(1)我国某科研团队设计了一种电解装置,将CO 和NaCl高效转化为CO和NaClO,原理如图1所示:
2
通入CO 气体的一极为_______(填“阴极”、“阳极”、“正极”或“负极”),写出该极的电极反应式:
2
_______。
(2)全钒液流电池是利用不同价态的含钒离子在酸性条件下发生反应,其电池结构如图2所示。已知酸性溶
液中钒以VO (黄色)、V2+(紫色)、VO2+(蓝色)、V3+(绿色)的形式存在。放电过程中,电池的正极反应式为
________,右侧储液罐中溶液颜色变化为_______。
(3)如果用全钒液流电池作为图1电解装置的电源,则催化电极b应与该电池的_______极(填“X’或
“Y’)相连;若电解时电路中转移0.4mol电子,则理论上生成NaClO的质量为_______g;电池左储液罐溶
液中n(H+)的变化量为_______。
【答案】(1)阴极 2H++CO+2e-=CO+HO
2 2
(2)2H++VO +e-=VO2++HO 溶液由紫色变为绿色
2
(3)X 14.9 0.4mol
【解析】(1)该装置为电解池,CO→CO,碳元素化合价降低,发生还原反应,则通入CO 气体的一极为阴
2 2
极,电极反应式:2H++CO+2e-=CO+HO;
2 2
(2)由电子流入的一极为正极,则X为正极,放电时正极上反应式:2H++VO +e-=VO2++HO;放电过程中,
2右罐为负极,反应式:V2+-e-═V3+,则溶液颜色逐渐由紫色变为绿色;
(3)图2是原电池,Y极电子流出,则Y为负极,X为正极,图1是电解池,催化电极b是阳极,由电解
池的阳极接原电池的正极,则催化电极b应与该电池的X极,催化电极b的电极反应式为:HO+Cl--2e-
2
=HClO+H+,电路中转移0.4mol电子,则理论上生成0.2mol NaClO,质量
为m=nM=0.2mol×74.5g/mol=14.9g,充电时,左槽正极上反应式:2H++VO +e-=VO2++HO,若转移电子
2
0.4mol,消耗氢离子为0.8mol,通过交换膜定向移动通过0.4mol电子,则左槽溶液中n(H+)的变化量为
0.8mol-0.4mol=0.4mol。
B 组 提升练
1.(2022·浙江·模拟预测)一种双阴极微生物燃料电池装置如图所示,电解质溶液呈酸性,该装置可
以同时进行硝化和反硝化脱氮,下列叙述错误的是
A.电池工作时, 的迁移方向为“厌氧阳极”→“缺氧阴极”和“厌氧阳极”→“好氧阴极”
B.电池工作时,“缺氧阴极”电极附近的溶液pH增大
C.“好氧阴极”存在反应:
D.“厌氧阳极”区质量减少28.8g时,该电极输出电子2.4mol
【答案】C
【解析】“厌氧阳极”上, 失去电子生成 和 ,电极反应式为;“缺氧阴极”上, 得到电子生成 , 再转化为 ,电极反应式分别为
、 。“好氧阴极”上, 得到电子生成
,电极反应式为 ,同时 还能氧化 生成 , 还可以被 氧化为
,离子方程式分别为 、 ;A.在该电池中,
“阳极”代表负极,“阴极”代表正极,阳离子由负极移向正极,电池工作时,“厌氧阳极”产生的 通
过质子交换膜向“缺氧阴极”和“好氧阴极”迁移,A正确;B.由分析可知,电池工作时,“缺氧阴极”
上消耗 多于从“厌氧阳极”迁移过来的 ,且反应生成水,其附近的溶液pH增大,B正确;
C.由题干可知,电解质溶液呈酸性,C错误;D.“厌氧阳极”的电极反应式为
,1mol 参与反应消耗6mol ,输出24mol电子,“厌
氧阳极”区质量减少288g,故“厌氧阳极”区质量减少28.8g时,该电极输出电子2.4mol,D正确;故答
案为:C。
2.(2023·安徽宣城·安徽省宣城市第二中学模拟预测)我国科学家在“绿氢”研究方面取得新进展。
四种电解槽结构如图所示。已知:法拉第常数(F)表示 电子所带电量, 。下列说法正确的是
A.图a、d装置中 作用是降低阳极反应的活化能
B.图c装置的阴极反应式为
C.图a装置工作一段时间后,阳极区溶液 明显下降
D.电流强度为a安培,通电时间为b小时,阳极理论最多产生
【答案】D
【解析】A.图d装置在阴极区加入 且两个装置中 起增强导电作用,增强电解效率,不是作催化
剂,故A错误;B.据装置图知,图c装置阴极上水被还原生成氢气和氧离子,阴极反应式为
,故B错误;C.据图a装置可知,阳极反应式为 ,隔膜
为阴离子交换膜, 向阳极区迁移,故C错误;D.通过电量 ,根据阳极反应可知,生成
转移 电子, ,故D正确;故选D。
3.(2023·湖北·统考一模)1,2-二氯乙烷主要用作聚氯乙烯单体制取过程的中间体,用电有机合成法
合成1,2-二氯乙烷的装置如图所示。下列说法中正确的是A.直流电源电极a为负极
B.X为阳离子交换膜,Y为阴离子交换膜
C.液相反应中, 被氧化为1,2-二氯乙烷
D.该装置总反应为
【答案】C
【解析】由电解池装置图可知,左侧亚铜离子失去电子生成二价铜离子,为电解池的阳极,则a为电源正
极,溶液中的氯离子经过阴离子交换膜X移向阳极,右侧氢离子得到电子生成氢气,为阴极,则b为电源
的负极,溶液中的钠离子经过阳离子交换膜Y移向阴极,同时生成氢氧化钠。液相反应中氯化铜与乙烯反
应生成1,2—二氯乙烷和氯化亚铜。A.根据分析,直流电源电极a为正极,A错误;B.由分析可知,X
为阴离子交换膜,Y为阳离子交换膜,B错误;C.液相反应中,CH 与CuCl 反应生成1,2-二氯乙烷时碳
2 4 2
元素化合价升高,发生氧化反应,应为CH 被CuCl 氧化为1,2-二氯乙烷,C正确;D.以NaCl溶液和乙
2 4 2
烯为原料合成1,2-二氯乙烷中, CuCl循环使用,其实质是NaCl、HO与 CH=CH 反应,所以总反应为
2 2 2
CH=CH+2HO+2NaCl H↑+2NaOH+ClCHCHCl,D错误;故答案选C。
2 2 2 2 2 2
4.(2023·湖南衡阳·统考一模)钾离子电池因其低成本和较高的能量/功率密度,引起了广泛关注。一
种钾离子电池的总反应为 ,其工作原理如图所示。下列说法正确
的是A.该电池的交换膜为阳离子交换膜
B.充电时,a极接电源的负极发生氧化反应
C.放电时,b极发生的反应为
D.放电时,理论上电路通过 ,a极质量减小39g
【答案】AC
【解析】总反应: ,放电时,a极: ;b极:
,因此该电池交换膜为阳离子交换膜,以保证充放电时K+能够顺利通过。
A.由分析可知,该电池的交换膜为阳离子交换膜,A正确;B.根据总反应可知,充电时,a极电极反应式
为: ,因此a极接电源的负极,发生还原反应,B错误;C.由总反应式可知,放电时,b
极发生的反应为 ,C正确;D.放电时,a极电极反应式为:
,当转移1个电子时,a极减少一个K+的质量;当电路通过 ,a极减少4molK+的
质量,即146g,D错误。本题选AC。
5.(2021·北京·模拟预测)根据下列要求回答下列问题。
(1)次磷酸钴[Co(HPO)]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,
2 2 2
原理如图:则Co的电极反应式为___________,A、B、C为离子交换膜,其中B为___________离子交换膜(填“阳”
或“阴”)。
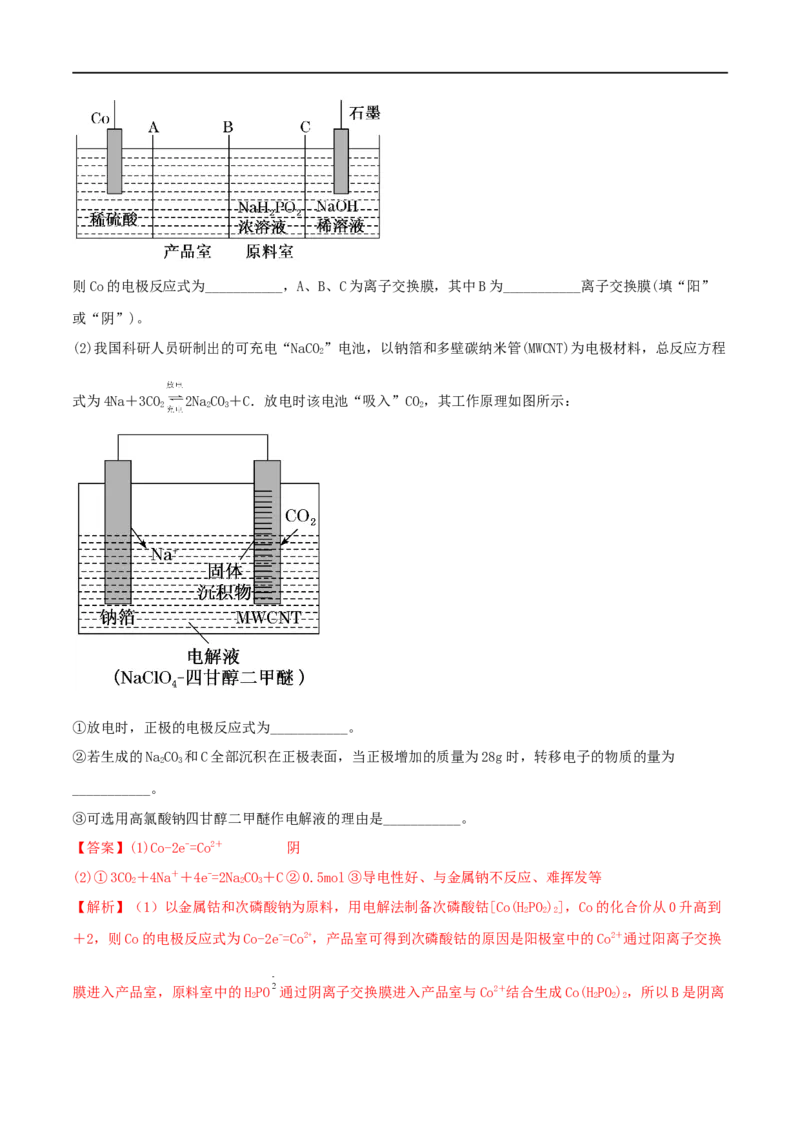
(2)我国科研人员研制出的可充电“NaCO”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程
2
式为4Na+3CO 2NaCO+C.放电时该电池“吸入”CO,其工作原理如图所示:
2 2 3 2
①放电时,正极的电极反应式为___________。
②若生成的NaCO 和C全部沉积在正极表面,当正极增加的质量为28g时,转移电子的物质的量为
2 3
___________。
③可选用高氯酸钠四甘醇二甲醚作电解液的理由是___________。
【答案】(1)Co-2e-=Co2+ 阴
(2)①3CO+4Na++4e-=2NaCO+C②0.5mol③导电性好、与金属钠不反应、难挥发等
2 2 3
【解析】(1)以金属钴和次磷酸钠为原料,用电解法制备次磷酸钴[Co(HPO)],Co的化合价从0升高到
2 2 2
+2,则Co的电极反应式为Co-2e-=Co2+,产品室可得到次磷酸钴的原因是阳极室中的Co2+通过阳离子交换
膜进入产品室,原料室中的HPO 通过阴离子交换膜进入产品室与Co2+结合生成Co(HPO),所以B是阴离
2 2 2 2子交换膜;
(2)①放电时,正极发生得到电子的还原反应,则根据总反应式可知电极反应式为3CO+4Na++4e-
2
=2NaCO+C;
2 3
②根据反应式可知每转移4mol电子,正极质量增加2×106g+12g=224g,所以当正极增加的质量为28g时,
转移电子的物质的量为 ×4mol=0.5mol;
③根据题干信息以及金属钠的化学性质可知可选用高氯酸钠四甘醇二甲醚作电解液的理由是其导电性好、
与金属钠不反应、难挥发等。
C 组 真题练
1.(2022·广东·高考真题)以熔融盐为电解液,以含 和 等的铝合金废料为阳极进行电解,
实现 的再生。该过程中
A.阴极发生的反应为 B.阴极上 被氧化
C.在电解槽底部产生含 的阳极泥 D.阳极和阴极的质量变化相等
【答案】C
【解析】根据电解原理可知,电解池中阳极发生失电子的氧化反应,阴极发生得电子的还原反应,该题中
以熔融盐为电解液,含 和 等的铝合金废料为阳极进行电解,通过控制一定的条件,从而可使阳
极区Mg和Al发生失电子的氧化反应,分别生成Mg2+和Al3+,Cu和Si不参与反应,阴极区Al3+得电子生成
Al单质,从而实现Al的再生。A.阴极应该发生得电子的还原反应,实际上Mg在阳极失电子生成Mg2+,A
错误;B.Al在阳极上被氧化生成Al3+,B错误;C.阳极材料中Cu和Si不参与氧化反应,在电解槽底部
可形成阳极泥,C正确;D.因为阳极除了铝参与电子转移,镁也参与了电子转移,且还会形成阳极泥,而
阴极只有铝离子得电子生成铝单质,根据电子转移数守恒及元素守恒可知,阳极与阴极的质量变化不相等,
D错误;故选C。
2.(2022·辽宁·统考高考真题)镀锌铁钉放入棕色的碘水中,溶液褪色;取出铁钉后加入少量漂白粉,
溶液恢复棕色;加入 ,振荡,静置,液体分层。下列说法正确的是
A.褪色原因为 被 还原 B.液体分层后,上层呈紫红色
C.镀锌铁钉比镀锡铁钉更易生锈 D.溶液恢复棕色的原因为 被氧化
【答案】D【解析】A. 比 活泼,更容易失去电子,还原性更强,先与 发生氧化还原反应,故溶液褪色原因为
被 还原,A项错误;B.液体分层后, 在 层, 的密度比水大,则下层呈紫红色,B项错误;
C.若镀层金属活泼性大于 ,则 不易生锈,反之,若 活泼性大于镀层金属,则 更易生锈,由于活
泼性: ,则镀锡铁钉更易生锈,C项错误;D.漂白粉的有效成分为 ,其具有强氧化性,
可将 氧化,D项正确;答案选D。
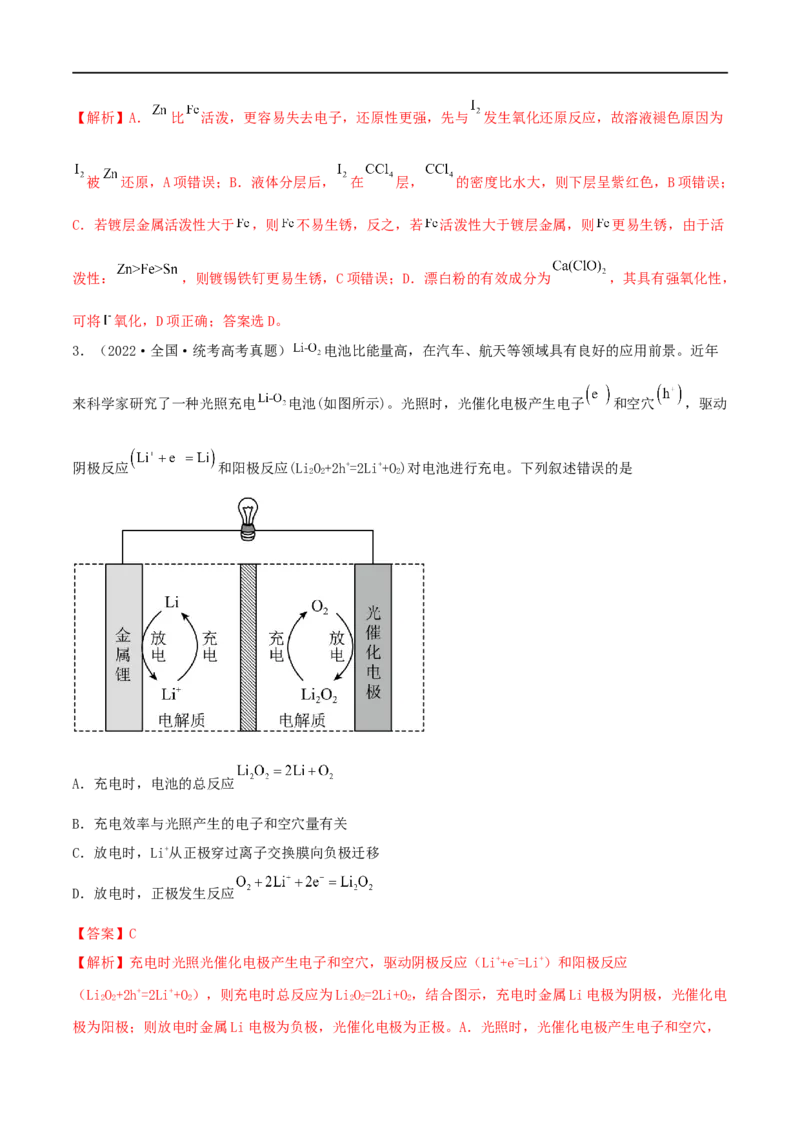
3.(2022·全国·统考高考真题) 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年
来科学家研究了一种光照充电 电池(如图所示)。光照时,光催化电极产生电子 和空穴 ,驱动
阴极反应 和阳极反应(LiO+2h+=2Li++O)对电池进行充电。下列叙述错误的是
2 2 2
A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
【答案】C
【解析】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应
(LiO+2h+=2Li++O),则充电时总反应为LiO=2Li+O,结合图示,充电时金属Li电极为阴极,光催化电
2 2 2 2 2 2
极为阳极;则放电时金属Li电极为负极,光催化电极为正极。A.光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳极反应,充电时电池的总反应为
LiO=2Li+O,A正确;B.充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与
2 2 2
空穴有关,故充电效率与光照产生的电子和空穴量有关,B正确;C.放电时,金属Li电极为负极,光催
化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;D.放电时总反应为2Li+O=LiO,正极反
2 2 2
应为O+2Li++2e-=LiO,D正确;答案选C。
2 2 2
4.(2022·辽宁·统考高考真题)如图,c管为上端封口的量气管,为测定乙酸溶液浓度,量取
待测样品加入b容器中,接通电源,进行实验。下列说法正确的是
A.左侧电极反应:
B.实验结束时,b中溶液红色恰好褪去
C.若c中收集气体 ,则样品中乙酸浓度为
D.把盐桥换为U形铜导线,不影响测定结果
【答案】A
【解析】本装置为电解池,左侧阳极析出氧气,右侧阴极析出氢气。A.左侧阳极析出氧气,左侧电极反
应: ,A正确;B.右侧电极反应2CHCOOH+2e-=H +2CHCOO-,反应结束时溶液中存
3 2 3
在CHCOO-,水解后溶液显碱性,故溶液为红色,B错误;C.若c中收集气体 ,若在标况下,c中
3
收集气体的物质的量为0.5×10-3mol,转移电子量为0.5×10-3mol×4=2×10-3mol,故产生氢气:1×10-
3mol,则样品中乙酸浓度为:2×10-3mol ÷10÷10-3= ,并且题中未给定气体状态不能准确计算,
C错误;D.盐桥换为U形铜导线则不能起到传递离子使溶液呈电中性的效果,影响反应进行,D错误;答
案选A。5.(2022·浙江·统考高考真题)pH计是一种采用原电池原理测量溶液pH的仪器。如图所示,以玻璃电
极(在特制玻璃薄膜球内放置已知浓度的HCl溶液,并插入Ag—AgCl电极)和另一Ag—AgCl电极插入待测
溶液中组成电池,pH与电池的电动势E存在关系:pH=(E-常数)/0.059。下列说法正确的是
A.如果玻璃薄膜球内电极的电势低,则该电极反应式为:AgCl(s)+e-=Ag(s)+Cl-(0.1mol·L-1)
B.玻璃膜内外氢离子浓度的差异不会引起电动势的变化
C.分别测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH
D.pH计工作时,电能转化为化学能
【答案】C
【解析】A. 如果玻璃薄膜球内电极的电势低,则该电极为负极、负极发生氧化反应而不是还原反应,A
错误;B.已知:pH与电池的电动势E存在关系:pH=(E-常数)/0.059,则玻璃膜内外氢离子浓度的差异会
引起电动势的变化,B错误;C.pH与电池的电动势E存在关系:pH=(E-常数)/0.059,则分别测定含已知
pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH,C正确;D. pH计工作时,利用原电池
原理,则化学能转化为电能,D错误;答案选C。
6.(2022·河北·高考真题)科学家研制了一种能在较低电压下获得氧气和氢气的电化学装置,工作原
理示意图如图。下列说法正确的是
A.电极b为阳极
B.隔膜为阴离子交换膜
C.生成气体M与N的物质的量之比为2:1
D.反应器I中反应的离子方程式为4[Fe(CN)]3—+4OH— 4[Fe(CN)]4—+O↑+2HO
6 6 2 2
【答案】BD
【解析】由图可知,a电极为阳极,碱性条件下[Fe(CN)]4—离子在阳极失去电子发生氧化反应生成
6
[Fe(CN)]3—离子,催化剂作用下,[Fe(CN)]3—离子与氢氧根离子反应生成[Fe(CN)]4—离子、氧气和水,b
6 6 6
电极为阴极,水分子作用下DHPS在阴极得到电子发生还原反应生成DHPS—2H和氢氧根离子,催化剂作用
下,DHPS—2H与水反应生成DHPS和氢气,氢氧根离子通过阴离子交换膜由阴极室向阳极室移动,则M为
氧气、N为氢气。
A.由分析可知,b电极为电解池的阴极,故A错误;B.由分析可知,氢氧根离子通过阴离子交换膜由阴
极室向阳极室移动,则隔膜为阴离子交换膜,故B正确;C.由分析可知,M为氧气、N为氢气,由得失电
子数目守恒可知,氧气和氢气的的物质的量之比为1:2,故C错误;D.由分析可知,反应器I中发生的
反应为催化剂作用下,[Fe(CN)]3—离子与氢氧根离子反应生成[Fe(CN)]4—离子、氧气和水,反应的离子方
6 6
程式为4[Fe(CN)]3—+4OH— 4[Fe(CN)]4—+O↑+2HO,故D正确;故选BD。
6 6 2 2