文档内容
高考解密14 综合实验探究
A 组 基础练
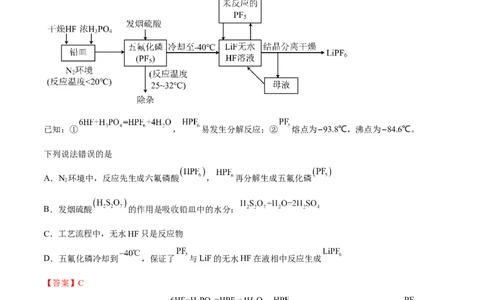
1.(2023·广东清远·清新一中校考模拟预测)六氟磷酸锂 是锂离子电池的关键材料。一种 的
制备工艺流程如图所示。
已知:① , 易发生分解反应;② 熔点为−93.8℃,沸点为−84.6℃。
下列说法错误的是
A.N 环境中,反应先生成六氟磷酸 , 再分解生成五氟化磷
2
B.发烟硫酸 的作用是吸收铅皿中的水分:
C.工艺流程中,无水HF只是反应物
D.五氟化磷冷却到 ,保证了 与LiF的无水HF在液相中反应生成
【答案】C
【解析】在铅皿中HF和磷酸发生 , 不稳定,易发生分解反应生成 和
HF,发烟硫酸加入,发烟硫酸和水结合,在常温下除杂,再五氟化磷冷却到 ,加到LiF和无水HF
的混合物中反应生成 。A.N 环境中,根据题中信息 , 易发生分解反
2
应;则反应先生成六氟磷酸 , 再分解生成五氟化磷 ,故A正确;B.发烟硫酸的作用是吸收铅皿中的水分: ,将HF变为无水HF,故B正确;C.工艺流程中,
无水HF不仅只是反应物,在 发生分解反应中是产物,故C错误;D.无水HF在 状态下是液态,
五氟化磷冷却到 ,保证了 与LiF的无水HF在液相中反应生成 ,故D正确。综上所述,答案
为C。
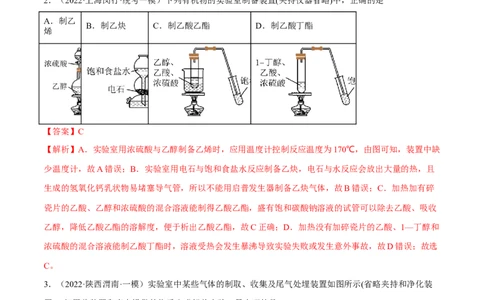
2.(2022·上海闵行·统考一模)下列有机物的实验室制备装置(夹持仪器省略)中,正确的是
A.制乙
B.制乙炔 C.制乙酸乙酯 D.制乙酸丁酯
烯
【答案】C
【解析】A.实验室用浓硫酸与乙醇制备乙烯时,应用温度计控制反应温度为170℃,由图可知,装置中缺
少温度计,故A错误;B.实验室用电石与饱和食盐水反应制备乙炔,电石与水反应会放出大量的热,且
生成的氢氧化钙乳状物易堵塞导气管,所以不能用启普发生器制备乙炔气体,故B错误;C.加热加有碎
瓷片的乙酸、乙醇和浓硫酸的混合溶液能制得乙酸乙酯,盛有饱和碳酸钠溶液的试管可以除去乙酸、吸收
乙醇,降低乙酸乙酯的溶解度,便于析出乙酸乙酯,故C正确;D.加热没有加碎瓷片的乙酸、1—丁醇和
浓硫酸的混合溶液能制乙酸丁酯时,溶液受热会发生暴沸导致实验失败或发生意外事故,故D错误;故选
C。
3.(2022·陕西渭南·一模)实验室中某些气体的制取、收集及尾气处埋装置如图所示(省略夹持和净化装
置)。仅用此装置和表中提供的物质完成相关实验,最合理的是
选项 a物质 b物质 c收集的气体 d中的物质A 稀硫酸 CaCO CO HO
3 2 2
B 稀盐酸 Zn H 澄清石灰水
2
C 浓硝酸 Cu NO HO
2 2
D 浓盐酸 KMnO Cl NaOH溶液
4 2
【答案】D
【解析】A. 应用稀盐酸与碳酸钙反应制二氧化碳,不用稀硫酸,可用向上排空气法收集,但二氧化碳不
是空气污染物且可溶于水,不用倒扣的漏斗吸收尾气,故A错误;B. 稀盐酸与锌反应制取氢气,氢气不
溶于澄清石灰水,不能用澄清石灰水吸收氢气,故B错误;C. 浓硝酸与铜生成的是NO ,二氧化氮和水
2
反应生成NO,NO与水不反应,不能用水吸收尾气,故C错误;D. 浓盐酸与KMnO 在常温下发生氧化
4
还原反应生成氯气,氯气的密度大于空气,可以使用向上排空气方法收集,氯气是大气污染物,可以用
NaOH溶液进行尾气处理,故D正确;答案选D。
4.(2023·广东广州·一模)将浓盐酸加到 中进行如图(a~c均为浸有相应试液的棉花)所示的探究实
验,反应一段时间后,下列分析正确的是
A.a处变黄色,说明 具有还原性 B.b处变橙色,说明非金属性
C.c处红色逐渐变浅,说明 具有漂白性 D.浓盐酸与 反应,只体现HCl的酸性
【答案】B
【解析】高锰酸钾和浓盐酸反应生成氯气,氯气具有强氧化性;A.a处变黄色,说明 好和亚铁离子反
应生成铁离子,氯元素化合价降低,体现氧化性,A错误;B.b处变橙色,说明氯气和溴化钠反应生成溴
单质,则非金属性 ,B正确;C.挥发出的盐酸能和氢氧化钠反应,导致c处红色逐渐变浅,故不
能说明 具有漂白性,C错误;D.浓盐酸与 反应,反应中氯元素化合价升高,HCl也体现出还
原性,D错误;故选B。5.(2023春·河南漯河·高三漯河高中校考开学考试)某小组为了探究KI的性质,设计了如表实验:
操作图示 实验 试剂X 现象
I AgNO 溶液 产生黄色沉淀
3
II AgCl浊液 产生黄色沉淀
III FeCl 溶液和淀粉溶液 溶液变为蓝色
3
IV NaSO 溶液 溶液由蓝色变为无色
2 2 3
注:实验在实验III反应后的基础上进行。
下列推断正确的是A.实验I、II发生反应的离子方程式相同
B.实验II足以说明K (AgCl)>K (AgI)
sp sp
C.由实验III知,还原性:I->Fe2+
D.由实验IV知:NaSO 具有氧化性
2 2 3
【答案】C
【解析】A.书写离子方程式时,AgCl不能拆开, 必须拆开,故离子方程式不同,A错误;B.碘
化钾溶液中碘离子浓度大,加入的AgCl浊液为过饱和溶液,生成黄色的AgI沉淀,并不一定是发生了沉
淀的转化,不能说明 ,B错误;C.由实验Ⅲ现象可知: 溶液和KI反应生成碘单
质,离子方程式为 ,使淀粉溶液变蓝,还原性: ,C正确;D. 具有氧化
性,与 发生氧化还原反应,生成 ,溶液颜色褪去,反应中 体现还原性,D错误;答案
选C。
6.(2023春·河北邯郸·高三校联考开学考试)下列实验方案不能达到探究目的的是
选项 实验方案 探究目的
两个封有 和 混合气体的圆底烧瓶分别浸泡在热水和冷水中,比 探究温度对化学平衡移
A
较两个烧瓶里气体的颜色 动的影响
向两支盛有 溶液的试管中分别加入 的 溶液和 探究 、 对
B
的 溶液,比较产生气泡速率 分解速率的影响C 向苯酚浊液中加入 溶液,观察溶液变化 探究苯酚、 酸性
强弱
向盛有 溶液的试管中滴加2滴 的 溶
探究 与
D
液,振荡,再向其中滴加4滴 的 溶液,观察沉淀及颜色变
的大小
化
【答案】B
【解析】A. 是红棕色气体, 是无色气体,可以观察颜色变化探究温度对化学平衡移动的影响,
A项能达到实验目的;B.未控制单一变量,阴离子种类不同,B项不能达到实验目的;C.向苯酚浊液中
加入碳酸钠,溶液变澄清,可说明酸性:苯酚 ,C项能达到实验目的;D.因加入 的物质
的量小, 无剩余,且加入的 少量,若生成 沉淀,可以证明 ,D项能达到实
验目的;故选B。
7.(2023·福建·校联考一模)某实验小组设计如下实验探究 的制备,下列有关分析不合理的是
实验 操作 现象
一分钟后,晶块表面仍为浅绿色,溶液呈更浅
Ⅰ 将一块 晶体浸入 蒸馏水中
的绿色。
将另一块 晶体浸入 一分钟后,晶块表面变白;捞出晶块露置空气
Ⅱ
溶液中 中,表面逐渐变为红褐色。
将 溶液与 立即出现大量灰绿色浑浊,一分钟后,液面附
Ⅲ
近出现红褐色浑浊。
溶液混合
A.实验Ⅰ起对照作用,排除 晶体自身在水中的颜色变化
B.实验Ⅱ晶块表面长时间保持白色,与 难溶、未分散于水有关
C.捞出晶块后发生了反应:
D.实验Ⅲ溶液中氧气含量明显多于实验Ⅱ中
【答案】D
【解析】A.实验Ⅰ中,晶块表面为浅绿色,起对照作用,目的是排除实验Ⅱ中晶块表面变白,不是因为晶体自身在水中的颜色变化引起的,A符合题意;B. 具有较强的还原性,易被溶液中溶
解的氧气氧化,因此实验Ⅱ晶块表面之所以能长时间保持白色,与 难溶、未分散于水有关,B符
合题意;C. 具有较强的还原性,易被氧气氧化,捞出晶块后发生的反应为
,C符合题意;D.根据控制单一变量的原则,实验Ⅱ和Ⅲ反应条件不
一样(实验Ⅱ为 晶体,而实验Ⅲ为 溶液),单从实验结果,无法得出实验Ⅲ溶液中氧气含量
明显多于实验Ⅱ的结论,D不符合题意; 故选D。
8.(2023秋·河南三门峡·高三统考期末)下列方案设计、现象和结论不正确的是
目的 方案设计 现象和结论
取 与 溶液于试 观察到氯化镁溶液出现白色沉淀,氯化
比较镁与铝元素的金属性
A 管,加入足量NaOH溶液,观 铝溶液先出现白色沉淀后溶解。证明镁
强弱
的金属性更强
察现象
检验溶液中是否含有 取少量溶液于试管中,先滴加 先产生白色沉淀,再加稀盐酸,沉淀不
B
溶液,再加入稀盐酸 溶解,则说明溶液中一定含有
溶液由黄色变为橙色,则说明增大氢离
探究氢离子浓度对 向 溶液中缓慢滴加硫
C
子浓度,转化平衡向生成 的方向
酸观察实验现象
、 相互转化的影响
移动
向盛有少量待测液的试管里滴 试管中溶液出现血红色,证明溶液中含
D 检验溶液中是否含有
加2滴KSCN溶液,观察现象 有
【答案】B
【解析】A.取 与 溶液于试管,加入足量NaOH溶液,观察现象,观察到氯化镁溶液出现白色
沉淀,氯化铝溶液先出现白色沉淀后溶解,证明氢氧化镁的碱性强于氢氧化铝,故镁的金属性更强,选项
A正确;B.取少量溶液于试管中,先滴加 溶液,再加入稀盐酸,先产生白色沉淀,再加稀盐酸,沉
淀不溶解,产生的不溶于盐酸的白色沉淀可能为氯化银也可能为硫酸钡,则溶液中不一定含有 ,选项B不正确;C.向 溶液中缓慢滴加硫酸观察实验现象,溶液由黄色变为橙色,则说明增大氢离子浓
度,转化平衡向生成 的方向移动 ,选项C正确;D.向盛有少量待测
液的试管里滴加2滴KSCN溶液,试管中溶液出现血红色,证明溶液中含有 ,选项D正确;答案选
B。
9.(2023秋·河北邯郸·高三统考期末)配制一定物质的量浓度的NaOH溶液并用来滴定白醋样品,下列图
示操作不能达到实验目的的是
A.操作甲:用玻璃棒搅拌以加速NaOH固体溶解
B.操作乙:配制NaOH溶液时向容量瓶中加水至刻度线
C.操作丙:弯曲并挤压胶管中玻璃珠以排除滴定管尖端气泡
D.操作丁:滴定时滴入液体和摇动锥形瓶同时进行
【答案】B
【解析】A.搅拌可以加速固体的溶解,则操作甲为用玻璃棒搅拌以加速氢氧化钠固体溶解,故A正确;
B.配制一定物质的量浓度浓度溶液定容时,应用玻璃棒引流向容量瓶中加水至刻度线1—2cm处,则操作
乙中缺少玻璃棒引流,故B错误;C.排出碱式滴定管中尖嘴部分气泡时应使带有玻璃小球的橡胶管弯曲
并挤压胶管中玻璃珠迅速排液以排除滴定管尖端气泡,则操作丙为弯曲并挤压胶管中玻璃珠以排除滴定管
尖端气泡,故C正确;D.中和滴定时,左手应控制滴定管滴入液体,同时右手摇动锥形瓶进行滴定,眼
睛注视锥形瓶中溶液颜色变化,故D正确;故选B。
10.(2023·辽宁·校联考一模)金属M与单质碘在无水醋酸中反应,得到化合物 ,提纯干燥后测得其
熔点为144.5℃。为确定 的组成,进行以下实验:称取0.6263g ,置于特制的梨形瓶中,加入50mL6mol L-1的盐酸,同时加入适量 ,用0.1000mol L-1的碘酸钾溶液进行滴定。随着碘酸钾溶液的加入,
可观察到 层呈紫色,后逐渐变浅,滴至紫色褪去为终点,此时 层呈淡黄色,滴定消耗碘酸钾溶
液20.00mL。在 中显黄色的物质在历史上曾被误认为 。下面有关实验细节的描述中,错误的是
A.滴定终点时的操作:当滴入最后半滴标准液时,溶液恰好由紫色变为淡黄色,且半分钟不变色
B.滴定结束后 中主要的溶质为
C.如果用过量的碘化钾溶液滴定碘酸钾溶液,则滴定过程中 层颜色逐渐加深,直至不变
D.紫色褪去反应的离子方程式为:
【答案】C
【解析】用碘酸钾溶液进行滴定,随着碘酸钾溶液的加入,可观察到 层呈紫色,是生成碘单质,后逐
渐变浅,滴至紫色褪去是碘单质、碘酸根离子、氢离子和氯离子发生反应生成氯化碘,此时 层呈淡黄
色。A.滴定终点时的操作:当滴入最后半滴标准液时,溶液恰好由紫色变为淡黄色,且半分钟不变色,A
正确;B.根据上述分析可知,滴定结束后 中主要的溶质为 ,B正确;C.碘离子与碘酸根离子反
B 组 提升练
应中需消耗氢离子,当氢离子不足时不会再生成碘单质, 层颜色不会加深,C错误;D.紫色褪去反应
的离子方程式为: ,D正确; 故选C。
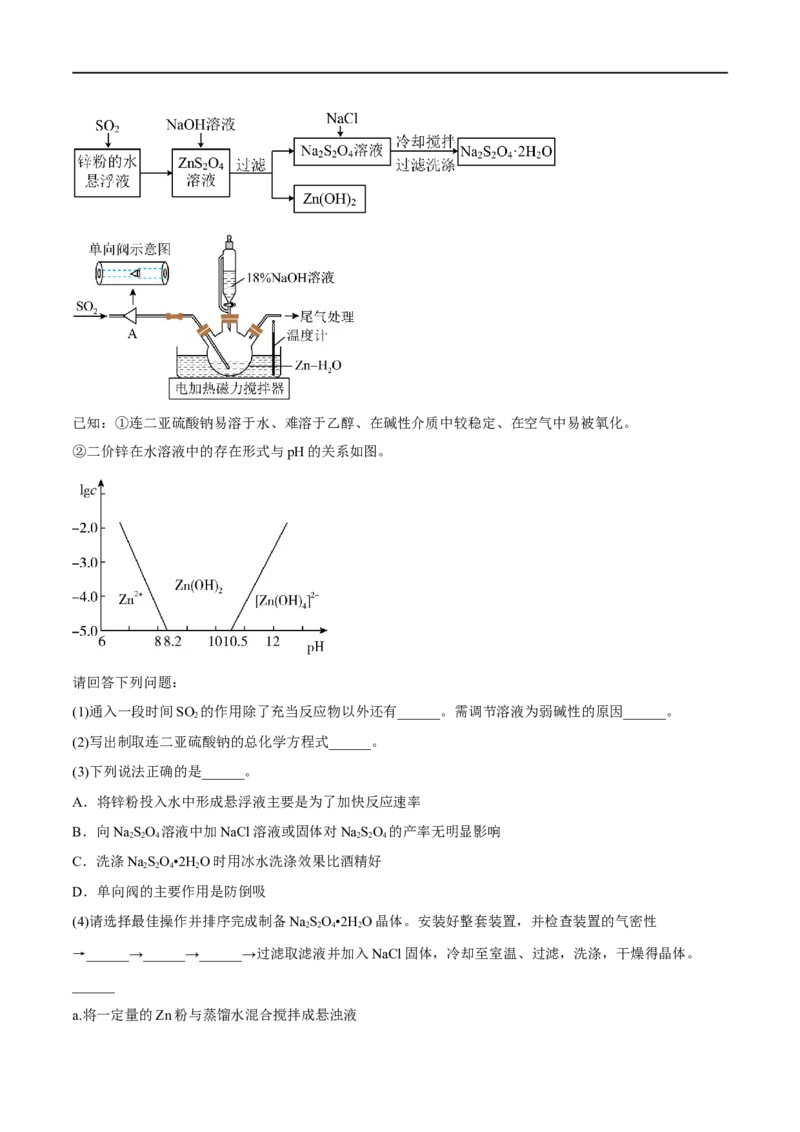
1.(2023·浙江杭州·学军中学校考模拟预测)连二亚硫酸钠(Na SO)是重要的化工产品,可用SO 与Zn、
2 2 4 2
NaOH溶液反应制取。实验室模拟制备的工艺流程及制取装置如图。已知:①连二亚硫酸钠易溶于水、难溶于乙醇、在碱性介质中较稳定、在空气中易被氧化。
②二价锌在水溶液中的存在形式与pH的关系如图。
请回答下列问题:
(1)通入一段时间SO 的作用除了充当反应物以外还有______。需调节溶液为弱碱性的原因______。
2
(2)写出制取连二亚硫酸钠的总化学方程式______。
(3)下列说法正确的是______。
A.将锌粉投入水中形成悬浮液主要是为了加快反应速率
B.向NaSO 溶液中加NaCl溶液或固体对NaSO 的产率无明显影响
2 2 4 2 2 4
C.洗涤NaSO•2H O时用冰水洗涤效果比酒精好
2 2 4 2
D.单向阀的主要作用是防倒吸
(4)请选择最佳操作并排序完成制备NaSO•2H O晶体。安装好整套装置,并检查装置的气密性
2 2 4 2
→______→______→______→过滤取滤液并加入NaCl固体,冷却至室温、过滤,洗涤,干燥得晶体。
______
a.将一定量的Zn粉与蒸馏水混合搅拌成悬浊液b.将一定量的Zn粉与NaOH溶液混合搅拌成悬浊液
c.将一定量的Zn粉与HCl混合搅拌成悬浊液
d.向悬浊液中通入SO 至澄清,并加热
2
e.28~35℃加热条件下,向悬浊液中通入SO 至澄清
2
f.28~35C加热条件下,向悬浊液中加入NaSO 溶液
2 3
g.向溶液中滴加NaOH至pH在8.2~10.5之间
h.向溶液中滴加HCl至pH在8.2以下
i.向溶液中滴加1mol•L-1NaOH至pH在10.5以上
(5)称取上述制得的连二亚硫酸钠样品0.0870g加入另一三颈烧瓶,通过自动电位滴定仪控制滴定管向三颈
烧瓶中快速滴加K[Fe(CN) ]溶液将连二亚硫酸钠氧化为硫酸钠,记录终点读数,共消耗
3 6
10.00mL0.2000mol•L-1的K[Fe(CN) ]溶液,则样品中连二亚硫酸钠的纯度为______。(结果保留1位小数),
3 6
样品中可能存在的杂质有______。
【答案】(1)排除装置内的空气,防止连二亚硫酸钠没氧化;碱性条件下, 能稳定存在;
(2)
(3)D
(4)a e g
(5)66.7% 、
【解析】(1)连二亚硫酸钠空气中易被氧化、在碱性介质中较稳定,故通入 可以排除装置内的空气,
防止连二亚硫酸钠被氧化;溶液显碱性,使 能稳定存在。
(2) 的水溶液中通入 发生反应: 和 ,制取连
二亚硫酸钠的总化学方程式为:
(3)A. 将锌粉投入水中形成悬浮液主要是为了增大接触面,加快反应速率,A 正确;
B. 向 溶液中加 固体,使 增大,减小 的溶解量,促进 晶体析出,产率增大,加入 溶液, 减小,减少 晶体析出,产率降低,B错误;
C. 连二亚硫酸钠易溶于水、难溶于乙醇,洗涤 时用酒精洗涤效果比冰水好,C错误;
D. 单向阀的主要作用是防止氧气防倒吸进入装置中,将连二亚硫酸钠氧化,D正确;
故选D。
(4)制备 晶体,先安装好整套装置,并检查装置的气密性→将一定量的Zn粉与蒸馏水混
合搅拌成悬浊液→28~35℃加热条件下,向悬浊液中通入 至澄清→向溶液中滴加 至pH在8.2~
10.5之间,过滤取滤液并加入 固体,冷却至室温、过滤,洗涤,干燥得晶体。故答案为:a→e→g;
(5) 与 发生反应,根据 升高6价, ,降
1价,根据得失电子守恒, ,
, 晶体的纯度为: ;
可能被氧化成 ,结晶过程中可能含有 等杂质。
2.(2022·全国·校联考模拟预测)2022年8月7日欧盟官方公报(OJ)发布RoHS2.0修订指令
(EU)2015/863,欧盟RoHS2.0更新终于尘埃落定,由原来的六项管控物质变为十项管控物质,新增物质中
有邻苯二甲酸二丁酯,实验室制备该物质的装置和实验操作如下(已知邻苯二甲酸二丁酯温度超过180℃时
易发生分解)。
实验所需相关物质的物理性质如下表:
物质 摩尔质量/( ) 密度/( ) 沸点/℃ 20℃100g水中溶解质量/g
正丁醇 74 0.80 117.6 7.7
乙醇 46 0.79 78.3 互溶
硫酸 98 1.83 337.0 互溶
邻苯二甲酸酐 148 1.53 284 不溶步骤一:125mL三颈烧瓶上分别装温度计、搅拌器、分水器及冷凝管,如图所示;
步骤二:向三颈烧瓶内依次加入44.4g邻苯二甲酸酐、36.0g正丁醇、1.0mL浓硫酸;
步骤三:向分水器中加入某种试剂X,与支管口相平;
步骤四:小火加热并不断搅拌,温度升高到120~130℃时,发现冷凝管中有正丁醇一水的共沸物蒸出,明
显看出共沸物中的小液珠沉降至分水器的底部;
步骤五:温度上升至145~160℃,依据相关实验现象,判断反应停止;
步骤六:待三颈烧瓶温度降至70℃以下时,将反应液转移至分液漏斗中,依次用15mL5%的碳酸钠溶液与
温热的饱和食盐水,分别洗涤三次;
步骤七:将上述洗涤好的油层转移到圆底烧瓶中,安装减压蒸馏装置,收集馏分。
(1)分水器中加入某种试剂X,最好选用_______(填字母序号)。A.乙醇 B.浓硫酸 C.
正丁醇 D.邻苯二甲酸二丁酯
(2)初始阶段,三颈烧瓶内邻苯二甲酸酐的物质的量浓度是_______,(忽略混合时细微的体积变化)该实验中
温度计最好选择的规格为_______(填字母序号)。
A.100℃ B.145℃ C.160℃ D.200℃
(3)第五步操作中,判断反应停止所依据的相关实验现象是_______。
(4)三颈烧瓶温度降至70℃以下才进行洗涤的原因为_______。
(5)探究该反应的最佳条件时,考虑仅改变邻苯二甲酸酐和正丁醇的物质的量之比(酸醇比)对反应的影响,
反应270min后,测得实验结果如下表:
实验序号 1 2 3 4
酸醇比 1∶2.4 1∶3.0 1∶3.5 1∶4.0
收率% 88.3 94.2 94.1 93.3
结合上述信息分析当酸醇比小于1∶3.0时,随着正丁醇的量不断增加,收率呈现上述变化的原因:
_______。(6)第七步在进行分离油状液体时采用减压蒸馏装置,其原因是_______。
【答案】(1)C
(2)4mol/L D
(3)当不在有小液珠沉降至分水器的底部,水的量不在增加的时候,没有水的生成则反应停止
(4)酯类物质在后续用碳酸钠溶液洗涤,为减少皂化反应对产物的影响,应降低温度再进行后续洗涤
(5)正丁醇的量增多会导致体系中核心反应物的浓度降低,单位时间内生成的产品量减少,收率降低
(6)邻苯二甲酸二丁酯在温度超过180℃时易发生分解
【解析】邻苯二甲酸酐、正丁醇、浓硫酸在三颈烧瓶中加热反应生成邻苯二甲酸二丁酯和水,水是反应产
物之一,根据平衡移动的原理,不断从分水器下部分离出产物水的目的是:使平衡向生成苯二甲酸二丁酯
的方向移动,提高产率;水层和有机物互不相溶,当不在有小液珠沉降至分水器的底部,水的量不在增加
的时候,则反应停止;
(1)分水器中加入某种试剂X,最好选用正丁醇,根据冷凝管中有正丁醇一水的共沸物蒸出,明显看出共
沸物中的小液珠沉降至分水器的底部,可知分水器是分离出水的,需要选密度小于水且与水不互溶的,故
选用正丁醇,故选C;
(2)初始阶段,混合后溶液的体积为 =75mL,邻苯二甲酸酐的物质的量为
,则三颈烧瓶内邻苯二甲酸酐的物质的量浓度是 =4mol/L;根据实验中温度需要
上升至145~160℃,所选用温度计量程应该略大于160℃,故该实验中温度计最好选择的规格为200℃,故
选D;
(3)根据分析,当不在有小液珠沉降至分水器的底部,水的量不在增加的时候,没有水的生成则反应停
止;
(4)酯类物质在后续用碳酸钠溶液洗涤,温度较高时酯在碱性溶液中会水解,为减少皂化反应对产物的
影响,应降低温度再进行后续洗涤;
(5)正丁醇的量增多会导致体系中核心反应物的浓度降低,单位时间内生成的产品量减少,收率降低;
(6)邻苯二甲酸二丁酯在温度超过180℃时易发生分解,减压蒸馏装置可以降低邻苯二甲酸二丁酯的沸点,
避免温度过高造成分解使产率降低。
3.(2022·陕西汉中·统考模拟预测)实验室模拟拉希法用氨和次氯酸钠反应制备肼( )并探究肼的性质。
制备装置如图所示。
已知:硫酸肼为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。回答下列问题:
(1)装置C中仪器b的名称是_______。
(2)装置A试管中反应的化学方程式为________,仪器a的作用是_______。
(3)装置B中制备肼反应的离子方程式为___________________。
(4)上述装置存在一处缺附,会导致肼的产率降低,改进方法是_________________。
(5)①探究性质。取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,容器底部有无色晶体析出。过
滤后用______洗涤,洗涤是否完成,可通过检测洗出液中是否存在 来判断。检测的方法是________。
②测定产品中肼的质量分数。称取 装置B中溶液,加入适量 固体(滴定过程中,调节溶液的
保持在6.5左右),加水配成 溶液,移取 置于锥形瓶中,并滴加2~3滴指示剂,用
的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定过程中指示剂可选用_______________,
滴定终点平均消耗标准溶液 ,产品中肼质量分数的表达式为_______________。
【答案】(1)滴液恒压漏斗
(2)2NH Cl+Ca(OH) 2NH ↑+ CaCl + 2H O 将氨气通入装置B中,且球形部分可以防止倒吸
4 2 3 2 2
(3)ClO-+2NH=Cl-+ +H O
3 2
(4)在装置B、C之间加装盛有饱和食盐水的洗气瓶,除去氯化氢气体
(5)冷水 取最后一次洗涤液,用稀盐酸酸化,无明显现象,再滴入几滴BaCl 溶液,若没有白色沉淀产生,
2
证明没有 ,说明洗涤完成,若有白色沉淀产生,证明有 ,说明洗涤未完成 淀粉溶液
【解析】实验室模拟拉希法用氨和次氯酸钠反应制备肼,装置A为生成氨气的装置,装置C为生成氯气装
置,氯气和氢氧化钠反应生成次氯酸钠,次氯酸钠再和氨生成。
(1)装置C中仪器b的名称是滴液恒压漏斗。
(2)装置A中加热NH Cl和Ca(OH) 的混合物制取氨气,化学方程式为:2NH Cl+Ca(OH) 2NH ↑+
4 2 4 2 3
CaCl + 2H O;氨气极易溶于水,仪器a的作用是将氨气通入装置B中,且球形部分可以防止倒吸。
2 2
(3)装置B中氨和次氯酸钠反应生成肼,氮元素化合价升高,次氯酸具有氧化性则氯元素化合价降低生
成氯化钠,根据得失电子守恒和电荷守恒配平离子方程式为:ClO-+2NH=Cl-+ +H O。
3 2
(4)装置C反应生成氯气,浓盐酸具有挥发性,导致氯气不纯,氯化氢会和装置B中氢氧化钠溶液反应,
导致肼的产率降低,改进方法是在装置B、C之间加装盛有饱和食盐水的洗气瓶,除去氯化氢气体。
(5)①已知硫酸肼为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水,过滤后用冷水洗涤,洗
涤是否完成,可通过检测洗出液中是否存在 来判断,检测的方法是:取最后一次洗涤液,用稀盐酸
酸化,无明显现象,再滴入几滴BaCl 溶液,若没有白色沉淀产生,证明没有 ,说明洗涤完成,若有
2
白色沉淀产生,证明有 ,说明洗涤未完成。②碘溶液能使淀粉变蓝色,故滴定过程中指示剂可选用
淀粉溶液;滴定过程中有无色无味无毒气气体产生,碘具有氧化性,则碘和肼发生氧化还原反应生成碘离
子和氮气,根据电子守恒可知,2I~4e-~N H,则产品中NH 质量为cV×10-3 mol× × ×32g/ mol=
2 2 4 2 4
64cV×10-3g ,质量分数的表达式为 。
4.(2023·北京朝阳·北京八十中校考模拟预测)某研究小组为探究饱和NaHCO 溶液中是否还能溶解少量
3
NaHCO 固体,设计并完成了下列实验。
3
【查阅资料】
常温下:Ksp(CaCO )=4.96×10−9 ;Ksp(MgCO )=6.82×10−6
3 3
碳酸的电离常数:HCO HCO + H+ K=4.3×10−7 ;HCO CO + H+ K=5.6×10−12
2 3 1 2Mg(OH) 沉淀范围:pH 9.4 ~ 12.4
2
【实验过程】
实验
实验操作 现象或结论
编号
ⅰ 测饱和NaHCO 溶液的pH pH为8.3
3
向20 mL 饱和NaHCO 溶液中再加入少量的 少量的气体X从溶液底部固体中缓慢逸出,最
ⅱ 3
NaHCO 固体,静置24小时。 终固体全部溶解,得到溶液Y
3
【分析解释】
(1)用化学用语解释饱和NaHCO 溶液pH为8.3的原因:______。
3
(2)为探究NaHCO 固体溶解的原理,取实验ⅱ反应后的气体X和溶液Y,检验其成分。
3
a.气体X能使澄清的石灰水变浑浊。
b.测得溶液Y的pH为8.7。
c.向溶液Y中滴加MgCl 溶液,有白色沉淀生成。
2
d.将c的悬浊液加热,继续有气体产生,白色沉淀不消失。
e.向2 mL饱和NaHCO 溶液中加入MgCl 溶液,无明显现象。
3 2
f.向2 mL饱和NaCO 溶液中加入MgCl 溶液,有白色沉淀生成。
2 3 2
① 气体X是______。
② 步骤d中反应的化学方程式是______。
③ 步骤e中若用CaCl 溶液代替MgCl 溶液完成实验,会观察到白色沉淀。其原因是______。
2 2
④ 步骤e、f的目的是______。
【得出结论】
(3)通过上述实验证明饱和NaHCO 溶液中还能溶解少量NaHCO 固体,结合化学用语解释其原因______。
3 3
【答案】(1)HCO +H O HCO+OH-
2 2 3
(2)CO 溶液中存在平衡 ,Ksp(CaCO)<
2 3
Ksp(MgCO ),说明 结合 能力比 强,所以可以得到 沉淀 证明饱和 溶液中
3
离子浓度不足以和 溶液反应生成沉淀(3)体系中存在平衡:2HCO (aq) CO (aq)+CO↑+H O(l),由于CO 不断逸出,平衡正向移动,固体
2 2 2
溶解。
【解析】(1)NaHCO 为强碱弱酸盐,HCO 发生水解HCO +H O HCO+OH-,碳酸氢根也能电离,
3 2 2 3
但水解程度大于电离程度,使c(OH-)>c(H+),溶液显碱性;故答案为HCO +H O HCO+OH-;
2 2 3
(2)①根据题中信息可知,气体X能使澄清石灰水变浑浊,则气体X为CO;故答案为CO;
2 2
②步骤c中产生的白色沉淀可能是Mg(OH) ,也可能是MgCO ,但根据题中所给信息可知,Mg(OH) 沉淀
2 3 2
范围是9.4~12.4,而此时溶液的pH为8.7,因此白色沉淀为MgCO ,将步骤c生成的MgCO 悬浊液加热,
3 3
继续有气体产生,由于Mg(OH) 比MgCO 更难溶,因此加热过程中发生反应的化学方程式为
2 3
,故答案为 ;
③HCO 既能发生电离,也能发生水解,碳酸氢钠溶液中存在HCO CO +H+,根据题中数据
Ksp(CaCO)<Ksp(MgCO ),说明CaCO 比MgCO 更难溶,所以得到CaCO 沉淀;故答案为溶液中存在平
3 3 3 3 3
衡 ,Ksp(CaCO)<Ksp(MgCO ),说明 结合 能力比 强,所以可以得到
3 3
沉淀;
④步骤d和e作对照实验,e中证明碳酸氢钠溶液中CO 不足以和MgCl 反应产生白色沉淀;故答案为证
2
明饱和 溶液中 离子浓度不足以和 溶液反应生成沉淀;
(3)根据上述分析,饱和碳酸氢钠溶液中存在2HCO (aq) CO (aq)+CO↑+H O(l),由于CO 不断
2 2 2
逸出,平衡正向移动,固体溶解,故答案为体系中存在平衡:HCO (aq) CO (aq)+CO↑+H O(l),由
2 2
于CO 不断逸出,平衡正向移动,固体溶解。
2
5.(2023·北京顺义·一模)某化学小组探究铜和稀硝酸的反应:
资料1 铜与浓度低于 反应很慢,且放热极少。(1)实验预测
①铜与稀 反应的离子方程式为_______。
②小组同学预测铜与稀 的反应速率应逐渐减慢,其理论依据是_______。
(2)实验实施
实验I:铜丝与 反应。
实验装置 实验操作 实验现象
反应较慢阶段A:反应前90min几
在洁净的注射器中装入已活化铜丝2.3g,再用 乎没有现象,90min左右才有很少气
泡产生(该气体遇空气变成红棕色),
注射器抽取 ,同时排尽
溶液为浅蓝色;反应较快阶段B:
注射器中的空气,关闭注射器止水开关,以保
之后溶液逐渐变为绿色;最后阶段
证铜丝与稀 反应体系处于无氧环境中。 C:在反应结束前15min左右时,体
系溶液为深蓝色。
实验II:探究Cu与稀 在无氧环境下反应所得溶液显绿色的原因:
操作及 实验现象
现象 取不同阶段的溶液进行实
实验序 验操作
阶段A溶液 阶段B溶液 阶段C溶液
号
滴加 酸性 褪色,滴6滴后溶 褪色,但滴20滴后溶 褪色,滴10滴后溶
1
液不褪色 液仍然褪色 液不再褪色
溶液
2 滴加3% 溶液 无明显现象 少量淡黄色沉淀 较多黄色沉淀
3 滴加稀 溶液 无明显现象 变蓝色 无明显现象
资料2:
i.上述溶液中均不存在-3价的氮; 为淡黄色沉淀。
ii. 是一种弱酸, ;
①通过上述实验,证明铜与稀 反应过程中可能有 生成,理由是_______。
②分析阶段B溶液呈绿色的原因_______。
③从平衡角度分析实验II中,阶段B溶液中滴加稀硫酸溶液由绿色变蓝的原因_______。④写出铜和稀 反应的生成 的化学方程式_______。
(3)继续探究:
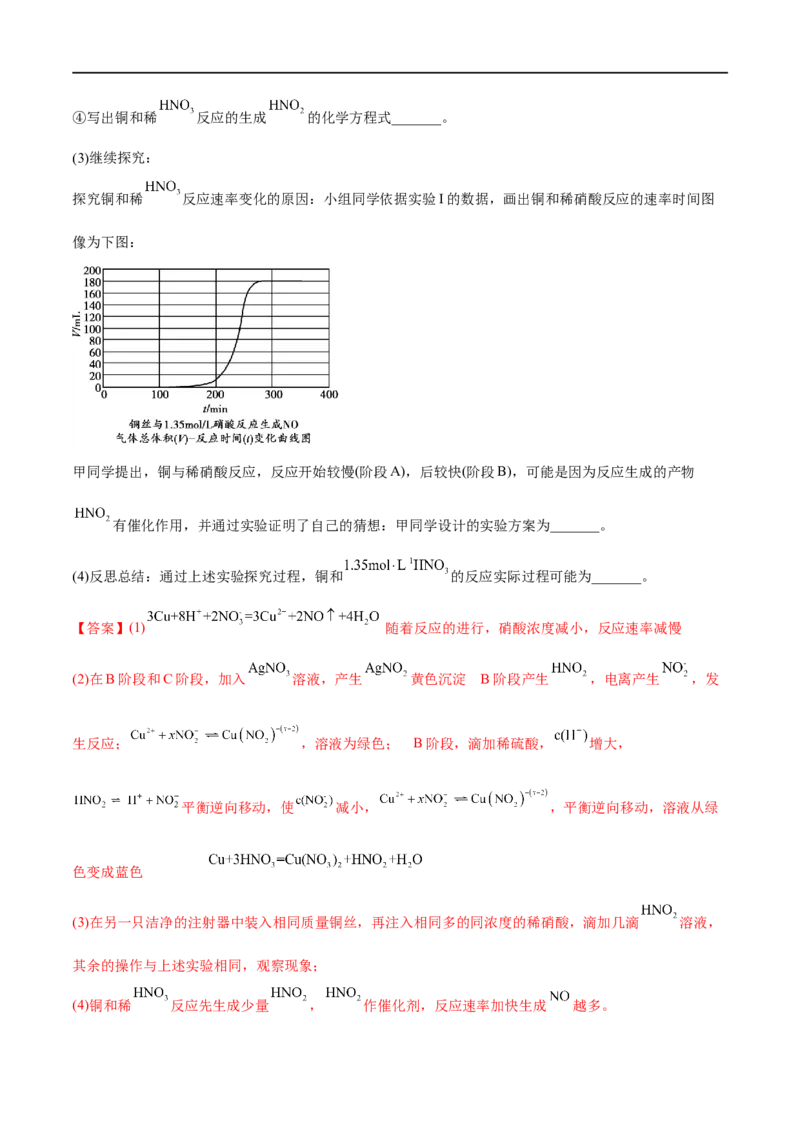
探究铜和稀 反应速率变化的原因:小组同学依据实验I的数据,画出铜和稀硝酸反应的速率时间图
像为下图:
甲同学提出,铜与稀硝酸反应,反应开始较慢(阶段A),后较快(阶段B),可能是因为反应生成的产物
有催化作用,并通过实验证明了自己的猜想:甲同学设计的实验方案为_______。
(4)反思总结:通过上述实验探究过程,铜和 的反应实际过程可能为_______。
【答案】(1) 随着反应的进行,硝酸浓度减小,反应速率减慢
(2)在B阶段和C阶段,加入 溶液,产生 黄色沉淀 B阶段产生 ,电离产生 ,发
生反应; ,溶液为绿色; B阶段,滴加稀硫酸, 增大,
平衡逆向移动,使 减小, ,平衡逆向移动,溶液从绿
色变成蓝色
(3)在另一只洁净的注射器中装入相同质量铜丝,再注入相同多的同浓度的稀硝酸,滴加几滴 溶液,
其余的操作与上述实验相同,观察现象;
(4)铜和稀 反应先生成少量 , 作催化剂,反应速率加快生成 越多。【解析】(1)铜和稀硝酸反应的离子方程式为: ,随着反应的进行,
硝酸浓度减小,反应速率减慢;
(2)在B阶段和C阶段,加入 溶液,产生 黄色沉淀,说明在反应的过程有 生成;B
阶段产生 ,电离产生 ,发生反应; (绿色),所以溶液为绿色;B
阶段,滴加稀硫酸, 增大, 平衡逆向移动,使 减小,
,平衡逆向移动,溶液从绿色变成蓝色;铜和稀 反应的生成 的化
学方程式为: ;
(3)要证明 在该反应中作催化剂,直接加入 溶液,其他的试剂和操作和上述一样,形成更好
的对比,所以方案设计为:在另一只洁净的注射器中装入相同质量铜丝,再注入相同多的同浓度的稀硝酸,
滴加几滴 溶液,其余的操作与上述实验相同,观察现象。
(4)根据实验现象和实验探究,铜和稀 反应先生成少量 , 作催化剂,反应速率加快,
生成 越多。
C 组 真题练
1.(2021·湖北·统考高考真题)某兴趣小组为制备1—氯—2—甲基丙烷(沸点69℃),将2—甲基—1—丙醇
和POCl 溶于CHCl 中,加热回流(伴有HCl气体产生)。反应完全后倒入冰水中分解残余的POCl ,分液
3 2 2 3
收集CHCl 层,无水MgSO 干燥,过滤、蒸馏后得到目标产物。上述过程中涉及的装置或操作错误的是
2 2 4
(夹持及加热装置略)A. B. C. D.
【答案】B
【解析】A.将2-甲基-1-丙醇和POCl 溶于盛在三口烧瓶中的CHCl 中,搅拌、加热回流(反应装置中的球
3 2 2
形冷凝管用于回流),制备产物,A项正确;B.产生的HCl可用NaOH溶液吸收,但要防止倒吸,导气管
不能直接插入NaOH溶液中,B项错误;C.分液收集CHCl 层需用到分液漏斗,振摇时需将分液漏斗倒
2 2
转过来,C项正确;D.蒸馏时需要用温度计控制温度,冷凝水从下口进、上口出,D项正确;故选B。
2.(2022·广东·高考真题)实验室用 和浓盐酸反应生成 后,按照净化、收集、性质检验及尾气
处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是
【答案】D
【解析】A.浓盐酸易挥发,制备的氯气中含有HCl,可用饱和食盐水除去HCl,Cl 可用浓硫酸干燥,A
2
装置能达到实验目的,故A不符合题意;B.氯气的密度大于空气,用向上排空气法收集,B装置能收集
氯气,故B不符合题意;C.湿润的红布条褪色,干燥的红色布条不褪色,可验证干燥的氯气不具有漂白
性,故C不符合题意;D.氯气在水中的溶解度较小,应用NaOH溶液吸收尾气,D装置不能达到实验目
的,故D符合题意;答案选D。
3.(2022·湖北·统考高考真题)高技术领域常使用高纯试剂。纯磷酸(熔点为 ,易吸潮)可通过市售
85%磷酸溶液减压蒸馏除水、结晶除杂得到,纯化过程需要严格控制温度和水分,温度低于 易形成
(熔点为 ),高于 则发生分子间脱水生成焦磷酸等。某兴趣小组为制备磷酸晶体设计
的实验装置如下(夹持装置略):回答下列问题:
(1)A的名称是___________。B的进水口为___________(填“a”或“b”)。
(2) 的作用是___________。
(3)空气流入毛细管的主要作用是防止___________,还具有搅拌和加速水逸出的作用。
(4)升高温度能提高除水速度,实验选用水浴加热的目的是___________。
(5)磷酸易形成过饱和溶液,难以结晶,可向过饱和溶液中加入___________促进其结晶。
(6)过滤磷酸晶体时,除了需要干燥的环境外,还需要控制温度为___________(填标号)。
A. B. C.
(7)磷酸中少量的水极难除去的原因是___________。
【答案】(1)圆底烧瓶 b
(2)干燥气体
(3)防止暴沸
(4)使溶液受热均匀
(5)磷酸晶体
(6)B
(7)磷酸可与水分子间形成氢键
【解析】空气通过氯化钙除水,经过安全瓶后通过浓硫酸除水,然后通过五氧化二磷,干燥的空气流入毛
细管对烧瓶中的溶液进行搅拌,同时还具有加速水逸出和防止溶液沿毛细管上升的作用,将85%磷酸溶液
进行减压蒸馏除水、结晶除杂得到纯磷酸。
(1)由仪器构造可知,仪器A为圆底烧瓶,仪器B为直形冷凝管,泠凝水应从b口近、a口出,形成逆流
冷却,使冷却效果更好。
(2)纯磷酸制备过程中要严格控制温度和水分,因此五氧化二磷的作用为干燥气体。
(3)空气流入毛细管可以对烧瓶中的溶液防止暴沸,同时还具有加速水逸出和防止溶液沿毛细管上升的
作用。
(4)升高温度能提高除水速度,而纯磷酸制备过程中要严格控制温度,水浴加热可以避免直接加热造成的过度剧烈与温度的不可控性,使溶液受热均匀。
(5)过饱和溶液暂时处于亚稳态,当加入一些固体的晶体或晃动时可使此状态失去平衡,过多的溶质就
会结晶,因此可向磷酸的过饱和溶液中加入磷酸晶体促进其结晶。
(6)纯磷酸纯化过程中,温度低于 易形成 (熔点为 ),高于 则发生分子间脱水
生成焦磷酸,纯磷酸的熔点为42℃,因此过滤磷酸晶体时,除了需要干燥的环境外,还需要控制温度为
30 42℃,这个区间内答案选B。
∼
(7)磷酸的结构式为: ,分子中含羟基,可与水分子间形成氢键,因此磷酸中少量的水极难除去。
4.(2022·海南·统考高考真题)磷酸氢二铵[ ]常用于干粉灭火剂。某研究小组用磷酸吸收氨气
制备 ,装置如图所示(夹持和搅拌装置已省略)。
回答问题:
(1)实验室用 和 制备氨气的化学方程式为_______。
(2)现有浓 质量分数为85%,密度为1.7g/mL。若实验需100mL1.7mol/L的 溶液,则需浓
_______mL(保留一位小数)。
(3)装置中活塞 的作用为_______。实验过程中,当出现_______现象时,应及时关闭 ,打开 。
(4)当溶液pH为8.0~9.0时,停止通 ,即可制得 溶液。若继续通入 ,当 时,
溶液中 、_______和_______(填离子符号)浓度明显增加。(5)若本实验不选用pH传感器,还可选用_______作指示剂,当溶液颜色由_______变为_______时,停止通
。
【答案】(1)
(2)11.5
(3)平衡气压防倒吸 倒吸
(4)
(5)酚酞 无 浅红
【解析】(1)实验室用NH Cl(s)和Ca(OH) (s)在加热的条件下制备氨气,反应的化学方程式为
4 2
2NH Cl+Ca(OH) CaCl +2H O+2NH ↑;
4 2 2 2 3
(2)根据公式 可得,浓HPO 的浓度 ,溶液稀释
3 4
前后溶质的物质的量不变,因此配制100mL 1.7mol/L的HPO 溶液,需要浓HPO 的体积V=
3 4 3 4
;
(3)由于NH 极易溶于水,因此可选择打开活塞K 以平衡气压,防止发生倒吸,所以实验过程中,当出
3 2
现倒吸现象时,应及时关闭K,打开K;
1 2
(4)继续通入NH ,(NH )HPO 继续反应生成(NH )PO ,当pH>10.0时,溶液中OH-、 、 的浓
3 4 2 4 4 3 4
度明显增加;
(5)由(4)小问可知,当pH为8.0~9.0时,可制得(NH )HPO ,说明(NH )HPO 溶液显碱性,因此若不选
4 2 4 4 2 4
用pH传感器,还可以选用酚酞作指示剂,当溶液颜色由无色变为浅红时,停止通入NH ,即可制得
3
(NH )HPO 溶液。
4 2 4
5.(2020·北京·高考真题)探究NaSO 固体的热分解产物。
2 3
资料:①4NaSO NaS+3Na SO ②NaS能与S反应生成NaS,NaS 与酸反应生成S和HS。③BaS易
2 3 2 2 4 2 2 x 2 x 2溶于水。
隔绝空气条件下,加热无水NaSO 固体得到黄色固体A,过程中未检测到气体生成。黄色固体A加水得到
2 3
浊液,放置得无色溶液B。
(1)检验分解产物NaS:取少量溶液B,向其中滴加CuSO 溶液,产生黑色沉淀,证实有S2-。反应的离子
2 4
方程式是____。
(2)检验分解产物NaSO :取少量溶液B,滴加BaCl 溶液,产生白色沉淀,加入盐酸,沉淀增多(经检验该
2 4 2
沉淀含S),同时产生有臭鸡蛋气味的气体(H S),由于沉淀增多对检验造成干扰,另取少量溶液B,加入足
2
量盐酸,离心沉降(固液分离)后,____(填操作和现象),可证实分解产物中含有SO 。
(3)探究(2)中S的来源。
来源1:固体A中有未分解的NaSO ,在酸性条件下与NaS反应生成S。
2 3 2
来源2:溶液B中有NaS,加酸反应生成S。
2 x
针对来源1进行如图实验:
①实验可证实来源1不成立。实验证据是____。
②不能用盐酸代替硫酸的原因是____。
③写出来源2产生S的反应的离子方程式:____。
(4)实验证明NaSO 固体热分解有NaS,NaSO 和S产生。运用氧化还原反应规律分析产物中S产生的合
2 3 2 2 4
理性:____。
【答案】(1)S2-+Cu2+=CuS↓
(2)滴加BaCl 溶液,产生白色沉淀,
2
(3)①向溶液2中加入KMnO 溶液,溶液没有褪色
4
②盐酸中Cl元素为-1价,是Cl元素的最低价,具有还原性,会与KMnO 溶液发生氧化还原反应,使
4
KMnO 溶液应该褪色,干扰实验现象和实验结论;
4
③S2-+2H+=H S↑+(x-1)S↓
x 2
(4)根据反应4NaSO NaS+3Na SO 可知,NaSO 发生歧化反应,其中的S元素化合价即可升高也可降低,
2 3 2 2 4 2 3能从+4价降为-2价,也应该可以降到0价生成硫单质
【解析】(1)Na S和CuSO 溶液反应生成硫化铜和硫酸钠,反应的离子方程式是S2-+Cu2+=CuS↓;
2 4
(2)根据题干资料:NaS能与S反应生成NaS,NaS 与酸反应生成S和HS,取少量溶液B,滴加BaCl 溶
2 2 x 2 x 2 2
液,产生白色沉淀,加入盐酸,沉淀增多(经检验该沉淀含S),同时产生有臭鸡蛋气味的气体(H S),说明
2
B溶液中含有NaS,NaS 与酸反应生成S和HS,由于沉淀增多对检验造成干扰,另取少量溶液B,加入
2 x 2 x 2
足量盐酸,离心沉降(固液分离)后,滴加BaCl 溶液,产生白色沉淀,可证实分解产物中含有SO ;
2
(3)①实验可证实来源1不成立。根据分析,溶液2为HSO ,向溶液2中加入少量KMnO 溶液,HSO 具
2 3 4 2 3
有还原性,酸性条件下KMnO 具有强氧化性,二者混合和后应发生氧化还原反应,KMnO 溶液应该褪色,
4 4
但得到的仍为紫色,说明溶液B中不含NaSO ;
2 3
②不能用盐酸代替硫酸的原因是盐酸中Cl元素为-1价,是Cl元素的最低价,具有还原性,会与KMnO 溶
4
液发生氧化还原反应,使KMnO 溶液应该褪色,干扰实验现象和实验结论;
4
③来源2认为溶液B中有NaS,加酸反应生成S,反应的离子方程式:S2-+2H+=H S↑+(x-1)S↓;
2 x x 2
(4)根据已知资料:4NaSO NaS+3Na SO ,亚硫酸钠中硫为+4价,硫酸钠中硫为+6价,硫化钠中硫为-2
2 3 2 2 4
价,根据反应可知NaSO 发生歧化反应,其中的S元素化合价即可升高也可降低,能从+4价降为-2价,
2 3
也应该可以降到0价生成硫单质。